Изобретение относится к ветеринарной микробиологии, в частности к лабораторной диагностике возбудителей инфекционных заболеваний, а именно к средствам диагностики инфекции у животных с помощью полимеразной цепной реакции.
Известны тест-системы, предусматривающие использование ПЦР с уникальным набором олигонуклеотидных праймеров, где продукты амплификации разделяют методом электрофореза в агарозном геле. Результаты ПЦР учитывают, визуализируя окрашиванием бромистым этидием. Наличие в исследуемом биоматериале генов патогенности инфекционных возбудителей определяют по размерам образовавшихся фрагментов ДНК (патенты RU №№2483114, 2542396, 2514663, 2445370).
Достоинством ПЦР с электрофорезом, в котором продукты амплификации разделяют методом электрофореза в агарозном геле - является качественный анализ, позволяющий определить наличие остаточных (следовых) количеств искомых молекул ДНК в образце. Кроме того этот метод является наиболее дешевым, чем ПЦР в реальном времени.
Также известен набор для выявления генома полевых изолятов вируса заразного узелкового дерматита (нодулярного дерматита) КРС в реакции полимеразной цепной реакции в режиме реального времени с использованием олигонуклеотидных праймеров и флуоресцентно-меченого зонда для амплификации и детекции фрагмента гена наружного капсидного белка EEV вируса заразного узелкового дерматита (ЗУД) КРС (патент RU 2668398, кл. C12Q 1/68, 2018 г.).
Известный набор предназначен для выявления генетического материала полевого вируса ЗУД КРС в биологических и культуральных образцах для постановки и уточнения диагноза, для решения научно-исследовательских задач по мониторингу распространения вируса ЗУД КРС среди восприимчивых животных методом полимеразной цепной реакции (ПЦР) с гибридизационно-флуоресцентной детекцией в режиме реального времени (РВ) с использованием олигонуклеотидных праймеров и флуоресцентно-меченого зонда для амплификации и детекции фрагмента гена наружного капсидного белка EEV вируса заразного узелкового дерматита (ЗУД) КРС. Недостатками известного набора является ограниченный спектр биологического материала и недостаточная чувствительность, т.к. в качестве мишени используют образцы гетерологичных вирусов, депонированных в коллекции штаммов микроорганизмов, которые перед использованием необходимо разморозить. Известно, что в результате заморозки и разморозки происходит нарушение строения микроорганизма, что влияет на чувствительность выявления вируса нодулярного дерматита.
Наиболее близким по технической сущности является техническое решение (патент РФ №2680094, кл. C12Q 1/68, G01N 33/569, 2019 г.), включающее буфер для проведения полимеразной цепной реакции, смесь для ее проведения, состоящая из дезоксинуклеозидтрифосфатов, олигонуклеотидных праймеров специфичные для участка генома возбудителя инфекционного заболевания, внутреннего контрольного образца в виде суспензии бактериофага Т4 с концентрацией 5×103 фаговых частиц на 1 мкл; смеси ферментов из ДНК полимеразы с антителами, ингибирующих активность фермента, TAQ POLYMERASE, положительный контрольный образец, представляющий собой смесь рекомбинантных плазмидных ДНК, содержащих фрагмент генома возбудителя инфекционного заболевания и фрагмент генома бактериофага Т4.
Недостатками известного технического решения является отсутствие возможности определения остаточных (следовых) количеств искомых молекул ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных и высокая стоимость метода, для проведения которого требуется около 2-х млн. руб.
Техническим результатом является расширение функциональных возможностей, повышение специфичности при выявлении остаточных количеств искомых молекул ДНК вируса нодулярного дерматита и снижение стоимости метода.
Технический результат достигается тем, что в тест-системе для выявления ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных методом ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле, включающей буфер для проведения ПЦР, смесь для ее проведения, состоящая из дезоксинуклеозидтрифосфатов, олигонуклеотидных праймеров специфичные для участка генома возбудителя инфекционного заболевания и для внутреннего контрольного образца в виде суспензии бактериофага Т4 с концентрацией 5×103 фаговых частиц на 1 мкл; смесь ферментов из ДНК полимеразы с антителами, ингибирующих активность фермента, TAQ POLYMERASE, положительный контрольный образец, представляющий собой смесь рекомбинантных плазмидных ДНК, содержащей фрагмент генома возбудителя инфекционного заболевания и фрагмент генома бактериофага Т4, взятых в объемном соотношении 1:1, согласно изобретению для положительного контрольного образца используют фрагменты геномов бактериофага Т4 и фрагмент генома вируса нодулярного дерматита (LSDV) со следующими нуклеотидными последовательностями:
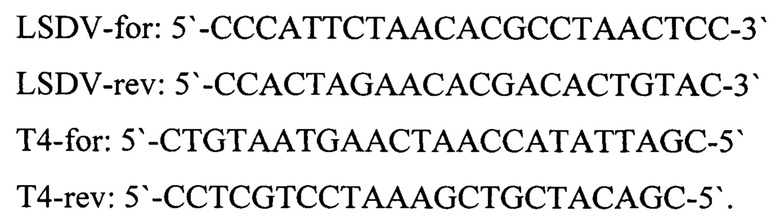
Новизна заявляемой тест-системы состоит в идентификации ДНК вируса нодулярного дерматита с помощью полимеразной цепной реакции (ПЦР) с электрофоретической детекцией с использованием специфичных для участка генома олигонуклеотидных праймеров и разных видов контроля для которых используют различные формы материала бактериофага Т4: суспензия и фрагмент генома со специфическими к нему праймерами. Такая постановка ПЦР обеспечивает возможность определения остаточных количеств искомых молекул ДНК вируса нодулярного дерматита (LSDV).
Признаки, отличающие заявляемое техническое решение от прототипа, направлены на достижение технического результата и не выявлены при изучении данной и смежной областей науки и техники и, следовательно, соответствуют критерию «изобретательский уровень».
Заявляемая тест-система рекомендована для использования в специализированных ветеринарных, санитарно-эпидемиологических, животноводческих, сельскохозяйственных предприятиях, что соответствует критерию «промышленная применимость».
Тест-система для определения ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных методом ПЦР с электрофоретической детекцией продуктов амплификации используется следующим образом.
Предварительно выделяют ДНК из биологического материала животного сорбционным методом. В качестве биологического материала может быть использованы: цельная кровь, фрагменты пораженных кожных покровов (высыпания, корки, узелковые поражения-нодулы), легких, бронхов, селезенки, лимфоузлы, мазки со слизистых конъюнктивы и ротоглотки, молоко и сперма, которые подвергают определенной обработке.
Проводят полимеразную цепную реакцию с электрофоретической детекцией продуктов амплификации в агарозном геле с проведением 45 циклов амплификации с использованием специфичных для участка генома ДНК вируса нодулярного дерматита олигонуклеотидных праймеров, флуоресцентного красителя, внутреннего контрольного образца в виде суспензии бактериофага Т4 с концентрацией 5×103 фаговых частиц на 1 мкл и положительного контрольного образца в виде смеси рекомбинантных плазмидных ДНК, содержащую в одинаковом объемном соотношении фрагмент генома ДНК вируса нодулярного дерматита и фрагмент генома бактериофага Т4 со следующими нуклеотидными последовательностями:

Для амплификации используют прибор типа RotorGene, получают электрофореграмму ДНК со специфическими полосами амплифицированной продукции, визуализированные путем окрашивания флуоресцентным красителем - бромид этидия. Учет и проведение интерпретации результатов ПЦР проводят по наличию или отсутствию на электрофореграмме ДНК специфической полосы фрагмента ДНК вируса нодулярного дерматита, совпадающей по размеру с полосой фрагмента этого же ДНК, амплифицированным из положительного контрольного образца.
Для повышения точности идентификации вируса нодулярного дерматита (LSDV) для положительного контрольного образца используют смесь, содержащую фрагменты геномов бактериофага Т4 и ДНК вируса нодулярного дерматита (LSDV), взятых в соотношении 1:1, со следующими нуклеотидными последовательностями:
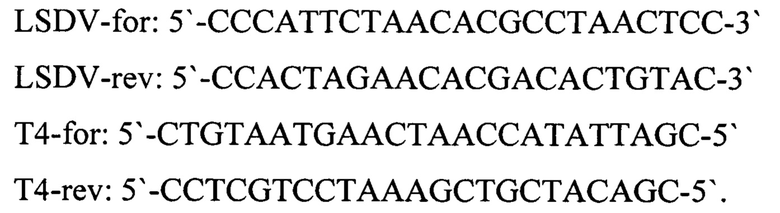
Заявляемый способ обеспечивает высокую специфичность, что позволяет достоверно и количественно определять наличие следовых количеств искомых молекул ДНК вируса нодулярного дерматита (LSDV) в исследуемых пробах.
При конструировании праймеров основными требованиями были: степень гомологии (комплементарность) с выбранным участком гена; отсутствие самокоплементарных участков внутри олигонуклеотидов и комплементарности друг другу, чтобы не допускать возникновения устойчивых вторичных структур (димеров); близость значений температуры отжига праймеров.
Конструирование специфических праймеров осуществляли с помощью компьютерных программ на основании анализа нуклеотидных последовательностей референтных штаммов и изолятов, опубликованных на ресурсе GenBank и подбора условий для проведения ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле с применением разработанных праймеров, несущего флуорофора и тушителя, и комплементарного части амплифицируемого со специфическими праймерами фрагмента. Праймеры, специфичные для генома вируса нодулярного дерматита, были отобраны на нуклеотидной последовательности участка генома, кодирующей гипотетический белок гликопротеин (Lumpy skin disease virus strain LSDV/Russia/Saratov/2017, complete genome 150606 bp DNA linear VRL 18-NOV-2018, код MH646674, участок между 19000 и 20000 парами оснований). Праймеры были разработаны с использованием Primer Express Software v3.0 (Applied Biosystems) и исследованы с использованием BLAST, чтобы подтвердить их специфичность. Используя программу "Oligo 6.0" описаны основные свойства рассчитанных олигонуклеотидов, определившие возможность их использования в ПЦР. Заявляемая нуклеотидная последовательность имеет следующий набор:

В качестве внутреннего контроля использовался бактериофаг Т4, имеющий геномную ДНК порядка 170 тысяч пар нуклеотидов (Enterobacteria phage Т4Т, complete genome GenBank: HM137666.1). В результате анализа был выбран участок между 200 и 1000 нуклеотидами, содержащий уникальную нуклеотидную последовательность. Последовательности праймеров были выбраны с использованием Primer Express Software v3.0 (Applied Biosystems). Специфичность выбранных праймеров оценивали используя программу BLAST на сервере NCBI.
Заявляемая нуклеотидная последовательность имеет следующий набор:
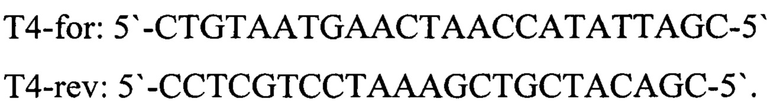
Пример конкретного использования тест-системы для выявления ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных с помощью полимеразной цепной реакции с электрофоретической детекцией продуктов амплификации в агарозном геле
Для исследований используют следующий биологический материал, который может быть взят по выбору от КРС, а также от овец или коз:
1. Цельная кровь (в ранний период заболевания, во время виремии). Кровь забирается в пробирку с 3-6% ЭДТА из расчета 50 мкл раствора ЭДТА на 1 мл крови, закрытую пробирку с кровью несколько раз переворачивают.
2. Фрагменты пораженных кожных покровов (высыпания, корки, узелковые поражения-нодулы), легких, бронхов, селезенки отбирают в стерильный контейнер.
3. Лимфоузлы берут на исследование целиком.
4. Мазки со слизистых конъюнктивы и ротоглотки снимают с помощью стерильного зонда, зонд помещают в пластиковую микропробирку объемом 1,5 мл с 0,5 мл стерильного физиологического раствора/фосфатного буфера/транспортной среды.
5. Молоко отбирают в объеме 10-30 мл в стерильную посуду;
6. Сперму (0,5-1 мл) отбирают в стерильный контейнер.
Полученные образцы можно транспортировать и хранить в следующих
режимах:
- при комнатной температуре - в течение 48 часов;
- при температуре от 2 до 8°С - в течение двух недель;
- при температуре не выше минус 20°С - в течение месяца;
- при температуре не выше минус 68°С - длительно,
- оттаивание биологического материала.
Чтобы избежать ложноположительных результатов необходимо после вакцинации выдержать 3-4 недели перед сдачей анализа.
Далее исследуемые образцы обрабатывают следующим образом:
Мазки со слизистых конъюнктивы, ротоглотки, пробы цельной крови, молоко исследуют без предварительной подготовки.
Сперму разводят физиологическим раствором 1:3, тщательно перемешивают на вортексе. Для экстракции ДНК используют аликвоту 0,1 мл суспензии.
Из тканей и органов вырезают небольшие кусочки до 1 г весом. Растирают пробы в фарфоровых ступках или гомогенизируют на автоматических гомогенизаторах. Затем готовят 20% суспензию на стерильном физиологическом растворе или фосфатном буфере. Суспензию переносят в пробирку объемом 1,5 мл и центрифугируют при 600-1000 g (2000 об./мин на центрифуге «MiniSpin», Eppendorf, Германия) в течение 2 мин. Аликвоту надосадочной жидкости (0,1 мл) используют для экстракции ДНК.
Для подтверждения эффективности способа были использованы пробы по выбору, например мазки со слизистых конъюнктивы, ротоглотки КРС, которые исследуют без предварительной подготовки.
Лабораторные пробы (20-40 мг) отбирают на исследование в одноразовые микропробирки вместимостью 1,5 мл в двух повторах. Отобранные лабораторные пробы направляют на выделения ДНК.
Исследование проводят с помощью набора реагентов «ПЦР-Ф-НОДУЛЯРНЫЙ-ДЕРМАТИТ-КРС-ФАКТОР». Набор состоит из комплекта реагентов для проведения мультиплексной ПЦР (комплект №1) и комплекта контрольных образцов (комплект №2). Набор выпускается в двух вариантах: 1) Для анализа 55 образцов (включая контрольные образцы)
2) Для анализа 110 образцов (включая контрольные образцы).
Наборы используют в соответствии с инструкцией по применению набора реагентов «ПЦР-Ф-НОДУЛЯРНЬ1Й-ДЕРМАТИТ-КРС-ФАКТОР» для выявления ДНК вируса нодулярного дерматита (Lumpy skin disease virus, LSDV) в биологическом материале методом полимеразной цепной реакции (ПЦР) с электрофоретической детекцией продуктов амплификации в агарозном геле, ТУ21.10.60-112-51062356-2016, для диагностики in vitro, http://www.vetfaktor.ru/.
Состав набора приведен в Таблицах 1 и 2.
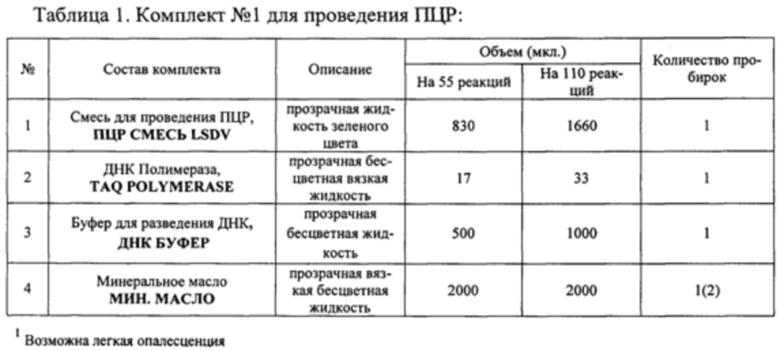
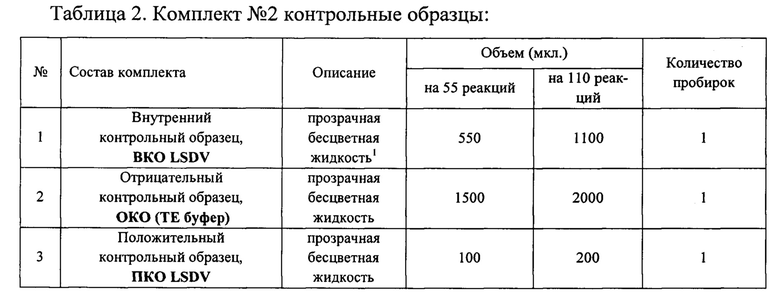
Исследование с помощью набора реагентов<<ПЦР-Ф-НОДУЛЯРНЬ1Й-ДЕРМАТИТ-КРС-ФАКТОР» состоит из трех этапов:
• экстракция НК (на этом этапе дополнительно используют реактивы для экстракции, например набор «ДНК/РНК-С-ФАКТОР»);
• проведение ПЦР;
• анализ продуктов амплификации методом электрофореза (на этом этапе дополнительно используют набор реагентов для электрофоретического анализа, например набор «ПЦР-ЭФ-ФАКТОР»);
• учет результатов анализа.
Для экстракции (выделение) НК из исследуемых проб, отбирают необходимое количество одноразовых пробирок объемом 1,5 мл, включая отрицательный контроль выделения. Вносят во все пробирки с исследуемыми образцами, включая пробирку для ОКО (отрицательный контрольный образец, по 10 мкл ВКО (внутренний контрольный образец) LSDV в виде суспензии бактериофага Т4.
Вносят исследуемые пробы в объеме согласно инструкции к набору для выделения НК, в пробирку отрицательного контроля выделения вместо исследуемой пробы вносят ОКО (пробирку обозначить как ВК-).
Выделяют ДНК из анализируемых и контрольных образцов согласно протоколу инструкции производителя набора для выделения НК.
Выделенную ДНК можно хранить в течение одной недели при температуре от 2°С до 8°С или в течение года при температуре не выше минус 16°С.
Далее готовят образцы к проведению ПЦР.
Общий объем реакционной смеси - 25 мкл, объем ДНК-пробы - 10 мкл. Успешное прохождение реакции контролируют использованием ПКО LSDV (положительный контрольный образец) в виде смеси, содержащей фрагменты геномов бактериофага Т4 и ДНК вируса нодулярного дерматита (LSDV) взятых в соотношении 1:1, со следующими нуклеотидными последовательностями: 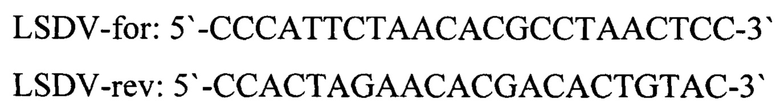
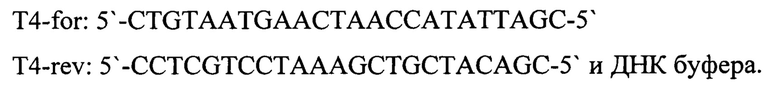
В отдельной пробирке смешивают компоненты набора реагентов из расчета на каждую реакцию*2:
15 мкл ПЦР СМЕСЬ LSDV;
0,3 мкл TAQ POLYMERASE
Перемешивают смесь на вортексе (без вспенивания) и сбрасывают капли кратковременным центрифугированием.
Отбирают необходимое количество пробирок для амплификации ДНК исследуемых и контрольных проб. Вносят по 15 мкл приготовленной реакционной смеси.
В случае использования амплификаторов без подогревающейся крышки (например, «Терцик», «ДНК технология») сверху в пробирки вносят по капле минерального масла для ПЦР (примерно 25 мкл).
Используют наконечники с фильтром в подготовленные пробирки (под масло или непосредственно на масло) вносят:
а) в пробирку отрицательного контроля ПЦР (К-) 10 мкл ДНК буфера;
б) в ряд пробирок для исследуемых проб - в каждую вносят по 10 мкл ДНК соответствующей пробы, (включая пробу ВК-);
в) в пробирку положительный контроль ПЦР (К+) - 10 мкл ПКО LSDV.
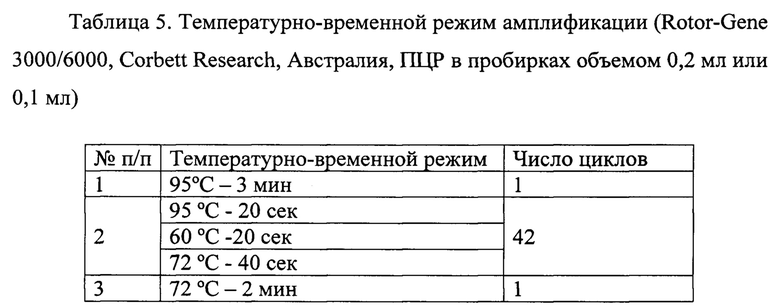
Рекомендуется перед постановкой в амплификатор осадить капли со стенок пробирок кратким центрифугированием на вортексе (1-2 секунды). Установить пробирки в амплификатор, для исследований был использован прибор «ДТ 96». Режим термоциклирования для разных приборов приведен в таблицах 3, 4 и 5.

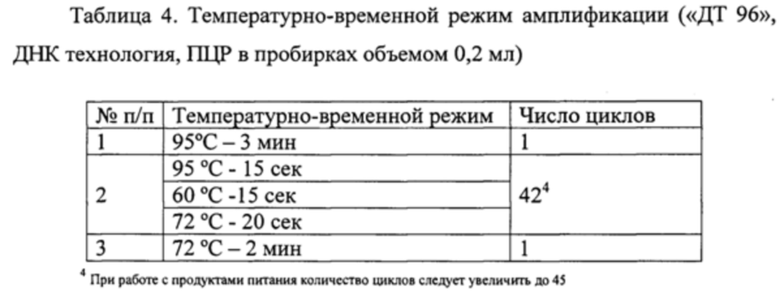
После окончания реакции переставить пробирки в специальный штатив и отправить в помещение для детекции продуктов ПЦР.
Пробы после амплификации можно хранить в течение 16 ч при комнатной температуре. Для длительного хранения требуется заморозка.
Анализ продуктов амплификации проводится методом электрофореза в агарозном геле.
Затем проводят учет результатов ГЩР-анализа по наличию или отсутствию на электрофореграмме специфических полос амплифицированной НК.
Результат считается достоверным в случае корректного прохождения положительных и отрицательных контролей амплификации и экстракции ДНК в соответствии с таблицей 6.

Появление специфической полосы ПЦР продукта 500 пн для отрицательного контроля этапа экстракции (ВК-) и полос 500 пн и/или 300 пн для отрицательного контроля этапа ПЦР (К-) свидетельствует о наличии контаминации реактивов или образцов. В этом случае результаты анализа для всех проб считаются недействительными. Требуется повторить анализ всех проб, а также предпринять меры по выявлению и ликвидации источника контаминации.
На дорожках с исследуемыми образцами должно наблюдаться одна или две полосы, совпадающими по подвижности с полосами от образца К+(ПКО LSDV).
Образец считается отрицательным (ДНК вируса LSDV отсутствует) если не наблюдается амплификации специфической полосы на уровне 300 пар нуклеотидов (пн) и при этом наблюдается специфическая полоса ВКО на уровне 500 пар нуклеотидов.
Образец считается положительным (ДНК вируса LSDV присутствует) если наблюдается полоса, подвижность которой совпадает с подвижностью нижней полосы (300 пар нуклеотидов) на дорожке К+(ПКО LSDV). Наличие полосы ВКО (500 пар нуклеотидов) при этом не обязательно.
Исследуемые образцы, для которых на дорожках отсутствуют обе полосы, требуют повторного проведения исследования. Отсутствие полосы ВКО (500 пар нуклеотидов) при отсутствии амплификации целевого ПЦР продукта вируса LSDV (300 пар нуклеотидов) указывает на наличие ингибиторов в пробе(ах) или на ошибки при постановке реакции. Необходимо провести исследование, начиная с этапа экстракции ДНК.
Для доказательства эффективности использования ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле для выявления ДНК вируса нодулярного дерматита в агарозном геле проводился сравнительный анализ заявляемой тест-системы с известными техническими решениями (патенты №№2648773, 2668398), а также с прототипом (патент №2680094).
В заявляемой тест-системе при обнаружении остаточных ДНК LSDV за счет повышения специфичности, точность определения остаточных (следовых) количеств искомых молекул ДНК вируса нодулярного дерматита (LSDV) больше на 3,4-4,5%, чем в известных способах и заявляемый способ в 8-10 раз дешевле, чем методы с использование ПЦР в реальном времени.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных методом ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле | 2019 |
|
RU2728660C1 |
| Тест-система для выявления ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных с помощью полимеразной цепной реакции в режиме реального времени | 2019 |
|
RU2726242C1 |
| Способ выявления ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных с помощью полимеразной цепной реакции в режиме реального времени | 2019 |
|
RU2719719C1 |
| Тест-система для идентификации ДНК ткани перепелки обыкновенной (Coturnix coturnix) в сухих кормах и мясных полуфабрикатах | 2019 |
|
RU2725210C1 |
| Способ выявления ДНК вируса ринотрахеита (bovine herpes virus 1, BoHV-1) у крупного рогатого скота | 2018 |
|
RU2700449C1 |
| Способ выявления ДНК провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) | 2018 |
|
RU2700245C1 |
| Тест-система для выявления ДНК провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) | 2018 |
|
RU2700450C1 |
| Тест-система для выявления ДНК вируса ринотрахеита (bovine herpes virus 1, BoHV-1) у крупного рогатого скота | 2018 |
|
RU2700254C1 |
| Тест-система для обнаружения генома возбудителя ДНК Bordetella bronchiseptica инфекции у сельскохозяйственных животных | 2018 |
|
RU2700477C1 |
| Способ обнаружения ДНК генома возбудителя бордетеллеза (Bordetella bronchiseptica) у сельскохозяйственных животных | 2018 |
|
RU2703405C1 |


Изобретение отноcится к области биотехнологии. Изобретение представляет собой тест-систему для выявления ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных методом ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле, включающей буфер для проведения ПЦР, смесь для ее проведения, состоящую из дезоксинуклеозидтрифосфатов, олигонуклеотидных праймеров, специфичных для участка генома возбудителя инфекционного заболевания и для внутреннего контрольного образца в виде суспензии бактериофага Т4 с концентрацией 5×103 фаговых частиц на 1 мкл; смесь ферментов из ДНК полимеразы с антителами, ингибирующими активность фермента, TAQPOLYMERASE, положительный контрольный образец, представляющий собой смесь рекомбинантных плазмидных ДНК, содержащей фрагмент генома возбудителя инфекционного заболевания и фрагмент генома бактериофага Т4, взятых в объемном соотношении 1:1, согласно изобретению для положительного контрольного образца используют фрагменты геномов бактериофага Т4 и фрагмент генома вируса нодулярного дерматита (LSDV) со следующими нуклеотидными последовательностями. Для расширения функциональных возможностей - повышение специфичности при выявлении остаточных количеств искомых молекул ДНК вируса нодулярного дерматита и снижение стоимости метода. Изобретение позволяет расширить функциональные возможности, повысить специфичность при выявлении остаточных количеств искомых молекул ДНК вируса нодулярного дерматита. 6 табл.
Тест-система для выявления ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных методом ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле, включающая буфер для проведения ПЦР, смесь для ее проведения, состоящая из дезоксинуклеозидтрифосфатов, олигонуклеотидных праймеров, специфичных для участка генома возбудителя инфекционного заболевания и для внутреннего контрольного образца в виде суспензии бактериофага Т4 с концентрацией 5×103 фаговых частиц на 1 мкл; смесь ферментов из ДНК полимеразы с антителами, ингибирующими активность фермента, TAQ POLYMERASE, положительный контрольный образец, представляющий собой смесь рекомбинантных плазмидных ДНК, содержащей фрагмент генома возбудителя инфекционного заболевания и фрагмент генома бактериофага Т4, взятых в объемном соотношении 1:1, отличающаяся тем, что для положительного контрольного образца используют фрагменты геномов бактериофага Т4 и фрагмент генома вируса нодулярного дерматита (LSDV) со следующими нуклеотидными последовательностями:
LSDV-for: 5`-CCCATTCTAACACGCCTAACTCC-3`
LSDV-rev: 5`-CCACTAGAACACGACACTGTAC-3`
T4-for: 5`-CTGTAATGAACTAACCATATTAGC-5`
T4-rev: 5`-CCTCGTCCTAAAGCTGCTACAGC-5`.
| Тест-система для выявления ДНК возбудителя лептоспироза (Leptospira spp.) у сельскохозяйственных животных | 2018 |
|
RU2680094C1 |
| CN 106435008 A, 22.02.2017 | |||
| CN 108624659 A, 09.10.2018. | |||
Авторы
Даты
2020-07-14—Публикация
2019-10-16—Подача