Изобретение относится к медицине, а именно к созданию средства, обладающего противогипоксической, антиамнестической и нейропротекторной активностью, в частности, для лечения острых и хронических нарушений мозгового кровообращения, таких как ишемический инсульт, транзиторная ишемическая атака и хроническая ишемия головного мозга, а также других заболеваний центральной нервной системы, сопровождающихся снижением когнитивных функций и нейродегенерацией, в том числе при старении.
В современной медицине проблема лечения цереброваскулярных заболеваний продолжает оставаться одной из наиболее сложных и актуальных. Так, ишемический инсульт занимает лидирующие позиции среди причин смерти и инвалидизации, в том числе и у ранее трудоспособных пациентов. Это связано как с неуклонным ростом количества больных с указанной патологией, так и с отсутствием высокоэффективных и безопасных средств ее патогенетической терапии [7, 12, 13].
Ближайший аналог заявляемого средства по химическому строению - никотиновая кислота, которую в качестве лекарственного средства широко применяют с середины прошлого века. Она оказывает противопеллагрическое, гиполипидемическое, антиатерогенное, нейропротекторное, сосудорасширяющее (в том числе на сосуды головного мозга) действие, улучшает микроциркуляцию, повышает фибринолитическую активность крови и уменьшает агрегацию тромбоцитов (за счет уменьшения образования тромбоксана А2), а также обладает дезинтоксикационными и другими свойствами [11, 16, 17]. Однако в настоящее время никотиновую кислоту не используют для фармакотерапии ишемического инсульта по причине недостаточной эффективности и наличия выраженных побочных эффектов.
Другой ближайший аналог заявляемого средства (как по химическому строению -является производным 3-гидроксипиридина и содержит в своей структуре пиридиновый гетероцикл, так и по фармакологическим свойствам) - отечественный лекарственный препарат мексидол (этилметилгидроксипиридина сукцинат: 2-этил-6-метил-3-гидроксипиридина сукцинат). Он относится к антигипоксантам/антиоксидантам, обладает уникальным спектром фармакологических свойств, а также его уже более 20 лет широко и успешно применяют в различных областях медицины, в частности в неврологии при ишемическом инсульте и его последствиях [2, 3]. Однако иногда в клинике препарат бывает неэффективен - положительный эффект наблюдался лишь у 63% больных, преобладая у пациентов с дисциркуляторной энцефалопатией атеросклеротического генеза [8, 9]. Более того, мексидол имеет недостаточную противогипоксическую и ноотропную активность.
В связи с этим необходимо изыскание в ряду производных пиридина новых веществ, имеющих широкий спектр фармакологического действия и способных более эффективно, чем мексидол, действовать, в частности, на моделях инсульта, острой гипоксии и амнезии в эксперименте.
Поэтому задачей настоящего изобретения является создание нового средства, обладающего противогипоксической, антиамнестической и нейропротекторной активностью.
Поставленная цель достигается применением в качестве нового средства магния-бис(-3-пиридинкарбоноата) (МБПК) в эффективных количествах, имеющего выраженное нейропротекторное действие в сочетании с противогипоксической и антиамнестической активностью.
Изобретение иллюстрируется следующими ниже примерами. При этом примеры 2-4 иллюстрируют эффективность МБПК в качестве противогипоксического, антиамнестического и нейропротекторного средства в сравнении с ближайшим аналогом мексидолом.
Синтез нового соединения осуществляли путем взаимодействия 3-пиридинкарбоновой кислоты и оксида магния.
Пример 1. Синтез магния-бис(-3-пиридинкарбоноата)
В трехгорлую колбу, снабженную мешалкой, термометром и обратным холодильником, загружают 60 мл воды, 4,92 г (0,04 М) 3-пиридинкарбоновой кислоты, после растворения добавляют 0,8 г (0,02 М) оксида магния. Массу нагревают до кипения и выдерживают в течение 1 часа при кипении. Полученный раствор фильтруют, отгоняют воду в вакууме, сухой остаток перекристаллизовывают из 50% этилового спирта. Получают 4,87 г белого кристаллического порошка. Тпл около 300°С.
C12H8N2O4Mg мм 268,51
Найдено, %: С 53,62; Н 3,04; N 10,39; Mg 9,01
Вычислено, %: С 53,68; Н 3,01; N 10,43; Mg 9,05; О 23,83
ИК (v, см-1): 3350 (-N=); 2860, 2380 (СН); 1584 (COO) УФ: 0,002% раствор в воде, максимум поглощения при 268±2 нм. ТСХ: на пластинах silicagel УФ 254 в системе растворителей этанол:ацетон:вода (3:5:2) - в зоне адсорбции одно пятно.

При выполнении экспериментальной части работы (опыты на животных - примеры 2-4) в соответствии с Российскими национальными правилами исследований (Приказ Министерства здравоохранения РФ от 1 апреля 2016 г. №199н «Об утверждении Правил надлежащей лабораторной практики» и др.) и международными требованиями в основном были использованы модели и методы, рекомендованные для проведения подобных исследований, утвержденные Министерством здравоохранения РФ и соответствующие рекомендациям ВОЗ, касающимся правил надлежащей лабораторной практики (GLP -"Good Laboratory Practice") [6]. Животных получали из филиала «Андреевка» Федерального государственного бюджетного учреждения науки «Научный центр биомедицинских технологий» Федерального медико-биологического агентства (р/п Андреевка, Солнечногорский район, Московская область). Содержание животных соответствовало правилам GLP и осуществлялось в соответствии с нормативным документом «Санитарные правила по устройству, оборудованию и содержанию вивариев», утвержденным Главным государственным санитарным врачом 06.04.1973 г. №1045-73, и приказом МЗ РФ №199н от 01.04.2016 г.
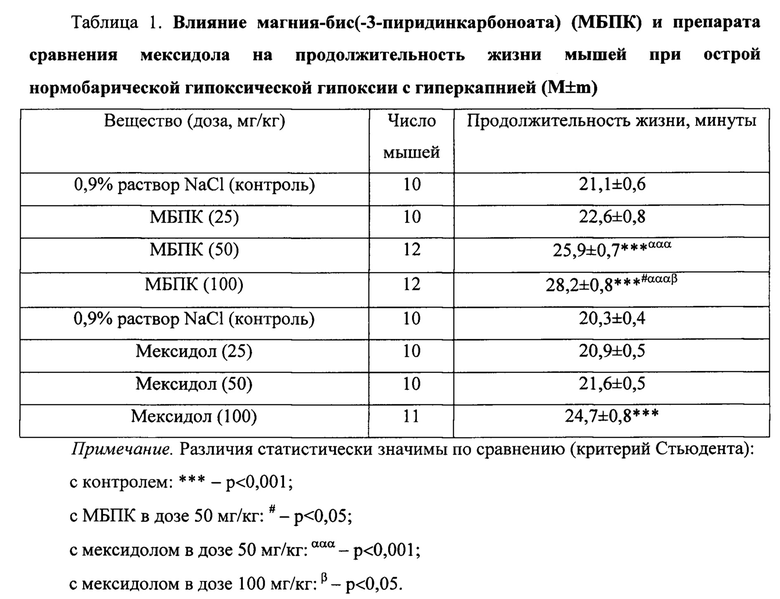
Пример 2. Противогипоксическое действие магния-бис(-3-пиридинкарбоноата) (МБПК) на разных моделях острой гипоксии у мышей (табл. 1-3)
Исследования выполнены на белых мышах-самцах линии BALB/c массой 20-24 г по методикам, описанным в «Методических рекомендациях по экспериментальному изучению препаратов, предлагаемых для клинического изучения в качестве антигипоксических средств» [4] и «Руководстве по проведению доклинических исследований лекарственных средств» [6].
Острую нормобарическую гипоксическую гипоксию с гиперкапнией воспроизводили путем помещения мышей (поодиночке) в термокамеру. Острую гемическую гипоксию воспроизводили путем подкожного (п/к) введения мышам метгемоглобинообразователя натрия нитрита в дозе 300 мг/кг. Острую гистотоксическую гипоксию моделировали путем п/к введения мышам натрия нитропруссида в дозе 20 мг/кг. Острую гипобарическую гипоксию моделировали у мышей в проточно-вытяжной барокамере; животных поднимали со скоростью 50 м/с до «высоты» 11000 м. Регистрировали продолжительность жизни животных. Исследуемое вещество и препарат сравнения мексидол вводили однократно внутрибрюшинно (в/б) за 60 минут до опыта. Животным контрольных групп вводили в/б 0,9% раствор натрия хлорида (NaCl) в том же объеме.
На модели острой нормобарической гипоксической гипоксии с гиперкапнией (в термокамере) МБПК оказывал противогипоксическое действие в зависимости от дозы: в дозе 25 мг/кг существенно не изменял продолжительность жизни животных, а в дозах 50 и 100 мг/кг значимо (р<0,001) увеличивал этот показатель на 23% и 34% соответственно (табл.1). При этом следует подчеркнуть, что указанное вещество в дозе 100 мг/кг по выраженности действия значимо (р<0,05) превосходило свой эффект в дозе 50 мг/кг в 1,1 раза.
Препарат сравнения мексидол в дозах 25 и 50 мг/кг существенно не изменял данный показатель, а в дозе 100 мг/кг значимо (р<0,001) увеличивал его на 22%.
По выраженности противогипоксического действия МБПК в дозе 50 мг/кг значимо (р<0,001) превосходил мексидол в аналогичной дозе в 1,2 раза и не уступал ему в дозе 100 мг/кг; а в дозе 100 мг/кг значимо (р<0,05) превосходил его в аналогичной дозе в 1,1 раза.
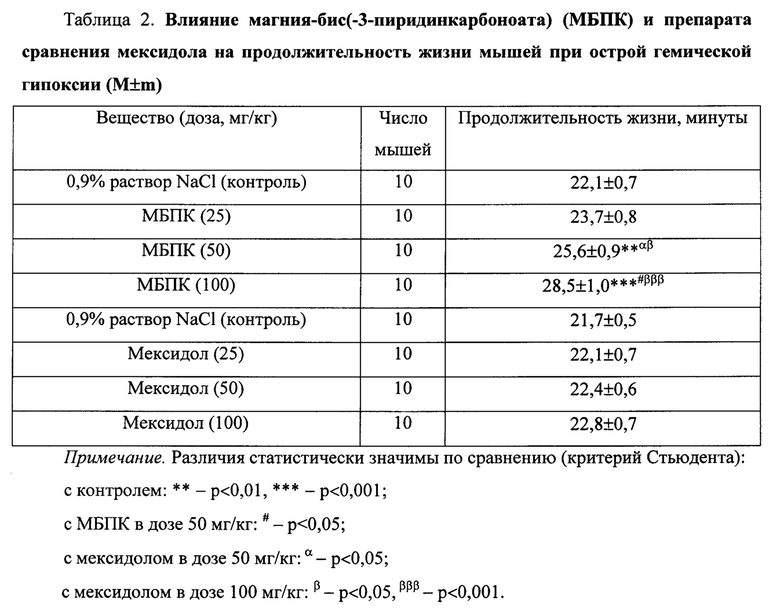
На модели острой гемической гипоксии МБПК, как и на предыдущей модели, оказывал противогипоксическое действие в зависимости от дозы: в дозе 25 мг/кг существенно не изменял продолжительность жизни животных, а в дозах 50 и 100 мг/кг значимо увеличивал этот показатель на 16% (р<0,01) и 29% (р<0,001) соответственно (табл. 2). При этом следует отметить, что указанное соединение в дозе 100 мг/кг по выраженности действия значимо (р<0,05) превосходило свой эффект в дозе 50 мг/кг в 1,1 раза.
Препарат сравнения мексидол в дозах 25, 50 и 100 мг/кг существенно не влиял на данный показатель.
По выраженности противогипоксического действия МБПК в дозе 50 мг/кг значимо (р<0,05) превосходил мексидол в дозах 50 и 100 мг/кг в 1,1 раза, а в дозе 100 мг/кг значимо (р<0,001) превосходил его в аналогичной дозе в 1,2 раза.
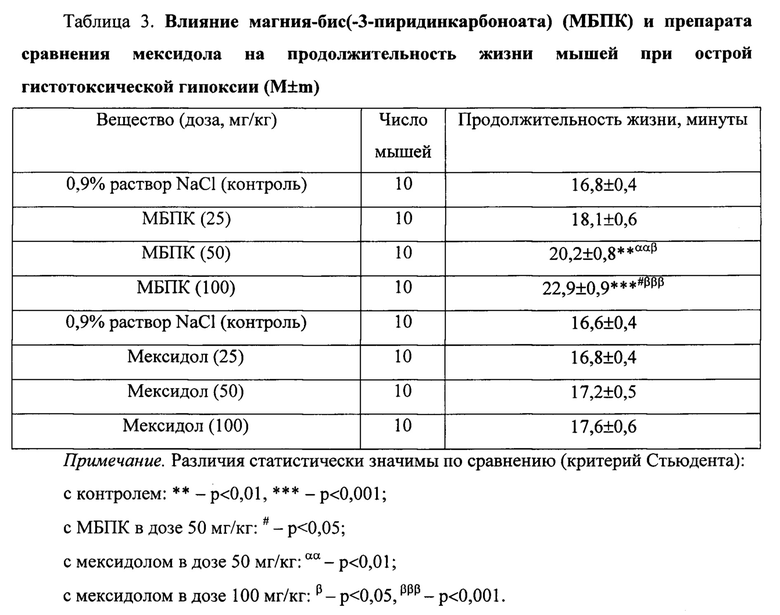
На модели острой гистотоксической гипоксии МБПК, как и на двух предыдущих моделях острой гипоксии, оказывал противогипоксическое действие в зависимости от дозы: в дозе 25 мг/кг существенно не влиял на продолжительность жизни животных, а в дозах 50 и 100 мг/кг значимо увеличивал этот показатель на 20% (р<0,01) и 36% (р<0,001) соответственно (табл.3). При этом следует подчеркнуть, что указанное вещество в дозе 100 мг/кг по выраженности действия значимо (р<0,05) превосходило свой эффект в дозе 50 мг/кг в 1,1 раза.
Препарат сравнения мексидол в дозах 25, 50 и 100 мг/кг существенно не изменял данный показатель.
По выраженности противогипоксического действия МБПК в дозе 50 мг/кг значимо превосходил мексидол в дозах 50 и 100 мг/кг в 1,2 (р<0,01) и 1,1 раза (р<0,05) соответственно, а в дозе 100 мг/кг значимо (р<0,001) превосходил его в аналогичной дозе в 1,3 раза.
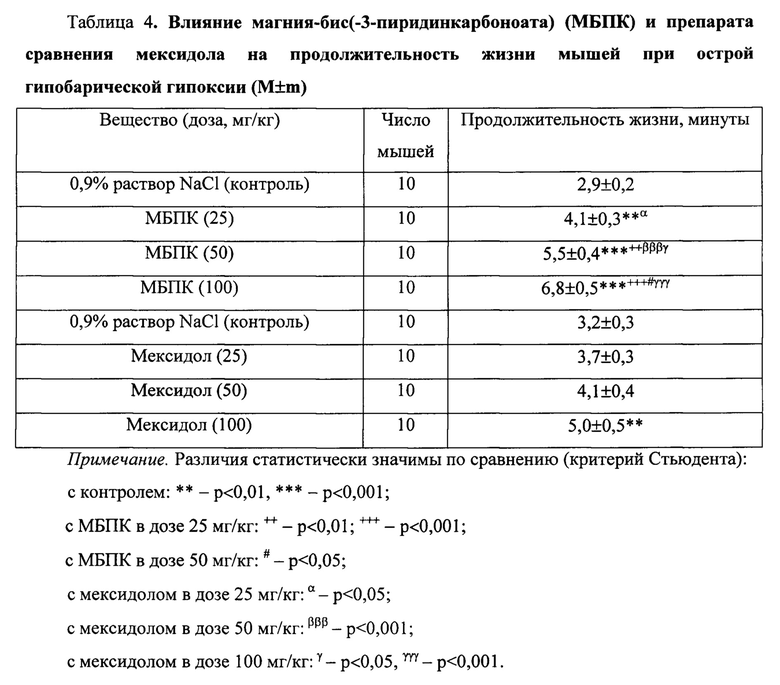
На модели острой гипобарической гипоксии МБПК оказался эффективен во всех 3 испытанных дозах, значимо увеличивая продолжительность жизни мышей в барокамере в дозе 25 мг/кг на 41% (р<0,01), в дозе 50 мг/кг - на 90% (р<0,001), а в дозе 100 мг/кг - на 134% (р<0,001) (табл. 4). При этом выраженность эффектов в каждой дозе статистически достоверно отличалась между собой: так, в дозе 50 мг/кг по выраженности действия данное вещество значимо превосходило свой эффект в дозе 25 мг/кг в 1,3 раза (р<0,01), а в дозе 100 мг/кг - эффект в дозе 25 и 50 мг/кг в 1,7 (р<0,001) и 1,2 раза (р<0,05) соответственно.
Препарат сравнения мексидол в дозах 25 и 50 мг/кг существенно не влиял на данный показатель, а в дозе 100 мг/кг значимо (р<0,01) увеличивал его на 56%.
По выраженности противогипоксического действия МБПК в дозе 25 мг/кг значимо (р<0,05) превосходил мексидол в аналогичной дозе в 1,2 раза и не уступал ему в дозах 50 и 100 мг/кг, в дозе 50 мг/кг значимо превосходил его в дозах 50 и 100 мг/кг в 1,5 (р<0,001) и 1,2 раза (р<0,05) соответственно, а в дозе 100 мг/кг - мексидол в аналогичной дозе в 1,5 раза (р<0,001).
Таким образом, можно заключить, что МБПК обладает выраженными противогипоксическими свойствами на всех изученных моделях острой гипоксии, оказывая эффект в зависимости от дозы. При этом по выраженности противогипоксического действия данное соединение превосходит препарат сравнения мексидол.
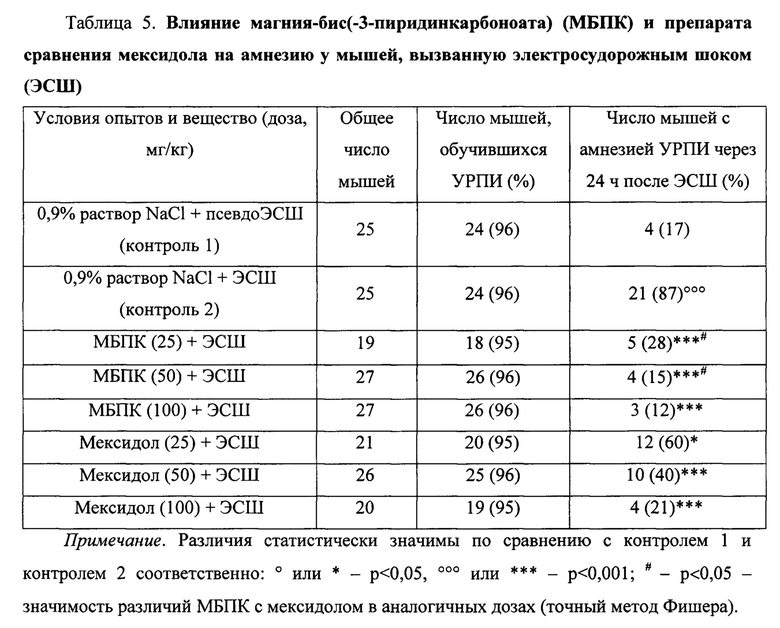
Пример 3. Антиамнестическое действие магния-бис(-3-пиридинкарбоноата) (МБПК) на различных моделях амнезии у мышей (табл. 5-7)
Исследования выполнены на белых мышах-самцах линии BALB/c массой 20-24 г. Влияние МБПК и препарата сравнения мексидола на процессы обучения и памяти у животных исследовали, используя условную реакцию пассивного избегания (УРПИ) электрокожного раздражения [1]. Выработку УРПИ у мышей производили на основе электрокожного подкрепления по методу Cumin et al. (1982) [10] с учетом рекомендаций Mondadori et al. (1990) [15]. Мышей подвергали воздействию электросудорожного шока (ЭСШ) (50 Гц, 50 мА, 0,3 с, транспиннеально) сразу после обучения УРПИ [6]. У животных контрольной группы вызывали псевдоЭСШ. Для воспроизведения модели скополаминовой амнезии м-холиноблокатор вводили мышам в/б в дозе 1 мг/кг сразу после обучения УРПИ [6]. Острую нормобарическую гипоксическую гипоксию с гиперкапнией воспроизводили путем помещения мышей (поодиночке) в термокамеру. Исследуемое соединение и препарат сравнения мексидол вводили однократно в/б за 60 минут до обучения мышей. Животные контрольных групп получали (в/б) в том же объеме 0,9% раствор NaCl. Сохранность УРПИ проверяли через 24 часа после амнезирующего воздействия.
На модели амнезии, вызванной ЭСШ, было установлено, что у мышей МБПК оказался эффективен во всех трех испытанных дозах. Так, он в дозе 25 мг/кг значимо (р<0,001) уменьшал выраженность амнезии в 3,1 раза, а в дозах 50 и 100 мг/кг полностью предупреждал ее развитие (табл.5).
Препарат сравнения мексидол также обладал антиамнестическими свойствами во всех 3 испытанных дозах: в дозах 25 и 50 мг/кг он значимо уменьшал выраженность амнезии в 1,4 (р<0,05) и 2,2 раза (р<0,001) соответственно, а в дозе 100 мг/кг почти полностью предупреждал ее развитие.
По выраженности антиамнестического действия МБПК в дозах 25 и 50 мг/кг значимо (р<0,05) превосходил мексидол в аналогичных дозах в 2,1 и 2,7 раза соответственно, а в дозе 50 мг/кг действовал также как и мексидол в дозе 100 мг/кг.
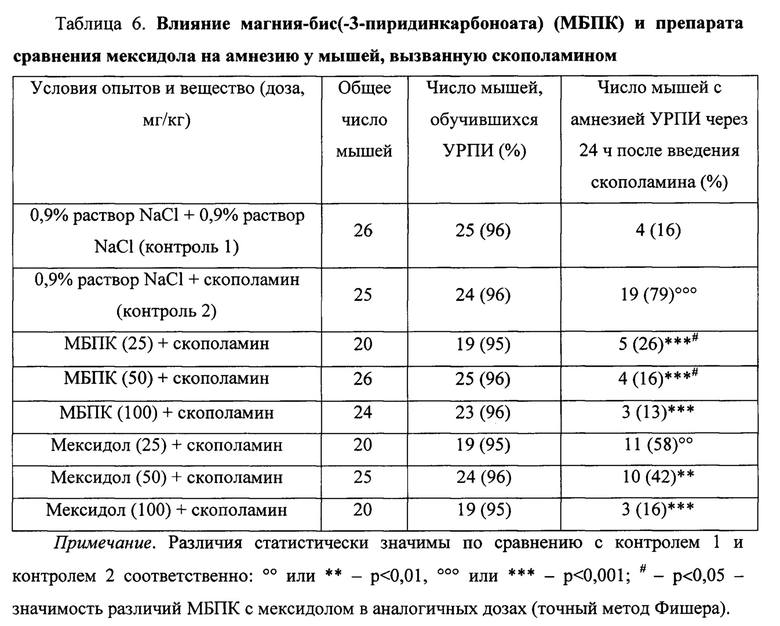
На модели скополаминовой амнезии было обнаружено, что у мышей МБПК, как и на предыдущей модели амнезии, был эффективен во всех трех испытанных дозах: он в дозе 25 мг/кг значимо (р<0,001) ослаблял амнестический эффект в 3,0 раза, а в дозах 50 и 100 мг/кг полностью предупреждало его развитие (табл. 6).
Препарат сравнения мексидол оказывал антиамнестическое действие в дозах 50 и 100 мг/кг, в первой дозе значимо уменьшая выраженность амнезии в 1,9 раза (р<0,001), а во второй - полностью предупреждая ее развитие. В дозе 25 мг/кг он был неэффективен.
По выраженности антиамнестического действия МБПК в дозах 25 и 50 мг/кг значимо (р<0,05) превосходил мексидол в аналогичных дозах в 2,2 и 2,6 раза соответственно, а в дозе 50 мг/кг действовал также как и мексидол в дозе 100 мг/кг.
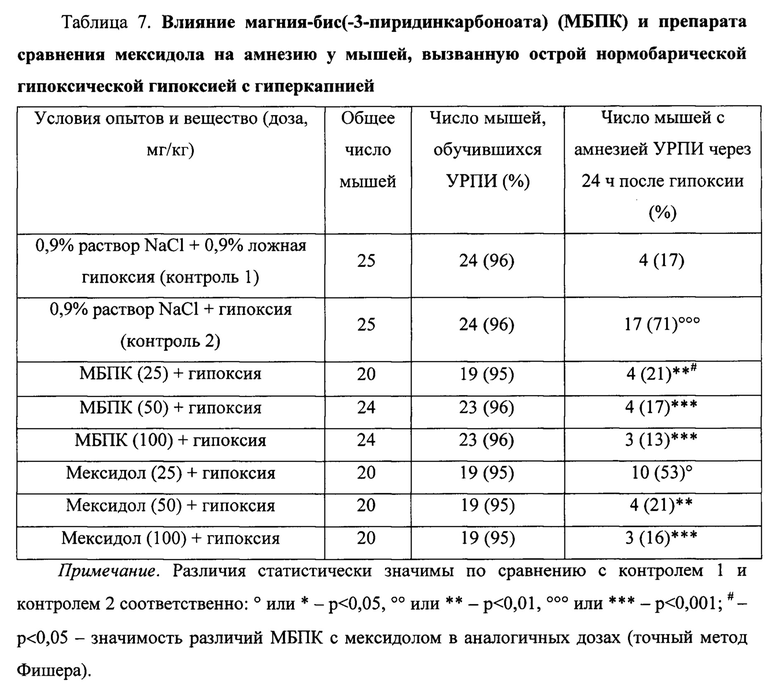
На модели амнезии, вызванной острой нормобарической гипоксической гипоксией с гиперкапнией (в термокамере), было обнаружено, что у мышей МБПК, как и на двух предыдущих моделях амнезии, оказался эффективен во всех трех испытанных дозах. Так, он в дозе 25 мг/кг значимо (р<0,01) уменьшал выраженность амнезии в 3,4 раза, а в дозах 50 и 100 мг/кг полностью предупреждал ее развитие (табл. 7).
Препарат сравнения мексидол обладал антиамнестической активностью в дозах 50 и 100 мг/кг, почти полностью или полностью предупреждая развитие амнезии, а в дозе 25 мг/кг существенно не влияя на ее выраженность.
По выраженности антиамнестического действия МБПК в дозе 25 мг/кг значимо (р<0,05) превосходил мексидол в аналогичной дозе в 2,5 раза, действуя также как и мексидол в дозе 50 мг/кг; а в дозе 50 мг/кг он действовал также как и мексидол в дозе 100 мг/кг.
Итак, МБПК обладает выраженными антиамнестическими свойствами на различных моделях амнезии у мышей (вызванной ЭСШ, скополомином и острой нормобарической гипоксической гипоксией с гиперкапнией). При этом по выраженности антиамнестического действия на первых двух моделях он в дозах 25 и 50 мг/кг превосходил мексидол в аналогичной дозе, а на третьей - только в дозе 25 мг/кг, действуя также как и мексидол в дозе 50 мг/кг. Кроме того, на всех трех моделях амнезии МБПК в дозе 50 мг/кг действовал также как и мексидол в дозе 100 мг/кг.
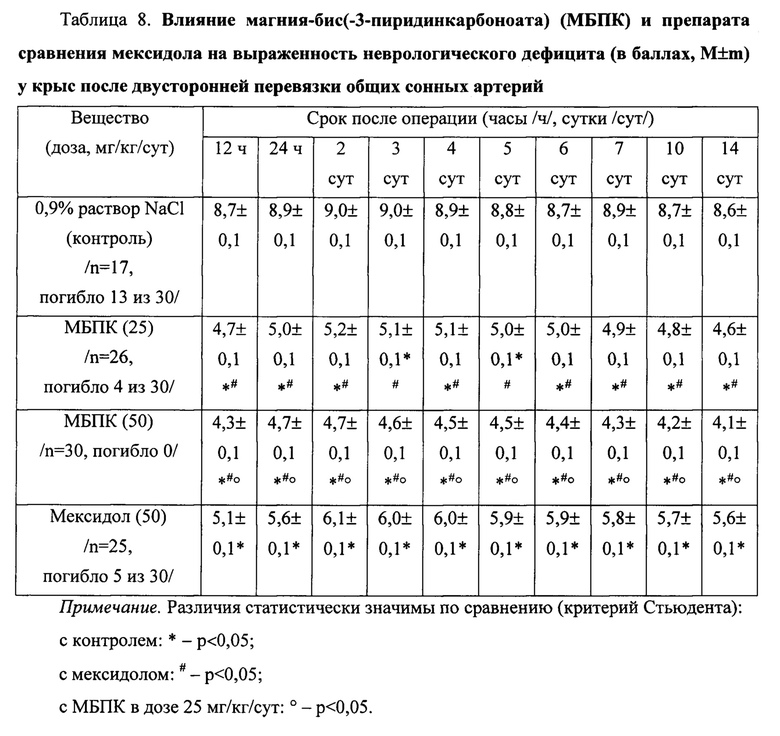
Пример 4. Нейропротекторное действие магния-бис(-3-пиридинкарбоноата) (МБПК) у крыс (табл. 8)
Исследовали нейропротекторное действие МБПК и препарата сравнения мексидола у белых нелинейных крыс-самцов (массой 220-260 г) с экспериментальной ишемией головного мозга (модель ишемического инсульта). В качестве препарата сравнения был выбран мексидол, широко используемый сегодня в неврологии при лечении ишемического инсульта [2, 3]. Ишемию головного мозга у крыс воспроизводили путем одномоментной перевязки (под общей анестезией диэтиловым эфиром) обеих общих сонных артерий с учетом рекомендаций Р.С. Мирзояна и соавт. [5]. У ложнооперированных животных (n=10) операция была ограничена этапом доступа к общим сонным артериям. В контрольной группе крысы получали только 0,9% раствор NaCl в/б. В подопытных группах животным вводили в/б МБПК и мексидол 1 раз в сутки (сут) в течение 7 сут; в первые сутки - через 1 час (ч) после операции. Животных после операции наблюдали в течение 2 недель с учетом выживаемости крыс. Неврологический дефицит (НД) у животных определяли (слепым методом) по шкале McGraw et al. [14] (в баллах) каждый час в течение 24 ч, а затем 1 раз в сутки. Тяжесть состояния определяли по сумме соответствующих баллов. У ложнооперированных животных неврологический дефицит отсутствовал.
Было установлено, что у крыс контрольной группы НД был наиболее выражен (9,0±0,1 балла) через 2 и 3 сут после двусторонней перевязки общих сонных артерий. При этом в контроле погибло 43% (13 крыс из 30) животных (табл. 8).
МБПК в дозе 25 мг/кг/сут в течение 7 суток оказывал нейропротекторное действие, значимо (р<0,05) уменьшая летальность животных до 13% (погибли 4 крысы из 30). Также данное соединение в указанной дозе достоверно (р<0,05) уменьшало и выраженность НД в разные сроки наблюдения в 1,7-1,9 раза (табл. 8).
МБПК в более высокой дозе - 50 мг/кг/сут в течение 7 суток - уменьшал летальность животных до 0%, а выраженность НД в разные сроки наблюдения в 1,9-2,1 раза.
Необходимо отметить, что по выраженности действия в отношении уменьшения НД в разные сроки наблюдения МБПК в дозе 50 мг/кг/сут значимо (р<0,05) превосходил свой эффект в дозе 25 мг/кг/сут в 1,1 раза.
Препарат сравнения мексидол в дозе 50 мг/кг/сут в течение 7 суток также обладал нейропротекторными свойствами, значимо (р<0,05) уменьшая летальность крыс до 17% (погибло 5 животных из 30) и НД в 1,5-1,7 раза (табл. 8).
Следует подчеркнуть, что при этом уровень летальности при использовании МБПК в дозе 50 мг/кг/сут был достоверно (р<0,05) ниже на 17% по сравнению с мексидолом (в аналогичной дозе).
По выраженности действия в отношении уменьшения НД в разные сроки наблюдения МБПК в дозах 25 и 50 мг/кг/сут значимо (р<0,05) превосходил мексидол в 1,1-1,2 и 1,2-1,4 раза соответственно.
Таким образом, можно заключить, что на модели ишемического инсульта у крыс, вызванного одномоментной перевязкой обеих общих сонных артерий, МБПК обладает выраженными нейропротекторными свойствами, превосходя в дозе 50 мг/кг/сут препарат сравнения мексидол в аналогичной дозе по влиянию на летальность животных, а в дозах 25 и 50 мг/кг/сут - в отношении уменьшения выраженности НД.
Итак, МБПК обладает выраженными противогипоксическими свойствами на всех изученных моделях острой гипоксии (острой нормобарической гипоксической гипоксии с гиперкапнией, гемической, гистотоксической и гипобарической). При этом по выраженности противогипоксического действия данное соединение превосходит препарат сравнения мексидол.
На различных моделях амнезии у мышей (вызванной ЭСШ, скополомином и острой нормобарической гипоксической гипоксией с гиперкапнией) МБПК обладает выраженными антиамнестическими свойствами. При этом по выраженности антиамнестического действия указанное вещество также превосходит мексидол.
Кроме того, МБПК обладает выраженными нейропротекторными свойствами на модели ишемического инсульта у крыс, причем по влиянию на летальность и выраженность неврологического дефицита на протяжении всего срока наблюдения МБПК значимо превосходит мексидол.
Таким образом, на различных экспериментальных моделях МБПК превосходит ближайший аналог заявляемого средства мексидол.
Литература
1. Буреш Я., Бурешова О., Хьюстон П.Д. Методики и основные эксперименты по изучению мозга и поведения: пер. с англ./Под. ред. Батуева А.С. - М., Высш. шк., 1991. - 399 с.
2. Воронина Т.А. Пионер антиоксидантной нейропротекции. 20 лет в клинической практике // Рус.мед. журн. - 2016. - Т. 24, №7. - С. 434-438.
3. Машковский М.Д. Лекарственные средства. 16-е изд., перераб., испр. и доп. М.: Новая волна: Издатель Умеренков, 2019. - 1216 с.
4. Методические рекомендации по экспериментальному изучению препаратов, предлагаемых для клинического изучения в качестве антигипоксических средств / Под редакцией Л.Д. Лукьяновой. - М., 1990. - 18 с.
5. Мирзоян Р.С, Плотников М.Б., Ганыпина Т.С.и др. Методические рекомендации по доклиническому изучению лекарственных средств для лечения нарушений мозгового кровообращения и мигрени // Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012. - С. 478-485.
6. Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012. - 944 с.
7. Скворцова В.И., Шетова И.М., Какорина Е.П. и др. Результаты реализации «Комплекса мероприятий по совершенствованию медицинской помощи пациентам с острыми нарушениями мозгового кровообращения в Российской Федерации» // Журн. неврол. и психиатр. - 2018. - Т. 118, №4. - С. 5-12.
8. Суслина З.А., Смирнова И.Н., Танашян М.М. и др. Клиническая эффективность мексидола и влияние его на реологические свойства крови и гемоперфузию головного мозга при хронических формах цереброваскулярных заболеваний. - М., 2002. - 19 с.
9. Суслина З.А., Гулевская Т.С., Максимова М.Ю., Моргунов В.А. Нарушения мозгового кровообращения: диагностика, лечение, профилактика. М.: МЕДпресс-информ., 2016. - 536 с.
10. Cumin R., Bandle E.F., Gamzu Е., Haefely W.E. Effect of the novel compound antiracetam (Ro 13-5057) upon impared learning and memory in rodents // Psychopharmacol. - 1982. - Vol. 78.-P. 104-111.
11. Gasperi V., Sibilano M., Savini I., Catani M.V. Niacin in the central nervous system: an update of biological aspects and clinical applications // Int. J. Mol. Sci. 2019. - V. 20, No 4. -pii: E974.
12. Kuriakose D., Xiao Z. Pathophysiology and treatment of stroke: present status and future perspectives // Int. J. Mol. Sci. - 2020. - Vol. 21, No 20:7609.
13. Leng Т., Xiong Z.G. Treatment for ischemic stroke: From thrombolysis to thrombectomy and remaining challenges // Brain Circ. 2019. - Vol.5, No 1. - P. 8-11.
14. McGraw C.P., Pashayan A.G., Wendel O.T. Cerebral infarction in the Mongolian gerbil exacerbated by phenoxybenzaminetreatment // Stroke. - 1976 - Vol.7, No 5. - P. 485-488.
15. Mondadori C., Bhatnagar A., Borkovski J., Hausler A. Involvement of a steroidal component in the mechanism of action of piracetam-like nootropics // Brain Res. - 1990. - Vol. 506 - P. 101-108.
16. Schandelmaier S., Briel M., Saccilotto R. et al. Niacin for primary and secondary prevention of cardiovascular events // Cochrane Database Syst. Rev. - 2017. - No 6:CD009744.
17. Sharma A., Madan N. Role of niacin in current clinical practice // Minerva Med. - 2019. -V. 110, No l. - P. 79-83.
| название | год | авторы | номер документа |
|---|---|---|---|
| НЕЙРОТРОПНОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ, АНТИАМНЕСТИЧЕСКОЙ И ВЕСТИБУЛОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2547728C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АКТОПРОТЕКТОРНОЙ, ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ, АНТИАМНЕСТИЧЕСКОЙ И ТЕРМОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2460529C1 |
| НЕЙРОТРОПНОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИОКСИДАНТНОЙ, ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ, АНТИАМНЕСТИЧЕСКОЙ И ПРОТИВОУКАЧИВАЮЩЕЙ АКТИВНОСТЬЮ И СПОСОБНОСТЬЮ УЛУЧШАТЬ КОГНИТИВНЫЕ ФУНКЦИИ | 2008 |
|
RU2394816C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ И АНТИАМНЕСТИЧЕСКОЙ АКТИВНОСТЬЮ И ПОВЫШАЮЩАЯ ФИЗИЧЕСКУЮ РАБОТОСПОСОБНОСТЬ | 2010 |
|
RU2435605C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ И АНТИАМНЕСТИЧЕСКОЙ АКТИВНОСТЬЮ И ПОВЫШАЮЩАЯ ФИЗИЧЕСКУЮ РАБОТОСПОСОБНОСТЬ | 2010 |
|
RU2425670C1 |
| КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ НЕЙРОПРОТЕКТИВНОЙ, АНТИАМНЕСТИЧЕСКОЙ, ПРОТИВОГИПОКСИЧЕСКОЙ И ПРОТИВОИШЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2006 |
|
RU2440132C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 2022 |
|
RU2797210C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ОСТРЫХ И ХРОНИЧЕСКИХ НАРУШЕНИЙ МОЗГОВОГО КРОВООБРАЩЕНИЯ, ПРИМЕНЕНИЕ И СПОСОБ ЛЕЧЕНИЯ | 2011 |
|
RU2468813C1 |
| СРЕДСТВО С ПАНКРЕО- И ГЕПАТОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ ДЛЯ ПАРЕНТЕРАЛЬНОГО ВВЕДЕНИЯ | 2017 |
|
RU2662324C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ И АНТИМНЕСТИЧЕСКОЙ АКТИВНОСТЬЮ И ПОВЫШАЮЩАЯ ФИЗИЧЕСКУЮ РАБОТОСПОСОБНОСТЬ | 2013 |
|
RU2564008C2 |
Настоящее изобретение относится к магнию-бис(-3-пиридинкарбоноату), обладающему противогипоксической, антиамнестической и нейропротекторной активностью. Также настоящее изобретение относится к применению соединения для профилактики и лечения гипоксий различного генеза и ишемического инсульта. Техническим результатом настоящего изобретения является создание нового средства, обладающего противогипоксической, антиамнестической и нейропротекторной активностью. 2 н.п. ф-лы, 4 пр., 8 табл.
1. Магния-бис(-3-пиридинкарбоноат), обладающий противогипоксической, антиамнестической и нейропротекторной активностью.
2. Применение соединения по п. 1 для профилактики и лечения гипоксий различного генеза и ишемического инсульта.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ И АНТИАМНЕСТИЧЕСКОЙ АКТИВНОСТЬЮ И ПОВЫШАЮЩАЯ ФИЗИЧЕСКУЮ РАБОТОСПОСОБНОСТЬ | 2010 |
|
RU2425670C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГИПОКСИЧЕСКИМ, ПРОТИВОИНСУЛЬТНЫМ, УЛУЧШАЮЩИМ ПАМЯТЬ ДЕЙСТВИЕМ | 2007 |
|
RU2326665C1 |
| СРЕДСТВО, ОКАЗЫВАЮЩЕЕ НЕЙРОПРОТЕКТОРНОЕ ДЕЙСТВИЕ В ОСТРОМ ПЕРИОДЕ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЫ | 2009 |
|
RU2414901C2 |
| КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ НЕЙРОПРОТЕКТИВНОЙ, АНТИАМНЕСТИЧЕСКОЙ, ПРОТИВОГИПОКСИЧЕСКОЙ И ПРОТИВОИШЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2006 |
|
RU2440132C2 |
| US 5780512 A1, 14.07.1998 | |||
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ ЭТИЛМЕТИЛГИДРОКСИПИРИДИНА СУКЦИНАТА И ПИРИДОКСИНА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 2008 |
|
RU2405552C2 |
Авторы
Даты
2021-06-28—Публикация
2020-11-20—Подача