Изобретение относится к медицине, а именно к лазерным катетерам длля внутрисосудистого облучения крови.
Известен способ лечения атеросклероза, в котором используется He-Ne лазер со съемным многоцелевым световодным катетером для лечения атеросклероза [1]
Недостатком аналога является функциональная ограниченность, низкая оперативность и надежность.
Известен лазерный аппарат для внутривенного облучения крови АЛОК-1, выбранный в качестве прототипа, содержащий малогабаритный He-Ne лазер с выходной мощностью излучения 2 мВт, длиной волны 0,63 мкм. Лазерное излучение передается в кровеносный сосуд через гибкий моноволоконный световод с наружным диаметром 1 мм.
Недостатком прототипа является функциональная ограниченность, низкая оперативность и надежность. Это обусловлено тем, что в устройствах аналога и прототипа используются только источник света λ0,63 мкм.
Технический эффект расширение функциональных возможностей с высокой оперативностью и надежностью.
Это достигается тем, что в камере вдоль оптической оси последовательно установлены трехкомпонентные управляемые по интенсивности лазерные источники, светосместитель, цилиндрическая управляемая пьезокерамическая ячейка, причем электрические выходы последних подключены к блоку управления, а на выходе устройства установлен канализатор-фокон, являющийся одновременно внутрисосудистым катетером.
Сопоставительный анализ с прототипом показывает, что заявляемый акустооптический внутрисосудистый многокомпонентный лазерный катетер отличается тем, что устройство содержит трехкомпонентный источник света, сместитель света и цилиндрическую пьезокерамическую ячейку, при этом сместитель позволяет формировать световые потоки в зависимости от стимула в различных сочетаниях трех спектральных составляющих, а цилиндрическая пьезокерамическая ячейка модулирует проходящие потоки, образуя модулированное акустооптическое трехкомпонентное излучение для локальной концентрации энергии, обеспечивая толерантные дозы действия внутри сосудов.
На фиг.1 представлена блок-схема предлагаемого катетера.
В камере 1 оптически последовательно установлены трехкомпонентные лазерные источники 2, светосместитель 3, цилиндрическая пьезокерамическая ячейка 4, которые своими электрическими выходами подключены к входу блока 5 управления, а на выходе установлен канализатор-фокон 6, являющийся внутрисосудистым катетером.
Катетер работает следующим образом.
Лазерный источник 2 света, содержащий три источника света, отличающийся по длине волны, формирует потоки вида;
A{x,y,f( λ1)}lAo(x,y)lcos[2πf( λ1)t +Θ ( λ1)] красный
A{x,y,f( λ2)}lAo(x,y,f( λ2)|cos[2 πf( λ2)+ + Θ ( λ2) зеленый
λ3)}lAo(x,y,f( λ3)lcos[2 πf (λ3)t+ Θ ( λ3 )] синий (1)
где Ao(x,y,f( λ1)), Ao(x,y,f( λ2), Ao(x,y,f( λ3)) управляемые по интенсивности световые потоки;
f( λ1), f( λ2), f( λ3) частота световых потоков, соответствующих длине волны λ1 λ2 λ3;
Θ (λ1), Θ (λ2), Θ (λ3), фазы соответствующих волн, которые поступают на светосместитель 2.
В зависимости от цели клинических исследований светосместитель 2, управляемый блоком 5, формирует одно из сочетаний цветов по λi интенсивности, определяемый функционалом
f(λi)  [λ1, λ2, λ3; λ1λ2, λ1λ3, λ2λ3; λ1λ2λ3}
[λ1, λ2, λ3; λ1λ2, λ1λ3, λ2λ3; λ1λ2λ3}
Сформирование возможных значений предопределяется единичным стимулом, соответствующим белому цвету, компоненты которого численно равны:
A{x,y,f( λ1)} (красный) λ1700 ммк в 1 молюмен
A{x,y,f( λ2)} (зеленый) λ2=546,1 ммк в 1 молюмен
A{x,y,f( λ3)} (синий) λ3453,8 ммк в 1 молюмен
Цветовое уравнение, соответствующее сумме единиц красного, синего, зеленого цветов и образующее единичное цветовое уравнение или единичный стимул представляется в виде
F(x,y,f(λ ))=rlA{x,y,f( λ1)}+glA{x,y,f ( λ2)}+blA{x,y,f( λ3) (3)
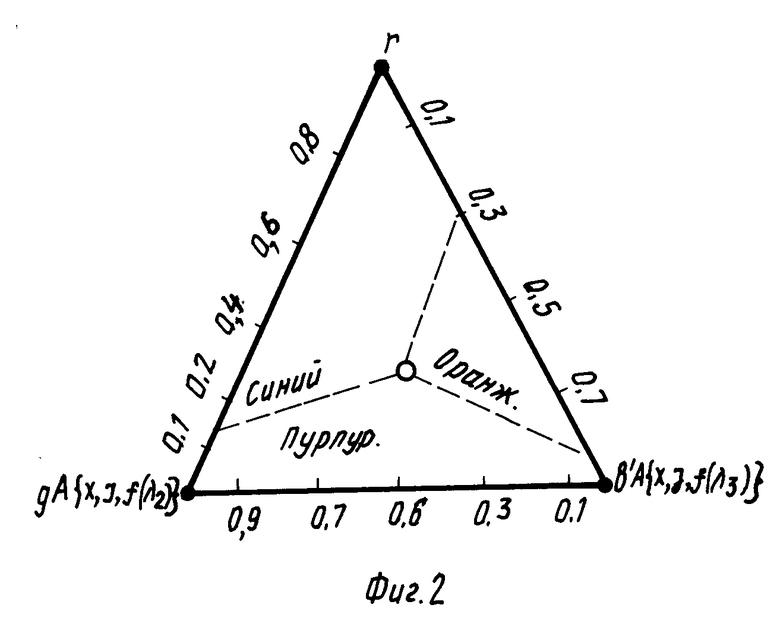
Данное уравнение является уравнением управления светосмесителя блоком 5. Более широкое цветовое поле можно воспроизвести, если использовать в управлении блока 5 формирователь цветного треугольника, представленного на фиг.2. Цвета, получаемые смещением двух основных цветов без участия третьего, располагаются по сторонам треугольника. Всякий цвет, получаемый сочетанием всех трех основных цветов, будет изображаться на диаграмме точкой, лежащей внутри треугольника. Положение этой точки определяется тем, что она представляет собою центр тяжести треугольника, если в его вершинах поместить основных три цвета, вес которых пропорционален r', b', g' в соответствии с условием (2). На основе принципа цветового треугольника блок 5 управления формирует любое сочетание цветов, не ограничиваясь только трехкомпонентным раздельным влиянием цветов f( λ1), f( λ2), f( λ3) на заболевание. Влияние, которое оказывает каждый из компонентов красный, синий, зеленый на заболевание представлено в клинических результатах исследования. Однако необходимость более широкого рассмотрения вопроса влияния спектральных составляющих и соответственно разработка цветового треугольника с целью выработки сигнала управления блоком 5 для воздействия на светосместитель, предопределяется тем, что человеческий организм в трехмерном пространстве всю спектральную составляющую семи цветов воспринимает избирательно. Следовательно, влияние каждого из спектральных составляющих на организм в соответствующих дозах в целом является необходимым условием его существования. Таким образом, разработка треугольника цветов с целью использования для внутрисосудистого воздействия всех спектральных составляющих является предопределяющим фактором клинических исследований.
Сфоpмиpованный светосместителем 2 световой поток, представляемый в виде
Φ{x,y,f)λi)} 0

поступает на вход пьезокерамической цилиндрической ячейки 4, управляемый электрическим сигналом с блока 5 управления, электрический сигнал
U=Umjcos2 π fjt (5)
где Umj управляемая амплитуда
fj частота, управляемая по j
создает посредством цилиндрической ячейки 4 акустические волны сжатия в пространстве R(x, y, t) где R радиус цилиндра. Следствием сжатия световые потоки (4), проходящие через ячейку 4, модулируются по фазе в соответствии с выражением:
H(x,y,t) 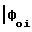 {x,y,f(λi)}
{x,y,f(λi)}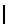 cos[2πf(λi)t+
cos[2πf(λi)t+ 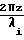 no+Δncos2πfjt}
no+Δncos2πfjt}
где Н(х,y,t) амплитуда выходной волны, с (4);
Φoix,y,f( λi) амплитуда падающей световой волны (4);
Δ n приращение показателя, вызванное волной сжатия акустического поля;
Z протяженность области взаимодействия (4).
Учитывая, что падающий световой поток (4) символизирует равномерное облучение всей акустической ячейкой, то индекс модуляции, который связывает амплитуду прошедшей волны с амплитудой падающей световой волны, определяемый выражением
mj (-j)iJ
(-j)iJ 2π
2π 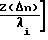
где Ji(. ) функция Бесселя I-го рода представляется функцией управления блока 5. Из (7) видно, что при больших значениях Δ n и Z индекс модуляции велик. В практической сфере стремятся, чтобы Z было бы наибольшим, так как это существенно уменьшает потери световой энергии.
Управляющий сигнал с блока 5 также должен характеризовать связь с пространственной частотой f( λ1) и длиной акустической волны. Длина акустической волны внутри ячейки 4 выбирается из условия Λ 
Отсюда пространственная частота
f( λi)=1/
дает важное соотношение между пространственными частотами (4) и временными частотами (5), т.е.
1/^j j=fi/V, (5)
каждой временной частоте, содержащейся в приложенном сигнале (5), соответствует генерируемая ячейкой 4 пространственная частота. Отсюда следует, что управляющий сигнал с блока 5 осуществляет связь между физическими параметрами света (4) в процессе его распространения. Световой акустооптический модулированный поток поступает на вход канализатора-фокона 6, который, в свою очередь, служит внутрисосудистым катетером.
Экспериментальные исследования заявляемого акустооптического многокомпонентного лазерного катетера показали, что по сравнению с прототипом заявляемый катетер имеет более широкое применение и сферу его использования в медицине трудно переоценить.
Электромагнитные волны для внутрисосудистого воздействия используются в данном устройстве с более широких позиций, необходимых в медицинской практике. При воздействии лучей (1) в отдельности или в сочетании происходит процесс поглощения или прекращения действия электромагнитного колебания. Учитывая, что кровь является сложным биохимическим субстратом, в котором содержится ряд ферментов, световой поток (1) воспринимается различными структурами неоднородно, т. е. селективно. Эритроциты, масса которых соответствует примерно 60-70% массы крови, в целом поглощают длину волны λ0,63 нкм и поэтому можно считать применение красного лазера целесообразным. Спектры поглощения оставшихся 30-35% форменных элементов (а при различных заболеваниях их масса достигает 40-50%) то же селективны к длинам световых волн зеленому, синему или их вариациям. После проведенных клинических исследований с позиций поглощения света (1) с точки зрения молекулярной теории можно утверждать, что ультразвуковое поле, создаваемое заявляемым устройством, предназначено для локальной концентрации энергии в заданной области, обеспечивая совместно с оптическим потоком толерантные дозы в тех областях, где интенсивное ультразвуковое воздействие нецелесообразно. Акустическое поле внутри кровеносных сосудов позволяет возбуждать пространство, подготавливая его для воздействия лазерного излучения. Акустическое поле является активатором и, изменяя в заданных пределах интенсивность и частоту излучения, можно использовать как внутрисосудистый массаж.
Результаты медицинских исследований.
П р и м е р 1. Больной Г.Л. 45 лет, поступил в стационар с диагнозом: инфаркт миокарда, передне-боковой стенки левого желудочка. Сразу после госпитализации больному пунктирована подключичная вена, установлен катетер и начато облучение крови. После окончания процедуры отмечено уменьшение нарушений ритма сердца, снижалась активность МБ-креатинфосфокиназы со 140 ме/л до ЭСМЕ/Л, общей креатинфосфокиназы с 900 до 62% ме/л. Отмечалось снижение активности перекисного окисления липидов крови, что проявлялось в уменьшении малонового диальдегида с 4,21 до 2,42 нм/мл, а диеновые коньюгаты уменьшались с 8,4 до 5,2 нм/мл. Вместе с этим повышалась активность ферментов каталазы с 5,72 до 7,11 нм/мин/мг и супероксиддисмутазы с 0,74 до 1,30 ед. Срок активации больного уменьшился на 3 дня, а выписан был на 5 дней раньше общепринятых сроков госпитализации.
П р и м е р 2. Больной З.Г. 62 года, поступил в стационар с диагнозом: ишемическая болезнь сердца, нестабильная стенокардия, атеросклероз аорты, атеросклеротический кардиосклероз, сахарный диабет средней тяжести, инсулинзависимый. Поступил с жалобами на загрудные боли при ходьбе и в покое, до 20 приступов в сутки, купирующиеся приемом нитроглицерина (до 45 таблеток в сутки) на фоне приема сустака форте, корватона и нитрогранулонга 4 раза в день. Больному проведено облучение крови. В результате лечения пациент уменьшил прием нитроглицерина с 45 до 12 таблеток в сутки. Загрудные боли значительно уменьшились, повысилась толерантность к нагрузке. На ЭКГ отмечалось улучшение коронарного кровообращения в области боковой стенки левого желудочка.
П р и м е р 3. Больной М.Х. 63 года, находился на стационарном лечении с диагнозом: ишемическая болезнь сердца, нестабильная стенокардия. При поступлении жаловался на приступы загрудных болей, для купирования которых в сутки получал до 25 таблеток нитроглицерина, 4 таблеток сустака форте, 60 мг обзидана. В 1987 году перенос трансмуральный переднебоковой инфаркт миокарда. В течение последнего месяца загрудные боли участились, увеличилось также и количество принимаемых медикаментозных средств, в связи с чем больной был госпитализирован. Проведено внутрисердечное облучение крови. Самочувствие больного значительно улучшилось, загрудные боли прекратились, снизилось потребление нитроглицерина до 10 таблеток в сутки. Биохимические показатели крови улучшились. После выписки из стационара больной приступил к работе.
| название | год | авторы | номер документа |
|---|---|---|---|
| Интерференционное вычислительное устройство | 1981 |
|
SU1012285A1 |
| Устройство для измерения высокого напряжения | 1983 |
|
SU1126882A1 |
| СПОСОБ ОБНАРУЖЕНИЯ ОПТИЧЕСКИХ И ОПТИКО-ЭЛЕКТРОННЫХ СРЕДСТВ НАБЛЮДЕНИЯ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2013 |
|
RU2524450C1 |
| Устройство для разрушения атеросклеротических отложений в сосудах | 1986 |
|
SU1461428A1 |
| Многоканальный оптико-электронный ковариатор | 1976 |
|
SU638984A1 |
| УСТРОЙСТВО ДЛЯ РАСПОЗНАВАНИЯ ОПТИЧЕСКИХ ДИФРАКЦИОННЫХ МЕТОК | 1998 |
|
RU2208248C2 |
| Электронно-оптическое время-импульсное вычислительное устройство | 1975 |
|
SU608180A1 |
| ЛИНЗА ВВОДА-ВЫВОДА, ОСВЕТИТЕЛЬНОЕ УСТРОЙСТВО И ЭЛЕКТРОННОЕ УСТРОЙСТВО | 2009 |
|
RU2473933C1 |
| Оптико-электронный анализатор спектра | 1976 |
|
SU643809A1 |
| Оптическая система формирования и наведения лазерного излучения | 2016 |
|
RU2663121C1 |

Изобретение относится к медицине, а именно к медицинской технике. Технологический эффект - расширение функциональных возможностей с высокой оперативностью и надежностью. Внутрисосудистый лазерный катетер содержит трехкомпонентные управляемые по интенсивности лазерные источники (или перестраиваемые источники), светосмеситель, цилиндрическую управляемую пьезокерамическую ячейку, причем электрические выходы последних подключены к блоку управления, а на выходе катетера установлен катализатор-фокон, являющийся одновременно внутрисосудистым катетером. Новым является то, что предлагаемый катетер содержит трехкомпонентный источник света, смеситель света и цилиндрическую пьезокерамическую ячейку, смеситель позволяет формировать световые потоки в зависимости от стимула в различных сочетаниях трех спектральных составляющих, а цилиндрическая пьезокерамическая ячейка модулирует проходящие потоки, образуя модулированное акусто-оптическое трехкомпонентное излучение для локальной концентрации энергии, обеспечивая толерантные дозы действия внутри сосудов. 2 ил.
ВНУТРИСОСУДИСТЫЙ ЛАЗЕРНЫЙ КАТЕТЕР, содержащий гелий-неоновый лазер и световод, отличающийся тем, что в катетер дополнительно введены лазерные источники синего и зеленого цвета для образования перестраиваемого лазера, смеситель света, цилиндрическая пьезокерамическая ячейка, которые оптически последовательно соединены между собой и электрические входы которых подключены к блоку управления, а на выходе установлен канализатор-фокон акустикооптического модулированного поля.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Медицинская техника, 1990, N 1, с.42 и 43. | |||
Авторы
Даты
1995-04-10—Публикация
1991-07-05—Подача