Изобретение относится к способу получения замещенных ароматических нитрилов путем взаимодействия ароматических карбоновых кислот с газообразным аммиаком в присутствии катализатора дегидратации.
Простые ароматические нитрилы, как нитрил никотиновой кислоты и нитрил терефталевой кислоты, представляют собой важные промежуточные продукты в органической промышленной химии. Соответственно замещенные ароматические нитрилы, например 4-(транс-4-пропилциклогексил) бензонитрил (жидкий кристалл), также могут быть высокоценными целевыми продуктами.
В случае получаемых в крупном промышленном масштабе ароматических нитрилов, в качестве способа получения доминирует окисление с аммиаком, в случае метилароматических соединений взаимодействие с аммиаком и кислородом в присутствии катализатора.
Известно, что, например, п- и м-ксилол благодаря окислению с аммиаком переводят в соответствующие динитрилы, а нитрил никотиновой кислоты получают из 3-пиколина по этому способу (K. Weissermel и H. -J. Arpe, Industrielle Organishe Chemie, 3-е изд. с. 422, VCH, 1988).
Известны способы получения фталодинитрила из бистрихлорбензонитрила и аммиака в присутствии катализатора, а для получения изофталонитрила путем взаимодействия изофталоилхлорида с аммиаком в присутствии катализатора.
Для получения алифатических нитрилов, например нитрилов жирных кислот, оcущеcтвляетcя взаимодейcтвие cоответcтвующих киcлот с аммиаком в присутствии катализатора при температуре 250-550оС.
Известны способы получения окси- и аминобензонитрилов из соответствующих сложных эфиров бензойной кислоты с помощью аммиака в присутствии катализаторов.
В противоположность этому, предлагаемые исходные продукты это свободные, замещенные ароматические карбоновые кислоты, заместители которых на основании реакционных условий склонны к реакциям изомеризации, диспропорционирования или трансалкилирования.
Получение замещенных ароматических нитрилов с алифатическими боковыми цепями, которые в случае необходимости содержат также гетероатомы, как кислород, или центр хиральности в боковой цепи и другие заместители в ароматическом кольце (например, атомы галогенов), из соответствующих кислот при указанных условиях до сих пор неизвестно. Известно, что в случае алкилароматических соединений, например ксилол, в области 200-260оС в присутствии цеолитных катализаторов и при 400-500оС в присутствии Al2O3 SiO2 возможны как изомеризации, так и диспропорционирования и трансалкилирования. Возможны также реакции карбонизации.
В то время как алифатические жирные кислоты ни в виде свободной кислоты, ни в виде соли не могут декарбоксилироваться (например, J. March, Advanced Organic Chemistry, с. 562, 1985), известно, что ароматические карбоновые кислоты декарбоксилируются при повышенных температурах, например при нагревании с медью и солями меди в хинолине, при нагревании с сильными кислотами и при нагревании их солей. Кроме того, ароматические карбоновые кислоты изомеризуются при нагревании в присутствии солей цинка и кадмия.
Такие замещенные нитрилы, в общем, получают тем, что сначала строится основное "тело" молекулы, которое составляется из стерически единой, алифатической и ароматической или гетероциклической части. Затем путем бромирования ароматического соединения и последующего замещения брома на СN (например, с помощью цианида меди) получают нитрил. Если ароматическая часть уже содержит карбоксильную группу, то циано-группу вводят путем трехстадийной реакционной последовательности (хлорангидрид кислоты, амид, нитрил). Например, получают п-(транс, транс-4-алкилбициклогексил)-3-фторбензонитрилы таким образом, только с выходом 14% (например, Е. Poetsch, Kontakte, 1988, 2, с. 21).
Дальнейшими важными способами получения замещенных ароматических нитрилов являются дегидратация соответствующих альдоксимов и введение нитрильной группы по Зандмейеру.
Всем указанным способом с промышленной точки зрения присущи различные недостатки. Так, при введении нитрильной группы с помощью высокоядовитого цианида меди образуются состоящие из бромида меди и избыточного цианида меди плохо удаляемые отходы.
Многостадийные способы, как переведение кислот через хлорангидриды и амиды в нитрилы, очень дорогостоящие. В зависимости от используемых реагентов также образуются вызывающие проблемы отходы, как SO2 и HCl, при использовании тионилхлорида или фосфорной кислоты, и HCl при использовании POCl3 или PCl3.
Реакции Зандмейера присущи многочисленные отягчающие недостатки, здесь необходим большой избыток цианида. На основании водосодержащей реакционной смеси в случае аминов с большим неполярным остатком нужно работать в суспензии, что зачастую отрицательно влияет на превращение и скорость реакции. Также здесь образуются значительные количества цианидсодержащих солей меди в качестве отходов.
Задачей изобретения являлась разработка способа получения замещенных ароматических нитрилов, который не обладает или обладает только в незначительной мере описанными недостатками прежних способов.
Замещенные бензойные пиридинкарбоновые и пиримидинкарбоновые кислоты с высоким выходом (путем введения во взаимодействие с аммиаком в присутствии катализатора при 200-350оС) можно переводить в соответствующие замещенные ароматические нитрилы, причем в достойной упоминания степени не наступают снижающие выход побочные реакции.
При этой реакции из карбоновой кислоты и аммиака in situ получают соответствующие амиды, которые дегидратируют до нитрила. Эти амиды можно также дегидратировать непосредственно по предлагаемому способу.
Предметом изобретения является способ получения замещенных ароматических нитрилов, состоящий в том, что замещенные ароматические карбоновые кислоты вводят во взаимодействие с газообразным аммиаком в присутствии катализатора дегидратации.
Понятие замещенные ароматические нитрилы охватывает замещенные бензонитрилы, замещенные пиридин- и пиримидинкарбонитрилы, а также замещенные и незамещенные цианнафталины.
В качестве заместителей принимают во внимание линейные и разветвленные алкильные и оксиалкильные группы (также хиральные), циклоалкильные группы, как циклогексил и алкил- и оксаалкилциклогексил, фенильные, алкилфенильные и оксаалкилфенильные группы, а также соответствующие пиридильные и пиримидильные группы. Фенильное кольцо наряду с алкильной группой может содержать еще другие заместители, например галогены, в особенности фтор и хлор.
По предлагаемому способу можно получать ароматические нитрилы формулы I
R (AI ZI/m (A2 Z2)n Ar CN (I) где R H галоген, СN, незамещенный, однократно замещенный CN или CF3или, по крайней мере, однократно замещенный галогеном алкильный или алкенильный остаток с 1-15 атомами, причем в этих остатках также одна или несколько СH2-групп, смотря по обстоятельствам, независимо друг от друга, могут быть заменены -S-, -O-, -CO-, так, что S- и/или О-атомы непосредственно друг с другом не связаны.
А1 и А2, cмотря по обстоятельствам, независимо друг от друга, обозначают:
(а) транс-1,4-циклогексильный остаток, где также одна или несколько не соседних СН2-групп могут быть замещены -О- или -S-,
(б) 1,4-фениленовый остаток, где одна или две СН-группы могут быть заменены на N,
(в) остаток из группы 1,4-циклогексилена, 1,4-бицикло-(2,2,2)-октилена, пиперидин-1,4-диила, нафталин-2,6-диила декагидронафталин-2,6-диила и 1,2,3,4-тетрагидронафталин-2,6-диила,
Ar 1, 4-фениленовый, нафталин-2,6-диильный, пиридин-2,5-диильный или пиримидин-2,5-диильный остаток, причем остатки (а), (б) и Ar могут быть замещены СN или галогеном,
Z1 и Z2, смотря по обстоятельствам, независимо друг от друга, обозначают -СН2-CН2-OCH2-, -CH2O-, однократную связь, m и n, смотря по обстоятельствам, независимо друг от друга, обозначают 0,1 или 2.
Ради упрощения далее Phe обозначает 1,4-фениленовую группу, где также одна или две CH-группы могут быть заменены на N, причем 1,4-фениленовая группа также может быть замещена одним или двумя атомами галогена и/или CN-группами, Сy обозначает 1,4-циклогексиленовую группу, где также одна или две из не соседних CH2-групп могут быть заменены -S- и/или О-атомами.
Эти замещенные 1,4-фениленовые группы предпочтительно представляют собой 2-фтор, 3-фтор или 2,3-дифторфениленовые группы.
Выше и в последующем R, A1, A2, A, Z1, Z2, m и n имеют указанное значение, если не указано ничего другого.
Получаемые по предлагаемому способу соединения формулы I охватывают таковые формулы Ia Ik: R-A1-Phe-CN (1a); R-A1-Z1-Phe-CN (1b); R-A1-A2-Phe-CN (1с); R-A1-A2-Z2-Phe- -CN (1d). R-A1-Z1-A2-Phe-CN (1e); R-A1-Z1-A2-Z2--Phe-CN (1f); R-A1-A1-A2-Phe-CN (1g); R-A1-Z1-A1-A2--Phe-CN (1h); R-A1-A1-Z1-A2-Phe-CN (1i); R-A1-A1-A2-Z2-Phe-CN (1j); R-A1-Z1-A1-A2-Z2-Phe-CN (1k).
Из них предпочтительны особенно соединения формул Ia, Ib, Ic, Id и Ie.
Из соединений формул Ia особенно предпочтительны таковые частичных формул Iaa Ia алкил -Сy-Phe-CN (1aa) алкил Pne-Phe-CN (Iab)
алкокси -Phe-Phe-CN (Iac) алкокси Сy-Phe-CN (Iad)
алкил -Cy-CH2CH2-Phe-CN (Iae) алкокси -Cy-CH2CH2-Phe-CN (1af).
В предпочтительных соединениях выше- и нижеприведенных формул R обозначает алкильную группу предпочтительно с 1-10 С-атомами, алкоксильную или алканоилокси-группу, предпочтительно, смотря по обстоятельствам, с 1-10 С-атомами.
Особенно предпочтительными алкильными группами являются гексил, пентил, бутил, изобутил, пропил, изопропил, метил и этил, в особенности метил, особенно предпочтительными алкоксильными группами являются гексокси, пентокси, изобутокси, пропокси, изопропокси, метокси и этокси, в особенности метокси, особенно предпочтительными алканоилокси-группами, являются гексаноилокси, пентаилокси, бутирилокси, пропионилокси, ацетилокси, и формилокси, в особенности ацетилокси.
В предпочтительных соединениях выше и нижеприведенных формул алкильные остатки, в которых также одна СH2-группа (алкокси или оксаалкил) может быть заменена О-атомом, могут быть линейными или разветвленными. Предпочтительно они содержат 2,3,4,5,6,7,8,9 или 10 С-атомов и соответственному этому предпочтительно обозначают этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил, пропокси, этокси, бутокси, пентокси, гексокси, гептокси, октокси, нонокси и децокси, далее, также индецил, додецил, индецокси, додецокси, 2-оксапропил (-метоксиметил), 2-(-этоксиметил) или 3-оксабутил)= 2-метокси-этил), 2-, 3- или 4-оксапентил, 2-, 3-, 4- или 5-оксагексил, 2-, 3-, 4-, 5- или 6-оксагептил. А1 и А2 предпочтительно обозначают Сy или Phe. В соединениях выше- и нижеприведенных формул Phe обозначает предпочтительно 1,4-фениленовую (Ph), одно- или двукратно замещенную F или СN 1,4-фениленовую группу (Phe Х), пиримидин-2,5-диильную (Pyr), пиридин-2,5-диильную (Pyn), пиразин-2,6-диильную или пиридазин-2,5-диильную группу, в особенности предпочтительны Ph, Pheх, Pyr или Pyn. Предпочтительно полученные по предлагаемому в изобретении способу соединения содержит не более чем одну 1,4-фениленовую группу, где одна или две СН-группы заменены азотом, Сy обозначает предпочтительно 1,4-циклогексиленовую группу. В особенности предпочтительны соединения формулы I, где одна из групп А1 и А2 обозначает замещенную в 1- или 4-положении СN-группой 1,4-циклогексиленовую группу, а нитрильная группа находится в аксиальном положении, т.е. группа А1, соответственно А2 имеет следующую конфигурацию 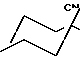 . Особенно предпочти- тельны соединения формулы I и вышеприведенных частичных формул, которые содержат группировку -Phe-Phe, -Phe-Phe-, предпочтительно представляет собой -Ph-Ph-, -Pyr-Phe- или -Ph-Pyn. Особенно предпочтительны группы:
. Особенно предпочти- тельны соединения формулы I и вышеприведенных частичных формул, которые содержат группировку -Phe-Phe, -Phe-Phe-, предпочтительно представляет собой -Ph-Ph-, -Pyr-Phe- или -Ph-Pyn. Особенно предпочтительны группы: 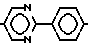 и
и 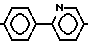 а также далее незамещенный или одно- или многократно замещенный фтором 4,4-бифенилил.
а также далее незамещенный или одно- или многократно замещенный фтором 4,4-бифенилил.
Особенно предпочтительны соединения формулы I и нижеследующих частичных формул, которые содержат 2,3-дифтор-1,4-фениленовую группу.
Группы Z1 и Z2 обозначают, смотря по обстоятельствам, независимо друг от друга предпочтительно однократную связь, во вторую очередь предпочтительно -CH2- -CH2-OCH2-; -CH2O-.
Из соединений формулы I, а также Ia-Ic, предпочтительны те, в которых, по меньшей мере, один из содержащихся в них остатков имеет одно из указанных предпочтительных значений.
Пригодными катализаторами дегидратации являются, например, оксид алюминия, оксид цинка, ацетат кобальта, фосфат бора и дигидрофосфат аммония. Концентрация катализатора составляет 0,1-5,0, предпочтительно 0,2-5,0 мас. в расчете на превращаемую карбоновую кислоту, когда реакция осуществляется в круглодонной колбе.
При применении реакционной трубки необходимое количество катализатора соответственно больше, а именно 0,5-20, предпочтительно 1,0-11 мас. в расчете на превращаемую карбоновую кислоту. Катализатор затем используется предпочтительно в гранулированной форме или на соответствующем носителе.
Необходимые в качестве исходных веществ замещенные ароматические карбоновые кислоты известны или получаются само по себе известными способами, а именно при реакционных условиях, которые известны и пригодны для указанных превращений.
Ароматические карбоновые кислоты, например, можно получить путем разложения галоидной формы соответствующих арилметилкетонов, которые легко получаются ацилированием по Фриделю-Крафтсу (Губен-Вейл, том 8, с. 415, 1952).
Также путем взаимодействия ароматических углеводородов с фосгеном в присутствии хлорида алюминия через первоначально образующиеся хлор-ангидриды карбоновых кислот и после омыления можно получать соответствующие карбоновые кислоты. Соответствующее взаимодействие с оксалилхлоридом, после отщепления монооксида углерода, также приводит к карбоновым кислотам (например, Губен-Вейл, том 8, с. 378, 1952).
Ароматические карбоновые кислоты можно получать путем взаимодействия галогенароматических углеводородов, которые легко получаются путем галогенирования соответствующих ароматических углеводородов, с монооксидом углерода в присутствии воды и катализаторов на основе никеля, кобальта, железа, родия или палладия, причем может требоваться дополнительное облучение УФ-светом (например, Губен-Вейл, том Е 5, ч. I, с. 310, 1985).
Галогенароматические углеводороды путем металлирования, например, с помощью бутиллития или магния и последующего карбоксилирования с помощью диоксида углерода можно превращать в соответствующие карбоновые кислоты (Губен-Вейл, т. Е 5, ч.1, с. 323, 1985).
Осуществление реакции по предлагаемому способу простое. Так, при 200-400оС, предпочтительно при 200-300оС, в особенности при 220-280оС, легкий ток аммиака пропускают через расплав ароматической карбоновой кислоты, в котором растворен катализатор (например, оксид цинка) или суспендирован (например, оксид алюминия). С избыточным аммиаком удаляется образующаяся при реакции вода. Нитрил затем можно прямо выделять из реакционной смеси путем пригодного способа (например, путем отгонки в трубке с расширением или тонкопленочной дистилляции).
Во время реакции из карбоновой кислоты образуется соответствующий амид, который in situ дегидратируется. Согласно предлагаемому способу также можно использовать непосредственно вместо карбоновой кислоты соответствующий амид кислоты.
Предпочтительно, реакционные сосуды снабжаются восходящей обогреваемой трубкой, которая заполнена гранулированным катализатором дегидратации, предпочтительно гранулированным оксидом алюминия, в особенности Compalox  фирмы Martins-Werk, ФРГ.
фирмы Martins-Werk, ФРГ.
Пригодны катализаторы из гранулированного минерального носителя без каталитических свойств (например, глина) после того как они пропитаны раствором катализатора дегидратации (например, 5% -ным раствором ацетата кобальта) и затем высушены.
От катализатора дегидратации в восходящей трубке требуется, чтобы в случае необходимости сублимирующийся или увлекаемый с током аммиака амид превращался в нитрил.
Реакция может протекать при различных давлениях, предпочтительно при 1-10 бар, в особенности при 1-3 бара.
В указанных условиях не происходит ни изомеризация ароматических углеводородов, ни изомеризация в циклоалифатических (например, цис-) транс-изомеризация (или хиральных алифатических боковых цепях) например, рацемизация. Также нельзя наблюдать дезалкилирования или трансалкилирования. В качестве единственного побочного продукта обнаружен продукт декарбоксилирования I с выходом менее чем 2% Конверсия составляет 95-99% R-Ar-COOH + NH3 катализатор R-Ar-CN+R-
Ar H + H2O + CO2 R остаток, например, (I) алкил.
Примеры поясняют изобретение, не ограничивая его объема. Т.пл. точка плавления, Т. о точка осветления, выше- и нижеуказанные данные в процентах обозначают массовый процент, все температуры указаны в градусах Цельсия.
Введены обозначения:
К кристаллическитвердое состояние, С смектическая фаза (показатель характеризует тип фазы), Н нематическое состояние, Х холестерическая фаза, И изотропная фаза. Число, стоящее между двумя символами, дает температуру превращения в градусах Цельсия.
Аппарат I. Обогреваемая круглодонная колба с мешалкой, внутренним термометром, газоподводящей трубкой и восходящей, обогреваемой длиной 30-50 cм трубкой. Восходящая трубка заполнена гранулированным катализатором дегидратации.
Обогреваемая трубка через соединение связана с холодильником, приемником (для образующейся во время реакции воды) и счетчиком пузырьков.
Аппарат 2. Обогреваемая реакционная трубка длиной 30 см и с внутренним диаметром 2,5 см, с термоэлементом, обогреваемым подводящим сосудом, зумпфовой колбой (Sumpfblase) c газоподводящей трубкой и отгоночной частью с нисходящим холодильником. Реакционная трубка заполнена гранулированным катализатором дегидратации.
Указанные в примерах соединения известны. Идентичность устанавливалась путем сравнения газожидкостных хроматограмм или хроматограмм, получаемых путем жидкостной хроматографии высокого давления, ИК-спектров и в случае необходимости величин вращения с соответствующими значениями аутентичных образцов.
П р и м е р 1. Смесь из 192,1 г 4-(транс-4-пентилциклогексил)бензойной кислоты (2) и 3,0 г ацетата кобальта (II) в аппарате 1 нагревают при 200оС при введении аммиака. Перемешивают 0,5 ч при этой температуре и затем нагревают далее при 270оС до тех пор, пока более не будет отгоняться никакой воды (примерно 6 ч). Неочищенный продукт перегоняют при 170оC и давлении 0,02 мбара благодаря тонкопленочному испарителю и затем перекристаллизовывают. Получают 169,8 г 4-(транс-4-пентилциклогексил)-бензонитрила, К 31, Н 55, И.
П р и м е р 2. 192,1 г (2) с 1,0 г (0,01 моль) оксида цинка превращают и обрабатывают как описано в примере 1. Выход спустя 4 ч времени реакции составляет 175,4 г 4-(транс-4-фенилциклогексил)бензонитрила, К 31, Н 55, И.
П р и м е р 3. 192,1 г (2) с 5,0 г оксида алюминия превращают и обрабатывают как описано в примере 1. Выход спустя 6 ч времени реакции составляет 169,3 г 4-(транс-4-пентилциклогексил)бензонитрила, К 31, Н 55, И.
П р и м е р 4. 192,1 г (2) в 3,8 г фосфата бора превращают и обрабатывают как описано в примере 1. Выход после 6 ч времени реакции составляет 153,9 г 4-(транс-4-пентилциклогексил)бензонитрила. К 31, Н 55, И.
П р и м е р 5. 192,1 г (2) с дигидрофосфатом аммония в количестве 2,0 г превращают и обрабатывают как описано в примере 1. Получают 174,9 г 4-(транс-4-пентилциклогексил)бензонитрила, К 31, H 55, И.
П р и м е р 6. 229,5 г 4'-Додецилокси-4-бифенилкарбоновой кислоты с 2,3 г оксида цинка превращают как описано в примере 1. После дистилляции в тонкопленочном вы- парном аппарате при 250oC (0,1 мбар) и перекристаллизации получают 209,2 г 4-циано-4'-додецилоксибифенила, К 70 Н 90, И.
П р и м е р 7. 194,7 г 4'-нонил-4-бифенилкарбоновой кислоты превращают и обрабатывают как описано в примере 5. Получают 176,2 г 4-циано-4'-нонилбифенила, К 42, С 49, Н 50, И.
П р и м е р 8. 138,7 г Бифенил-2-карбоновой кислоты с 5,0 г оксида цинка превращают как описано в примере 1. Неочищенный продукт перегоняют при 140oC и давлении 0,3 мбара на тонкослойном выпарном аппарате. После перекристаллизации получают 119,6 г 2-цианобифенила, К 34-35, И.
П р и м е р 9. 49,9 г S-4'-(2-метилбутил)бифенил-4-карбоновой кислоты с 0,5 г оксида цинка превращают как описано в примере 1. После перегонки в трубке с шаровым расширением при 170оС и давлении 0,1 мбар получают 45,1 г S-4-циано-4'-(2-метилбутил)бифенила.
П р и м е р 10. 66,8 г 2'-фтор-4'-(транс-4-пропилциклогексил) -бифенил-4-карбоновой кислоты с 0,5 г дигидрофосфата аммония превращают как описано в примере 1. После фильтрации и перекристаллизации получают 59,7 г 4-циано-2'-фтор-4'-(транс-4- пропилциклогексил)бифенила, К 69, Н 191, И.
П р и м е р 11. 51,3 г 4-(5-Бутилпиримидин-2-ил)фенил -1-карбоновой кислоты превращают и обрабатывают как описано в примере 10. Получают 44,7 г 4-(5-бутилпиримидин-2-ил)бензонитрила, К 63, Н 40, И.
П р и м е р 12. 34,4 г α -нафталинкарбоновой кислоты превращают и обрабатывают как описано в примере 1. Получают 13,8 г α-нафталинкарбонитрила, К 36-38, И.
П р и м е р 13. 30,4 г м-Метоксибензойной кислоты превращают и обрабатывают как описано в примере 1. Получают 10,4 г метоксибензонитрила, т.кип. 111-112oC (13 мм).
Аналогично получают следующие замещенные бензонитрилы: м-нитробензонитрил, т.пл. 115-117oC; м-трифторметилбензонитрил, т.кип. 189-190oC; 4-метил-3-бромбензонитрил, т. кип. 140оС/ 0,4 мбар; 4-трет-бутилбензонитрил, т.кип. 12-14oC; 2,5-диметилбензонитрил, т. пл. 13-15оС; 2,2-дицианобифенил, т.пл. 172-173oC.
Метиловый эфир 4-цианобензойной кислоты, т.пл. 138-139oC 4-(4-гексилоксибензоилокси)бензонитрил.
Дополнительные примеры сведены в таблицу.
Аналогично примеру 1 проводят взаимодействие 0,5 моль кислоты А с 1 г окиси цинка в течение 6 ч с аммиаком. Получают соответствующие нитрилы В.
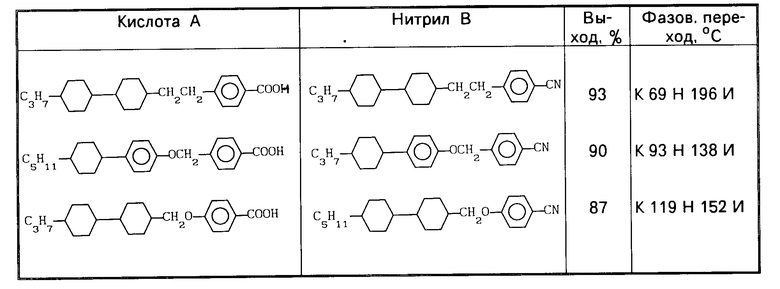
Использование: в химии замещенных нитрилов - промежуточных продуктов в органическом синтезе. Сущность изобретения: получение замещенных ароматических нитрилов ф-лы I: R-(A′-Z′)m-(A″-Z″)n-Ar-CN , где R - галоген, CN, алкильный C1-C15 - остаток, причем в этих остатках одна или несколько метиленовых групп независимо одна от другой могут быть заменены кислородом, серой или карбонилом таким образом, чтобы сера и/или кислород не соединялись непосредственно друг с другом; A′, A″ - независимы друг от друга и означают транс-1, 4-циклогексильный остаток; Z′, Z″ - простая связь;; Ar - 1,4-фениленовый остаток, ведут пропусканием газообразного аммиака через расплав соответствующей ароматической карбоновой кислоты, в которой суспендирован катализатор, с удалением образующейся реакционной воды избыточным аммиаком. 4 з.п. ф-лы, 1 табл.
R-(A1 Z1)m (A2 - Z2)n-A2-CN,
где R галоген, CN, незамещенный алкильный остаток с 1 15 атомами углерода, причем в этих остатках одна или несколько групп CH2 независимо друг от друга могут быть замещены на О-, S, CO, таким образом, чтобы S и/или атом кислорода непосредственно не соединялись друг с другом;
A1, A2 независимо друг от друга означают
а) транс-1,4-циклогексильный остаток, где одна или две СН-группы могут быть заменены на О и/или S;
б) 1,4-фениленовый остаток, где одна или две СН-группы могут быть заменены на азот;
в) 1,4-циклогексанилен, 1,4-бицикло-(2,2,2)-октилен, пиперидин-1,4-диил, нафталин-2,6-диил, декагидронафталин-2,6-диил и 1,2,3,4-тетрагидронафталин-2,6-диил;
Ar 1,4-фениленовый, нафталин-2,6-диильный, пиридин-2,5-диильный или пиримидин-2,5-диильный остаток, причем остатки, указанные в а), б) и Ar могут быть замещены CN-группой или галогеном;
Z1 и Z2 простая связь, -CH2CH2-OCH2- и CH2O-,
n 0,1,
путем взаимодействия соответствующей ароматической карбоновой кислоты в виде расплава с газообразным аммиаком в присутствии катализатора дегидратации, отличающийся тем, что газообразный аммиак пропускают через расплав ароматической карбоновой кислоты, в котором растворен или суспендирован катализатор, с удалением образующейся воды избыточным аммиаком.
| Патент США N 2901504, кл | |||
| Термометр | 1923 |
|
SU558A1 |
Авторы
Даты
1995-06-19—Публикация
1991-03-19—Подача