Изобретение касается стабилизированных водных фармацевтических составов для назального введения коротких и среднего размера пептидов (вплоть до примерно эйкозапептидов), таких как десмопрессин (1-деамино-8-D-аргинин вазопрессин; DDAVP).
Используемый здесь термин "стабилизированный состав" относится к водному раствору для терапевтического использования, содержащему по меньшей мере один короткий или среднего размера биологически активный пептид. Такая стабилизация должна позволить составу храниться при комнатной температуре в течение длительного периода без потери биологической активности.
Известно, что значительное число биологически активных пептидов, их производных и аналогов (в дальнейшем обозначаемые "пептиды") являются терапевтически полезными. По различным причинам их часто вводят в форме водных составов, то есть стерильных водных растворов, содержащих известное количество пептида.
Биологическая активность вводимых пептидов часто исключительно высока. Таким образом, для единичной дозы необходимы только очень малые количества пептидов. Такие разбавленные растворы пептидов обычно нестабильны при комнатной температуре в течение длительных периодов времени, даже если хранить их в герметичных контейнерах. Терапевтическиактивный пептидный гормонный аналог десмопрессин является таким пептидом. Его водный раствор должен храниться при температуре, не превышающей 8oC. Хранение при более высоких температурах, таких как, например, комнатная температура, приводит к деградации десмопрессина из-за гидролитических и/или окислительных процессов, которые не останавливаются добавлением консерванта, такого как хлорбутанол (1,1,1-трихлор-2-метил-пропанол). Тем не менее, хлорбутанол эффективно защищает десмопрессин от действия микробов.
Другая проблема, связанная с разбавленными водными растворами пептидов, заключается в адсорбции незначительных количеств пептида на стенках контейнера, в котором раствор хранится. Так как такие пептидные растворы обычно очень разбавлены, адсорбция даже малых количеств может существенно снизить количество пептида, доступного для введения.
Наиболее привлекательным путем введения коротких и среднего размера пептидов в растворе является путь через назальную слизистую оболочку в виде капель или аэрозоля, который даже более удобен и более воспроизводим. Десмопрессин, например, может быть введен таким путем в водном 0,9%-ном растворе хлорида натрия (физиологический раствор).
Известен (патент Великобритании 1454105, кл. A 61 K 9/00// (A 61 K 9/00 9/72), 1976) водный состав для назального введения биологически активного пептида, содержащий биологически активный пептид, буфер, выбранный из группы, состоящей из цитрата, фосфата и смеси цитрата и фосфата, поддерживающий рН указанного состава между 4 и 6, контролирующий осмотическое давление агент и консервант, в котором биологически активным пептидом является рилизинг-фактор лютеинизирующего гормона.
Недостатком этого состава является невозможность его хранения при комнатной температуре из-за деградации пептида и адсорбция пептида на стенках контейнера, в котором он хранится.
Специалистам известны различные типы устройств для интраназального введения аэрозоля. Вообще пептиды в водном растворе вводят с помощью дозировочного аэрозольного насоса, такого как насосы, производимые Ing. Erich Pfeiffer KG, Radolfzell, Германия. Существует альтернативный путь - через градуированную пластиковую тубу специальной конструкции, называемую "райнил", которая частично заполнена водным раствором, содержащим пептид. Один конец райнила помещают в рот, а другой конец вставляют в желаемую ноздрю. Затем раствор подается в ноздрю вдуванием.
Из указанного выше патента Великобритании 1454105 известен герметичный контейнер для назального введения аэрозоля, наполненный указанным выше водным составом, содержащим пептид.
Таким образом, задачей настоящего изобретения является создание стабилизированного водного состава для назального введения коротких или среднего размера пептидов, в частности десмопрессина, который можно удобно хранить при комнатной температуре в течение длительных периодов времени, например один год, без риска частичной или полной деградации или микробного загрязнения содержащегося в нем пептида и который предотвращает прилипание пептида к стенкам контейнера без использования посторонних добавок, специально предназначенных для этой цели, а также создание контейнера, наполненного таким водным составом.
Эта задача решается тем, что предложен водный состав для назального введения биологически активного пептида, содержащий биологически активный пептид, буфер, выбранный из группы, состоящей из цитрата, фосфата и смеси цитрата и фосфата, поддерживающий pH указанного состава между 4 и 6, консервант и контролирующий осмотическое давление агент, отличающийся тем, что указанный биологически активный пептид представляет собой по меньшей мере один пептид, выбранный из группы, содержащей окситоцин, вазопрессин, терлипрессин (N-α-триглицил-8-лизин)- вазопрессин), атосибан ((Mpa1, D-Tyr(Et)2, Thr4, Orn8)-окситоцин), карбетоцин ((1-деамино-1-монокарба-2(O-метил)-тирозин)окситоцин) и трипторелин ((D-Trp6)-LHRH), и их аналоги и производные, а в качестве консерванта состав содержит бензалконийхлорид, причем указанный состав способен сохранять указанный биологически активный пептид в функционально стабильном состоянии в течение длительных периодов и при комнатной температуре.
Предпочтительно указанный пептид является десмопрессином.
Целесообразно, чтобы указанный буфер сохранял вышеуказанное pH при значении около 5,0. Указанный буфер предпочтительно включает в себя смесь цитрата и динатрийгидрофосфата таким образом, что молярное соотношение ионов цитрата, фосфата и натрия составляет от приблизительно 1 : 3 : 3 до приблизительно 1 : 1 : 2.
Указанный контролирующий осмотическое давление агент предпочтительно является хлоридом натрия, причем указанный хлорид натрия добавлен к указанному составу в количестве, достаточном, чтобы сделать осмотическое давление указанного состава соответствующим осмотическому давлению человеческой плазмы.
Следует отметить, что компоненты буфера также вносят существенный вклад в контроль осмотического давления.
Предпочтительным составом по изобретению является состав, который включает в себя: от 0,025 до 1,5 мг ацетата десмопрессина, от 1,35 до 1,75 мг лимонной кислоты, от 2,25 до 2,65 мг динатрийгидрофосфата, от 0,05 до 0,20 мг бензалконийхлорида, хлорид натрия в количестве, достаточном для создания в указанном составе осмотического давления, сравнимого с осмотическим давлением человеческой плазмы.
Указанная задача решается также тем, что предложен герметичный контейнер для назального введения аэрозоля, наполненный водным составом, содержащим пептид, отличающийся тем, что контейнер наполнен вышеуказанным предпочтительным составом по изобретению.
Используемый в качестве консерванта бензалконийхлорид представляет собой четвертичный амин формулы (NR1R2R3R)+CI-; где R1, R2 = метил, R3 = бензил, R4 = C8H17 до C18H37. Вдобавок к своим прямым функциям, он обладает неожиданной способностью препятствовать адсорбции коротких или среднего размера пептидных компонентов с прилипанием к стенкам контейнера, особенно стенкам контейнеров, сделанных из полимерных материалов.
Состав по изобретению может дополнительно содержать по меньшей мере одно вещество, усиливающее сорбционную способность слизистой оболочки, такое как соли желчи, макроголовые эфиры монолауриновой кислоты и производные фузидата.
Пептиды для назального введения часто имеют очень высокую биологическую активность, и для единичной дозы необходимо только очень малое количество пептида. Однако конкретная форма введения может потребовать некоторого минимального объема жидкости для хорошей воспроизводимости. Таким образом, области эффективных концентраций для назального введения пептидов обычно весьма низкие. Например, единичная доза десмопрессина для назального введения, как правило, составляет между 10 и 40 мкг, но может быть даже столь мала, как 2,5 мкг и столь высока, как 300 мкг. Типичные объемы доз составляют от 100 до 400 мкл (4 x 100 мкл). Эти дозы обычно регулярно принимают по меньшей мере один раз в день.
Фиг. 1 графически показывает результаты проверки стабильности для составов, приготовленных согласно настоящему изобретению.
Данное изобретение будет теперь более детально разъяснено с отнесением к следующим экспериментальным примерам.
Пример 1. Приготовление составов для испытания. Были приготовлены пять составов для испытания, содержащих ацетат десмопрессина (DDAVP) для назальных аэрозольных или капельных составов, содержащих различные консерванты, составы A, B, C, D и E (см. табл. 1). Каждый образец для испытания содержал 0,089 мг свободного основания DDAVP в 1 мл, а в табл. 1 обозначен тип используемого в каждой системе буфера. В качестве растворителя использовали профильтрованную через Millipore воду.
Составы A и B были приготовлены в соответствии с настоящим изобретением. Составы C, D и E были приготовлены для сравнительного испытания других консервантов.
Стабильность известного, не содержащего буфер Minirin (DDAVP) аэрозоля, содержащего NaCI и хлорбутанол, имеет практическую сохраняемость 3 года при хранении в холодильнике в запаянных стеклянных контейнерах. Он нестабилен при комнатной температуре, когда хранится в течение более длительных периодов времени. Отметим, что состав E содержит NaCI и хлорбутанол, но является буферным раствором.
Пример 2. Исследование стабильности по определению деградации пептидов.
DDAVP-составы, приготовленные в примере 1, сохраняли в 10 мл стеклянных флаконах (гидролитический класс 1, снабженных тефлоновыми пробками) в темноте при 65oC в течение до 13 недель. Образцы были отобраны после 1, 2, 3, 5, 7, 11 и 13 недель и проанализированы на DDAVP методом ЖХВР (Varian Star system; Lichospher PR-18 5 мкм колонка (50x4 мм); градиент элюции с различными пропорциями ацетонитрил/0,0667 водного фосфатного буфера pH 7).
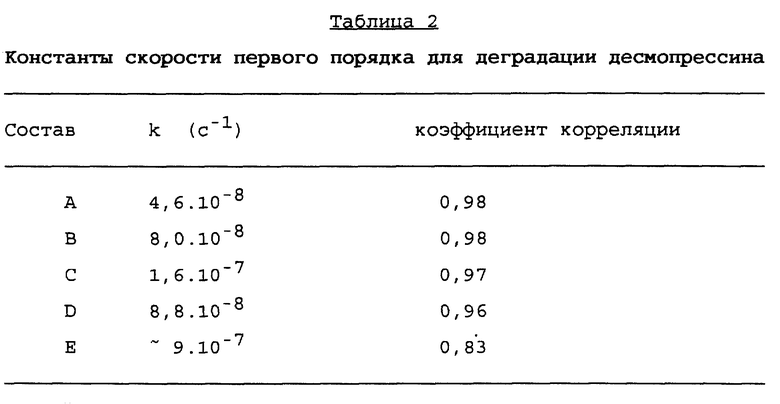
Результаты представлены графически на фиг. 1 и показывают большее стабилизирующее действие состава в соответствии с настоящим изобретением. Экспериментальные данные, содержащиеся на фиг. 1, были также использованы для расчета констант скорости первого порядка, показанных в табл. 2.
Пример 3. Расчет практической сохраняемости.
Из наклона кривых на фиг. 1 и из соответствующих испытаний по хранению, проведенных при 37; 50 и 60oC, были получены энергии активации Аррениуса (Ea) для составов A, B, C и D. Состав E не обнаружил поведения типа по Аррениусу, так как оказался значительно наименее стабильным.
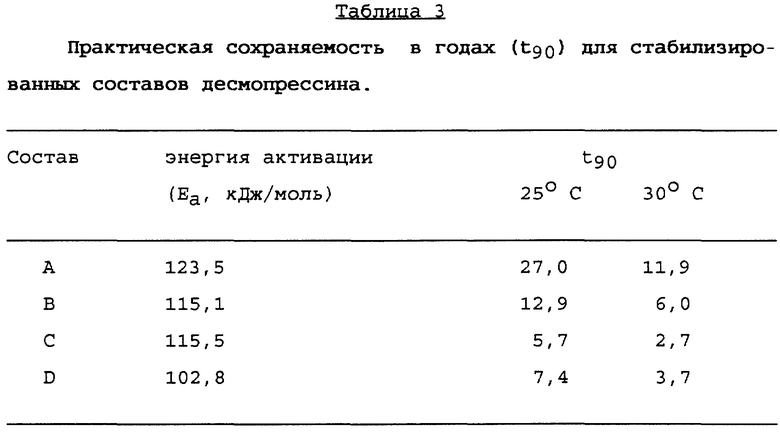
Время хранения, в течение которого общее содержание DDAVP в каждом составе снизилось на 10% (tgo) при 25 и 30oC, "практическая сохраняемость", было рассчитано из Ea, что представлено в табл. 3.
Как показывает табл. 3, десмопрессин в составах A и B сохраняется при комнатной температуре в течение длительного периода времени, демонстрируя таким образом способность настоящего изобретения к хранению и использованию в течение длительных периодов без охлаждения.
Пример 4. Сравнение интраназального поглощения десмопрессина.
24 здоровым голодающим субъектам мужского пола был дан (рандомизированным образом) десмопрессин (20 мкл) интраназально в виде аэрозоля (200 мкл), используя либо состав B, либо коммерчески доступный безбуферный Minirin состав, содержащий хлорбутанол в качестве консерванта. С интервалами отбирали пробы крови и следили за плазменными уровнями десмопрессина в течение 12 ч периода методом десмопрессин-специфического RIA плазменного анализа (Lundin, S и др., Acta Endocrinologica (Copenhagen) 108 (1985) 170-183). Для двух составов был обнаружен по существу одинаковый профиль плазменного уровня. Это - неожиданный результат, так как H.A.Batts с сотр. (J. Pharm. Pharmacol. 1989, 156-159) обнаружил, что хлорбутанол и бензалконийхлорид значительно различаются в своем действии на скорость слизисто-мерцательного переноса в модели неба лягушки. Скорость слизисто-мерцательного выведения влияет на сравнительно медленное интраназальное всасывание пептидов и других назально вводимых активных соединений.
Пример 5. Адсорбционно-блокирующее действие десмопрессина.
Стерильные водные растворы десмопрессина, меченого 125I (приблизительно 10000 СРМ/мл), содержащие бензалконийхлорид + физиологический раствор, хлорбутанол + физиологический раствор или только физиологический раствор, были все инкубированы в пробирках из полистирола, полипропилена или стекла в течение 24 ч при комнатной температуре.
В растворах, содержащих бензалконийхлорид и хлорбутанол соответственно десмопрессин показал незначительную адсорбцию, тогда как из свободных от консерванта растворов из пластиковых пробирок можно было извлечь только примерно половину всего количества десмопрессина.
Несмотря на то, что различные черты и воплощения настоящего изобретения были здесь описаны, возможно, что какой-либо специалист сможет модифицировать различные аспекты настоящего изобретения и достигнуть тех же самых результатов. Такие модификации следует считать входящими в объем настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОСТАВЫ ДЛЯ НАЗАЛЬНОГО ВВЕДЕНИЯ ДЕСМОПРЕССИНА | 1994 |
|
RU2135204C1 |
| НАЗАЛЬНОЕ ВВЕДЕНИЕ ДЕСМОПРЕССИНА | 1997 |
|
RU2173559C2 |
| СТАБИЛИЗИРОВАННАЯ КОМПОЗИЦИЯ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ ПЕПТИДОВ | 1995 |
|
RU2140790C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2011 |
|
RU2604690C2 |
| Фармацевтическая композиция | 2011 |
|
RU2737264C2 |
| ГЕПТАПЕПТИДНЫЕ АНАЛОГИ ОКСИТОЦИНА | 1997 |
|
RU2180668C2 |
| АНАЛОГИ ОКСИТОЦИНА | 2009 |
|
RU2496788C2 |
| БЕЗОПАСНОЕ ПРИМЕНЕНИЕ ДЕСМОПРЕССИНА | 2010 |
|
RU2569756C2 |
| ПЕРОРАЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЕСМОПРЕССИНА | 2008 |
|
RU2474414C2 |
| ПЕПТИДНЫЕ СОЕДИНЕНИЯ | 2007 |
|
RU2415149C2 |

Изобретение относится к области медицины. Предложен стабилизированный водный состав для введения пациенту, включающий биологически активный пептид, например вазопрессин, буфер, консервант типа четвертичного амина или дезинфектант и контролирующий осмотрическое давление агент, причем этот состав можно хранить и использовать при комнатной температуре. Буфер стабилизирует рН состава между приблизительно 4 и 6. Предпочтительный буфер содержит цитрат и/или фосфат, а предпочтительный консервант или дезинфектант является бензалкониум хлоридом. Состав препятствует пептидам, содержащимся в нем, прилипать к стенкам контейнера, особенно в контейнерах, изготовленных из полимерных материалов. Изобретение касается также герметичного контейнера для введения указанного состава интраназально. Техническим результатом изобретения является расширение арсенала биологически активных пептидов для интраназального введения. 2 с. и 5 з.п. ф-лы, 3 табл., 1 ил.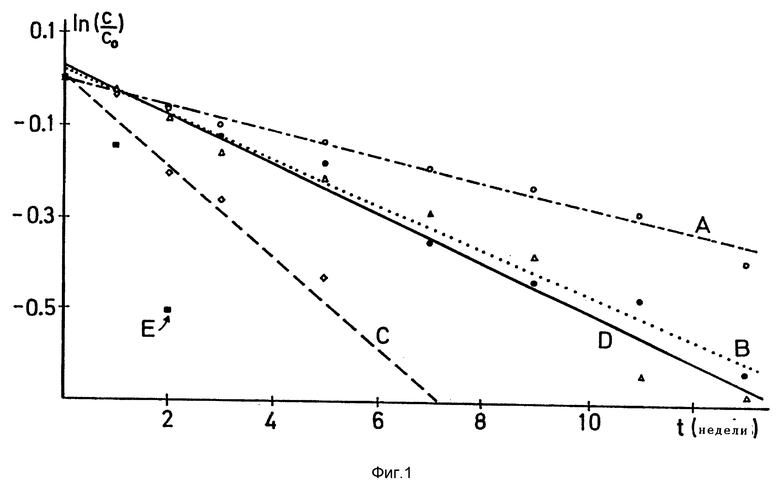
| WO 9303744 A1, 04.03.93 | |||
| Машковский М.Д | |||
| Лекарственные средства | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
Авторы
Даты
1999-10-27—Публикация
1994-06-22—Подача