Изобретение относится к области медицинского материаловедения, а конкретнее к технике подготовки поверхностей медицинских полимеров с улучшенными гемосовместимыми свойствами. В перспективе изобретение найдет использование в имплантационной хирургии при протезировании различных органов человека: искусственных кровеносных сосудов, артериовенозных шунтов, клапанов сердца, кардиостимуляторов и др.
В трансплантационной медицине существует проблема биосовместимости чужеродных поверхностей искусственных органов с кровью и другими тканями организма. Решение этой проблемы включает определение типа структуры поверхности имплантационного органа, позволяющей обеспечить оптимальные условия контакта крови человека с чужеродным телом, в т.ч. минимальные тромбообразование и конформные изменения структуры белков плазмы крови, улучшение других медико-технических параметров, и способа его получения.
Известны медицинская структура, включающая полимер (политетрафторэтилен) - приповерхностный модифицированный слой, и способ ее получения, заключающийся в модифицировании поверхности полимера гидроксильными функциональными группами [1]. Такая структура обладает улучшенными гемосовместимыми свойствами. "Привитые" кислородные и (или) гидроксильные функциональные группы к поверхности политетрафторэтилена улучшают его гемосовместимые свойства за счет повышения адгезивной способности клеток эндотелия, которые, в свою очередь, защищают поверхность искусственных кровеносных сосудов, сердечных полостей от тромбообразования. Способом модификации поверхности подложки структуры в данном случае является микроволновая плазменная обработка в газообразной среде, содержащей водород и воду.
Однако эта работа описывает частный случай, а именно конкретный фторсодержащий полимер и только одну из множества составляющих улучшения гемосовместимых свойств - адгезию клеток эндотелия. В то время как не учитывается поведение основных белков плазмы крови на поверхности различных полимеров, используемых в медицинском материаловедении. Отметим, что последние играют немаловажную роль в процессах, обеспечивающих или нарушающих гемосовместимость поверхности.
Наиболее близкой по технической сущности к предлагаемому изобретению является работа [2]. В данной работе предлагается структура полимер - приповерхностный модифицированный слой, состоящий из локальных приповерхностных областей в виде чередующихся по химическому составу стриппов (полосок) шириной 20-130 мкм, что позволяет использовать, по крайней мере, две соседствующие области поверхности, обладающие различными биохимическими свойствами по адгезивной способности к нескольким компонентам крови. За счет этого достигается эффект гемосовместимости. Способом получения такой структуры является базовый литографический процесс планарной технологии микроструктур, включающий нанесение активного к ультрафиолетовому (УФ) излучению полимерного или сополимерного слоя, экспонирование его через маску с рисунком из полос шириной 20-130 мкм и вымывание растворителем необлученных (закрытых рисунком маски) полос.
Недостатком описанной структуры являются достаточно большие размеры приповерхностных областей (20-130 мкм) с различной химической, а следовательно, адгезивной способностью. Вероятно, эти области должны иметь субмикронные размеры, а еще лучше, если их размеры будут соответствовать размерам адсорбируемых молекул, необходимых на поверхности полимеров для улучшения гемосовместимых свойств, и быть меньше для исключения адсорбции нежелательных молекул белков плазмы крови. Для формирования структур с такими размерами областей рассмотренный способ не пригоден, т.к. его разрешение не может быть лучше 2 мкм [3].
Целью предлагаемого изобретения является улучшение гемосовместимых свойств медицинских структур на основе полимеров.
Поставленная цель достигается тем, что в структуре, состоящей из полимерной основы и ее приповерхностного модифицированного слоя, который содержит совокупность локальных приповерхностных областей, обладающих отличными от полимерной основы биохимическими свойствами, локальные приповерхностные области выполнены из углеродных кластеров размерами 5-12 нм.
В способе изготовления структуры, состоящей из полимерной основы и ее приповерхностного модифицированного слоя, включающем модификацию поверхности полимера, модификацию поверхности полимера проводят импульсным плазменным распылением графитовой мишени с частотой следования импульсов 1-2 Гц со скоростью осаждения углерода 0,1-0,2 нм/с до толщины 5-12 нм.
Выбор углерода как химической основы модифицирующего слоя не случаен. Углеродосодержащие пленки, в том числе алмазоподобные, являются универсальным материалом по критериям биосовместимости с компонентами крови и физиологическим раствором человека [4], кроме того, они химически инертны, имеют гладкую поверхность и хорошую износостойкость.
В настоящее время существует гипотеза о построении биосовместимых поверхностей медицинских материалов, заключающаяся в том, что такая поверхность должна представлять собой мозаичную структуру, состоящую из чередующихся по биохимическим свойствам адсорбционных центров, например, гидрофильных и гидрофобных по своей природе [5].
Вероятно, шаг такой мозаичной структуры должен быть в строгом соответствии с размерами молекул белков плазмы крови. Известно, что размеры основных белков плазмы крови находятся в диапазоне от 4-50 нм, поэтому шаг мозаичной структуры должен быть соразмерен с молекулами адсорбирующихся веществ, т.е. белков плазмы крови. Подобную мозаичную структуру на поверхности матричных полимеров можно сформировать с помощью углеродсодержащих кластеров. Тогда адсорбционными центрами для белков плазмы крови будет пространство, не занятое кластерными образованиями, поскольку большинство применяемых в имплантационной медицине материалов изначально обладают лучшими адсорбционными поверхностными свойствами, чем материалы, поверхность которых содержит углеродные слои. Причем при формировании мозаичной структуры размеры адсорбированных центров должны быть меньше, чем, например, размеры молекулы фибриногена - белка плазмы крови, адсорбция которого к поверхности полимера приводит к увеличению адгезии тромбоцитов, а следовательно, к снижению тромборезистентности матричного полимера. С другой стороны, размеры адсорбированного "посадочного" места мозаичной структуры должны обеспечить, по крайней мере, пространственную возможность адсорбции "полезных" молекул белков, например альбумина - одного из важнейших компонентов крови, превращающих поверхность в менее тромбогенную.
Молекулярный вес, усредненные диаметр и длина для молекул фибриногена и сывороточного альбумина составляют 340 000; 6,5 нм; 47,5 нм и 69 000; 4 нм, 11,5 нм, соответственно. Показано [5], что адсорбция молекул белка на поверхность твердого тела происходит той частью, которая занимает меньшую площадь. Однако в таком состоянии молекула не может существовать слишком долго - она либо десорбируется, либо переходит в более выгодное энергетическое состояние, располагаясь большей своей частью и образуя большее количество химических связей с поверхностью матрицы. Особенно важно, чтобы при таком переходе в наиболее выгодное энергетическое состояние молекулы белков плазмы крови не конформировались, т.е. не изменяли своей структуры. Следовательно, верхним пределом шага мозаичной структуры должна быть величина ~12 нм, а нижним - 5 нм, т. к. именно такой шаг должен обеспечить "посадку" молекул, подобных молекуле альбумина, и "запретить" адсорбцию молекул фибриногена. Таким образом, при формировании подобной структуры удается изготовить поверхность, способную адсорбировать "полезные" белки плазмы крови типа альбумина и экранировать адсорбцию белков, способствующих тромбообразованию, - фибриногена.
Известно, что для образования кластерной структуры на поверхности твердого тела условия нанесения вещества, связанные с фазовым переходом 1-го рода, например газообразное - твердое агрегатное состояние, должны быть сильно неравновесными. Основные термодинамические особенности процессов осаждения описаны теорией Фольмера - Вебера и связаны с островковым механизмом роста пленки, наносимой из газовой фазы. Размеры островка - зародыша, находящегося в сильно неравновесных условиях, соизмеримо с толщиной пленки до тех пор, пока не наступит ее сплошность. Таким образом, плоскостные размеры получаемых углеродных кластеров должны соответствовать их высоте.
Пример.
Для демонстрации предлагаемых решений нами выбран плазменный метод распыления углерода на установке типа УВИИПА - 1 с мишенью из графита, расположенной напротив подложки на расстоянии 30 см. Импульсный плазменный метод позволяет достаточно просто переходить от равновесных к разной степени неравновесным условиям конденсации углерода из газовой фазы за счет длительности импульсов воздействия плазмы на углеродную мишень. Этот факт подтверждался изучением морфологии, модифицированной углеродсодержащими слоями поверхности полимеров на сканирующем туннельном микроскопе.
Влияние частоты следования импульсов, непосредственно определяющей скорость осаждения углерода, на морфологическое качество модифицирующего покрытия показано в таблице 1. Все эксперименты проводились при ускоряющем движении ионов углерода, равном 200 В. Влияние частоты следования импульсов рассмотрено для пленок толщиной 5-20 нм.
В качестве исходного полимерного материала были использованы широко применяемые в медицинской практике полиэтилен низкой плотности (ПЭНП) ГОСТ 10354-73 и полиэфируретана Витур (НПО "Полимерсинтез", г. Владимир).
Поскольку модификация носит физический характер и определяется, в основном, условиями фазового перехода при осуществлении процессов распыления в газовую фазу и конденсации вещества из газовой фазы, т. е. не зависит от химической природы поверхности полимера, формирование кластеров практически не зависит от типа исходного материала.
Из таблицы 1 видно, что оптимальной частотой следования импульсов и скоростью осаждения углеродсодержащих пленок с точки зрения образования кластерной структуры на поверхности полимеров являются частота 1-2 Гц и скорость осаждения 0,1-0,2 нм/сек.
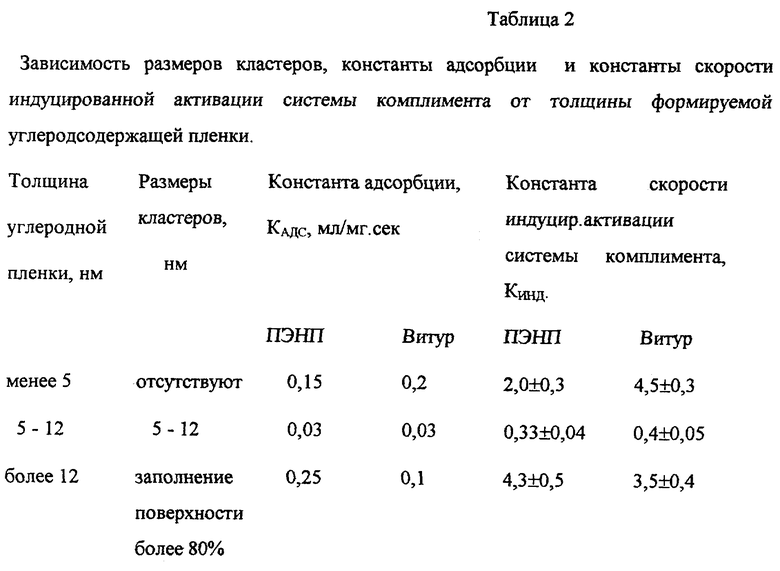
В таблице 2 показана зависимость формируемых размеров кластеров, а также константы адсорбции белков плазмы крови на модифицированную поверхность и константы активации системы комплимента модифицированной поверхности полимеров от толщины осаждаемых углеродсодержащих пленок.
Адсорбционные параметры определялись посредством изучения кинетики сывороточного альбумина человека (СДЧ) на поверхности полимеров методом флюоресценции полного внутреннего отражения. Белки САЧ метили радиоизотопом флуоресцеин изотиоцианатом с уровнем мечения 0,7-0,8 молекул красителя на 1 молекулу САЧ. Адсорбцию проводили из модельных фосфатных растворов с рН 7,35 при комнатной температуре и сдвиговой скорости у поверхности 4800 с-1.
В качестве биологического параметра выбрана степень активации системы комплимента сыворотки крови человека до и после инкубации. Свежая сыворотка крови человека инкубировалась с поверхностью полимера в течение 60 мин при температуре 37oC при отношении площади образца к объему сыворотки, равной 20: 1. По времени полулизиса сенсибилизированных эритроцитов барана сывороткой человека до и после инкубации с образцом вычисляли константы скорости активации системы комплимента, индуцированной поверхностью исследуемого и контрольного образцов (Кинд). В качестве контрольного образца использовалась поверхность гидратцеллюлозной мембраны Купрофана, которая используется для изготовления искусственной почки и относится к материалам с низкой активирующей поверхностью относительно системы комплимента. Поверхность является гемосовместмой, если величина Кинд меньше или равна 1,5.
Отметим, что для исходных поверхностей полимеров значения Кинд составляли для ПЭНП Кинд = 5,1 и для полиэфируретана Кинд = 5,5.
Анализ таблицы 2 показывает, что модифицирование значительно улучшает гемосовместимые свойства поверхности полимеров, причем этот эффект проявляется особо в диапазоне толщин осаждаемых углеродсодержащих пленок, равном 5 - 12 нм.
Заключение.
Медико-технические испытания образцов, изготовленных в соответствии со структурой и по способу, описанному выше, позволяют сделать вывод о том, что цель изобретения достигается успешно, особенно в части снижения адсорбционной способности поверхности полимеров по отношению к белкам плазмы крови и значительного снижения вероятности их структурных изменений. Использование результатов предлагаемого изобретения в имплантационной хирургии приведет к сокращению срока реабилитации больных, снижению риска послеоперационных осложнений, расширению контингента оперируемых больных.
Литература
1. F. Simon, G. Hermel and oth. "Surface modification of expended poly(tetraflnoroethylene) by means of mikrowave plasma treatment for improvement of adhesion and growth of human endothelia cells"./ Macromol. Symp. 103, 243-257, 1996).
2. Matsuda Т., Sugawara Т. Control of cell adhesion, migration, and orientation on microprocessed surfaces; J. Biomedical Materials Research, 32, 165-173, 1996.
3. Моро У. Микролитография, T.I, Москва, Мир, стр.466.
4. Helmus М., Overview of biomedical materials, Mater.Res.Soc.Bull., v. l6, 33-38, 1991.
5. Тремсина Ю. С., Севастьянов В.И./Конкурентная адсорбция альбумина и глобулина человека на поверхность силоксанов. Биосовместимость, 1995, 3, 115-123.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДИФИКАЦИИ ПОВЕРХНОСТИ ПОЛИМЕРА | 2006 |
|
RU2325192C2 |
| НАКОПИТЕЛЬ ДЛЯ ПОСТОЯННОГО ЗАПОМИНАЮЩЕГО УСТРОЙСТВА | 1990 |
|
RU2006968C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЛЕНКИ ДИОКСИДА КРЕМНИЯ НА ПОДЛОЖКЕ | 1996 |
|
RU2116686C1 |
| ДВУХЗАТВОРНАЯ МДП-СТРУКТУРА С ВЕРТИКАЛЬНЫМ КАНАЛОМ | 1995 |
|
RU2106721C1 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКИХ БУФЕРНЫХ СЛОЕВ | 1991 |
|
RU2006996C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСОВМЕСТИМЫХ ПОЛИМЕРОВ | 1983 |
|
SU1114039A1 |
| УСТРОЙСТВО ДЛЯ ЭЛЕКТРОХИМИЧЕСКОГО ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ОРГАНИЧЕСКИХ ПРИМЕСЕЙ В ВОДЕ | 1993 |
|
RU2095802C1 |
| СПОСОБ МОДИФИЦИРОВАНИЯ УГЛЕРОДНОГО ГЕМОСОРБЕНТА И УГЛЕРОДНЫЙ ГЕМОСОРБЕНТ С ИММОБИЛИЗОВАННЫМ БЕЛКОМ | 2011 |
|
RU2452499C1 |
| ПОЛИМЕРНАЯ СИСТЕМА, ОБЛАДАЮЩАЯ СЕЛЕКТИВНОСТЬЮ АДСОРБЦИИ ПО РАЗМЕРАМ | 2011 |
|
RU2590225C2 |
| ПОЛУПРОВОДНИКОВЫЙ ПРИБОР | 1980 |
|
SU1840207A1 |

Изобретение относится к медицинскому материаловедению, а конкретнее к технике подготовки поверхностей медицинских полимеров с улучшенными гемосовместимыми свойствами, и может использоваться в имплантационной хирургии при протезировании различных органов человека: искусственных кровеносных сосудов, артериовенозных шунтов, клапанов сердца, кардиостимуляторов и др. Структура обладает улучшенными гемосовместимыми свойствами медицинских структур на основе полимеров. Она состоит из полимерной основы и ее приповерхностного модифицированного слоя, который содержит совокупность локальных приповерхностных областей, обладающих отличными от полимерной основы биохимическими свойствами, и локальные приповерхностные области выполнены из углеродных кластеров размерами 5-12 нм. Способ изготовления структуры, состоящей из полимерной основы и ее приповерхностного модифицированного слоя, включает модификацию поверхности полимера импульсным плазменным распылением графитовой мишени с частотой следования импульсов 1-2 Гц со скоростью осаждения углерода 0,1-0,2 нм/с до толщины 5-12 нм. 2 с.п.ф-лы, 2 табл.
| Способ размножения копий рисунков, текста и т.п. | 1921 |
|
SU89A1 |
| СПОСОБ ПРОИЗВОДСТВА ХЛЕБНОГО КВАСА | 2015 |
|
RU2577142C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНЫХ ИМПЛАНТАТОВ | 1994 |
|
RU2074674C1 |
Авторы
Даты
2000-08-10—Публикация
1998-04-16—Подача