Изобретение относится к медицине, а именно к кардиохирургии и кардиологии, и может быть использовано для диагностики нарушений центральной гемодинамики при электростимуляции сердца.
Хирургическое лечение нарушений ритма сердца посредством постоянной электрокардиостимуляции имеет большое медицинское и социальное значение. Ежегодно в мире имплантации постоянных искусственных водителей ритма сердца выполняются у 350 - 400 тысяч больных.
Наиболее часто (в 70-79% случаев имплантаций кардиостимуляторов) применяют однокамерную желудочковую электростимуляцию сердца в режиме VVI. Такой режим сердца позволяет надежно устранить жизнеугрожающие состояния при брадикардии и увеличить по сравнению с медикаментозным лечением выживаемость больных. Недостатком является невозможность моделировать дромотропную и хронотропную функции сердца, заключающиеся соответственно в сохранении предсердно-желудочковой синхронизации и регуляции частоты сердечных сокращений при нагрузке. Отклонения, возникающие во внутрисердечной и системной гемодинамике при изолированной желудочковой электростимуляции сердца в режиме VVI, приводят к развитию у части (от 5 до 65% случаев) больных так называемого синдрома кардиостимулятора. Это обстоятельство вызывает необходимость замены изолированной желудочковой электростимуляции сердца на более физиологичные режимы: предсердный или двухкамерный.
Известны различные способы выявления синдрома кардиостимулятора:
оценка клинических жалоб и состояния больного с постоянной электростимуляцией сердца;
исследование вентрикулоатриального проведения неинвазивным (чреспищеводным) и инвазивным (эндокардиальным, эпикардиальным) методами;
оценка размеров полостей сердца, центральной гемодинамики и направления потоков крови через атриовентрикулярные клапаны ультразвуковым и радионуклидным методиками;
измерение концентрации натрийуретического гормона и катехоламинов крови, внутриполостного давления крови, давления на плечевой артерии по Н.С.Короткову;
исследование изменений при венозной окклюзионной плетизмографии, перинейральной микронейрографии (Новые перспективы в электрокардиостимуляции. / Под ред. Мюжика Ж. , Егорова Д., Барольда С. - СПб: Сильван, 1995. - С. 153-154).
Недостатками описанных способов являются либо низкая специфичность полученных результатов; либо инвазивность, связанная с риском развития гемо- и пневмоторакса, повреждения структуры нерва; либо дороговизна, обусловленная необходимостью рентгенологического контроля местоположения катетера при заборе проб крови, наличия биохимической и гормональной лабораторий и связанного с этим большого штата персонала.
Прототипом предлагаемого способа является метод диагностики, включающий измерение у больного в ходе имплантации желудочкового кардиостимулятора величины артериального давления неинвазивным способом по Н.С. Короткову, исследование вентрикулоатриальной проводимости (Бредикис Ю.Ю., Стирбис П.П., Дрогайцев А. Д. Программируемая электростимуляция сердца (клинические аспекты). - М.; Медицина. 1989. - С. 63-65). Достоверным признаком наличия у больного синдрома кардиостимулятора является снижение величины систолического артериального давления при изолированной желудочковой электрокардиостимуляции более чем на 20 мм рт. ст. в сравнении с аналогичной величиной, измеренной при спонтанном ритме сердца, в сочетании с вентрикулоатриальным проведением или без него.
Недостатками метода являются низкая специфичность результатов, затруднение чреспищеводной регистрации предсердных потенциалов, низкие возможности выбора оптимального режима и параметров электростимуляции сердца, возможность проведения только в ходе имплантации кардиостимулятора.
Изобретение направлено на решение задач:
повышение точности способа диагностики синдрома кардиостимулятора;
подбор оптимального режима электростимуляции сердца;
обоснование показаний и противопоказаний для операции замены кардиостимулятора.
Указанные задачи решаются за счет оценки показателей гемодинамики у больного при различных режимах электростимуляции сердца.
Новым в способе является то, что проводят оценку направления кровотока в легочных, яремных и печеночной венах, а также наличия застойных изменений в печени при изменении режима электростимуляции сердца. В тех случаях, когда после изменения режима электростимуляции с двухкамерного предсердно-желудочкового на изолированный желудочковый выявляют кровоток ретроградного направления в легочных, яремных и печеночной венах по причине опорожнения предсердий при закрытых атриовентрикулярных (митральный и трикуспидальный) клапанах сердца вследствие несинхронизированного с активностью предсердий желудочкового стимула, а также увеличение реогепатографических диастолического и диастолосистолического индексов диагностируют синдром кардиостимулятора.
Выявление при изолированной желудочковой электростимуляции сердца ретроградного кровотока в легочных, яремных и печеночной венах, нарастание застойных явлений в печени являются достоверными признаками синдрома кардиостимулятора.
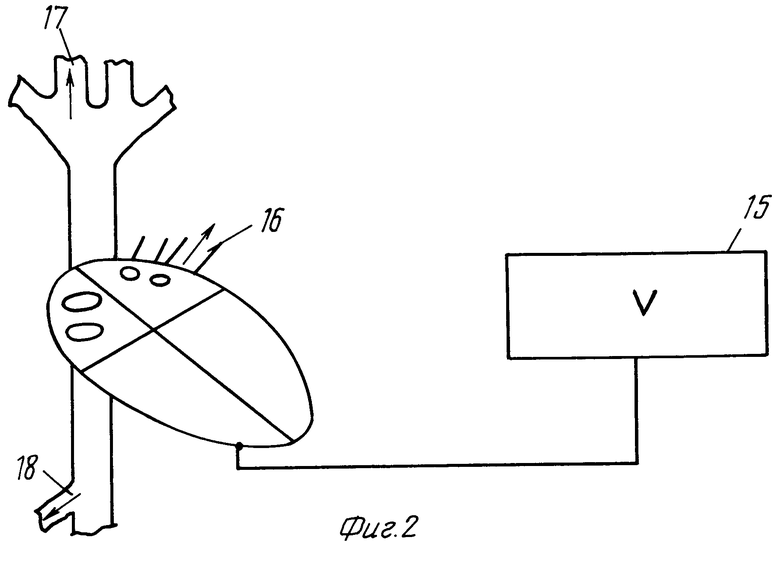
Способ изображен на схеме, где на фиг. 1 показаны некоторые особенности центральной гемодинамики у больного при двухкамерной предсердно-желудочковой электростимуляции сердца, на фиг. 2 - особенности центральной гемодинамики у того же больного при изолированной желудочковой электростимуляции сердца и синдроме кардиостимулятора. Условные обозначения: 1 - легочная вена, 2 - печеночная вена, 3 - яремная вена, 4 - кардиостимулятор, запрограммированный на двухкамерный предсердно-желудочковый режим электростимуляции сердца, 5 - антеградный кровоток в легочной вене, 6 - антеградный кровоток в яремных венах, 7 - антеградный кровоток в печеночной вене, 8 - правое предсердие, 9 - левое предсердие, 10 - митральный клапан сердца, 11 - трикуспидальный клапан сердца, 12 - антеградный кровоток через атриовентрикулярный клапан сердца, 13 - правый желудочек сердца, 14 - левый желудочек сердца, 15 - кардиостимулятор, запрограммированный на изолированный желудочковый режим электростимуляции сердца, 16 - ретроградный кровоток в легочной вене, 17 - ретроградный кровоток в яремных венах, 18 - ретроградный кровоток в печеночной вене.
Способ выполняют следующим образом: у больного с предсердным ритмом синусового происхождения и налаженной электростимуляцией сердца проводят оценку направления кровотока в легочных (1) и печеночной (2) венах посредством допплерэхокардиографии, кровотока в яремных венах (3) - посредством допплерографии магистральных сосудов шеи, исследование кровотока в печени - с помощью реогепатографии.
Допплерэхокардиографию в режиме цветного картирования потоков по стандартной методике проводят в положении больного лежа, используя эхокардиографическую установку, например аппарат "АСПЕН" производства фирмы "АКУСОН Корпорэйшн" (США), оснащенного мультичастотным датчиком 4V2C производства фирмы "АКУСОН Корпорэйшн" (США). Визуализацию легочных и печеночной вен проводят по общепринятым методикам (Шиллер Н., Осипов М.А. Клиническая эхокардиография. М.: Мир. 1993). Регистрацию полученного изображения потоков проводят на дисплее аппарата, а также на видеомагнитофонную ленту.
Допплерографию магистральных сосудов шеи проводят в положении больного лежа, используя допплерографический аппарат, например, "СОНОМЕД 300" производства АО "Спектромед" (Россия), оснащенного ультразвуковым датчиком с частотой функционирования 4,0 МГц. Регистрацию направления скоростных и спектральных характеристик кровотока в яремной вене проводят на дисплее персонального компьютера и посредством принтера.
Реогепатографию проводят в положении больного лежа, применяя компьютерную реогепатографическую установку, включающую персональный IBM совместимый компьютер, реограф, например Р4-02 производства НПО РЭМА (Украина), пластинчатые электроды. Электроды накладывают на больного следующим образом: 1-й электрод (размерами 3,0 x 4,0 см) устанавливают спереди, располагая его в области пересечения правой срединно-ключичной линии с реберной дугой, так чтобы большая часть его площади находилась латеральнее этой линии; 2-й электрод (размерами 6,0 x 10,0 см) следует расположить на уровне нижней границы правого легкого на середине расстояния между позвоночником и правой задней подмышечной линии. Регистрацию реогепатограммы и ее первой производной проводят на дисплее персонального компьютера и посредством принтера. Математический расчет величин реогепатографических индексов производится программным обеспечением персонального компьютера.
Оценку направления кровотока в легочных, яремных и печеночных венах у одного больного проводят при различных режимах и частотах электростимуляции сердца в следующей последовательности: при двухкамерном предсердно-желудочковом - частота электростимуляции сердца при исследовании составляет либо 70 имп/мин (в тех случаях, когда частота предсердного ритма синусового происхождения менее 70 в минуту) или соответствует частоте предсердного ритма (когда частота последнего превышает 70 в минуту). При изолированном желудочковом режиме исследование проводят при частоте импульсов 70 в минуту (в тех случаях, когда частота предсердного ритма синусового происхождения менее 70 в минуту), либо при частоте соответствующей или на 5 имп/мин превышающей частоту предсердного ритма (когда частота последнего превышает 70 в минуту). Изменение режима и частоты электростимуляции проводят посредством регулирующего устройства (программатора).
Исследование направления кровотока в легочных, яремных и печеночной венах проводят через 5 мин после программирования режима электростимуляции сердца, оценку реогепатографических индексов - через 1 сутки.
При двухкамерной предсердно-желудочковой электростимуляции сердца (4) в легочных, яремных и печеночной венах регистрируют кровоток антеградного направления (5, 6, 7) по причине своевременного опорожнения предсердий (8, 9) через атриовентрикулярные клапаны (10, 11) в желудочки сердца (12, 13, 14).
В тех случаях, когда после программирования режима электростимуляции сердца с двухкамерного предсердно-желудочкового на изолированный желудочковый (15) выявляют ретроградный кровоток в легочных (16), яремных (17) и печеночной (18) венах по причине опорожнения предсердий при закрытых атриовентрикулярных клапанах, а также увеличение реогепатографических диастолического и диастолосистолического индексов выявляют синдром кардиостимулятора.
Примеры конкретного выполнения.
Пример 1. Больная К., 66 лет. Диагноз: ишемическая болезнь сердца. Бинодальное поражение. Синдром слабости синусового узла - II тип, синоатриальная блокада. Транзиторная атриовентрикулярная блокада II ст. Имплантированный однокамерный желудочковый кардиостимулятор ЭКС-222. Истощение источника питания. Функциональный класс III по Нью-Йоркской Ассоциации кардиологов (NYHA).
Учитывая наличие истощения кардиостимулятора, низкую толерантность больной к повседневной нагрузке, для диагностики нарушений центральной гемодинамики при изолированной желудочковой электростимуляции сердца, выбора оптимального режима и параметров постоянной электростимуляции сердца при будущей замене стимулирующей системы у больной провели диагностику синдрома кардиостимулятора по разработанному способу.
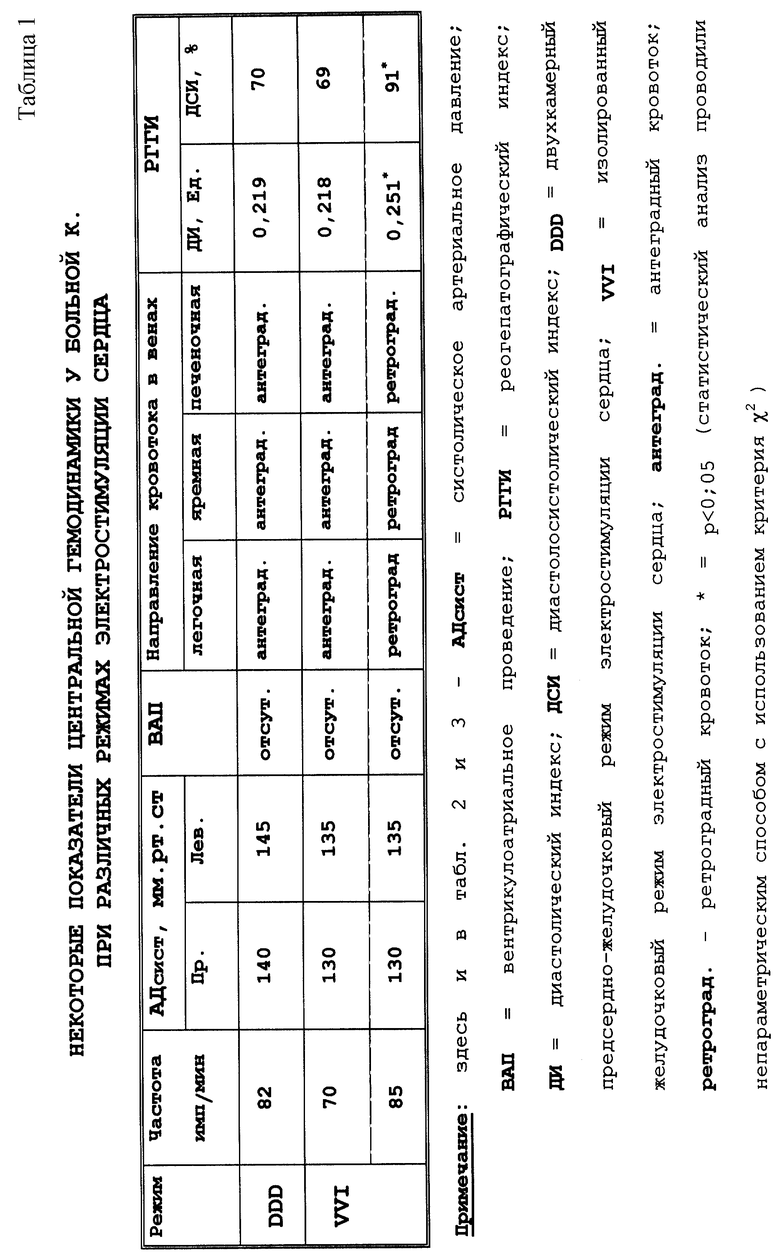
Некоторые показатели центральной гемодинамики больной К. при различных режимах электростимуляции сердца (однокамерной желудочковой, двухкамерной) приведены в табл. 1.
Исследование показало при изолированной желудочковой электростимуляции сердца с частотой 80 импульсов в минуту наличие ретроградного кровотока в легочных, яремных и печеночной венах, увеличение диастолического (+14,6%; χ2 = 14,1, p < 0,05) диастолосистолического (+30%; χ2 = 45,6, p < 0,05) реогепатографических индексов. При этом снижения артериального давления на плечевой артерии и признаков вентрикулоатриальной проводимости не выявили.
При нагрузочном тестировании на велоэргометре у больной определили наличие хронотропной недостаточности (неадекватной частотной реакции) синусового и атриовентрикулярного узлов сердца.
Заключение: 1) у больной выявлен синдром кардиостимулятора, 2) оптимальным режимом является двухкамерный частотно-адаптирующий DDDR режим, 3) показана операция замены желудочкового кардиостимулятора на двухкамерный.
С учетом полученных результатов больной была проведена замена однокамерного нечастотно-адаптирующего кардиостимулятора ЭКС-222 на двухкамерный частотно-адаптирующий аппарат СИНХРОНИ II, производства фирмы Пейссеттер-Сент Джуд Медикал (США). Осмотрена через 6, 12, 18 мес. Состояние оперированной улучшилось. Двойное слепое рандомизированное исследование показало, что за счет сохранения предсердно-желудочковой синхронизации и моделирования частотной реакции сердца толерантность больной к физической нагрузке на велоэргометре при двухкамерном частотно-адаптирующем режиме электростимуляции DDDR возросла на 50% в сравнении с аналогичным тестом, выполненным при желудочковом нечастотно-адаптирующем режиме VVI. Выполняет работу по дому и в саду. Величина функционального класса по NYHA снизилась до 1.
Пример 2. Больная В., 47 лет. Диагноз: ревматизм, неактивная фаза. Состояние после инструментальной коррекции стеноза левого атриовентрикулярного отверстия (закрытая митральная комиссуротомия). Миокардитический кардиосклероз. Синдром слабости синусового узла - III тип, синоатриальная блокада, пароксизмальная форма фибрилляции предсердий. Имплантированный однокамерный желудочковый кардиостимулятор ЭКС-500. Истощение источника питания. Функциональный класс III по NYHA.
Учитывая наличие истощения кардиостимулятора, низкую толерантность больной к повседневной нагрузке, для диагностики нарушений центральной гемодинамики при изолированной желудочковой электростимуляции сердца, выбора оптимального режима и параметров постоянной электростимуляции сердца при будущей замене стимулирующей системы провели диагностику синдрома кардиостимулятора по разработанному способу.
Некоторые показатели центральной гемодинамики больной К. при различных режимах электростимуляции сердца (однокамерной желудочковой, двухкамерной) приведены в табл. 2.
При изолированной желудочковой электростимуляции сердца выявили кровоток ретроградного направления в легочных, яремных и печеночной венах, увеличение диастолического (+24,7%; χ2 = 19,4, p < 0,05) и диастолосистолического (+18,4%; χ2 = 49,1, p < 0,05) реогепатографических индексов, вентрикулоатриальное проведение и отсутствие снижения величины артериального давления на плечевой артерии.
Нагрузочное тестирование на тредмилле показало наличие у больной изолированной хронотропной недостаточности синусового узла.
Заключение: 1) у больной выявлен синдром кардиостимулятора, 2) оптимальным режимом является двухкамерный частотно-адаптирующий DDDR режим, 3) показана операция замены желудочкового кардиостимулятора на двухкамерный. С учетом полученных результатов больной была проведена замена однокамерного нечастотно-адаптирующего кардиостимулятора ЭКС-500 на двухкамерный частотно-адаптирующий кардиостимулятор РИЛЭЙ 29403, производства фирмы Интермедикс (США). Осмотрена через 6, 12, 18, 24, 36, 48 мес. Состояние оперированной улучшилось. Двойное слепое рандомизированное исследование показало, что за счет сохранения предсердно-желудочковой синхронизации и моделирования частотной реакции сердца толерантность больной к физической нагрузке в ходе тредмилл-теста при двухкамерном частотно-адаптирующем режиме электростимуляции DDDR возросла на 100% в сравнении с аналогичным тестом, выполненным при желудочковом нечастотно-адаптирующем режиме VVI. Работает по прежней специальности (инженером). Величина функционального класса по NYHA снизилась до I.
Пример 3. Больной С. , 72 года. Диагноз: ишемическая болезнь сердца. Постинфарктный кардиосклероз. Атриовентрикулярная блокада III ст. Пароксизмальная форма трепетания предсердий. Имплантированный двухкамерный частотно-адаптирующий кардиостимулятор СИНХРОНИ. "Блокада выхода" импульса предсердного электрода. Неэффективная предсердная электростимуляция сердца. Функциональный класс II по NYHA.
Учитывая наличие "блокады выхода" предсердного электрода, обусловленной ростом порога возбуждения до 10 В в послеоперационном периоде, целесоообразность сохранения двухкамерного частотно-адаптирующего DDDR режима электростимуляции сердца по причине антиаритмического и ортохронотропного эффекта, для диагностики нарушений центральной гемодинамики при изолированной желудочковой электростимуляции сердца, решения вопроса о необходимости повторной операции с целью восстановления предсердной электростимуляции у больного провели диагностику синдрома кардиостимулятора по разработанному способу.
Некоторые показатели центральной гемодинамики больной С. при различных режимах электростимуляции сердца (однокамерной желудочковой, двухкамерной) приведены в табл. 3.
При изолированной желудочковой электростимуляции сердца выявили умеренное снижение величины систолического артериального давления 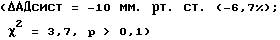 кровоток антеградного направления в легочных, яремных и печеночной венах, отсутствие вентрикулоатриального проведения и динамики величин диастолического и диастолосистолического реогепатографических индексов. При нагрузочном тестировании на велоэргометре определили хронотропную недостаточность синусового и атриовентрикулярного узлов сердца.
кровоток антеградного направления в легочных, яремных и печеночной венах, отсутствие вентрикулоатриального проведения и динамики величин диастолического и диастолосистолического реогепатографических индексов. При нагрузочном тестировании на велоэргометре определили хронотропную недостаточность синусового и атриовентрикулярного узлов сердца.
3аключение: 1) у больного синдром кардиостимулятора не выявлен; 2) возможно проведение однокамерной желудочковой частотно-адаптирующей злектростимуляции сердца до стабилизации величины порога возбуждения миокарда предсердий; 3) необходимость повторной операции с целью реимплантации предсердного электрода отсутствует.
С учетом полученных результатов больному было произведено программирование режима электростимуляции с двухкамерного частотно-адаптирующего DDDR на однокамерный желудочковый частотно-адаптирующий VVIR. Больной осмотрен через 2 мес. Состояние оперированного не изменилось. Толерантность к повседневной нагрузке средняя. Выполняет работу по дому. Сохраняется II функциональный класс по NYHA. Величина предсердного порога возбуждения миокарда снизилась до 2 В, что позволило восстановить двухкамерную стимуляцию сердца в режиме DDDR.
Способ диагностики синдрома кардиостимулятора неинвазивен, повышает точность диагностики нарушений центральной гемодинамики, может быть выполнен в отдаленном послеоперационном периоде после имплантации искусственного водителя ритма сердца, повышает эффективность применения электростимуляции сердца посредством проведения адекватного выбора режима и типа кардиостимулятора индивидуально у больного, способствует улучшению результатов применения электростимуляции сердца в клинической практике. Способ диагностики синдрома кардиостимулятора может быть применен для выбора оптимальных параметров электростимуляции сердца, оценки клинических преимуществ двухкамерной электростимуляции, обоснования показаний и противопоказаний к повторной операции.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ТРЕХКАМЕРНОЙ ЭЛЕКТРОСТИМУЛЯЦИИ СЕРДЦА | 1999 |
|
RU2159134C1 |
| СПОСОБ ДВУХКАМЕРНОЙ ЭЛЕКТРОСТИМУЛЯЦИИ СЕРДЦА | 1998 |
|
RU2169586C2 |
| СПОСОБ БИАТРИАЛЬНОЙ ЭЛЕКТРОСТИМУЛЯЦИИ СЕРДЦА | 1999 |
|
RU2167682C2 |
| СПОСОБ ОЦЕНКИ КОРОНАРНОГО И МИОКАРДИАЛЬНОГО РЕЗЕРВОВ СЕРДЦА ПРИ ТАХИКАРДИИ В УСЛОВИЯХ ДВУХКАМЕРНОЙ ЭЛЕКТРОКАРДИОСТИМУЛЯЦИИ | 1995 |
|
RU2119765C1 |
| СПОСОБ ОПТИМИЗАЦИИ ЧАСТОТНО-АДАПТИВНОЙ АТРИОВЕНТРИКУЛЯРНОЙ ЗАДЕРЖКИ В ДВУХКАМЕРНЫХ ЭЛЕКТРОКАРДИОСТИМУЛЯТОРАХ | 2007 |
|
RU2355444C1 |
| СПОСОБ ОЦЕНКИ ХРОНОТРОПНОЙ ФУНКЦИИ СЕРДЦА | 1994 |
|
RU2099003C1 |
| СПОСОБ ДИАГНОСТИКИ РАННИХ ПРИЗНАКОВ ХРОНИЧЕСКОГО ЛЕГОЧНОГО СЕРДЦА НА ДОКЛИНИЧЕСКОЙ СТАДИИ СИЛИКОЗА | 2000 |
|
RU2202941C2 |
| СПОСОБ ДИАГНОСТИКИ ПРОГРЕССИРУЮЩЕЙ СТЕНОКАРДИИ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА | 2000 |
|
RU2194995C2 |
| СПОСОБ КАТЕТЕРИЗАЦИИ СЕРДЦА ДЛЯ УСТАНОВКИ ЭНДОКАРДИАЛЬНОГО ЭЛЕКТРОДА ДЛЯ ВРЕМЕННОЙ ЭЛЕКТРОКАРДИОСТИМУЛЯЦИИ У ПАЦИЕНТОВ С ОСТРЫМ КОРОНАРНЫМ СИНДРОМОМ, С ПОДЪЕМОМ СЕГМЕНТА ST, ОСЛОЖЕННЫМ НАРУШЕНИЯМИ ПРОВОДИМОСТИ (ВАРИАНТЫ) | 2015 |
|
RU2594243C1 |
| СПОСОБ ПУНКЦИИ И КАНЮЛЯЦИИ ПОДМЫШЕЧНОЙ ВЕНЫ | 2017 |
|
RU2641385C1 |


Изобретение относится к медицине, кардиохирургии, кардиологии. Проводят последовательную смену режима электростимуляции с двухкамерного на изолированный желудочковый. Одновременно регистрируют направление кровотока в легочных, яремных и печеночной венах. При определении в случае изолированной желудочковой электростимуляции сердца ретроградного кровотока в легочных, яремных и печеночной венах, увеличения диастолического и диастолосистолического реогепатографических индексов выявляют синдром кардиостимулятора. Способ позволяет производить подбор оптимального режима электростимуляции сердца, исключив синдром кардиостимулятора. 2 ил., 3 табл.
Способ диагностики синдрома кардиостимулятора путем измерения артериального давления и оценки вентрикулоатриального проведения сердца, отличающийся тем, что дополнительно проводят последовательную смену режима электростимуляции с двухкамерного на изолированный желудочковый с одновременной регистрацией направления кровотока в легочных, яремных и печеночной венах, и при определении в случае изолированной желудочковой электростимуляции сердца ретроградного кровотока в легочных, яремных и печеночной венах, увеличения диастолического и диастолосистолического реогепатографических индексов выявляют синдром кардиостимулятора.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| БРЕДИКИС Ю.Ю., СТИРБИС П.П | |||
| и др | |||
| Программируемая электростимуляция сердца | |||
| - М.: Медицина, 1989, с.63 - 65 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ШИЛЛЕР Н., ОСИПОВ М.А | |||
| Клиническая эхокардиография | |||
| - М.: Мир, 1993, с. | |||
Авторы
Даты
2001-05-27—Публикация
1998-10-23—Подача