Настоящее изобретение относится к применению экстрактов сем. Iridaceae по п.1 и экстрактов Cimicifuga racemosa по п.5 в качестве действующего по типу эстрогена органселективного лекарственного препарата, а также к применению текторигенина и/или гликозидов текторигенина в качестве лекарственного препарата по п.13.
Образующийся в яичниках 17-β-эстрадиол (где бы эстрадиол ни упоминался далее, это всякий раз относится к физиологическому 17-β-эстрадиолу [далее также упоминаемому как Е2]) в организме обычно имеет функцию ускорения пролиферации. Помимо регулирования женского цикла, он, например, оказывает гомеостатическое влияние на костный метаболизм и предотвращает образование атеросклеротических бляшек на эндотелии сосудов.
Во время менопаузы из-за прекращения функции яичников происходит снижение уровня эстрадиола. Это вызывает ослабление процессов пролиферации и в гипоталамусе приводит к повышенной активности генератора импульсов ГтВГ (генератор импульсов гонадотропинвысвобождающего гормона является таймером в гипоталамусе и поэтому отбивает такт периодической секреции ЛГ (лютеинизирующего гормона) стероидами, влияющими на ее амплитуду и частоту). В итоге у женщин в климаксе простимулированная секреция ЛГ влечет за собой так называемые “приливы”, которые ощущаются как раздражающие.
При отсутствии достаточно высокого уровня эстрадиола в крови активность остеокластов и, таким образом, разрушение костной массы преобладает, что сопровождается увеличением риска переломов костей. В то же время существует долгосрочный риск образования бляшек в сосудистой системе и, следовательно, возрастает риск инфарктов.
Экстракты Cimicifuga racemosa и Belamcanda sinensis хорошо известны в народной медицине, как способные смягчать пери-менопаузные и пост-менопаузные нарушения. До настоящего времени это объясняли тем фактом, что экстракты обоих растительных лекарственных веществ проявляют действие, подобное эстрогену, со всеми его положительными воздействиями на множество органов человеческого тела, в особенности на мозг, яичники, кости, сосудистую систему. В свою очередь, подобное эстрогену воздействие на матку, влагалище, ткани молочной железы и печени будет неблагоприятным.
Известно получение лекарственных препаратов на основе экстрактов из растений семейства Iridaceae, например, посредством получения спиртовых эссенций с последующей экстракцией активных ингредиентов эфиром, как описано в JP 63-196522, для лечения язвенных заболеваний или водных, а также спиртовых экстрактов из Belamcanda sinensis на основе низших и многоатомных спиртов для предотвращения старения кожи, как показано в JP 07-138179.
Известно также, что одним из активных компонентов растительных экстрактов семейства Iridaceae является текторигенин, различные соединения которого, выделенные из растений Belamcanda sinensis, подробно описаны в JP 63-030417 для применения в качестве противоаллергенных препаратов.
Наиболее близким источником является патент DE 19652183, в котором описано получение экстрактов из Cimicifuga racemosa для лечения эстрогензависимых опухолей. Согласно патенту на основе указанных экстрактов получены терапевтические препараты, оказывающие экстрогенподобное действие и ингибирующие пролиферацию опухолевых клеток.
Плохо, однако, то, что вплоть до настоящего времени лекарство из этих лекарственных растений, которое можно было бы использовать в органселективной профилактике или в лечении в случаях эстрогенной недостаточности и которое при этом не оказывало бы неблагоприятного воздействия на матку, влагалище и другие органы, не было доступно.
Исходя из этого, задачей настоящего изобретения, таким образом, является получение растительных лекарственных веществ с действием, подобным эстрогену, при этом таким образом, чтобы их действие являлось органселективным без воздействия или со слабым воздействием на матку.
Задача независимо достигается согласно признакам п.1 путем применения экстрактов сем. Iridaceae и п.5 посредством применения экстрактов Cimicifuga racemosa для получения подобного эстрогену органселективного лекарственного препарата, не имеющего утеротропного эффекта или имеющего таковой, каким, по меньшей мере, можно пренебречь. Вышеуказанная задача, более того, может быть решена посредством применения лекарственных препаратов на основе текторигенина и/или его гликозидов за исключением экстрактов сем. Iridaceae, или экстрактов, обогащенных текторигенином и/или экстрактом текторигенина, для получения подобных эстрогену органселективных лекарственных препаратов, не имеющих утеротропного эффекта или имеющих таковой, каким можно, по меньшей мере, пренебречь согласно п.9 и 13.
В экспериментах как in vitro, так и in vivo, к удивлению, было обнаружено, что экстракты, получаемые как из сем. Iridaceae, в особенности Belamcanda sinensis, так и из Cimicifuga racemosa органическими растворителями или сверхкритическим СО2, органселективно воздействуют на центральную нервную систему, костную систему и сосудистую систему при отсутствии воздействия на матку, т.е. при отсутствии так называемого утеропропного эффекта. Экстракты, используемые в соответствии с изобретением, таким образом подходят для производства лекарственных препаратов в готовой рецептурной форме для селективного лечения и/или профилактики остеопороза.
Более того, такие экстракты подходят для производства лекарственных препаратов в готовой рецептурной форме для селективного лечения и/или профилактики кардиоваскулярных заболеваний, в особенности атеросклероза.
Более того, они подходят для получения лекарственных препаратов с готовой рецептурой для селективного лечения и/или профилактики пери-менопаузных и пост-менопаузных психовегетативных расстройств таких, как, например, приливы.
Более того, было обнаружено, что компонент текторигенин, который был выделен из Belamcanda sinensis, по существу вызывает тот же эффект, что и экстракт в целом.
Текторигенин
Помимо Belamcanda sinensis, этот компонент был обнаружен в других представителях сем. Iridaceae, таких как, например, Iris germanica, I. tectorum, I. illyrica, I. dichotoma.
Таксономически Belamcanda sinensis классифицируется следующим образом:
Порядок Liliales
Семейство Iridaceae
Род Belamcanda
Виды Belamcanda sinensis (Leman) DC=Pardanthus chinensis (L.)Ker-Gawler, a также Ixia chinensis L.(=Gemmingia chinensis (L.) O. Kuntze).
Для получения экстрактов предпочтительно использовать корневища, стебли, листья и/или лепестки.
Фундаментальное фитохимическое описание Belamcanda sinensis и его составных частей дано в диссертации г-жи A.Nenninger (LMU Munchen, 1997), озаглавленной "Phytochemische und pharmakologische Untersuchungen von Belamcanda sinensis, einer Arzneipflanze der TCM und anderer Irisarten".
С лекарственными препаратами согласно изобретению впервые были получены лекарственные вещества из Cimicifuga racemosa и Belamcanda sinensis и других сем. Iridaceae и лекарственные препараты на основе текторигенина, которые действуют как полные антагонисты рецепторов эстрогена в костях, кардиоваскулярной системе и мозге.
Дальнейшие преимущества и признаки настоящего изобретения будут ясны из описания экспериментальных данных со ссылками на фигуры, показывающие:
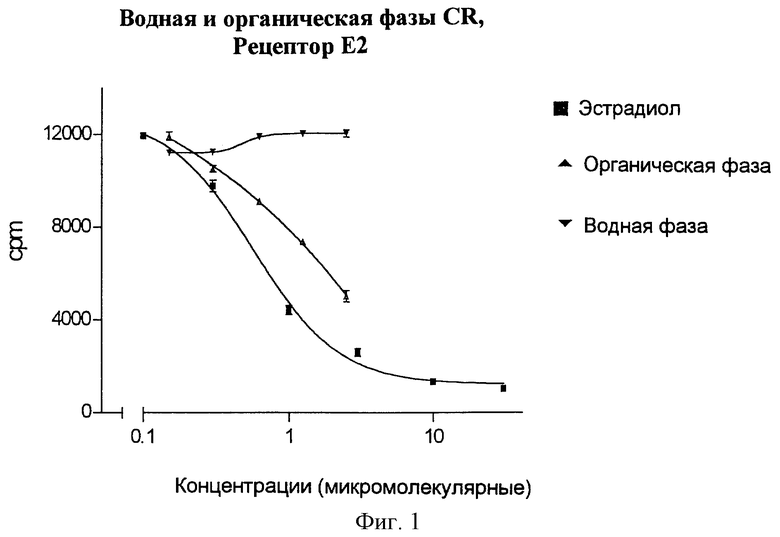
фиг.1: сравнение органической и водной фаз Cimicifuga racemosa. График замещения типичного эстрогенового рецептора в опытах по связыванию лигандов. Концентрация стартового раствора 17.66 мг/мл с последующим разбавлением 1:2, 1:4 и т.д. до 1:64.
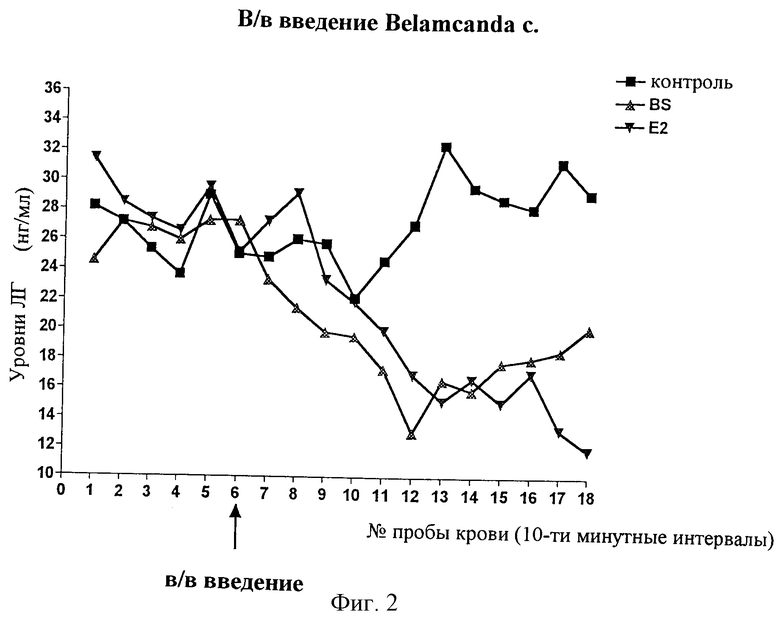
фиг.2: ЛГ в сыворотке до и через 2 часа после внутривенного введения экстракта Belamcanda sinensis, E2 и наполнителя. Экстракт Belamcanda sinensis имеет аналогичную способность снижать повышенный уровень ЛГ в сыворотке как и E2.
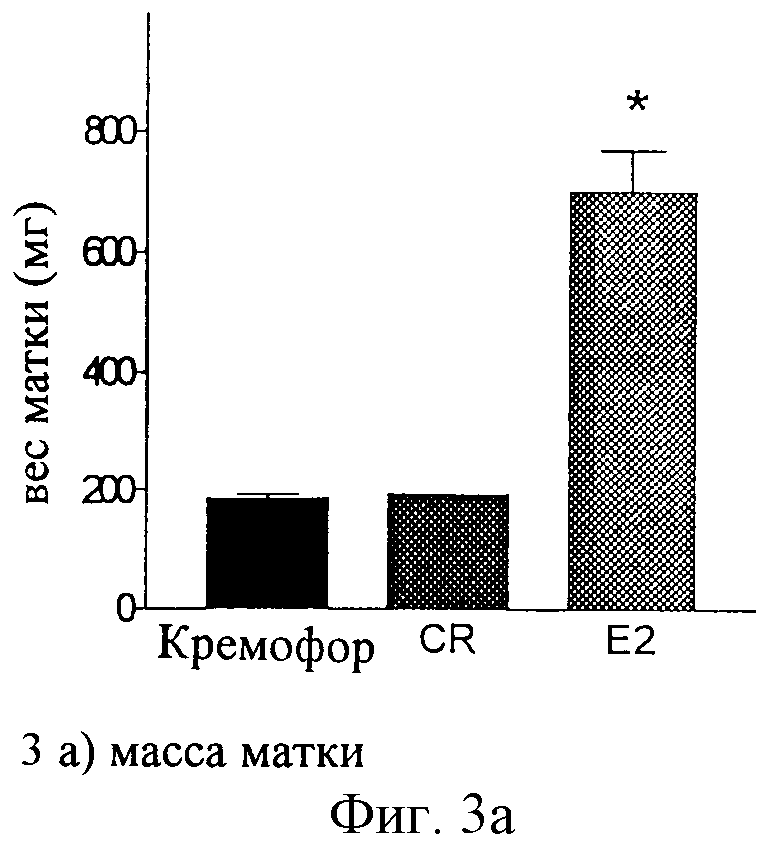
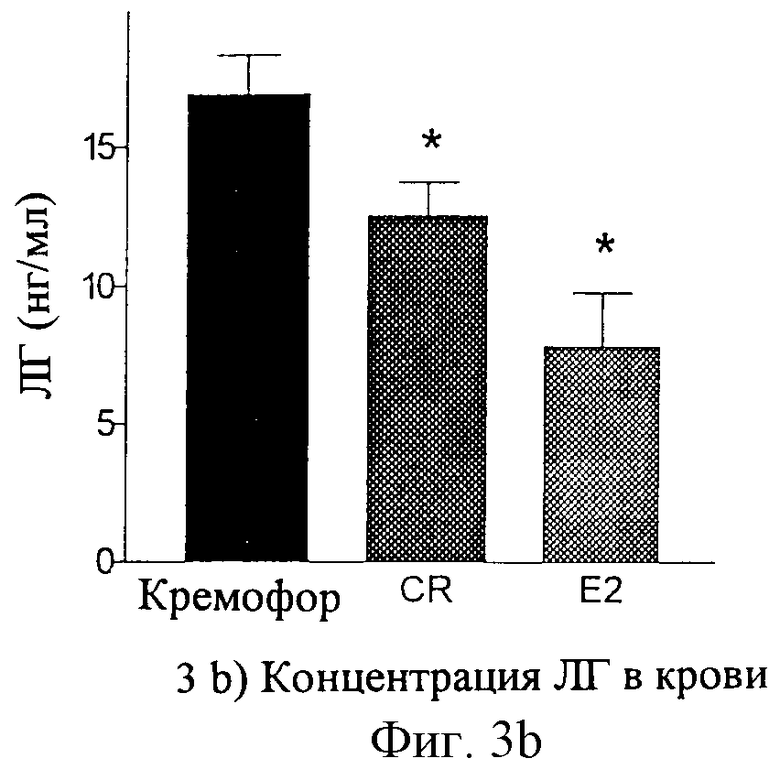
фиг.3: влияние Cimicifuga racemosa и E2 на вес матки (Фиг.3а) и уровни ЛГ в крови (Фиг.3b) у овариэктомированных крыс после семидневного подкожного введения (среднее значение + СВЗ, n=8*, р<0.05 в сравнении с кремофором в качестве наполнителя);
фиг.3а): массы матки;
фиг 3b): концентрации ЛГ в крови;
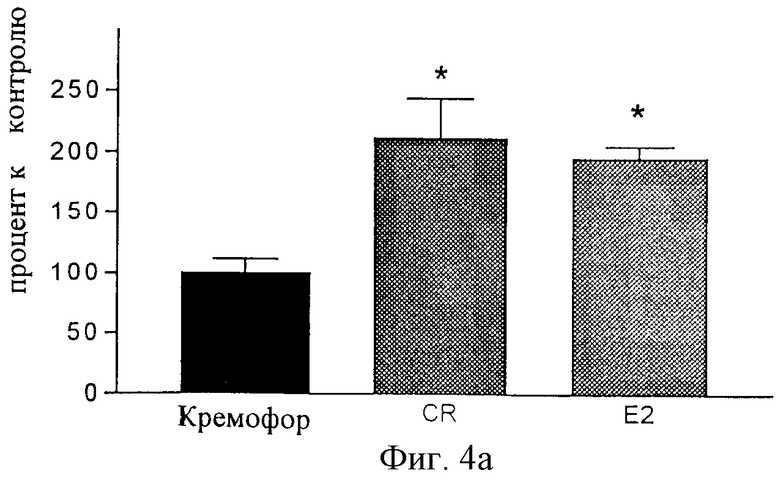
фиг.4а): влияние Cimicifuga racemosa и E2 у овариэктомированных крыс после семидневного подкожного введения (среднее значение + СВЗ, n=8*, р<0.05 в сравнении с кремофором в качестве наполнителя) на экспрессию мРНК для Е2-рецептора α в преоптической зоне гипоталамуса;
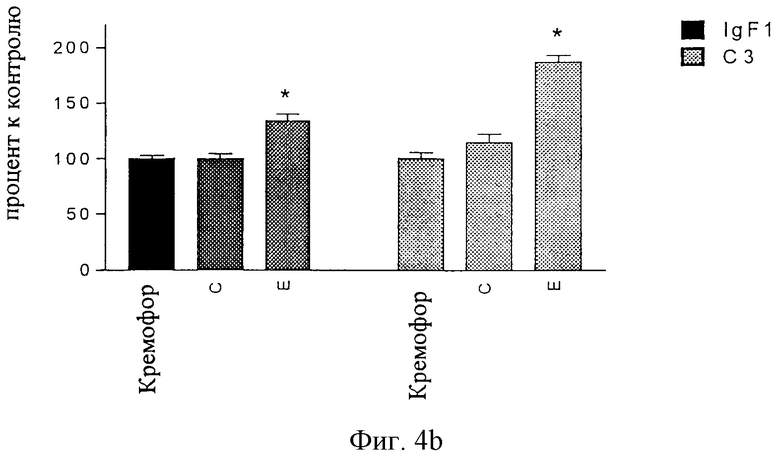
фиг 4b): экспрессия мРНК для IGF1 и С3 в матке овариэктомированных крыс после семидневного подкожного введения и
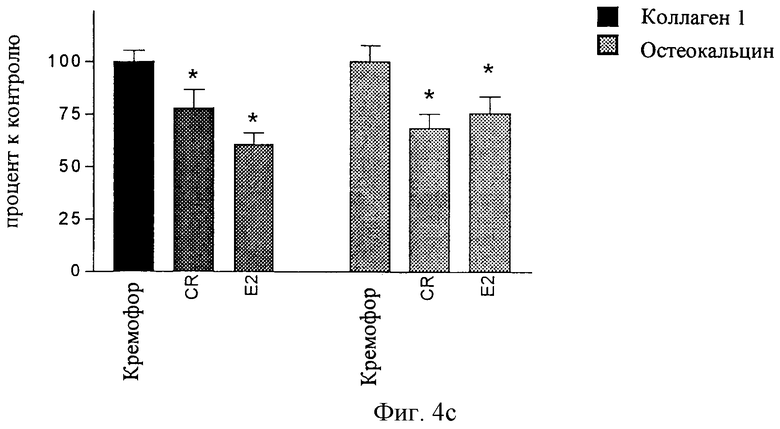
фиг.4с): экспрессия мРНК для коллагена 1 (Coll 1) и остеокальцина в кости овариэктомированных крыс после 7 дней подкожного введения.
Экспериментальное подтверждение подобного эстрогену воздействия Cimicifuga racemosa и Belamcanda sinensis
Подобное эстрогену селективное воздействие было продемонстрировано по стадиям по порядку на сериях тест-систем различной степени сложности.
1. Эксперименты in vitro
1.1. Эксперименты in vitro на Cimicifuga racemosa
Распознавание эстрогеноподобной структуры компонентов антителами, направленньми против 17-β-эстрадиола (=Е2) показано in vitro.
Экстракт Cimicifuga racemosa выпаривали над остатком. Вещества, имеющие разные полярности, обогащали фазовым разделением между дихлорметаном и водой. Сродство к связыванию компонентами обеих фаз было определено in vitro на эстрогенных рецепторах из матки свиньи. Цитозольные эстрогенные рецепторы из матки свиньи выделяли в соответствии с обычной методикой и использовали в экспериментах по замещению лигандов.
При этом было обнаружено, что эстрогеноподобные структуры, например, из Cimicifuga racemosa по природе своей не гидрофильны, а липофильны, поскольку их можно извлекать из экстракта органическими растворителями. Вещества, присутствующие в органически экстрагированной фазе, имели сродство с антителами, в десять раз более сильное, чем вещества, остающиеся в водной фазе.
Различия между двумя фазами в сериях опытов со связыванием с рецепторами эстрадиола были еще больше. Сродство связывающих веществ к эстрадиолу должно быть достаточно высоким, чтобы обеспечить селективно-конкурентное взаимодействие с рецептором эстрадиола в свободном от клеток препарате. В пределах данной тест-системы водная фаза не обладала активностью, тогда как органическая фаза имела очень сильное связывание с рецептором.
Результаты представлены на фиг.1.
1.2. in vitro Belamcanda sinensis
По результатам других исследований известно, что экстракты Belamcanda sinensis также имеют компоненты, которые распознаются антителами, направленными против 17-β-эстрадиола, и связываются с рецептором 17-β-эстрадиола (cf. Nenninger loc. cit.). К удивлению авторов настоящей заявки было обнаружено, что эти экстракты оказывают подобное эстрогену различное воздействие на разные системы органов и, в частности, отсутствие у них утеротропного эффекта.
2. Эксперименты in vivo: Подтвержение эстрогенного воздействия на овариэктомированную крысу
Связывание с рецептором Е2 очень селективно; однако невозможно сказать, ускоряются или ингибируются последущие процессы внутри клетки, т.е. является ли вещество агонистом или антагонистом. Это свойство может быть определено только в подходящих клеточных системах или на целом животном.
Овариэктомированная крыса является признанной моделью пост-менопаузной женщины, у которой прекращается выработка эстрадиола. В результате внешнего поступления 17-β-эстрадиола или веществ, имеющих подобное эстрогену воздействие, происходит восстановление эстроген-чувствительных анатомо-морфологических параметров, таких как увеличение веса матки и распространение ороговевших клеток, т.е. бляшковых эпителиальных клеток в эпителии влагалища, или гормональные изменения, такие, как снижение уровня ЛГ в крови обработанных животных.
Все описанные далее эксперименты проводили на овариэктомированных крысах Sprague-Dawley (=овэ крысы), имеющих вес от 240 до 280 г.
2.1. Однократное применение Belamcanda sinensis
Проявление действия экстракта Belamcanda sinensis, действующего по типу эстрадиола, происходит очень быстро. Даже после однократного в/в введения наполнителя, эстрадиола и экстракта Belamcanda sinensis ОВЭ крысам пульсативность прекращается как под действием Е2, так и под действием Belamcanda sinensis. При оценке степени усовершенствования лекарственного препарата происходит достоверное снижение уровня ЛГ в сыворотке как в сравнении с предыдущими уровнями, так и в сравнении с обрабатываемыми кремафором контрольными животными. Кремафор является эмульгатором на основе полиэтоксилированных производных касторового масла.
Результаты представлены на фиг.2.
В матке животных через шесть часов после введения экстракта Belamcanda sinensis экспрессия маточных генов VEGF, IGF 1 и С3 не менялась по сравнению с контролем, тогда как введение эстрадиола вызвало четкое увеличение экспрессии генов этих трех эстрогенрегулируемых белков. На конститутивно экспрессируемый ген ССО ни одна из этих обработок не оказала достоверного влияния.
Эти находки указывают на то, что компоненты Belamcanda sinensis вызывают ингибирование генератора импульсов ГтВГ в эстрогенрецептивных структурах гипоталамуса и таким образом имеют эстрогенагонистический эффект. При этом гипофизарная секреция ЛГ значительно ингибируется как компонентами Belamcanda sinensis, так и эстрадиолом. В противоположность эстрадиолу компоненты Belamcanda sinensis не имеют утеротропного действия. Эстрадиол существенно регулирует экспрессию генов VEGF, IGF1 и С3 в сторону увеличения - действие, которое не наблюдается у Belamcanda sinensis.
Проведение активных опытов по влиянию в/в инъекций
экстракта Belamcanda sinensis
24 крысам (т.е. по 8 животных в группе) под эфирной анестезией за день до начала эксперимента в яремную вену имплантировали катетер. В день эксперимента отобрали 6 проб крови с интервалом в 10 минут. Сразу после отбора шестой пробы 62.5 мг (5%) экстракта Belamcanda sinensis или 10 микрограмм 17-β-эстрадиола (Е2) или раствор (5%) кремофора в изотоническом NaCl 1 мл соответственно вводили внутривенно и в течение еще 2 часов с 10-минутным интервалом отбирали пробы крови. Через 6 часов после внутривенного введения животных обезглавили, отобрали кровь, вырезали яичники, взвесили и подвергли глубокой заморозке в жидком азоте.
2.2. Однократное применение текторигенина
После однократного введения текторигенина было определено его влияние во времени на уровень ЛГ в крови и подобная эстрадиолу иммунореактивность. Концентрация текторигенина в крови животных, определенная с помощью Е2-РИА через 20 минут, соответствует эквивалентам примерно 100 пикограммов эстрадиола.
Текторигенин иницирует быстрое снижение ЛГ. Кинетика снижения ЛГ, полученная под действием текторигенина до 60 минут вслед за в/в введением, прекрасно соотносится с таковой эстрадиола, но затем не приводит к дальнейшему снижению, а вновь медленно возрастает.
Проведение: ОВЭ-крысы имели катетеры, помещенные в наружную яремную вену под эфирной анестезией за 24 часа до начала эксперимента в соответствии с методикой Harms & Qjega (Harms PG and Ojega SR: A rapid and simple procedure for chronic cannulation of the rat jugular vein. J. Appl. Physiol. (1974) 36:391-392). Конец трубки помещали в кожный карман на шее. С тем чтобы при отборе проб крови не надо было трогать животных, катетер удлинили с помощью силиконовой трубки. Катетер и трубку промыли раствором Рингера, содержащим 50 IU (международных единиц) гепарина/мл.
Пробы крови, каждая по 100 микрограмм, отбирали у животных с 10-минутными интервалами, а отобранный объем возмещали раствором Рингера с гепарином. После отбора 6-й пробы внутривенно вводили по 1.0 мл соответствующего тестируемого раствора. В качестве тестируемых растворов использовали: 2% кремофор (=раствор наполнителя), текторигенин 7 мг/мл наполнителя, 17-β-эстрадиол 10 микрограмм/мл наполнителя. Кровь с 10 минутными интервалами брали еще в течение 140 минут.
Пробы крови, полученные таким образом, помещали в сосуд для реакций Eppendorf объемом 0.5 мл с 10 мл гепарин-Losung (5000 международных единиц/мл, Liquemin), центрифугировали в течение 10 минут при 10000*g и плазму хранили при -20°С до проведения радиоиммунологических анализов.
РИА для ЛГ и пролактина основаны на антисыворотке, контрольные и иодирующие препараты от фирмы NIH (Bethesda, Maryland, USA). Концентрации эстрадиола и перекрестно реагирующих изофлавонов измеряли при помощи РИА из DPC, Bad Nauheim.
2.3. Влияие экстракта Belamcanda sinensis
после введения в течение 7 дней
Влияние неоднократного введения эстрадиола, экстракта Belamcanda sinensis и наполнителя на общую массу, массу матки, гормональный уровень и активацию генов матки и кости было исследовано на овариэктомированных крысах после ежедневного подкожного введения в течение 7 дней.
Средние массы тел животных, получавших кремофор и Belamcanda sinensis, не различались, тогда как животные, получавшие Е2, были достоверно легче. Также достоверно не различались массы маток животных, получавших кремофор и Belamcanda sinensis, тогда как те, которые получали Е2, более чем утроили массу маток.
Уровни сывороточного ЛГ у животных, получавших Belamcanda sinensis, снижались незначительно, но достоверно по сравнению с контрольными кремофорными, снижение под действием эстрадиола было более выраженным.
В маточном экстракте мРНК экстрадиол достоверно повышал экспрессию генов VEGF до 149% по сравнению с контролем после одной недели введения. Под действием экстракта Belamcanda sinensis экспрессия слегка, но недостоверно, возрастала. Не была затронута экспрессия неэстрогенрегулируемых основных генов на примере цитохром С оксидазы (=ЦСО).
В экстракте головки бедренной кости была определена экспрессия генов коллаген-1А1, остеокальцина, IGF1 и TGF β-мРНК. Эстрадиол так же, как и Belamcanda sinensis, достоверно ингибирует экспрессию всех 4 генов, не оказывая влияния на ген ЦСО.
Различие в действии эстрадиола и Belamcanda становится ярко выраженным после семидневной обработки. Экстракт Belamcanda sinensis имеет эстрадиолагонистическое влияние на гипофизарную секрецию ЛГ путем ингибирования генератора импульсов ГтВГ и на генную экспрессию четырех эстрогенрегулируемых генов в кости. В отличие от этого эстрогенное воздействие на матку отсутствует: ни масса матки, ни эстрогензависимый ген VEGF не подвергаются влиянию экстракта Belamcanda sinensis. В отличие от этого эстрадиол вызывает раздувание матки и активацию гена VEGF.
Проведение подострых опытов по влиянию ежедневного подкожного введения в течение 7 дней:
8-ми животным из каждой опытной группы (всего 24) ежедневно с 8:00 до 9:00 подкожно вводили 62.5 мг экстракта Belamcanda sinensis, 10 микрограмм эстрадиола или растворителя (кремафор 5%, 1 мл) соответственно. Через 6 часов после последнего введения животных обезглавливали и у каждого животного отбирали аорту, матку, головку левой бедренной кости, очищали и замораживали в жидком азоте.
В пробах крови определяли ЛГ и иммунореактивность эстрадиола.
2.4. Повторное применение Cimicifuga racemosa
Не ранее 14 дней после овариэктомии животным подкожно вводили соответствующие тестируемые вещества в дозах 62.5 мг Cimicifuga racemosa на крысу или 8 микрограмм эстадиола на крысу один раз в день утром в течение 7 дней. Оба вещества были растворены в 5% кремофоре, контрольные животные получали только наполнитель.
Вслед за обезглавливанием животных мозг, матку и бедро препарировали для регенерации мРНК. Концентрацию ЛГ в крови животных определяли с помощью РИА. Экспрессию эстрогенрегулируемых генов в вышеназванных органах определяли с помощью полуколичественного анализа RT-PCR.
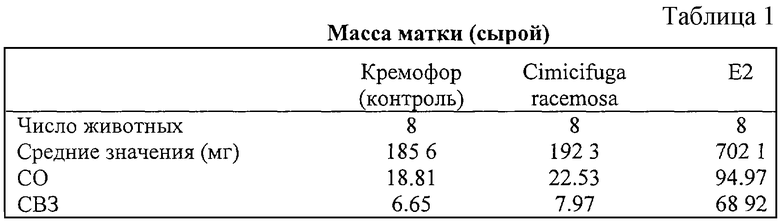
Матки животных, обработанных эстрадиолом, были более чем в три раза больше по массе, чем таковые животных, обработанных Cimicifuga racemosa и наполнителем, которые по существу не отличались по своим средним значениям. Это означает, что компоненты Cimicifuga racemosa не влияют на матку животных. Это же справедливо для влагалища, где не происходит ороговения эпителиальных тканей у животных, получавших Cimicifuga racemosa и наполнитель, в прямую противоположность животным, получающим эстрадиол.
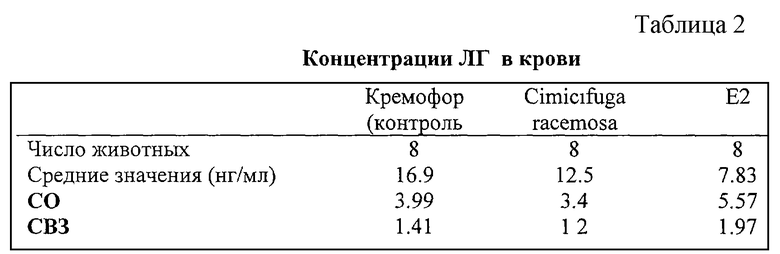
Уровни ЛГ животных, получавших наполнитель, оставались высокими, однако достоверно снижались под действием как эстрадиола, так и Cimicifuga racemosa.
Результаты представлены на фиг.3а), 3b) и в табл. 1 и 2.
Масса матки (сырой) дана в табл. 1. Концентрации ЛГ в крови даны в табл. 2.
В качестве другого маркера эстрогенного влияния была измерена активация мРНК эстрогенстимулируемых белков. В данной работе измерения проводили на тканях из матки, из кости (бедреная) и из преоптической зоны гипоталамуса.
В гипоталамусе как Cimicifuga racemosa, так и Е2 стимулировали экспрессию мРНК для эстрогенного рецептора α (фиг.4а). В костной ткани Cimicifuga racemosa тоже ведет себя, как эстроген, и снижает по аналогии с эстрадиолом экспрессию мРНК для костно-специфического коллагена 1 и для генов остеокальцина (фиг.4b).
Напротив, не наблюдали влияния Cimicifuga racemosa на эстрогенрегулируемые гены в матке. Только эстрадиол повышает мРНК для IGF и комплиментарного фактора С3 (фиг.4с).
Эти находки доказывают, что компоненты Cimicifuga racemosa селективно воздействуют на отдельные органы: экстракт действует эстрогеноподобно в гипоталамусе (экспрессия Е2 рецептора α, высвобождение ЛГ) и на кость, что доказано экспрессией генов для коллагена 1 и остеокальцина. Однако в отличие от эстрадиола Cimicifuga racemosa не влияет на матку, поскольку проявляется отсутствие влияния на массу матки и экспрессию генов IFG1 и С3.
Экспериментами, проведенными in vivo и in vitro, может быть продемонстрировано, что экстракты Cimicifuga racemosa и Belamcanda sinensis оказывают подобное эстрогену действие. К удивлению, было обнаружено, что экстракты из названных лекарственных веществ действуют органселективно на центральную нервную систему, кость и сосуды, но не на матку и таким образом отлично подходят для профилактики и лечения эстрогенной недостаточности без отрицательного влияния на эндометрий.
Идентичные эффекты были достигнуты при использовании текторигенина, содержащегося в Belamcanda.
Таким образом, впервые стали доступными лекарственные препараты с действием, подобным эстрогену, но без утеротропного эффекта.
Подобные лекарственные препараты могут быть использованы для лечения и/или профилактики кардиоваскулярных заболеваний, особенно атеросклероза, остеопороза и пери- и пост-менопаузных психовегетативных расстройств, таких как, например, приливы.
Известны оральный, внутривенный и подкожный способы употребления.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ ЭКСТРАКТА BELAMCANDA CHINENSIS В КАЧЕСТВЕ ПОДОБНОГО ЭСТРОГЕНУ ОРГАН-СЕЛЕКТИВНОГО ЛЕКАРСТВЕННОГО ПРЕПАРАТА, НЕ ИМЕЮЩЕГО УТЕРОТРОПНОГО ЭФФЕКТА | 1999 |
|
RU2263505C2 |
| ПРИМЕНЕНИЕ ЭКСТРАКТОВ И ПРЕПАРАТОВ ИЗ РАСТЕНИЙ СЕМЕЙСТВА IRIDACEAE И ТЕКТОРИГЕНИНА В КАЧЕСТВЕ МЕДИКАМЕНТА ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ МОЧЕПОЛОВОГО ТРАКТА, СВЯЗАННЫХ С ПОЛОВЫМИ ГОРМОНАМИ | 2002 |
|
RU2300387C2 |
| Композиция для предупреждения, облегчения или лечения климактерического синдрома у женщин, содержащая логанин или его производные в качестве активного ингредиента | 2017 |
|
RU2697672C1 |
| 17,17-ДИМЕТИЛ-D-ГОМО-B-НОР-8α-ЭСТРОН, ОБЛАДАЮЩИЙ ГИПОЛИПИДЕМИЧЕСКОЙ И КАРДИОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2391351C1 |
| СПОСОБЫ ЛЕЧЕНИЯ РАКА | 2016 |
|
RU2737496C2 |
| 15β-ЗАМЕЩЕННЫЕ СТЕРОИДЫ С ИЗБИРАТЕЛЬНОЙ ЭСТРОГЕННОЙ АКТИВНОСТЬЮ | 2005 |
|
RU2386637C2 |
| СПОСОБЫ ЛЕЧЕНИЯ И/ИЛИ ПОДАВЛЕНИЯ ПРИРОСТА МАССЫ | 2000 |
|
RU2327461C2 |
| ГИДРОКСИМАТАИРЕЗИНОЛ В ПРОФИЛАКТИКЕ РАКА | 2000 |
|
RU2241453C2 |
| ПРОИЗВОДНЫЕ СУЛЬФАМАТА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ СОСТАВЫ | 1996 |
|
RU2159774C2 |
| СПОСОБЫ ЛЕЧЕНИЯ И/ИЛИ ПОДАВЛЕНИЯ ПРИРОСТА МАССЫ | 2000 |
|
RU2519642C2 |
Настоящее изобретение относится к использованию экстрактов сем. Iridaceae и Cimicifuga racemosa и текторигенина в качестве подобного эстрогену, органселективного лекарственного препарата для селективного лечения и/или профилактики кардиоваскулярных заболеваний, особенно атеросклероза, остеопороза и климактерических нарушений, например, для предотвращения или смягчения приливов. Технический результат: утеротропный эффект практически не наблюдается. 4 с. и 10 з.п. ф-лы, 4 ил., 2 табл.
| JP 63030417, 09.02.1988.DE 19652183, 12.02.1998.RU 2012348 C1, 15.05.1994.RU 2114629 C1, 10.07.1998. |
Авторы
Даты
2004-05-10—Публикация
1999-03-19—Подача