Изобретение относится к медицине, а именно к нейрохирургической реанимации и интенсивной терапии, и может быть использовано для определения причин внутричерепной гипертензии (ВЧГ) в остром периоде субарахноидального кровоизлияния (САК) у больных после разрыва артериальных аневризм (АА).
Актуальность предлагаемого способа продиктована высоким риском формирования осложнений в остром периоде САК у больных после разрыва АА, а именно отека головного мозга и острой гидроцефалии после прорыва крови в желудочковую систему мозга с обтурацией путей ликворооттока.
В настоящее время «золотым стандартом» измерения внутричерепного давления (ВЧД) у нейрохирургических больных, в том числе с острой сосудистой патологией головного мозга, является метод регистрации ВЧД с помощью вентрикулярного датчика (Lieberman D., Matz Р., Rosgay H. History of the Strain Gauge in Measurement of the Intracranial Pressure: From Engineers to Physiologists and Clinicians, J. Trauma. 2002, 52:172-8). Известный метод позволяет осуществлять не только мониторинг ВЧД, но и выполнять сброс ликвора из полости желудочков при формировании ВЧГ, что соответственно приводит к нормализации ВЧД.
Однако при измерении ВЧД у больных в остром периоде САК с угрозой развития отека головного мозга и острой гидроцефалии после прорыва крови в желудочковую систему головного мозга данный способ не позволяет четко отследить динамику развития обоих осложнений и соответственно выбрать оптимальный метод борьбы с синдромом ВЧГ. В ходе мониторинга ВЧД у таковых больных при использовании вентрикулярного датчика установить истинную причину ВЧГ не удается, поскольку увеличение объема ликвора при острой гидроцефалии влечет за собой нарастание ликворного давления; ликворное давление также возрастает и при формировании отека мозга, хотя объем ликвора уменьшается путем его замещения отечной тканью мозга. Соответственно при обеих причинах ВЧГ вентрикулярные датчики регистрируют подобные данные (повышение уровня ликворного давления), не отражая патофизиологических механизмов развития ВЧГ. В таком случае необходима нейровизуализация (компьютерная томография (КТ) головного мозга) для выявления истинной причины ВЧГ, что не всегда возможно в силу тяжести состояния больного.
Формирование острой гидроцефалии приводит к повышению ВЧД по данным вентрикулярного датчика, что требует выведения ликвора путем его сброса по дренажу (датчик и дренаж совмещены). Такой метод облегчает состояние больного и позволяет улучшить его неврологический статус.
Формирование изолированного отека головного мозга также сопровождается повышением ликворного давления в ответ на увеличение объема отечной мозговой ткани (объем ликвора уменьшается). В этом случае сброс ликвора по дренажу не позволяет в должной мере облегчить состояние больного, поскольку выведение ликвора из желудочковой системы не обеспечивает борьбу с отеком мозга, а является лишь компенсаторным механизмом борьбы с ВЧГ (отражается лишь значением ВЧД, механическое его снижение). Таким образом, в этом случае для проведения противоотечной терапии необходима нейровизуализация, которая позволит четко установит причину повышения ВЧД и выбрать адекватный метод борьбы с синдромом ВЧГ.
Из уровня техники также известны методики, позволяющие осуществить измерение ВЧД с помощью субдурального датчика (Lieberman D., Matz P., Rosgay H. History of the Strain Gauge in Measurement of the Intracranial Pressure: From Engineers to Physiologists and Clinicians, J. Trauma. 2002, 52:172-8).
Однако изолированное измерение ВЧД с помощью субдурального датчика у больных в остром периоде САК после разрыва АА с угрозой развития отека мозга и острой гидроцефалии при прорыве крови в желудочковую систему позволяют своевременно зарегистрировать ВЧГ, обусловленную только отеком мозгового вещества. При наличии изолированной гидроцефалии субдуральный датчик до определенного времени не позволяет зафиксировать повышение ВЧД. Данная ситуация обусловлена таким свойством мозга, как упругость. Т.е. накопление жидкости (ликвора) в желудочковой системе оказывает давление изнутри на мозговую ткань. Но упругоригидные свойства мозгового вещества не позволяют передать давление желудочковой системы на мозговое вещество и соответственно на субдуральное пространство (при условии, что ликворные пространства (желудочковая система и субдуральное) разобщены). В этом случае при ложно нормальном уровне давления, регистрируемого из субдурального пространства, тяжесть состояния больного определяется гидроцефалией, которую можно распознать с помощью нейровизуализации или же с помощью мониторинга, но отсрочено, когда ликворное давление достигнет того уровня, при котором будет преодолено сопротивление мозговой ткани и субдуральный датчик зафиксирует начальные стадии повышения ВЧД. Нормальный уровень ВЧД в данной ситуации ложно рассматривают как отсутствие ВЧГ.
При одновременном присутствии острой гидроцефалии и отека головного мозга незначительное повышение ВЧД (по данным субдурального датчика) сопровождается выраженным неврологическим дефицитом и резким снижением уровня бодрствования. Повышение ВЧД расценивают как формирование ВЧГ, обусловленной отеком головного мозга. Применение противоотечной терапии в данной ситуации позволяет воздействовать только на одно патофизиологическое звено ВЧГ и обеспечивает лишь частичное решение проблемы, в то время как гидроцефалия сохраняется и обуславливает сохранение тяжести состояния. Помогает в этом случае неировизуализация, которую не всегда возможно выполнить из-за тяжести состояния больного.
Достигаемый в предлагаемом способе технический результат заключается в следующем. Одновременная регистрация ВЧД из желудочковой системы головного мозга (ликворное давление) и субдурального пространства позволяет выявить превалирование одной из причин повышения ВЧД и соответственно связать с ней ухудшение неврологического статуса, и выбрать адекватный путь борьбы с синдромом ВЧГ.
Способ осуществляется следующим образом.
Выполняют установку 2-х датчиков измерения давления: один внедряют в субдуральное пространство на стороне поражения (локализация аневризмы), второй - в желудочковую систему (рог бокового желудочка). Далее проводят одновременную регистрацию ВЧД с помощью обоих датчиков в режиме реального времени. Длительность мониторинга ВЧД определяется временем сохранения ВЧГ и соответственно тяжестью состояния больного.
При наличии гидроцефалии ВЧД в субдуральном пространстве будет соответствовать норме (5-15 мм рт.ст.), а ВЧД в желудочковой системе будет нарастать согласно скорости накопления ликвора. Таким образом, превалирование ВЧД ликворного над ВЧД субдуральным (ВЧД ликворн. более ВЧД субдур.) свидетельствует о формировании ВЧГ за счет развития острой гидроцефалии.
При развитии отека головного мозга давление в субдуральном пространстве и в желудочковой системе повышается синхронно до того момента, пока ткань отечного мозга полностью не вытеснит ликвор из желудочковой системы и вентрикулярный датчик не зарегистрирует нулевое значение (0 мм рт.ст.). После того как ликвор полностью выдавливается из желудочков мозга (один из механизмов компенсации ВЧГ - перераспределение ликвора в ликворном пространстве), ликворное ВЧД соответствует 0 мм рт.ст., а субдуральное ВЧД продолжает нарастать. Таким образом, превалирование ВЧД субдурального над ВЧД ликворным (ВЧД субдур. более ВЧД ликворн.) в ходе мониторинга указывает на развитие отека головного мозга.
Таким образом, установка 2-х датчиков и последующее одновременное измерение ВЧД у больных в остром периоде САК после разрыва АА с угрозой развития отека мозга и формированием острой гидроцефалии является целесообразной, т.к. позволяет определить причину ВЧГ на ранних стадиях ее формирования, оценить скорость развития ВЧГ, своевременно выбрать адекватный способ борьбы с синдромом ВЧГ.
Полученные данные подтверждаются данными исследования больных, находящихся в остром периоде САК после разрыва АА.
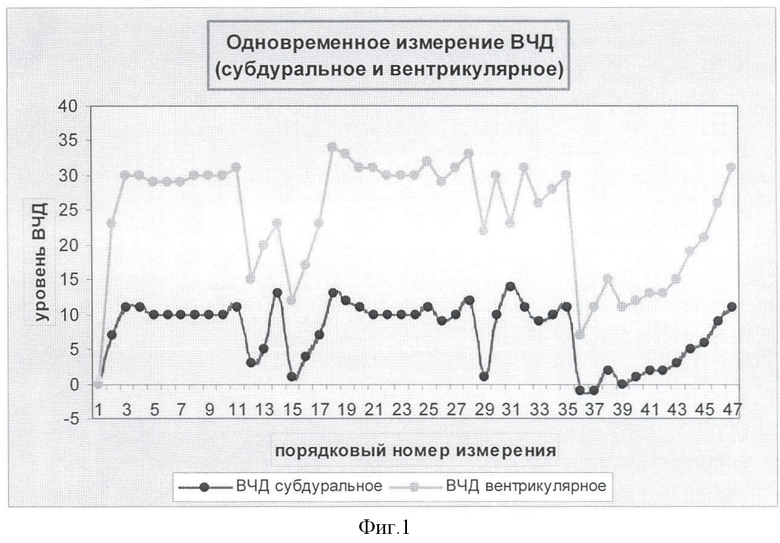
В таблице 1 и на фиг.1 представлены данные одновременного измерения ликворного и субдурального ВЧД у 1-го больного.
Больной перенес острое САК вследствие разрыва АА с прорывом крови в желудочковую систему, который послужил причиной острой гидроцефалии (установлен вентрикулярный датчик). Учитывая наличие крови в субарахноидальном пространстве, ожидалось формирование отека мозга (установлен субдуральный датчик). Зарегистрировано повышение ликворного давления до 22 мм рт.ст., которое сопровождалось угнетением сознания больного. Благодаря упругоэластическим свойствам мозговой ткани предотвращена передача давления на субдуральное пространство и одновременно исключен отек мозга.
В ходе измерения обоих давлений разница между субдуральным и вентрикулярным показателями достигла 3-14 мм рт.ст.
Таким образом, тяжесть состояния больного продиктована ВЧГ, связанной исключительно с острой гидроцефалией. Лечебные мероприятия направлены на купирование гидроцефалии: открывание дренажа, сброс ликвора до нормализации ВЧД.
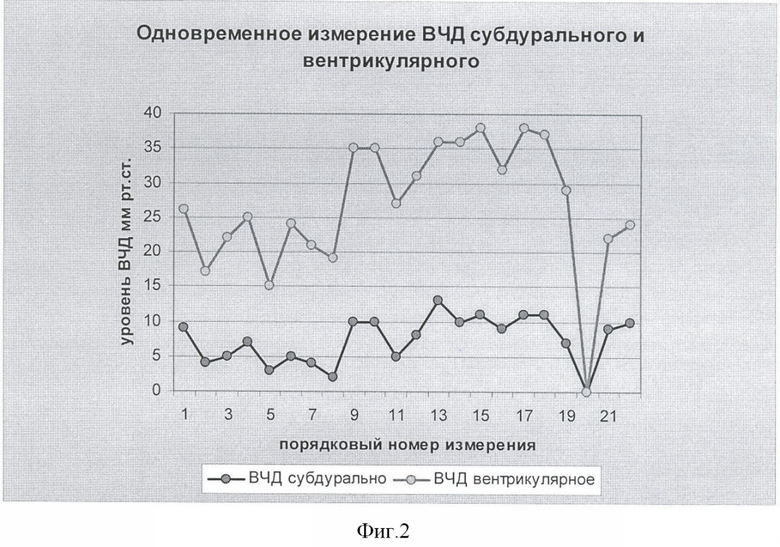
В таблице 2 и на фиг.2 представлены данные одновременного мониторинга ВЧД у 2-го больного с исходно диагностированной острой гидроцефалией после перенесенного САК вследствие разрыва АА и прорыва крови в желудочковую систему. Острая гидроцефалия при нарастании ВЧД сопровождалась снижением уровня бодрствования больного и потребовала открывания вентрикулярного дренажа и сброса ликвора вплоть до нормализации ликворного давления, что сопровождалось повышением неврологического уровня больного. В более позднем периоде у больного наблюдали отек головного мозга, зарегистрированный субдуральным датчиком.
Хронология изменения давлений (см. измерение №62-64): отмечено увеличение ликворного давления до 22 мм рт.ст.(сохраняющаяся гидроцефалия), выполнен сброс ликвора. После нормализации вентрикулярного давления (6 мм рт.ст.) дренаж перекрыт на измерение. С помощью субдурального датчика зафиксирован подъем субдурального давления до 20 мм рт.ст., обусловленного нарастанием отека мозга. Проведена массивная противоотечная терапия, которая позволила снизить уровень субдурального давления до 10 мм рт.ст. Учитывая наличие гидроцефалии, диагностировано постепенное увеличение ликворного давления до 20 мм рт.ст.
Разница измерений ВЧД ликворного и ВЧД субдурального за весь период регистрации составила 5-14 мм рт.ст.
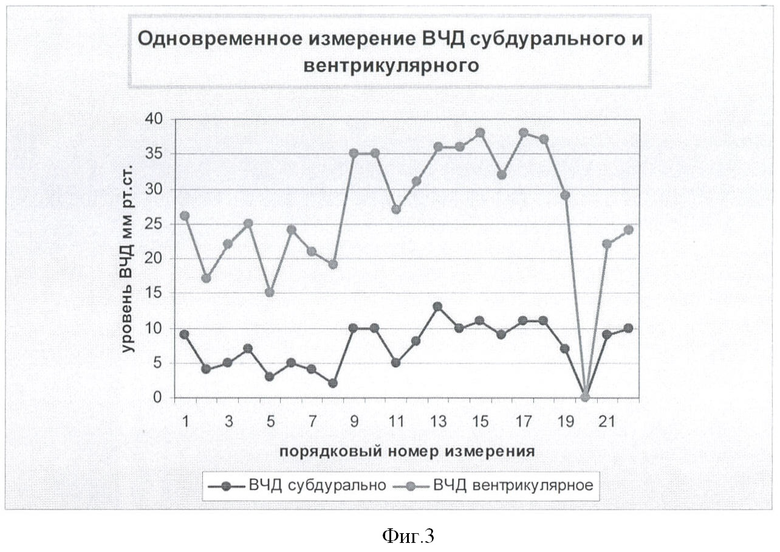
В таблице 3 и на фиг.3 представлены данные измерения субдурального и ликворного давлений у 3-го больного.
Исходно у больного присутствовала острая гидроцефалия, связанная с обструкцией путей ликворооттока после прорыва крови в желудочковую систему мозга вследствие разрыва АА. В ходе одновременного мониторинга ВЧД из желудочковой системы и субдурального пространства отмечена разница давлений в пределах 4-17 мм рт.ст. Тяжесть состояния больного после госпитализации в стационар обусловлена острой гидроцефалией, контролируемой с помощью вентрикулярного датчика и разрешаемой путем сброса ликвора по дренажу. Упругоэластические свойства мозговой ткани позволили сохранить субдуральное давление в пределах нормы (3-13 мм рт.ст.), несмотря на подъем ликворного давления до 27 мм рт.ст.
Таким образом, в данной ситуации измерение ВЧД с помощью одного субдурального датчика не позволило бы своевременно выявить причину ВЧГ - гидроцефалию, которую диагностировали и контролировали с помощью вентрикулярного датчика.
Таким образом, предлагаемый способ позволяет одновременно регистрировать повышение давления из субдурального пространства и желудочковой системы мозга у больных в остром периоде САК после разрыва АА с угрозой развития синдрома ВЧГ, обусловленного острой гидроцефалией или отеком головного мозга, а также в случае присутствия обоих осложнений.
Необходимость и целесообразность использования именно данного метода измерения давлений опирается на знания о разнице давлений в различных отделах интракраниальной полости и в ряде клинических случаев невозможности полной передачи давления из одного пространства на другое (разобщенность интракраниальной полости). Одновременная регистрация ликворного и субдурального ВЧД позволяет своевременно установить причину ВЧГ на основании подъема давления либо в желудочковой системе, либо в субдуральном пространстве.
Нарастание ликворного (вентрикулярного ВЧД) происходит за счет наличия гидроцефалии (нарушение оттока ликвора при его сохраненной продукции). Накопление ликвора в желудочковой системе головного мозга приводит к давлению на мозговую ткань изнутри. Исходно ликворное давление не достигает необходимого уровня, чтобы преодолеть упругоэластические свойства мозговой ткани и быть переданным на мозговое вещество, а соответственно и на субдуральный датчик, который лежит на поверхности головного мозга. Но в определенный момент времени, когда сила давления изнутри становится настолько высока, что преодолевает сопротивление мозгового вещества и оказывает воздействие на субдуральный датчик, повышение внутрижелудочкового давления сопровождается подъемом субдурального давления. Открывание вентрикулярного дренажа на несколько минут приводит к выбросу некоторого (индивидуального, согласно уровню ВЧД) объема ликвора, который оказывал воздействие, и сопровождается параллельным снижением ликворного и субдурального давлений.
По той же причине (упругоэластические свойства мозгового вещества), субдуральный датчик, установленный у таких больных, не позволяет на ранних стадиях диагностировать развитие гидроцефалии.
Разница между давлениями всегда неодинакова у разных пациентов и уровень ликворного давления, способный передаваться на субдуральный датчик за счет воздействия на мозговое вещество, соответственно также неодинаков. Это объясняется индивидуальными морфологическими свойствами мозгового вещества у каждого пациента: возрастной особенностью, наличием артериальной гипертензии и гипертонической энцефалопатией, перенесенным кровоизлиянием, присутствием отека мозга, ишемического поражения мозгового вещества, обширностью патологического процесса в мозге.
Поэтому у больных в остром периоде САК, обусловленном разрывом АА с угрозой развития ВЧГ на основании формирования отека мозга и/или острой гидроцефалией, для ранней диагностики причин ВЧГ показана установка 2-х датчиков (субдурального и вентрикулярного) для ранней диагностики причины ВЧГ и своевременного ее разрешения адекватными лечебными мероприятиями.
Изобретение относится к медицине, а именно к нейрохирургии. Устанавливают два датчика измерения давления: один внедряют в субдуральное пространство на стороне поражения, второй - в желудочковую систему головного мозга. Проводят одновременную регистрацию внутричерепного давления (ВЧД) с помощью обоих датчиков. При превалировании в процессе мониторинга давления субдурального ВЧД над ликворным ВЧД определяют наличие отека головного мозга; при превалировании в процессе мониторинга давления ликворного ВЧД над субдуральным ВЧД определяют формирование ВЧГ за счет развития острой гидроцефалии. Способ расширяет арсенал средств для определения причин внутричерепной гипертензии в остром периоде субарахноидального кровоизлияния после разрыва артериальных аневризм. 3 табл., 3 ил.
Способ определения причин внутричерепной гипертензии в остром периоде субарахноидального кровоизлияния (САК) после разрыва артериальных аневризм (АА), отличающийся тем, что выполняют установку двух датчиков измерения давления: один внедряют в субдуральное пространство на стороне поражения, второй - в желудочковую систему головного мозга, далее проводят одновременную регистрацию внутричерепного давления (ВЧД) с помощью обоих датчиков и при превалировании в процессе мониторинга давления - субдурального ВЧД над ликворным ВЧД определяют наличие отека головного мозга; при превалировании в процессе мониторинга давления - ликворного ВЧД над субдуральным ВЧД определяют формирование ВЧГ за счет развития острой гидроцефалии.
| Способ диагностики патологического состояния головного мозга | 1982 |
|
SU1351575A1 |
| US 2008033400 A1, 07.02.2008 | |||
| ГРИНЕНКО У.А | |||
| Ранняя диагностика внутричерепной гипертензии у больных в остром периоде субарахноидального кровоизлияния из аневризм сосудов головного мозга | |||
| Автореф | |||
| дисс | |||
| - М., 2007, с.11-20 | |||
| TSUNODA A | |||
| et al | |||
| Clinical experience with a dual switch valve (Miethke) for the management of adult hydrocephalus | |||
| Neurol Med Chir (Tokyo), 2007 Sep; 47 (9)^403-408. | |||
Авторы
Даты
2009-11-10—Публикация
2008-08-08—Подача