Настоящее изобретение относится к области медицины и ветеринарии, преимущественно к хирургии, и может быть использовано для разрушения биотканей различных органов, пораженных патологическим процессом.
В последние годы широко используются способы и устройства термокоагуляции биоткани (см., например, Kelvin Kwok-Chai Ng et al. Thermal ablative therapy for malignant liver tumors: A critical appraisal. J.Gastroenterology and Hepatology. 2003, 18, 616-629) за счет тепла, выделяемого при поглощении биотканью энергии электромагнитного поля широкого диапазона частот от оптического до радиоволнового. Общим недостатком этих способов является сравнительно небольшая глубина прогрева биоткани. Основными причинами ограничения объема нагрева биоткани являются поглощение энергии электромагнитного поля вблизи от излучателя или электрода, плохая теплопроводность и электропроводность биоткани, препятствующая распространению в ней тепла и электрического тока, а также высушивание слоя биоткани непосредственно контактирующего с поверхностью излучателя или электрода, которое еще больше усугубляет ситуацию.
Для преодоления этих недостатков был предложен виртуальный электрод для высокочастотного разрушения биотканей, состоящий из полой металлической иглы с отверстиями, окруженной слоем биосовместимой токопроводящей жидкости низкой вязкости типа водных растворов электролитов, контактирующей с наружной поверхностью иглы (Патенты США 6409722, 6736810, 6849073, 7169144, 7247155). Токопроводящая жидкость, вводимая через отверстия иглы в биоткань до начала процесса высокочастотного нагрева и в процессе нагрева, уменьшает электрическое сопротивление биоткани, прилегающей к электроду, что позволяет использовать большие токи без перегрева слоев, непосредственно примыкающих к поверхности электрода. Это равнозначно по эффекту увеличению геометрических размеров электрода, чем и объясняется его название. Кроме того, постоянное смачивание поверхности препятствует высушиванию биоткани, что позволяет поддерживать электропроводность и теплопроводность биоткани на относительно высоком уровне. В конечном счете, все это приводит к увеличению объема разрушенной биоткани. Однако использование данного устройства связано с существенным недостатком - неопределенностью в распределении токопроводящей жидкости по объему разрушаемой биоткани, что связано в первую очередь с гетрогенностью структуры биоткани. В то же время, происходят нежелательные утечки вводимой жидкости по разрушенным при введении электрода сосудам и протокам, а также по зазору между поверхностью электрода и биотканью, что приводит к незапланированному разрушению здоровой биоткани, а также к увеличению вероятности рассева злокачественных клеток в случае разрушения раковых опухолей.
Наиболее близким к предлагаемому является виртуальный электрод для высокочастотного разрушения биотканей, состоящий из полой металлической иглы с отверстиями, окруженной слоем биосовместимого токопроводящего геля (Заявка США 20040215181). Такая конструкция во многом устраняет недостатки вышеописанного электрода и благодаря более правильной сферической или элиптической конфигурации вводимого в биоткань электропроводящего геля позволяет более точно планировать и осуществлять разрушение. Однако это устройство дает возможность использовать только сравнительно небольшие токи из-за значительно возрастающего сопротивления на поверхности иглы при нагреве, что существенно ограничивает объем разрушения биоткани.
Задачей предлагаемого устройства является увеличение объема разрушаемой биоткани.
Для этого в известном виртуальном электроде для высокочастотного разрушения биотканей, состоящем из полой металлической иглы с отверстиями, окруженной слоем биосовместимого токопроводящего геля, между поверхностью иглы и гелем имеется прослойка из токопроводящей жидкости низкой вязкости, например водного электролита.
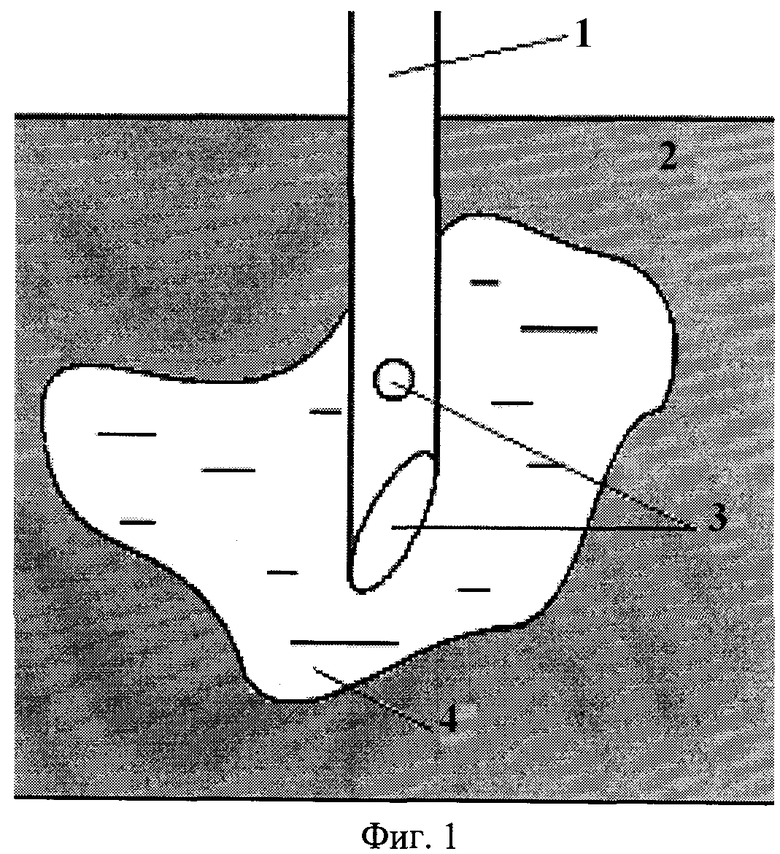
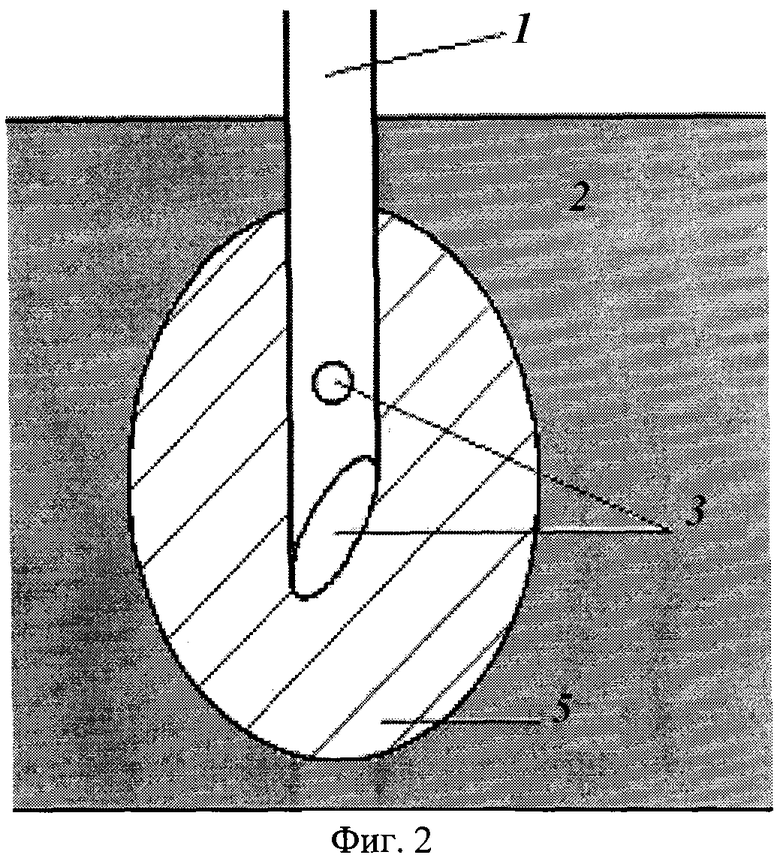
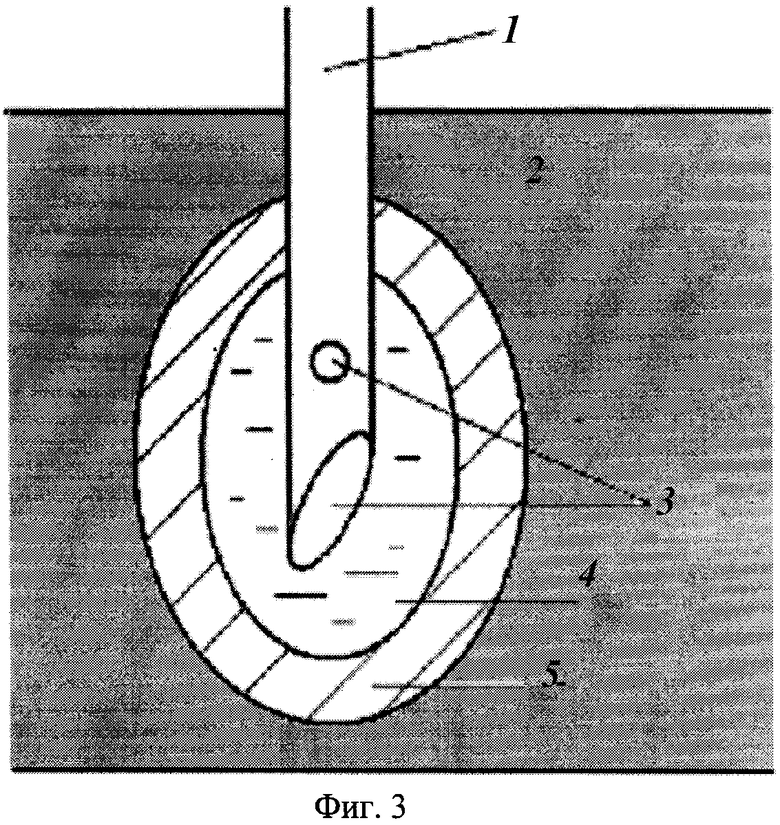
На фиг.1 схематически показан виртуальный электрод по Патентам США. Он состоит из полой металлической иглы 1, введенной в биоткань 2. В торце и боковой стенке иглы имеются отверстия 3 для введения токопроводящей жидкости низкой вязкости 4. На фиг.2 схематически показан виртуальный электрод по Заявке США. Он также состоит из полой металлической иглы 1, введенной в биоткань 2. В торце и боковой стенке иглы имеются отверстия 3 для введения токопроводящего геля 5. На фиг.3 схематически показан предлагаемый виртуальный электрод, который также состоит из полой металлической иглы 1, введенной в биоткань 2. В торце и боковой стенке иглы имеются отверстия 3 для введения токопроводящего геля 5. Между поверхностью иглы и гелем имеется прослойка 4 из токопроводящей жидкости низкой вязкости, например водного электролита. Проведенные эксперименты показали, что введение в конструкцию электрода такой прослойки значительно увеличивает величину тока, используемого для нагрева биоткани, что в конечном счете приводит к существенному увеличению объема разрушения. По-видимому, прослойка из токопроводящей жидкости низкой вязкости усиливает теплоотвод с поверхности иглы за счет увеличения конвекции жидкости. Это предотвращает повышение сопротивления на поверхности иглы, которое имеет место в случае контакта с токопроводящим гелем.
Известен способ изготовления и применения виртуального электрода для высокочастотного разрушения биотканей, включающий введение в биоткань полой металлической иглы с отверстиями, инъекцию в биоткань токопроводящей жидкости низкой вязкости типа водных электролитов с последующим высокочастотным нагревом биоткани (Патенты США 6409722, 6736810, 6849073, 7169144, 7247155). Способ дает возможность разрушать сферические объемы биоткани диаметром до 4 см. Однако использование данного способа связано с существенным недостатком - неопределенностью в распределении токопроводящей жидкости по объему разрушаемой биоткани, что связано с гетерогенностью структуры биоткани. В то же время, происходят нежелательные утечки вводимой жидкости по разрушенным при введении электрода сосудам и протокам, а также по зазору между поверхностью электрода и биотканью, что приводит к незапланированному разрушению здоровой биоткани, а также к увеличению вероятности рассева злокачественных клеток в случае разрушения раковых опухолей.
Наиболее близким к предлагаемому является способ изготовления и применения виртуального электрода для высокочастотного разрушения биотканей, включающий введение в биоткань полой металлической иглы с отверстиями, инъекцию в биоткань токопроводящего геля с последующим высокочастотным нагревом биоткани (Заявка США 20040215181). Способ дает возможность разрушать биоткани благодаря более правильной сферической или элиптической конфигурации вводимого в биоткань электропроводящего объема, что позволяет более точно планировать и осуществлять разрушение. Однако этот способ дает возможность использовать только сравнительно небольшие токи из-за значительно возрастающего сопротивления на поверхности иглы при нагреве, что существенно ограничивает объем разрушения биоткани. Для полного разрушения большего объема биоткани процедуру приходится повторять, что приводит к увеличению травматичности и трудоемкости способа.
Задачей настоящего изобретения является уменьшение травматичности и трудоемкости способа за счет увеличения объема разрушаемой биоткани за одну процедуру.
Для этого в известном способе изготовления и применения виртуального электрода для высокочастотного разрушения биотканей, включающем введение в биоткань полой металлической иглы с отверстиями, инъекцию в биоткань токопроводящего геля с последующим высокочастотным нагревом биоткани, после введения в биоткань токопроводящего геля осуществляют инфузию в биоткань токопроводящей жидкости низкой вязкости в объеме 0,5-1,0 от объема введенного геля, а высокочастотный нагрев биоткани осуществляют с одновременным введением токопроводящей жидкости низкой вязкости.
Техническим результатом выполнения вышеуказанных новых условий и режимов изготовления и применения виртуального электрода для высокочастотного разрушения биотканей является увеличение эффективности передачи тепла в биоткань, а также уменьшение травматичности и трудоемкости известного способа за счет увеличения объема разрушенной биоткани за одну процедуру.
Способ осуществляют следующим образом. В разрушаемую биоткань под контролем ультразвукового сканера вводят иглу с отверстиями. Через иглу в биоткань вводят токопроводящий гель. После введения в биоткань токопроводящего геля осуществляют инфузию в биоткань токопроводящей жидкости низкой вязкости в объеме 0,5-1,0 от объема введенного геля. Подключают нейтральный электрод и иглу к генератору высокочастотного тока и проводят нагрев с одновременным введением токопроводящей жидкости низкой вязкости.
Испытания предлагаемого устройства и способа его изготовления и применения были проведены на печени собаки. Под общим наркозом животное фиксировали на операционном столе и с помощью ультразвукового сканера вводили иглу в различные доли печени. В качестве токопроводящего геля использовали 25% раствор отечественного триблоксополимера полиэтиленоксида и полипропиленоксида ЭМУКСОЛ, растворенного в 20% водном растворе хлорида натрия, вязкостью 1500·10-2 пуаза, при 20°С. Последний использовали в качестве токопроводящей жидкости низкой вязкости. В первом варианте опыта, соответствующем прототипу, в ткань печени вводили 5 мл раствора ЭМУКСОЛА и затем осуществляли высокочастотный нагрев ткани в течение 10 минут. Во втором варианте, после введения 5 мл раствора ЭМУКСОЛА, вводили 3 мл 20% раствора хлорида натрия вязкостью 1,7·10-2 пуаза, а затем осуществляли высокочастотный нагрев ткани в течение 10 минут с одновременной инфузией этого раствора со скоростью 0,5 мл/мин. Нагрев растворов до 80-90°С приводит к 3-кратному снижению вязкости раствора хлорида натрия и многократному увеличению вязкости раствора ЭМУКСОЛА с формированием структуры геля. Для инфузии использовали стерильные растворы. В течение эксперимента регистрировали изменения сопротивления между двумя электродами - активным (игла) и нейтральным. Мощность генератора фиксировали на уровне, обеспечивающем прирост сопротивления не более 20% от исходной величины. Испытания показали, что мощность генератора в первом варианте опыта, оказалась почти в 2 раза меньше, чем во втором варианте. Измерения диаметра коагулированного участка ткани печени, имеющей сферическую конфигурацию, проводили по ультразвуковой эхограмме. Объем коагулированной биоткани, рассчитанный на основе измеренного диаметра коагулированного участка ткани печени во втором варианте опыта, оказался почти на 50% больше, чем в первом. Через три дня после проведения процедуры животное по основным жизненным показателям вернулось к норме, что свидетельствует о безопасности обоих способов.
Таким образом, использование предлагаемого устройства и способа его изготовления и применения уменьшает травматичность и трудоемкость, по сравнению с использованием известного устройства и способа его применения, за счет увеличения объема коагуляции за одну процедуру.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РАЗРУШЕНИЯ БИОТКАНИ | 2007 |
|
RU2354420C1 |
| СПОСОБ ТЕРМОКОАГУЛЯЦИИ БИОТКАНИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2316283C1 |
| СПОСОБ ВЫСОКОТЕМПЕРАТУРНОГО РАЗРУШЕНИЯ БИОТКАНИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2317793C1 |
| СПОСОБ МИКРОВОЛНОВОЙ ДИАТЕРМОКОАГУЛЯЦИИ БИОТКАНИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2318465C1 |
| Внутритканевый СВЧ-излучатель и способ его изготовления | 1987 |
|
SU1535533A1 |
| Термоиндикаторный состав | 1985 |
|
SU1326910A1 |
| БИОАРМИРОВАНИЕ АТРОФИЧЕСКОЙ КОЖИ ТОКАМИ РАДИОЧАСТОТНОГО ДИАПАЗОНА | 2008 |
|
RU2372872C1 |
| КОМПЛЕКС ДЛЯ ВЫСОКОТЕМПЕРАТУРНОГО ВОЗДЕЙСТВИЯ НА БИОЛОГИЧЕСКУЮ ТКАНЬ (варианты) | 2016 |
|
RU2636877C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ ПУТЕМ РЕГИОНАЛЬНОЙ ГИПЕРТЕРМИИ БРЮШНОЙ ПОЛОСТИ | 2005 |
|
RU2288752C2 |
| Термоиндикаторный состав для оценки распределения температуры в объеме | 1987 |
|
SU1566230A1 |
Изобретения относятся к области медицины и ветеринарии, преимущественно к хирургии, и могут быть использованы для разрушения биотканей различных органов, пораженных патологическим процессом. Виртуальный электрод для высокочастотного разрушения биотканей состоит из полой металлической иглы с отверстиями, окруженной слоем биосовместимого токопроводящего геля. Между поверхностью иглы и гелем имеется прослойка из токопроводящей жидкости низкой вязкости. Способ высокочастотного разрушения биоткани с помощью электрода включает введение в биоткань полой металлической иглы с отверстиями, инъекцию в биоткань токопроводящего геля с последующим высокочастотным нагревом биоткани. После введения в биоткань токопроводящего геля осуществляют инфузию в биоткань токопроводящей жидкости низкой вязкости в объеме 0,5-1,0 от объема введенного геля, а высокочастотный нагрев биоткани осуществляют с одновременным введением токопроводящей жидкости низкой вязкости. Использование изобретений уменьшает травматичность и трудоемкость процедуры разрушения биотканей за счет увеличения объема коагуляции за один сеанс. 2 н.п. ф-лы, 3 ил.
1. Виртуальный электрод для высокочастотного разрушения биотканей, состоящий из полой металлической иглы с отверстиями, окруженной слоем биосовместимого токопроводящего геля, отличающийся тем, что между поверхностью иглы и гелем имеется прослойка из токопроводящей жидкости низкой вязкости.
2. Способ высокочастотного разрушения биоткани с помощью виртуального электрода, включающий введение в биоткань полой металлической иглы с отверстиями, инъекцию в биоткань токопроводящего геля с последующим высокочастотным нагревом биоткани, отличающийся тем, что после введения в биоткань токопроводящего геля осуществляют инфузию в биоткань токопроводящей жидкости низкой вязкости в объеме 0,5-1,0 от объема введенного геля, а высокочастотный нагрев биоткани осуществляют с одновременным введением токопроводящей жидкости низкой вязкости.
| US 2008281321 A1, 13.11.2008 | |||
| US 5622168 A, 22.04.1997 | |||
| US 2008071265 A1, 20.03.2008 | |||
| Приспособление к швейным машинам для получения спиральной строчки, например, при прошивании полировальных кругов из ткани | 1940 |
|
SU58905A1 |
| RU 2006113533 A, 20.11.2007 | |||
| СПОСОБ ВЫСОКОТЕМПЕРАТУРНОГО РАЗРУШЕНИЯ БИОТКАНИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2317793C1 |
| DEQUESNE J.H | |||
| Thermoregulated radiofrequency endometrial ablation | |||
| // Int J Fertil Womens Med | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| Устройство для усиления микрофонного тока с применением самоиндукции | 1920 |
|
SU42A1 |
| Способ приготовления массы для карандашей | 1921 |
|
SU311A1 |
Авторы
Даты
2010-09-27—Публикация
2008-12-19—Подача