Настоящее изобретение относится к области техники диагностической визуализации. Обнаружено конкретное применение гибридных систем позитронно-эмиссионной томографии и магнитного резонанса (PET-MR) и будет описано с конкретной ссылкой на него. Однако следует понимать, что настоящее изобретение используется и для других гибридных систем, но не ограничено гибридными системами. Скорее его можно использовать при последовательном сканировании посредством PET и MR на автономных или коаксиальных сканерах, или в других системах, и оно не ограничено вышеупомянутым применением.
Как PET, так и MRI страдают от присущих им ограничений. Динамическая томография PET (dPET) обеспечивает прямое обнаружение концентрации контрастного вещества функциональной и метаболической информацией с высоким разрешением по времени, в сочетании с высокой чувствительностью способа прослеживания радиоактивным индикатором согласно PET. Одним из недостатков способа является то, что он часто страдает от низкой количественной точности физиологических, функциональных и морфологических параметров опухолей, и т.д. В отличие от dPET измеренный сигнал, обнаруживаемый динамической контрастной магнитно-резонансной томографией (DCE MRI), зависит от последовательностей импульсов, используемых для обнаружения, то есть при скоростях релаксации T1 и T2. Это не всегда может быть линейная зависимость от концентрации контрастного вещества. Концентрация контрастного вещества не является непосредственно наблюдаемым экспериментом, и обычно для большинства случаев ее получают численно. Дополнительно, разрешение по времени обычно ограничено несколькими секундами, что может быть недостаточно для некоторых процессов быстрой релаксации. Магнитный резонанс обладает относительно высоким пространственным разрешением, а PET обладает относительно высоким разрешением по времени. В результате, системы PET и MR используются в сочетании друг с другом, в качестве двух способов воздействия, которые дополняют друг друга.
Поскольку в двух способах воздействия использованы существенно различающиеся способы формирования изображения, для получения изображения или для способствования получению изображения использованы различные механизмы. В позитронно-эмиссионной томографии реальное вещество, которое отображается, выбирается из ткани, представляющей интерес, и отображается, пока оно в ней присутствует. При магниторезонансной томографии ткань возбуждают и отображают непосредственно, тогда как контрастные вещества можно использовать для облегчения различения ткани, представляющей интерес, и окружающей кровеносной системы. Как правило, магниторезонансное контрастное вещество не поглощается тканью, представляющей интерес, а скорее свободно течет в кровотоке, до его окончательного отфильтровывания. При комбинированных исследованиях PET/MR обычно как MR-контрастное вещество, так и PET-радиофармпрепарат вводят до сканирования, причем они оба тяжело переносятся почками и печенью пациента.
В некоторых применениях, таких как применение, при котором отображаются раковые опухоли или артериальные бляшки, кровь легко достигает области, представляющей интерес. С ростом опухоли создаются новые кровеносные сосуды, адаптированные к этому росту. В таких ситуациях магниторезонансные контрастные вещества можно использовать для подсвечивания ткани, представляющей интерес, вместо того чтобы отличать представляющую интерес ткань от окружающей кровеносной системы. Однако для этого оно должно осесть и закрепиться на ткани, представляющей интерес, таким образом, чтобы это способствовало формированию изображения.
Для сбора информации об отобранной ткани часто используют биопсию. Ее можно использовать для сбора информации о микрососудистой биологии, но они могут обеспечивать лишь неполное отображение такой кровеносной системы. Биопсия иногда бывает подвержена ошибке, связанной с выборочным обследованием, а в случае раковых тканей возникает риск стимуляции метастатический активности.
Настоящее изобретение обеспечивает новое и усовершенствованное контрастное вещество и радиофармпрепарат, а также способ и устройство для их использования, который преодолевает вышеописанные проблемы и другие.
В соответствии с одной особенностью обеспечено контрастное вещество. Контрастное вещество включает в себя первый компонент, который пригоден для отображения устройством для магниторезонансной томографии. Второй компонент контрастного вещества включает в себя радиофармпрепарат, который пригоден для отображения устройством для радионуклидной визуализации. Контрастное вещество также включает в себя систему нацеливания, которая пользуется биологическими процессами, заставляя контрастное вещество накапливаться в целевой области.
В соответствии с другим аспектом, обеспечен способ диагностической визуализации. В объект вводят контрастное вещество, пригодное для отображения, как путем магниторезонансной томографии, так и путем позитронно-эмисионной томографии. Магнитный резонанс возбуждают в выбранных диполях объекта и контрастного вещества. Обнаруживают магнитный резонанс. Радиоактивное излучение, указывающее на события радиоактивного распада контрастного вещества, обнаруживают с помощью детекторной матрицы. В представлении изображения объекта реконструируют, по меньшей мере, одно из обнаруженного магнитного резонанса и радиоактивного излучения. Представление изображения выводят на дисплей.
Одно преимущество связано с повышенным общим отношением сигнал/шум.
Другое преимущество связано с симбиотическим сочетанием кинетических параметров, полученных вследствие высокого разрешения по времени, с анатомическими и морфологическими данными, с трехмерным пространственным разрешением.
Другое преимущество связано с улучшением визуализации кровеносной системы с временными данными.
Другое преимущество связано с расширенной кинетической и функциональной обработкой комбинированных PET-MR данных компьютерной программой и средствами моделирования.
Другое преимущество связано с улучшенным подбором друг к другу 4-мерных изображений PET и MR, с использованием динамического PET для получения точных данных, в зависимости от времени.
Другое преимущество связано с применением для ангиогенеза и кардиологии.
Другое преимущество состоит в том, что устраняется необходимость в делении пополам доз контрастного вещества, вводимого объекту для комбинированной PET/MR-томографии.
Другое преимущество связано с ранним обнаружением рака и мониторингом лечения.
Другое преимущество связано с непроникающим диагнозом реваскуляризацией.
Другое преимущество связано с повышенной биосовместимостью контрастного вещества с пациентом.
Дополнительные преимущества настоящего изобретения должны быть понятны обычным специалистам в данной области техники при прочтении ими и разборе следующего подробного описания.
Изобретение также может принимать форму различных компонентов и расположений компонентов, и различных этапов и последовательностей этапов. Чертежи приведены лишь в целях иллюстрации предпочтительных вариантов воплощения, и их не следует рассматривать в качестве ограничений изобретения.
Фиг.1 представляет собой схематическое изображение комбинированного PET/MR сканера в соответствии с настоящим изобретением.
Фиг.2 представляет собой один вариант воплощения контрастного вещества для комбинированного способа PET/MR.
Фиг.3 представляет собой другой вариант воплощения контрастного вещества для комбинированного способа PET/MR.
Фиг.4 представляет собой другой вариант воплощения контрастного вещества для комбинированного способа PET/MR.
Фиг.5 представляет собой блок-схему, отображающую получение соответствующих изображений для PET/MR.
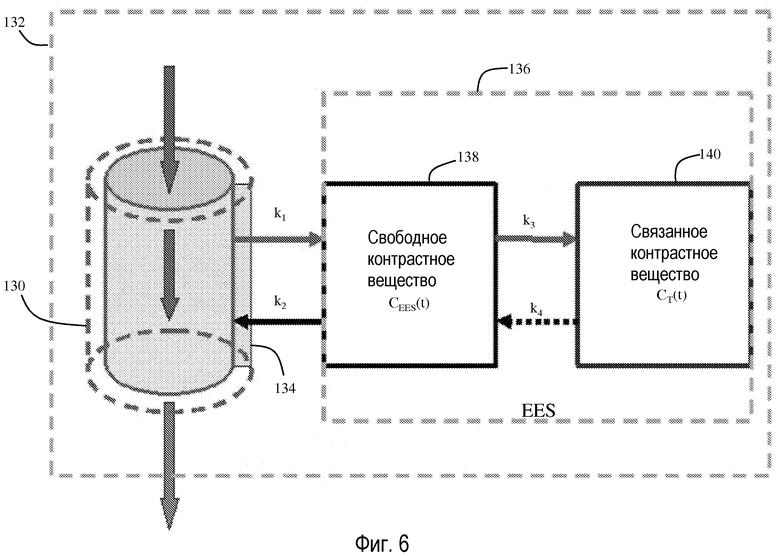
Фиг.6 показывает режимы кровотока в области, представляющей интерес.
Настоящее изобретение можно использовать при исследованиях кардиологии, например, в исследованиях ангиографии, ишемии и миокарда или диагноза уязвимых бляшек. Также найдено применение в онкологии для количественного определения ангиогенеза. Ангиогенез представляет собой процесс роста новых кровеносных сосудов, который возникает в различных физиологических состояниях. Опухоли обладают способностью к стимулированию роста эндотелиальных клеток, и, таким образом, ангиогенез становится ключевым путем для роста опухоли, инвазии окружающих здоровых тканей и метастатической активности. Поскольку твердые опухоли требуют доступа к кровотоку для метастазирования вторичных участков по всему телу, кровеносные сосуды опухоли являются важным параметром и целью терапии рака.
Фактор эндотелиального роста сосудов играет важную роль при стимулировании ангиогенеза. Для роста опухоли, выходящей за пределы размера примерно 2 мм3, требуется построение реоваскулярной сети. Существует точная корреляция между ангиогенным ростом и прогнозом роста опухолей, таких как рак молочной железы, рак предстательной железы и раковых опухолей прямой кишки. Опухоли хорошо реагируют на ангиогенные ингибиторы, которые поражают метаболические пути, способствующие фактору эндотелиального роста кровеносных сосудов. Настоящее изобретение способствует осмыслению молекулярных путей метаболизма, лежащих в основе ангиогенеза, и идентификации подходящих медикаментов для лечения.
Лечение часто включает в себя разрушение существующей кровеносной сети вокруг опухоли и предотвращение образования новых кровеносных сосудов. То есть как антиваскулярные, так и антиангиогенные вещества обладают ценностью при лечении опухолей. Ингибирование ангиогенезиса является одной из многообещающих стратегий, которые могут оказывать содействие при терапии рака. Описанное в настоящее время обнаружение несколькими способами способствует ранней диагностики, мониторингу терапии и следованию такой терапии.
Со ссылкой на фиг.1 описан вариант воплощения комбинированной или гибридной системы 10 получения данных магнитно-резонансной (MR) и позитронно-эмиссионной томографии PET, которая генерирует по существу совмещенные изображения PET и MR. Следует понимать, что комплексная система является идеальной для изображений, совмещенных по времени и по пространству; также предполагается, что изображения, полученные с различных сканеров, расположенных удаленно или перемещенных пространственно, могут быть приемлемыми аналогичным образом. Проиллюстрированный сканер 10 представляет собой интегрированную систему, но также равно возможны и другие расположения сканеров, такие как параллельные системы, встроенные системы, коаксиальные системы и т.п. Показанный магниторезонансный сканер включает в себя кольцевой магнит 12, включающий в себя множество проводящих катушечных обмоток (схематически изображенных на фиг.1 в виде прямоугольников с пересекающимися линиями), которые генерируют статическое магнитное поле B0 в области 14 формирования изображения. Магнит 12 может быть сверхпроводящим или резистивным по природе; в предыдущем случае магнит 12 обычно расположен в криогенном сосуде Дьюара или в другой системе охлаждения (не показанной). Проиллюстрированный магнит 12 представляет собой соленоидальный магнит, обладающий относительно горизонтальным полем B0, проходящим через области 14 формирования изображения. Хотя полярность поля B0 показана справа налево, также возможна и противоположная полярность. В других вариантах воплощения магнит 12 может иметь C-образную или другую конфигурацию, предназначенную для получения вертикального или иначе ориентированного статического магнитного поля.
Магниторезонансное сканирующее устройство также включает в себя блок градиента магнитного поля, который в иллюстративном варианте воплощения согласно фиг.1 включает в себя градиентные катушечные обмотки 16, которые совместно накладывают градиенты магнитного поля на статическое магнитное поле B0, отвечающее за селективное энергоснабжение выбранных градиентных катушечных обмоток 16. При желании катушка для градиентного магнитного поля, магнит или они оба могут включать в себя и другие признаки (не показанные) для формирования, стабилизации и динамической регулировки магнитного поля, например, пассивные ферромагнитные шиммы, активные шиммирующие обмотки и т.п. Магниторезонансный сканер дополнительно включает в себя радиочастотную систему возбуждения и приема. Радиочастотная система включает в себя, по меньшей мере, один компонент, такой как проиллюстрированная радиочастотная катушка 18, предназначенная для всего тела, на которую можно подавать ток на подходящей радиочастоте для возбуждения магнитного резонанса в объекте, расположенном в области 14 формирования изображения. Катушка 18 также может функционировать как радиочастотный приемник, принимающий или обнаруживающий магнитный резонанс, возникающий в области 14 формирования изображения после возбуждения радиочастоты. В некоторых вариантах воплощения различные катушки используют для операций возбуждения и приема. Например, встроенную катушку 18 можно использовать для возбуждения магнитного резонанса, а другую локальную катушку или выделенную приемную катушку (не показана) можно размещать выше, на или близко к объекту в области 14 формирования изображения, для обнаружения магнитного резонанса. Радиочастотную систему в одном варианте воплощения настраивают на резонансную частоту 1H, а в другом варианте воплощения настраивают на резонансную частоту 19F. Радиочастотная система может иметь двойную настройку для параллельной или последовательной 1H- и 19F-визуализации. Ее рассматривают для одного и того же магниторезонансного сканера, который был сконфигурирован различными способами, с использованием различных комбинаций встроенных катушек, локальных катушек или тех и других.
Градиентный блок и радиочастотная система работают вместе, вызывая магнитный резонанс с последовательностью формирования изображений, такой как одна из: быстрой последовательности формирования изображений, например, последовательности градиентных эхосигналов, быстрых спиновых эхосигналов и т.д. Более быстрые системы формирования изображения максимизируют магниторезонансное разрешение по времени. Полученные выборки магнитного резонанса сохраняют в запоминающем устройстве 20 для выборок магнитного резонанса. Процессор 22 реконструкции магнитного резонанса применяет подходящий алгоритм реконструкции для реконструкции выборок магнитного резонанса для формирования реконструированного изображения или ряда возрастающих во времени изображений, которые сохраняются в памяти для магниторезонансных изображений или в буфере 24. Процессор 22 реконструкции применяет алгоритм реконструкции, который согласуется с выбранным пространственным кодированием, используемым при генерировании магниторезонансных данных. Например, для реконструкции магниторезонансных данных, закодированных в декартовой системе координат, может быть пригоден алгоритм реконструкции согласно преобразованию Фурье. Часть реконструкции магниторезонансных сигналов (не обязательно) может быть выполнена последовательно, до сохранения данных и завершения реконструкции.
Продолжим рассмотрение фиг.1, где проиллюстрированная комбинированная или гибридная система получения данных магнитно-резонансной (MR) и позитронно-эмиссионной томографии PET 10 дополнительно включает в себя детекторы излучения для осуществления приема данных PET. В иллюстративном примере согласно фиг.1 кольцевая матрица детекторов 30 излучения окружает канал гибридной системы. Проиллюстрированная матрица 30 включает в себя слой сцинтиллятора и слой фотонных детекторов на основе электронного умножителя, однако здесь рассматриваются и другие конфигурации детектора, такие как планарные детекторные матрицы, расположенные вблизи области 14 формирования изображения. Также рассматриваются и твердотельные детекторы излучения и твердотельные оптические детекторы. Матрица 30 детектора излучения 30 спроектирована для обнаружения гамма-лучей 511 кэВ, которые испускаются во время событий аннигиляции позитронно-электронной пары. При приеме данных PET предполагается, что два практически одновременных события обнаружения гамма-излучения 511 кэВ возникают из того же события аннигиляции позитронно-электронной пары, которое происходит где-то на «линии отклика» (LOR) соединяющей два практически одновременных события обнаружения гамма-излучения 511 кэВ. Эту линию отклика также иногда называют проекцией или лучом, а собранные данные PET называют проекционными данными.
При стандартной PET практически одновременные события обнаружения гамма-излучения 511 кэВ заданы как два события обнаружения гамма-излучения 511 кэВ, возникающие в выбранном кратковременном интервале, например, с интервалом в четыре наносекунды между ними. Какая бы аннигиляция позитрона в центре поля обзора (FOV) ни происходила, она будет обладать небольшой разностью во времени прихода сигнала на противоположных детекторных элементах, пропорциональной разности во времени прохождения сигнала для гамма-лучей, - примерно четыре наносекунды на краях поля обзора. Соответствующая технология, называемая технологией времени пролета частицы при позитронно-эмиссионной томографии (time of flight PET или TOF-PET), обладает преимуществом в том, что эта маленькая разность во времени дополнительно локализует событие позитронно-электронной аннигиляции на протяжении LOR с точностью до субнаносекунды.
Матрицу 30 детекторов излучения гибридной системы 10 используют для приема данных PET или TOF-PET. События обнаружения гамма-излучения обрабатываются блоком 32 оцифровки данных PET, который выполняет аналого-цифровое преобразование времени (TDC) и преобразование из аналоговой формы в цифровую (ADC) событий обнаружения, и блоком 34 обработки сигналов, который выполняет кластеризацию, вычисление величины энергии, фиксирование отметок времени и позиционирование. Блок 34 обработки сигналов отфильтровывает (не обязательно) сигналы обнаружения, которые находятся за пределами выбранного канала регистрации излучения для ожидаемой энергии гамма-излучения 511 кэВ. В некоторых вариантах воплощения детекторы излучения являются пикселизированными. В других вариантах воплощения кластеризацию применяют в виде алгоритма поблочного считывания, такого как логика Анже и т.п., для обеспечения дополнительного уточнения пространственной локализации событий обнаружения гамма-излучения, задающих проекцию. Процессор 36 обнаружения совпадения использует временное кадрирование для идентификации событий обнаружения гамма-излучения, которые произошли практически одновременно и, таким образом, соответствуют событию общей аннигиляции пары позитрон-электрон и, таким образом, задают проецирование или линию отклика.
Для обработки TOF разность во времени между идентифицированными практически одновременными или совпадающими событиями обнаружения используют для пространственной оценки события аннигиляции позитронно-электронной пары вдоль линии отклика.
Результирующие данные PET или TOF-PET хранятся в запоминающем устройстве 38 для данных PET. Следует понимать, что данные PET можно сохранять до или после определения совпадения. Процессор 40 реконструкции PET обрабатывает LOR или данные по локализованному проецированию, с использованием подходящего алгоритма реконструкции для генерирования последовательности возрастающих во времени сигналов изображения, которые сохраняются в запоминающем устройстве для изображений PET или в буфере 42. В одном варианте воплощения данные PET сохраняют в режиме списка, т.е. каждую LOR сохраняют с разметкой по времени. Это облегчает регулировку окна (окон) времени по данным таким образом, чтобы каждое реконструированное изображение попадало в выбранное и отрегулированное окно времени.
Прием данных MR и PET осуществляют (не обязательно) одновременно. Это способствует максимальному пространственному разрешению магниторезонансного сканирования, улучшаемому за счет максимального разрешения по времени позитронно-эмиссионного сканирования, путем создания четырехмерного представления, которое более полное, чем представление, которое каждый способ воздействия может продуцировать сам на себя. В качестве альтернативы или дополнительно прием данных магниторезонансной и позитронно-эмиссионной томографии можно осуществлять последовательно (например, сначала MR, затем PET, или наоборот) или это можно чередовать. Процессор 50 регистрации и улучшения изображения регистрирует в пространстве и (не обязательно) по времени реконструированные MR- и PET-изображения. Совместно зарегистрированные изображения сохраняются в памяти для совместно зарегистрированных изображений или в буфере 52. Дополнительно, отдельные изображения PET или MR могут быть улучшены с помощью другого способа воздействия и могут храниться, соответственно, в памяти 24, 42. Изображения, зарегистрированные или улучшенные таким образом, подходящим образом отображенные на индикаторном устройстве 54, визуально воспроизводятся с использованием подходящего двух- или трехмерного программного обеспечения для визуализации или обрабатываются иным образом.
Одно из преимуществ точного знания о молекулярных биохимических процессах, которые лежат в основе медицинских изображений, пригодных, чтобы охарактеризовать ткани определенных типов, например, раковых, при непроникающем расположении на живом организме (in vivo). Магниторезонансная томография с динамическим улучшением контрастности (DCE) обеспечивает визуальное представление как анатомии, так и микрососудистой биологии раковой опухоли путем измерения изменений во времени при интенсивности магниторезонансного сигнала, связанного с внутрисосудистой инъекцией контрастного вещества. Считается, что пространственная неоднородность в кинетике контрастного вещества отражает изменения в тканевой перфузии, микрососудистой проницаемости и создание новых кровеносных сосудов, приспособленных к росту опухолей (ангиогенезу). Ангионетические микрососуды поддерживают рост раковых клеток. Такие микрососуды отчасти распознаются по крупным эндотелиальным клеточным образованиям, приводящим к более высокой проницаемости для мелких молекул. Гадолиний (Gd3+) содержится в мелкомолекулярном контрастном веществе для магнитного резонанса, используемом в настоящее время. Gd3+ может проходить из пространства кровеносного сосуда во внутритканевое внеклеточное пространство, но не проходит через клеточные мембраны. Скорость, при которой Gd3+ переходит во внеклеточное пространство, зависит от перфузии опухоли и проницаемости капилляров. Поскольку ионы Gd3+ могут наполнять внеклеточное пространство, они пригодны для идентификации развития новых сосудов, с ростом злокачественной опухоли.
В PET трудно допустить гетерогенность в заданном объеме, представляющем интерес (V), из-за относительно низкого пространственного разрешения PET. В динамической PET (dPET) объект обычно вводят, а информационные точки получают со связанными с ними отметками времени. По истечении некоторой временной задержки получают большее количество информационных точек с отметками времени. Таким образом, с продвижением метки к области, представляющей интерес, получают четырехмерный набор данных. Общая активность в элементе трехмерного изображения (QOBS(t)), измеряемая в dPET, является уникальной достижимой наблюдаемой величиной для dPET. (QOBS(t)) наблюдают во внеклеточном, внесосудистом пространстве (VEES), и ее можно вычислить следующим образом:
QOBS(t)=VEESCOBS(t)=(l-β)VEES[CEES(t)+CT(t)]+βVEESCP(t)
где β - доля объема крови в кровеносной структуре, CP(t) - функция ввода плазмы, CT(t) - концентрация радиофармацевтического препарата, который специфическим образом связывается с вокселом, а CEES(t) - концентрация радиофармацевтического препарата в области, которая не имеет специфических связей. Васкулярный коэффициент βVEESCP(t) играет значительную роль в оценке параметрической карты и может привести к систематической ошибке в случае пренебрежения им. Общую активность QOBS вычисляют с помощью процессора 56.
В дополнение, функция введения плазмы, отображающая концентрацию свободного, несвязанного радиофармацевтического препарата, необходимого для надежного фармакинетического анализа, не является обязательной, с учетом активности, измеренной непосредственно в левом желудочке сердца, поскольку это возможно не отображает только количество свободного контрастного вещества в плазме крови. Однако контрастное вещество для магниторезонансной томографии не связано с плазмой крови и не способно проходить через гистогематический барьер. В результате, с ним можно обращаться исключительно как с внеклеточным маркером пула крови.
Надежное количественное определение кинетики радиофармацевтического препарата является желательным для лучшего количественного определения физиологических параметров поврежденных тканей, такого как проницаемость кровеносных сосудов, объемов кровотока и кровяного затека. Как DCE-MR, так и 19F-MR дают дополнительную морфологическую информацию о строении кровеносных сосудов в вокселе. Из этой дополнительной информации комбинированное обнаружение способов воздействия dPET и MR может добавить дополнительную наблюдаемую величину, то есть долю 58 объема крови в общей измеренной активности (измеренной способом dPET).
Дополнительная информация о строении кровеносных сосудов может быть очень полезна при определении стадии рака и его лечении. Вообще, чем больше кровеносная сеть вокруг участка опухоли, тем опухоль более развита. Более развитые опухоли часто вырабатывают некротические сердцевинные ткани, которые обладают тем же клеточным строением, что и остальная часть опухоли, но в клетках в этих сердцевинных тканях прекращена чуть ли не вся метаболическая активность или репликация. Такие сердцевинные ткани чуть ли не все недоступны для лечения, поскольку типичные способы лечения опираются на чрезмерно продуктивную природу удвоения раковых клеток. Зная строение новой кровеносной сети, сформировавшейся вокруг таких сердцевин и замещающей окружающую раковую ткань, поддающиеся лечению ткани (такие как быстро удваивающиеся раковые клетки и сама по себе сосудистая сеть) можно идентифицировать и наметить в качестве мишени для реализации схемы лечения.
Другое преимущество комбинирования dPET и MR состоит в допущении значительного повышения отношения сигнал/шум, например, коррекции парциального объема. В комбинированной последовательности, в которой использованы как способы воздействия, так и общая, внеклеточная метка, успешно сочетаются высокое пространственное разрешение способа воздействия MRI и высокое разрешение по времени dPET.
В одном варианте воплощения в комбинированной метке использована молекула-мишень, которая имеет полезную нагрузку в виде контрастного вещества для DCE-MR или MR (такого как Gd3+ или 19F) и метки PET (такой как 18F.)
Описывая настоящую заявку, обратимся теперь к некоторым вариантам воплощения двойного контрастного вещества для PET и MR. Один вариант воплощения контрастного вещества облегчает формирование сигнала как от dPET, так и от DCE-MRI или 19F-MRI. Как показано на фиг.2, контрастное вещество включает в себя молекулу 80. Молекула 80 включает в себя носитель 82, который представляет собой радиоактивную метку PET. В настоящем варианте воплощения носителем является 18F. Молекула 80 также включает в себя систему 84 нацеливания. Система 84 нацеливания состоит в том, что она позволяет молекулам 80 накапливаться в области, представляющей интерес. Возможными кандидатами для системы 84 нацеливания являются моноканальные антитела, адаптамеры, пептидомиметики, полисахариды и т.п. Молекула также включает в себя полезную нагрузку 86, которая включает в себя контрастное вещество DCE-MRI, такое как Gd3+. Также возможны и другие полезные нагрузки, такие как медикаменты. Вариант воплощения согласно фиг.2 включает в себя как контрастное вещество для DCE-MRI, так и метку для dPET, что делает его пригодным для комбинированной технологии формирования изображения dPET/DCE-MRI. Как правило, при комбинированном PET/MR-сканировании дозы контрастного вещества и метки PET приходилось делить пополам, чтобы не возникало избыточной нагрузки на почки и печень пациента. Поскольку пациенту вводили два вещества, ему можно было давать только половину от каждого. При комбинировании меток пациент может получать эквивалент полной дозы каждого вещества, без реального дублирования рабочей нагрузки на почки и печень объекта. Это приводит к общему увеличению соотношения сигнал/шум.
В другом варианте воплощения, как показано на фиг.3, описана молекула 90 другого контрастного вещества. В этом варианте воплощения молекула 90 включает в себя носитель 92, который имеет как радиоактивную метку PET 92a (такую как 18F), так и метку 19F-MRI 92b, которая представляет собой 19F. Молекула 90 также включает в себя систему 94 нацеливания, аналогичную системе 84 нацеливания молекулы 80 согласно фиг.2. Молекула 90 согласно фиг.3 может быть пригодна для технологии формирования изображения dPET/19F-MRI.
Обратимся теперь к фиг.4, где описан другой вариант воплощения молекулы 100. Подобно молекуле 90, молекула 100 имеет комбинированный носитель 102, который включает в себя, как метку PET 102a (18F), так и контрастное вещество 19F-MRI 102b (19F). Дополнительно, молекула 100 включает систему 104 нацеливания, аналогичную подобной системе в предыдущих вариантах воплощения. Этот вариант воплощения также имеет полезную нагрузку 106 контрастного вещества DCE. Таким образом, вариант воплощения согласно фиг.5 пригоден для технологии формирования изображения dPET/19F-MRI, либо для технологии формирования изображения dPET/DCE-MRI.
Обратимся теперь к фиг.5, где контрастное вещество, как ранее было описано, вводят 110 в объект. Известны свойства составных компонентов контрастного вещества. С относительной определенностью можно ожидать, что контрастное вещество будет оставаться за пределами клеток и представляет собой маркер пула чистой крови, который не попадает в эритроциты, не образует связи с белками плазмы крови и не может проходить через гистогематический барьер. После введения контрастное вещество перераспределяется 112 по кровеносной системе до тех пор, пока оно не достигнет области, представляющей интерес, такой как область поражения, вызванная опухолевыми клетками. Вблизи пораженной области контрастное вещество протекает 114 через поврежденные стенки капилляра во внутритканевую область, причем в область как внеклеточную, так и внесосудистую. По истечении некоторого времени контрастное вещество связывается 116 со своей мишенью.
Параллельно осуществляют прием данных изображения. В dPET данные непрерывно собирают все время или собирают в течение последовательных этапов времени таким образом, чтобы можно было все время наблюдать развитие контрастного вещества. Это происходит в противоположность статической PET, где метке позволяют оседать в области, представляющей интерес, а прием данных начинается после того, как метка уже прибыла. В одном варианте воплощения прием данных PET и MR осуществляют одновременно. Это такие временные характеристики, собираемые при приеме PET, которые можно применять к данным MR. Соответствующие изображения затем реконструируют 120. Затем изображения используют таким образом, чтобы они дополняли друг друга. Одно или оба получаемых изображения улучшаются 122 за счет данных, полученных из другого изображения. Этот этап также может включать в себя создание гибридного PET-MR-изображения. Наконец, улучшенные или гибридные данные представляются 124 пользователю для анализа. В одном варианте воплощения пользователь может выбирать, какие изображения следует рассмотреть, например, исходные или гибридные, относительно взвешенных данных по изображениям PET и MR, и решают, желательны ли дополнительные улучшения. Данные также могут поступать в форме параметрических карт, иллюстрирующих градиенты потока k1, k2, k3 и k4. Пользователь может также видеть карты объемных долей области или кривые время-активность, иллюстрирующие поведение контрастного вещества как функции времени.
Этот физиологический процесс можно описать математически, следуя ячеечному подходу. Распределение контрастного вещества в организме пациента теперь отслеживается одновременно с помощью способа воздействия dPET и MRI в течение одного и того же периода времени. Измерение того же количества, а именно, концентрации контрастного вещества, одновременно с различными взаимодополняющими способами воздействия, повышает общие характеристики отношения сигнал/шум, поскольку различные способы воздействия приводят к различным картинам распределения шумов.
Обратимся теперь к фиг.6, где контрастное вещество течет вместе с кровью по капилляру 130, который расположен в вокселе, представляющем интерес 132. Внутренняя стенка капилляра 130 представлена сплошной линией, тогда как внешняя стенка представлена пунктирной линией. Контрастное вещество может проходить по эндотелию 134 сосуда во внесосудистое, внеклеточное пространство (EES, ((l-β)V)) 136. Поток из капилляра 130 в EES 136 представлен как k1. Наоборот, поток из EES 136 в капилляр 130 представлен как k2. В объеме VEES EES 136 контрастное вещество может находиться свободно 138, то есть не быть специфическим образом связанным с другими объектами, представленными как CEES(t). Контрастное вещество в EES 136 также может быть связано с поверхностью ткани-мишени 140, представленной как CT(t). Изменение контрастного вещества из несвязанного состояния 138 в связанное состояние 140 в EES 136 представлено как k3, а изменение контрастного вещества из связанного состояния 140 в несвязанное состояние 138 в EES 124 представлено как k4. Иными словами, k1 указывает на перфузию контрастного вещества, тогда как k3 указывает на его накопление в области. Зная кинетические скорости, разрешение в параметрических картах можно повысить, то есть получить большую информацию о кинетике контрастного вещества в пространстве. Это приводит к общему повышению пространственного разрешения системы PET/MR.
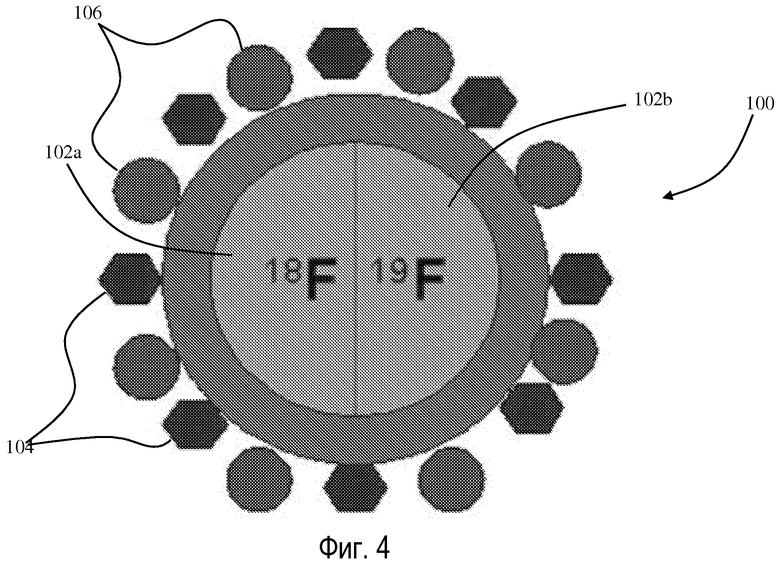
Математическое описание топологии ячейки согласно фиг.6 можно затем описать с помощью следующих линейных дифференциальных уравнений:

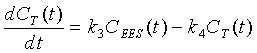
которые можно решать, как показано в вычислениях QOBS(t), приведенных выше. При использовании сопутствующих данных для решения этих уравнений данный этап можно исключить.
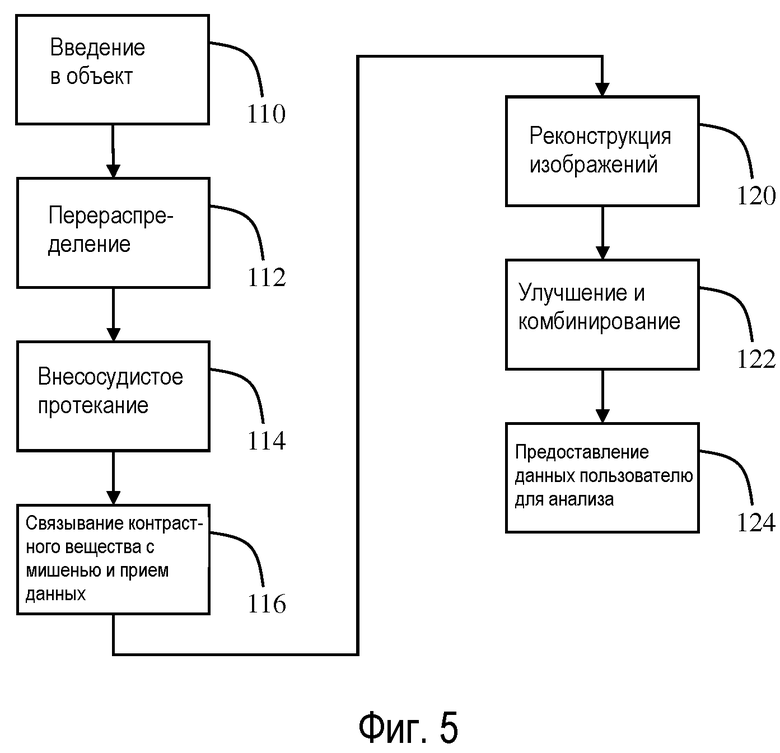
Эти вычисления используют для количественного определения динамических изменений в состоянии контрастного вещества. Например, когда несвязанное контрастное вещество прекращает становиться связанным в EES (т.е. 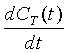
Дополнительная информация о физиологических параметрах, относящихся к фармакокинетическому веществу, позволяет осуществлять более точное количественное определение кинетических параметров. Средневзвешенную сумму связанных 140 и несвязанных 138 частей контрастного вещества можно наблюдать и определять количественно как QOBS(t), из-за высокого пространственного разрешения магниторезонансного изображения. Можно получать трехмерные параметрические карты с высоким разрешением, которые могут привести к корреляциям между кинетическими параметрами и морфологией, которые могут представлять собой клиническую ценность для диагностики, мониторинга терапии и дополнительную терапию.
Вышеописанное обнаружение множеством способов воздействия способствует более адекватному морфологическому анализу и повышает параметрическую оценку фармакокинетического моделирования. Возможность получения комбинированной информации с высоким разрешением по времени для информации по обоим исследованиям и высокое пространственное разрешение расширяет количество достижимых наблюдаемых величин при ограничении пространства параметров до подмножества, соответствующего физиологически релевантных значений, повышающих идентифицируемость модели и физиологическую релевантность кинетических параметров.
Другое возможное применение настоящего контрастного вещества с двойным способом воздействия используется в кардиологии, поскольку систему нацеливания можно приводить в действие для нацеливания и прикрепления к бляшкам, откладывающимся в артериях пациента.
Изобретение было описано со ссылкой на предпочтительные варианты воплощения. По прочтении и понимании предшествующего подробного описания могут быть созданы модификации и изменения и для других вариантов воплощения. Предполагается, что изобретение рассматривается как включающее в себя все такие модификации и изменения, до тех пор пока они охватываются объемом прилагаемой формулы изобретения или ее эквивалентами.


Использование: для диагностической визуализации. Сущность: заключается в том, что выполняют комбинированное формирование изображений посредством РЕТ-МР томографии (позитронно-эмиссионная (РЕТ)-магниторезонансная (MP) томография) для создания гибридных или улучшенных изображений, которые объединяют в себе преимущества обоих способов воздействия. В такой комбинированной конфигурации способов воздействия можно использовать контрастное вещество (80), которое включает в себя как РЕТ-метку (82), так и магниторезонансное средство усиления контраста (86). Контрастное вещество (80) также включает в себя систему (84) нацеливания, которая позволяет контрастному веществу (80) накапливаться в области, представляющей интерес. Технический результат: повышение качества диагностической визуализации. 6 н. и 9 з.п. ф-лы, 6 ил.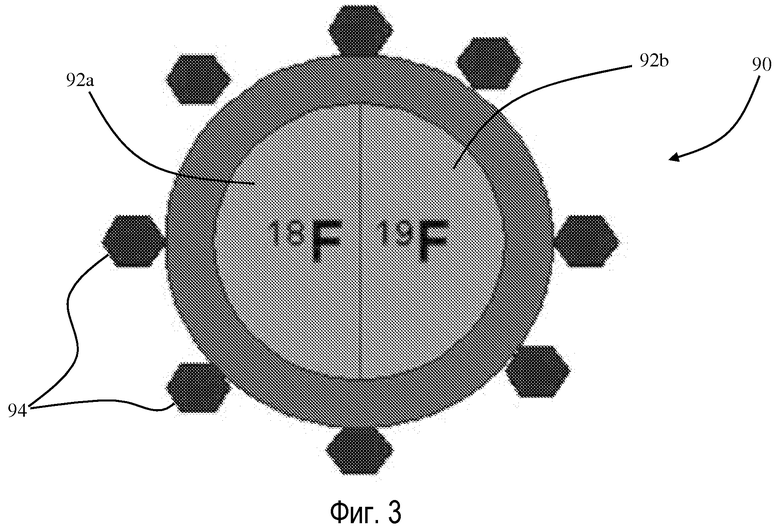
1. Контрастное вещество для параллельной F19-магниторезонансной и ядерной томографии, при которой каждая молекула содержит:
- несущую часть, которая способна проходить по капиллярам эндотелия, но не способна попадать в клетку;
- первый компонент (86), который пригоден для формирования изображения посредством устройства F19-магниторезонансной томографии;
второй компонент (82), который включает в себя радиофармацевтический препарат, который пригоден для формирования изображения посредством устройства для радионуклидной визуализации;
- систему (84) нацеливания, в которой использованы преимущества биологических процессов, заставляющих контрастное вещество накапливаться в целевой области;
причем:
- первый компонент представляет собой фтор-19 или гадолиний; и
- второй компонент представляет собой фтор-18.
2. Контрастное вещество по п.1, в котором система нацеливания включает в себя, по меньшей мере, одно из моноклонального антитела, которое прикрепляется к оболочке клетки определенного типа, или антифибриновой парамагнитной наночастицы.
3. Контрастное вещество по любому из пп.1-2, в котором первый компонент представляет собой F19.
4. Диагностическое устройство формирования изображения для формирования изображения с улучшенным контрастом, в котором использовано контрастное вещество по любому из пп.1-3, причем устройство содержит:
- магниторезонансную часть, которая включает в себя:
- корпус (12) основной электромагнитной катушки для генерирования основного магнитного поля в области (14) формирования изображения устройства;
- корпус (16) градиентной катушки для наложения градиентных магнитных полей на основное магнитное поле;
- корпус (18) радиочастотной катушки, по меньшей мере, для передачи радиочастотных сигналов с частотой, которая возбуждает резонанс в F19, в область формирования изображения;
- часть для позитронно-эмиссионной томографии, которая включает в себя:
- детекторную матрицу (30) для обнаружения излучения, указывающего на события ядерного распада;
- по меньшей мере, один процессор (22, 40) реконструкции для формирования представления изображения из обнаруженных сигналов, исходящих от контрастного вещества по любому из предыдущих пп.1-3, которое накапливается в области формирования изображения; и
- дисплей (54) для отображения реконструированного представления изображения.
5. Способ диагностической визуализации, включающий в себя этапы, на которых:
- вводят в объект контрастное вещество (80) по любому из пп.1-3;
- возбуждают магнитный резонанс в F19-диполях объекта и контрастного вещества (80);
- обнаруживают магнитный резонанс;
- обнаруживают излучение, указывающее на события радиоактивного распада с F18-излучением с помощью детекторной матрицы (30);
- реконструируют обнаруженный F19-магнитный резонанс и F18-излучение в представление изображения объекта; и
- выводят на дисплей представление изображения.
6. Способ по п.5, дополнительно включающий в себя этап, на котором одновременно выполняют этапы обнаружения F19-магнитного резонанса и обнаружения F18-излучения.
7. Способ по любому из п.5 или 6, дополнительно включающий в себя этап, на котором
многократно реконструируют F19-магнитный резонанс и F18-излучение для генерирования последовательности изображений с разрешением по времени для ядерного формирования изображения и пространственного разрешения для F19-магниторезонансного формирования изображения, причем эти изображения отображают изменения распределения контрастного вещества с течением времени.
8. Способ по п.5, дополнительно включающий в себя этап, на котором:
- выполняют расчет степени активности QOBS(t) в вокселе (132) с помощью соотношения:
QOBS(t)=(l-β)VEES[CEES(t)+CT(t)]+βVEESCp(t),
где VEES - объем внеклеточного, внесосудистого пространства (136) в вокселе (132), β - доля объема крови, СТ - концентрация контрастного вещества, связанного (140) в объеме VEES, CEES - концентрация контрастного вещества, несвязанного (138) в объеме VEES, а Ср - функция ввода плазмы.
9. Способ по п.8, дополнительно включающий в себя этап, на котором:
- выполняют расчет топологии ячейки воксела (132) с помощью дифференциальных уравнений:

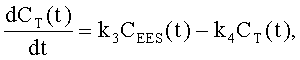
где k1 - поток из капилляра (130) во внеклеточное, внесосудистое пространство (136), k2 - поток из внеклеточного, внесосудистого пространства (136) в капилляр, k3 - переход контрастного вещества из несвязанного состояния (138) в связанное состояние (140) во внеклеточном, внесосудистом пространстве (136), а k4 - переход контрастного вещества из связанного состояния (140) в несвязанное состояние (138) во внеклеточном, внесосудистом пространстве (136).
10. Способ по п.8, дополнительно включающий в себя этапы, на которых:
- обнаруживают перфузию контрастного вещества в и из объема внеклеточного, внесосудистого пространства (136); и
- обнаруживают задержку контрастного вещества в объеме внеклеточного, внесосудистого пространства (136).
11. Способ по любому из пп.5, 6 или 8-10, дополнительно включающий в себя этап, на котором
создают трехмерную параметрическую карту для использования в диагностике или лечении.
12. Процессор, запрограммированный на управление гибридным сканером для магниторезонансной и позитронно-эмиссионной томографии, с помощью которого выполняют способ по любому из пп.5, 6 или 8-10.
13. Машиночитаемый носитель информации, на который записана программа для управления процессором гибридного сканера для магниторезонансной и позитронно-эмиссионной томографии для выполнения способа по любому из пп.5, 6 или 8-10.
14. Медицинское устройство формирования изображений для генерирования изображений с улучшенным контрастом, с использованием контрастного вещества по п.13, содержащее:
- F19-магниторезонансную часть, которая включает в себя:
- корпус (12) основной электромагнитной катушки для генерирования основного магнитного поля в области формирования изображения (14) устройства;
- корпус (16) градиентной катушки для наложения градиентных магнитных полей на основное магнитное поле;
- корпус (18) радиочастотной катушки, по меньшей мере, для передачи радиочастотных сигналов при F19-резонансной частоте в область формирования изображения;
- часть для позитронно-эмиссионной томографии, которая включает в себя:
- детекторную матрицу (30) для обнаружения излучения, указывающего на события ядерного распада;
по меньшей мере, один процессор (22, 40) реконструкции для формирования представления изображения из обнаруженных сигналов, исходящих от контрастного вещества для комбинированной позитронно-эмиссионной/магниторезонансной томографии, которое накапливается в области формирования изображения;
- процессор (56) активности для расчета значения общей наблюдаемой активности, возникающей в вокселе пространства в области формирования изображения; и
- дисплей (54) для отображения реконструированного представления изображения,
причем процессор (56) активности вычисляет значение общей наблюдаемой активности QOBSC(t) с соотношением;
QOBS(t)=(1-β)VEES[CEES(t)+CT(t)]+βVEESCP(t),
где VEES - объем внеклеточного, внесосудистого пространства (136) в вокселе (132), β - доля объема крови, СТ - концентрация контрастного вещества, связанного (140) в объеме VEES, CEES - концентрация контрастного вещества, несвязанного (138) в объеме VEES, а Ср - функция ввода плазмы.
15. Медицинское устройство формирования изображения по п.14, в котором процессор (56) активности рассчитывает топологию ячейки воксела (132) с помощью дифференциальных уравнений:
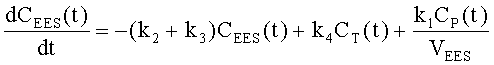
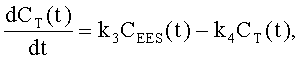
где k1 - поток из капилляра (130) во внеклеточное, внесосудистое пространство (136), k2 - поток из внеклеточного, внесосудистого пространства (136) в капилляр, k3 - переход контрастного вещества из несвязанного состояния (138) в связанное состояние (140) во внеклеточном, внесосудистом пространстве (136), а k4 - переход контрастного вещества из связанного состояния (140) в несвязанное состояние (138) во внеклеточном, внесосудистом пространстве (136).
| RU 2006132814 A, 20.03.2008 | |||
| RU 2006141979 A, 10.06.2008 | |||
| US 2004241158 A1, 02.12.2004 | |||
| US 2008058636 A1, 06.03.2008 | |||
| WO 2007113759 A2, 11.10.2007. |
Авторы
Даты
2013-11-10—Публикация
2009-06-22—Подача