Изобретение относится к медицине, конкретно к способам имплантации внутренних фиксирующих устройств, и может быть использовано в онкологии и нейрохирургии при хирургическом лечении больных опухолями основания черепа, врастающими в полость черепа, а также при обширных травматических поражениях основания передней черепной ямки.
Полость черепа у взрослых является ригидной структурой и допускает возможность лишь минимального расширения интракраниального содержимого через большое затылочное отверстие и небольшие отверстия для сосудов и нервов. В связи с этим у больных с распространенными опухолями головы и шеи врастание краниофациальных опухолей в полость черепа, инвазия твердой мозговой оболочки, инфильтрация и сдавление вещества головного мозга являются одной из причин смерти. Эффективное хирургическое лечение опухолей этой локализации подразумевает выполнение радикальных онкологических операций, которые сопровождаются широким иссечением не только опухолевого узла, но и прилежащих мягких тканей, костных структур черепа и требуют адекватной реконструкции послеоперационных дефектов в области передней черепной ямки. Восстановление барьера между полостью черепа и внечерепным пространством предотвращает возникновение ликворреи, пневмоцефалии, гнойно-септических осложнений, менинго- и энцефалоцеле, сосудистых, неврологических и ликворродинамических расстройств, представляющих опасность для жизни пациента.
Известен способ реконструкции обширных дефектов дна передней черепной ямки с использованием перикраниального надкостничного лоскута, кровоснабжаемого надглазничными и надблоковыми артериями (Johns ME, Winn HR, McLean WC, Cantrell RW. /Pericranial flap for the closure of defects of craniofacial resection. //Laryngoscope. 1981 Jun;91(6):952-9). Данный способ позволяет герметезировать полость черепа, предотвратить возникновение ликворреи. Недостатком способа при обширных дефектах является потеря опорной функции структур основания черепа, формирование менинго-, энцефалоцеле, пульсирующего экзофтальма.
Известен способ реконструкции дефектов дна передней черепной ямки с использованием васкуляризированного костного лоскута на височной мышце для пластики дефектов основания черепа (Kwon S. G., Kim Y. О., Rah D. К. Anterior Cranial Base Reconstruction with a Reverse Temporalis Muscle Flap and Calvarial Bone Graft // Arch Plast Surg. 2012 July; 39(4): 345-351). Способ позволяет герметезировать полость черепа и восстановить опорную функцию основания черепа. Недостатками метода являются увеличение времени оперативного вмешательства за счет необходимости формирования костно-мышечного лоскута, невозможность применения метода у онкологических больных при плохих местных тканях (после лучевой, химиотерапии, предыдущих резекций, эмболизации опухоли, после перевязки наружной сонной артерии), а также значительная частота осложнений со стороны донорского участка, в том числе нарушений открывания рта.
Наиболее близким к заявляемому является способ реконструкции обширных дефектов дна передней черепной ямки с использованием эндопротеза из пористого никелида титана (Сыркашев В.А., Новиков В.А., Рябова А.И. и др. Первичная пластика послеоперационных дефектов основания и свода черепа у онкологических больных // Сибирский онкологический журнал. 2011. №4. С. 54-58). При осуществлении указанного способа индивидуальный эндопротез изготавливают заранее с учетом размеров дефекта и особенностей рельефа основания черепа. Изготовленный эндопротез укладывают на дно передней черепной ямки с опорой на края костного дефекта.
Недостатком прототипа является отсутствие надежной герметизации полости черепа в раннем послеоперационном периоде вследствие проницаемости пористой структуры имплантата, что влечет возможность возникновения ликворреи с последующими внутричерепными осложнениями, а также инфицирования эндопротеза микрофлорой из нижележащих отделов послеоперационной полости, сообщающихся с полостью рта и полостью носа. На фоне инфицирования и воспаления процесс прорастания соединительной ткани идет неправильно и формируется грубый рубец как на нижней поверхности эндопротеза, так и на верхней со стороны полости черепа с образованием глиального рубца. Кроме того, темп эпителизации эндопротеза замедлен в силу частичного контакта его с тканями - только по периметру костного дефекта и, как правило, в нескольких точках касания.
Изобретение направлено на достижение технического результата, обеспечивающего, наряду с восстановлением опорной функции, надежную герметизацию полости черепа, предотвращение ликворреи, отграничение эндопротеза от микрофлоры нижележащих полостей носа и околоносовых пазух, исключение формирования грубого соединительного рубца и ускорение темпа эпителизации.
Указанный технический результат достигается тем, что при осуществлении известного способа реконструкции обширных дефектов дна передней черепной ямки, включающего замещение дефекта заранее изготовленным индивидуальным эндопротезом из пористого никелида титана, укладываемым на краях дефекта со стороны полости черепа, отличие состоит в том, что дефект дна передней черепной ямки предварительно укрывают перикраниальным надкостничным лоскутом на надблоковых и надглазничных артериях, фиксируя его к краям дефекта основания черепа клеевой композицией, поверх перикраниального лоскута устанавливают указанный эндопротез, после чего ушивают дефект твердой мозговой оболочки с использованием широкой фасции бедра. Изобретение поясняется иллюстрациями фиг. 1-4.
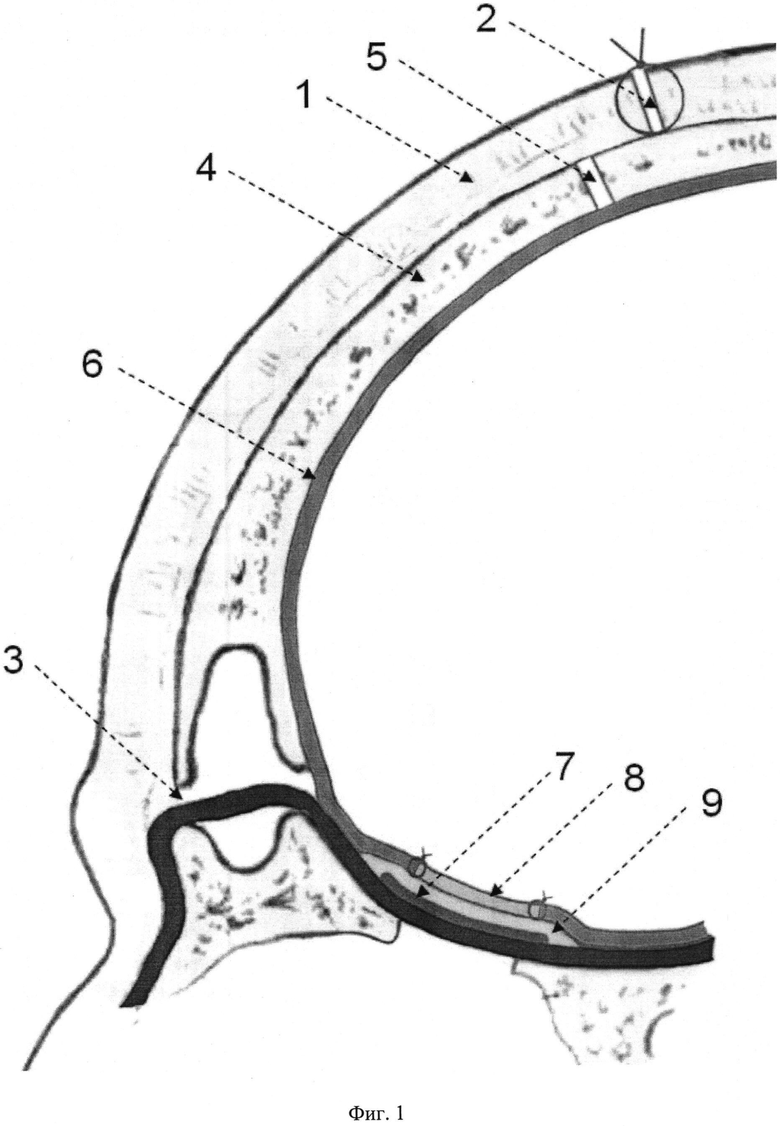
На фиг. 1 представлена схема реконструкции обширного дефекта дна передней черепной ямки. Цифрами обозначены:
1 - кожно-апоневротический слой скальпа;
2 - кожный разрез;
3 - перикраниальный надкостничный лоскут;
4 - лобная кость;
5 - верхняя граница костного лоскута;
6 - твердая мозговая оболочка;
7 - эндопротез из пористого никелида титана;
8 - пластика дефекта твердой мозговой оболочки свободным лоскутом широкой фасции бедра;
9 - герметизация твердой мозговой оболочки тахокомбом.
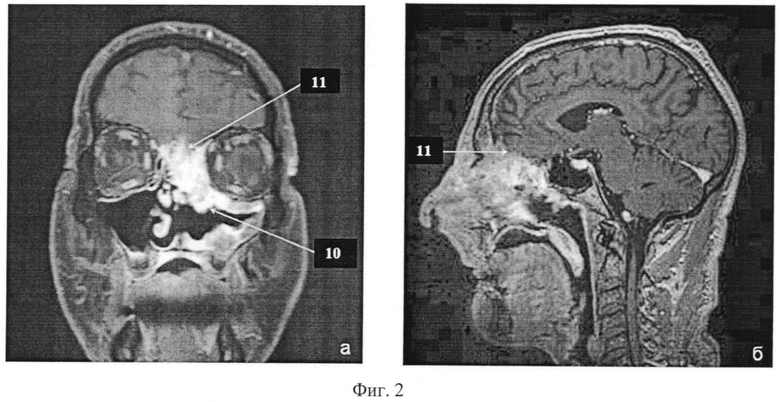
На фиг. 2 представлена МРТ головного мозга больного с контрастированием до операции: «а» - во фронтальной проекции, «б» - в сагиттальной проекции. Цифрами обозначены: 10 - опухоль решетчатого лабиринта, распространяющаяся на медиальные стенки глазниц, верхние отделы гайморовой пазухи слева, переднюю черепную ямку; 11 - инфильтрация опухолью твердой мозговой оболочки.
На фиг. 3 представлена трехмерная реконструкция основания черепа больного с дефектом дна передней черепной ямки (12) по данным компьютерной томографии.
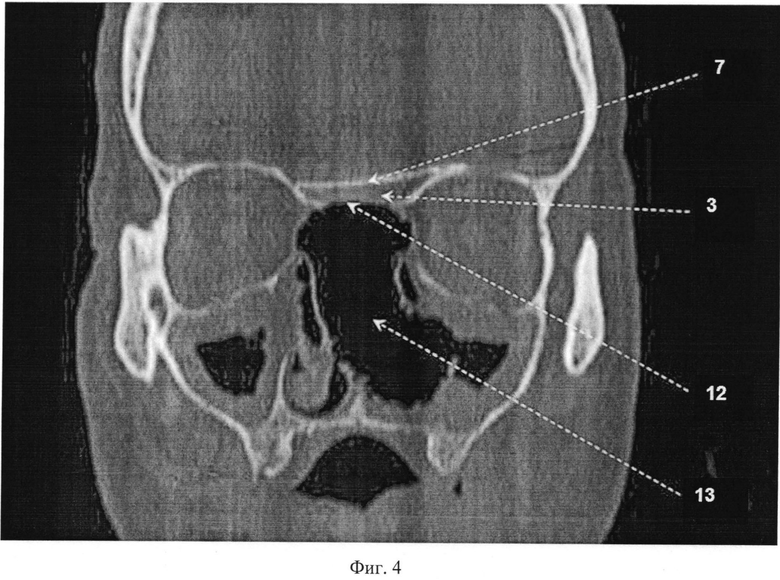
На фиг. 4 представлена компьютерная томограмма (КТ) лицевого скелета в костном режиме больного после операции: 7 - эндопротез из пористого никелида титана; 3 - перикраниальный лоскут; 12 - дефект медиальных отделов дна передней черепной ямки; 13 - послеоперационная полость.
Способ реконструкции обширных дефектов дна передней черепной ямки включает замещение дефекта заранее изготовленным индивидуальным эндопротезом из пористого никелида титана, укладываемым на краях дефекта со стороны полости черепа. При этом предварительно дефект дна передней черепной ямки укрывают перикраниальным надкостничным лоскутом на надблоковых и надглазничных артериях. По краям дефекта лоскут фиксируют клеевой композицией. Поверх лоскута устанавливают указанный эндопротез. Дефект твердой мозговой оболочки ушивают с использованием широкой фасции бедра.
Способ осуществляют следующим образом. После выполнения бикоронарного разреза 2 кожи, подкожной клетчатки и апоневроза 1 производят диссекцию в слое между апоневротическим шлемом 1 и перикраниальной надкостницей 3. Формируют широкий надкостничный лоскут 3 на надглазничных и надблоковых артериях. После удаления краниофациальной опухоли перикраниальный лоскут укладывают на основание черепа по типу забраловидного лоскута и фиксируют клеевой композицией, что предотвращает его миграцию в ходе манипуляций. Поверх перемещенного лоскута 3 для восстановления опорной функции помещают заранее изготовленный эндопротез 7 из пористого никелида титана, который опирается на костные структуры краев дефекта дна передней черепной ямки. Конгруэнтность формы эндопротеза 7 внутренней поверхности основания черепа обеспечивается в ходе его моделирования средствами ультразвуковой и рентгеновской томографии. Надкостничный лоскут 3 служит эластичной прокладкой, увеличивающей качество герметизации по всему периметру дефекта. Таким путем наряду с обеспечением опорной функции, обусловленной эндопротезом, создается герметичный барьер между послеоперационной полостью (полость носа и придаточных пазух) и полостью черепа посредством закрытия нижней поверхности эндопротеза, граничащей с послеоперационной полостью, перикраниальным надкостничным лоскутом 3. Тем самым эндопротез изолируется от инфицирования микрофлорой из указанных полостей, предотвращается возникновение ликворреи и инфицирование внутричерепного пространства. Состоятельность герметичного барьера достигается благодаря сохранению кровоснабжения перемещаемого надкостничного лоскута надблоковыми и надглазничными артериями. Ускорение темпов эпителизации обусловлено контактом всей нижней поверхности эндопротеза с эффективно подпитываемым перемещенным перикраниальным лоскутом и выстоянием в послеоперационную полость слоя рыхлой соединительной ткани. Вследствие ускоренных темпов прорастания эндопротеза снизу, со стороны надкостницы, прорастание со стороны твердой мозговой оболочки остается ниже уровня конкуренции, благодаря чему исключается формирование грубого соединительнотканного рубца на верхней стороне эндопротеза.
Неординарность достигаемого результата обусловлена отсутствием априорных сведений об успешном исходе заявляемого способа, что требовало экспериментального подтверждения.
Во-первых, подлежала проверке состоятельность сформированной многослойной структуры, включающей костное основание, перикраниальный надкостничный лоскут, пористый эндопротез и твердую мозговую оболочку в композите с бедренной фасцией. В отличие от типичных условий непосредственного контакта с костью интегрирование эндопротеза происходит дистанционно через надкостничный лоскут. При этом следовало убедиться в отсутствии возможности миграции эндопротеза, а также ущемления сосудов, питающих надкостницу.
Во-вторых, подлежало проверке отсутствие сдавления мозгового вещества в условиях утолщения дна передней черепной ямки сформированной многослойной структурой.
Экспериментально подтверждено отсутствие рисков, связанных с вышеуказанными факторами.
Заявляемый способ разработан и прошел клинические испытания на базе отделения опухолей головы и шеи ФГБУ «НИИ онкологии» СО РАМН.
Пример: выписка из истории болезни больного В., 66 лет.
Диагноз заболевания: Рак решетчатого лабиринта слева T3N0M0, состояние после комбинированнного лечения. Продолженный рост опухоли с деструкцией основания черепа и распространением в переднюю черепную ямку.
КТ лицевого скелета от 15.01.14: В передних отделах послеоперационной полости определяется опухоль, инфильтрирующая наружный нос, передние и средние клетки решетчатого лабиринта, разрушает левую и частично правую носовую кость, левый лобный отросток верхней челюсти, медиальную стенку левой орбиты на протяжении 13 мм. Определяется деструкция дна передней черепной ямки 21×14 мм (фиг. 2).
МРТ головного мозга с контрастированием от 21.01.2014: На протяжении 25 мм в передне-заднем измерении опухоль прилежит к ТМО лобной доли, местами не прослеживаются контуры между опухолью и ТМО, высока вероятность ее инфильтрации (фиг. 3).
Учитывая гистологическую структуру опухоли, объем проведенного ранее специализированного лечения, деструкцию основания черепа и инфильтрацию твердой мозговой оболочки, 30.01.14 выполнено плановое оперативное вмешательство в объеме краниофациальной резекции опухоли с пластикой твердой мозговой оболочки широкой фасцией бедра и первичной пластикой основания черепа, согласно заявляемому способу, путем формирования перикраниального надкостничного лоскута после выполнения бикоронарного разреза кожи, подкожной клетчатки и апоневроза с формированием надкостничного лоскута шириной 10 см, достаточного для закрытия дефекта. Лоскут фиксирован к краям дефекта основания черепа клеевой композицией. Для восстановления опорной функции поверх лоскута со стороны дна передней черепной ямки помещен индивидуальный эндопротез из пористого никелида титана. Дефект твердой мозговой оболочки ушит с использованием фрагмента широкой фасции бедра. Послеоперационная полость (полость носа и околоносовые пазухи) заполнена йодоформной турундой. Швы на мягкие ткани лица.
Ранний послеоперационный период протекал гладко. Турунда удалена на 7-е сутки. Больной вертикализирован на 5-е сутки. Ликворреи не отмечалось. Швы сняты поэтапно на 8-14 сутки. На контрольной КТ головного мозга (фиг. 4) эндопротез стоит удовлетворительно, энцефалоцеле нет. Гистологическое исследование образцов с краев области резекции: раковых клеток не обнаружено.
Использование предложенного способа реконструкции обширных дефектов дна передней черепной ямки позволяет повысить надежность герметизации полости черепа, предотвратить менинго-, энцефалоцеле и снизить количество осложнений, связанных с ликворреей и внутричерепными инфекционными осложнениями.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ реконструкции основания передней черепной ямки при выполнении блок-резекции распространенной опухоли переднего отдела основания черепа | 2019 |
|
RU2730955C1 |
| СПОСОБ ПЛАСТИКИ ОБШИРНЫХ ПОСТРЕЗЕКЦИОННЫХ ОКОНЧАТЫХ ДЕФЕКТОВ СТЕНОК ГРУДНОЙ КЛЕТКИ И/ИЛИ СВОДА ЧЕРЕПА | 2009 |
|
RU2393808C1 |
| Способ пластики дефектов основания передней черепной ямки | 2015 |
|
RU2607183C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ СТЕНОК ОРБИТЫ | 2014 |
|
RU2565375C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИМПЛАНТАТА ДЛЯ ПРОТЕЗИРОВАНИЯ СТЕНОК ОРБИТЫ | 2015 |
|
RU2639429C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 2011 |
|
RU2475194C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 2012 |
|
RU2487681C1 |
| СПОСОБ ПЛАСТИЧЕСКОГО ЗАКРЫТИЯ ДЕФЕКТОВ ОСНОВАНИЯ ЧЕРЕПА | 2007 |
|
RU2347535C1 |
| СПОСОБ ПЛАСТИКИ КОСТНОГО ДЕФЕКТА ОСНОВАНИЯ ЧЕРЕПА | 2019 |
|
RU2722406C1 |
| СПОСОБ РЕКОНСТРУКЦИИ АЛЬВЕОЛЯРНОГО ОТРОСТКА ВЕРХНЕЙ ЧЕЛЮСТИ У БОЛЬНЫХ С ВРОЖДЕННЫМИ РАСЩЕЛИНАМИ | 2005 |
|
RU2286730C1 |

Изобретение относится к медицине, а именно к нейрохирургии. Осуществляют замещение дефекта дна передней черепной ямки заранее изготовленным индивидуальным эндопротезом из пористого никелида титана, укладываемым на краях дефекта со стороны полости черепа. При этом дефект дна передней черепной ямки предварительно укрывают перикраниальным надкостничным лоскутом на надблоковых и надглазничных артериях, фиксируя его к краям дефекта основания черепа клеевой композицией. Поверх перикраниального лоскута устанавливают указанный эндопротез и ушивают дефект твердой мозговой оболочки с использованием широкой фасции бедра. Способ позволяет снизить послеоперационные осложнения, что достигается за счет надежной герметизации полости черепа, приводящей к предотвращению ликвореи и защите околоносовых пазух носа от инфицирования. 4 ил., 1 пр.
Способ реконструкции обширных дефектов дна передней черепной ямки, включающий замещение дефекта заранее изготовленным индивидуальным эндопротезом из пористого никелида титана, укладываемым на краях дефекта со стороны полости черепа, отличающийся тем, что дефект дна передней черепной ямки предварительно укрывают перикраниальным надкостничным лоскутом на надблоковых и надглазничных артериях, фиксируя его к краям дефекта основания черепа клеевой композицией, поверх перикраниального лоскута устанавливают указанный эндопротез, после чего ушивают дефект твердой мозговой оболочки с использованием широкой фасции бедра.
| СЫРКАШЕВ В.А | |||
| и др | |||
| Первичная пластика послеоперационных дефектов основания черепа у онкологических больных | |||
| Сибирский онкологический журнал | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
| СПОСОБ ПЛАСТИЧЕСКОГО ЗАКРЫТИЯ ДЕФЕКТОВ ОСНОВАНИЯ ЧЕРЕПА | 2007 |
|
RU2347535C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ НАЗАЛЬНОЙ ЛИКВОРЕИ | 2012 |
|
RU2512782C1 |
| Устройство для контроля чувствительности и т. п. приборов к инфракрасному излучению | 1957 |
|
SU115495A1 |
| US 2010234896 A1, 16.09.2010 | |||
| ЧЕРЕКАЕВ В.А | |||
| и др | |||
| Хирургия опухолей основания черепа, распространяющихся | |||
Авторы
Даты
2015-12-10—Публикация
2014-05-22—Подача