Изобретение относится к области медицинской диагностики, может быть использовано для прогнозирования риска развития гипертонической болезни у индивидуумов, имеющих наследственную отягощенность.
Гипертоническая болезнь является одним из наиболее распространенных сердечно-сосудистых заболеваний [2013 ESH/ESC guidelines for the management of arterial hypertension [Text] /G. Mancia, R. Fagard, K. Narkiewicz [et al.] //J. Hypertens. - 2013. - Vol.31, №7. - P. 1281-1357]. Это важнейший фактор риска развития ишемической болезни сердца, сердечной недостаточности, а также таких грозных сердечно-сосудистых осложнений как инфаркт миокарда, острые нарушения мозгового кровообращения [Al-Ansary L. A., Tricco A. C., Adi Y., 2013. A systematic review of recent clinical practice guidelines on the diagnosis, assessment and management of hypertension [Text] /L.A. Al-Ansary, A.C. Tricco, Y. Adi //PLoS One. - 2013. - Vol.8, №1. - Art.e53744].
Генетическая предрасположенность является неоспоримым этиологическим фактором развития гипертонической болезни, как указано в источнике [Kreutz, R. Hypertension and cardiovascular end organ damage [Electronic resource]/R. Kreutz //Herz-Kreislauf-Netz /NationalesGenomforschungsnetz (National Genomics Research Network), University of Heidelberg. - Heidelberg, 2014. -Mode of access:
http://www.herz-kreislauf-netz.de/index.php?id=13&L=1&BF=0/lostpw.php].
Согласно литературным данным, у больных гипертонической болезнью с наследственной отягощенностью заболевание может развиться на 8 лет раньше, чем у людей, не имеющих отягощенного семейного анамнеза [Genetic basis of essential arterial hypertension in Colombia: advances in nine years of work [Text] /D. Aristizabal, E. Garcia, J. McEwen [et al.] //Rev. Colomb. Cardiol. - 2006. - Vol.12, №6. - P. 409-430].
С практической точки зрения представляется крайне необходимым выделение критериев индивидуального прогнозирования риска развития гипертонической болезни у индивидуумов, имеющих наследственную отягощенность на основании исследованных полиморфных вариантов генов цитокинов с целью выявления индивидуумов, предрасположенных к гипертонической болезни.
Гипертоническая болезнь имеет мультифакториальную природу [Пузырев В.П. Генетический взгляд на феномен сочетанной патологии у человека [Текст]/В.П. Пузырев //Медицинская генетика. - 2008. - Т. 7, №9. - С. 3-9], в развитии которой в настоящее время важное патогенетическое значение придается неспецифическому воспалению [Inflammation and hypertension: the interplay of interleukin-6, dietary sodium and the renin-angiotensin system in humans [Text] /B.Chamarthi, G. H. Williams, V.Ricchiuti [et al.] //Am. J. Hypertens. - 2011. - Vol.24, №10. - P. 1143-1148]. Одно из центральных мест в этом процессе занимают факторы некроза опухолей и их рецепторы [Zhang, C. The role of inflammatory cytokines in endothelial dysfunction [Text] /C. Zhang //Basic Res. Cardiol. - 2008. - Vol.103, №5. - P. 398-406].
TNFα - многофункциональный цитокин, обеспечивающий широкий спектр биологических процессов [Implications of dynamic changes among tumor necrosis factor - alpha (TNF-alpha), membrane TNF receptor, and soluble TNF receptor levels in regard to the severity of dengue infection [Text] /L.Wang, R.F. Chen, J.W. Liu et al. //Am. J. Trop. Med. Hyg. - 2007. - Vol.77. - №2. - P. 297-302]. Он может нарушать структурную целостность и функцию эндотелиальных клеток, что приводит к дисфункции эндотелия, которая выражается снижением синтеза и высвобождения вазодилататоров (оксид азота) и повышенной секрецией вазоконстрикторов (эндотелина и простагландина), что ускоряет сужение сосудов, а также влияет на гладкомышечные клетки, изменяя эксрессию их рецепторов к ангиотензину типа I, что приводит к повышению общего периферического сопротивления сосудов и подъему артериального давления [Li, C. Q.The association of the TNF-α Gene of G-308A genotypes in Chinese hyperuricemia patients and cardiovascular risk factors [Text] /C. Q. Li, F. Wang, Y. G. Wang //Molecular Cardiology of China. - 2010. - №1. - P. 29-32].
TNFβ (лимфотоксин α, Ltα) представляет собой гликопротеид, который содержит 171 аминокислотных остатков. Ltα участвует в развитии первичного иммунитета и защите организма от вирусов, а также задействован в процессах апоптоза [Lymphotoxin beta receptor - dependent control of lipid homeostasis [Text] /J. C.Lo, Y.Wang, A. V. Tumanov [et al.] //Science. - 2007. - Vol.316, №5822. - P. 285-288]. Это один из цитокинов, продуцируемых на ранних стадиях сосудистых воспалительных процессов [Effects of lymphotoxin-alpha gene and galectin-2 gene polymorphisms on inflammatory biomarkers, cellular adhesion molecules and risk of coronary heart disease [Text] /F. W. Asselbergs, J. K. Pai, K. M. Rexrode [et al.] //Clin. Sci. (Lond). - 2007. - Vol.112, №5. - Р. 291-298]. Ltα активирует молекулы адгезии и цитокины (RANTES, IP-10, МСР-1, BLC, SLC, ELC), выделяющиеся эндотелиальными клетками, а также оказывает влияние на метаболизм глюкозы, липидов [Haplotype-based association of four lymphotoxin-alpha gene polymorphisms with the risk of coronary artery disease in Han Chinese [Text] /Y. Liu, H. Sheng, L.Lu [et al.] //Tohoku J. Exp. Med. - 2011. - Vol.224,№2. - P. 119-125]. Лимфотоксин α обладает рядом подобных TNFα биологических активностей [Cytokine gene polymorphism in human disease /M.V. Hollegaard, J.L. Bidwell //Genes Immun. - 2006. - Vol.7. - Suppl. 3. - P. 269-276], связываясь с теми же рецепторами, что и TNFα.
В настоящее время идентифицированы два типа рецепторов TNFα: TNFR1 и TNFR2. TNFR1 представляет собой гликопротеин с молекулярной массой 55 кДа и состоит из 435 аминокислот. Он реализует все возможные виды действий факторов некроза опухолей, такие как апоптоз, пролиферация и дифференцировка клеток, плюс ко всему проявляет противовирусную активность, регулирует воспалительный ответ [Peripheral receptor targets for analgesia: novel approaches to pain treatment [Text] /ed. by E. C. Brian. - Hoboken, N.J.: John Wiley Sons, 2009. - 541 p.].
В изученной научно-медицинской и доступной патентной литературе авторами не было обнаружено способа прогнозирования риска развития гипертонической болезни у индивидуумов, имеющих наследственную отягощенность на основе данных о сочетаниях генетических полиморфизмов -308G/A TNFα,+250A/G Ltα,+36A/G TNFR1.
Для оценки сложившейся патентной ситуации был выполнен поиск по охранным документам за период с 1990 по 2012 гг. Анализ документов производился по направлению: способ прогнозирования риска развития гипертонической болезни у индивидуумов, имеющих наследственную отягощенность на основе молекулярно-генетических данных в зависимости от полиморфных маркеров генов факторов некроза опухолей и их рецепторов.
Выявлен патент РФ №2257139 (дата публикации 27.07.2005), где предложен «Способ прогнозирования возникновения гипертонической болезни», заключающийся в оценке гемодинамических показателей в ответ на нагрузочную пробу. При этом в качестве нагрузочной пробы пациент делает глубокий вдох и задерживает дыхание.
В патенте РФ №2307577 (дата публикации 10.10.2007) предложен «Способ прогнозирования возможности возникновения гипертонической болезни для коренных сельских жителей-телеутов юга Кузбасса», который основан на антропометрических измерениях массы тела, роста, окружностей груди, талии, бедер и расчете соматического индекса.
Общий недостаток указанных способов заключается в том, что не рассматриваются генетические полиморфизмы и их сочетания с риском развития гипертонической болезни.
В патенте РФ №2456608 (дата публикации 20.07.2012) предложен «Способ прогнозирования риска возникновения гипертонической болезни у мужчин», согласно которому для оценки риска развития гипертонической болезни производят генотипирование полиморфных локусов генов флавиновой монооксигеназы 3 типа, цитохрома Р-450 1 В1, N-ацетилтрансферазы 2 типа и анализ средовых факторов риска.
Недостаток метода заключается в том, что он рассматривает риск развития гипертонической болезни только у мужчин, а согласно литературным данным гипертоническая болезнь развивается чаще у женщин [Эпидемиология артериальной гипертонии в России. Результаты федерального мониторинга 2003-2010 гг. /Р.Г. Оганов [и др.] //Кардиоваскулярная терапия и профилактика. - 2011. - №1. - С. 9-13]. Кроме того, не учитываются сочетания генов и не рассматриваются гены-кандидаты, связанные с воспалительным механизмом развития гипертонической болезни.
За прототип выбран патент РФ №2287158 (дата публикации 10.11.2006) «Способ прогнозирования возникновения гипертонической болезни по генетическим факторам риска», который заключается в выделении ДНК из лимфоцитов периферической венозной крови методом полимеразной цепной реакции синтеза ДНК, амплификации фрагментов генов PON1 и СЕТР, проведении анализа полиморфизма длин рестрикционных фрагментов ампликонов и в зависимости от выявляемых генотипов пациентов относят в группу с высоким или низким риском возникновения гипертонической болезни.
Недостаток метода заключается в том, что не учитывается наследственная отягощенность и сочетания генетических вариантов индивидуумов русской национальности, уроженцев Центрального Черноземья, а также не рассматриваются гены-кандидаты, связанные с воспалительным механизмом развития гипертонической болезни.
Задачей настоящего исследования является расширение арсенала способов диагностики, а именно создание способа прогнозирования развития гипертонической болезни у индивидуумов, имеющих наследственную отягощенность на основе данных о сочетаниях генетических вариантов -308G/A TNFα,+250A/G Ltα,+36A/G TNFR1.
Технический результат использования изобретения - получение критериев оценки риска развития гипертонической болезни у индивидуумов русской национальности, уроженцев Центрального Черноземья, имеющих наследственную отягощенность на основе данных о сочетаниях генетических вариантов локусов -308G/A TNFα,+250A/G Ltα,+36A/G TNFR1.
В соответствии с поставленной задачей был разработан способ прогнозирования риска развития гипертонической болезни у индивидуумов, имеющих наследственную отягощенность, включающий:
- выделение ДНК из периферической венозной крови;
- анализ полиморфизмов генов -308G/A TNFα,+250A/G Ltα,+36A/G TNFR1;
- прогнозирование повышенного риска развития гипертонической болезни у индивидуумов русской национальности, уроженцев Центрального Черноземья, имеющих наследственную отягощенность в случае выявления сочетания аллеля -308A TNFα с аллелем+36G TNFR1;
- прогнозирование низкого риска развития данного заболевания у индивидуумов русской национальности, уроженцев Центрального Черноземья при выявлении следующих сочетаний: алелля -308G TNFα с генотипом+250AA Ltα или аллеля -308G TNFα с аллелем+250A Ltα.
Новизна и изобретательский уровень заключаются в том, что из уровня техники не известна возможность прогноза риска развития гипертонической болезни у индивидуумов, имеющих наследственную отягощенность по данным о сочетаниях генетических вариантов локусов -308G/A TNFα,+250A/G Ltα,+36A/G TNFR1.
Способ осуществляют следующим образом.
ДНК выделяют из образцов периферической венозной крови индивидуумов в 2 этапа. На первом этапе к 4 мл крови добавляют 25 мл лизирующего буфера, содержащего 320 мМ сахарозы, 1% тритон Х-100, 5 мМ MgCl2, 10 мМ трис-HCl (pH=7,6). Полученную смесь перемешивают и центрифугируют при 4°С, 4000 об/мин в течение 20 минут. После центрифугирования надосадочную жидкость сливают, к осадку добавляют 4 мл раствора, содержащего 25 мМ ЭДТА (рН=8,0) и 75 мМNaCl, ресуспензируют. Затем прибавляют 0,4 мл 10% SDS, 35 мкл протеиназы К (10 мг/мл) и инкубируют образец при 37°С в течение 16 часов.
На втором этапе из полученного лизата последовательно проводят экстракцию ДНК равными объемами фенола, фенол-хлороформа (1:1) и хлороформа с центрифугированием при 4000 об/мин в течение 10 минут. После каждого центрифугирования производят отбор водной фазы. ДНК осаждают из раствора двумя объемами охлажденного 96% этанола. Сформированную ДНК растворяют в бидистиллированной, деионизованной воде и хранят при -20°С. Выделенную ДНК использовали для проведения полимеразной цепной реакции синтеза ДНК.
Анализ всех локусов (-308G/A TNFα,+250G/A Ltα,+36A/G TNFR1) осуществляют методами полимеразной цепной реакции (ПЦР) синтеза ДНК. ПЦР проводилась на аппарате IQ5 (Bio-Rad) в режиме real time с использованием ДНК-полимеразы Thermus aquaticus производства фирмы «Силекс-М» и стандартных олигонуклеотидных праймеров и зондов, синтезированных фирмой «Синтол» с последующим анализом полиморфизмов методом дискриминации аллелей. Для дискриминации аллелей использовалась программа Bio-Rad «IQ5-Standart Edition».
Изобретение охарактеризовано на следующих фигурах:
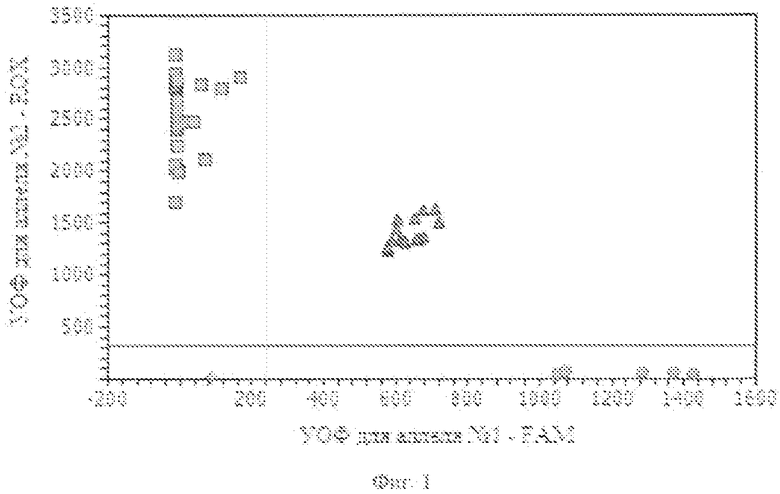
фиг. 1, где представлена дискриминация аллелей по локусу -308G/A TNFα, где ○ - гомозиготы -308АА TNFα, □ - гомозиготы -308GG TNFα, ∆ - гетерозиготы -308GA TNFα, ◊ - отрицательный контроль;
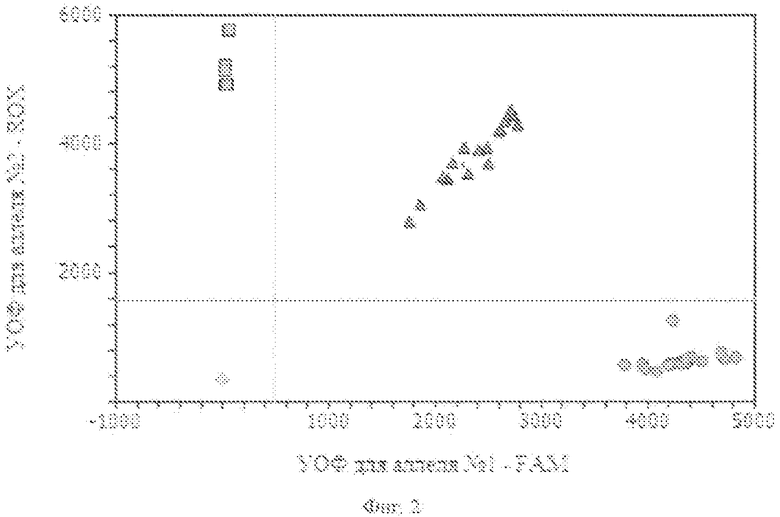
фиг. 2, где представлена дискриминация аллелей по локусу+250A/G Ltα, где
○ - гомозиготы+250GG Ltα, ∆- гетерозиготы+250AG Ltα, □ - гомозиготы+250AA Ltα, ◊ - отрицательный контроль;
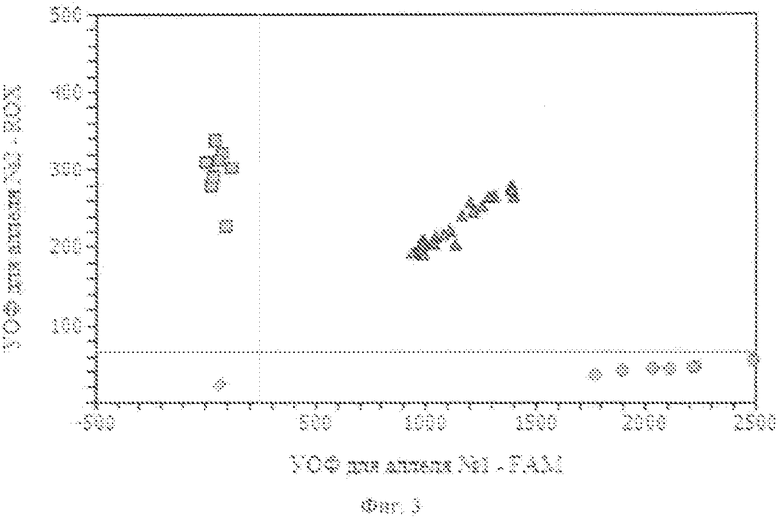
фиг. 3, где представлена дискриминация аллелей по локусу+36A/G TNFR1, где ○ - гомозиготы+36AA TNFR1, ∆- гетерозиготы+36AG TNFR1, □ - гомозиготы+36GG TNFR1, ◊ - отрицательный контроль;
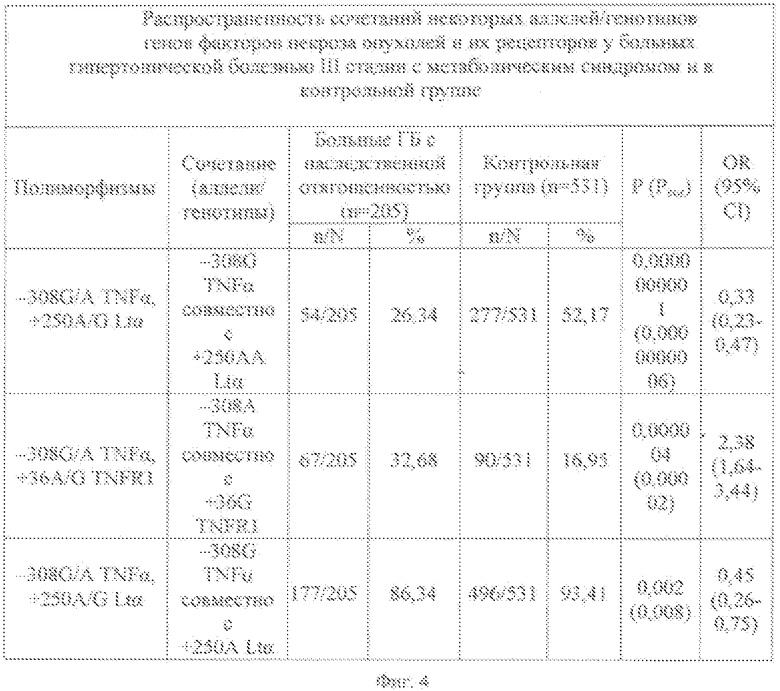
фиг. 4, на которой представлена таблица, где показана распространенность сочетаний аллелей/генотипов генов факторов некроза опухолей и их рецепторов у больных гипертонической болезнью III стадии с метаболическим синдромом и в контрольной группе.
На фигурах 1-3 две полосы, вертикальная и горизонтальная, делят график на четыре секции: одна для каждого гомозиготного состояния, одна для гетерозиготного состояния и секция без реакции. Присвоение генотипов неизвестным образцам определяется вычерчиванием уровня относительной флуоресценции (далее УОФ) для одного флуорофора (на оси x) относительно УОФ для другого флуорофора (на оси y) на диаграмме дискриминации аллелей.
• Если значения УОФ неизвестного образца находятся выше горизонтальной полосы и правее вертикальной полосы, генотип гетерозиготен (GA).
• Если значения УОФ неизвестного образца находятся ниже горизонтальной полосы и левее вертикальной, определение генотипа невозможно (в данном случае неопределенный образец - отрицательный контроль).
Для фигур 1, 3:
• Если значения УОФ неизвестного образца находятся выше горизонтальной полосы и левее вертикальной полосы, генотип гомозиготен по аллелю A, т.к. УОФ аллеля A отложены по оси y.
• Если значения УОФ неизвестного образца находятся ниже горизонтальной полосы и правее вертикальной, генотип гомозиготен по аллелю G, т.к. УОФ аллеля G отложены по оси x.
Для фигуры 2:
• Если значения УОФ неизвестного образца находятся выше горизонтальной полосы и левее вертикальной полосы, генотип гомозиготен по аллелю G, т.к. УОФ аллеля G отложены по оси y.
• Если значения УОФ неизвестного образца находятся ниже горизонтальной полосы и правее вертикальной, генотип гомозиготен по аллелю A, т.к. УОФ аллеля A отложены по оси x.
Возможность использования предложенного способа для оценки риска развития гипертонической болезни у индивидуумов, имеющих наследственную отягощенность подтверждает анализ результатов наблюдений 205 индивидуумов русской национальности, являющихся уроженцами Центрального Черноземья РФ, больных гипертонической болезнью с отягощенным семейным анамнезом, и 531 человек контрольной группы. Формирование выборок больных и контроля осуществлялись на базе кардиологического отделения Белгородской областной клинической больницы Святителя Иоасафа.
Критерии включения в исследуемые выборки:
1. Индивидуумы русской национальности, являющиеся уроженцами Центрального Черноземья РФ и не имеющие родства между собой.
2. Добровольное согласие пациентов на проведение исследования.
3. В группу больных включались индивидуумы только после установления диагноза гипертонической болезни, который подтверждался клиническими и лабораторно-инструментальными методами обследования, в соответствии с обязательными диагностическими стандартами, рекомендованными ВНОК [Рекомендации ВНОК, 2010].
Критерии исключения из исследуемых выборок:
1. Пациенты с симптоматическими артериальными гипертензиями.
2. Наличие тяжелой соматической патологии (печеночная, почечная недостаточность, аутоиммунные и онкологические заболевания).
3. Больные нерусской национальности, родившиеся вне Центрального Черноземья России.
4. Индивидуумы, отказавшиеся от проводимого исследования.
Типирование молекулярно-генетических маркеров осуществлялось в лаборатории «Молекулярной генетики человека» медицинского института Белгородского государственного национального исследовательского университета.
Изучение роли комбинаций генетических вариантов -308G/A TNFα,+250 A/G Ltα,+36A/G TNFR1 в формирование гипертонической болезни у индивидуумов, имеющих наследственную отягощенность проводилось с помощью программного обеспечения АРSampler [http://sources.redhat.com/cygwin/], использующего метод Монте-Карло марковскими цепями и байесовскую непараметрическую статистику [A Gibbs sampler for identification of symmetrically structured, spaced DNA motifs with improved estimation of the signal length [Text] /A. V.Favorov, M. S. Gelfand, A. V. Gerasimova [et al.] //Bioinformatics. - 2005. - Vol.21, №10. - P. 2240-2245]. С целью минимизации ошибок 1-го рода, связанных с получением ложноположительных результатов при проведении множественных сравнений, вводили поправку Бонферрони - производили перерасчет уровня значимости р для множественных парных сравнений по формуле: рcor=р×n, где р - полученный уровень статистической значимости, n - количество парных сравнений. За статистически значимый уровень принимали рcor≤ 0,05 [Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA /О. Ю. Реброва. - [3-е изд.]. - Москва: Медиа Сфера, 2006. - 305 с.: ил].
Как следует из данных, представленных в таблице на фиг. 4:
- зарегистрированы различия в распространенности сочетания аллеля -308A TNFα с аллелем+36G TNFR1 между больными с наследственной отягощенностью (32,68%) и контролем (16,95%). Эта комбинация аллельных вариантов является фактором риска формирования гипертонической болезни у индивидуумов с отягощенным семейным анамнезом (р=0,000004, pcor=0,00002, ОR=2,38, 95% CI 1,64-3,44).
Сочетание аллеля -308G TNFα с генотипом+250AA Ltα имеют 26,34% больных гипертонической болезнью с наследственной отягощенностью, а в контрольной группе оно выявлено у 52,17%. Эта комбинация полиморфных вариантов генов факторов некроза опухолей является протективным фактором развития гипертонической болезни у индивидуумов с отягощенным семейным анамнезом, о чем свидетельствует величина ОR, равная 0,33 при 95% доверительном интервале 0,23-0,47, рcor=0,0000000006.
Также, выявлены достоверные различия в концентрациях сочетания аллеля -308G TNFα с аллелем+250A Ltα между больными гипертонической болезнью с наследственной отягощенностью (86,34%) и контрольной группой (93,41%). Данная комбинация полиморфных вариантов генов факторов некроза опухолей является протективной для развития гипертонической болезни у индивидуумов с наследственной отягощенностью по гипертонической болезни (р=0,002, pcor=0,008, ОR=0,45, 95% CI 0,26-0,75).
Таким образом, результаты, полученные с помощью биоинформатического анализа, свидетельствуют о вовлеченности комбинаций полиморфных вариантов генов фактора некроза опухоли α (-308G/A TNFα), лимфотоксина α (+250A/G Ltα) и рецептора фактора некроза опухоли 1-го типа (+36A/G TNFR1) в формирование гипертонической болезни у индивидуумов с отягощенным семейным анамнезом.
В качестве примеров конкретного выполнения разработанного способа приведено генетическое обследование по локусам -308G/A TNFα,+250A/G Ltα,+36A/G TNFR1 трех добровольцев русской национальности, являющихся жителями Центрального Черноземья, имеющих среди родственников 1-й степени родства больных гипертонической болезнью.
У индивидуума А. было выявлено сочетание аллеля -308A TNFα с аллелем+36G TNFR1. На основании этих результатов данный индивидуум включен в группу риска по развитию гипертонической болезни и ему назначен комплекс профилактических мероприятий по предупреждению развития гипертонической болезни (динамический контроль показателей артериального давления, спортивная ходьба не менее 1 часа в день, ограничение употребления поваренной соли, нормализация психо-эмоционального состояния и др.).
У индивидуума В. было выявлено сочетание аллеля -308G TNFα с генотипом+250AA Ltα. На основании этих результатов у данного индивидуума прогнозируют минимальный риск развития гипертонической болезни.
У индивидуума С. было выявлено сочетание аллеля -308G TNFα с аллелем+250A Ltα. На основании этих результатов у данного индивидуума прогнозируют минимальный риск развития гипертонической болезни, что подтверждено дальнейшим наблюдением.
Применение данного способа позволит формировать среди индивидуумов, имеющих наследственную отягощенность по гипертонической болезни на доклиническом этапе группы риска и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития гипертонической болезни.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ III СТАДИИ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ У БОЛЬНЫХ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНЬЮ С МЕТАБОЛИЧЕСКИМ СИНДРОМОМ | 2014 |
|
RU2598745C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПЕРВИЧНОЙ ОТКРЫТОУГОЛЬНОЙ ГЛАУКОМЫ У ИНДИВИДУУМОВ В ЗАВИСИМОСТИ ОТ НАЛИЧИЯ/ОТСУТСТВИЯ СОПУТСТВУЮЩЕЙ ПАТОЛОГИИ ГЛАЗ | 2014 |
|
RU2597784C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ФОРМИРОВАНИЯ ХРОНИЧЕСКОЙ ИСТИННОЙ ЭКЗЕМЫ У ИНДИВИДУУМОВ В ЗАВИСИМОСТИ ОТ НАЛИЧИЯ НАСЛЕДСТВЕННОЙ ОТЯГОЩЕННОСТИ | 2014 |
|
RU2585382C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПЕРВИЧНОЙ ОТКРЫТОУГОЛЬНОЙ ГЛАУКОМЫ III-IV СТАДИЙ | 2014 |
|
RU2580308C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ХРОНИЧЕСКОЙ ИСТИННОЙ ЭКЗЕМЫ У ЛИЦ МУЖСКОГО ПОЛА | 2014 |
|
RU2574015C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ УРОВНЯ ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ У БОЛЬНЫХ С ПОУГ В ЗАВИСИМОСТИ ОТ ГЕНЕТИЧЕСКИХ ДАННЫХ | 2014 |
|
RU2580307C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ УРОВНЯ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ У БОЛЬНЫХ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНЬЮ | 2014 |
|
RU2572336C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПОДОСТРОЙ СТАДИИ ХРОНИЧЕСКОЙ ИСТИННОЙ ЭКЗЕМЫ | 2014 |
|
RU2572338C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ III СТАДИИ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ | 2014 |
|
RU2565407C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ СРЕДНЕТЯЖЕЛОГО ТЕЧЕНИЯ ХРОНИЧЕСКОЙ ИСТИННОЙ ЭКЗЕМЫ | 2014 |
|
RU2578441C1 |
Изобретение относится к области медицины. Изобретение представляет способ прогнозирования риска развития гипертонической болезни у индивидуумов, имеющих наследственную отягощенность. Изобретение обеспечивает создание способа прогнозирования развития гипертонической болезни у индивидуумов, имеющих наследственную отягощенность на основе данных о сочетаниях генетических вариантов -308G/A TNFα,+250A/G Ltα,+36A/G TNFR1. 4 ил.
Способ прогнозирования риска развития гипертонической болезни у индивидуумов, имеющих наследственную отягощенность, включающий выделение ДНК из периферической венозной крови методом полимеразной цепной реакции синтеза ДНК, анализ полиморфизмов, отличающийся тем, что анализируют полиморфизмы генов -308G/A TNFα, +250A/G Ltα, +36A/G TNFR1 и прогнозируют:
- повышенный риск развития гипертонической болезни у индивидуумов русской национальности, являющихся уроженцами Центрального Черноземья РФ, имеющих наследственную отягощенность в случае выявления сочетания аллеля -308A TNFα с аллелем +36G TNFR1;
- низкий риск развития гипертонической болезни у индивидуумов русской национальности, являющихся уроженцами Центрального Черноземья РФ при выявлении следующих сочетаний: алелля -308G TNFα с генотипом +250AA Ltα или аллеля -308G TNFα с аллелем +250A Ltα.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗНИКНОВЕНИЯ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ | 2003 |
|
RU2257139C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ ПО ГЕНЕТИЧЕСКИМ ФАКТОРАМ РИСКА | 2005 |
|
RU2287158C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗМОЖНОСТИ РАЗВИТИЯ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ ДЛЯ КОРЕННЫХ СЕЛЬСКИХ ЖИТЕЛЕЙ-ТЕЛЕУТОВ ЮГА КУЗБАССА | 2006 |
|
RU2307577C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ВОЗНИКНОВЕНИЯ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ У МУЖЧИН | 2011 |
|
RU2456608C1 |
| Кривошей И.В / Изучение ассоциаций полиморфизма генов цитокинов со стадией гипертонической болезни / Научные ведомости | |||
| Серия медицина | |||
| Фармация | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
Авторы
Даты
2016-04-10—Публикация
2014-12-17—Подача