Настоящая заявка относится к технике формирования медицинских изображений. Она находит конкретное применение в сочетании с сегментацией медицинских изображений и будет описана с конкретной ссылкой на нее.
В медицинских изображениях сегментация является процессом, посредством которого четко идентифицируется граница между одним или более органами или тканями. Точная сегментация медицинских изображений крайне важна для многих клинических применений. Однако некоторые органы или ткани трудно отличить от прилегающих органов или тканей.
Например, в радиотерапии, предпочтительно подавать к целевому объему, например, опухоли, относительно большую дозу облучения. Но с целевыми объемами часто тесно соседствуют и даже прилегают органы высокого риска, которые могут быть повреждены высокими или даже умеренными дозами излучения. Планируя траектории пучка, важно точно знать границы целевого объема и органов риска. Неудача при попытке облучить все участки опухоли может привести к быстрому рецидиву. Облучение даже участка органа риска большими дозами, предназначенными для опухоли, может иметь неблагоприятные физические последствия для здоровья.
Для автоматизации сегментации полутоновых медицинских изображений пациента были предложены многочисленные автоматизированные технологии сегментации. Хотя эти автоматизированные технологии сегментации успешно используются во многих применениях, автоматизированная сегментация часто неосуществима из-за недостаточной информации различения, обеспечиваемой стандартными способами формирования медицинских изображений для некоторых типов ткани. Одной из автоматизированных технологий сегментации является сегментация на основе модели. В сегментации на основе модели модель или контуры номинального органа, который должен сегментироваться, извлекаются из запоминающего устройства компьютера. Признаки на поверхности органа, подлежащего сегментации, которые могут идентифицироваться, коррелируются с соответствующими признаками модели. Модель затем масштабируется, вращается, позиционируется и деформируется так, что модель накладывает изображение на идентифицируемое изображение и признаки модели и изображения непосредственно накладываются друг на друга. Области поверхности органа, которые невозможно отличить от окружающих тканей, предполагаются поверхностью, определяемой моделью, которая была подогнана к признакам изображения, которые могут быть различены. Поскольку такие предположения не всегда правильны, требуется большая достоверность точности сегментации.
Настоящая заявка описывает специализированное решение улучшения признака для конкретного органа, направленное на повышение точности сегментации медицинских изображений и, в частности, использующее способы на основе трехмерной модели.
В соответствии с одним аспектом, обеспечивается устройство сегментации медицинских изображений. В запоминающем устройстве хранится медицинское яркостное изображение (изображение интенсивностей). Один или более процессоров запрограммированы с возможностью обрабатывать яркостное изображение с помощью улучшающего фильтра, основываясь на массиве признаков, чтобы создать улучшенное изображение, которое отличает целевой объем от соседней ткани лучше, чем яркостное изображение. Улучшенное изображение сохраняется в запоминающем устройстве.
В соответствии с другим аспектом, обеспечивается способ сегментации медицинских изображений. Идентифицируется область яркостного изображения, содержащая выбранный целевой объем. Идентифицированная область яркостного изображения обрабатывается с помощью улучшающего фильтра, основываясь на массиве признаков, для создания целевого объема, отделенного от соседней ткани, чтобы создать улучшенное изображение.
Одно из преимуществ заключается в повышенной точности сегментации.
Другим преимуществом является повышенная надежность клинических применений, основанных на сегментированных изображениях.
Другим преимуществом является улучшенная охрана здоровья.
Другие дополнительные преимущества настоящего изобретения должны оценить специалисты в данной области техники после прочтения и понимания последующего подробного описания.
Изобретение может принимать форму различных компонентов и компоновок компонентов и различных этапов и компоновок этапов. Чертежи служат только для целей иллюстрирования предпочтительных вариантов осуществления и не должны рассматриваться как ограничение изобретения.
Фиг. 1 - схематическое изображение системы сегментации медицинских изображений;
Фиг. 2 - двумерное яркостное изображение для левой подчелюстной железы;
Фиг. 3 - то же самое изображение среза левой подчелюстной железы в том же самом масштабе и в том же самом положении, что и на фиг. 2, после улучшения изображения с помощью настоящей технологии;
Фиг. 4 - улучшенное изображение среза с отмеченной поверхностью или границей подчелюстной железы;
Фиг. 5 - схематическое представление технологии создания улучшающих или классифицирующих фильтров для использования с системой, показанной на фиг. 1;
Фиг. 6 - двумерный яркостный срез левой околоушной железы и окружающей биологической структуры;
Фиг. 7 - срез того же самого интересующего объема, что и на фиг. 6, в том же самом масштабе и при том же самом расположении в изображении после улучшения в соответствии с настоящей технологией; и,
Фиг. 8 - блок-схема последовательности выполнения операций способа сегментации медицинских изображений.
Как представлено на фиг. 1, система 10 формирования изображения, такая как система магнитно-резонансной томографии, сканер компьютерной томографии (СТ), сканер позитронной эмиссионной томографии (PET), сканер однофотонной эмиссионной компьютерной томографии (гамма-томографии) (SPECT), ультразвуковой сканер, рентгенографические системы, другие системы формирования изображения и их комбинации, выполняет исследование объекта. Процессор 12 реконструкции реконструирует данные, получаемые от сканера 10 формирования изображения, в яркостное или полутоновое изображение 14, которое хранится в буфере или в запоминающем устройстве 16. При СТ-сканировании, например, шкала полутонов может представить интенсивность или величину излучения, поглощенного (или проходящего) каждым вокселом. Как другой пример, в РЕТ-изображении, шкала полутонов яркостного изображения может представлять энергию или величину радиоизотопных явлений, возникающих в каждом вокселе. Запоминающее устройство 16 может находиться на рабочей станции, связанной со сканером, на центральной больничной базе данных и т.п.
Блок 20 идентификации целевого объема определяет целевой объем в яркостном или полутоновом изображении. В одном варианте осуществления блок идентификации целевого объема включает в себя видеомонитор, на котором отображаются срезы яркостного изображения, и клинический врач, используя устройство 22 интерфейса пользователя, отмечает местоположение целевого объема. В другом варианте осуществления устройство идентификации целевого объема включает в себя традиционную программу сегментации трехмерной модели, которая идентифицирует целевой объем в яркостном изображении и подгоняет к нему трехмерную модель. Блок 24 ограничения объема определяет ограниченный участок трехмерного изображения, содержащий весь целевой объем или выбранный участок, который должен быть сегментирован с помощью настоящей технологии. В одном варианте осуществления ограниченный объем определяется клиническим врачом вручную, используя интерфейс 22 пользователя. В другом варианте осуществления граница сегментации на основе модели или другой автоматизированной сегментации увеличивается в трех измерениях в достаточной степени, чтобы гарантировать получение в изображении интересующего объема или выбранного его участка. Например, автоматическая сегментация может увеличиваться на фиксированную процентную часть, например, на 25%. В другом варианте осуществления степень увеличения может быть функцией степени достоверности точности сегментации яркостного изображения.
Классификатор или блок 30 улучшения изображения работает с ограниченным объемом с использованием улучшающего или классифицирующего фильтра, извлеченного из запоминающего устройства 32 улучшающих или классифицирующих фильтров. Запоминающее устройство 32 фильтров заранее загружается соответствующими фильтрами для каждого из множества целевых объемов. Применение выбранного фильтра к ограниченному объему включает в себя классификацию каждого воксела ограниченного объема, основываясь на большом массиве признаков, в том числе, на признаках относительного положения, признаках текстуры, признаках яркости, признаках соседних вокселов и т.п. К таким признакам относится, в частности, априорная информация о форме выбранного целевого объема, структуре и относительных структурных признаках выбранного целевого объема, градиентах яркости в окружении каждого воксела, вариации и отклонения яркости и т.п. Математически, применение фильтра может включать в себя рассмотрение положения воксела, применение первой или второй производных, тензоров второго или более высоких порядков, Лапласовых преобразований, Гауссовых функций, вычисления собственных значений матриц Гессе, и использование других математических операций первого, второго и более высоких порядков. Применение фильтра приводит в результате к улучшенному изображению. В одном варианте осуществления значения вокселов улучшенного изображения более не представляют яркость, а представляют скорее вероятность, что каждый воксел классифицируется или не классифицируется как элемент целевого объема, например, вероятность, что каждый воксел находится в целевом органе или опухоли, которая должна сегментироваться.
На фиг. 2 представлен срез ограниченного объема яркостного СТ-изображения, в котором целевым объемом является левая подчелюстная железа. В примере, показанном на фиг. 2, светлая область представляет кость (повышенное поглощение излучения), а различные полутона представляют подчелюстную железу и различные окружающие ткани и органы. На фиг. 3 представлен один вариант осуществления улучшенного изображения 34 того же самого среза подчелюстной железы, где подчелюстная железа показана в том же самом положении и в том же самом масштабе, что и на фиг. 2. В улучшенном изображении шкала полутонов обозначает определяемую классификатором при применении фильтра вероятность, что каждый воксел является элементом выбранного целевого объема, причем более яркие вокселы указывают более высокие вероятности, а более темные вокселы указывают более низкую вероятность. Следует заметить, что на фиг. 3 периферия подчелюстной железы идентифицируется намного более ясно, чем на фиг. 2.
Процессор 40 сегментации сегментирует улучшенное изображение, чтобы идентифицировать внешнюю поверхность, обозначенную как 42 на фиг. 4, целевого объема. В одном варианте осуществления процессор 40 сегментации применяет автоматическую технологию сегментации, основанную, в частности, на технологии сегментации на основе модели. Процессор 40 сегментации выбирает модель из запоминающего устройства 44 моделей, соответствующую выбранному целевому объему. Процессор 40 сегментации подгоняет модель сегментации, преобразуя, вращая и масштабируя модель сегментации. Процессор сегментации может также выполнять на модели сегментации нелинейные операции, чтобы более точно подогнать ее к целевому объему, идентифицированному в улучшенном изображении. Например, алгоритм может заставить схожие точки в улучшенном изображении и модели притягиваться друг к другу. Как вариант, клинический врач может корректировать модель 42 сегментации, используя блок 46, применяющий ручные инструменты для придания формы. Дополнительно или альтернативно, блок 48 сегментации яркостного изображения применяет подогнанную модель сегментации к яркостному изображению 14, чтобы создать сегментированное яркостное изображение. Окончательное сегментированное изображение хранится в запоминающем устройстве 49, которое может быть таким, как запоминающее устройство 16, локальный буфер, запоминающее устройство рабочей станции, база данных пациентов и т.п.
Приведенные выше функции или этапы для простоты иллюстрации были описаны как выполняемые блоками. Следует понимать, что эти функции или этапы могут быть выполнены алгоритмами или программами, реализуемыми одним или более процессорами, специализированными микросхемами (ASIC), специализированными устройствами обработки и их комбинациями. Настоящая заявка дополнительно предполагает считываемый компьютером носитель данных, такой как портативное запоминающее устройство, например, диск DVD, карта памяти и т.п., которое содержит соответствующие программы программного обеспечения для программирования одного или более процессоров, чтобы выполнить описанный выше способ.
Сегментированное изображение в запоминающем устройстве изображений может быть получено из запоминающего устройства 48 видеопроцессором 50 и отображено на мониторе 52. В другом варианте осуществления сегментированное изображение из запоминающего устройства 48 получается системой 54 планирования радиотерапии, создающей план радиотерапии для лечения целевого объема с учетом других сегментированных объемов.
Хотя операция сегментации была описана как сегментация целевого объема, следует понимать, что эта технология может применяться, например, неоднократно или одновременно, чтобы сегментировать множество различных целевых объемов в реконструированном яркостном изображении 14. Например, опухоль, которая должна облучаться, может быть сегментирована, поскольку могут иметься соседствующие органы, которые должны подвергнуться облучению в меньшей степени, и должен быть создан план лучевой терапии, чтобы достаточно большое излучение доставлялось к опухоли и достаточно малое излучения доставлялось к различным окружающим органам.
На фиг. 5 представлен один вариант осуществления для создания улучшающих или классифицирующих фильтров, которые хранятся в запоминающем устройстве 32 фильтров. Многочисленные изображения сегментируются клиническим врачом, специализирующимся по сегментации, и хранятся в запоминающем устройстве 60 сегментированных тренировочных изображений. Множество признаков номинального целевого объема идентифицируются и хранятся в запоминающем устройстве 62 признаков. В идеале, десятки признаков, например, порядка ста или более, идентифицируются и хранятся. Эти признаки могут содержать априорную информацию о форме выбранного целевого объема, структуре и относительных структурных признаках выбранного целевого объема, градиентах яркости в окружении каждого воксела, вариациях яркости и отклонениях и т.п.
Тренировочный процессор 64 использует сегментированные тренировочные изображения, чтобы разработать соответствующие веса для каждого из идентифицированных признаков каждого из множества целевых объемов. Тренировочный процессор может осуществлять различные алгоритмы для идентификации признаков, используемых для классификации любого конкретного органа или целевого объема из массива мультимасштабированных текстурных, структурных и других признаков, идентифицированных посредством этапа автоматического выбора признаков из запоминающего устройства 62 признаков. В одном варианте осуществления этап выбора признаков, основанный на последовательном прямом плавающем выборе (SFFS), используется для выбора оптимального поднабора признаков для заданного целевого объема. Этот процесс включает в себя этап прямого выбора (FS), сопровождаемый этапом обратного выбора (BS). Этап FS начинается с пустого набора и постепенно добавляет признаки, пока улучшается критерий качества. Затем этап BS многократно удаляет наименее значащие признаки в соответствии с критерием качества. Этапы FS и BS могут многократно повторяться. Результат по критерию качества оценивается при каждой итерации. Прямые и обратные итерации продолжаются многократно, пока размерность пространства признака не достигнет точки, после которой улучшение становится незначительным. Блок или алгоритм 66 оптимизации определяет уровень достоверности, который должен использоваться для классификации каждого воксела. Для заданного критерия качества область под кривой рабочей характеристики приемника (ROC) максимизируется. Кривая ROC определяется, изменяя порог для каждого классификатора и затем вычерчивают график зависимости отношения ложных положительных результатов от отношения истинных положительных результатов. В одном варианте осуществления, в котором фильтр создает значение для каждого признака, который обозначает, что определяется масштабированная вероятность, что каждый воксел тренировочных изображений находится (или не находится) в интересующем объеме. Регулируя уровень вероятности, создается соответствующий порог или вес для каждого признака фильтра. Эти фильтры затем сохраняются в запоминающем устройстве 32 фильтров.
На фиг. 6 представлен срез трехмерного яркостного изображения 14′ левой околоушной железы. Фиг. 7 соответствует тому же самому срезу с тем же самым масштабом улучшенного изображения 34 околоушной железы, показанной на фиг. 6.
Когда улучшающая фильтрация закончена, улучшенное изображение может быть зарегистрировано как второе изображение. В одном варианте осуществления улучшенное изображение регистрируется как второе улучшенное изображение, в котором для вычисления критерия подобия между изображениями вместо значений тонов используются значения вероятности. Жесткое или нежесткое преобразование, которое максимизирует подобие между обоими изображениями, определяется и применяется к одному из изображений в целом, чтобы произвести регистрацию изображения.
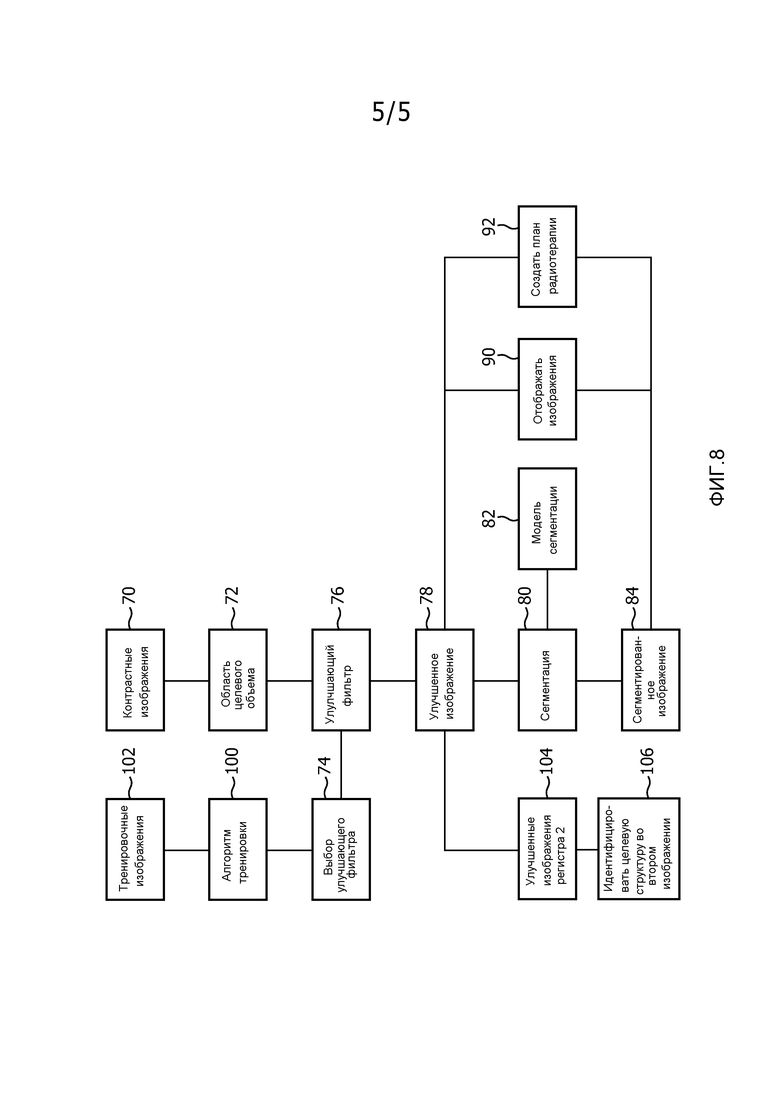
Как показано на фиг. 8, яркостное изображение создается на этапе 70. Область яркостного изображения, содержащая выбранный целевой объем, выбирается на этапе 72. На этапе 74 выбирается один из множества улучшающих фильтров, соответствующий целевому объему. На этапе 76 идентифицированная область яркостного изображения обрабатывается с помощью выбранного улучшающего фильтра, основываясь на массиве признаков, чтобы отличить выбранный целевой объем от соседней ткани для создания улучшенного изображения 78. В одном варианте осуществления улучшенное изображение является трехмерным изображением, включающим в себя трехмерную матрицу вокселов, причем значение каждого воксела представляет вероятность, что каждый воксел принадлежит целевому объему. В одном варианте осуществления идентификация области целевого объема включает в себя применение алгоритма сегментации на основе модели.
На этапе 80 улучшенное изображение сегментируется, используя процесс сегментации на основе модели, в котором модель 82 сегментации подгоняется к целевому объему улучшенного изображения, чтобы создать сегментированное изображение 84. На этапе 90, отображается улучшенное или сегментированное изображение. В этапе 92 создается план радиотерапии, исходя из улучшенного или из сегментированного изображения.
На этапе 100 тренировочный алгоритм применяется к множеству точно сегментированных тренировочных изображений 102 для создания семейства улучшающих фильтров. Каждое из тренировочных изображений имеет массив признаков, которые отличают целевой объем от других тканей. Тренировочный алгоритм включает в себя осуществление алгоритма последовательного прямого плавающего выбора, который включает в себя добавление признаков из массива признаков к тренировочному набору, чтобы выбрать поднабор признаков, применение которого повышает точность и удаление значительных признаков, способствующих снижению точности. Эти добавления и удаления признаков многократно повторяются, пока не будет достигнуто предварительно выбранное качество. На этапе 104 улучшенное изображение регистрируется как второе улучшенное изображение. На этапе 106 отличительное целевое значение используется для идентификации соответствующей структуры во втором улучшенном изображении.
Изобретение было описано со ссылкой на предпочтительные варианты осуществления.
После прочтения и понимания предшествующего подробного описания специалистами в данной области техники могут быть предложены модификации и альтернативы.
Подразумевается, что изобретение истолковывается таким образом, что оно содержит все такие изменения и альтернативы, насколько они попадают в рамки объема приложенной формулы изобретения или ее эквивалентов.




Изобретение относится к области формирования медицинских изображений. Техническим результатом является повышение точности сегментации изображений. Устройство содержит: запоминающее устройство, в котором хранится медицинское яркостное изображение, подлежащее сегментированию; один или более процессоров, запрограммированных с возможностью: применять алгоритм предварительной сегментации к яркостному изображению для оценки границы целевого объема и увеличения упомянутой оцененной границы для гарантии включения упомянутого целевого объема в упомянутую увеличенную оцененную границу; обрабатывать яркостное изображение внутри увеличенной оцененной границы с помощью улучшающего фильтра, основываясь на массиве признаков, чтобы создать улучшенное изображение, в котором целевой объем отличается от соседней ткани, улучшенное изображение является трехмерным изображением, включающим в себя трехмерную матрицу вокселов, значение каждого воксела представляет вероятность, что каждый воксел принадлежит целевому объему; запоминающее устройство для хранения улучшенного изображения. 3 н. и 4 з.п. ф-лы, 8 ил.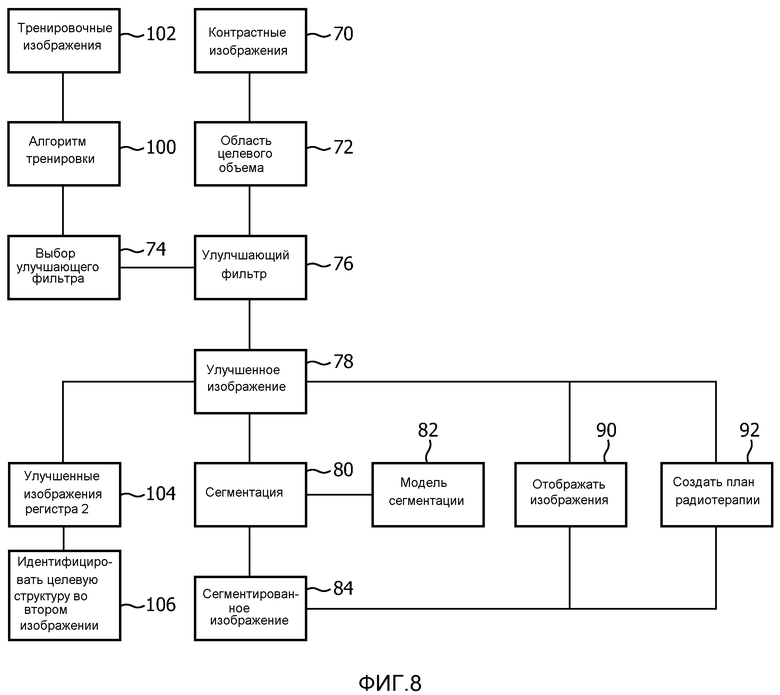
1. Устройство сегментации медицинских изображений, содержащее:
запоминающее устройство (16), в котором хранится медицинское яркостное изображение, подлежащее сегментированию;
один или более процессоров (30), запрограммированных с возможностью:
применять алгоритм предварительной сегментации к яркостному изображению для оценки границы целевого объема и увеличения упомянутой оцененной границы для гарантии включения упомянутого целевого объема в упомянутую увеличенную оцененную границу;
обрабатывать яркостное изображение внутри увеличенной оцененной границы с помощью улучшающего фильтра, основываясь на массиве признаков, чтобы создать улучшенное изображение, в котором целевой объем отличается от соседней ткани,
причем улучшенное изображение является трехмерным изображением, включающим в себя трехмерную матрицу вокселов, причем значение каждого воксела представляет вероятность, что каждый воксел принадлежит целевому объему;
запоминающее устройство (34) для хранения улучшенного изображения.
2. Устройство по п. 1, дополнительно включающее в себя:
запоминающее устройство (32) улучшающих фильтров для хранения множества улучшающих фильтров, соответствующих каждому из множества потенциальных целевых объемов.
3. Устройство по любому из пп. 1-2, дополнительно включающее в себя по меньшей мере одно из следующего:
монитор (52), который отображает улучшенное изображение;
систему (54) планирования радиотерапии, которая использует улучшенное изображение для создания плана радиотерапии;
устройство (10) формирования изображения и процессор (12) реконструкции, выполняющий обследование пациента и реконструирующий яркостное изображение из данных, созданных устройством формирования изображения.
4. Способ сегментации медицинских изображений, содержащий этапы, на которых:
идентифицируют область яркостного изображения, подлежащую сегментации, причем упомянутое изображение содержит выбранный целевой объем, при этом упомянутая идентификация включает в себя применение алгоритма предварительной сегментации к яркостному изображению для оценки границы упомянутого целевого объема и увеличения упомянутой оцененной границы для гарантии включения упомянутого целевого объема в упомянутую увеличенную оцененную границу;
обрабатывают яркостное изображение внутри увеличенной оцененной границы с помощью улучшающего фильтра, основываясь на массиве признаков для дифференциации выбранного целевого объема от соседней ткани, чтобы создать улучшенное изображение,
причем улучшенное изображение является трехмерным изображением, включающим в себя трехмерную матрицу вокселов, причем значение каждого воксела представляет вероятность, что каждый воксел принадлежит целевому объему.
5. Способ по п. 4, дополнительно включающий в себя этап, на котором:
выбирают из множества улучшающих фильтров один фильтр, соответствующий выбранному целевому объему.
6. Способ по любому из пп. 4-5, дополнительно включающий в себя по меньшей мере один из этапов, на котором:
отображают улучшенное или сегментированное изображение;
создают план радиотерапии, исходя из улучшенного или сегментированного изображения;
выполняют обследование пациента для создания данных формирования изображения и реконструируют данные формирования изображения в яркостное изображение.
7. Считываемый компьютером носитель данных, содержащий компьютерную программу, управляющую одним или более процессорами для выполнения способа по любому из пп. 4-5.
| US20050078858 A1, 14.04.2005 | |||
| US20030095715 A1, 22.05.2003 | |||
| US6246784 B1, 12.06.2001 | |||
| RU2008148845 A, 20.06.2010. |
Авторы
Даты
2016-06-20—Публикация
2011-07-25—Подача