Изобретение относится к области медицины, а именно к экспериментальной хирургии, и может быть использовано при диагностике энтеральной недостаточности при остром перитоните.
Перитонит занимает ведущее место в структуре хирургической летальности, являясь одним из наиболее тяжелых осложнений заболеваний и повреждений органов брюшной полости, представляющим собой комплекс грубых нарушений со стороны всех органов и систем организма. Основной причиной смерти больных перитонитом является эндотоксикоз. В генезе эндогенной интоксикации одну из ведущих ролей отводится кишечнику, морфо-функциональное состояние которого резко страдает при перитоните, развивается энтеральная недостаточность. Для хирургии чрезвычайно важной является оценка степени выраженности энтеральной недостаточности, поскольку на ее основе можно не только установить характер воспалительного процесса в брюшной полости, но и вовремя корригировать терапию.
Известен способ диагностики стадий энтеральной недостаточности при распространенном перитоните в эксперименте, в котором с помощью лазерной доплеровской флоуметрии на фоне модели экспериментального перитонита по изменениям гемодинамических показателей микроциркуляции тонкой кишки определяют функциональные показатели: показатель микроциркуляции 5,3±3,6 перф. единиц, вазомоции 106,0±24,3%, сосудистый тонус 471,5±60,0%, респираторные флуктуации 212,1±69,8%, пульсовые флуктуации 106,5±25,6%, реологический фактор 62,3±29,7%, индекс флаксмоций (ИФМ) 1,4±0,3% и при определении данных показателей на 1 сутки диагностируют локальную стадию энтеральной недостаточности. При значениях показателей: микроциркуляции 6,8±2,4 перф. единиц, вазомоции 183,1±43,2%, сосудистый тонус 402,3±76,4%, респираторные флуктуации 255,0±88,5%, пульсовые флуктуации 113,8±34,1%, реологический фактор 81,9±35,5%, индекс флаксмоций (ИФМ) 1,1±0,4%, полученных на 2 сутки, диагностируют дегенеративную стадию энтеральной недостаточности. При определении нижеследующих значений показателей на 3 сутки: микроциркуляции 7,3±2,9 перф. единиц, вазомоции 129,0±53,4%, сосудистый тонус 298,3±81,5%, респираторные флуктуации 285,4±85,5%, пульсовые флуктуации 132,7±36,7%, реологический фактор 91,2±20,5%, индекс флаксмоций (ИФМ) 0,7±0,2% диагностируют универсальную стадию энтеральной недостаточности (RU 2317593, МПК G09B 23/28, опубл. 20.02.2008 г.).
Недостатком известного способа является определение стадий энтеральной недостаточности только на основе нарушений микроциркуляции со стороны серозно-мышечной оболочки, что является неполным, поскольку функциональный статус кишечника (в том числе биологический барьер) в основном определен функциональным состоянием слизистой оболочки. Кроме того, известный способ не оценивает одно из важнейших проявлений энтеральной недостаточности - нарушение барьерной функции кишечника, что проявляется прорывом токсических продуктов в кровоток.
Наиболее близким по технической сущности к заявляемому решению является способ оценки энтеральной недостаточности по исследованию плазмы крови, а также перитонеального экссудата, кишечного содержимого у больных перитонитом, в которых определяют уровень содержания эндотоксина грамотрицательной микрофлоры в кишечном содержимом с помощью ЛАЛ-теста. Значения ЛАЛ-теста в плазме крови <1,0 ед/мл свидетельствуют о II стадии энгеральной дисфункции, а значения >1,0 ед/мл - III стадии. Значения ЛАЛ-теста в кишечном содержимом <8,0 ед/мл свидетельствуют о II стадии энтеральной дисфункции, а значения >8,0 ед/мл - III стадии (Миронов А.В. Синдром кишечной недостаточности при распространенном перитоните: диагностика и методы энтеральной коррекции. Автореф. дисс. … канд. мед. наук. - М., 2011).
Недостатком известного способа является возможность получения ложноположительных результатов в виде повышения содержания эндотоксина грамотрицательной микрофлоры при других воспалительных процессах, при которых этиологическим фактором может быть указанная микрофлора. Известный способ не отражает токсические продукты, образующиеся при кишечной недостаточности и отражающие степень выраженности нарушения барьерной функции кишечника, также необходимо исследовать три среды: плазма крови, перитонеальный экссудат и кишечное содержимое.
Технический результат заключается в повышении точности оценки степени тяжести синдрома энтеральной недостаточности при остром перитоните на основе оценки уровня гидрофильных, гидрофобных и амфифильных токсических продуктов в локальном и организменном кровотоках.
Сущность изобретения заключается в том, что в способе оценки энтеральной недостаточности при остром перитоните в эксперименте путем исследования крови, определяют содержание молекул средней массы и индекс токсичности плазмы по общей и эффективной концентрации альбумина в локальном и организменном кровотоках, на основе которых определяют индексы энтеральной недостаточности по формулам:

где ИЭН по МСМ - индекс энтеральной недостаточности по содержанию молекул средней массы;
MCM1 - содержание молекул средней массы в локальном кровотоке;
МСМ2 - содержание молекул средней массы в организменном кровотоке;

где ИЭН по ИТП - индекс энтеральной недостаточности по индексу токсичности плазмы;
ИТП1 - индекс токсичности плазмы в локальном кровотоке;
ИТП2 - индекс токсичности плазмы в организменном кровотоке.
Значения индекса энтеральной недостаточности по содержанию молекул средней массы менее 6,3 и индекса энтеральной недостаточности по индексу токсичности плазмы менее 8,3 показывают легкую степень энтеральной недостаточности; значения индекса энтеральной недостаточности по содержанию молекул средней массы от 6,4 до 24,7 и индекса энтеральной недостаточности по индексу токсичности плазмы от 8,4 до 36,4 - среднюю степень энтеральной недостаточности; значения индекса энтеральной недостаточности по содержанию молекул средней массы более 24,8 и индекса энтеральной недостаточности по индексу токсичности плазмы более 36,5 - тяжелую степень энтеральной недостаточности.
Новизна предлагаемого способа заключается в следующем.
1. Впервые проводится оценка уровня токсических продуктов в плазме крови в организменном и локальном кровотоках в ближайшие сроки послеоперационного периода, что позволяет точно определить «вклад» кишечника в эндогенное насыщение организма токсическими продуктами.
2. Выраженность эндогенной интоксикации в оттекающей от кишечника крови определяется фактически по всему спектру токсических продуктов: гидрофильной природы (по содержанию молекул средней массы); гидрофобной и амфифильной природы (по насыщенности лигандов молекул альбумина токсинами), что позволяет наиболее полно и качественно определить выраженность энтеральной недостаточности.
3. Способ позволяет точно установить степень энтеральной недостаточности по количественным показателям уровня токсических продуктов в организменном и локальном кровотоках в сравнительном аспекте.
Способ осуществляют следующим образом. Производят определение содержания молекул средней массы, общей и эффективной концентрации альбумина в венозной крови в локальном кровотоке (брыжеечные вены) и в венозной крови в организменном кровотоке (краниальная полая вена) в течение раннего послеоперационного периода. При остром перитоните большое внимание уделяется развитию эндогенной интоксикации, которая может приводить к полиорганной недостаточности и смерти больного. Своевременная диагностика и установление роли кишечной недостаточности в интоксикационном процессе при остром перитоните весьма значимы для назначения адекватной терапии по ее быстрой и адекватной коррекции. Указанный объем исследований позволяет оценивать степень выраженности энтеральной недостаточности и своевременно назначить повторные операции.
Определение молекул средней массы (МСМ). Сыворотку крови смешивают с 10% раствором трихлоруксусной кислоты в соотношении 1:2, центрифугировают 30 мин при скорости 3000 g. Затем 0,5 мл супернатанта смешивают с 4,5 мл дистиллированной воды и измеряют оптическую плотность на спектрофотометре СФ-46 при длине волны 254 нм. Результат выражают в условных единицах (Пикуза О.И., Шакирова Л.3., 1994).
Определение общей (ОКА) и эффективной концентрации альбумина (ЭКА) проводили по методике Грызунова Ю.А. и Добрецова Г.Е. (1994) на специализированном анализаторе АКЛ-01 «Зонд». Использовали набор реактивов «Зонд-Альбумин» (г. Москва) в соответствии с прилагаемыми инструкциями. Рассчитывали: индекс токсичности плазмы (ИТП), отражающий степень заполнения тканевых центров различными токсическими веществами, который определяли по формуле: ИТПКЖА/ЭКА-1.
На основе данных содержания молекул средней массы (МСМ), общей (ОКА) и эффективной концентрации альбумина (ЭКА) в локальном кровотоке (брыжеечные вены) и организменном кровотоке (краниальная полая вена) рассчитывают:
1) индекс энтеральной недостаточности по содержанию молекул средней массы (ИЭН по МСМ):
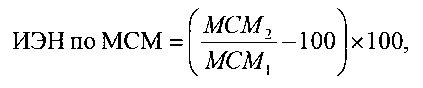
где МСМ1 - содержание молекул средней массы в локальном кровотоке;
МСМ2 - содержание молекул средней массы в организменном кровотоке;
2) индекс энтеральной недостаточности по индексу токсичности плазмы (ИЭН по ИТП);

где ИТП1 - индекс токсичности плазмы в локальном кровотоке;
ИТП2 - индекс токсичности плазмы в организменном кровотоке,
Значения индекса энтеральной недостаточности по содержанию молекул средней массы менее 6,3 и индекса энтеральной недостаточности по индексу токсичности плазмы менее 8,3 предполагают легкую степень энтеральной недостаточности (табл. 1).
Значения индекса энтеральной недостаточности по содержанию молекул средней массы от 6,4 до 24,7 и индекса энтеральной недостаточности по индексу токсичности плазмы от 8,4 до 36,4 предполагают среднюю степень энтеральной недостаточности, что является основанием для коррекции терапии, в том числе энтеропротекторного действия (табл. 2).
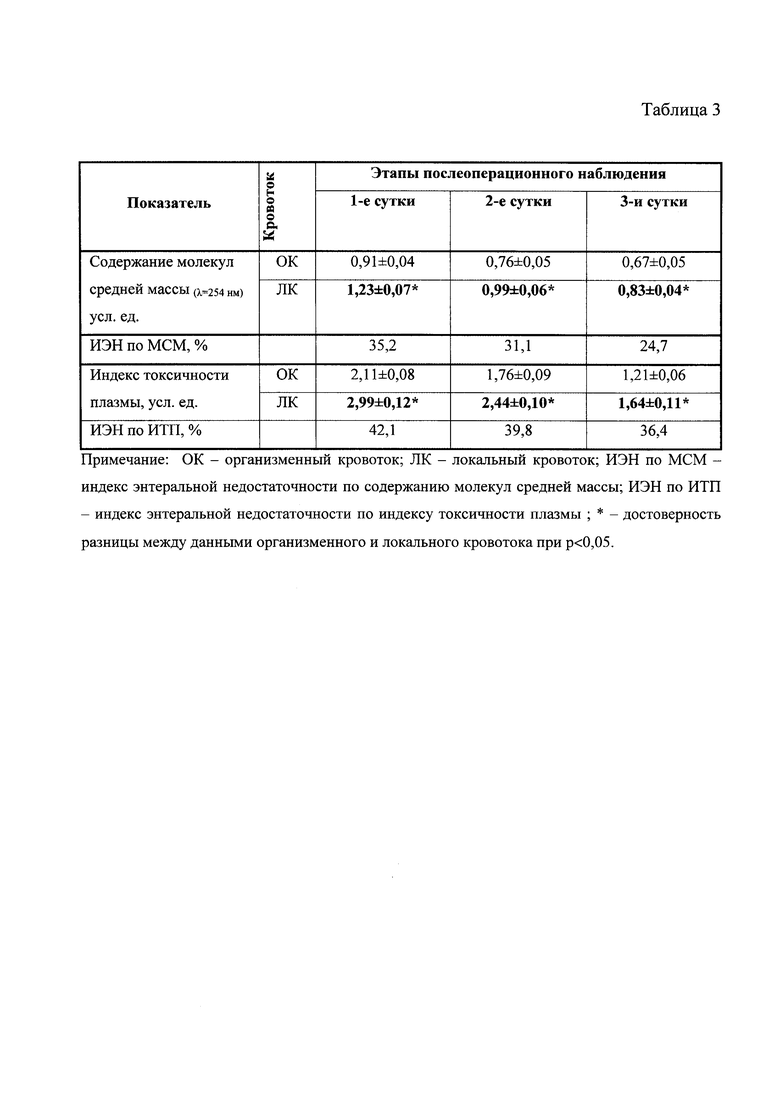
Значения индекса энтеральной недостаточности по содержанию молекул средней массы более 24,8 и индекса энтеральной недостаточности по индексу токсичности плазмы более 36,5 предполагают тяжелую степень энтеральной недостаточности, что является основанием для проведения повторных операций (табл. 3).
Определение индекса энтеральной недостаточности при остром перитоните в эксперименте позволяет судить о направленности (прогрессирование или купирование) течения синдрома энтеральной недостаточности и оценивать эффективность оперативного лечения острого перитонита, а также действия дезинтоксикационной и эфферентной терапии.
Апробация способа проведена на 36 взрослых беспородных половозрелых собаках, которым под тиопентал-натриевым наркозом (0,04 г/кг массы) моделировали перитонит путем введения в брюшную полость 20% каловой взвеси из расчета 0,5 мл/кг массы животного. Через 12 ч (первая группа), 24 ч (вторая группа) или 48 ч (третья группа) выполняли лапаротомию, санацию брюшной полости, шов лапаротомной раны. В контрольные сроки (1, 2 и 3-е суток) животным выполняли релапаротомию, забор крови общего (из краниальной полой вены) и локального (из брыжеечных вен) кровотока. В послеоперационном периоде животным проводилась антибактериальная (внутримышечные инъекции 2 раза в сутки раствора гентамицина из расчета 0,8 мг/кг массы тела) и инфузионная (внутривенные введения 5% раствора глюкозы и 0,89% раствора хлорида натрия из расчета 50 мл/кг массы животного) терапия.
Исследования проведены в соответствии с этическими требованиями к работе с экспериментальными животными («Правила проведения работ с использованием экспериментальных животных» (приказ МЗ СССР №755 от 12.08.1987 г.), Федеральный закон «О защите животных от жестокого обращения» от 01.01.1997 г., «Об утверждении правил лабораторной практики» (приказ МЗ РФ от 19.06.2003 г. №267), и одобрены локальным этическим комитетом.
Результаты исследования в первой группе. Через 12 ч после моделирования у животных возникал диффузный серозный перитонит. Ранний послеоперационный период после санации брюшной полости протекал гладко. Летальных исходов не было. При релапоротомии выявлена быстрая регрессия воспалительного процесса брюшной полости. Результаты динамики показателей эндогенной интоксикации представлены в табл. 1.
Результаты исследования во второй группе. Через 24 ч после моделирования у животных возникал распространенный серозно-гнойный перитонит. Ранний послеоперационный период после санации брюшной полости протекал по-разному. При релапоротомии у 9 животных выявлена регрессия воспалительного процесса брюшной полости, у 3 животных - сохранение или прогрессирование острого перитонита. 2 животных в последующем погибли от прогрессирующего перитонита. Результаты динамики показателей эндогенной интоксикации представлены в табл.2.
Результаты исследования в третьей группе. Через 48 ч после моделирования у животных возникал распространенный гнойно-фибринозный перитонит. Отмечены выраженные воспалительные явления со стороны кишечника. Ранний послеоперационный период после санации брюшной полости протекал тяжело. При релапоротомии у 8 животных выявлено прогрессирование воспалительного процесса брюшной полости, у 4 животных - сохранение или уменьшение воспалительного процесса. 6 животных в последующем погибли от прогрессирующего перитонита. Результаты динамики показателей эндогенной интоксикации представлены в табл. 3.
Результаты экспериментальных исследований подтвердили развитие энтеральной недостаточности при остром перитоните и об этом в первую очередь свидетельствует сравнительно больший уровень токсических продуктов гидрофильной, гидрофобной и амфифильной природы в оттекающей от кишечника крови, по сравнению с организменном кровотоком. Получены доказательства, что течение (прогрессирование) воспалительного процесса сопряжено с энтеральной недостаточностью, которую впервые удалось определить количественно.
По сравнению с известным решением предлагаемый способ позволяет повысить точность прогнозирования энтеральной недостаточности при остром перитоните на основе оценки уровня токсических продуктов гидрофильной, гидрофобной и амфифильной природы в локальном и организменном кровотоках, что позволяет своевременно принять меры по коррекции терапии (в том числе проведение повторных операций).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭНТЕРАЛЬНОЙ НЕДОСТАТОЧНОСТИ ПРИ ОСТРОМ ПЕРИТОНИТЕ В ЭКСПЕРИМЕНТЕ | 2015 |
|
RU2580664C1 |
| Способ оценки тяжести перитонита | 2017 |
|
RU2664419C1 |
| Способ оценки поражения кишечника при остром перитоните | 2022 |
|
RU2784413C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ У БОЛЬНЫХ ОСТРЫМ ПЕРИТОНИТОМ | 2014 |
|
RU2581024C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОСТРОЙ ПОЧЕЧНО-ПЕЧЕНОЧНОЙ НЕДОСТАТОЧНОСТИ | 2017 |
|
RU2657825C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ГЕПАТОРЕНАЛЬНОГО СИНДРОМА ПРИ ОСТРОЙ АБДОМИНАЛЬНОЙ ХИРУРГИЧЕСКОЙ ПАТОЛОГИИ | 2010 |
|
RU2431840C1 |
| Способ прогнозирования энтеральной недостаточности при перитоните | 2022 |
|
RU2790193C1 |
| Способ оценки течения раннего послеоперационного периода у больных ургентными болезнями живота | 2020 |
|
RU2729730C1 |
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ ПРИ НЕОТЛОЖНОЙ АБДОМИНАЛЬНОЙ ПАТОЛОГИИ В РАННЕМ ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ | 2006 |
|
RU2331882C1 |
| СПОСОБ ВЫБОРА ЭНТЕРАЛЬНОЙ ДЕТОКСИКАЦИИ ПРИ РАСПРОСТРАНЕННОМ ПЕРИТОНИТЕ | 2003 |
|
RU2241227C1 |

Изобретение относится к области медицины, а именно к экспериментальной хирургии, и может быть использовано для оценки энтеральной недостаточности при остром перитоните. Способ заключается в определении содержание молекул средней массы и индекса токсичности плазмы по общей и эффективной концентрации альбумина в локальном и организменном кровотоках, на основе которых определяют индексы энтеральной недостаточности по уровню молекул средней массы (ИЭН по МСМ) и по индексу токсичности плазмы (ИЭН по ИТП) по формулам. Значения индекса энтеральной недостаточности по содержанию молекул средней массы менее 6,3 и индекса энтеральной недостаточности по индексу токсичности плазмы менее 8,3 показывают легкую степень энтеральной недостаточности; значения индекса энтеральной недостаточности по содержанию молекул средней массы от 6,4 до 24,7 и индекса энтеральной недостаточности по индексу токсичности плазмы от 8,4 до 36,4 - среднюю степень энтеральной недостаточности; значения индекса энтеральной недостаточности по содержанию молекул средней массы более 24,8 и индекса энтеральной недостаточности по индексу токсичности плазмы более 36,5 - тяжелую степень энтеральной недостаточности. 3 табл.
Способ оценки энтеральной недостаточности при остром перитоните в эксперименте путем исследования плазмы крови, отличающийся тем, что определяют содержание молекул средней массы и индекс токсичности плазмы по общей и эффективной концентрации альбумина в локальном и организменном кровотоках, на основе которых определяют индексы энтеральной недостаточности по формулам:
 ,
,
где ИЭН по МСМ - индекс энтеральной недостаточности по уровню молекул средней массы;
MCM1 - содержание молекул средней массы в локальном кровотоке;
МСМ2 - содержание молекул средней массы в организменном кровотоке;
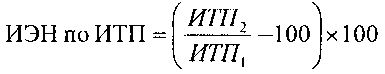 ,
,
где ИЭН по ИТП - индекс энтеральной недостаточности по индексу токсичности плазмы;
ИТП1 - индекс токсичности плазмы в локальном кровотоке;
ИТП2 - индекс токсичности плазмы в организменном кровотоке,
при этом значения индекса энтеральной недостаточности по содержанию молекул средней массы менее 6,3 и индекса энтеральной недостаточности по индексу токсичности плазмы менее 8,3 показывают легкую степень энтеральной недостаточности; значения индекса энтеральной недостаточности по содержанию молекул средней массы от 6,4 до 24,7 и индекса энтеральной недостаточности по индексу токсичности плазмы от 8,4 до 36,4 - среднюю степень энтеральной недостаточности; значения индекса энтеральной недостаточности по содержанию молекул средней массы более 24,8 и индекса энтеральной недостаточности по индексу токсичности плазмы более 36,5 - тяжелую степень энтеральной недостаточности.
| Шибитов В.А и др | |||
| / Патогенетические основы энтеральной недостаточности / Фундаментальные исследования, N4, 2012 | |||
| Волков Д.В / Клинико-экспериментальное обоснование лечения энтеральной недостаточности / Диссертация на соискание ученой степени доктора медицинских наук, Оренбург - 2014 | |||
| В.А | |||
| Шибитов и др | |||
| / Патогенетическое обоснование схем коррекции |
Авторы
Даты
2016-07-10—Публикация
2015-03-10—Подача