ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к конъюгатам антитело-лекарственное средство (ADC), в которых линкерное лекарственное средство сайт-специфичным образом конъюгировано с антителом через встроенный цистеин, и их применению в лечении солидных человеческих опухолей и гематологических злокачественных образований, в частности рака груди, рака желудка, рака ободочной и прямой кишки, рака уротелия, рака яичников, рака матки, рака легких, мезотелиомы, рака печени, рака поджелудочной железы, рака простаты и лейкемии.
УРОВЕНЬ ТЕХНИКИ
Конъюгаты антитело-лекарственное средство (ADC) являются развивающимся классом направленной терапии, имеющей улучшенный терапевтический индекс по сравнению с традиционной химиотерапией. Лекарственные средства и линкеры являлись центральными элементами разработки ADC, в дополнение к (моноклональному) антителу (mAb) и выбору мишени. Однако недавно была осознана важность гомогенности конъюгата. Обычные способы для прикрепления лекарственного средства к антителу приводят к разнородной смеси, и некоторые индивидуальные компоненты этой смеси могут иметь плохую работоспособность in vivo. Более новые способы для сайт-специфичного прикрепления лекарственного средства приводят к более гомогенным конъюгатам и позволяют контролировать сайт прикрепления лекарственного средства. Эти небольшие улучшения могут оказывать сильное воздействие на in vivo эффективность и/или in vivo безопасность, и, таким образом, на терапевтический индекс. Способы для сайт-специфичной конъюгации лекарственного средства с антителами всесторонне рассматриваются в обзоре C.R. Behrens и B. Liu в mAbs, Vol. 6, Issue 1, 2014.
Обычные ADC обычно продуцируют посредством конъюгации линкерного лекарственного средства с антителом через боковые цепи или находящиеся на поверхности лизины или свободные цистеины, полученные путем восстановления межцепочечных дисульфидных связей. Поскольку антитела содержат множество остатков лизина и дисульфидных связей цистеина, то обычная конъюгация обычно продуцирует гетерогенные смеси, которые представляют проблемы в отношении аналитической характеризации и производства. Кроме того, отдельные компоненты этих смесей демонстрируют различные физико-химические свойства и фармакологию в отношении их профилей фармакокинетики, эффективности и безопасности, препятствуя рациональному подходу к оптимизации этой процедуры.
Эти две обычных методики для химической модификации антител применялись для конструирования двух ADC с имеющимися в настоящий момент маркетинговыми разрешениями FDA. Брентуксимаб ведотин (Адцетрис™, Seattle Genetics) состоит из моноклонального антитела против CD30, конъюгированного с обладающим высокой цитотоксичностью лекарственным средством монометил ауристатином E (ММAE) через модификацию естественных тиолов боковой цепи цистеина. Производство включает в себя частичное восстановление подвергнутых воздействию растворителя межцепочечных дисульфидов, после которого проводится модификация полученных в результате тиолов с помощью содержащих малеимид линкерных лекарственных средств. Для брентуксимаб ведотина тиолы были изменены с помощью mc-vc-PAB-ММAE, который содержит сайт расщепления протеазы катепсина B (vc, валин-цитруллин) и саморасщепляющийся линкер (PAB, пара-аминобензилоксикарбонил) между малеимидной группой (mc, малеимидокапроил) и цитотоксическим средством (ММAE). Стратегия прикрепления цистеина дает максимум два лекарственных средства на восстановленный дисульфид. Большинство человеческих молекул IgG имеют четыре подвергаемых воздействию растворителя дисульфидных связи, и, таким образом, возможным является диапазон от ноля до восьми лекарственных средств на антитело. Точное число лекарственных средств на антитело определяется степенью восстановления дисульфидов и числом молярных эквивалентов линкерного лекарственного средства, используемого в последующей реакции конъюгации. Полное восстановление всех четырех дисульфидных связей дает гомогенную конструкцию с восемью лекарственными средствами на антитело, тогда как частичное восстановление обычно дает разнородную смесь с нолем, двумя, четырьмя, шестью или восемью лекарственными средствами на антитело. Брентуксимаб ведотин имеет в среднем около четырех лекарственных средств на антитело.
Другим ADC, имеющим текущее разрешение FDA, является адо-трастузумаб эмтанзин (T-DM1, кадцила™, Roche/Genentech), который был сконструирован путем соединения моноклонального антитела трастузумаба против HER2 с цитотоксическим лекарственным средством майтансином посредством модификации аминов боковой цепи лизина. Эта версия майтансина (DM1) была модифицирована с включением тиола, который может быть присоединен к малеимидному линкеру. Бифункциональный линкер (SMCC, сукцинимидил 4-(N-малеимидометил) циклогексан-1-карбоксилат) с малеимидом на одном из концов и сложным эфиром N гидроксисукцинимидила (NHS) на другом конце реагировал с боковыми цепями первичного амина лизина с формированием стабильной амидной связи. Модифицированный майтансин (DM1) затем был присоединен к антителу через конъюгацию с малеимидным концом бифункционального линкера. В отличие от линкера, используемого в брентуксимаб ведотине, этот линкер не имеет какого-либо (протеазного) сайта расщепления, и, таким образом, требует лизосомального разложения части антитела ADC для высвобождения активного метаболита DM1-линкер-лизин. Способ присоединения приводил к образованию гетерогенной смеси конъюгатов со средним количеством 3,5 лекарственных средств на антитело. По сравнению с цистеиновым способом, описанным выше, эта стратегия давала более гетерогенную смесь, поскольку была обнаружена модификация от 20 до 40 остатков лизина, тогда как только максимально 8 различных остатков цистеина модифицируется с применением способа модификации нативного цистеина.
Недавно сообщалось о том, что фармакологический профиль ADC может быть улучшен посредством применения технологий сайт-специфичной конъюгации, в которых используются находящиеся на поверхности остатки цистеина, сконструированные в антителах, которые затем конъюгируют с линкерным лекарственным средством, в результате чего получают конъюгированные сайт-специфичным образом ADC с заданными отношениями лекарственного средства к антителу (DAR). По сравнению с гетерогенными смесями, создаваемыми с использованием обычных технологий конъюгации лизина и цистеина, конъюгированные сайт-специфичным образом ADC обычно демонстрировали, по меньшей мере, эквивалентную активность in vivo, улучшенную фармакокинетику и расширенное терапевтическое окно.
Первый сайт-специфичный подход к конъюгации был разработан в Genentech посредством внедрения остатка цистеина с применением сайт-направленного мутагенеза в позициях, демонстрирующих высокую тиоловую реакционную способность, в соответствии с разработанным в WO 2006/034488. Эта обычная практика в белковой модификации была более сложной для антитела вследствие присутствия различных нативных остатков цистеина. Введение дополнительного остатка цистеина в неподходящей позиции могло бы привести к неправильному формированию межцепочечных дисульфидных связей, и, следовательно, к неправильному сворачиванию антитела. Встроенные остатки цистеина в подходящих позициях в подвергнутом мутации антителе часто покрываются другими тиолами, такими как цистеин или глутатион, с целью формирования дисульфидов.
Прикрепление лекарственного средства к остаткам мутанта было достигнуто путем восстановления как нативных межцепочечных, так и мутантных дисульфидов и последующего повторного окисления цистеинов с применением мягкого окислителя, такого как CuSO4 или дигидроаскорбиновая кислота, после чего проводилась стандартная конъюгация освобожденного мутантного цистеина с линкерным лекарственным средством. При оптимальных условиях будет прикреплено два лекарственных средства на антитело (если один цистеин будет искусственно встроен в тяжелую цепь или легкую цепь mAb). Способ с использованием встроенного цистеина оказался подходящим для разработки сайт-специфичного ADC SGN-CD33A (Seattle Genetics), который недавно вошел в клиническое исследование с увеличением дозы фазы I для лечения острой миелоидной лейкемии (AML), а также в клиническое исследование фазы 1b в комбинации со стандартной поддерживающей химиотерапией, включающей цитарабин и даунорубицин. Этот ADC содержит расщепляемый дипептидный линкер (то есть, валин-аланин) и перекрестно сшитый с ДНК пирролобензодиазепиновый (PBD) димер в качестве лекарственного средства, соединенного с позицией S239C тяжелой цепи в части Fc IgG1 mAb h2H12 (DAR 1.9; Sutherland et al. Blood 2013; 122(8):1455-1463).
В свою очередь, в WO 2006/034488 специфически поверхностно доступные остатки валина, аланина и серина, не участвующие во взаимодействиях для связывания антигена и удаленные от существующих межцепочечных дисульфидных связей, были замещены с целью получения встроенных остатков цистеина с высокой тиоловой реакционной способностью, а WO 2014/124316 компании Novartis специфично сосредотачивается на идентификации поверхностно доступных сайтов в константных областях тяжелой и легкой цепей антитела, в которых замена сайтов на остаток цистеина позволяет осуществлять эффективную конъюгацию полезных нагрузок и обеспечивает высокую стабильность конъюгатов.
В дополнение к стратегии конъюгации на основе встраиваемых цистеинов были разработаны другие способы для сайт-специфичного прикрепления лекарственных средств. Pfizer продемонстрировал новую методику для конъюгации с применением микробной трансглутаминазы для присоединения содержащего амины лекарственного средства к встроенному глютамину на антителе. Трансглутаминаза представляет собой фермент, который катализирует формирование амидной связи между ацильной группой боковой цепи глутамина и первичным амином боковой цепи лизина.
В дополнение к ферментативной конъюгации, ортогональная химическая конъюгация также применялась для сайт-специфичной модификации множества разнообразных белков с использованием неприродных аминокислот (в частности, технологии от Ambrx и Sutro Biopharma). В частности, p-ацетилфенил аланин и p-азидометил-L-фенилаланин были выбраны в качестве неприродных аминокислот, поскольку они содержат, соответственно, кетон и функциональную группу азида, которые не присутствуют ни в одной из боковых цепей 20 природных аминокислот. Это позволяет осуществлять специфичную модификацию кетона и азидных групп без помех от других аминокислот. Этот способ предоставил дополнительный путь для конструирования ADC с максимум двумя лекарственными средствами на антитело (на одну такую неприродную аминокислоту).
Во всех способах уровня техники, раскрытых до настоящего времени, акцент делался на сайт-специфичной конъюгации линкерных лекарственных средств в позициях на поверхности /подвергающихся воздействию растворителя, в позициях, демонстрирующих высокую тиоловую реакционную способность, и в позициях специфично в константных областях моноклональных антител, в целях повышения гомогенности и улучшения фармакокинетических свойств. Даже при том, что вышеописанные стандартные способы конъюгации на основе лизина и цистеина позволили получить одобренные FDA конъюгаты антитела-лекарственного средства, и они применяются для конструирования большинства из большого числа ADC, находящихся в настоящий момент в преклинических и клинических испытаниях, все еще существует потребность в новых стратегиях конъюгации с целью (дальнейшего) улучшения физико-химических, фармакокинетических, фармакологических и/или токсикологических свойств ADC для получения ADC, обладающих приемлемыми свойствами связывания антигена, эффективностью in vivo, терапевтическим индексом и/или стабильностью.
КРАТКОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к конъюгатам антитело-лекарственное средство (ADC), в которых линкерное лекарственное средство сайт-специфичным образом конъюгирован с антителом через встроенный цистеин, и их применению в лечении солидных человеческих опухолей и гематологических злокачественных образований, в частности, рака груди, рака желудка, рака ободочной и прямой кишки, рака уротелия, рака яичников, рака матки, рака легких, мезотелиомы, рака печени, рака поджелудочной железы, рака простаты и лейкемии.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1A. Идентификация подходящих позиций конъюгации линкерного лекарственного средства в части Fab антитела.
Фиг. 1B. Прикрепление линкерного лекарственного средства дуокармицина vc-seco-DUBA в Fab полости антитела (наложение множества докингов vc-seco-DUBA).
Фиг. 1C. Идентификация подходящих позиций конъюгации линкерного лекарственного средства в части Fc антитела.
Фиг. 1D. Прикрепление линкерного лекарственного средства дуокармицина vc-seco-DUBA в полости Fc антитела (наложение множества докингов vc-seco-DUBA).
Фиг. 2A. In vivo эффективность ADC (SYD1091) антитела против PSMA со встроенным цистеином (VH S41C) в сравнении с контрольным наполнителем, компартором ADC (SYD1035) антитела против PSMA со встроенным цистеином (CH T120C) и ADC (SYD998) с неизмененным антителом против PSMA wt (дикий тип), в концентрации 2 мг/кг каждый.
Фиг. 2B. In vivo эффективность ADC (SYD1091) антитела против PSMA со встроенным цистеином (VH S41C) в сравнении с контрольным наполнителем, компартором ADC (SYD1035) антитела против PSMA со встроенным цистеином (CH T120C) и ADC (SYD998) с неизмененным антителом против PSMA wt, в концентрации 10 мг/кг каждый.
Фиг. 3. Влияние на массу тела ADC (SYD1091) антитела против PSMA со встроенным цистеином (VH S41C) в сравнении с контрольным наполнителем, компартором ADC (SYD1035) антитела против PSMA со встроенным цистеином (CH T120C) и ADC (SYD998) с неизмененным антителом против PSMA wt, в концентрации 10 мг/кг каждый.
Фиг. 4A. In vivo эффективность ADC H8 (H8-41C-vc-seco-DUBA) антитела против 5T4 со встроенным цистеином (VH P41C) в сравнении с контрольным наполнителем и ADC H8 (H8-vc-seco-DUBA) с неизмененным антителом против 5T4 wt, в концентрации 3 мг/кг каждый.
Фиг.4В. In vivo эффективность ADC H8 (H8-41C-vc-seco-DUBA) антитела против 5T4 со встроенным цистеином (VH P41C) в сравнении с контрольным наполнителем и ADC H8 (H8-vc-seco-DUBA) с неизмененным антителом против 5T4 wt, в концентрации 10 мг/кг каждый.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Конъюгаты антитело-лекарственное средство (ADC) развиваются в качестве нового класса противораковой терапии, который комбинирует эффективность терапии малыми молекулами с возможностью нацеливания, обеспечиваемой антителами. Путем объединения этих двух компонентов в одну молекулярную сущность обладающие очень высокой цитотоксичностью низкомолекулярные лекарственные средства могут быть доставлены к раковым тканям-мишеням, посредством чего повышается эффективность при одновременном снижении потенциальных системных токсических побочных эффектов малых молекул.
Антитела были конъюгированы со множеством цитотоксических лекарственных средств, включая малые молекулы, которые связывают ДНК (например, антрациклины), алкилируют или сшивают ДНК (например, дуокармицины или димеры пирролобензодиазепина, соответственно), вызывают разрывы нити ДНК (например, калихеамицины) или разрывают микротрубки (например, майтанзиноиды и ауристатины).
Настоящее изобретение относится к соединению конъюгата антитело-лекарственное средство (ADC), в котором линкерное лекарственное средство сайт-специфичным образом конъюгирован с антителом через встроенный цистеин в одной или более позициях указанного антитела, выбранных из 40, 41, 89 (нумерация Kabat), 152, 153, 155, 171, 247, 297, 339, 375 и 376 (нумерация Eu) тяжелой цепи, и 40, 41 (нумерация Kabat), 165 и 168 (нумерация Eu) легкой цепи.
В одном из вариантов осуществления настоящее изобретение относится к соединению конъюгата антитело-лекарственное средство (ADC), в котором линкерное лекарственное средство сайт-специфичным образом конъюгирован с антителом через встроенный цистеин в одной или более позициях указанного антитела, выбранных из 40, 41, 89, 152, 153, 155, 171, 247, 297, 339 и 375 тяжелой цепи, и 40, 41, и 165 легкой цепи.
В особенно предпочтительном варианте осуществления настоящее изобретение относится к соединению конъюгата антитело-лекарственное средство, в котором линкерное лекарственное средство сайт-специфичным образом конъюгирован с антителом через встроенный цистеин в одной или более позициях указанного антитела, выбранных из 40, 41 и 89 (согласно нумерации Kabat) тяжелой цепи и 40 и 41 (согласно нумерации Kabat) легкой цепи.
Поскольку более ранняя работа над сайт-специфичными ADC была сосредоточена на нахождении позиций конъюгации, которые демонстрируют хорошую реакционную способность с линкерным лекарственным средством и одновременно имеют низкий риск формирования дисульфидных связей между антителами (приводящих к агрегации) или нарушения структуры антитела (так называемой перестановки дисульфидной связи), то влияние на гидрофобность конъюгатов в отношении сайта конъюгации не оценивалось. Кроме того, фокус прежде всего был сделан на нахождении подходящих сайтов в константных областях антитела, поскольку модификация вариабельных областей антитела, как обычно считается, связана с высоким риском частичной или полной потери связывания антигена.
Изобретатели по настоящему изобретению, однако, сосредоточились на влиянии характеристик гидрофобности на сайт-специфичные ADC.
Способ in silico, в котором используется пакет программного обеспечения YASARA (www.yasara.org, см.: Krieger и соавт. Proteins 2009; 77 Suppl 9: 114-122), применялся для идентификации сайтов сильного взаимодействия линкерного лекарственного средства с антителом. Подходящие местоположения демонстрируют минимальное увеличение гидрофобной поверхности. Вблизи идентифицированных таким образом сайтов взаимодействия были идентифицированы подходящие остатки (то есть, с достаточной доступностью) для преобразования в цистеины. В этом подходе отсутствует ограничение в отношении константных областей антитела, и также рассматривались аминокислоты из вариабельной области, если они не находились вблизи сайтов связывания антигена. Местоположения в вариабельном домене части Fab, как оказалось, являлись предпочтительными.
Прикрепление линкерных лекарственных средств к моделям Fab и Fc различных антител моделировалось с помощью обычно используемого алгоритма VINA (Trott O and Olson AJ. J. Comput. Chem. 2010; 31: 455-461), реализованного в YASARA. Используемые модели Fab и Fc антител были получены из рентгеновских структур или посредством гомологичного моделирования с применением YASARA.
Было показано, что линкерные лекарственные средства типа дуокармицина, например, vc-seco-DUBA (то есть, SYD980; его соединение ADC изображено в формуле II) имеют сильное предпочтение в отношении связывания в полостях, которые присутствуют во всех структурах антител (см. фиг. 1B и 1D для частей Fab и Fc антитела, соответственно). Множественные подходящие позиции конъюгации для прикрепления линкерного лекарственного средства были идентифицированы в этих полостях и в непосредственной близости от них, то есть, с хорошей доступностью встроенных цистеинов в этих местоположениях (см. фиг. 1A и 1C для частей Fab и Fc антитела, соответственно).
В контексте настоящего изобретения нумерация Kabat используется для указания положений аминокислот встроенных цистеинов в тяжелой цепи (HC) и легкой цепи (LC) вариабельных областей, и нумерация Eu используется для указания положений в константных областях тяжелой цепи и легкой цепи антитела. Ввиду вариабельности последовательности в вариабельных областях антител точная аминокислота, которая будет замещена цистеином, может отличаться для различных антител. Для большинства антител, в частности, антител IgG, в тяжелой цепи вариабельной области (VH) обычно присутствует A или S в позиции 40, P в позиции 41 и V в позиции 89, и в легкой цепи вариабельной области (VL) обычно присутствует P в позиции 40 и G в позиции 41. В тяжелой цепи константных областей (CH1, CH2 и CH3) обычно присутствует E в позиции 152, P в позиции 153, T в позиции 155, P в позиции 171, P в позиции 247, N в позиции 297, A в позиции 339, S в позиции 375 и D в позиции 376, и в легкой цепи κ константной области (CL) обычно присутствует E в позиции 165 и S в позиции 168. В пяти константных областях изотипа λ легкой цепи (CL) обычно присутствует S в позиции 165 и S в позиции 168.
Выражение «нумерация Kabat» обозначает систему нумерации, используемую для вариабельных доменов тяжелой цепи или вариабельных доменов легкой цепи компиляции антител в Kabat, E.A. et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD. (1991). При использовании этой системы нумерации фактическая линейная последовательность аминокислот может содержать меньше аминокислот или может содержать дополнительные аминокислоты, соответствующие укорачиванию или вставке в каркасную область (FR) или определяющую комплементарность область (CDR) вариабельного домена. Нумерация Kabat для остатков может быть определена для заданного антитела с помощью выравнивания в областях гомологии последовательности антитела со «стандартной» пронумерованной по Kabat последовательностью.
Выражение «нумерация Eu» обозначает индекс Eu в соответствии с Kabat, E.A. et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD., NIH publication no. 91-3242, pp. 662, 680, 689 (1991). «Индекс Eu как в Kabat» обозначает нумерацию остатков человеческого антитела IgG1 Eu (Edelman, G.M. et al., Proc. Natl. Acad. Sci. USA, 63, 78-85 (1969)).
Позиции тяжелой цепи 40, 41 и 89 располагаются в вариабельной области, и позиции 152, 153, 155, 171, 247, 297, 339, 375 и 376 располагаются в константной области антитела. Позиции легкой цепи 40 и 41 располагаются в вариабельной области, и позиции 165 и 168 располагаются в константной области антитела.
Позиции тяжелой цепи 40, 41, 89, 152, 153, 155 и 171 и позиции легкой цепи 40, 41, 165 и 168 располагаются в части Fab, и позиции тяжелой цепи 247, 297, 339, 375 и 376 располагаются в части Fc антитела.
В соответствии с настоящим изобретением, термин «встроенный цистеин» означает замену не являющейся цистеином аминокислоты в тяжелой цепи или легкой цепи антитела на цистеин. Как известно специалисту в данной области техники, это может быть сделано или на аминокислотном уровне, или на уровне ДНК, например, с применением сайт-направленного мутагенеза.
Изобретателями по настоящему изобретению неожиданно было обнаружено, что сайт-специфичным образом конъюгированные соединения ADC по настоящему изобретению продемонстрировали улучшенные физико-химические, фармакологические и/или фармакокинетические свойства по сравнению с ADC, в которых линкерное лекарственное средство конъюгировано через нативные межцепочечные дисульфидные связи антитела, и, кроме того, по сравнению с ADC со встроенными цистеинами, в которых линкерное лекарственное средство конъюгировано в позициях, раскрытых в предшествующем уровне техники, в отличие от специфично указанных в настоящей заявке на патент. Соединения ADC в соответствии с настоящим изобретением обладают способностями связывания, аналогичными обычным антителам, хорошей эффективностью in vivo, повышенным терапевтическим индексом и/или улучшенной стабильностью. В частности, было обнаружено, что соединения ADC обычно являются менее гидрофобными и менее подверженными расщеплению посредством катепсина B, и, следовательно, также, вероятно, посредством других внутри- или внеклеточных ферментов/протеаз в опухолевой массе (микросреде опухоли), чем ADC, которые сайт-специфичным образом конъюгированы в других позициях, но все еще демонстрируют аналогичную цитотоксичность in vitro. Неожиданно, ADC в соответствии с настоящим изобретением продемонстрировали улучшенную эффективность in vivo в ксенотрансплантатной модели опухоли животных по сравнению с ADC, которые были сайт-специфичным образом конъюгированы в других позициях.
Вне связи с какой-либо теорией, изобретатели по настоящему изобретению обнаружили, что когда линкерные лекарственные средства конъюгированы в определенных позициях антитела, как заявлено в настоящей заявке, указанное линкерное лекарственное средство встраивается или в полость Fab, которая сформирована доменами CH1, VH, VL и CL антитела, или в полость Fc, которая сформирована двумя доменами CH2 и двумя доменами CH3 антитела. В антителе IgG1 верх полости Fc сформирован гликозидом/углеводом, который прикреплен к позиции N297 тяжелой цепи. В результате линкерное лекарственное средство (которое обычно является более гидрофобным, чем антитело) экранируется от гидрофильной водной среды, окружающей антитело, и ADC, таким образом, является менее гидрофобным по сравнению с ADC, в которых линкерное лекарственное средство конъюгировано через нативные дисульфидные связи антитела, и является намного менее гидрофобным по сравнению с ADC, в которых линкерное лекарственное средство сайт-специфичным образом конъюгировано в различных позициях, которые не заявлены в настоящей заявке, и в которых линкерное лекарственное средство вытесняется за пределы антитела, то есть, направляется в направлении от антитела.
В одном конкретном варианте осуществления настоящее изобретение относится к соединению конъюгата антитело-лекарственное средство (ADC), в котором линкерное лекарственное средство сайт-специфичным образом конъюгировано с антителом через встроенный цистеин в одной или более позициях указанного антитела, выбранных из 40, 41, 152, 153, 247, 339 и 375 тяжелой цепи, и 40, 41, и 165 легкой цепи.
В другом варианте осуществления настоящее изобретение относится к соединению конъюгата антитело-лекарственное средство (ADC), в котором линкерное лекарственное средство сайт-специфичным образом конъюгировано с антителом через встроенный цистеин в одной или более позициях указанного антитела, выбранных из 40, 41, 89, 247, 297 и 376 тяжелой цепи, и 40 и 41 легкой цепи.
В одном из вариантов осуществления настоящее изобретение относится к соединению конъюгата антитело-лекарственное средство (ADC), в котором линкерное лекарственное средство сайт-специфичным образом конъюгировано с антителом через встроенный цистеин в одной или более позициях указанного антитела, выбранных из 40, 41, 89, 152, 153, 155 и 171 тяжелой цепи, и 40, 41, 165 и 168 легкой цепи в части Fab указанного антитела.
В другом варианте осуществления настоящее изобретение относится к соединению конъюгата антитело-лекарственное средство (ADC), в котором линкерное лекарственное средство сайт-специфичным образом конъюгировано с антителом через встроенный цистеин в одной или более позициях указанного антитела, выбранных из 40, 41, 152 и 153 тяжелой цепи, и 40, 41 и 165 легкой цепи в части Fab указанного антитела.
Модификаций вариабельной части антитела обычно избегают, поскольку они могут привести к частичной или полной потере способности связывать антиген. Однако, вопреки обычным ожиданиям, было обнаружено, что определенные остатки в каркасных областях и легких, и тяжелых цепей антитела являются подходящими для конъюгации, и при этом не приводят (к значимому) снижению связывания антигена после конъюгации линкерного лекарственного средства. Поэтому, в особенно предпочтительном варианте осуществления, настоящее изобретение относится к соединению конъюгата антитело-лекарственное средство (ADC), в котором указанный встроенный цистеин находится в одной или более позициях указанного антитела, выбранных из 40, 41 тяжелой цепи и 89 и 40 и 41 легкой цепи в части Fab указанного антитела. Предпочтительно, указанный встроенный цистеин находится в позициях 40 или 41 тяжелой цепи и/или позициях легкой цепи 40 или 41, более предпочтительно, в позиции тяжелой цепи 41 и/или позиции легкой цепи 40 или 41, наиболее предпочтительно, в позиции тяжелой цепи 41. Поскольку из литературы известно, что ассоциированные с опухолью протеазы в микросреде опухоли могут частично расщепить константные домены Fc под шарнирной областью, то конъюгация в части Fab является предпочтительной относительно конъюгации в части Fc. Расщепление константных доменов Fc привело бы к потере Fc-конъюгированных линкерных лекарственных средств, что, в свою очередь, привело бы к снижению активности ADC in vivo. (Fan et al. Breast Cancer Res. 2012; 14: R116 и Brezsky et al. PNAS 2009; 106: 17864-17869). Кроме того, конъюгация в этих позициях в части Fab также позволяет использовать связывающие антиген фрагменты.
В конкретном варианте осуществления соединение конъюгата антитело-лекарственное средство (ADC) из приведенного выше предпочтительного варианта осуществления может также содержать дополнительный встроенный цистеин в одной или более позициях антитела, выбранных из 152, 153, 155, 171, 339 и 375 тяжелой цепи, и 165 и 168 легкой цепи. Предпочтительно, указанный дополнительный встроенный цистеин находится в позиции тяжелой цепи 375 в части Fc указанного антитела.
В соответствии с настоящим изобретением, один или более остатков цистеина могут быть встроены в антитело с применением стандартных методик молекулярного клонирования, или домен(-ы) тяжелой цепи или легкой цепи антитела, несущий(-е) мутацию(-и) цистеина, может(-гут) синтезироваться сам(-и) по себе с применением известного оборудования и процедур синтеза (пептидов или ДНК).
В соответствии с настоящим изобретением, любое линкерное лекарственное средство, известный в области техники, относящейся к ADC, может применяться для сайт-специфичной конъюгации с антителом, если он имеет химическую группу, которая может реагировать с тиоловой группой встроенного цистеина, обычно малеимидной или галоацетильной группой. Подходящие линкерные лекарственные средства могут включать дуокармицин, калихеамицин, димер пирролобензодиазепина (PBD), производную майтанзиноида или ауристатина в качестве цитотоксического средства. Расщепляемый или нерасщепляемый линкер может применяться в соответствии с настоящим изобретением. Подходящие примеры майтанзиноидных лекарственных средств включают DM1 и DM4. Подходящие примеры ауристатиновых лекарственных средств включают ММAE и ММAF.
Эти аббревиатуры хорошо известны специалисту в данной области техники. Примеры подходящих линкерных лекарственных средств, известных специалисту в данной области техники, включают mc-vc-PAB-ММAE (также сокращаемый как mc-vc-ММAE и vc-ММAE), mc-ММAF, и mc-vc-ММAF. Предпочтительно, используемый линкер является расщепляемым линкером, таким как валин- цитруллин (vc) или валин-аланин (va).
Общие молекулярные структуры ADC vc-ММAE и ADC mc-ММAF изображены ниже.
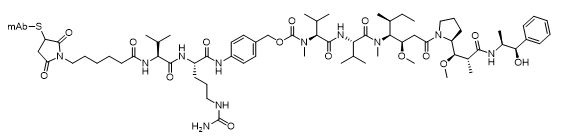
Молекулярная структура vc-ММAE, соединенного с mAb
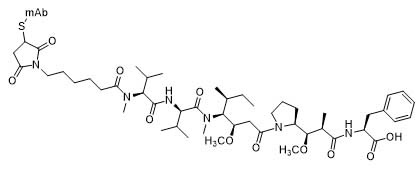
Молекулярная структура mc-ММAF, соединенного с mAb
В одном из вариантов осуществления настоящее изобретение относится к соединению ADC, в котором указанное линкерное лекарственное средство содержит производную дуокармицина.
Дуокармицины, исходно выделенные из культуральной жидкости видов Streptomyces, являются членами семейства противоопухолевых антибиотиков, которое включает дуокармицин A, дуокармицин SA и CC-1065. Эти чрезвычайно сильнодействующие средства предположительно получают свою биологическую активность вследствие способности к селективному по последовательности алкилированию ДНК в позиции N3 аденина в малой бороздке, которое инициирует каскад событий, который завершается в апоптотическом механизме гибели клеток.
WO 2011/133039 раскрывает ряд линкерных лекарственных средств, содержащих производную дуокармицина CC-1065. Подходящие производные линкер-дуокармицин, применяемые в соответствии с настоящим изобретением, раскрываются на страницах 182-197. Химический синтез многих этих линкерных лекарственных средств описывается в примерах 1-12 WO 2011/133039.
В одном из вариантов осуществления настоящее изобретение относится к соединению с формулой (I)
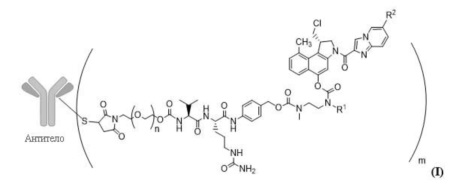
где n составляет 0-3, предпочтительно 0-1,
m представляет среднее DAR от 1 до 6, предпочтительно, от 1 до 4,
R1 выбирается из

y составляет 1-16, и
R2 выбирается из
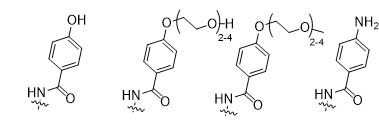 .
.
В структурных формулах, показанных в настоящей спецификации, n представляет целое число от 0 до 3, тогда как m представляет среднее отношение лекарственного средства к антителу (DAR) от 1 до 6. Как хорошо известно в технике, DAR и распределение содержания лекарственного средства могут быть определены, например, с применением хроматографии гидрофобного взаимодействия (HIC) или высокоэффективной жидкостной хроматографии с обращенными фазами (RP-HPLC). HIC является особенно подходящей для определения среднего DAR.
Соединения формулы (I) в соответствии с настоящим изобретением могут быть получены согласно способам и процедурам, которые известны специалисту в данной области техники. Подходящие способы для сайт-специфичной конъюгации линкерных лекарственных средств можно, например, найти в примерах 7 и 8 из WO 2005/084390, которые описывают стратегии полного восстановления для (частичной) загрузки антител линкерным лекарственным средством vc-ММAE, в примерах 11 и 12 из WO 2006/034488, которые описывают сайт-специфичную конъюгацию содержащего майтансин (DM1) линкерного лекарственного средства, и в работе Doronina и соавт. Bioconjugate Chem. 17 (2006): 114-124, в которой описана конъюгация с mc-MMAF.
Конъюгация с двумя или более сайтами встроенных цистеинов по настоящему изобретению позволяет приготовить ADC, содержащие классы гидрофобных лекарственных средств с более высоким DAR, а именно, с DAR равным 4, не получая слишком высокую агрегацию.
В соответствии с конкретным вариантом осуществления настоящего изобретения, один или два встроенных цистеина могут быть включены в тяжелую цепь и/или легкую цепь антитела, что при оптимальных условиях реакции дает соединение ADC, имеющее DAR, равный 2 или 4, соответственно. В случае, когда вносится один встроенный цистеин, он может быть помещен или в части Fab, или в части Fc антитела. Является предпочтительным внесение указанного цистеина в часть Fab антитела в позиции HC (тяжелой цепи) 40, 41, 89, 152 или 153 или LC (легкой цепи) 40, 41 или 165, предпочтительно, HC 40, 41 или 89 или LC 40, 41 или 165, более предпочтительно, HC 40 или 41 или LC 40 или 41, еще более предпочтительно, HC 41 или LC 40 или 41, наиболее предпочтительно, HC 41. В случае, когда вносятся два встроенных цистеина, эти два цистеина могут быть оба расположены в части Fab или в части Fc антитела или, предпочтительно, один из них может находиться в части Fab, предпочтительно, HC 40, 41, 152 или 153 или LC 40, 41 или 165, более предпочтительно, HC 40 или 41 или LC 40 или 41, еще более предпочтительно, HC 41 или LC 40 или 41, наиболее предпочтительно, HC 41, и другой может находиться в части Fc антитела, предпочтительно, HC 247, 297, 339 или 375, более предпочтительно, HC 339 или 375, наиболее предпочтительно, HC 375. В случае, когда два встроенных цистеина вносятся в часть Fab антитела, один остаток цистеина может быть представлен в тяжелой цепи, и другой цистеин может быть представлен в легкой цепи антитела, например. HC 40 или 41 и LC 40 или 41. Кроме того, когда два встроенных цистеина представлены в части Fab антитела, один остаток цистеина может быть внесен в одной из конкретных позиций в соответствии с идентифицированным в настоящем изобретении, например, HC 40 или 41, или LC 40 или 41, и другой может быть расположен в находящейся на поверхности (то есть, не заявляемой в настоящем описании) позиции встроенного цистеина, что приводит к более высокому DAR при все еще являющейся приемлемой гидрофобности.
В конкретном варианте осуществления настоящее изобретение относится к соединению формулы (I), как раскрыто выше, при этом n составляет 0-1, m представляет среднее DAR от 1 до 6, предпочтительно, от 1 до 4, более предпочтительно, от 1 до 2, наиболее предпочтительно, от 1,5 до 2,
R1 выбирается из
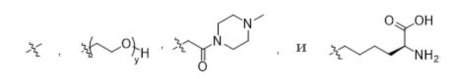
y равно 1-16, предпочтительно, 1-4, и
R2 выбирается из
 .
.
В конкретном варианте осуществления настоящее изобретение относится к соединению со структурной формулой (I), как раскрыто выше, при этом n составляет 0-1, m представляет среднее DAR от 1,5 до 2, R1 представляет собой

y равно 1-4, и R2 выбирается из
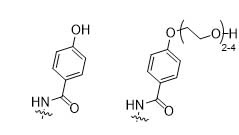 .
.
В особенно предпочтительном варианте осуществления настоящее изобретение относится к соединению с формулой (II)
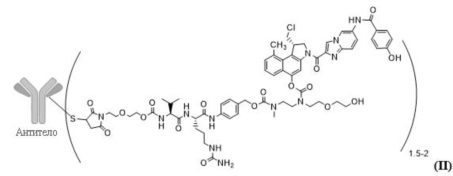 .
.
В соответствии с настоящим изобретением, любое антитело, в частности, любое антитело, которое, как известно, обладает терапевтической активностью, или любое антитело, известное в технике для ADC, или любой антиген, связывающий фрагмент такого антитела, может применяться для сайт-специфичной конъюгации линкерного лекарственного средства в конкретных позициях антитела, заявляемых в настоящем описании. Указанное антитело может представлять собой антитело IgA, IgD, IgE, IgG или IgM. Указанное антитело может иметь κ (каппа) легкие цепи или λ (лямбда) легкие цепи. Указанное антитело IgG может представлять собой антитело IgG1, IgG2, IgG3 или IgG4. Предпочтительно, антитело связывается с антигеном-мишенью a(n), который экспрессируется в или на клеточной мембране (например, на поверхности клеток) опухолевой клетки, более предпочтительно, антитело поглощается клеткой после связывания с (антигеном)-мишенью, после чего токсин высвобождается внутри клетки. Предпочтительно, антитело представляет собой антитело IgG, более предпочтительно, антитело IgG1, наиболее предпочтительно, антитело IgG1, имеющее κ легкие цепи. Предпочтительно, антитело IgG несет нативную молекулу гликозида/углевода, прикрепленную в позиции в N297 тяжелой цепи антитела.
Подходящие антитела включают антитело против аннексина A1, антитело против CD19, антитело против CD22, антитело против CD30, антитело против CD33, антитело против CD37, антитело против CD38, антитело против CD44, антитело против CD47, антитело против CD56, антитело против CD70, антитело против CD74, антитело против CD79, антитело против CD115, антитело против CD123, антитело против CD138, антитело против CD203c, антитело против CD303, антитело против CEACAM, антитело против CLL-1, антитело против c-MET (или против HGFR), антитело против Cripto, антитело против DLL3, антитело против EGFR, антитело против EPCAM, антитело против EphA2, антитело против EphB3, антитело против ETBR, антитело против FcRL5, антитело против FOLR1, антитело против GCC, антитело против GPNMB, антитело против Her2, антитело против HMW-MAA, антитело против интегрина, антитело против подобного Льюис А углевода, антитело против Льюис Y, антитело против LIV1, антитело против мезотелина, антитело против MN, антитело против MUC1, антитело против MUC16, антитело против NaPi2b, антитело против нектина-4, антитело против PSMA, антитело против SIRPα, антитело против SLC44A4, антитело против STEAP-1, антитело против 5T4 (или против TPBG, трофобластного гликопротеина), антитело против Tag72, антитело против TF (или антитканевый фактор), антитело против TROP2, антитело и антитело против VLA.
Предпочтительно, антитело представляет собой антитело против аннексина A1, антитело против CD115, антитело против CD123, антитело против CLL-1, антитело против c-MET, антитело против MUC1, антитело против PSMA, антитело против 5T4 или антитело против TF. Более предпочтительно, антитело представляет собой антитело против PSMA или антитело против 5T4.
Антитело, которое будет применяться в соответствии с настоящим изобретением, предпочтительно, является моноклональным антителом (mAb) и может являться химерным, гуманизированным или человеческим mAb. Более предпочтительно, в соответствии с настоящим изобретением применяется гуманизированное или человеческое mAb, еще более предпочтительно, гуманизированное или человеческое антитело IgG, наиболее предпочтительно, гуманизированное или человеческое mAb IgG1. Предпочтительно, указанное антитело имеет κ (каппа) легкие цепи, то есть, оно является гуманизированным или человеческим IgG1-κ антителом.
В гуманизированных антителах связывающие антиген CDR в вариабельных областях получают из антител не являющихся человеком видов, обычно из мыши, крысы или кролика. Эти нечеловеческие CDR размещаются в пределах человеческой каркасной области (FR1, FR2, FR3 и FR4) вариабельной области, и комбинируются с человеческими константными областями. Как и человеческие антитела, эти гуманизированные антитела могут быть пронумерованы согласно системе нумерации Kabat. Настоящее изобретение, в частности относится к соединению ADC, в котором указанный встроенный цистеин находится в положении, выбранном из VH 40, VH 41, VH 89, VL 40 или VL 41 в человеческой каркасной области (то есть, VH 40, VH 41, VL 40 и VL 41 находится в середине FR2, VH 89 находится в FR3) гуманизированного антитела, более конкретно, в VH 40, VH 41, VL 40 или VL 41, еще более конкретно, в VH 41, VL 40 или VL 41, особенно в VH 41.
В соответствии с настоящим изобретением, эти конкретные остатки в каркасных областях являются подходящими для конъюгации линкерного лекарственного средства, и при этом не приводят к значительному снижению способности связывания антигена для антитела после конъюгации линкерного лекарственного средства. Кроме того, эти сайты являются подходящими не только в антителах, но также и в любых связывающих антиген фрагментах таких антител.
В одном конкретном варианте осуществления настоящее изобретение относится к соединению ADC в соответствии с описанным выше в настоящем описании, при этом указанное антитело представляет собой антитело против аннексина A1, антитело против CD115, антитело против CD123, антитело против CLL-1, антитело против c-MET, антитело против MUC1, антитело против PSMA, антитело против 5T4 или антитело против TF, и указанное линкерное лекарственное средство содержит производную дуокармицина, предпочтительно, соединение ADC в соответствии с формулой (I) или (II).
В еще одном конкретном варианте осуществления настоящее изобретение относится к соединению ADC, в соответствии с описанным выше, в котором указанное антитело представляет собой (моноклональное) антитело против PSMA или (моноклональное) антитело против 5T4, и указанный линкерный лекарственный содержит производную дуокармицина, предпочтительно, соединение ADC в соответствии с формулой (I) или (II).
В предпочтительном варианте осуществления настоящее изобретение относится к соединению ADC в соответствии с описанным выше, в котором указанное линкерное лекарственное средство содержит производную дуокармицина и конъюгирован в позиции 41 из вариабельной области тяжелой цепи (моноклонального) антитела против PSMA или (моноклонального) антитела против 5T4, наиболее предпочтительно, соединение ADC согласно формуле (II). Подходящие антитела против PSMA описаны в WO 98/03873 (например, пример 12), WO 02/098897 (например, фиг. 1-2), WO 2007/002222 (например, таблица 1) и WO 2011/069019 (например, фиг. 2). Подходящие антитела против 5T4 включают H8, которое описано в WO 2006/031653, и антитела A1 и A3, которые описаны в WO 2007/106744, а также любые антитела, связывающиеся с тем же самым эпитопом, что и эти известные антитела.
В более предпочтительном варианте осуществления тяжелая цепь антитела против PSMA содержит последовательность аминокислот SEQ ID (идентификатор последовательности) NO:2, и легкая цепь антитела против PSMA содержит последовательность аминокислот SEQ ID NO:5. Более предпочтительно, тяжелая цепь антитела против PSMA содержит последовательности аминокислот SEQ ID NO:2 и SEQ ID NO:3, и легкая цепь антитела против PSMA содержит последовательности аминокислот SEQ ID NO:5 и SEQ ID NO:6.
В особенно предпочтительном варианте осуществления настоящее изобретение относится к соединению ADC формулы (II), в котором антитело представляет собой антитело против PSMA, тяжелая цепь указанного антитела против PSMA содержит последовательность аминокислот SEQ ID NO:2, и легкая цепь указанного антитела против PSMA содержит последовательность аминокислот SEQ ID NO:5. Более предпочтительно, тяжелая цепь указанного антитела против PSMA содержит последовательности аминокислот SEQ ID NO:2 и SEQ ID NO:3, и легкая цепь указанного антитела против PSMA содержит последовательности аминокислот SEQ ID NO:5 и SEQ ID NO:6.
В другом более предпочтительном варианте осуществления тяжелая цепь антитела против 5T4 содержит последовательность аминокислот SEQ ID NO:8, и легкая цепь антитела против 5T4 содержит последовательность аминокислот SEQ ID NO:11. Более предпочтительно, тяжелая цепь антитела против 5T4 содержит последовательности аминокислот SEQ ID NO:8 и SEQ ID NO:9, и легкая цепь антитела против 5T4 содержит последовательности аминокислот SEQ ID NO:11 и SEQ ID NO:6.
В особенно предпочтительном варианте осуществления настоящее изобретение относится к соединению ADC формулы (II), в котором антитело представляет собой антитело против 5T4, тяжелая цепь указанного антитела против 5T4 содержит последовательность аминокислот SEQ ID NO:8, и легкая цепь указанного антитела против 5T4 содержит последовательность аминокислот SEQ ID NO:11. Более предпочтительно, тяжелая цепь указанного антитела против 5T4 содержит последовательности аминокислот SEQ ID NO:8 и SEQ ID NO:9, и легкая цепь указанного антитела против 5T4 содержит последовательности аминокислот SEQ ID NO:11 и SEQ ID NO:6.
Настоящее изобретение также относится к соединению ADC в соответствии с описанным выше для применения в качестве медикамента.
В одном из вариантов осуществления настоящее изобретение относится к соединению ADC в соответствии с описанным выше для применения в лечении человеческих солидных опухолей и гематологических злокачественных образований.
В еще одном варианте осуществления настоящее изобретение относится к соединению ADC в соответствии с описанным выше для применения в лечении человеческих солидных опухолей, выбранных из группы, состоящей из рака груди, рака желудка, рака ободочной и прямой кишки, рака уротелия (например, рака мочевого пузыря), рака яичников, рака матки, рака легких (в особенности, немелкоклеточного рака легких и мелкоклеточного рака легких), мезотелиомы (в особенности, злокачественной плевральной мезотелиомы), рака печени, рака поджелудочной железы и рака простаты.
В предпочтительном варианте осуществления настоящее изобретение относится к соединению ADC в соответствии с описанным выше, в частности, к соединению, содержащему (моноклональное) антитело против PSMA и производную дуокармицина в качестве линкерного лекарственного средства, для применения в лечении рака простаты.
В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению ADC в соответствии с описанным выше, в частности, к соединению, содержащему (моноклональное) антитело против 5T4 и производную дуокармицина в качестве линкерного лекарственного средства, для применения в лечении человеческих солидных опухолей, выбранных из группы, состоящей из рака груди, рака желудка, рака ободочной и прямой кишки, рака яичников о рака, рака легких (в особенности, немелкоклеточного рака легких (NSCLC) и мелкоклеточного рака легких (SCLC)) и злокачественной плевральной мезотелиомы.
В еще одном варианте осуществления настоящее изобретение относится к соединению ADC в соответствии с описанным выше для применения в лечении человеческих гематологических злокачественных образований, в частности лейкемии, выбранной из группы, состоящей из острой лимфобластной и миелоидной лейкемии (ALL и AML, соответственно).
Настоящее изобретение также относится к фармацевтической композиции, содержащей соединение ADC в соответствии с описанным выше и один или более фармацевтически приемлемых эксципиентов. Типичные фармацевтические составы терапевтических белков, такие как моноклональные антитела и конъюгаты (моноклональное) антитело-лекарственное средство, принимают форму лиофилизированных таблеток (лиофилизированных порошков), которые требуют (водного) растворения (то есть, восстановления) перед внутривенным вливанием, или форму замороженных (водных) растворов, которые требуют размораживания перед использованием.
Как правило, фармацевтическая композиция предоставляется в форме лиофилизированной таблетки. Подходящие фармацевтически приемлемые эксципиенты для включения в фармацевтическую композицию (перед сублимационной сушкой) в соответствии с настоящим изобретением включают буферные растворы (например, содержащие цитрат, гистидин или сукцинат солей в воде), лиопротекторы (например, сахароза, трегалоза), регуляторы тоничности (например, хлорид натрия), поверхностно-активные вещества (например, полисорбат) и наполнители (например, маннитол, аминоуксусная кислота). Эксципиенты, используемые для подвергнутых сублимационной сушке белковых составов, выбирают по их способности предотвращать денатурацию белка во время процесса сублимационной сушки, а также во время хранения. Например, состав в форме стерильного лиофилизированного порошка для одноразового использования Kadcyla™ (Roche) содержит - после восстановления с использованием бактериостатической или стерилизованной воды для инъекций (BWFI или SWFI) - 20 мг/мл адо-трастузумаб эмтанзина, 0,02% вес/объем полисорбат 20, 10 мМ сукцинат натрия и 6% вес/объем сахарозы с pH, равным 5,0.
Настоящее изобретение также относится к применению соединения или фармацевтической композиции в соответствии с описанным выше для лечения человеческих солидных опухолей и гематологических злокачественных образований в соответствии с описанным выше.
Настоящее изобретение также относится к применению последовательно или одновременно вводимой комбинации соединения или фармацевтической композиции в соответствии с описанным выше с терапевтическим антителом и/или химиотерапевтическим средством для лечения человеческих солидных опухолей и гематологических злокачественных образований в соответствии с описанным выше.
В одном из вариантов осуществления настоящего изобретения терапевтическое антитело представляет собой адецатумумаб, алемтузумаб, аматуксимаб, бевацизумаб, цетуксимаб, деносумаб, этарацизумаб, фарлетузумаб, гемтузумаб, лабетузумаб, мапатумумаб, минретумомаб, нимотузумаб, ниволумаб, ореговомаб, панитумумаб, пемтумомаб, пертузумаб, рамуцирумаб, сибротузумаб, трастузумаб или волоциксимаб, и химиотерапевтическое средство представляет собой: i) алкилирующий агент, в частности азотистые иприты, такие как мехлорэтамин, хлорамбуцил, циклофосфамид, ифосфамид и мелфалан, нитрозомочевины, такие как стрептозоцин, кармустин и ломустин, алкилсульфонаты, такие как бисульфан, триазины, такие как дакарбазин и темозоломид, этиленимины, такие как тиотепа и алтретамин, или платиновые препараты, такие как цисплатин, карбоплатин и оксалиплатин; ii) ингибиторы обмена веществ, в частности 5-фторурацилы, 6-меркаптопурин, капецитабин, цитарабин, флоксуридин, флударабин, гемцитабин, гидроксимочевина, метотрексат или пеметрексед; iii) противопухолевый антибиотик, в частности, даунорубицин, доксорубицин, эпирубицин, идарубицин, актиномицин D, блеомицин, митомицин-C или митоксантрон; iv) ингибитор топоизомеразы, в частности ингибитор топоизомеразы I, такой как топотекан и иринотекан, или ингибиторы топоизомеразы II, такие как этопозид, тенипозид и митоксантрон; v) митотический ингибитор, в частности таксаны, такие как паклитаксел, карбазитаксел и доцетаксел, эпотилоны, такие как иксабепилон, алкалоиды барвинка, такие как винбластин, винкристин и винорелбин, или эстрамустин; vi) ингибитор сигнального каскада, в частности ингибиторы mTOR (мишень млекопитающего для рапамицина), такие как темсиролимус и эверолимус, или ингибиторы тирозинкиназы, такие как гефитиниб, эрлотиниб, иматиниб, пазопаниб, церитиниб, кризотиниб, лапатиниб и афатиниб; vii) кортикостероид, в частности преднизон, метилпреднизолон или дексаметазон; viii) гормональное терапевтическое средство, в частности средства модуляции андрогенового рецептора, такие как бикалутамид, энзалутамид и абиратерон ацетат, антиэстрогены, такие как тамоксифен, или ингибирующие ароматазу или модифицирующие стеродиды средства, такие как анастрозол, летрозол, фулвестрант и эксеместан; ix) ингибитор PARP, в частности олапариб; или x) другой химиотерапевтический лекарственный препарат, в частности L-аспарагиназу или бортезомиб. Специалист в данной области техники не испытает затруднений в выборе подходящей комбинированной терапии для применения в лечении человеческих солидных опухолей и гематологических злокачественных образований в соответствии с описанным выше.
В другом варианте осуществления настоящего изобретения, особенно в случае соединения ADC против PSMA, содержащего производную дуокармицина в качестве линкерного лекарственного средства, терапевтическое антитело представляет собой бевацизумаб, деносумаб, или трастузумаб, и химиотерапевтическое средство представляет собой ингибитор топоизомеразы II, в частности, митоксантрон, митотический ингибитор, в частности, таксан, более конкретно, карбазитаксел или доцетаксел, кортикостероид, в частности, преднизон, или гормональное терапевтическое средство, в частности, средство модуляции андрогенового рецептора, более конкретно, энзалутамид или абиратерон ацетат.
В еще одном варианте осуществления настоящего изобретения, в частности, в случае соединения ADC против 5T4, содержащего производную дуокармицина в качестве линкерного лекарственного средства, терапевтическое антитело представляет собой бевацизумаб, цетуксимаб, ниволумаб или рамуцирумаб, и химиотерапевтическое средство представляет собой алкилирующий агент, в частности платиновый лекарственный препарат, более конкретно, цисплатин или карбоплатин, ингибитор обмена веществ, в частности гемцитабин или пеметрексед, ингибитор топоизомеразы II, в частности, этопозид, митотический ингибитор, в частности таксан или алкалоид барвинка, более конкретно, паклитаксел или доцетаксел, или винбластин или винорелбин, или ингибитор сигнального каскада, в частности ингибитор тирозинкиназы, более конкретно, эрлотиниб, церитиниб, кризотиниб или афатиниб.
В еще одном варианте осуществления настоящего изобретения, в частности в случае соединения ADC против 5T4, содержащего производную дуокармицина в качестве линкерного лекарственного средства, терапевтическое антитело представляет собой бевацизумаб, и химиотерапевтическое средство представляет собой алкилирующий агент, в частности азотистый иприт, платиновый лекарственный препарат или триазин, более конкретно, циклофосфамид, ифосфамид, цисплатин, или темозоломид, противопухолевый антибиотик, в частности доксорубицин, антиметаболит, в частности гемцитабин, ингибитор топоизомеразы I или II, в частности топотекан, иринотекан или этопозид, или митотический ингибитор, в частности таксан или алкалоид барвинка, более конкретно паклитаксел или доцетаксел, или винкристин или винорелбин.
В еще одном варианте осуществления настоящего изобретения, в частности, в случае соединения ADC против 5T4, содержащего производную дуокармицина в качестве линкерного лекарственного средства, терапевтическое антитело представляет собой аматуксимаб, и химиотерапевтическое средство представляет собой алкилирующий агент, в частности платиновый лекарственный препарат, более конкретно, цисплатин или карбоплатин, ингибитор обмена веществ, в частности гемцитабин или пеметрексед, или митотический ингибитор, в частности, алкалоид барвинка, более конкретно, винорелбин.
Терапевтически эффективное количество соединений в соответствии с настоящим изобретением находится в диапазоне от около 0,01 до около 15 мг/кг массы тела, в частности в диапазоне от около 0,1 до около 10 мг/кг массы тела, более конкретно, в диапазоне от около 0,3 до около 10 мг/кг массы тела. Этот последний диапазон примерно соответствует фиксированной дозе в диапазоне от 20 до 800 мг соединения ADC. Соединение по настоящему изобретению может вводиться раз в неделю, раз в две недели, раз в три недели или раз в месяц, например еженедельно в течение первых 12 недель и затем каждые три недели до прогрессирования болезни. Альтернативные схемы лечения могут применяться в зависимости от серьезности болезни, возраста пациента, вводимого соединения, и подобных других факторов, которые мог бы принять во внимание лечащий врач.
Примеры
Транзиентная экспрессия антител со встроенными цистеинами (мутантных антител)
1a) Подготовка кДНК
Последовательность кДНК для тяжелой цепи была получена из аминокислотных последовательностей лидерной последовательности (SEQ ID NO:1) вариабельной области тяжелой цепи антитела против PSMA (SEQ ID NO:2, нумерация Kabat, имеет остаток цистеина в позиции 41) и константной области тяжелой цепи человека IgG1 (SEQ ID NO:3, последовательная нумерация, нумерация Eu начинается в аланине 118) посредством обратной трансляции объединенных аминокислотных последовательностей в последовательность кДНК, оптимизированную для экспрессии в клетках человека (Homo sapiens) (SEQ ID NO:4).
Аналогично, последовательность кДНК для легкой цепи была получена из последовательностей аминокислот сигнала секреции (SEQ ID NO:1), вариабельной области легкой цепи антитела против PSMA (SEQ ID NO:5, нумерация Kabat) и константной области κ легкой цепи человеческого Ig (SEQ ID NO:6, последовательная нумерация) посредством обратной трансляции объединенных аминокислотных последовательностей в последовательность кДНК, оптимизированную для экспрессии в клетках человека (Homo sapiens) (SEQ ID NO:7).
Аналогично, последовательность кДНК для тяжелой цепи антитела против 5T4 H8-HC41 (SEQ ID NO:10) была получена из аминокислотных последовательностей лидерной последовательности (SEQ ID NO:1), вариабельной области тяжелой цепи антитела H8 (SEQ ID NO:8, последовательная нумерация, имеет остаток цистеина в позиции 41) и константной области тяжелой цепи человеческого IgG1 (SEQ ID NO:9, последовательная нумерация, нумерация Eu начинается с аланина 118).
Последовательность кДНК для легкой цепи антитела H8 (SEQ ID NO:12) была получена из аминокислотных последовательностей лидерной последовательности (SEQ ID NO:1), вариабельной области легкой цепи антитела H8 (SEQ ID NO:11, нумерация Kabat) и константной области κ легкой цепи человеческого Ig (SEQ ID NO:6, последовательная нумерация).
Последовательность кДНК для тяжелой цепи натализумаба (SEQ ID NO:16) была получена из аминокислотных последовательностей лидерной последовательности (SEQ ID NO:13), вариабельной области тяжелой цепи натализумаба (SEQ ID NO:14, нумерация Kabat) и константной области тяжелой цепи человеческого IgG4 (SEQ ID NO:15, последовательная нумерация, нумерация Eu начинается в аланине 118; имеет остаток пролина в позиции 225 и остаток цистеина в позиции 375).
Последовательность кДНК для легкой цепи натализумаба (SEQ ID NO:19) была получена из аминокислотных последовательностей лидерной последовательности (SEQ ID NO:17), вариабельной области легкой цепи натализумаба (SEQ ID NO:18, нумерация Kabat) и константной области κ легкой цепи человеческого Ig (SEQ ID NO:6, последовательная нумерация).
Конструкции кДНК тяжелой цепи и легкой цепи синтезировались химически и были получены из коммерческого источника (Life Technologies). Расщепление лидерной последовательности соответствовало предсказанному с использованием программы SignalP (http://www.cbs.dtu.dk/services/SignalP/) сайту расщепления.
1b) Векторная конструкция и стратегия клонирования
Для экспрессии цепей антитела экспрессионный вектор млекопитающего 0098 был создан следующим образом. Кассета экспрессии CMV:BGHpA была иссечена из плазмиды pcDNA3.1 (-) (Life Technologies) и повторно вставлена назад в тот же самый исходный вектор (все еще содержащий интактную кассету экспрессии CMV:BGHpA), посредством чего осуществлялась дупликация кассеты экспрессии CMV:BGHpA в целях обеспечения экспрессии кДНК и HC, и LC из единственного плазмидного вектора. Впоследствии, фрагмент IRES-DHFR был выделен из вектора pOptiVEC-TOPO (Life Technologies) и вставлен между промотором CMV и последовательностью полиаденилирования BGHpA в одной из кассет экспрессии CMV:BGHpA.
кДНК для тяжелой цепи (HC) и легкой цепи (LC) были лигированы в пламидные векторы pMA-RQ и pMA-T (Life Technologies), соответственно с использованием сайтов рестрикции SfiI. После переноса в E. coli K12 и размножения, кДНК LC была перенесена в экспрессионный вектор млекопитающего 0098 с использованием сайтов рестрикции AscI и HpaI. Конечный вектор был расщеплен рестрикционными ферментами BamHI и NheI и лигирован с фрагментом кДНК HC, расщепленным теми же самыми рестрикционными ферментами. Конечный вектор, содержащий кассеты экспрессии и HC, и LC (CMV:HC:BGHpA и CMV:LC-BGHpA, соответственно) был перенесен и размножен в клетках E. coli NEB 5-альфа (New England Biolabs).
Крупномасштабное продуцирование конечного вектора экспрессии мутантного антитела для трансфекции выполнялось с применением наборов Maxi-Megaprep (Qiagen).
2) Транзиентная экспрессия в клетках млекопитающих
Коммерчески доступные клетки Expi293F (Life Technologies) были трансфецированы экспрессионным вектором мутантного антитела, приготовленным в соответствии с пунктом 1) выше с применением средства для трансфекции ExpiFectamine (Life Technologies) согласно инструкциям производителя следующим образом: 75×107 клеток были посеяны в 300 мл экспрессионной среды Expi293; 300 мкг экспрессионного вектора мутантного антитела были объединены с 800 мкл средства ждя трансфекции ExpiFectamine и добавлены к клеткам. Через день после трансфекции, 1,5 мл энхансера 1 и 15 мл энхансера 2 было добавлено к культуре. Через шесть дней после трансфекции супернатант клеточной культуры был собран посредством центрифугирования на 4000g в течение 15 минут и фильтрации очищенных собранных клеток через фильтры MF 75 (Nalgene).
3) Очистка экспрессированных белков
Очищенные собранные клетки были сначала проверены на уровень экспрессии с применением электрофореза SDS-PAGE. Если продуцирование признавалось адекватным, антитела очищали с применением коммерчески доступной смолы на основе белка А (MabSelect SuRe, GE Healthcare) с применением хроматографического оборудования Äkta (GE Healthcare). Колонка с высотой слоя 20 см использовалась с предельно допустимой загрузкой упакованной смолы, составляющей 25 мг/мл. Процесс выполнялся RT.
После уравновешивания (PBS pH7,4) и загрузки этап очистки включал в себя два этапа промывки (PBS pH7.4 и NaAc pH5, соответственно) и этап элюции (25 мМ NaAc, pH3), после которых проводились этапы регенерации, прополаскивания и чистки, соответственно, до начала нового цикла. Во время этапа элюции целевой белок был собран в пике, начинающемся и заканчивающемся при поглощающей способности 0,05-0,1 AU (длина клетки 0,2 см). После очистки белок хранился при температуре от -20°C до -80°C.
4) Концентрация и замена буфера на буфер конъюгации ADC
Элюаты белка А, при необходимости, концентрировались до 20-25 мг/мл с применением устройств центрифугирования Vivaspin (отсечение 5 или 30 кДа, Vivaproducts). После получения требуемых концентраций концентрированные растворы (обычно 25 мг/мл) диализировались дважды с применением колонок PD10 (GE Healthcare E) и буфера 4,2 мМ L-гистидин+50 мМ трегалоза, pH 6,0. Альтернативно, когда концентрации элюата белка А составляли приблизительно 10 мг/мл, этап концентрации не проводился, и элюат сразу же диализировался три раза с применением гофрированной трубки для диализа (отсечение 10 кДа, Thermo Scientific) против буфера 4,2 мМ L-гистидин+50 мМ трегалоза, pH 6,0. Любой появившийся осадок удалялся посредством фильтрации после завершения диализа. Концентрации были измерены посредством УФ-спектроскопии с применением Nanodrop или кюветного УФ- спектрофотометра (оба производства Thermo Scientific). Анализ качества показал, что белок имел чистоту >95% и содержал незначительное количество димеров или фрагментов, в соответствии с определенным посредством HPSEC. Изоэлектрическая точка мутанта со встроенным цистеином была идентична дикому типу.
С применением аналогичной/той же самой процедуры, как описана выше, для приготовления и очистки антитела против PSMA со встроенным цистеином (VH 41C, нумерация Kabat), антитела H8-HC41 со встроенным цистеином (VH 41C, нумерация Kabat) и натализумаба со встроенным цистеином (CH 225P, 375C, нумерация Kabat), также и другие антитела из примеров были приготовлены и очищены.
Общий протокол сайт-специфичной конъюгации
К раствору антитела со встроенным цистеином (5-10 мг/мл в 4,2 мМ гистидине, 50 мМ трегалозе, pH=6) была добавлена EDTA (25 мМ в воде, 4% объем/объем). pH был скорректирован до ~7,4 с использованием Трис-буфера (1М в воде, pH=8), после чего был добавлен TCEP (10 мМ в воде, 20 эквивалентов), и полученная в результате смесь инкубировалась при комнатной температуре в течение 1-3 часов. Избыточный TCEP был удален с помощью деминерализующей колонки PD-10 или концентрирующей центрифуги Vivaspin (отсечение 30 кДа, PES) с использованием 4,2 мМ гистидина, 50 мМ трегалозы, pH=6. pH полученного в результате раствора антитела был поднят до ~7,4 с использованием Трис-буфера (1М в воде, pH=8), после чего была добавлена дигидроаскорбиновая кислота (10 мМ в воде, 20 эквивалентов), и полученная в результате смесь культивировалась при комнатной температуре в течение 1-2 часов. Был добавлен DMA, после чего добавлялся раствор линкерного лекарственного средства (10 мМ в DMA). Конечная концентрация DMA составляла 5-10%. Полученная в результате смесь культивировалась при комнатной температуре в отсутствие света в течение 1-16 часов. В целях удаления избытка линкерного лекарственного средства был добавлен активированный уголь, и смесь культивировалась при комнатной температуре в течение 1 часа. Уголь был удален с использованием PES-фильтра на 0,2 мкм, и полученный в результате ADC был составлен в 4,2 мМ гистидине, 50 мМ трегалозе, pH=6 с использованием концентрирующей центрифуги Vivaspin (отсечение 30 кДа, PES). Наконец, раствор ADC подвергался стерильной фильтрации с применением фильтра PES 0,22 мкм.
Общий протокол конъюгации для конъюгации через частично восстановленные эндогенные дисульфиды (конъюгация дикого типа)
К раствору антитела (5-10 мг/мл в 4,2 мМ гистидине, 50 мМ трегалозе, pH=6) была добавлена EDTA (25 мМ в воде, 4% объем/объем). pH был скорректирован до ~7,4 с использованием Трис-буфера (1М в воде, pH=8), после чего был добавлен TCEP (10 мМ в воде, 1-3 эквивалента в зависимости от антитела и требуемого DAR), и полученная в результате смесь культивировалась при комнатной температуре в течение 1-3 часов. Был добавлен DMA, после чего добавлялся раствор линкерного лекарственного средства (10 мМ в DMA). Конечная концентрация DMA составляла 5-10%. Полученная в результате смесь культивировалась при комнатной температуре в отсутствие света в течение 1-16 часов. Для того чтобы удалить избыток линкерного лекарственного средства, был добавлен активированный уголь, и смесь культивировалась при комнатной температуре в течение 1 часа. Уголь был удален с использованием PES-фильтра на 0,2 мкм, и полученный в результате ADC был составлен в 4,2 мМ гистидине, 50 мМ трегалозе, pH=6 с использованием концентрирующей центрифуги Vivaspin (отсечение 30 кДа, PES). Наконец, раствор ADC подвергался стерильной фильтрации с применением фильтра PES 0,22 мкм.
С применением указанных выше общих процедур, ADC со встроенным цистеином и ADC дикого типа, основанные на vc-seco-DUBA (SYD980; то есть соединение 18b, n=1 в примере 10 на странице 209 WO2011/133039), vc-ММAE и линкерные лекарственные средства mc-ММAF были синтезированы и охарактеризованы с применением аналитической хроматографии гидрофобного взаимодействия (HIC), эксклюзионной хроматографии (SEC), экранированной гидрофобной фазовой хроматографии (SHPC), RP-HPLC и тестированием эндотоксина LAL.
Для аналитической HIC 5-10 мкл образца (1 мг/мл) было инъецировано в колонку TSKgel Butyl-NPR (4,6 мМ ID x 3,5 см L, Tosoh Bioscience, кат. номер 14947). Метод элюирования состоял в линейном градиенте от 100%-ного буфера А (25 мМ фосфат натрия, 1,5М сульфат аммония, pH=6,95) до 100%-ного буфера B (25 мМ сульфат аммония, pH=6,95, 20% изопропанол) со скоростью 0,4 мл/мин в течение более чем 20 минут. Использовалась система Waters Acquity H-Class UPLC, оборудованная детектором PDA и программным обеспечением Empower. Поглощающая способность была измерена при 214 нм, и было определено время удержания ADC.
Как видно из аналитической HIC, имелись различия во времени удержания (RT) для разновидностей DAR2 различных ADC со встроенными цистеинами по сравнению с конъюгатами wt (таблицы 1, 2 и 3). Наиболее интересно, конъюгация линкерного лекарственного средства в специфичных сайтах в полости Fab или полости Fc (в соответствии с предсказанным с помощью алгоритма молекулярного моделирования) вызывала (существенное) сокращение времени удержания по сравнению с ADC, которые были конъюгированы через частично восстановленные эндогенные дисульфиды, что позволило изобретателям по настоящему изобретению заключить, что на основании данных HIC ADC со встроенными цистеинами, в которых линкерное лекарственное средство конъюгировано со специфичными сайтами в полости Fab или полости Fc, являются менее гидрофобными, чем конъюгаты wt. В целях дальнейшей квантификации данного эффекта, вводится термин «относительная гидрофобность», который определяется как:
(RTDAR2 - RTDAR0)/(RTDAR2, ADC wt - RTDAR0, ADC wt).
По существу, относительная гидрофобность представляет собой меру, которая позволяет легко сравнить гидрофобность ADC со встроенными цистеинами с wt-конъюгированными аналогами на основании данных HIC. Данные резюмированы в таблицах 1-3.
Таблица 1. Относительная гидрофобность ADC vc-seco-DUBA на ранее указанной аналитической колонке HIC
(%) 2
1 Случайное - не сайт-специфичное - прикрепление
2 HMW представляют собой молекулы с высоким молекулярным весом, отражающие количество сформированных агрегатов
3 Определена как (RTDAR2 - RTDAR0)/(RTDAR2, wt-ADC - RTDAR0, wt-ADC), RT представляет собой время удержания
4 Основано на данных MS
5 RT, wt DAR4 =12,2
6 Компарторные ADC с линкерным лекарственным средством, конъюгированным с остатком цистеина, указывающим наружу
7 ADC с линкерным лекарственным средством, конъюгированным с одним цистеином в полости Fab и одним цистеином, указывающим наружу; процесс еще не оптимизирован
8 Также мутация 225P для предотвращения димеризации IgG4
Таблица 2. Относительная гидрофобность ADC vc-ММAE на ранее указанной аналитической колонке HIC
(%) 1
1 HMW представляют собой молекулы с высоким молекулярным весом, отражающие количество сформированных агрегатов
2 Определена как (RTDAR2 - RTDAR0)/(RTDAR2, wt-ADC - RTDAR0, wt-ADC), RT представляет собой время удержания
3 ND означает «не определено»; дикий тип H8-vc-ММAE не был подготовлен
Таблица 3. Относительная гидрофобность ADC mc-ММAF на ранее указанной аналитической колонке HIC
(%) 1
1 HMW представляют собой молекулы с высоким молекулярным весом, отражающие количество сформированных агрегатов
2 Определена как (RTDAR2 - RTDAR0)/(RTDAR2, wt-ADC - RTDAR0, wt-ADC), RT представляет собой время удержания
Клеточное связывание
Три ADC против PSMA SYD998 (wt), SYD1091 (HC41) и компартор SYD1035 (HC120) обладали равными связывающими способностями на PSMA-экспрессирующих клетках LNCaP-C4.2 (EC50 в диапазоне 0,1-0,2 мкг/мл), аналогичными антителу дикого типа, и все три ADC не были способны связываться с PSMA-отрицательными клетками DU-145 (EC50 >10 мкг/мл).
Два ADC против 5T4 H8-wt и H8-HC40 обладали равными связывающими способностями на 5T4-экспрессирующих клетках MDA-MB-468 (EC50 в диапазоне 0,1-1,2 мкг/мл), аналогичными антителу дикого типа H8, и оба ADC не были способны связываться с 5T4-отрицательными клетками SK-MEL-30 (EC50 >10 мкг/мл).
На способности связывания антигена ADC, таким образом, не оказывал влияния прикрепленный линкерное лекарственное средство на основе производной дуокармицина.
Цитотоксичность in vitro
Активности сайт-специфичным образом конъюгированных ADC против PSMA были аналогичны обычно соединенному ADC дикого типа (SYD998) на PSMA-экспрессирующих клетках LNCaP-C4.2 (IC50 в диапазоне 0,1-0,5 нМ, на основании эквивалентов лекарственного средства, см. таблицу 4 ниже). Все ADC были неактивны на PSMA-отрицательных клетках DU-145 (IC50 >70 нМ), что демонстрирует селективное уничтожение опухолевых клеток через PSMA.
Два несвязывающих контрольных ADC были по меньшей мере в 50 раз менее активны, чем ADC против PSMA, на каждой из оцененных клеточных линий.
Таблица 4. Цитотоксичность in vitro ADC против PSMA vc-seco-DUBA в человеческих опухолевых клетках, экспрессирующих PSMA
1 95% CI является 95%-м доверительным интервалом
2 Процент эффективности приведен для самой высокой тестируемой концентрации (~100 нМ) и вычислен путем деления измеренной люминесценции для каждого лекарственного средства или ADC на среднее значение необработанных клеток (только среда для выращивания), умноженное на 100.
Конъюгация vc-ММAE в позициях HC41, LC40 и LC41 на антителах против PSMA давала цитотоксические активности в PSMA-положительных клетках LNCaP-C4.2, аналогичные ADC против PSMA-vc-seco-DUBA, соединенным в этих сайтах цистеина (таблицы 4 и 5). ADC против PSMA-vc-ММAE не обладали активностью на PSMA-отрицательных клетках DU-145 (IC50 >70 нМ).
Таблица 5. Цитотоксичность in vitro ADC против PSMA-vc-ММAE в человеческих опухолевых клетках, экспрессирующих PSMA
1 95% CI являются 95%-м доверительным интервалом
2 Процент эффективности приведен для самой высокой тестируемой концентрации (~100 нМ) и вычислен путем деления измеренной люминесценции для каждого лекарственного средства или ADC на среднее значение необработанных клеток (только среда для выращивания), умноженное на 100.
Активности ADC против 5T4 со встроенными цистеинами были равны активностям связанных обычным способом ADC H8-wt на 5T4-экспрессирующих клетках MDA-MB-468 (IC50 между 0,07 и 0,09 нМ, таблица 6). ADC против 5T4 были неактивны на 5T4-отрицательных клетках SK-MEL-30 (IC50 >90 нМ).
Таблица 6. Цитотоксичность in vitro ADC против 5T4-vc-seco-DUBA в человеческих опухолевых клетках, экспрессирующих 5T4
5T4-положительная клеточная линия MDA-MB-468
1 95% CI являются 95%-м доверительным интервалом
2 Процент эффективности приведен для самой высокой тестируемой концентрации (~100 нМ) и вычислен путем деления измеренной люминесценции для каждого лекарственного средства или ADC на среднее значение необработанных клеток (только среда для выращивания), умноженное на 100.
Вместе, эти данные показывают, что протестированные позиции цистеина для сайт-специфичной конъюгации не оказывали влияние на способность уничтожения опухолевых клеток для ADC, содержащих два различных линкерных лекарственных средств. Кроме того, сайт-специфичное связывание линкерных лекарственных средств в вариабельной области части Fab различных антител является общеприменимым.
Ферментативное расщепление катепсином B
Молекула валина-цитруллина, присутствующая в линкере ADC с vc-seco-DUBA (SYD980) и vc-ММAE, может быть расщеплена цистеинпротеазами, такими как катепсин B, что приводит к последующему внутриклеточному высвобождению лекарственного средства (seco-) DUBA или ММAE в лизосомах опухоли или внеклеточному высвобождению в микросреде опухоли. Для оценки чувствительности к катепсину B ADC обрабатывались в течение 2 минут и 4 часов активированным катепсином B (Calbiochem). Цитотоксическая активность высвобожденного лекарственного средства из ADC против PSMA была измерена на PSMA-отрицательных клетках DU-145. Цитотоксическая активность высвобожденного лекарственного средства из ADC против 5T4 была измерена на 5T4-отрицательных клетках SK-MEL-30. Во время этапа предварительной инкубации при 37°C 1 мг/мл каждого ADC был смешан с 5 мкг/мл катепсина B (0,04 единицы/лунка) в 0,1M Na-ацетате с pH=5, содержащим 4 мМ DTT. В качестве контроля 1 мг/мл каждого ADC было непосредственно разбавлено в культуральной среде (RPMI 1640, 10% разбавленный FBS). Серийные разведения были выполнены для этих растворов ADC в культуральной среде. Для измерения высвобождения соответствующих свободных токсинов DUBA или ММAE PSMA-отрицательные клетки DU-145 (1000 клеток/лунка) и 5T4-отрицательные клетки SK-MEL-30 (2000 клеток/лунка) культивировались с ADC в течение 6 дней, и жизнеспособность клеток была измерена после 6 дней с применением набора для анализов CellTiter-GloTM (CTG).
Различия в активности высвобожденного лекарственного средства на PSMA-отрицательных клетках DU-145 и 5T4-отрицательных клетках SK-MEL-30 отражают количество лекарственного средства, которое отщепляется от ADC, и, таким образом, доступность сайта расщепления валина-цитруллина для катепсина B. Как показано в таблице 7, чувствительность для протеолитического расщепления отличалась среди ADC после четырех часов воздействия активированного катепсина B (см. значения IC50), в то время как ни один из ADC не был расщеплен после короткого периода воздействия катепсина B в течение 2 минут (IC50 >0 нМ, данные не показаны в таблице).
Вместе эти данные показывают, что сайт конъюгации влияет на доступность линкерного лекарственного средства для ферментативного расщепления, и что линкерное лекарственное средство vc-seco-DUBA (SYD980) в ADC против PSMA ADC-HC41, ADC-HC152, ADC-HC339, ADC-HC375, ADC-LC41 и ADC-LC165 больше всего экранируется от расщепления указанным ферментом. Конъюгация vc-ММAE в позициях HC41 и LC41 антител против PSMA приводила к аналогичному экранированию сайта расщепления валина-цитруллина (Таблица 7). Подобная тенденция была также замечена для антитела против 5T4 H8-HC41, конъюгированного с vc-seco-DUBA (SYD980) через ту же самую позицию HC41.
Совместно эти данные показывают, что, в частности, позиция 41C является подходящей позицией для сайт-специфичного соединения линкерных лекарственных средств с различными антителами.
Таблица 7. Цитотоксичность свободного лекарственного средства, расщепленного катепсином B
* LNCaP-C4.2 использовалась в качестве 5T4-отрицательной клеточной линии.
Модель ксенотрансплантата опухоли животных
In vivo эффективность трех ADC против PSMA была оценена в ксенотрансплантатной модели LNCaP C4-2 рака простаты. Клеточная линия LnCaP-C4.2 представляет собой линию человеческих эпителиальных клеток рака простаты, полученную из ксенотрансплантата, который был последовательно распространен у мышей после вызванной кастрацией регрессии и рецидива парентеральной, андроген-зависимой клеточной линии ксенотрансплантата LnCaP-FGC.
Опухоли были индуцированы подкожно путем инъецирования 1×107 клеток LnCap C4.2 в 200 мкл 1640 RPMI, содержащем матригель (50:50, объем:объем) в правый бок мышей-самцов CB17-SCID. Имплантация опухолевых клеток LnCaP-C4.2 выполнялась спустя 24-72 часа после облучения всего тела источником γ-излучения (1,44 Gy, 60Co, BioMep, Bretenières, Франция). Лечение было запущено, когда опухоли достигли среднего объема 100-200 мм3. Мыши были рандомизированы в группы в соответствии с их индивидуальным объемом опухоли, и получали одну в/в инъекцию ADC против PSMA (2 или 10 мг/кг) или наполнителя в хвостовую вену. Наблюдались изменения в объемах опухоли (фиг. 2) и массе тела (фиг. 3). Все три ADC имели среднее DAR, составляющее приблизительно 1,8.
Фиг. 2A демонстрирует, что при 2 мг/кг компарторный ADC против PSMA со встроенным цистеином SYD1035 является менее активным по сравнению с нативным, не имеющим встроенных цистеинов SYD998. Однако, эффективность SYD1091, ADC со встроенным цистеином в соответствии с настоящим изобретением, значительно выше, чем эффективность компартора SYD1035, и выше, чем эффективность нативного, не имеющего встроенных цистеинов SYD998. Различие между компарторным SYD1035 и SYD1091 является еще более явным при 10 мг/кг, как показано на фиг. 2B. У мышей, имеющих опухоли LnCap C4.2, развивалась кахексия, как проиллюстрировано на фиг. 3. Эта потеря массы тела часто восстанавливается после введения эффективного лечения и считается биомаркером эффективности чувствительности. Лечение SYD1091 приводило к намного более быстрому восстановлению массы тела, чем наблюдалось для компартора SYD1035 или нативного, не имеющего встроенных цистеинов SYD998 (фиг. 3).
In vivo эффективность двух ADC против 5T4, то есть нативного H8-vc-seco-DUBA (среднее DAR 2,0) и ADC со встроенным цистеином (VH P41C) H8-41C-vc-seco-DUBA (среднее DAR 1,7), была оценена в ксенотрансплантатной модели PA-1 рака яичников. Клеточная линия PA-1 был построена из клеток, взятых из асцитической жидкости, собранной у женщины с раком яичников (Zeuthen J. et al. Int. J. Cancer 1980; 25(1): 19-32).
Опухоли PA-1 были индуцированы подкожно посредством инъецирования 1×107 клеток в 100 мкл 1640 RPMI, содержащем матригель (50/50, объем/объем) в правый бок мышей-самок без вилочковой железы Balb/c. Инъецирование PA-1 выполнялось спустя 24-72 часа после облучения всего тела источником γ-излучения (2Gy, 60Co, BioMep, Bretenières, Франция). Лечение было запущено, когда опухоли достигли среднего объема 200-300 мм3. Мыши были рандомизированы в группы в соответствии с их индивидуальным объемом опухоли, и получали одну в/в инъекцию ADC против 5T4 (3 или 10 мг/кг) или наполнителя в хвостовую вену, и наблюдались изменения в объемах опухоли (фиг. 4A и 4B). Даже притом, что оба варианта имели аналогичную эффективность при более высокой дозе 10 мг/кг (фиг. 4B), при 3 мг/кг ADC против 5T4 со встроенным цистеином H8-41C-vc-seco-DUBA являлся явно более активным при сравнении с нативным, не имеющим встроенных цистеинов ADC против 5T4, H8-vc-seco-DUBA (фиг. 4A).
Совместно эти результаты исследования демонстрируют, что, in vivo, сайт-специфичные ADC со встроенными цистеинами согласно настоящему изобретению демонстрируют предпочтительные свойства в отношении эффективности в мышиных моделях опухоли.
SEQ ID NO:1 (лидерная последовательность HAVT20)
1 MACPGFLWAL VISTCLEFSM A
SEQ ID NO:2 (антитело против PSMA HC S41C)
1 EVQLVQSGAE VKKPGASVKI SCKTSGYTFT EYTIHWVKQA CGKGLEWIGN
51 INPNNGGTTY NQKFEDRATL TVDKSTSTAY MELSSLRSED TAVYYCAAGW
101 NFDYWGQGTT VTVSS
SEQ ID NO:3 (константная область тяжелой цепи (HC) человеческого антитела IgG1)
1 ASTKGPSVFP LAPSSKSTSG GTAALGCLVK DYFPEPVTVS WNSGALTSGV
51 HTFPAVLQSS GLYSLSSVVT VPSSSLGTQT YICNVNHKPS NTKVDKKVEP
101 KSCDKTHTCP PCPAPELLGG PSVFLFPPKP KDTLMISRTP EVTCVVVDVS
151 HEDPEVKFNW YVDGVEVHNA KTKPREEQYN STYRVVSVLT VLHQDWLNGK
201 EYKCKVSNKA LPAPIEKTIS KAKGQPREPQ VYTLPPSRDE LTKNQVSLTC
251 LVKGFYPSDI AVEWESNGQP ENNYKTTPPV LDSDGSFFLY SKLTVDKSRW
301 QQGNVFSCSV MHEALHNHYT QKSLSLSPGK
SEQ ID NO:4 (антитело против PSMA HC S41C, кДНК)
1 ATGGCCTGTC CTGGATTTCT GTGGGCCCTC GTGATCAGCA CCTGTCTGGA ATTCAGCATG
61 GCCGAGGTGC AGCTGGTGCA GTCTGGCGCC GAAGTGAAGA AACCAGGCGC CAGCGTGAAG
121 ATCAGCTGCA AGACCAGCGG CTACACCTTC ACCGAGTACA CCATCCACTG GGTCAAGCAG
181 GCCTGTGGCA AGGGCCTGGA ATGGATCGGC AACATCAACC CCAACAACGG CGGCACCACC
241 TACAACCAGA AGTTCGAGGA CCGGGCCACC CTGACCGTGG ACAAGAGCAC AAGCACCGCC
301 TACATGGAAC TGAGCAGCCT GCGGAGCGAG GACACCGCCG TGTACTATTG TGCCGCCGGA
361 TGGAACTTCG ACTACTGGGG CCAGGGCACC ACCGTGACAG TGTCTAGCGC CAGCACAAAG
421 GGCCCCAGCG TGTTCCCTCT GGCCCCTAGC AGCAAGTCTA CCTCTGGCGG AACAGCCGCC
481 CTGGGCTGCC TCGTGAAGGA CTACTTTCCC GAGCCCGTGA CCGTGTCCTG GAACTCTGGC
541 GCTCTGACAA GCGGCGTGCA CACCTTTCCA GCCGTGCTGC AGAGCAGCGG CCTGTACTCT
601 CTGAGCAGCG TCGTGACTGT GCCCAGCAGC AGCCTGGGCA CCCAGACCTA CATCTGCAAC
661 GTGAACCACA AGCCCAGCAA CACCAAGGTG GACAAAAAGG TGGAACCCAA GAGCTGCGAC
721 AAGACCCACA CCTGTCCCCC TTGTCCTGCC CCTGAACTGC TGGGCGGACC TTCCGTGTTC
781 CTGTTCCCCC CAAAGCCCAA GGACACCCTG ATGATCAGCC GGACCCCCGA AGTGACCTGC
841 GTGGTGGTGG ATGTGTCCCA CGAGGACCCT GAAGTGAAGT TCAATTGGTA CGTGGACGGC
901 GTGGAAGTGC ACAACGCCAA GACCAAGCCC AGAGAGGAAC AGTACAACAG CACCTACCGG
961 GTGGTGTCCG TGCTGACAGT GCTGCACCAG GACTGGCTGA ACGGCAAAGA GTACAAGTGC
1021 AAGGTGTCCA ACAAGGCCCT GCCTGCCCCC ATCGAGAAAA CCATCAGCAA GGCCAAGGGC
1081 CAGCCCCGCG AACCCCAGGT GTACACACTG CCTCCCAGCA GGGACGAGCT GACCAAGAAC
1141 CAGGTGTCCC TGACATGCCT CGTGAAAGGC TTCTACCCCT CCGATATCGC CGTGGAATGG
1201 GAGAGCAACG GCCAGCCCGA GAACAACTAC AAGACCACCC CCCCTGTGCT GGACAGCGAC
1261 GGCTCATTCT TCCTGTACAG CAAGCTGACT GTGGATAAGT CCCGGTGGCA GCAGGGCAAC
1321 GTGTTCAGCT GCAGCGTGAT GCACGAGGCC CTGCACAACC ACTACACCCA GAAAAGCCTG
1381 TCCCTGAGCC CCGGCAAG
SEQ ID NO:5 (легкая цепь (LC) антитела против PSMA)
1 DIVMTQSPSS LSASVGDRVT ITCKASQDVG TAVDWYQQKP GKAPKLLIYW
51 ASTRHTGVPD RFTGSGSGTD FTLTISSLQP EDFADYFCQQ YNSYPLTFGG
101 GTKLEIK
SEQ ID NO:6 (κ константная область LC человеческого антитела IgG)
1 RTVAAPSVFI FPPSDEQLKS GTASVVCLLN NFYPREAKVQ WKVDNALQSG
51 NSQESVTEQD SKDSTYSLSS TLTLSKADYE KHKVYACEVT HQGLSSPVTK
101 SFNRGEC
SEQ ID NO:7 (легкая цепь (LC) антитела против PSMA, кДНК)
1 ATGGCTTGTC CTGGATTTCT GTGGGCCCTC GTGATCAGCA CCTGTCTGGA ATTCAGCATG
61 GCCGACATCG TGATGACCCA GAGCCCCAGC TCTCTGAGCG CCAGCGTGGG CGACAGAGTG
121 ACCATCACAT GCAAGGCCAG CCAGGACGTG GGCACCGCCG TGGATTGGTA TCAGCAGAAG
181 CCTGGCAAGG CCCCCAAGCT GCTGATCTAC TGGGCCAGCA CCAGACACAC CGGCGTGCCC
241 GATAGATTCA CAGGCAGCGG CTCCGGCACC GACTTCACCC TGACAATCAG CAGCCTGCAG
301 CCCGAGGACT TCGCCGACTA CTTCTGCCAG CAGTACAACA GCTACCCCCT GACCTTCGGC
361 GGAGGCACCA AGCTGGAAAT CAAGCGGACA GTGGCCGCTC CCAGCGTGTT CATCTTCCCA
421 CCTAGCGACG AGCAGCTGAA GTCTGGCACC GCCTCTGTCG TGTGCCTGCT GAACAACTTC
481 TACCCCCGCG AGGCCAAGGT GCAGTGGAAG GTGGACAATG CCCTGCAGAG CGGCAACAGC
541 CAGGAAAGCG TGACCGAGCA GGACAGCAAG GACTCCACCT ACAGCCTGAG CAGCACCCTG
601 ACCCTGAGCA AGGCCGACTA CGAGAAGCAC AAGGTGTACG CCTGCGAAGT GACCCACCAG
661 GGCCTGTCTA GCCCCGTGAC CAAGAGCTTC AACCGGGGCG AGTGC
SEQ ID NO:8 (H8 HC P41C)
1 QVQLVQSGAE VKKPGASVKV SCKASGYSFT GYYMHWVKQS CGQGLEWIGR
51 INPNNGVTLY NQKFKDRVTM TRDTSISTAY MELSRLRSDD TAVYYCARST
101 MITNYVMDYW GQGTLVTVSS
SEQ ID NO:9 (константная область HC человеческого антитела IgG1)
1 ASTKGPSVFP LAPSSKSTSG GTAALGCLVK DYFPEPVTVS WNSGALTSGV
51 HTFPAVLQSS GLYSLSSVVT VPSSSLGTQT YICNVNHKPS NTKVDKKVEP
101 KSCDKTHTCP PCPAPELLGG PSVFLFPPKP KDTLMISRTP EVTCVVVDVS
151 HEDPEVKFNW YVDGVEVHNA KTKPREEQYN STYRVVSVLT VLHQDWLNGK
201 EYKCKVSNKA LPAPIEKTIS KAKGQPREPQ VYTLPPSREE MTKNQVSLTC
251 LVKGFYPSDI AVEWESNGQP ENNYKTTPPV LDSDGSFFLY SKLTVDKSRW
301 QQGNVFSCSV MHEALHNHYT QKSLSLSPGK
SEQ ID NO:10 (H8 HC P41C, кДНК)
1 ATGGCCTGTC CTGGATTTCT GTGGGCCCTC GTGATCAGCA CCTGTCTGGA ATTCAGCATG
61 GCCCAGGTGC AGCTGGTGCA GTCTGGCGCC GAAGTGAAGA AACCAGGCGC CAGCGTGAAG
121 GTGTCCTGCA AGGCCAGCGG CTACAGCTTC ACCGGCTACT ACATGCACTG GGTCAAGCAG
181 AGCTGCGGCC AGGGCCTGGA ATGGATCGGC AGAATCAACC CCAACAACGG CGTGACCCTG
241 TACAACCAGA AATTCAAGGA CCGCGTGACC ATGACCCGGG ACACCAGCAT CAGCACCGCC
301 TACATGGAAC TGAGCCGGCT GAGAAGCGAC GACACCGCCG TGTACTACTG CGCCCGGTCC
361 ACCATGATCA CCAACTACGT GATGGACTAC TGGGGCCAGG GCACCCTCGT GACAGTGTCT
421 AGCGCCAGCA CAAAGGGCCC CAGCGTGTTC CCTCTGGCCC CTAGCAGCAA GAGCACATCT
481 GGCGGAACAG CCGCCCTGGG CTGCCTCGTG AAGGATTACT TCCCCGAGCC CGTGACCGTG
541 TCCTGGAATA GCGGAGCCCT GACAAGCGGC GTGCACACCT TTCCAGCCGT GCTGCAGAGC
601 AGCGGCCTGT ACTCTCTGAG CAGCGTCGTG ACTGTGCCCA GCAGCAGCCT GGGCACCCAG
661 ACCTACATCT GCAACGTGAA CCACAAGCCC AGCAACACCA AGGTGGACAA GAAGGTGGAA
721 CCCAAGAGCT GCGACAAGAC CCACACCTGT CCCCCTTGTC CTGCCCCTGA ACTGCTGGGC
781 GGACCTTCCG TGTTCCTGTT CCCCCCAAAG CCCAAGGACA CCCTGATGAT CAGCCGGACC
841 CCCGAAGTGA CCTGCGTGGT GGTGGATGTG TCCCACGAGG ACCCTGAAGT GAAGTTCAAT
901 TGGTACGTGG ACGGCGTGGA AGTGCACAAC GCCAAGACCA AGCCCAGAGA GGAACAGTAC
961 AACAGCACCT ACCGGGTGGT GTCCGTGCTG ACAGTGCTGC ACCAGGACTG GCTGAACGGC
1021 AAAGAGTACA AGTGCAAGGT GTCCAACAAA GCCCTGCCTG CCCCCATCGA GAAAACCATC
1081 AGCAAGGCCA AGGGCCAGCC CCGCGAACCC CAGGTGTACA CACTGCCTCC CAGCCGGGAA
1141 GAGATGACCA AGAACCAGGT GTCCCTGACA TGCCTCGTGA AAGGCTTCTA CCCCTCCGAT
1201 ATCGCCGTGG AATGGGAGAG CAACGGCCAG CCCGAGAACA ACTACAAGAC CACCCCCCCT
1261 GTGCTGGACA GCGACGGCTC ATTCTTCCTG TACAGCAAGC TGACCGTGGA CAAGTCCCGG
1321 TGGCAGCAGG GCAACGTGTT CAGCTGCAGC GTGATGCACG AGGCCCTGCA CAACCACTAC
1381 ACCCAGAAGT CCCTGAGCCT GAGCCCCGGC AAA
SEQ ID NO:11 (H8 LC)
1 DIVMTQSPDS LAVSLGERAT INCKASQSVS NDVAWYQQKP GQSPKLLISY
51 TSSRYAGVPD RFSGSGSGTD FTLTISSLQA EDVAVYFCQQ DYNSPPTFGG
101 GTKLEIK
SEQ ID NO:12 (H8 LC, кДНК)
1 ATGGCCTGTC CTGGATTTCT GTGGGCCCTC GTGATCAGCA CCTGTCTGGA ATTCAGCATG
61 GCCGACATCG TGATGACCCA GAGCCCCGAT AGCCTGGCCG TGTCTCTGGG AGAGAGAGCC
121 ACCATCAACT GCAAGGCCAG CCAGAGCGTG TCCAACGACG TGGCCTGGTA TCAGCAGAAG
181 CCCGGCCAGA GCCCTAAGCT GCTGATCTCC TACACCAGCA GCAGATATGC CGGCGTGCCC
241 GACAGATTTT CCGGCAGCGG CTCTGGCACC GACTTCACCC TGACAATCAG CTCCCTGCAG
301 GCCGAGGACG TGGCCGTGTA CTTCTGTCAG CAAGACTACA ACAGCCCCCC CACCTTCGGC
361 GGAGGCACCA AGCTGGAAAT CAAGCGGACA GTGGCCGCTC CCAGCGTGTT CATCTTCCCA
421 CCTAGCGACG AGCAGCTGAA GTCCGGCACA GCCTCTGTCG TGTGCCTGCT GAACAACTTC
481 TACCCCCGCG AGGCCAAGGT GCAGTGGAAG GTGGACAATG CCCTGCAGAG CGGCAACAGC
541 CAGGAAAGCG TGACCGAGCA GGACAGCAAG GACTCCACCT ACAGCCTGAG CAGCACCCTG
601 ACCCTGAGCA AGGCCGACTA CGAGAAGCAC AAGGTGTACG CCTGCGAAGT GACCCACCAG
661 GGACTGAGCA GCCCTGTGAC CAAGAGCTTC AACCGGGGCG AGTGC
SEQ ID NO:13 (лидерная последовательность зародышевой линии)
1 MDWTWRILFL VAAATGAHS
SEQ ID NO:14 (натализумаб, HC)
1 QVQLVQSGAE VKKPGASVKV SCKASGFNIK DTYIHWVRQA PGQRLEWMGR
51 IDPANGYTKY DPKFQGRVTI TADTSASTAY MELSSLRSED TAVYYCAREG
101 YYGNYGVYAM DYWGQGTLVT VSS
SEQ ID NO:15 (натализумаб, HC S225P, S375C)
1 ASTKGPSVFP LAPCSRSTSE STAALGCLVK DYFPEPVTVS WNSGALTSGV
51 HTFPAVLQSS GLYSLSSVVT VPSSSLGTKT YTCNVDHKPS NTKVDKRVES
101 KYGPPCPPCP APEFLGGPSV FLFPPKPKDT LMISRTPEVT CVVVDVSQED
151 PEVQFNWYVD GVEVHNAKTK PREEQFNSTY RVVSVLTVLH QDWLNGKEYK
201 CKVSNKGLPS SIEKTISKAK GQPREPQVYT LPPSQEEMTK NQVSLTCLVK
251 GFYPCDIAVE WESNGQPENN YKTTPPVLDS DGSFFLYSRL TVDKSRWQEG
301 NVFSCSVMHE ALHNHYTQKS LSLSLGK
SEQ ID NO:16 (натализумаб, HC S225P, S375C, кДНК)
1 ATGGACTGGA CCTGGCGCAT CCTGTTTCTG GTGGCCGCTG CTACCGGCGC TCACTCCCAG
61 GTGCAGCTGG TGCAGTCTGG CGCCGAAGTG AAGAAACCTG GCGCCTCCGT GAAGGTGTCC
121 TGCAAGGCCT CCGGCTTCAA CATCAAGGAC ACCTACATCC ACTGGGTCCG ACAGGCCCCT
181 GGACAGCGGC TGGAATGGAT GGGCAGAATC GACCCCGCCA ACGGCTACAC TAAGTACGAC
241 CCCAAGTTCC AGGGCAGAGT GACCATCACC GCCGACACCT CCGCCTCCAC AGCCTACATG
301 GAACTGTCCT CCCTGCGGAG CGAGGACACC GCCGTGTACT ACTGCGCCAG AGAGGGCTAC
361 TACGGCAACT ACGGCGTGTA CGCCATGGAC TACTGGGGCC AGGGCACCCT GGTCACCGTG
421 TCCTCCGCTT CCACCAAGGG CCCCTCCGTG TTCCCTCTGG CCCCTTGCTC CCGGTCCACC
481 TCCGAGTCTA CCGCCGCTCT GGGCTGCCTG GTCAAGGACT ACTTCCCCGA GCCCGTGACC
541 GTGTCCTGGA ACTCTGGCGC CCTGACCTCT GGCGTGCACA CCTTCCCTGC TGTGCTGCAG
601 TCCTCCGGCC TGTACTCCCT GTCCTCCGTC GTGACCGTGC CCTCCAGCTC CCTGGGCACC
661 AAGACCTACA CCTGTAACGT GGACCACAAG CCCTCCAACA CCAAGGTGGA CAAGCGGGTG
721 GAATCTAAGT ACGGCCCTCC CTGCCCCCCC TGCCCTGCCC CTGAATTTCT GGGCGGACCT
781 TCCGTGTTCC TGTTCCCCCC AAAGCCCAAG GACACCCTGA TGATCTCCCG GACCCCCGAA
841 GTGACCTGCG TGGTGGTGGA CGTGTCCCAG GAAGATCCCG AGGTCCAGTT CAATTGGTAC
901 GTGGACGGCG TGGAAGTGCA CAACGCCAAG ACCAAGCCCA GAGAGGAACA GTTCAACTCC
961 ACCTACCGGG TGGTGTCCGT GCTGACCGTG CTGCACCAGG ACTGGCTGAA CGGCAAAGAG
1021 TACAAGTGCA AGGTGTCCAA CAAGGGCCTG CCCAGCTCCA TCGAAAAGAC CATCTCCAAG
1081 GCCAAGGGAC AGCCTCGCGA GCCCCAGGTG TACACCCTGC CTCCAAGCCA GGAAGAGATG
1141 ACCAAGAACC AGGTGTCCCT GACCTGTCTG GTCAAGGGCT TCTACCCCTG CGATATCGCC
1201 GTGGAATGGG AGTCCAACGG CCAGCCCGAG AACAACTACA AGACCACCCC CCCTGTGCTG
1261 GACTCCGACG GCTCCTTCTT CCTGTACTCT CGGCTGACCG TGGACAAGTC CCGGTGGCAG
1321 GAAGGCAACG TCTTCTCCTG CTCCGTGATG CACGAGGCCC TGCACAACCA CTACACCCAG
1381 AAGTCCCTGT CCCTGAGCCT GGGCAAG
SEQ ID NO:17 (лидерная последовательность зародышевой линии)
1 MDMRVPAQLL GLLLLWLRGA RC
SEQ ID NO:18 (натализумаб, LC)
1 DIQMTQSPSS LSASVGDRVT ITCKTSQDIN KYMAWYQQTP GKAPRLLIHY
51 TSALQPGIPS RFSGSGSGRD YTFTISSLQP EDIATYYCLQ YDNLWTFGQG
101 TKVEIK
SEQ ID NO:19 (натализумаб, LC, кДНК)
1 ATGGACATGA GAGTGCCCGC CCAGCTGCTG GGACTGCTGC TGCTGTGGCT GAGAGGCGCC
61 AGATGCGACA TCCAGATGAC CCAGTCCCCC TCCAGCCTGT CCGCCTCCGT GGGCGACAGA
121 GTGACCATCA CATGCAAGAC CTCCCAGGAC ATCAACAAGT ACATGGCCTG GTATCAGCAG
181 ACCCCCGGCA AGGCCCCTCG GCTGCTGATC CACTACACCT CCGCTCTGCA GCCTGGCATC
241 CCCTCCAGAT TCTCCGGCTC CGGCTCTGGC CGGGACTATA CCTTCACCAT CTCCAGTCTG
301 CAGCCCGAGG ATATCGCCAC CTACTACTGC CTGCAGTACG ACAACCTGTG GACCTTCGGC
361 CAGGGCACCA AGGTGGAAAT CAAGCGGACC GTGGCCGCTC CCTCCGTGTT CATCTTCCCA
421 CCCTCCGACG AGCAGCTGAA GTCCGGCACC GCCTCCGTCG TGTGCCTGCT GAACAACTTC
481 TACCCCCGCG AGGCCAAGGT GCAGTGGAAG GTGGACAACG CCCTGCAGTC CGGCAACTCC
541 CAGGAATCCG TCACCGAGCA GGACTCCAAG GACAGCACCT ACTCCCTGTC TCCACCCTG
601 ACCCTGTCCA AGGCCGACTA CGAGAAGCAC AAGGTGTACG CCTGCGAAGT GACCCACCAG
661 GGCCTGTCCA GCCCCGTGAC CAAGTCCTTC AACCGGGGCG AGTGC
| название | год | авторы | номер документа |
|---|---|---|---|
| САЙТ-СПЕЦИФИЧНАЯ КОНЪЮГАЦИЯ ЛИНКЕРНЫХ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ С АНТИТЕЛАМИ И ПОЛУЧАЕМЫЕ В РЕЗУЛЬТАТЕ ADC | 2015 |
|
RU2773536C2 |
| АНТИТЕЛА ПРОТИВ 5T4 И КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2016 |
|
RU2736720C2 |
| НЕЛИНЕЙНЫЕ САМОРАСЩЕПЛЯЮЩИЕСЯ ЛИНКЕРЫ И ИХ КОНЪЮГАТЫ | 2017 |
|
RU2755899C2 |
| СПОСОБ ДВОЙНОЙ КОНЪЮГАЦИИ ДЛЯ ПОЛУЧЕНИЯ КОНЪЮГАТОВ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2018 |
|
RU2771310C2 |
| ФИЛЬТРУЕМЫЕ КОМПОЗИЦИИ ДУОКАРМИЦИН-СОДЕРЖАЩИХ КОНЪЮГАТОВ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2019 |
|
RU2774642C1 |
| АНТИТЕЛА ПРОТИВ EDB И КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2017 |
|
RU2758632C2 |
| АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И ИХ ПРИМЕНЕНИЯ | 2007 |
|
RU2639543C9 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО ДУОКАРМИЦИН | 2016 |
|
RU2687237C1 |
| АНТИ-CD79b АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2791984C2 |
| КОНЪЮГАТ "ЦИСТЕИН-МОДИФИЦИРОВАННОЕ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО" И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2017 |
|
RU2762594C2 |
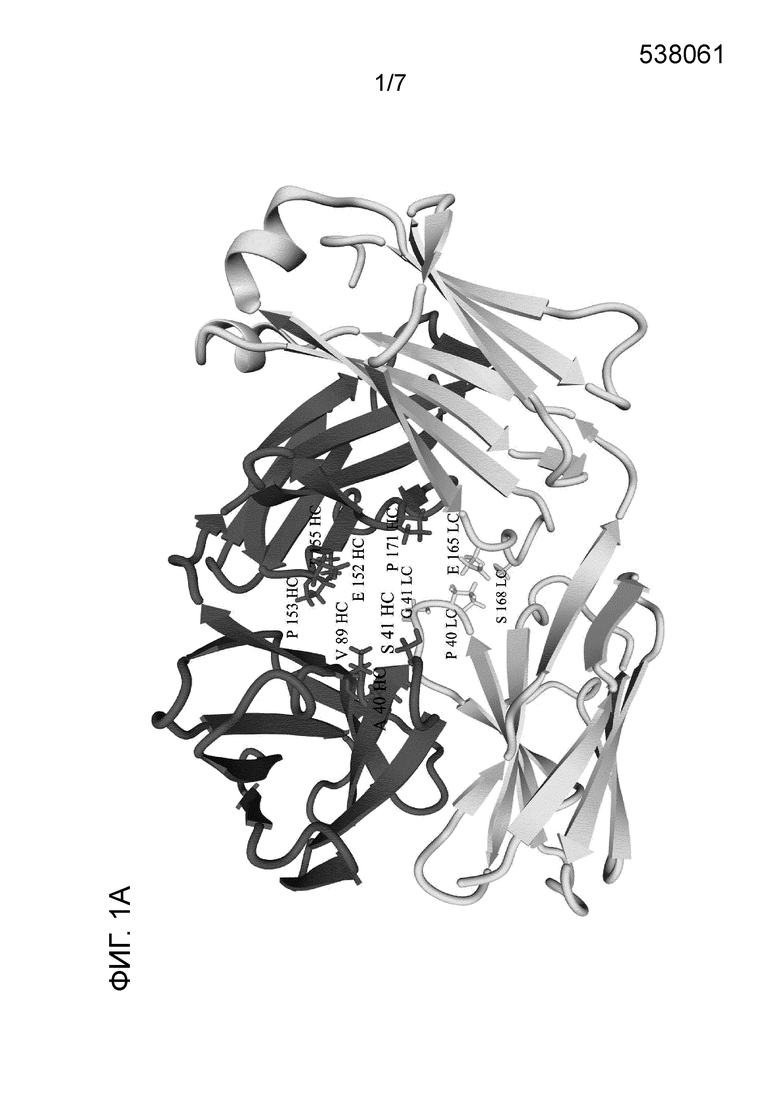

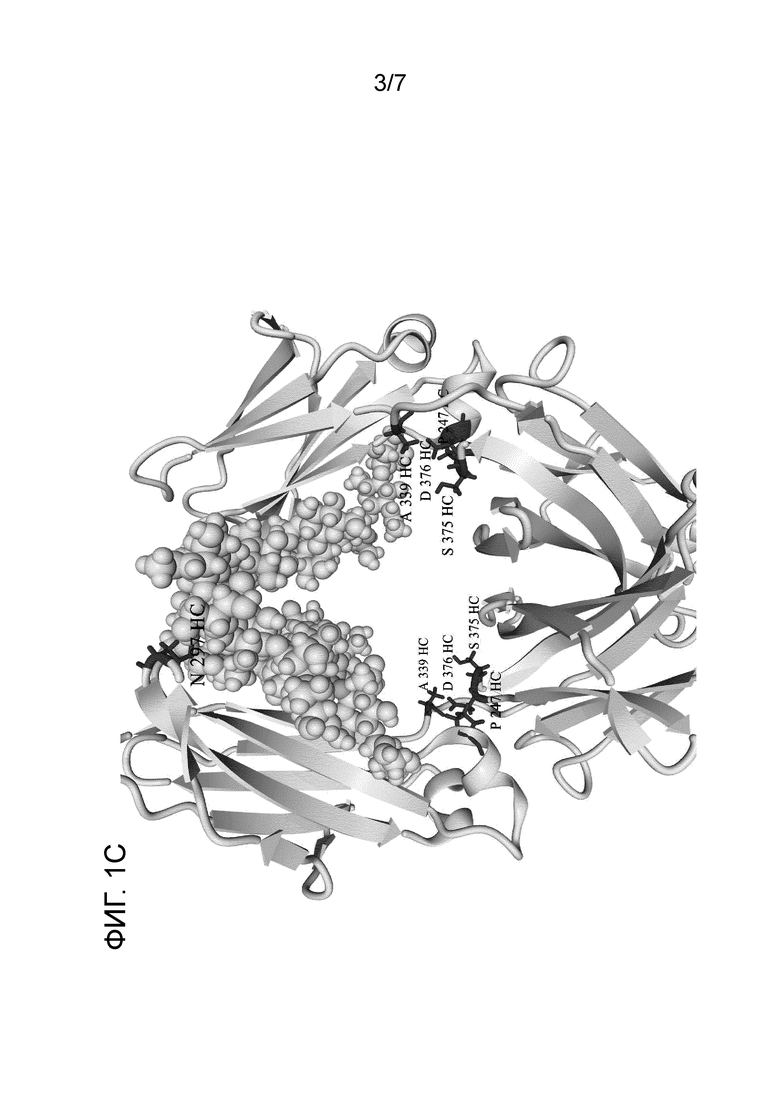



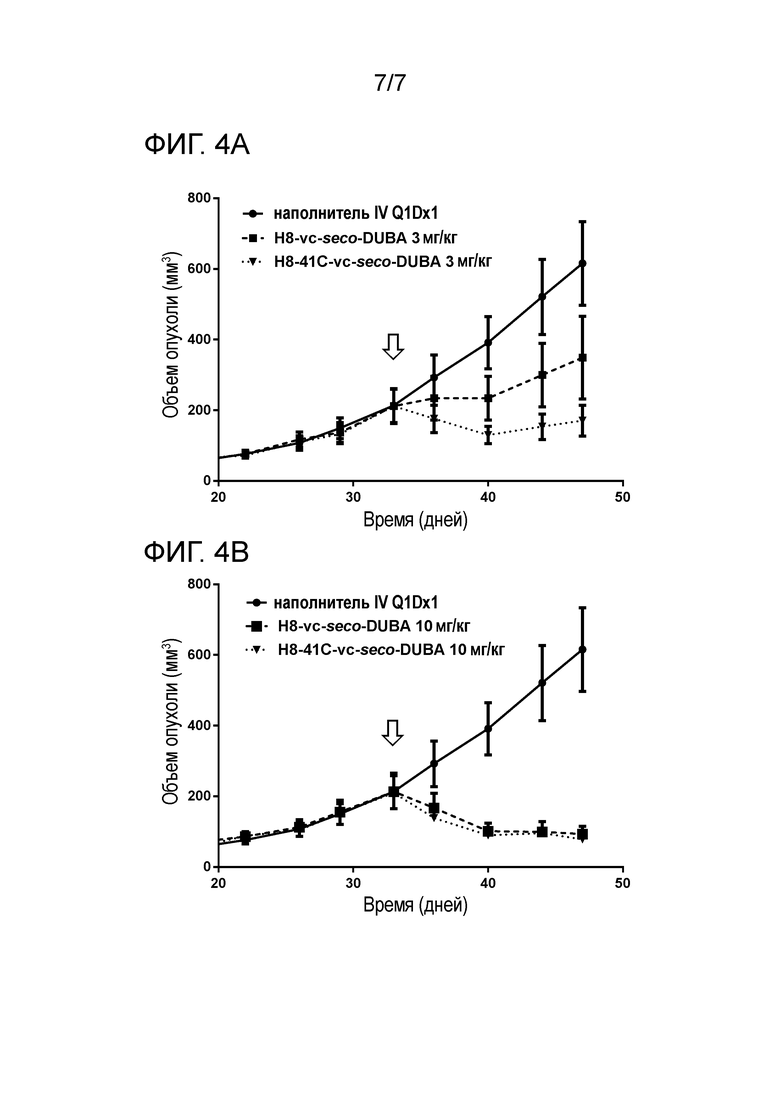
Изобретение относится к конъюгатам антитело-лекарственное средство для лечения солидных опухолей и гематологических злокачественных образований, в котором лекарственное средство с линкером сайт-специфичным образом конъюгировано с антителом или его антигенсвязывающим фрагментом, которое связывается с антигеном-мишенью, экспрессируемом опухолевой клеткой, через встроенный цистеин в указанном антителе или его антигенсвязывающем фрагменте в положении 41 тяжелой цепи согласно нумерации Kabat, где указанное лекарственное средство с линкером представляет собой цитотоксическое средство с линкером. Изобретение расширяет арсенал средств для лечения солидных опухолей. 2 н. и 13 з.п. ф-лы, 4 ил., 7 табл., 1 пр.
1. Соединение конъюгат антитело-лекарственное средство для лечения солидных опухолей и гематологических злокачественных образований, в котором лекарственное средство с линкером сайт-специфичным образом конъюгировано с антителом или его антигенсвязывающим фрагментом, которое связывается с антигеном-мишенью, экспрессируемом опухолевой клеткой, через встроенный цистеин в указанном антителе или его антигенсвязывающем фрагменте в положении 41 тяжелой цепи согласно нумерации Kabat, где указанное лекарственное средство с линкером представляет собой цитотоксическое средство с линкером.
2. Соединение по п. 1, дополнительно содержащее встроенный цистеин в позиции 375 в части Fc указанного антитела или его антигенсвязывающего фрагмента, согласно нумерации Eu.
3. Соединение по п. 1 или 2, в котором указанное лекарственное средство с линкером содержит производную дуокармицина.
4. Соединение по любому из пп. 1-3 с формулой (I) 
при этом n составляет 0-3, m представляет среднее DAR от 1 до 6, R1 выбирается из

y равно 1-16 и R2 выбирается из
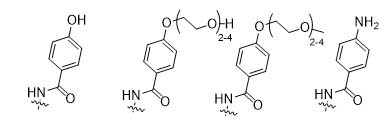 .
.
5. Соединение по п. 4, в котором n составляет 0-1, m представляет среднее DAR от 1,5 до 2, R1 представляет собой
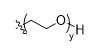
y равно 1-4 и R2 выбирается из
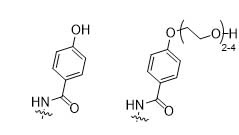 .
.
6. Соединение по любому из пп. 1-5 с формулой (II)
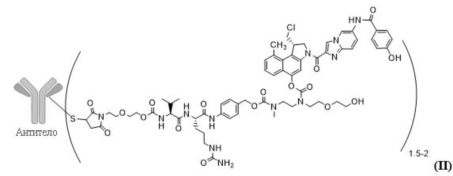
7. Соединение по любому из пп. 1-6, в котором указанное антитело или его антигенсвязывающий фрагмент связывается с антигеном-мишенью, который экспрессирован в или на клеточной мембране опухолевой клетки, и при этом указанное антитело или его антигенсвязывающий фрагмент поглощается клеткой после связывания с указанной целью.
8. Соединение по любому из пп. 1-7, в котором указанное антитело представляет собой антитело против аннексина A1, антитело против CD115, антитело против CD123, антитело против CLL-1, антитело против c-MET, антитело против MUC1, антитело против PSMA, антитело против 5T4 или антитело против TF.
9. Соединение по любому из пп. 1-8, в котором указанное антитело представляет собой моноклональное антитело против PSMA или моноклональное антитело против 5T4.
10. Соединение по п. 9, в котором тяжелая цепь указанного антитела против PSMA содержит последовательность аминокислот с SEQ ID, NO:2, и легкая цепь указанного антитела против PSMA содержит последовательность аминокислот с SEQ ID NO:5.
11. Соединение по п. 9, в котором тяжелая цепь указанного антитела против 5T4 содержит последовательность аминокислот с SEQ ID NO:8, и легкая цепь указанного антитела против 5T4 содержит последовательность аминокислот SEQ ID NO:11.
12. Фармацевтическая композиция для лечения солидных опухолей и гематологических злокачественных образований, содержащая соединение по любому из пп. 1-9 и один или более фармацевтически приемлемых эксципиентов, предпочтительно в форме лиофилизированного порошка.
13. Соединение по любому из пп. 1-11 или фармацевтическая композиция по п. 12 для применения в качестве медикамента.
14. Соединение по любому из пп. 1-11 или фармацевтическая композиция по п. 12 для применения в лечении человеческих солидных опухолей и гематологических злокачественных образований.
15. Соединение или фармацевтическая композиция по п. 14, при этом человеческие солидные опухоли выбираются из группы, состоящей из рака груди, рака желудка, рака ободочной и прямой кишки, рака уротелия, рака яичников, рака матки, рака легких, мезотелиомы, рака печени, рака поджелудочной железы и рака простаты.
| WO 2006034488 A2, 30.03.2006 | |||
| Деев С.М | |||
| Современные технологии создания неприродных антител для клинического применения, ACTA NATURE, 2009. |
Авторы
Даты
2018-10-18—Публикация
2015-05-22—Подача