Изобретение относится к химико-фармацевтической промышленности и может быть использовано при изготовлении лекарственных средств, обладающих регенерирующим и ранозаживляющим действием. Препарат стабилен при хранении, обладает пролонгированным антимикробным и адсорбирующим действием.
Актуальной задачей современной медицины является проблема лечения гнойных ран, что связано с распространенностью ран различной этиологии, гнойными осложнениями, высокой летальностью, большими материальными затратами на лечение. По данным некоторых авторов от всех хирургических заболеваний гнойные осложнения составляют 30-35%, а летальность от них достигает 25%.
Лекарственные препараты на основе ферментов, применяемые при лечении гнойных ран, на российском рынке представлены незначительной группой лекарственных средств. Ферменты, входящие в их состав, способствуют быстрому энзиматическому очищению ран, лизису некроза и сгустков крови. Однако использование многих ферментов в свободном состоянии (в растворе) не дает высокого эффекта, т.к. фермент нестабилен в таких условиях, достаточно быстро инактивируется, не обеспечивает длительного контакта с раневой поверхностью и эффективного всасывания активного вещества. Наиболее эффективными композициями являются гели, мази и повязки, позволяющие при локальном воздействии на рану одновременно влиять на патогенную микрофлору и стимулировать процессы заживления. В хирургической практике широко применяются следующие средства: отечественный препарат "Левомеколь", из зарубежных препаратов "Фибролан", "Ируксол" и "Ируксол моно", курс лечения которыми является достаточно дорогостоящим [Патент RU 2191574, МПК А61Р 17/02, А61K 31/00, опубл. 27.10.2002].
Несмотря на разработку и внедрение новых методов лечения гнойных ран, использование лекарственных средств под повязкой является сегодня основным благодаря его доступности, простоте применения и экономической выгоде.
На сегодняшний день для воздействия на многообразие микроорганизмов, которые вызывают гнойно-воспалительный процесс, используют средства местного применения с антибиотиками и антисептиками. Однако следует отметить, что массовое, а порой бесконтрольное их применение приводит сначала к появлению, а затем к преобладанию в ране резистентной к ним микрофлоры [Патент RU 2542373, МПК А61Р 31/04, А61Р 17/02, А61K 9/06, А61K 47/48, А61K 47/34, А61K 31/4164, А61R 31/14, опубл. 20.02.2015].
Целью изобретения является создание высокоэффективного лекарственного средства, обладающего одновременно противовоспалительным, регенераторным и репаративным действием, позволяющего лечить гнойные и длительно незаживающие раны различной этиологии, не вызывая аллергических реакций.
В качестве прототипа служил СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ГНОЙНО-НЕКРОТИЧЕСКИХ РАН (SU 1814764, МПК А61K 31/557, А61K 47/48, опубл. 20.03.1995), включающий иммобилизацию ферментного препарата, с целью повышения лечебного эффекта средства, иммобилизацию проводили путем обработки 2%-ного геля хитозана 2%-ным раствором глутарового альдегида в фосфатном буфере при рН 7.5, взятых в соотношении 1:1, выдерживания его при температуре 18-20°С в течение 30 мин, после чего пропускали через гель экстракт гепатопанкреаса камчатского краба, содержащего комплекс ферментов.
Технический результат заключается в разработке способа получения нового ранозаживляющего и регенерирующего материала на основе фицина, который позволит сократить расход ранозаживляющего средства благодаря высокой стабильности препарата при температурах выше физиологических и его пролонгированному действию.
Действующим веществом предлагаемого средства является фицин, который обладает противовоспалительным действием и ускоряет процессы регенерации тканей. Фицин (КФ 3.4.22.3) - протеолитический фермент, выделенный из плодов, стеблей и листьев тропических растений рода Ficus, принадлежит к группе цистеиновых протеаз. Фермент имеет широкую субстратную специфичность и гидролизует казеин с большей скоростью, чем папаин или трипсин; предпочтительно гидролизует в белках связи тирозина и фенилаланина, в то же время совершенно не наблюдается процесс расщепление по связям аргинина и лизина. Фицин проявляет высокую активность в широком диапазоне значений рН (6.5-9.5). Его изоэлектрическая точка составляет 9.0. Фермент устойчив к денатурирующему влиянию мочевины, инактивируется при 80°С. Способность фицина воздействовать на белковые компоненты как мышечной, так и соединительной тканей делает фермент перспективным для медицины и ветеринарии, при этом он действует гораздо более эффективно, чем папаин и бромелайн [Мосолов В.В. Протеолитические ферменты. - М.: Наука, 1971. - 404 с.]. Кроме того, в качестве носителя для иммобилизации фицина (основы повязки) нами были выбраны ионообменные волокна ВИОН - ранозаживляющие материалы, характеризующиеся высокой степенью сорбции, очищающие и дезинфицирующие рану [Патент RU 2229311, МПК A61L 15/00, A61L 15/16, A61L 15/22, опубл. 27.05.2004].
Технический результат достигается тем, что в способе получения гетерогенного препарата на основе фицина, обладающего ранозаживляющими и регенерирующими свойствами, включающем иммобилизацию ферментного препарата в буферном растворе, инкубирование и промывку, согласно изобретению, иммобилизацию фицина проводят на матрицу ионообменных волокон ВИОН КН-1 в соотношении 20 мл раствора фермента в концентрации 1 мг/мл на 1 г волокон; в качестве буферного раствора для иммобилизации на ВИОН КН-1 используют трис-HCl буфер (рН 7.0); инкубация проводится в течение 24 часов при комнатной температуре с периодическим перемешиванием; образовавшийся осадок промывают использованным при иммобилизации буфером до отсутствия в промывных водах белка.
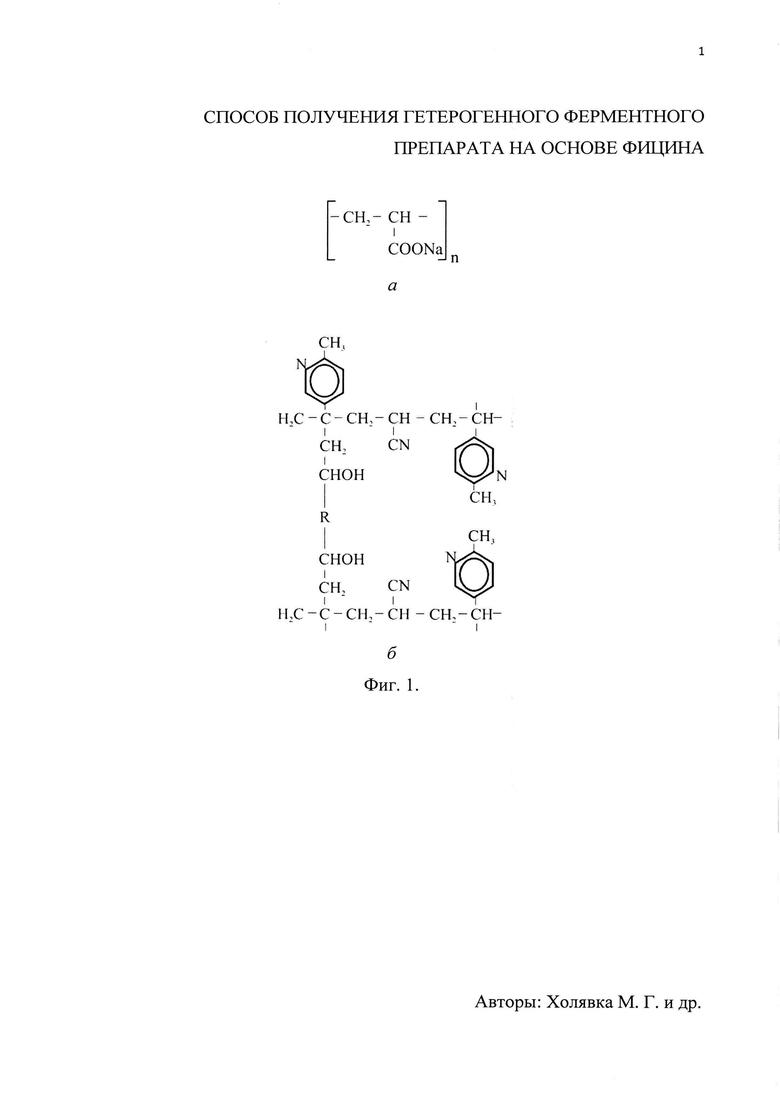
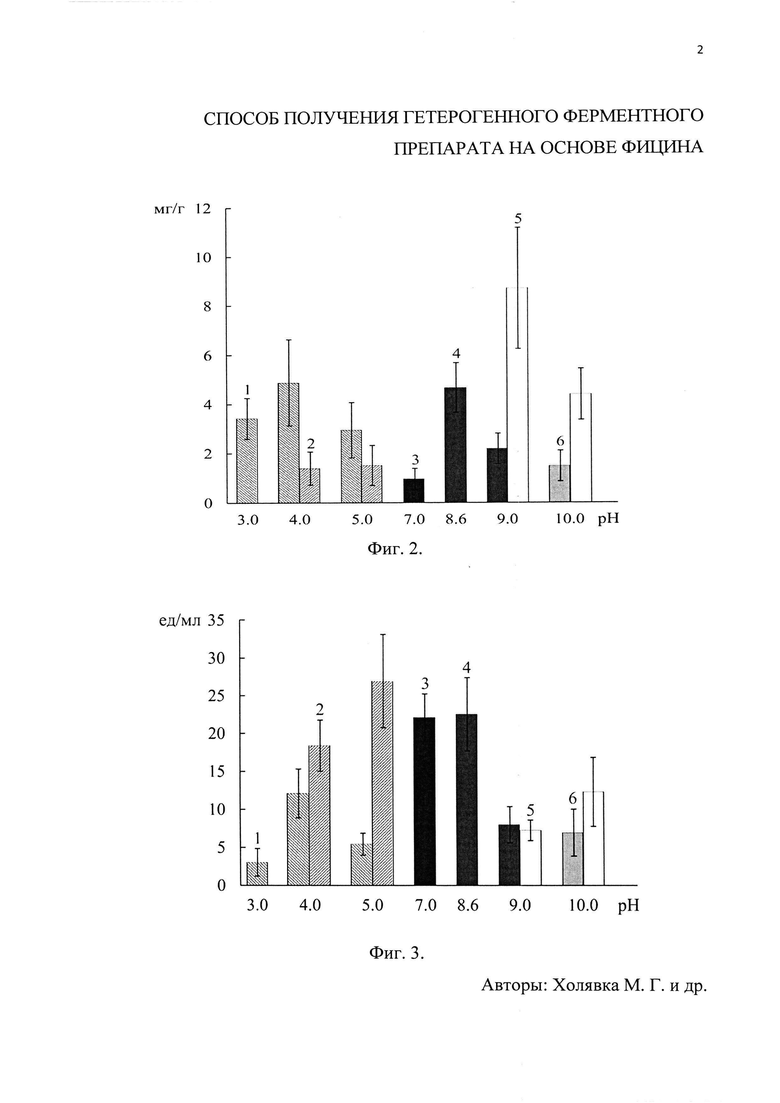
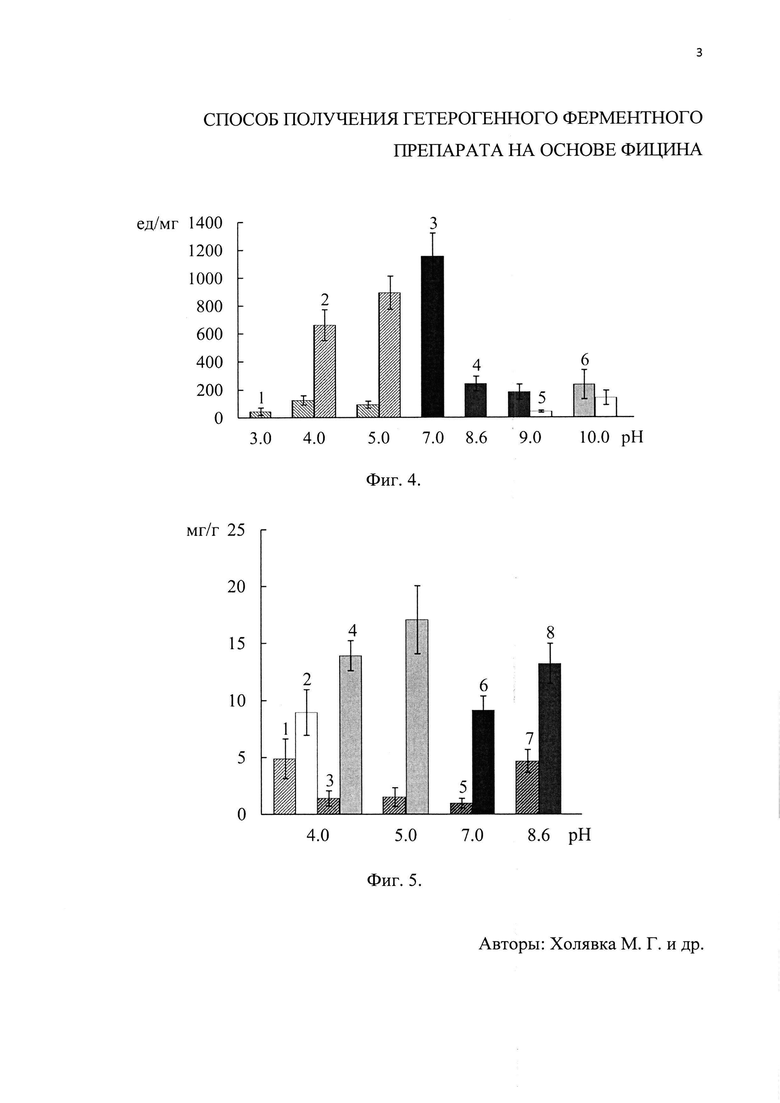
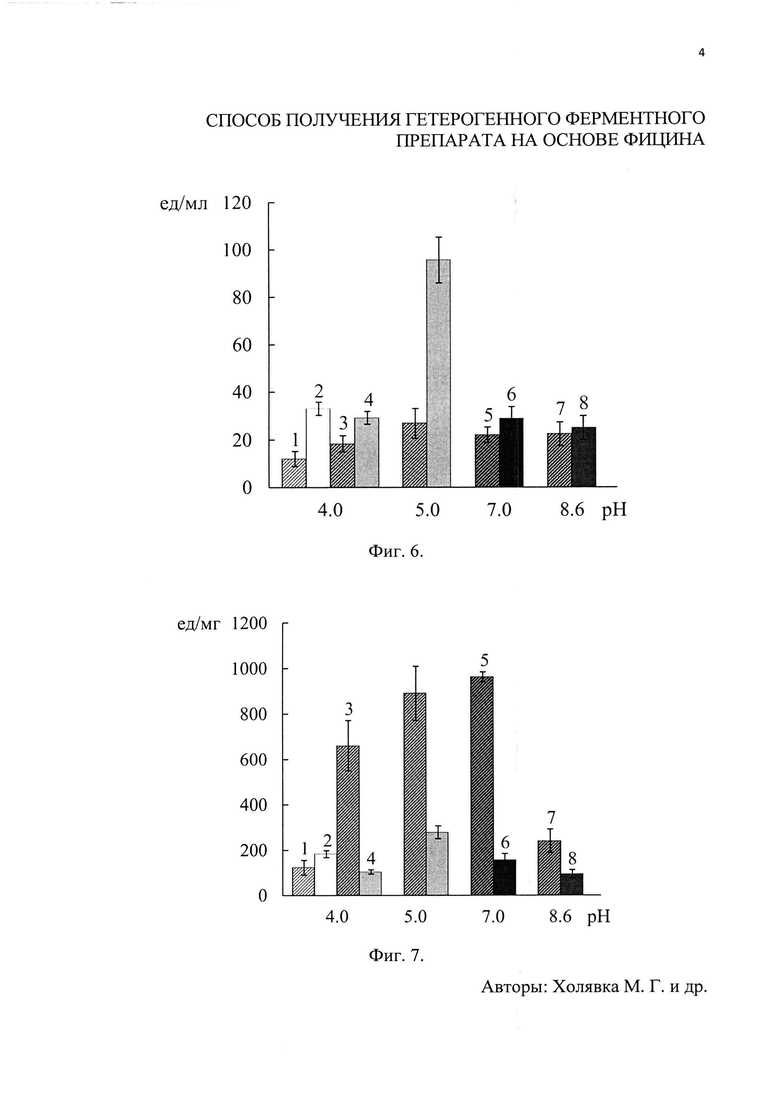
Фиг. 1. Структура элементарного звена катеонита ВИОН КН-1 (а) и анионита ВИОН АН-1 (б). Фиг. 2. Приведена диаграмма содержания белка в препаратах фицина, иммобилизованных на ВИОН КН-1: цитратный. 2 - ацетатный, 3 - трис-HCl, 4 - глициновый, 5 - боратный, 6 - боратный с добавлением КСl. Фиг. 3. Приведена диаграмма общей активности препаратов фицина, иммобилизованных на ВИОН КН-1: цитратный. 2 - ацетатный, 3 - трис-НСl, 4 - глициновый, 5 - боратный, 6 - боратный с добавлением КСl. Фиг. 4. Приведена диаграмма удельной активности препаратов фицина, иммобилизованных на ВИОН КН-1: цитратный. 2 - ацетатный, 3 - трис-НСl, 4 - глициновый, 5 - боратный, 6 - боратный с добавлением КСl. Фиг. 5. Приведена диаграмма содержания белка в препаратах фицина, иммобилизованных на ВИОН КН-1: 1 - цитратный (1 мг/мл), 2 - цитратный (10 мг/мл), 3 - ацетатный (1 мг/мл), 4 - ацетатный (10 мг/мл), 5 - трис-НСl (1 мг/мл), 6 - трис-НСl (10 мг/мл), 7 - глициновый (1 мг/мл), 8 - глициновый (10 мг/мл). Фиг. 6. Приведена диаграмма общей активности препаратов фицина, иммобилизованных на ВИОН КН-1: 1 - цитратный (1 мг/мл), 2 - цитратный (10 мг/мл), 3-ацетатный (1 мг/мл), 4 - ацетатный (10 мг/мл), 5 - трис-НСl (1 мг/мл), 6 - трис-НСl (10 мг/мл), 7 - глициновый (1 мг/мл), 8 - глициновый (10 мг/мл). Фиг. 7. Приведена диаграмма удельной активности препаратов фицина, иммобилизованных на ВИОН КН-1: 1 - цитратный (1 мг/мл), 2 - цитратный (10 мг/мл), 3 - ацетатный (1 мг/мл), 4 - ацетатный (10 мг/мл), 5 - трис-НСl (1 мг/мл), 6 - трис-НСl (10 мг/мл), 7 - глициновый (1 мг/мл), 8 - глициновый (10 мг/мл).
В качестве объекта исследования был выбран фицин быка фирмы «Sigma-Aldrich», субстратом для гидролиза служил азоказеин фирмы «Sigma-Aldrich», носителями для иммобилизации - ионообменные волокна ВИОН КН-1 и ВИОН АН-1 (фиг. 1А и 1Б, соответственно). Содержание белка в препаратах определяли методом Лоури [Lowry О.Н., Rosebrough N.J., Faar A.L., Randall R.J. Protein measurement with folin-phenol reagent // J. Biol. Chem. - 1951. - V. 193. - P. 265-275.]. Методики подготовки носителей подробно описаны в работе [Kovaleva Т.A., Kholyavka M.G., Takha A.S. Development of a Heterogenous Biocatalyst on the basis of Immobilized Inulinase Preparation from Kluyveromyces marxianus // Biotechnology in Russia. - 2007. - №3. - P. 106-116]. Статистическую обработку полученных результатов проводили при уровне значимости 5% с использованием t-критерия Стьюдента.
На первом этапе экспериментов для получения гетерогенных биокатализаторов на основе фицина, иммобилизованного на матрице ионообменных волокон ВИОН КН-1 и ВИОН АН-1, в качестве иммобилизационной среды мы использовали следующие буферные растворы: 0.05 М глициновый (рН 8.6-10.0), 0.2 М ацетатный (рН 4.0-5.0), 0.1 М цитратный (рН 3.0-6.0), 0.1 фосфатный (рН 6.0-8.0), 0.05 М боратный буфер с добавлением KCl (рН 8.0-10.0), 0.1 М боратный буфер без добавления KCl (8.0-10.0) и 0.05 М трис-HCl буфер (рН 7.0-9.3), 0.1 карбонатный (9.0-10.0).
В ходе выполнения эксперимента по определению содержания белка было выявлено, что сорбция белка на матрице ионообменного волокна ВИОН КН-1 происходит при использовании цитратного (рН 3.0-4.0), ацетатного (4.0-5.0), трис-HCl (рН 7.0), глицинового (рН 8.6-9.0), боратного (рН 9.0-10.0) и боратного с добавлением KCl (рН 10.0) буферов.
Установлено, что наибольшее содержание белка (в мг на г носителя) в препаратах фицина, иммобилизованных на матрице ионообменных волокон ВИОН КН-1, наблюдается при иммобилизации в следующих буферных растворах: цитратный (рН 3.0-4.0), глициновый (рН 8.6), боратный (рН 9.0-10.0) (фиг. 2).
Высокую общую активность (в ед на мл раствора) показали препараты фицина, приготовленные с помощью ацетатного буфера (рН 4.0 и 5.0), трис-HCl буфера (рН 7.0) и глицинового буфера (рН 8.6) (фиг. 3).
Максимальная удельная активность (в ед на мг белка) гетерогенного биокатализатора на основе фицина, сорбированного на матрице ионообменного волокна ВИОН КН-1, наблюдается при использовании ацетатного буфера (рН 5.0) и трис-HCl буфера (рН 7.0) (фиг. 4).
При разработке гетерогенного биокатализатора на основе фицина, иммобилизованного на матрице ионообменного волокна ВИОН АН-1, выяснилось, что активность полученных препаратов существенно ниже, чем при иммобилизации фермента на ВИОН КН-1, поэтому в дальнейших исследованиях ВИОН АН-1 не использовался.
На втором этапе эксперимента мы увеличили концентрацию фицина в иммобилизационной среде в 10 раз и использовали цитратный (рН 4.0.), ацетатный (рН 4.0-5.0), трис-HCl (рН 7.0) и глициновый (рН 8.6) буферы. Наибольшее содержание белка (по сравнению с препаратами, где исходная концентрация белка в иммобилизационной системе равнялась 1 мг/мл) наблюдалось в препаратах, сорбированных с использованием следующих буферных систем: ацетатный (рН 4.0-5.0), трис-HCl (рН 7.0) и глициновый (рН 8.6) буферы (фиг. 5). Удельная активность гетерогенных биокатализаторов с концентрацией фермента 10 мг/мл в ходе иммобилизации оказалась существенно ниже по сравнению с препаратами, полученными при концентрации энзима 1 мг/мл. Общая активность образцов при использовании концентрации фицина 10 мг/мл была выше лишь для ацетатного буфера (рН 5.0) в сравнении с концентрацией 1 мг/мл (фиг. 6 и 7).
Технология синтеза ВИОН КН-1, тканых и нетканых прошивных полотен из него известна и легко осуществима на заводах по производству полиакрилонитрильного волокна [Патент RU 2102544, МПК D01F 11/04, C08J 5/20, опубл. 20.01.1998]. Сочетание недорогих компонентов позволит сделать доступным этот технологичный метод для отечественных лабораторий.
Известно, что иммобилизация фермента на нерастворимом носителе позволяет решить несколько важных задач для медицины: 1) получение препаратов пролонгированного действия, благодаря стабилизации и увеличению времени полужизни фермента, 2) решение проблемы диффузии вещества в организме, 3) направленное регулирование оптимумов функционирования препарата (температурный оптимум, оптимум рН).
Нами разработана методика получения ранозаживляющего и регенерирующего гетерогенного препарата медицинского и ветеринарного назначения на основе фицина и ионообменного волокна ВИОН КН-1. Препарат обладает выраженным разрушающим эффектом по отношению к бактериальным биопленкам, что характеризует его как эффективное средство борьбы с гнойными осложнениями ран, вызванными микроорганизмами различных таксономических групп. Кроме того, препарат не проявляет цито- и генотоксических свойств по отношению к клеткам пациентов.
Предлагаемый нами продукт - современная безопасная альтернатива антибиотикам и химиопрепаратам при лечении ран и раневых инфекций, в том числе устойчивых к действию антибиотиков.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОГЕННОГО ПРЕПАРАТА НА ОСНОВЕ ПАПАИНА | 2017 |
|
RU2677873C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОГЕННОГО ПРЕПАРАТА НА ОСНОВЕ БРОМЕЛАЙНА, ОБЛАДАЮЩЕГО РАНОЗАЖИВЛЯЮЩИМИ СВОЙСТВАМИ | 2017 |
|
RU2677343C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННОГО ПРЕПАРАТА БРОМЕЛАЙНА И АЛЬГИНАТА НАТРИЯ В ВИДЕ ГУСТОГО РАСТВОРА | 2022 |
|
RU2792785C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ФИЦИНА В ГЕЛЕ НА ОСНОВЕ КАРБОКСИМЕТИЛЦЕЛЛЮЛОЗЫ | 2021 |
|
RU2771183C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОГЕННОГО ФЕРМЕНТНОГО ПРЕПАРАТА НА ОСНОВЕ ФИЦИНА И НИЗКОМОЛЕКУЛЯРНОГО ХИТОЗАНА | 2021 |
|
RU2769243C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОГЕННОГО ПРЕПАРАТА РАЗЛИЧНОЙ ДИСПЕРСНОСТИ НА ОСНОВЕ БРОМЕЛАЙНА И ХИТОЗАНА | 2017 |
|
RU2677232C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИБРИДНОГО ПРЕПАРАТА БРОМЕЛАЙНА И КАРБОКСИМЕТИЛЦЕЛЛЮЛОЗЫ В ВИДЕ ГУСТОГО РАСТВОРА | 2022 |
|
RU2788454C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИБРИДНОГО ПРЕПАРАТА ПАПАИНА И КАРБОКСИМЕТИЛЦЕЛЛЮЛОЗЫ В ВИДЕ ГУСТОГО РАСТВОРА | 2022 |
|
RU2795425C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННОГО ПРЕПАРАТА ПАПАИНА И АЛЬГИНАТА НАТРИЯ В ВИДЕ ГУСТОГО РАСТВОРА | 2022 |
|
RU2788455C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИБРИДНОГО ПРЕПАРАТА ФИЦИНА И N-МАЛЕОИЛХИТОЗАНА В ВИДЕ ГУСТОГО РАСТВОРА | 2022 |
|
RU2792784C1 |
Изобретение относится к области медицины и химико-фармацевтической промышленности, а именно к способу получения средства на основе фицина, обладающего ранозаживляющим и регенерирующим действием, согласно которому осуществляют иммобилизацию фицина в буферном растворе на матрицу ионообменных волокон ВИОН КН-1 в соотношении 20 мл буферного раствора фицина в концентрации 1 мг/мл на 1 г волокон, при этом в качестве буферного раствора используют 0.05 М трис-HCl буфер с рН 7,0; далее проводят инкубирование в течение 24 часов при комнатной температуре с периодическим перемешиванием; а затем промывают образовавшийся осадок 0.05 М трис-HCl буфером с рН 7,0 до отсутствия в промывных водах фицина. Изобретение обеспечивает сокращение расхода ранозаживляющего средства за счет его высокой стабильности и пролонгированного действия. 7 ил.
Способ получения средства, обладающего ранозаживляющим и регенерирующим действием, на основе фицина, включающий иммобилизацию фицина в буферном растворе на матрицу ионообменных волокон ВИОН КН-1 в соотношении 20 мл буферного раствора фицина в концентрации 1 мг/мл на 1 г волокон, при этом в качестве буферного раствора используют 0.05 М трис-HCl буфер с рН 7,0; инкубирование в течение 24 часов при комнатной температуре с периодическим перемешиванием; промывание образовавшегося осадка 0.05 М трис-HCl буфером с рН 7,0 до отсутствия в промывных водах фицина.
| Холякова М.Г | |||
| и др | |||
| Гетерогенные биокатализаторы на основе фицина, иммобилизованного на матрице хитозана / МЕДИАЛЬ, 2015, Т.15, N.1, с.293 | |||
| Холякова М.Г | |||
| и др | |||
| Гетерогенные биокатализаторы на основе трипсина, иммобилизованного на матрице ионообменных волокон / МЕДИАЛЬ, 2015, Т.15, N.1, с.294 | |||
| Yildiz H | |||
| et al | |||
| Catalase immobilization in cellulose acetate beads and determination of its hydrogen peroxide decomposition level by using a catalase biosensor / Artificial Cells Blood Substitutes and Biotechnology, 2004, V.32, N.3, pp.443-452 | |||
| Ташмухамедова Ш.С | |||
| и др | |||
| ИФА стафилококкового токсина с применением полиамидных микропористых мембран / Вопросы медицинской химии, 1996, Т.42, N.1, с.39-45 | |||
| РАНОЗАЖИВЛЯЮЩИЙ МАТЕРИАЛ | 2001 |
|
RU2229311C2 |
Авторы
Даты
2019-01-22—Публикация
2017-07-03—Подача