Изобретение относится к медицине, а именно к ортопедии, и может быть использовано для пластики дефектов крупных трубчатых костей (бедренной, большеберцовой и плечевой), образовавшихся после удаления эндостально расположенных очаговых опухолеподобных новообразований и заболеваний.
Востребованность использования заявляемого способа возникает в случаях патологического перелома кортикальной пластины, либо ее тотального поражения патологическим процессом. При этом возникает необходимость использования трансплантата для закрытия дефекта, в т.ч. и гранул биокомпозита, используемого для пластики полостей. Кроме того, иногда интраоперационно возникает необходимость дозаполнения костной полости, в то время, как количество биокомпозитного материала ограничено.
Известен способ пластики дефекта при новообразованиях метаэпифизарной зоны большеберцовой кости («Способ замещения костного дефекта при новообразованиях метаэпифизарной зоны большеберцовой кости», авторы: Николаенко А.Н., Котельников Г.П., Иванов В.В. / Патент РФ 2559135, 10.08.2015, бюл. 22), где для пластики дефекта используют два костных аутотрансплантата определенных размеров, взятых из гребня подвздошной кости и из малоберцовой кости в сочетании с сосудистым пучком и участком мышцы сгибателя большого пальца, устанавливаемых враспор один относительно друг друга. Способ-аналог позволяет осуществлять пластику дефекта только большеберцовой кости и только с использованием двух аутотрансплантатов, для взятия которых, требуются два автономных оперативных доступа. Кроме того, васкуляризация зоны костного дефекта увеличивает время операции.
Известен способ пластики дефектов костей («Способ пластики дефекта кости», авторы: Малахов О.А., Омельяненко Н.П., Кожевников О.В., Петров И.А., Карпов И.Н., / Патент РФ 2012271 15.05.1994, бюл. №14), где для закрытия дефекта используют плечевую кость человеческого плода (выкидыш 15-25 недель) на сосудистой ножке из подключичных сосудов. При такой пластике накладывают микроанастомозы между сосудами трансплантата и реципиента. Данный способ-аналог требует забора специфического трансплантата, получение которого связано с различными медицинскими, этическими и юридическими трудностями, для наложения микрососудистых анастомозов необходимо наличие в операционной сосудистого хирурга и специального оборудования.
Известен способ костной пластики («Способ костной пластики», авторы: Давыдов Б.Н., Соловьев В.А., Сулейманов А.Б., Шинкаренко Т.В. / Патент РФ 2185791 27.07.2002, бюл. №21) с использованием для закрытия дефекта кости костного регенерата на питающей ножке, образованного через 20-25 дней под надкостницей у места дефекта кости после введения туда остеопластического материала (Коллапан-Л). Недостатком такого способа-аналога является необходимость повторного оперативного вмешательства для замещения дефекта кости образовавшимся регенератом. Кроме того, площадь образовавшегося регенерата может быть недостаточна для замещения обширного костного дефекта.
Наиболее близким техническим решением является известный способ замещения дефектов костей у детей («Способ замещения дефектов костей у детей», автор: Давыдов Б.Н. / Авторское свидетельство №814344 от 23.03.81 г., бюл. №9), при котором, образующуюся после удаления эндостального образования, костную полость заполняют консервированным аллотрансплантатом, причем надкостницу по краям дефекта отслаивают. Затем обнажают послойно переднюю поверхность большеберцовой кости и выкраивают участок надкостницы, равный по длине костному дефекту, шириной 5-10 мм. Далее свободные надкостничные трансплантаты укладывают на аллотрансплантат и подшивают к отслоенной надкостнице. Предлагаемый способ-прототип не позволяет добиться прочной фиксации трансплантата в костной полости, что особенно актуально при использовании мелких гранул биокомпозитных материалов, используемых для замещения костной полости. Кроме того, при наличии значительного дефекта кости без надкостницы остается значительных размеров донорский участок большеберцовой кости. Описанная авторами методика позволяет брать надкостницу только с поверхности большеберцовой кости, при локализации дефекта в других костях это делает необходимым дополнительное хирургическое вмешательство для взятия надкостницы.
Цель изобретения заключается в улучшении качества фиксации трансплантата, заполняющего полость после удаления новообразования, а также снижении травматичности операции.
Поставленная цель достигается тем, что полость трубчатой кости после удаления патологического очага очищают от измененных тканей до здоровой кости, обрабатывают растворами антисептика и заполняют туго биокомпозитными гранулами, отличающееся тем, что над зоной патологического процесса и донорским участком кости производят два разделенных между собой Н-образных рассечения надкостницы, отслаивают и разводят ее в виде П-образных лоскутов, после чего зона дефекта закрывается округлой, по внешней поверхности, пластиной-крышкой (аутотрансплантатом, взятым с донорского участка), имеющей толщину в половину кортикального слоя донорского участка кости, поперечные контуры которой, должны превышать зону дефекта на 2-3 мм, кроме того, формируют несколько кортикальных аутотрансплантатов, которые укладываются среди биокомпозитных гранул в полость образовавшегося дефекта кости, а сформированные лоскуты надкостницы укладывают на трансплантат и донорский участок кости.
Как правило, внутрикостные доброкачественные новообразования и опухолевые заболевания локализуются в кортикальном слое кости и часто не проявляются клинически до патологического перелома кортикальной пластинки в результате ее истончения, когда возникают боли. При этом кортикальная пластинка может как отсутствовать, так и быть настолько измененной патологическим процессом, что ее использование для закрытия костного дефекта после удаления внутрикостного образования становится невозможным. В процессе планирования удаления костного новообразования или опухолеподобного заболевания большеберцовой, бедренной или плечевой костей по данным рентгенограмм и компьютерной томографии пораженной конечности рассчитывают объем новообразования и объем предполагаемой костной полости после его удаления, который бывает несколько больше объема новообразования, поскольку его удаление производят в пределах здоровой кости. В зависимости от предполагаемого объема костной полости заготавливают необходимое количество биокомпозита и планируют место для взятия костной «крышки».
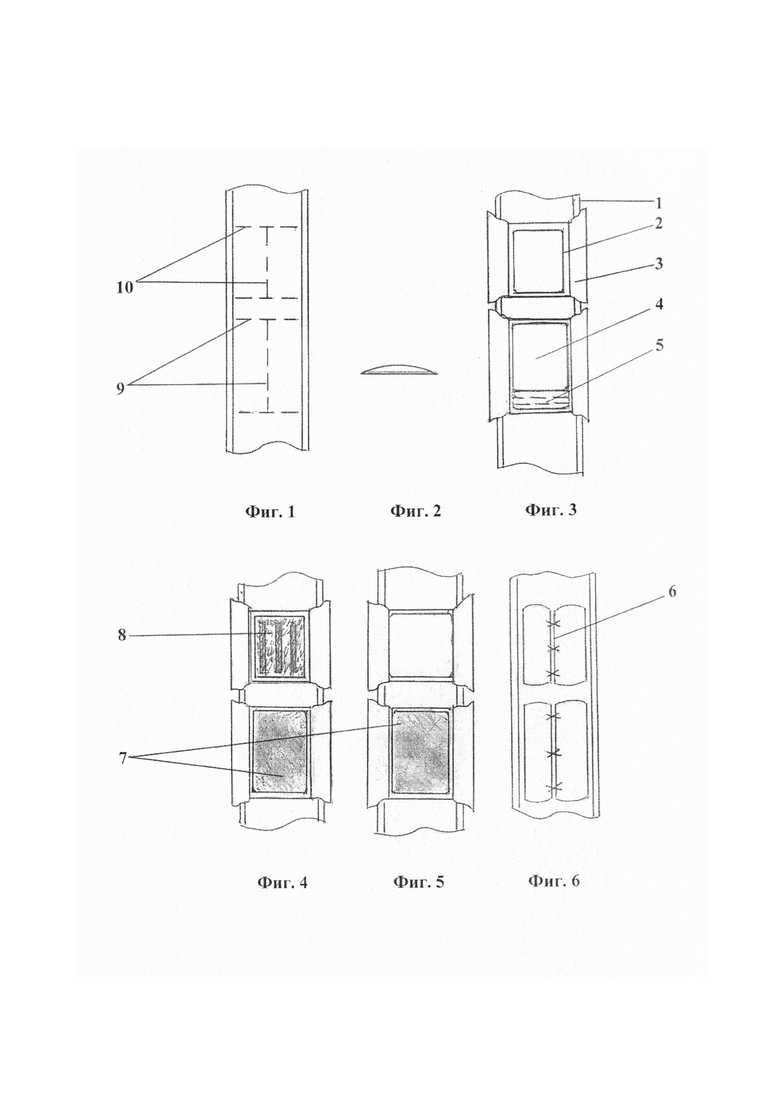
Сущность изобретения поясняется чертежами, где на фиг. 1 показаны планируемые варианты рассечения надкостницы над зонами удаления новообразования 10 и забора пластины-крышки и аутотрансплантатов 9; на фиг. 2 - боковой контур формируемой пластины-крышки, на фиг. 3 - те же зоны 9 и 10, но с развернутыми в стороны П-образными лоскутами надкостницы 3, контурами формируемого дефекта кортикального слоя 2 трубчатой кости (1), формируемых пластины-крышки 4 и трех фрагментов аутотрансплантата 5; на фиг. 4 - показано заполнение дефекта гранулами биокомпозитного материала 8 в прямой проекции и уложенными тремя фрагментами аутотрансплантата, а также зона после забора пластины-крышки 7; на фиг. 5 и 6 - изображены закрытая пластиной-крышкой зона дефекта трубчатой кости, зона забора пластины-крышки 7 до и после укрытия их надкостницей 6.
Способ осуществляется следующим образом. Перед удалением внутрикостного новообразования в его проекции освобождают кость от прилежащих мягких тканей. Н-образно 10 рассекают надкостницу, разводят два П-образных сформированных лоскута 3 надкостницы в противоположные стороны, причем площадь отслойки должна несколько превышать площадь планируемого дефекта 2 кортикального слоя кости 1. После тщательного удаления, внутрикостно расположенного новообразования, сформированную полость обрабатывают растворами антисептиков.
В зависимости от места расположения очага (новообразования), ниже или выше зоны образовавшегося дефекта кости, отступя 10-15 мм освобождают от прилежащих мягких тканей диафиз той же трубчатой кости 1 и вновь Н-образно рассекают 9 надкостницу. Между линиями сечения надкостницы должен быть промежуток 10-15 мм, что сохраняет кровоснабжение надкостницы. Отслаивают и разводят П-образно сформированные лоскуты в стороны. Маятниковой пилой снимают по касательной освобожденный кортикальный слой (в половину его толщины) кости на участке, превышающем на 10-12 мм поперечные размеры получившегося дефекта 2 кости 1 после удаления новообразования. Сформированная пластина-крышка 4 имеет плоское основание и округлую поверхность (фиг. 2). Пилой отсекают от пластины-крышки 4 несколько костных фрагментов 5, с учетом того, что оставшаяся ее часть полностью перекроет в дальнейшем зону дефекта 2 кости.
Полость, образовавшуюся после удаления новообразования, плотно заполняют гранулами биокомпозитного материала 8, куда укладывают и отсеченные 3-4 аутокостных фрагмента 5. Далее, оставшейся частью пластины-крышки 4 накрывают костный дефект 2, образовавшийся после удаления новообразования, поверх уложенного в полость биокомпозитного материала 8. Для плотного прилегания платины-крышки 4 к контурам дефекта, его поколачивают механическим путем с помощью добойника. П-образные лоскуты надкостницы 3 укладывают 6 сверху платины-крышки 4. Подобным образом закрывают надкостницей и донорский участок 7 трубчатой кости 1. Прилежащими мягкими тканями закрывают рану, которую ушивают наглухо.
Отличительной особенностью заявленного способа от прототипа является то, что жесткая кортикальная пластинка в сочетании с туго ушитой над ней надкостницей обеспечивает полноценное и прочное укрытие дефекта трубчатой кости. Сохранение половины кортикального слоя трубчатой кости на донорском участке (толщина кортикального слоя рассчитывается до операции по томограммам) и восстановление покрытия надкостницей не нарушает регенераторные свойства кости, в отличие от прототипа. Кроме того, при заявляемом способе, сформированные костные фрагменты-аутотрансплантаты, уложенные вместе с биокомпозитным материалом, оказывают стимулирующее регенеративное воздействие на кость, а округлая поверхность пластины-крышки восстанавливает первоначальный контур зоны дефекта трубчатой кости. Единый оперативный доступ к зоне дефекта и донорскому участку кости снижает травматичность вмешательства и обеспечивает полноценность пластики дефекта после удаления новообразования кости. Такой способ пластики костного дефекта надежно фиксирует гранулы биокомпозитного материала в костной полости, предотвращает их миграцию в послеоперационном периоде, способствует быстрейшему восстановлению кортикального слоя кости над костным дефектом и не затрудняет регенерацию кости в донорской зоне из-за восстановления целостности надкостницы.
Клинический пример применения заявляемого способа:
Пациент Т-н, 12 лет, находился на лечении по поводу: Очаговой монооссальной фиброзной дисплазии верхней трети правой большеберцовой кости. 06.10.16. выполнена операция - расширенная биопсия образования, аутопластика кортикальной пластинкой правой большеберцовой кости. По медиальной поверхности метафиза большеберцовой кости выполнена трепанация, удалена истонченная и патологически измененная кортикальная пластина размером 3,5*2,2*1,0 см. По удалению метафизарной ткани выявлена патологическая фиброзная ткань желто-коричневого цвета. Измененная ткань удалена, образовавшееся полость выскоблена до здоровой кости и обработана спиртовым раствором хлоргексидина, йодонатом. По латеральной поверхности большеберцовой кости тангенциально из кортикального слоя выкроена пластина-крышка 4,5*2,5 см. От нее отсечены три аутотрансплантата шириной по 0,3 см. Полость туго заполнена биокомпозитным материалом (в данном случае использован "TriCaFor") в виде гранул, среди которых, уложены три сформированных аутотрансплантата. Далее на дефект кости уложена платина-крышка и укрыта, как и донорский участок кости, надкостницей. Рана ушита наглухо. Рентгенологический контроль с использованием ЭОП: образование удалено радикально, вся полость заполнена трансплантатом. Иммобилизация окончатым гипсовым сапогом до средней трети бедра. Послеоперационный период протекал удовлетворительно, вертикализирован на вторые сутки после операции, ходьба с опорой на костыли. Через две недели после операции передвигается на костылях самостоятельно, на рентгенконтроле от 10.11.16. приживляемость биокомпозита и костной пластины-крышки удовлетворительная. Гипсовый сапог снят через месяц после операции и назначен реабилитационный курс.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВОССТАНОВЛЕНИЯ ДЕФЕКТА МЕТАДИАФИЗАРНОГО ОТДЕЛА ТРУБЧАТОЙ КОСТИ | 2018 |
|
RU2697371C1 |
| СПОСОБ КОСТНОЙ ПЛАСТИКИ | 1991 |
|
RU2092123C1 |
| Способ получения кортикально-губчатого аутотрансплантата с крыла подвздошной кости и устройство для его осуществления | 2020 |
|
RU2765433C2 |
| СПОСОБ СВОБОДНОЙ КОСТНОЙ ПЛАСТИКИ ЛОЖНЫХ СУСТАВОВ ДЛИННЫХ ТРУБЧАТЫХ КОСТЕЙ | 2013 |
|
RU2534524C1 |
| СПОСОБ ЛЕЧЕНИЯ ГНОЙНЫХ ОСЛОЖНЕНИЙ И ЗАБОЛЕВАНИЙ КОСТЕЙ С ДЕФЕКТОМ МЯГКИХ ТКАНЕЙ | 1994 |
|
RU2106121C1 |
| Способ непосредственной дентальной имплантации | 2017 |
|
RU2652585C1 |
| СПОСОБ ЗАБОРА АУТОТРАНСПЛАНТАТА ИЗ ГРЕБНЯ ПОДВЗДОШНОЙ КОСТИ | 2016 |
|
RU2625783C1 |
| СПОСОБ КОСТНОЙ ПЛАСТИКИ | 2007 |
|
RU2345724C2 |
| СПОСОБ ПЛАСТИКИ АЛЬВЕОЛЯРНОГО ОТРОСТКА ВЕРХНЕЙ ЧЕЛЮСТИ У ДЕТЕЙ ПРИ ВРОЖДЕННОЙ РАСЩЕЛИНЕ ГУБЫ, НЕБА И АЛЬВЕОЛЯРНОГО ОТРОСТКА | 2015 |
|
RU2594945C1 |
| Способ кожно-костной реконструкции пальца кисти и направитель для его осуществления | 2020 |
|
RU2747694C1 |
Изобретение относится к медицине, а именно к травматологии и ортопедии и может быть применимо для пластики дефекта трубчатой кости. Над зоной патологического процесса и донорским участком кости производят два, разделенных между собой, Н-образных рассечения надкостницы, отслаивают и разводят ее в виде П-образных лоскутов. Зона дефекта закрывается округлой, по внешней поверхности, пластиной-крышкой, т.е. аутотрансплантатом, взятым с донорского участка, имеющей толщину в половину кортикального слоя донорского участка кости, поперечные контуры которой должны превышать зону дефекта на 2-3 мм. Укладывают сформированные из оставшейся части аутотрансплантата кортикальные пластины среди биокомпозитных гранул в полость образовавшегося дефекта кости. Сформированные лоскуты надкостницы укладывают на пластину-крышку и донорский участок кости. Способ позволяет уменьшить травматичность операции, улучшить фиксацию трансплантата. 1 пр., 6 ил.
Способ пластики дефекта трубчатой кости, заключающийся в едином операционном доступе к зоне дефекта и донорскому участку, включающий очищение костной полости после удаления патологического очага до здоровой кости, обработку растворами антисептика и тугое ее заполнение трансплантатом, отличающийся тем, что над зоной патологического процесса и донорским участком кости производят два, разделенных между собой, Н-образных рассечения надкостницы, отслаивают и разводят ее в виде П-образных лоскутов, после чего зона дефекта закрывается округлой, по внешней поверхности, пластиной-крышкой, т.е. аутотрансплантатом, взятым с донорского участка, имеющей толщину в половину кортикального слоя донорского участка кости, поперечные контуры которой должны превышать зону дефекта на 2-3 мм, кроме того, из оставшейся части аутотрансплантата формируют кортикальные пластины, которые укладываются среди биокомпозитных гранул в полость образовавшегося дефекта кости, а сформированные лоскуты надкостницы укладывают на пластину-крышку и донорский участок кости.
| Способ замещения дефектовКОСТЕй у дЕТЕй | 1979 |
|
SU814344A1 |
| Теодолит | 1932 |
|
SU47640A1 |
| ВОЛКОВ М.В | |||
| и др | |||
| Детская ортопедия | |||
| М., "Медицина", 1980, c.235 | |||
| WENHAO WANG et al | |||
| Bone grafts and biomaterials substitutes for bone defect repair: A review | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2019-05-24—Публикация
2018-01-17—Подача