Область техники, к которой относится изобретение
Настоящее изобретение относится к способу производства кристаллических частиц антимускаринового лекарственного средства с помощью гидродинамической кавитации. Размер этих кристаллических частиц можно контролировать с помощью параметров способа, и он может лежать в диапазоне между 0,5 и 15 микрон.
Упомянутые частицы подходят для применения в получении фармацевтических композиций для предупреждения и/или лечения респираторных заболеваний.
Уровень техники изобретения
Известно, что водорастворимые соединения четвертичного аммония с антимускариновой активностью склонны к слипанию во время хранения; это объясняется образованием кристаллических мостиков между соседними частицами из-за поглощения влаги после микронизации и последующей рекристаллизации поверхностного аморфного содержимого, которое создается высокоэнергетичным процессом микронизации. Эта проблема особенно влияет на физическую стабильность лекарственного средства и его последующую эффективность в композициях.
Гликопирроний является антимускариновым лекарственным средством, много лет коммерчески доступным в виде бромида.
Бромид гликопиррония имеет два хиральных центра, что соответствует четырем изомерным формам, содержащим 2 пары диастереоизомеров, а именно (3S,2'R)-, (3R,2'S)-, (3R,2'R)- и (3S,2'S)-[(циклопентилгидроксифенилацетил)окси]-1,1-диметилпирролидиния бромиду. Коммерчески доступный гликопиррония бромид состоит из очищенных "трео" диастереоизомеров (3R,2'S) и (3S,2'R) и ниже в данном документе обозначается как rac-гликопиррония бромид.
Однако, как и другие антимускариновые средства, соли гликопиррония имеют значительные проблемы со стабильностью, особенно сразу после обычных процессов микронизации путем перемалывания.
Фактически, гликопиррония бромид после микронизации имеет сильную склонность к агрегации и/или слипанию, что серьезно затрудняет последующую обработку лекарственного средства, в частности получение сухих порошкообразных композиций для введения с помощью ингаляции, способных к доставке хорошей вдыхаемой фракции.
Для изменения некоторых физико-химических свойств лекарственного средства были предложены различные способы. Однако многие из этих способов связаны с использованием растворителей, которые, как правило, вызывают локальные процессы сольватации, которые, в свою очередь, приводят к росту частиц и/или необратимым агрегации и слипанию во время сушки или хранения.
Кроме того, хорошо известно, что процедуры высокоэнергетической физической обработки современного уровня техники, такие как воздушно-струйное перемалывание, шаровое перемалывание сухого порошка или гомогенизация при высоком давлении, приводят к частичной потере кристалличности лекарственного средства. Эти микронизированные материалы после микронизации часто подвергают кондиционированию при высокой температуре в течение длительного времени, для того чтобы исключить любое индуцированное процессом структурное нарушение и/или аморфное содержимое.
Ввиду этих соображений было бы очень выгодно обеспечить способ получения кристаллических частиц гликопиррониевой соли, физически стабильных, с небольшим размером частиц, подходящим для доставки путем ингаляции.
Данная задача решается с помощью способа настоящего изобретения.
Сущность изобретения
В первом аспекте настоящее изобретение относится к способу получения микронизированных кристаллизованных частиц фармацевтически приемлемой соли гликопиррония, причем данный способ содержит этапы:
(a) смешивания, в первой камере приспособления для гидродинамической кавитации с регулируемым потоком, потока F1 раствора, содержащего фармацевтически приемлемую соль гликопиррония и одно или несколько поверхностно-активных веществ, растворенных в растворителе, выбранном из группы, состоящей из 1-бутанола, 2-пропанола и их смесей с этанолом, с одним или несколькими потоками F2 антирастворителя, выбранного из группы, состоящей из диэтилового эфира, н-гептана и метил-трет-бутилового эфира (MTBE) и их смесей;
(b) подвергания смешанных потоков F1 и F2 воздействию локального сужения потока для создания гидродинамической кавитации с регулируемым потоком, что вызывает зародышеобразование и непосредственное образование нанокристаллов соли гликопиррония;
(c) переноса смешанных потоков во вторую камеру упомянутого приспособления для кавитации с регулируемым потоком и дополнительной обработки упомянутых смешанных потоков в течение периода времени, равного или меньшего 10 миллисекунд;
(d) сбора полученных потоков в приемник, содержащий смесь н-гептана и MTBE в отношении в диапазоне от 10:90 об/об до 40:60 об/об, что обеспечивает сборку наночастиц;
(e) сушки частиц для отверждения собранных частиц;
(f) устранения поверхностно-активных веществ; и
(g) дальнейшей сушки полученных микронизированных частиц.
Предпочтительно, поверхностно-активное вещество выбирают из группы, состоящей из лецитина, неиногенных поверхностно-активных веществ таких как Tween® и Span®, поверхностно-активных веществ на основе сахаров, таких как стеарат сахарозы и гексадеканоат сахарозы, и их смесей в любом соотношении.
Во втором аспекте настоящее изобретение относится к способу получения композиции для ингаляции, содержащему этап смешивания вышеуказанных микронизированных частиц с одним или несколькими пропеллентами или носителями.
В третьем аспекте настоящее изобретение относится к композиции для ингаляции под давлением, содержащей микронизированные частицы фармацевтически приемлемой соли гликопиррония, полученные с помощью заявленного способа, суспендированные в сжиженном под давлением пропелленте.
В четвертом аспекте настоящее изобретение относится к компрессорному дозирующему ингалятору (pMDI), заполненному вышеупомянутой композицией.
В пятом аспекте настоящее изобретение относится к сухой порошкообразной композиции, содержащей микронизированные частицы фармацевтически приемлемой соли гликопиррония, полученные с помощью заявленного способа, с частицами физиологически приемлемого фармакологически инертного твердого носителя.
В шестом аспекте настоящее изобретение относится к ингалятору сухого порошка, заполненному вышеупомянутой композицией.
Определения
Термин "приспособление для гидродинамической кавитации с регулируемым потоком" относится к любому приспособлению, подходящему для получения микрочастиц органического материала. Упомянутые устройства известны в данной области техники. Кавитация представляет собой образование пузырьков и полостей внутри потока жидкости, возникающих в результате локализованного падения давления в потоке жидкости. Документ, озаглавленный "Hydrodynamic cavitation as a tool to control macro-, micro- and nano-properties of inorganic materials", J. Find et al (Journal of Materials Research vol. 16, no. 12, December 2001) относится к гидродинамической кавитации для получения твердотельных материалов.
Термин "микронизация" относится к процессу уменьшения среднего диаметра частиц твердого материала. Обычно термин микронизация используют, когда получаемые частицы имеют диаметр только несколько микрометров. Традиционные методы микронизации основаны на использовании трения для уменьшения размера частиц. Такие способы включают в перемалывание и дробление. Уменьшение размера частиц также может происходить в результате столкновения и удара.
Глагол "агрегировать" означает собираться или объединяться вместе. Свежемикронизированные лекарственные средства обычно принимают форму тонкодисперсныого порошка, который обычно со временем спонтанно сливается с образованием агрегатов лекарственного средства. Эти агрегаты похожи на менее тонкодисперсный или даже крупнодисперсный порошок.
Глагол "слипаться" означает образовывать массу или скопление частиц, особенно в присутствии влаги. Агломераты микронизированных лекарственных средств при хранении имеют склонность, особенно в присутствии влаги, к образованию крупнодисперсного порошка, комков или даже по существу единой массы лекарственного средства.
Присутствие агломератов лекарственного средства в композиции может быть обнаружено с помощью спектрофотометра ближнего инфракрасного диапазона, снабженного микроскопом в соответствии с известными способами.
Термин "физически стабильный" означает, что нет доказательств роста частиц и/или слипания частиц лекарственного средства при хранении.
Размер частиц лекарственного средства и их слипание могут быть определены в соответствии с известными способами.
Одним конкретным приспособлением, которое можно использовать, является Sympatec Dry Dispersion Size Analyzer.
Термин "химически стабильный" относится к лекарственному средству, которое при хранении соответствует требованиям Руководства EMEA CPMP/QWP/122/02, озаглавленного "Stability Testing of Existing Active Substances and Related Finished Products".
Термин "антирастворитель" означает жидкость, имеющую небольшую или отсутствующую сольватирующую способность в отношении лекарственного средства. Растворимость лекарственного средства в антирастворителе должна составлять менее приблизительно 1 мг/мл при определении в соответствии с известными способами. Предпочтительно, растворимость лекарственного средства должна составлять менее приблизительно 100 мкг/мл. Более предпочтительно, растворимость лекарственного средства должна составлять менее приблизительно 10 мкг/мл.
Термин "несмешивающийся с водой" означает, что в антирастворителе может растворяться менее 100 ч/млн и, предпочтительно, менее 10 ч/млн воды. Количество остаточной воды может быть определено в соответствии с известными способами, такими как метод Карла Фишера.
Термин "кондиционирование" означает воздействие на порошок комбинации регулируемых условий температуры и относительной влажности.
"Размер частиц" представляет собой гауссово распределение диаметра частиц.
Упомянутый размер частиц можно количественно определить путем измерения объемного диаметра с помощью лазерной дифракции с использованием подходящих известных приборов, таких как, например, приспособление Malvern или Sympatec.
Объемный диаметр (VD) связан с массовым диаметром (MD) через плотность частиц (при условии, что плотность частиц не зависит от размера).
Размер частиц выражается через объемный диаметр, а распределение частиц по размеру выражается через d(v0,5), что соответствует диаметру 50 процентов по объему частиц, а также через d(v0,9) и d(v0,1), которые выражают значения, ниже которых 90% частиц и 10% частиц образца имеют меньший объемный диаметр, соответственно.
При аэрозолизации размер частиц выражается как массовый аэродинамический диаметр (MAD), а распределение частиц по размеру как масс-медианный аэродинамический диаметр (MMAD). MAD указывает на способность частиц к перемещению при суспендировании в потоке воздуха. MMAD соответствует массовому аэродинамическому диаметру 50 процентов по весу частиц.
Термин "хорошая текучесть" относится к композиции, с которой легко работать во время производственного процесса, и которая может обеспечивать точную и воспроизводимую доставку терапевтически эффективной дозы.
Характеристики потока могут быть оценены с помощью различных тестов, таких как на угол естественного откоса, индекс Карра, отношение Хауснера или скорость потока через отверстие.
Термин "хорошая гомогенность" относится к композиции, в которой после смешивания однородность распределения активного ингредиента, выраженная как коэффициент вариации (CV), также известный как относительное стандартное отклонение (RSD), равна или меньше 5,0%.
Термин "вдыхаемая фракция" относится к величине процентой доли активных частиц, которые достигнут глубоких легких пациента.
Вдыхаемую фракцию, также называемую фракцией тонкодисперсных частиц (FPF), оценивают с использованием подходящего in vitro приспособления, такого как Andersen Cascade Impactor (ACI), Multi Stage Liquid Impinger (MLSI) или Next Generation Impactor (NGI), предпочтительно от ACI, в соответствии с процедурами, описанными в общих фармакопеях, в частности в Европейской фармакопее (Eur. Ph.) 7.3, 7 издание. Ее рассчитывают как процентное соотношение между массой тонкодисперсных частиц (ранее дозой тонкодисперсных частиц) и доставляемой дозой.
Доставляемую дозу рассчитывают по кумулятивному осаждению в приспособлении, а массу тонкодисперсных частиц рассчитывают по отложению частиц, имеющих диаметр < 5,0 микрон.
Фигуры
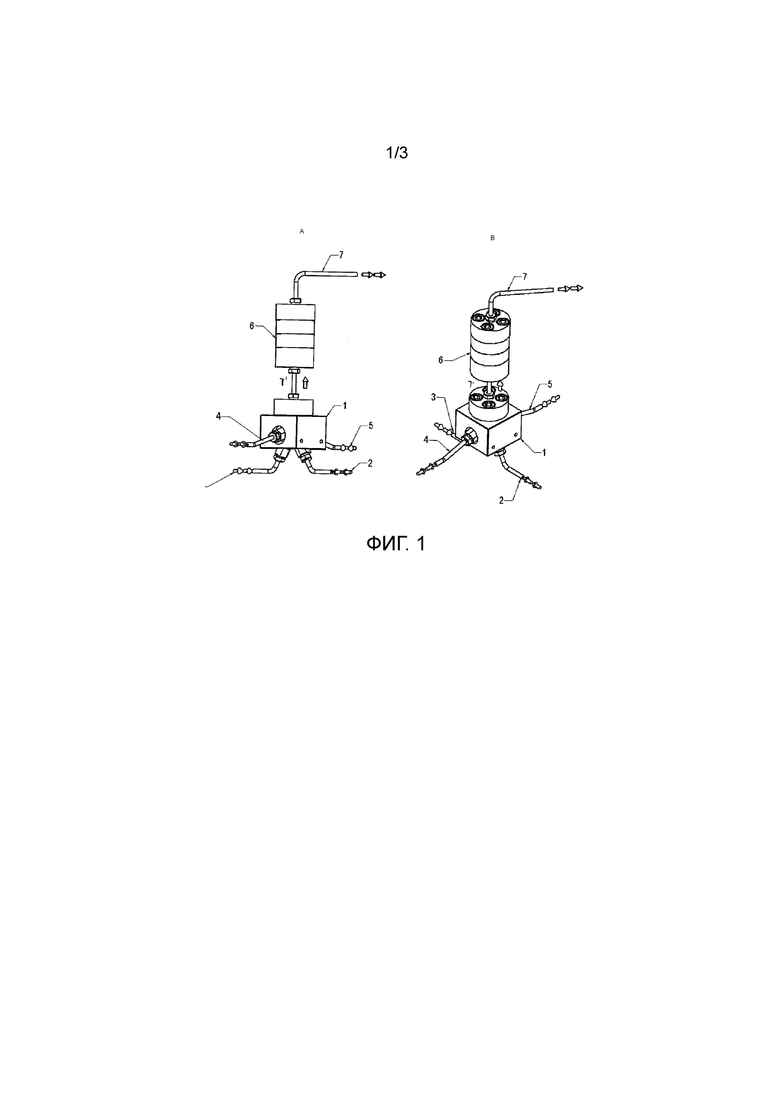
Фигуры 1a и 1b - Виды спереди (левый) и в перспективе (правый) приспособления для гидродинамической кавитации, соответственно.
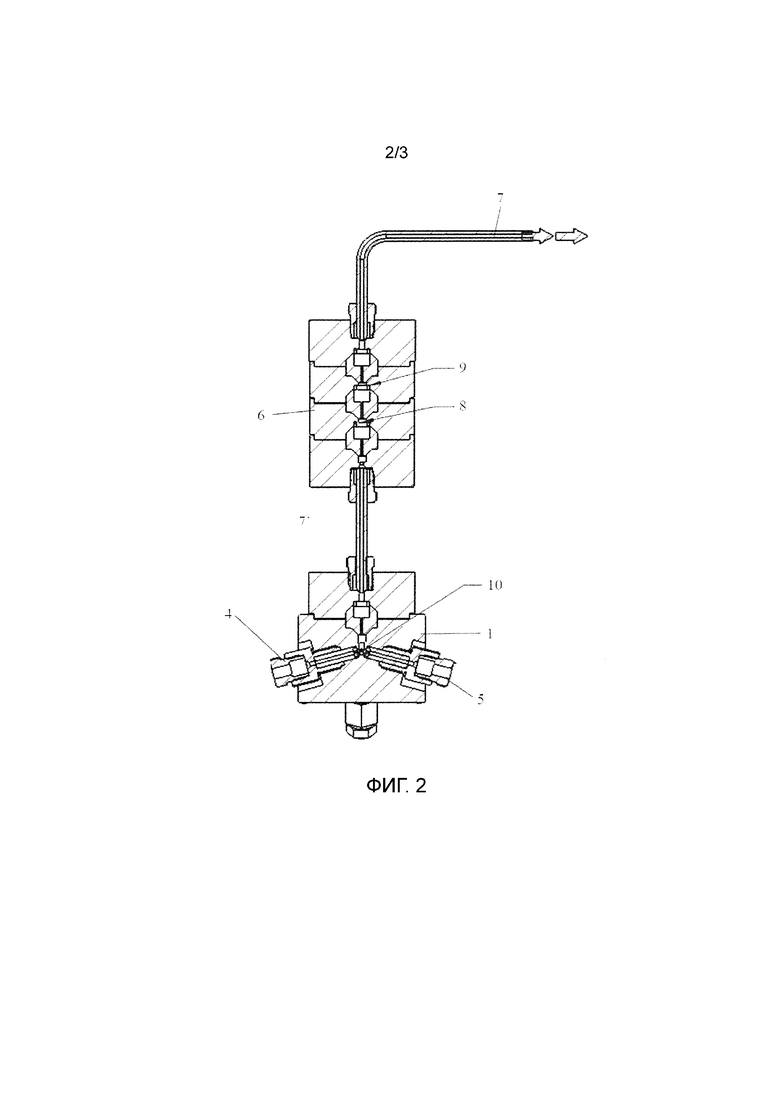
Фигура 2 - Вид в разрезе по продольному сечению приспособления для гидродинамической кавитации.
Фигура 3 - Различные увеличения SEM-изображений частиц rac-гликопиррония бромида.
Подробное описание изобретения
Настоящее изобретение направлено на способ получения микронизированных кристаллизованных частиц фармацевтически приемлемой соли гликопиррония с помощью гидродинамической кавитации с регулируемым потоком для осуществления зародышеобразования на этапе кристаллизации.
Было обнаружено, что, действуя в соответствии с условиями, раскрытыми ниже в данном документе, можно получить физически стабильный кристаллический порошок фармацевтически приемлемой соли гликопиррония с частицами, имеющими небольшой размер, подходящий для ингаляции.
В частности, было обнаружено, что частицы лекарственного средства, полученные способом настоящего изобретения, стабильны в том смысле, что они устойчивы к агрегации и/или слипанию. Другими словами, склонность получаемого сухого микронизированного материала к агрегации и/или слипанию после обработки минимизируется или полностью исключается.
Упомянутые частицы лекарственного средства также демонстрируют лучшие свойства потока по сравнению с традиционным струйно измельченным микронизированным материалом.
Предпочтительно, можно использовать любую органическую или неорганическую фармацевтически приемлемую соль гликопиррония. К органическим солям могут относиться, например, формиат, ацетат, трифторацетат, пропионат, бутират, лактат, цитрат, тартрат, малат, малеат, сукцинат, метансульфонат, бензолсульфонат и бензоат, тогда как к неорганическим солям могут относиться, но без ограничения, фторид, хлорид, бромид, йодид, фосфат, нитрат и сульфат.
Предпочтительно, используют неорганическую соль, выбранную из группы, состоящей из фторида, хлорида, бромида и йодида, предпочтительно хлорида или бромида, даже более предпочтительно, бромида.
Гликопирроний можно использовать в форме любого из чистых энантиомеров или диастереоизомеров или любой их комбинации.
Предпочтительно, используют рацемическую смесь (3S,2'R), (3R,2'S)-3-[(циклопентилгидроксифенилацетил)окси]-1,1-диметилпирролидиния бромида, также известную как rac-гликопиррония бромид.
Фигуры 1 иллюстрируют приспособление для гидродинамической кавитации, подходящее для осуществления способа настоящего изобретения. Фигура 2 иллюстрируют его вид в разрезе.
Приспособление с фигуры 1 содержит первую камеру 1 и четыре впускных отверстия для введения потоков текучей среды F1 в упомянутую камеру и первое выпускное отверстие 7' для переноса текучей среды во вторую камеру 6.
Вторая камера 6 содержит две внутренних зоны 8, 9 для смешивания (фигура 2) и второе выпускное отверстие 7 для выхода текучей среды.
Более подробно приспособление раскрыто в одновременно рассматриваемой патентной заявке США сериальный № 14/216188, идеи которой настоящим включены в настоящий документ посредством ссылки во всей полноте.
Хотя предпочтительно, чтобы поперечное сечение первой камеры 1 было прямоугольным, а второй камеры 6 было цилиндрическим, обе камеры могут иметь любую геометрическую форму, такую как квадратная или шестиугольная, без отклонения от объема настоящего изобретения.
Генераторы кавитации, такие как отверстия, расположены вдоль или вблизи осевой линии в первой камере 1.
Отверстия расположены так, что все потоки сходятся в одной точке. Вместо диска с отверстиями можно использовать крестовину, выходной винт или любое другое приспособление, которое вызывает незначительное падение давления.
Отверстия сконфигурированы так, чтобы генерировать гидродинамическое кавитационное поле ниже по потоку от перегородки посредством локального сужения потока текучей среды. В данном варианте осуществления отверстия представляют собой дыры, просверленные в круговом диске.
Хотя локальное сужение представляет собой кольцевое отверстие, специалисту будет понятно, что если поперечное сечение сквозного канала имеет любую геометрическую форму, отличную от круговой, то локальное сужение, сформированное между стенкой, образующей сквозной канал, и перегородкой, может быть не кольцевой формы.
Аналогично, если отверстие не является круглым в поперечном сечении, то локальное сужение может быть не кольцевой формы. Предпочтительно, геометрическая форма поперечного сечения первой камеры соответствует геометрической форме поперечного сечения перегородки (например, круговая-круговая, квадратная-квадратная и т.д.).
Для дальнейшего создания и управления кавитационными полями вниз по потоку от отверстия отверстие сконструировано так, чтобы его можно было удалить и заменить на любое отверстие, имеющее любую форму и конфигурацию, для создания разнообразных полей гидродинамической кавитации с регулируемым потоком. Форма и конфигурация отверстия может значительно влиять на характер кавитационного потока и, соответственно, на качество кристаллизации.
Хотя существует множество форм и конфигураций, которые могут быть использованы в пределах объема настоящего изобретения, несколько приемлемых форм и конфигураций перегородки раскрыты в документе U.S. 7314516, идеи которого настоящим включены в настоящий документ посредством ссылки во всей полноте.
Следует понимать, что отверстие может быть удаляемым образом выполнено на стержне любым приемлемым образом.
При работе приспособления, показанного на фигуре 1, первый поток текучей среды F1, состоящий из раствора, содержащего фармацевтически приемлемую соль гликопиррония, и одно или несколько поверхностно-активных веществ, растворенных в подходящем растворителе, входит в первую камеру 1 через впускное отверстие 2 и проходит через отверстия в диске в направлении точки сходимости. Второй поток текучей среды F2, состоящий из подходящего антирастворителя, входит в первую камеру 1 через одно или несколько впускных отверстий 3, 4 и 5 и смешивается с первым потоком текучей среды F1 в точке сходимости (зона кристаллизации, 10).
Приведенные выше указания в отношении используемых впускных отверстий являются только примером, поскольку они могут быть изменены.
Предпочтительно, весь поток антирастворителя разделяется по трем впускным отверстиям 3, 4 и 5 в любом соотношении.
Предпочтительно, весь поток антирастворителя разделяется по трем впускным отверстиям 3, 4 и 5 в отношении 40%:30%:30.
Значения давления, температуры и скорости потока должны варьироваться по четырем впускным отверстиям, как известно специалисту.
Предпочтительно, температура всех впускных отверстий поддерживается равной комнатной температуре. Более предпочтительно, давление впускного отверстия 1 поддерживается равным 400-600 фунт/кв.дюйм, предпочтительно 500 фунт/кв.дюйм, тогда как давление трех впускных отверстий 3, 4 и 5 поддерживается равным 2500-5000 фунт/кв.дюйм.
В предпочтительном варианте осуществления скорость потока раствора гликопиррония поддерживается равной 10-15%, более предпочтительно 12%, от полной скорости потока антирастворителя.
Смешанные первый и второй потоки текучей среды, т.е. F1 и F2, затем проходят через локальное сужение потока, где скорость первого и второго потоков текучей среды, т.е. F1 и F2, увеличивается до минимальной скорости (т.е. скорости, при которой начинают появляться кавитационные пузырьки), определяемой физическими свойствами первого и второго потоков текучей среды т.е. F1 и F2. Поскольку первый и второй потоки текучей среды, т.е. F1 и F2, проходят через локальное сужение потока, вниз по потоку от перегородки образуется поле гидродинамической кавитации (которое создает кавитационные пузырьки).
Текучая среда, содержащая крошечные кристаллы, выходит из первой камеры 1 через выпускное отверстие 7' и входит во вторую камеру 6 с двумя дополнительными зонами 8, 9 смешивания для обеспечения более длительного времени пребывания и обеспечения дополнительного смешивания растворителя и антирастворителя.
Предпочтительно, текучая среда, содержащая крошечные кристаллы, остается в упомянутой второй камере смешивания в течение периода времени от 1 до 5 миллисекунд, предпочтительно 2-3 миллисекунды.
Постоянство потоков в первой камере, а также в зонах смешивания второй камеры должно быть отрегулировано специалистом в данной области техники в соответствии с его знаниями и в зависимости от желаемого размера частиц.
Две текучие среды, используемые в данном способе, имеют различную композицию растворителя, причем одна текучая среда представляет собой раствор соединения, подлежащего обработке, в подходящем растворителе или комбинации растворителей ("исходный раствор"), а другая текучая среда представляет собой подходящий растворитель или комбинацию растворителей, способных инициировать осаждение этого соединения из раствора ("антирастворитель"), выбранную из-за ее относительно низкой сольватирующей способности по отношению к этому соединению.
Предпочтительно, растворитель выбирают из группы, состоящей из 1-бутанола, 2-пропанола и их смесей с этанолом в любом соотношении. Предпочтительно, растворитель представляет собой 2-пропанол.
Растворитель, используемый в способе настоящего изобретения, также содержит подходящие поверхностно-активные вещества, которые ослабляют слипание, которое может происходить во время процесса кристаллизации с помощью гидродинамической кавитации, и обеспечивают опосредованную поверхностно-активным веществом самосборку частиц с целевым размером частиц.
Предпочтительно, поверхностно-активное вещество присутствует в весовом отношении в диапазоне от 70:30 до 30:70 по отношению к количеству гликопиррониевой соли, предпочтительно от 65:35 до 55:45 вес/вес, более предпочтительно 62:38 вес/вес.
Поверхностно-активное вещество может быть выбрано из группы лецитинов из любого источника, такого как соя, неионогенных поверхностно-активных веществ, таких как твины и спаны, поверхностно-активных веществ на основе сахаров, таких как стеарат сахарозы и гексадеканоат сахарозы, и их смесей в любом соотношении.
Предпочтительно, можно использовать смесь лецитина и спана 60, предпочтительно в отношении 50:50 вес/вес.
В другом предпочтительном варианте осуществления можно использовать только лецитин.
В другом предпочтительном варианте осуществления можно использовать смесь соевого лецитина, моностеарата сорбитана (спана) 60 и стеарата сахарозы, более предпочтительно в отношении 47:47:6 вес/вес/вес.
Предпочтительно, антирастворитель выбирают из группы, состоящей из диэтилового эфира, н-гептана и метил-трет-бутилового эфира (MTBE) и их смесей, в любом соотношении.
Предпочтительно, антирастворитель представляет собой смесь н-гептана и MTBE в любом соотношении в отношении в диапазоне от 20:80 об/об до 30:70 об/об, даже более предпочтительно в отношении 25:75 об/об.
В конкретном варианте осуществления можно использовать только MTBE.
Обычно смешанный поток, выходящий из второй камеры 6 из выпускного отверстия 7, содержит частицы гликопиррониевой соли с размером частиц, равным или меньшим 100 нм, предпочтительно 50-70 нм.
Упомянутый поток текучей среды собирают в подходящем приемнике, таком как смесительный бак из нержавеющей стали с регулируемой температурой, содержащий смесь н-гептана и MTBE в отношении в диапазоне от 10:90 об/об до 40:60 об/об, предпочтительно от 20:80 об/об до 30:70 об/об, более предпочтительно в отношении 25:75 об/об.
Частицы смешивают внутри приемника в течение короткого промежутка времени, обычно менее 30 минут, предпочтительно менее 15 минут.
Как правило, время смешивания должно быть скорректировано специалистом для достижения желаемого размера частиц в микронах.
Продукт выделяют и собирают, используя обычные способы извлечения.
Например, вышеуказанные предпочтительные поверхностно-активные вещества растворимы в н-гептане.
Поэтому в предпочтительном варианте осуществления настоящего изобретения текучую среду, содержащую частицы гликопиррониевой соли, сначала фильтруют; затем собранные частицы сушат и повторно суспендируют в н-гептане, перемешивают, например, в течение одного часа, снова фильтруют, промывают второй раз н-гептаном и, наконец, сушат, например при 50°C под вакуумом.
Предпочтительно, общее количество поверхностно-активных веществ в конечном продукте составляет менее 5% вес/вес, более предпочтительно менее 1%, предпочтительно меньше или равно 0,1%, даже более предпочтительно меньше или равно 0,01% вес/вес.
Предпочтительно, чтобы собранные частицы гликопиррониевой соли были номинально кристаллическими, так что атомы или молекулы располагались бы регулярно, периодически. Однако кристаллическое лекарственное средство может содержать некоторые аморфные области. Предпочтительно, лекарственное средство должно иметь кристалличность, равную или превышающую 90%, или, более предпочтительно, превышающую 95%, более предпочтительно превышающую 98%, при определении в соответствии с известными способами.
Все полученные частицы гликопиррониевой соли должны иметь объемный диаметр от 0,5 микрон до 15 микрон.
Предпочтительно, по меньшей мере 90% полученных частиц d(v0,9) должны иметь диаметр меньше 10 микрон, предпочтительно менее 8 микрон, более предпочтительно менее 7 микрон. Предпочтительно, d(v0,5) составляет от 1 до 5 микрон, более предпочтительно от 1,5 до 4 микрон, предпочтительно от 2 до 3 микрон. Более предпочтительно, не более 10% всех гликопиррониевых частиц имеют диаметр, меньший 0,6 микрон, даже предпочтительно меньший или равный 0,8 микрон.
В этом контексте размер частиц определяют как объемный диаметр в соответствии с известными способами, такими как лазерная дифракция, основанными на использовании подходящего аппарата, такого как аппарат Mastersizer (Malvern Instruments Ltd, Worcestershire, Великобритания) или Dry Dispersion Size Analyzer (Sympatec GmbH, Clausthal-Zellerfeld, Германия).
Обычно частицы лекарственного средства такого размера подходят для введения путем ингаляции. Фактически, частицы, имеющие размер частиц более приблизительно 10 микрон, вероятно, воздействуют на стенки горла и обычно не достигают легкого.
Предпочтительно, микронизированные кристаллические частицы лекарственного средства, полученные с помощью способа настоящего изобретения, могут быть физически и химически стабильны в течение по меньшей мере одного месяца в условиях окружающей среды (22±2°C и относительная влажность 60%). Предпочтительно, упомянутые микронизированные частицы могут быть стабильны в течение по меньшей мере 3 месяцев при тех же условиях окружающей среды.
Физическую стабильность следует измерять с использованием Sympatec Dry Dispersion Size Analyzer, тогда как химическую стабильность следует определять в соответствии с известным способом, таким как ВЭЖХ.
Альтернативно, физическая стабильность может быть измерена с использованием анализа удельной площади поверхности частиц лекарственного средства с помощью адсорбционного анализа, измерения поверхности BET, в соответствии со способом, известным в данной области техники.
Необязательно, для дальнейшего уменьшения склонности гликопиррониевой соли к агрегации и/или слипанию во время хранения частицы, полученные с помощью способа настоящего изобретения, можно подвергать этапу кондиционирования в соответствии с условиями, приведенными в документе EP 2234595, идеи которого включены в настоящий документ посредством ссылки во всей полноте, но в течение гораздо меньшего времени (меньше одного часа).
Альтернативно, упомянутые частицы могут быть подвергнуты кондиционированию путем загрузки их во вращающийся барабан с влажным кондиционирующим газом. Затем частицы будут суспендированы в этой движущейся кондиционирующей камере в течение небольшого времени, например 1-30 минут. Вращающаяся трубка позволяет частицам оставаться достаточно далеко друг от друга, так что они не слипаются во время этапа кондиционирования. Этот подход к кондиционированию значительно быстрее, чем типичное кондиционирование в окружающей среде, которое может занимать несколько дней или недель.
Частицы гликопиррониевых солей, полученные в соответствии со способом настоящего изобретения, могут быть смешаны с пропеллентами или частицами носителя, что обеспечивает композиции, имеющие хорошую гомогенность.
Таким образом, настоящее изобретение также охватывает композиции, подходящие для введения путем ингаляции, содержащие гликопиррониевые частицы, получаемые с помощью способа настоящего изобретения, в комбинации с одним или несколькими лекарственными средствами, полезными при лечении респираторного заболевания, например короткодействующими и длительнодействующими бета2-агонистами, такими как тербуталин, салметерол, формотерол, милветерол, индакатерол, олодатерол и фенотерол, кортикостероидами, такими как рофлепонид, флунизолид, будесонид, циклесонид, мометазон и его сложный эфир, то есть фуроат, флутиказон и его сложный эфир, т.е. пропионат и фуроат.
В частности, в одном варианте осуществления настоящее изобретение охватывает ингаляционные композиции под давлением в форме суспензии вышеупомянутых микронизированных частиц в сжиженном под давлением пропелленте, предпочтительно гидрофторалкановом (HFA) пропелленте, выбранном из группы из 1,1,1,2-тетрафторэтана (HFA134a), 1,1,1,2,3,3,3-гептафторпропана (HFA227) и любых их смесей.
В другом варианте осуществления настоящее изобретение охватывает ингаляционные композиции сухого порошка, содержащие вышеупомянутые микронизированные частицы в смеси с частицами физиологически приемлемого фармакологически инертного твердого носителя, такого как лактоза, предпочтительно моногидрат альфа-лактозы, и, необязательно, с дополнительными добавками, такими как стеарат магния.
Упомянутые композиции можно вводить с помощью подходящих устройств, таких как компрессорные дозирующие ингаляторы (pMDI) или ингаляторы сухого порошка (DPI).
Микронизированные частицы, получаемые с помощью способа настоящего изобретения, можно использовать для профилактических целей или для облегчения симптомов для широкого спектра условий, включая: респираторные нарушения, такие как хроническая обструктивная болезнь легких (ХОБЛ) и астма всех типов. Другими респираторными заболеваниями, для которых может быть полезным продукт настоящего изобретения, являются характеризующиеся обструкцией периферических дыхательных путей в результате воспаления и наличия слизи, такие как хронический обструктивный бронхиолит, хронический бронхит, эмфизема, острое повреждение легких (ALI), кистозный фиброз, ринит и респираторный дистресс-синдром взрослых (ARDS).
Кроме того, упомянутые частицы могут быть полезны при лечении заболеваний гладкой мускулатуры, таких как недержание мочи и синдром раздраженной толстой кишки; заболеваний кожи, таких как псориаз; гипергидроза и желудочно-кишечных язв.
Настоящее изобретение дополнительно проиллюстрировано подробно следующими примерами.
Примеры
Пример 1. Получение микронизированного порошка rac-гликопиррония бромида
Способ осуществляли с использованием приспособления с фигуры 1.
6 грамм rac-гликопиррония бромида и 9,75 грамм смеси соевый лецитин:спан 60:стеарат сахарозы 47:47:6 вес/вес/вес растворяли в 400 мл 2-пропанола (раствор A). Полученный раствор A входил в первую камеру 1 через впускное отверстие 2, и его температуру поддерживали равной 50°C, а давление равным 500 фунт/кв.дюйм.
Антирастворитель н-гептан входил в ту же камеру 1 через впускные отверстия 3, 4 и 5, и общий поток, поддерживаемый при температуре 25°C и давлении 5000 фунт/кв.дюйм, разделяли приблизительно 40%:30%:30% по трем впускным отверстиям.
Скорость потока раствора A поддерживали равной приблизительно 12% от общего потока антирастворителя.
Гликопиррониевый раствор и антирастворитель затем проходили через отверстия, что вызывало осуществление гидродинамической кавитацией зародышеобразование. Давление поддерживали равным 5000 фунт/кв.дюйм.
4 потока смешивались в точке сходимости, где гидродинамическая кавитация с регулируемым потоком вызывала зародышеобразование. Затем смешанные потоки выходили из камеры 1 через выпускное отверстие 7' и входили во вторую камеру 6 при поддержании давления равным 5000 фунт/кв.дюйм, проходя еще через две зоны смешивания в течение периода, равного 2 миллисекундам. Поток выходил из второй камеры 6 через выпускное отверстие 7, и его собирали в приемник, который содержал гептан/MTBE в отношении 25%/75% об/об. В приемнике поддерживали постоянное соотношение гептан-MTBE дозирующим насосом. Смеси давали осторожно перемешиваться в приемнике в течение приблизительно 5 минут.
Полученные частицы фильтровали с использованием фильтра давления Millipore. Затем их сушили под вакуумом, повторно суспендировали в н-гептане при 60°C, смешивали в течение одного часа и снова фильтровали. Процедуру промывания повторяли три раза.
Количество остаточных поверхностно-активных веществ оказалось меньше 4% вес/вес.
Полученный материал затем тестировали, как описано в примере 2.
Пример 2. Анализ материала порошка rac-гликопиррония бромида из примера 1
Микрочастицы, полученные в примере 1, охарактеризовывали в отношении морфологии, содержания лекарственного средства, кристалличности, плотности, гигроскопичностьи и размера частиц.
Морфологию микрочастиц определяли с помощью сканирующего электронного микроскопа (SEM) с использованием прибора JSM-6480LV (JEOL Ltd, Токио, Япония). Исследование продемонстрировало необычную морфологию в виде цветочного лепестка (смотри фигуру 3).
Содержание лекарственного средства определяли с помощью анализа UPLC-PDA. Никаких пиков деградации/примесей не было обнаружено выше предела детектирования аналитического метода при изготовлении и/или через 3 месяца.
Кристалличность определяли с помощью дифференциальной сканирующей калориметрии (DSC) с использованием аппарата Q2000 (TA Instruments, New Castle, DE). Температуру повышали со скоростью 10°C мин-1 вплоть до 250°C. Образец продемонстрировал явную четкую точку плавления 191,5°C, за которой следовало начало деградации. Из-за высококристаллической природы образца не наблюдали никакого стеклования. Это было подтверждено XRD дифрактометрией порошка.
Свойства сорбции воды определяли с помощью динамической сорбции пара (DVS) с использованием аппарата Q5000SA (TA Instruments, New Castle, DE, США). Циклы сорбции измеряли путем прямого линейного изменения от 10% отн. вл. (относительной влажности) до 90% отн. вл. с начальным временем уравновешивания 60 минут при 0% отн. вл.
Поведение было типичным для кристаллического материала с низким поглощением влаги менее 2,5%.
Плотность порошка измеряли с помощью пикнометрии гелия с использованием прибора AccPyc II 1340 (Micromeritics, Milan, Италия). Среднее значение, рассчитанное по трем измерениям составляло 1,3917 г/см3.
Размер частиц определяли с помощью дифракции лазерного света с использованием Sympatec Dry Dispersion Size Analyzer (Clausthal-Zellerfeld, Германия).
Порошок диспергировали для двух условий измерения при давлении воздуха 1 и 4 бар.
Средние значения d[v,10], d[v,50], d[v,90] рассчитывали по трем измерениям. Размах рассчитывали с использованием следующего уравнения:
Размах=[d(v,0,9)-d(v,0,1)]/d(v,0,5)
На значения, полученные для размера частиц, которые приведены в таблице 1, не оказывало существенного влияния давление дисперсии, что указывает на свободнотекучий порошок без твердых агрегатов.
Таблица 1
Не наблюдали значительного роста размера частиц при хранении в течение по меньшей мере трех месяцев в условиях окружающей среды (22±2°C и относительная влажность 60%).
Пример 3. Получение сухой порошкообразной композиции, в которой активным ингредиентом является rac-гликопиррония бромид
Моногидрат альфа-лактозы SpheroLac 100 (Meggle) и стеарат магния в отношении 98:2% по весу совместно перемалывали в приспособлении для струйного размола (ниже в данном документе предварительная смесь). Затем эту предварительную смесь смешивали с моногидратом альфа-лактозы CapsuLac (212-355 микрон) в смесителе Turbula в течение 4 часов на 32 об/мин (ниже в данном документе носитель). Микронизированный rac-гликопиррония бромид, полученный в примере 1, добавляли к носителю и перемешивали в смесителе Turbula в течение 120 минут на 32 об/мин для получения соотношения 12,5 мкг активного вещества на 10 мг носителя (смесь A).
Композицию оценивали в отношении удовлетворительной однородности содержания насыпного порошка (RSD 1,1%).
Некоторое количество порошка для ингаляции загружали в мультидозовый ингалятор сухого порошка NEXThaler® (Chiesi Farmaceutici SpA, Италия).
Аэродинамическую оценку распределения частиц по размеру получали с использованием Next Generation Impactor (NGI) в соответствии с процедурой, подробно описанной в Европейской фармакопее (European Pharmacopoeia 7th Edition: 278-82). Были рассчитаны следующие параметры: i) доставляемая доза (DD), которая представляет собой количество лекарственного средства, доставленного из устройства, извлеченного из всех частей импактора; ii) масса тонкодисперсных частиц (FPM), которая представляет собой величину доставленной дозы с размером частиц, меньшим или равным 5,0 микрон, iii) фракция тонкодисперсных частиц (FPF), которая представляет собой отношение между массой тонкодисперсных частиц и доставленной дозой; iv) MMAD±GSD; и v) сверхтонкодисперсная FPF, которая представляет собой процентную долю массы тонкодисперсных частиц с размером частиц, меньшим или равным 1,0 микрон. Результаты (среднее значение, n= 6) приведены в таблице 2.
Таблица 2
(мкг)
(мкг)
(%)
(мкм)
< 1 мкм
Результаты показывают хорошую доставленную дозу, что указывает на отсутствие значительного удерживания в устройстве DPI. Фракция тонкодисперсных частиц также является удовлетворительной.

Настоящее изобретение относится к способу получения микронизированных частиц фармацевтически приемлемой соли гликопиррония. Способ содержит этапы: (a) смешивания, в первой камере приспособления для гидродинамической кавитации с регулируемым потоком, потока F1 раствора, содержащего фармацевтически приемлемую соль гликопиррония и смесь соевого лецитина, моностеарата сорбитана (спана) 60 и стеарата сахарозы в качестве поверхностно-активного вещества, растворенного в растворителе, выбранном из группы, состоящей из 1-бутанола, 2-пропанола и их смесей с этанолом, с одним или несколькими потоками F2 антирастворителя, представляющего собой н-гептан; (b) подвергания смешанных потоков F1 и F2 воздействию локального сужения потока для создания гидродинамической кавитации с регулируемым потоком, что вызывает зародышеобразование соли гликопиррония; (c) переноса смешанных потоков F1 и F2 во вторую камеру упомянутого приспособления для кавитации с регулируемым потоком, и обработки упомянутых смешанных потоков в течение периода времени, меньшего 10 миллисекунд; (d) сбора полученных потоков в приемник, содержащий смесь н-гептана и метил-трет-бутилового эфира (MTBE) в отношении в диапазоне от 10:90 об/об до 40:60 об/об; (e) сушки частиц для отверждения собранных частиц; (f) удаления поверхностно-активного вещества; и (g) дальнейшей сушки полученных микронизированных частиц. Также предложены способ получения композиции для ингаляции, композиция для ингаляции под давлением, компрессорный дозирующий ингалятор, сухая порошкообразная композиция, ингалятор сухого порошка. Предложенный способ позволяет получить частицы лекарственного средства, физически стабильные по отношению к слипанию и/или агрегации при хранении. 6 н. и 3 з.п. ф-лы, 3 ил., 2 табл., 3 пр.
1. Способ получения микронизированных частиц фармацевтически приемлемой соли гликопиррония, причем данный способ содержит этапы:
(a) смешивания, в первой камере приспособления для гидродинамической кавитации с регулируемым потоком, потока F1 раствора, содержащего фармацевтически приемлемую соль гликопиррония и смесь соевого лецитина, моностеарата сорбитана (спана) 60 и стеарата сахарозы в качестве поверхностно-активного вещества, растворенного в растворителе, выбранном из группы, состоящей из 1-бутанола, 2-пропанола и их смесей с этанолом, с одним или несколькими потоками F2 антирастворителя, представляющего собой н-гептан;
(b) подвергания смешанных потоков F1 и F2 воздействию локального сужения потока для создания гидродинамической кавитации с регулируемым потоком, что вызывает зародышеобразование соли гликопиррония;
(c) переноса смешанных потоков F1 и F2 во вторую камеру упомянутого приспособления для кавитации с регулируемым потоком, и обработки упомянутых смешанных потоков в течение периода времени, меньшего 10 миллисекунд;
(d) сбора полученных потоков в приемник, содержащий смесь н-гептана и метил-трет-бутилового эфира (MTBE) в отношении в диапазоне от 10:90 об/об до 40:60 об/об;
(e) сушки частиц для отверждения собранных частиц;
(f) удаления поверхностно-активного вещества; и
(g) дальнейшей сушки полученных микронизированных частиц.
2. Способ по п. 1, в котором фармацевтически приемлемая соль гликопиррония представляет собой бромид.
3. Способ по п. 1 или 2, в котором растворитель представляет собой 2-пропанол.
4. Способ по любому из предшествующих пунктов, где компоненты смеси поверхностно-активного вещества находятся в отношении 47:47:6 вес/вес/вес.
5. Способ получения композиции для ингаляции, содержащий этап смешивания микронизированных частиц, полученных в соответствии со способом по любому из пп. 1-4, с одним или несколькими пропеллентами или носителями.
6. Композиция для ингаляции под давлением, содержащая микронизированные частицы фармацевтически приемлемой соли гликопиррония, полученные в соответствии со способом по любому из пп. 1-4, суспендированные в сжиженном под давлением пропелленте.
7. Компрессорный дозирующий ингалятор (pMDI), заполненный композицией по п. 6.
8. Сухая порошкообразная композиция, содержащая микронизированные частицы фармацевтически приемлемой соли гликопиррония, полученные в соответствии со способом по любому из пп. 1-4, в смеси с частицами физиологически приемлемого фармакологически инертного твердого носителя.
9. Ингалятор сухого порошка, заполненный композицией по п. 8.
| US 20140322142 A1, 30.10.2014 | |||
| US 20150352127 A1, 10.12.2015 | |||
| WO 2005105043 A2, 10.11.2005 | |||
| WO 2001076575 A2, 18.10.2001 | |||
| СКВАЖИННЫЙ КЛАПАН-ОТСЕКАТЕЛЬ | 2002 |
|
RU2234595C1 |
| FIND J | |||
| et al., Hydrodynamic cavitation as a tool to control macro-, micro-, and nano-properties of inorganic materials, Journal of Materials Research, Materials Research Society, 2001, v | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
Авторы
Даты
2020-06-16—Публикация
2017-01-24—Подача