Область техники
Изобретение относится к устройствам низкоэнергетического малоинтенсивного ионно-лучевого воздействия на биологические ткани и агломераты клеток и может применяться в биологии для исследовательских целей, биотехнологии и медицине, в качестве оборудования для проведения процедур лучевой терапии и хирургии, как для онкологической, так и других патологий, требующих удаления с большой точностью, прецизионному введению препаратов в наноипикодозах, а также осуществления пучковой наноинвазивной прецизионной диагностики и непрерывного мониторинга и процедур лучевой терапии и хирургии.
О структуре описания изобретения
При патентном поиске прямых аналогов заявляемому изобретению обнаружено не было. В связи с этим, для облегчения восприятия информации, выделены три основные составляющие заявленного изобретения, по каждому из которых найдены патенты, отражающие предшествующий уровень техники.
Таким образом, начало описательной части изобретения структурно разделено на три функциональные группы (обозначаются римскими цифрами I, II и III - соответственно). Группа I - связана с описанием предшествующего уровня техники и сути изобретения для основной части пучкового устройства, обеспечивающего реализацию низкоэнергетического малоинтенсивного ионного пучка для воздействия на клетки биотканей или агломераты клеток разрушающего структурные элементы ядра, в частности ДНК с условным названием «нож». Группа II - связана с описанием предшествующего уровня техники и сути изобретения для части устройства сусловным названием «шприц» и обеспечивающего точечное внесение нано-пико-кубических см доз действующего вещества (препарата) назаданную глубину путем создания увлекающего пучка (потока) ионов описанного в группе I. Группа III - связана с описанием предшествующего уровня техники и сути изобретения для части устройства с условным названием «монитор» и обеспечивающего непрерывный мониторинг процессов воздействия и внесения с помощью частей устройства «нож» и «шприц» соответственно, по средством излучающих и регистрирующих головок в электромагнитном и акустическом полях колебаний генерируемых банчем непосредственно и излучательными элементами «монитора».
Далее идут разделы согласованные с пунктами формулы изобретения - «Описание изобретения пучкового устройства», «Описание изобретения пучковой системы», «Описание изобретения пучкового комплекса», список цитированной литературы (исключая патенты), рисунки и описание обозначений на рисунках.
Предшествующий уровень техники группы I
Областью наиболее интенсивного применения лучевых методов и устройств воздействия на биологические ткани и агломераты клеток, осуществляющих это в биологии, биотехнолигии и медицине является лучевая терапия. В лучевой терапии применяются пучки ионов высоких энергий, акрометогоипи-мезонов, нейтронов, электронов, рентгеновского и гамма излучения. Традиционная адронная лучевая терапия, являющаяся наиболее эффективной составляющей радиационной терапии, использует для облучения опухолей быстрые (высокоэнергетичные) частицы с большой массой (протоны и более тяжелые ионы).
Основная задача лучевой терапии состоит в обеспечении доставки достаточно высокой дозы радиации в область, занимаемую злокачественной опухолью, при условии приемлемо низкого уровня облучения близлежащих тканей и органов в трехмерной области.
Опасные последствия применения любых методов традиционной лучевой терапии связаны с риском заболевания вторичного и/или появления серьезных постлучевых осложнений вследствие неизбежного облучения здоровых тканей.
В принятых в развитых странах подходах к лечению подобных заболеваний, которые приводят к наиболее высокому уровню излечения онкологических пациентов, применяются все три дополняющих друг друга метода: хирургия, лучевая терапия и химиотерапия.
Адронная лучевая терапия является терапевтическим методом, при котором используют пучки протонов или более тяжелых заряженных частиц с массовым числом, превышающим 1.
Также известно, что при протонной лучевой терапии, которая является частным методом адронной лучевой терапии, основанной на использовании пучков протонов, используются терапевтические пучки относительно слабого тока (порядка нескольких наноампер), с энергией в области 60-250 МэВ и скоростью в диапазоне примерно от 25 до 62% скорости света. В случае использования разных ионов необходимы терапевтические пучки с более слабым током и более высокой энергией по сравнению с пучками протонов.
Например, в случае ионов углерода 12С6+ требуемые энергии находятся в области от примерно 1500 до 4800 МэВ (от примерно 120 до 400 МэВ/нуклон). Таким образом, для типичного иона требуемые энергии составляют от 50 до 500 МэВ/нуклон, соответствующие скоростям от 15 до 75% скорости света.
В области протонной лучевой терапии из разных типов существующих ускорителей используют как циклотроны (обычные или сверхпроводящие), так и синхротроны.
В патенте РФ 2409917 предложено использовать и линейные ускорители (Linac). Масса циклотронного магнита увеличивается с увеличением массового числа и энергии ускоренных ионов и становится очень большой, если преследуется цель охватить всю область энергии, необходимой для терапии ионами углерода и аналогичными ионами. В частности, в настоящее время нет ни одного специализирующегося на адронной терапии лечебного центра, базирующегося на циклотронах, ускоряющих ионы углерода до максимальной энергии порядка 5000 МэВ. Поэтому используются специальные синхротроны, приспособленные для такой терапии, и, в отличие от циклотронов, имеющие дополнительное преимущество в виде получения ионных пучков с изменяемой энергией.
Таким образом, специализирующиеся на адронной лучевой терапии центры, оснащенные синхротроном, очень сложны, так как они требуют большого количества единиц высокотехнологичного оборудования, полученного на основе сложных технологий ускорителей частиц. К тому же эти центры довольно велики по размерам, в том числе и из-за занимаемой синхротроном площади, и требуют больших вложений, а также больших площадей для оборудования, которые невсегда имеются в наличии рядом с лечебными учреждениями.
Для эффективной лучевой терапии требуются пучки составных заряженных частиц (полностью или частично ионизированных ядер или молекул) с массовым числом, превышающим 1, очень низкой интенсивностью (меньше, чем несколько наноампер). Такое требование не соблюдается при применении для этой цели циклотронов и синхротронов в качестве ускорителей частиц.
В патенте РФ 2409917 (Линак, Linac), а также патентах WO 2004/054331 и в US №10/602060 предложена такая ускоряющая ионы система, которая может изменять энергию и силу (слабую) тока терапевтического пучка с одновременным уменьшением затрат на ее создание и занимаемого ею пространства благодаря системе ускорения ионов для адронной терапии, имеющей ускоряющую систему для составных заряженных частиц, ядерных или молекулярных, с массовым числом, превышающим 1, в виде ионных пучков, например, для медицинских целей, характеризующаяся тем, что включает: обычный или сверхпроводящий циклотрон, радиочастотный линейный ускоритель (РЛУ), линию транспортировки пучка средней энергии, присоединенную на одном конце к выходу циклотрона или к выходу первой части радиочастотного линейного ускорителя, а на другом конце к входу линейного радиочастотного ускорителя или ко второй части указанного радиочастотного линейного ускорителя, и линию транспортировки пучка высокой энергии, присоединенную на одном конце к выходу радиочастотного линейного ускорителя, а на другом конце системе для распределения дозы облучения пациента.
В общем случае адронная лучевая терапия подразумевает использование адронов как низких так и высоких энергий. Современная тенденция состоит в преимущественном использовании высокоэнергетичных частиц (в частности ионов в диапазоне 50-500 МэВ/нуклон), что дает возможность пучку достигать практически любых точек внутри тела человека. Но при этом, происходит нежелательное облучение не пораженных тканей за и перед т.н. Брегговским пиком вследствие «попутного» облучения и образования осколков деления ядер при не упругих столкновениях ионов с ядрами тканей.
В настоящее время прогресс в области средств и методов традиционной адронной лучевой терапии основан на создании:
- компактных ускорителей ионов водорода (протонов) и более тяжелых ионов высокой энергии (50-500 МэВ/нуклон) с высоким качеством пучка (малое поперечное сечение (~0,1-1 мм), малой шириной энергетического спектра (~1%), достаточной интенсивности (>10+9 ионов/сек), малым шагом контроля энергии (~5 МэВ), частотой повторения в диапазоне 0,1-30 Гц, динамическим контролем числа частиц в пучке;
- эффективных протяженных (магнитооптических) систем транспортировки пучков от источника ионов до мест использования (процедурных кабинетов);
- эффективных систем многопольного (с разных направлений) облучения лежащего пациента (гантри, гентри) выведенными в процедурные кабинеты пучками мишеней (опухолей).
Техническая составляющая этого прогресса представляет собой весьма сложные, громоздкие и дорогостоящие элементы, включающая, в том числе, специальные помещения (здания), что требует вложений в сотни млн. евро.
Основной недостаток высокоэнергетической адронной терапии состоит в нежелательном облучении непораженных тканей за и перед т.н. Брегговским пиком в следствие «попутного» облучения и образования осколков деления ядер при неупругих столкновениях ионов с ядрами тканей, а также высокой стоимостью оборудования и услуг.
В патенте РФ №2644121 (2018) сообщается о применении пучков ионов малой энергии - до 1 МэВ/нуклон для способа малоинвазивной приповерхностной маркировки изделий с достигнутыми размерами пятна фокусировки ~1 мкм и точностью позиционирования также порядка ~1 мкм. Способ предложенный в данном патенте может быть применен для создания инструментов лучевого воздействия на биологические ткани, но методы создания и управления ионным пучком базирующиеся на СВЧ-резонаторах, электро- и магнитооптике приводят, как и в случае аппаратуры для высокоэнергетической адронной терапии, к сложным, громоздким и дорогостоящим элементам в конструкции, включающим, в том числе, специальные помещения.
Исходя из описанного состояния предшествующего уровня техники, актуальной задачей является разработка компактной системыускорения низкоэнергетических ионов и доставки их непосредственно к области воздействия.
Описание изобретения в части группы I
Низкоэнергетические ионы (НЭИ, диапазон энергий 0,01-30 МэВ/нуклон) несколько ограничены в диапазоне глубин проникновения в биологическую ткань, т.е. имеют гораздо меньший средний пробег и меньшую вероятность образования осколков ядер, но в остальном воздействие НЭИ остается аналогичным высокоэнергетичным ионам. То есть, величина дозы 1-2 Гр [1], внесенная НЭИ в ткань, фатально нарушает структуру ДНК клеток, в частности, пораженных клеток, лишая их способности воспроизведения. Так глубина проникновения для протонов с энергией 2 МэВ (100 КэВ) в биологическую ткань составляет ~180 мкм (5 мкм), а число протонов необходимых для внесения средней дозы облучения ~1 Гр - 5,5⋅107 (8⋅106) соответственно. Тяжелые ионы, как и в случае высоких энергий - более биологически эффективны. Глубина проникновения для ионов углерода с энергией 30 МэВ/нуклон (2 МэВ/нуклон) в биологическую ткань составляет ~17 мкм (1 мкм), а число ионов углерода необходимых для внесения средней дозы облучения ~1 Гр - 2,2⋅107 (7,5⋅106) соответственно.
Использование методов лазерного ускорения заряженных частиц позволяет создать компактное устройство генерирующее пучки НЭИ. Лазерное ускорение обеспечивается ускорением ионов кулоновским взрывом кластерных или твердотельных мишеней-излучателей (МИ). Кулоновский взрыв является следствием сверхмалой длительности импульса (масштаба фемто-аттосекунды) лазера. Временная структура генерируемых в этом случае пучков НЭИ также будет импульсной, состоящей из последовательности отдельных сгустков ионов, называемых банчами. Каждый банч ионов генерируется отдельным сверхкоротким лазерным импульсом.
Возможны также следующие варианты лазерного ускорения:
- ускорение ионов в при поверхностном слое МИ;
- ускорение ионов радиационным давлением света;
- ускорение ионов в магнитном вихре;
- ускорение ионов на фронте бесстолкновительной ударной волны [2].
В настоящее время максимальная энергия ионов, ускоренных с использованием тонких твердотельных мишеней-излучателей и фемтосекундных лазеров, составляет 40 МэВ [3], 45 МэВ [4], 160 МэВ [5] для протонов; 1 ГэВ (т.е. 83 МэВ/нуклон) для углерода [6].
Использование метода получения НЭИ кулоновским взрывом кластерных или твердотельных мишеней-излучателей позволяет создать компактную установку с Гигаваттной импульсной мощностью для генерации ионных банчей суммарной интенсивности 108-1012 ионов/сек и средней энергией до 50 МэВ/нуклон.
Процесс получения каким-либо (любым) методом ускоренных ионов сопровождается генерацией электронов разных энергий, дальнейшее распространение которых в веществе рождает также гамма-кванты и, реже, позитроны.
Распространение короткого во времени ионного банча в сопровождении электронов, гамма-квантов, позитронов в биоткани рождает отклик от нее в широком диапазоне электромагнитного и акустического спектров. Регистрация сигналов отклика позволяет осуществлять одновременно и мониторирование (диагностику) воздействия банча на биоткани [8, 9].
Применяемые мишени-излучатели состоят из 3-х - 5-ти слоев и имеют фрагментарно-секторальный характер, т.е. в каждый сектор включено пределенный набор фрагментов разных веществ, что обеспечивает возможность динамического выбора сочетания типов ионов банча в процессе работы (разноионный состав выходного пучка) и возможность более разнообразного воздействия. Например, если сформировать протонный пучок с небольшой добавкой ионов углерода и/или кислорода, то в тканях будет стимулироваться формирование оксидантов, которые будут дополнительно разрушать опухолевые клетки, ускоряя процесс дегенерации опухоли.
Использование метода получения НЭИ кулоновским взрывом кластерных или твердотельных мишеней-излучателей при попадании на них мощных лазерных импульсов фемто-, аттосекундой длительности позволяет пространственно разнести аппаратуру формирования лазерного импульса и банча НЭИ, соединив эти элементы установки гибким световодом, что позволяет создать компактный, легко перемещаемый и ориентируемый ионно-лучевой инструмент воздействия на биоткани и агломераты клеток.
Дополнительным преимуществом использования методов лазерной генерации банчей НЭИ является возможность заменить достаточно громоздкое и требующее больших электрических напряжений и токов управление и фокусировку непосредственно для банча НЭИ на манипуляции лазерным импульсом. Прецизионное электронное управление позиционированием и фокусировкой лазерных импульсов на мишени-излучателе осуществляется акустооптическими отклоняющими и фокусирующим элементами лазерной оптики. При этом лазерный импульс фокусируется и направляется в точку на поверхности мишени-излучателя совпадающую с проекцией центра заданного отверстия сетки-коллиматора. Заданное отверстие сетки-коллиматора формирует окончательно банч по форме и направлению движения. Таким образом, предварительное позиционирование и выбор направления движения банчей НЭИ осуществляется либо вручную перемещением инструмента, либо внешним электромеханическим манипулятором автоматически, с последующей электронной прецизионной корректировкой лазерного импульса формирующего банчи на соответствующей ячейке сетки-коллиматора и ориентированной на выбранную область биоткани с точностью позиционирования 1-10 мкм (шаг ячеек сетки-коллиматора).
Предшествующий уровень техники группы II
Существует ограниченное количество способов и средств ввода химических или других действующих веществ в биоткани. Наиболее распостраненными являются игольный и безыгольный варианты выполнения инъекций. Как следует из описания к патенту РФ 2129021, общепризнано, что методика, обеспечивающая неинвазивную систему подачи медикаментов с помощью безыгольного шприца, который выстреливает в газовом потоке легкие частицы, содержащие медикамент в регулируемых дозах, в неповрежденную кожу является чрезвычайно востребованной в настоящее время, поскольку может использоваться в широком круге задач: для повседневного введения медикаментов (инсулин), в иммунизационных программах, или для введения лекарств с замедленным выделением, таких как обезболивающие средства и противозачаточные средства; для подачи генетического материала в живые клетки кожи с целью долгосрочной генетической терапии для стабильного лечения таких заболеваний, как гемофилия или меланома кожи; для подачи генетического материала в кожу, мышцы, кровь, лимфу и, с минимальной хирургией, на поверхность внутренних органов.
В предыдущих работах была продемонстрирована возможность использования плотных частиц носителя для генетического превращения клеток растений. В этом способе плотные микроснаряды, сделанные, например, из вольфрама или золота, покрываются генетическим материалом и выстреливаются в целевые клетки. Как описано в заявке WO-A-92/04439, эти микроснаряды выстреливаются с помощью устройства, включающего удлиненное трубчатое приспособление, резервуар с жатого газа, подсоединенный к одному концу приспособления, между концами этого приспособления имеется средство для удерживания или введения частиц, которые будут приведены в движение. Мембрана закрывает проход через трубчатое приспособление до тех пор, пока она не будет разорвана под действием заданного давления газа из резервуара, в результате чего частицы приводятся в движение потоком газа из трубчатого приспособления. Как раскрыто в более раннем описании, эти частицы первоначально могут быть иммобилизованы, например, электростатически, на диафрагме или до нее (по потоку), которая разрывается, когда начинается поток газа, и которая может быть той же самой, что и разрываемая мембрана, которая разрывается для того, чтобы инициировать поток газа. Альтернативно предлагалась инжекция в газовый поток через полую иглу.
Предложенные в изобретениях способы устранения проблем традиционной игольной инъекции препаратов чрезвычайно важны и полезны, но они не решают таких серьезных для сегодняшнего дня проблем, как прецизионная адресная (повышенной точности) доставка нано- и пикодоз активных веществ при отсутствии высоких (относительных) доз балластной (а то и опасной) компоненты вводимой смеси в виде несущей части микрочастиц, доставка нано, пикодоз в активной фазе.
Описание изобретения в части группы II
Предлагается выполнять впрыск действующего вещества с помощью устройства, принцип действия которого аналогичен наноинвазивному низкоэнергетическому ионно-лучевому воздействию на биоткани, приведенному в разделе «Описание изобретения I».
Для реализации этой возможности в устройстве наноинвазивного ионно-лучевого низкоэнергетического воздействия на биоткани и агломераты клеток с функциями впрыска и мониторирования, краткое название - пучковое устройство лучевого воздействия (ПУЛВ) - импульс фемто- или аттосекундного лазера отклоняется и фокусируется с помощью управляемых элементов оптики на кольцевую много слойную азимутально-структурированную мишень-излучатель расположенную коаксиально относительно центральной мишени-излучателя в ПУЛВ. Банч ионов коллимируется и формируется в опорный банч соответствующим дрейфовым каналом в несущем цилиндрическом элементе ПУЛВ. На боковой поверхности каждого канала имеется сопло диаметром 1-100 нанометров, соединяющее внутренний объем канала с подводящей магистралью действующего вещества, находящегося внутри магистрали под давлением. В процессе движения опорного ионного банча вдоль канала в области сопла происходит поляризация молекул (атомов) действующего вещества, а затем вытягивание, захват порции в дрейфовый канал и формирование банча действующего вещества, двигающегося вслед за опорным банчем.
Дальнейшее прямолинейное движение последовательности опорных банчей и банчей действующего вещества в течение заданного промежутка времени обеспечивает введение (впрыск) необходимой дозы действующего вещества масштаба нано-пико-куб. см прецизионно в выбранную локальную зону биоткани или агломерата клеток.
Отработанные ионы компенсируют заряд на заземленных металлизированных внутренних поверхностях ПУЛВ, превращаясь в нейтральные атомы (молекулы) и вместе с избыточными молекулами (атомами) действующего вещества удаляются из ПУЛВ вакуумированием рабочего объема.
Предшествующий уровень техники группы III
К числу наиболее распространенной аппаратуры, применяемой в компактных устройствах, типа эндоскопов, для манипуляций с биологическими тканями и агломератами клеток в условиях ограниченного пространства внутренних полостей для мониторирования процесса являются видеоустройства на основе CCD- и CMOS-матриц чувствительных в разных частях электромагнитного спектра с разного рода ручным или автоматическим механическим или электромеханическим управлением, что отражено например в патентах РФ 2526948, USA 6638216, заявке на изобретение US 20100125166, а также в описаниях многочисленных аппаратов, в том числе видео эндоскопов, производимых промышленно, например - Olympus Viserа модель А 50003А (PAL).
Аппаратура данного типа не решает таких важных для сегодняшнего дня проблем в мониторировании как ограниченость мониторной информации только видимой и ближней инфракрасной областью электромагнитного спектра, а также отсутствие единой навигационно-информационной системы (данные, в том числе архивные, по УЗИ, Рентген, КТ, МРТ) по рабочей области операции и отсутствие высокоуровневой системы мониторирования воздействия во время операции, включающей информацию в расширенном диапазоне электромагнитного и акустического спектров с детализацией временной структуры отклика на воздействие.
Описание изобретения в части группы III
Для использования предлагаемого в данном изобретении устройства ионно-лучевого воздействия на биоткани в оптимальном режиме необходимо получение информации о ходе процесса в реальном времени. В рамках ПУЛВ вычисление значений рабочих параметров управления для ионно-лучевого воздействия или впрыска производится в блоке вычислений и управления на основе информации, поступающей от высокоуровневой системы мониторинга, соосно встроенной во внешнем отсеке ПУЛВ. Система мониторинга предназначена:
1. Для мониторинга дозы с наносекундным временным разрешением, при этом используется почти мгновенный всплеск электромагнитного излучения в различных частях спектра, зависящий от средней энергии банча ионов и сопровождающих его частиц [10, 11]. Для непрерывного наблюдения за остальными важными параметрами объектов рабочей области (геометрическими, химическими, биологическими) производится непрерывный сбор и анализ информации в активно (зондирующем)-пассивном режиме наблюдения оптико-акустического поля и других частей электромагнитного спектра;
2. Для первичного распознавания и мониторинга воздействия ионного банча, которые осуществляются на базе расположенных в одноименном отсеке коаксиальных электромагнитных датчиков и излучателей, пьезодатчиков и пьезоизлучателей ПУЛВ для создания зондирующего излучения и регистрации отклика на точечный впрыск или наноинвазивное ионно-лучевое воздействие. Принцип работы коаксиальных датчиков основан на интегрировании оптико- и радиоакустических методов детектированияи реализует алгоритмы визуализации структурных составляющих биоткани методами оптической когерентной томографии. Для повышения информативност и полученных данных возможна дополнительная обработка следующими методами: оптоакустическая томография, оптическая диффузионная спектроскопия и томография, флюоресцентная спектроскопия и томография.
Оптическая когерентная томография (ОКТ) основана на низко когерентной рефлектометрии: исследуемая среда зондируется широкополосным источником излучения, а пришедший с различных глубин обратно рассеянный свет, соответственно, имеющий различные временные задержки относительно падающего излучения, разрешается по времени с помощью интерферометра [12]. Приборы ОКТ созданные на базе фемтосекундных лазеров достигают пространственного разрешения ~1 мкм, что позволяет хорошо различать тканевые слои, в частности хорошо определять опухолевые образования. Улучшенный вариант - поляризационно-чувствительная спектроскопическая ОКТ (ПЧСОКТ) [13,14]. Достижимая глубина сканирования до 3 мм.
Оптоакустическая томография (ОАТ) основана на регистрации ультразвуковых импульсов, возбуждаемых в исследуемой среде при поглощении импульсного лазерного излучения хромофорами биоткани [15]. Регистрацию OA-импульсов осуществляют на поверхности исследуемой среды с помощью ультразвуковых антенн с электронным сканировнием. ОАТ достигает глубин [16, 17] до 5 см при пространственном разрешении ~0,1 мм.
Оптическая диффузионные спектроскопия и томография (ОДСиТ) основана на регистрации многократно рассеянной, диффузной компоненты света, прошедшей сквозь слой биологической ткани, и решении обратной задачи - восстановления показателей рассеяния и поглощения ткани на основе результатов этих измерений [18]. Измеряя спектр показателя поглощеия, можно оценивать концентрации хромофоров биоткани, парциальные спектры которых хорошо известны. Импульсная и модуляционная ОДСиТ достигает глубин до 10 см [19, 20, 21].
Флюоресцентная спектроскопия и томография (ФСиТ, анализ собственного постсвечения тканей) [22] основана на получении множества проекций исследуемого объекта при облучении источником, возбуждающим флуоресценцию, и регистрации эмиссии с последующей реконструкцией распределения флуорофорав ткани. Применяется, как интраоперационный контроль удаляемой опухоли, мониторинг процессов лучевой терапии (ЛТ).
3. Для непрерывной навигации в рамках рабочей области с целью прецизионного оконтуривания с точностью ~1 мкм обрабатываемых областей.
Описание изобретения пучкового устройства
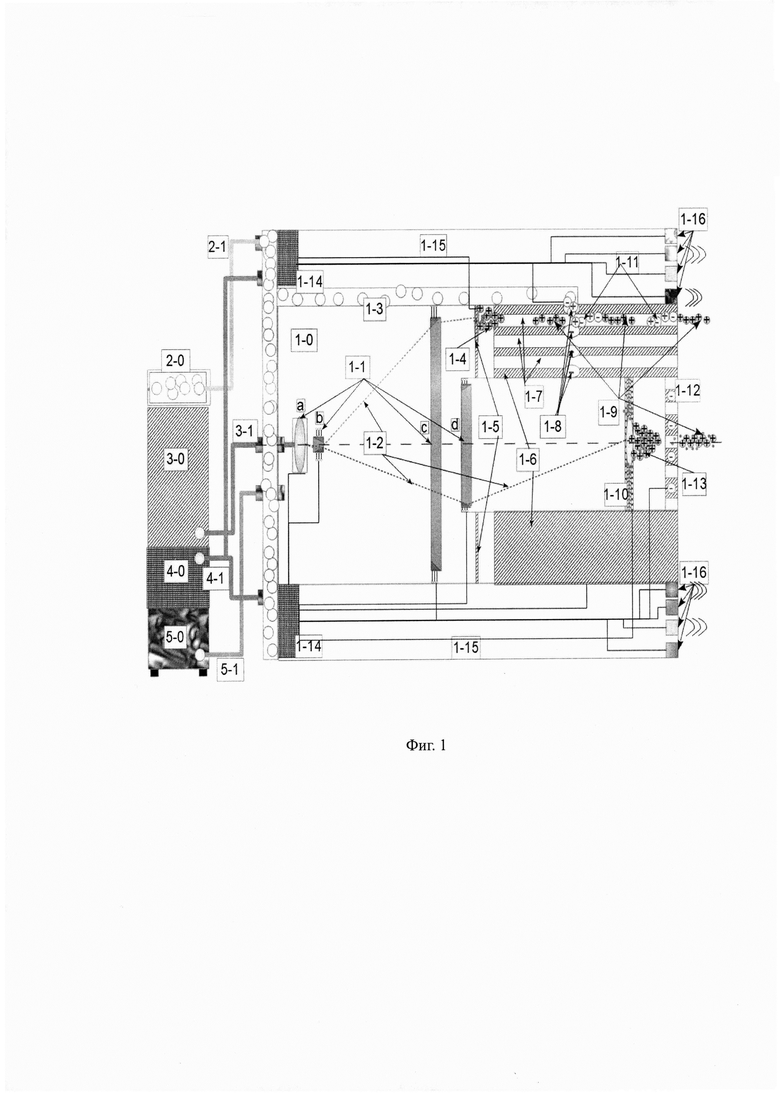
На Фиг. 1 приведена общая структурная схема пучкового устройства наноинвазивного ионно-лучевого низкоэнергетического воздействия на биоткани и агломераты клеток с функциями впрыска и мониторирования, краткое название - пучковоеустройство лучевого воздействия (ПУЛВ).
ПУЛВ (1-0) представляет собой цилиндрическую разъемную конструкцию изготовленную из нержавеющей стали внешним диаметром 10-15 мм и длиной 3-10 см, составленную из 3-х коаксиальных отсеков, при этом оба внутренних отсека находятся в едином вакуумируемом объеме с качеством вакуума 0,001-0,0001 атм.
Центральный отсек, в основном, включает элементы, обеспечивающие режим «Воздействие» - отклоняющие оптоакустические элементы (1-1b) и (1-1d), круглую 5-ти слойную мишень-излучатель (1-10), сетку-коллиматор (1-12). Начальная часть отсека занята вакуумным кабельным вводом (4-1) шлейфа от блока вычислений и управления (БВУ), приемным фланцем вакуумпровода (5-1), внутри стенки проложена подводящая магистраль действующего вещества от блока низкого давления (2-1), вакуумным вводом оптоволоконного световода (3-1), фокусирующим оптоакустическим элементом управляемой оптики и первым отклоняющим оптоакустическим элементом (1-1а) работающих во всех режимах ПУЛВ - «Воздействие» и «Впрыск».
Средний отсек, включает элементы, обеспечивающие режим «Впрыск» - отклоняющие оптоакустические элементы (1-1b) и (1-1с), кольцевую 3-ти слойную мишень-излучатель, несущий цилиндрический элемент ПУЛВ (1-6), коллимирующую сетку дрейфовых каналов формирования опорных банчей и банчей действующего вещества (1-7) с соплами подводящих каналов низкого давления диаметром 1-100 нм (1-8), которые встроены в несущий цилиндрический элемент (1-6).
Внешний отсек (1-15), включает элементы, обеспечивающие процесс мониторирования - коаксиальные электромагнитные датчики и излучатели, пьезодатчики и пьезоизлучатели (1-16) - для создания зондирующего излучения и регистрации отклика на точечный впрыск или наноинвазивное ионно-лучевое воздействие, концентраторы-коммутаторы сигналов блока вычислений и управления (1-14).
Лазерный импульс фемто-(атто)-секундной длительности с мощностью в импульсе не менее 10 ГВт вводится, с помощью гибких световодов (3-1) через оптоволоконные вакуумные вводы во внутренний объем ПУЛВ, попадая на электронно-управляемый оптоакустический фокусирующий элемент (1-1а), далее сфокусированный импульс (1-2) первым отклоняющим элементом лазерной оптики (1-1b) направляется на второй (1-1с) отклоняющий элемент в случае режима «Впрыск» или на третий (1-1d) отклоняющий элемент в случае режима «Воздействие», которые позиционируют сфокусированный импульс над заданным отверстием сетки-коллиматора на поверхности мишени-излучателя соответствующих выбранному режиму.
«Кулоновский взрыв» в заданной области мишени-излучателя рождает облако ионов движущихся в направлении перпендикулярном поверхности (1-4), (1-13), которое далее формируется в банч (1-9) отверстиями сеток-коллиматоров (1-7), (1-12). Ионы не прошедшие этап формирования осаждаются на металлизированных заземленных внутренних поверхностях ПУЛВ или удаляются в виде нейтральных атомов из внутреннего объема ПУЛВ при непрерывном вакуумировании в рабочем режиме. Далее, последовательность банчей сформированных в режиме «Воздействие» двигаясь прямолинейно в течение заданного промежутка времени обеспечивают воздействие необходимой дозы ионов со средней интенсивностью 108-1012 ионов/сек и средней энергией до 50 МэВ/нуклон прецизионно на выбранную локальную зону объекта воздействия (1-18) - биоткань или агломерат клеток.
Опорные банчи (1-9), сформированые в режиме «Впрыск» в начале дрейфовых каналов расположенных в несущем цилиндрическом элементе ПУЛВ, продолжая движение вдоль канала в области сопла (1-8), диаметр которого составляет 1-100 нм, поляризуют молекулы (атомы) действующего вещества, а затем вытягивают, захватывают порции в дрейфовый канал и формируют банч действующего вещества, двигающийся вслед за опорным банчем.
Дальнейшее прямолинейное движение последовательности опорных банчей и банчей действующего вещества (1-9) в течение заданного промежутка времени обеспечивает введение (впрыск) необходимой дозы действующего вещества масштаба нано-пико-куб. см прецизионно в выбранную локальную зону биоткани или агломерата клеток.
Для оптимального управления предлагаемым в данном изобретении устройством ионно-лучевого воздействия на биоткани необходимо получение и обработка информации о ходе процесса в реальном времени. Накопление и обработка информации производится во внешнем по отношению к ПУЛВ блоке вычислений и управления. В рамках использования ПУЛВ вычисляются значения рабочих параметров управления для ионно-лучевого воздействия или впрыска на основе информации поступающей от датчиков мониторингового (внешнего) отсека, соосно встроенного в ПУЛВ. Датчики, излучатели мониторингового отсека под управлением БВУ предназначены:
1. Для мониторинга дозы с наносекундным временным разрешением, при этом используется почти мгновенный всплеск электромагнитного излучения в различных частях спектра, зависящий от средней энергии банча ионов и сопровождающих его частиц [10, 11]. Для непрерывного наблюдения за остальными важными параметрами объектов рабочей области (геометрическими, химическими, биологическими) производится непрерывный сбор и анализ информации в активно (зондирующем, с использованием излучателей мониторингового отсека)-пассивном режиме наблюдения оптико-акустического поля и других частей электромагнитного спектра;
2. Для первичного распознавания и мониторинга воздействия ионного банча, которые осуществляются на базе расположенных во внешнем отсеке коаксиальных электромагнитных датчиков и излучателей, пьезодатчиков и пьезоизлучателей ПУЛВ для создания зондирующего излучения и регистрации отклика на точечный впрыск или наноинвазивное ионно-лучевое воздействие. Принцип работы коаксиальных датчиков основан на интегрировании оптико- и радиоакустических методов детектирования и реализует алгоритмы визуализации структурных составляющих биоткани методами оптической когерентной томографии. Для повышения информативности полученных данных возможна дополнительная обработка следующими методами: оптоакустическая томография, оптическая диффузионная спектроскопия и томография, флюоресцентная спектроскопия и томография.
3. Для непрерывной навигации в рамках рабочей области с целью прецизионного оконтуривания с точностью ~1 мкм обрабатываемых областей.
Описание изобретения пучковой системы
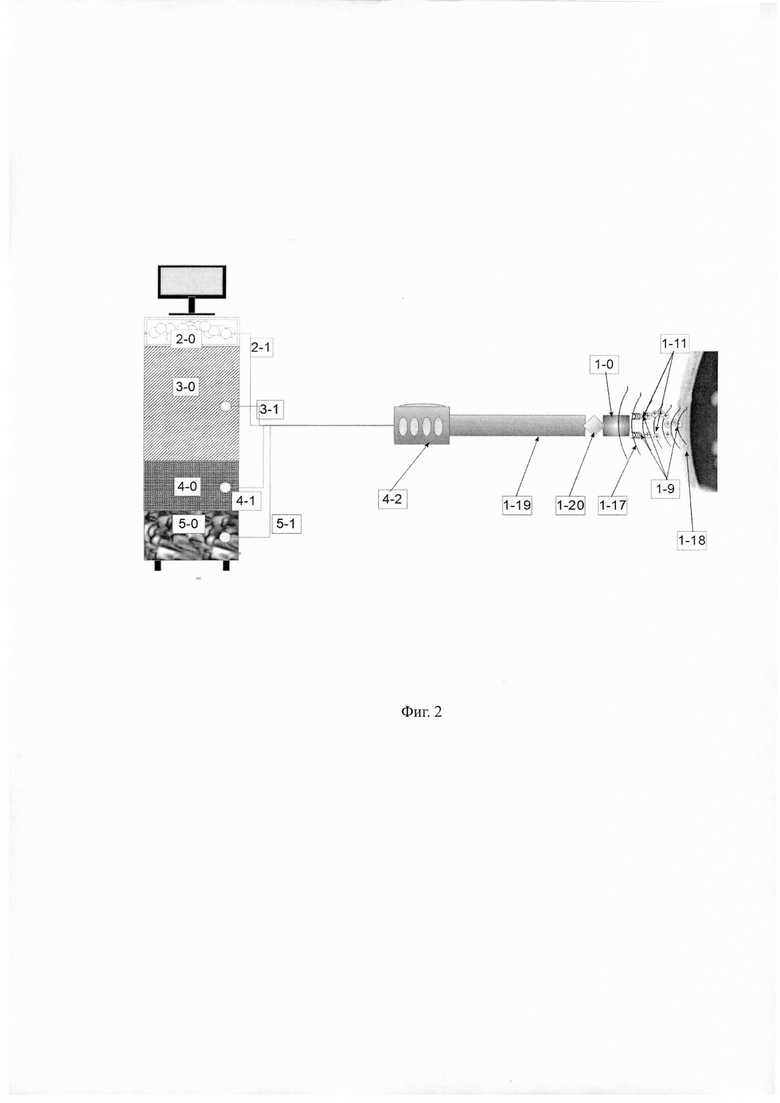
На Фиг. 2 приведена схема пучковой системы наноинвазивного ионно-лучевого низкоэнергетического воздействия на биоткани и агломераты клеток с функциями впрыска и мониторирования - пучковый инструмент лучевого воздействия на биоткани.
Подключение к ПУЛВ, описанному в разделе «Описание изобретения пучкового устройства» всех упомянутых внешних коммуникаций:
блока лазера сверхкоротких (фемто- или аттосекундных) импульсов через оптоволоконный световод;
блока (резервуара) низкого давления с действующим веществом через подводящую магистраль;
блока вакуумирования через вакуумпровод,
блока вычислений и управления через кабельный шлейф;
дополнительного блока ручной корректировки управления на кабельном шлейфе блока вычислений и управления, а также монтаж и сопряжение коммуникаций с полой несущей штангой, которая оснащена узлом крепления для дополнительного блока ручной корректировки и управляемого от БВУ шарнира типа «кардан» с узлом крепления для ПУЛВ позволяет получить действующую систему наноинвазивного ионно-лучевого низкоэнергетического воздействия на биоткани и агломераты клеток с функциями впрыска и мониторирования. Краткое название - пучковая система лучевого воздействия (ПСЛВ).
Внешний максимальный диаметр штанги в сборе с ПУЛВ не превышает 10-15 мм, что позволяет использовать ПСЛВ не только непосредственно, но и совместно, в технологиях воздействия на биоткани с применением классических троакаров.
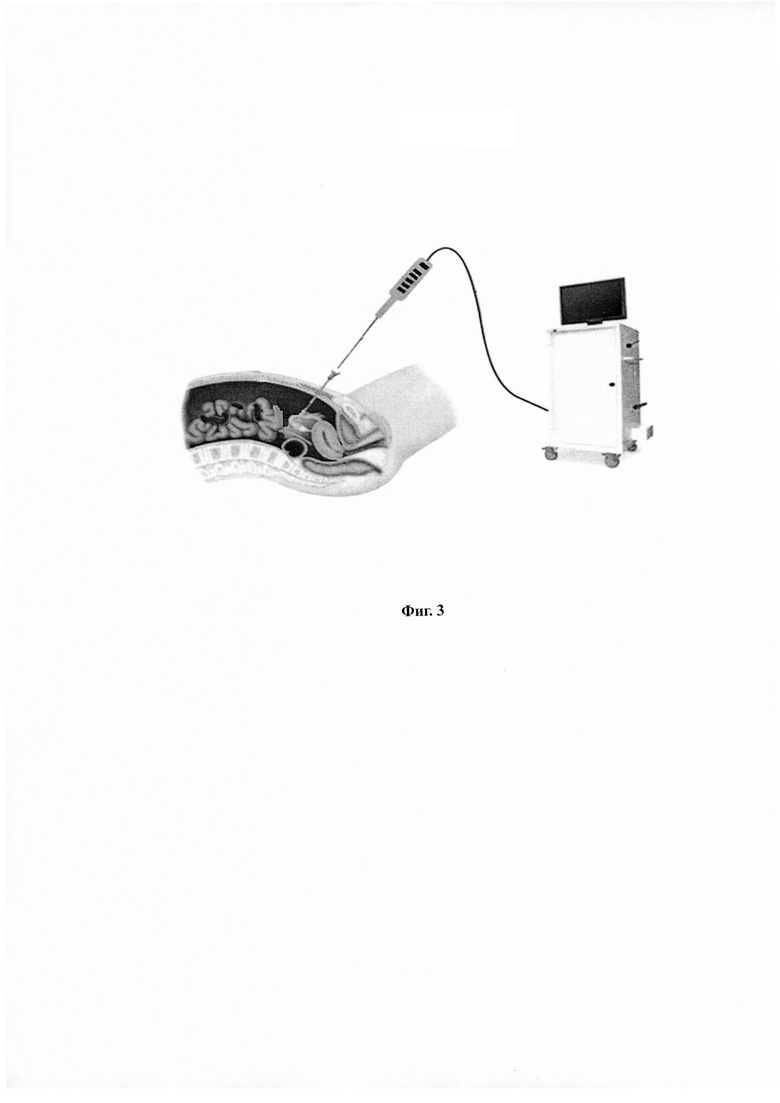
Описание изобретения пучкового комплекса
На Фиг. 3 приведена схема пучкового комплекса наноинвазивного ионно-лучевого низкоэнергетического воздействия на биоткани и агломераты клеток с функциями впрыска и мониторирования, впрыска и мониторирования на базе многоканального - до 30-ти идентичных входных оптоволоконных световодов (каналов) - ПУЛВ.
Структура ПУЛВ не изменяется. Добавляются лишь внутри стеночные каналы для протока охлаждающей жидкости блока охлаждения.
Перечень внешних блоков и соответствующих коммуникаций в этом случае расширяется и некоторые внешние блоки имеют увеличенную мощность. К ПУЛВ подключены:
30-ть блоков лазеров сверхкоротких (фемто- или аттосекундных) импульсов через жгут из 30-ти оптоволоконных световодов;
блок (резервуар) низкого давления с действующим веществом через подводящую магистраль;
блок вакуумирования увеличенной мощности через вакуумпровод;
блок охлаждения через подводящую магистраль;
блок вычислений и управления через кабельный шлейф;
дополнительный блок ручной корректировки управления на кабельном шлейфе блока вычислений и управления, а также коммуникации смонтированы и сопряжены с полой несущей штангой, которая оснащена узлом крепления для дополнительного блока ручной корректировки и управляемого от БВУ шарнира типа «кардан» с узлом крепления для ПУЛВ позволяет получить действующий мощный высокопроизводительный комплекс наноинвазивного ионно-лучевогонизкоэнергетическоговоздействия на биоткани и агломераты клеток с функциями впрыска и мониторирования. Краткое название - пучковый комплекс лучевого воздействия (ПКЛВ).
Внешний максимальный диаметр штанги в сборе с ПУЛВ не превышает 10-15 мм, что позволяет использовать ПКЛВ не только непосредственно, но и совместно, в технологиях воздействия на биоткани с применением классических троакаров.
Обозначения на рисунках.
1-0. Пучковое устройство наноинвазивного ионно-лучевого низкоэнергетического воздействия на биоткани и агломераты клеток с функциями впрыска и мониторирования, краткое название - пучковоеустройство лучевого воздействия (ПУЛВ).
1-1. Центральный отсек: оптика управления лазерным лучом ПУЛВ - фокусирующий (а) и отклоняющие (b, c, d) оптоакустические электронно-управляемые элементы.
1-2. Траектории лазерных лучей (иллюстративно) ПУЛВ при создании банча ионов для наноинвазивного воздействия и генерации сигналов отклика на воздействие, или для создания увлекающего потока ионов при точечном впрыске нано-пико-доз действующего вещества и генерации отклика на точечный впрыск.
1-3. Средний отсек: подводящая магистраль низкого давления действующего вещества внутри ПУЛВ.
1-4. Сгусток ионов, образованный в процессе «кулоновского взрыва» на мишени-излучателе для точечного впрыска нано-пико-доз действующего вещества.
1-5. Средний отсек: кольцевая 3-х слойная азимутально-структурированная мишень-излучатель для обеспечения точечного впрыска нано-пико-доз действующего вещества.
1-6. Средний отсек: несущий цилиндрический элемент ПУЛВ обеспечения точечного впрыска нано-пико-доз действующего вещества.
1-7. Средний отсек: в составе несущего элемента - коллимирующая сетка дрейфовых каналов ПУЛВ формирования опорных банчей и банчей действующего вещества для обеспечения точечного впрыска нано-пико-доз действующего вещества.
1-8. Средний отсек: в составе несущего элемента - сопла подводящих каналов низкого давления диаметром 1-100 нм для обеспечения точечного впрыска нано-пико-доз действующего вещества.
1-9. Ионные банчи сформированные для наноинвазивного воздействия и генерации сигналов отклика на воздействие, или для создания увлекающего потока ионов при точечном впрыске нано-пико-дозд ействующего вещества и генерации отклика на точечный впрыск.
1-10. Центральный отсек: круглая 5-ти-слойная азимутально-структурированная мишень-излучатель для наноинвазивного воздействия и генерации сигналов отклика на воздействие.
1-11. Банчи поляризованных молекул (атомов) действующего вещества сформированные для точечного впрыска нано-пико-доз и генерации отклика на точечный впрыск.
1-12. Центральный отсек: коллимирующая сетка (перегородка) формирователя банчей ионов для наноинвазивного воздействия и генерации сигналов отклика на воздействие.
1-13. Сгусток ионов образованный в процессе «кулоновского взрыва» на мишени-излучателе для наноинвазивного воздействия и генерации сигналов отклика на воздействие.
1-14. Внешний отсек: концентраторы-коммутаторы блока вычислений и управления.
1-15. Внешний отсек: мониторинговый отсек ПУЛВ для создания зондирующего излучения и регистрации отклика на точечный впрыск и наноинвазивное воздействие.
1-16. Внешний отсек: датчики и излучатели отсека коаксиальных электромагнитных датчиков и излучателей, пьезодатчиков и пьезоизлучателей ПУЛВ для создания зондирующего излучения и регистрации отклика на точечный впрыск и наноинвазивное воздействие.
1-17. Сигналы электромагнитного и акустического отклика на точечный впрыск, наноинвазивное воздействие и импульс зондирующих излучений.
1-18. Объект воздействия ПУЛВ - биологические ткани и/или агломераты биологических клеток.
1-19. Полая несущая штанга, с узлом крепления для дополнительного блока ручной корректировки.
1-20. Шарнир типа «кардан» с узлом крепления для ПУЛВ управляемый от БВУ.
2-0. Блок (резервуар) низкого давления с действующим веществом.
2-1. Подводящая магистраль действующего вещества от блока низкого давления.
3-0. Блок лазера сверхкоротких импульсов.
3-1. Световод от блока лазера сверхкоротких импульсов.
4-0. Блок вычислений и управления.
4-1. Кабельный шлейф от блока вычислений и управления.
4-2. Дополнительный блок ручной корректировки управления на кабельном шлейфе блока вычислений и управления.
5-0. Блок вакуумирования.
5-1. Вакуум провод от блока вакуумирования.
Литература
1. PuckTTSci.Am.202(4) 142(1960).
LodishHetal.MolecularCellBiology5thed.(NewYork: W.H. Freeman, 2003).
2. OguraKetal.Opt.Lett.372868(2012).
3. KimIJetal.Phys.Rev.Lett.111165003(2013).
4. HegelishBMetal.,arXiv:1310.8650.
5. JungDetal.Phys.Plasmas20083103(2013).
6. HaberbergerDetaLNaturePhys.895(2012).
7. KorzhimanovAVetal.Phys.Rev.Lett. 109245008(2012).
8. NishiuchiMetal.Rev.Sci.Instrum.8502B904(2014).
9. MinC-Hetal.Appl.Phys.Lett.89183517(2006).
10. VerburgJVetal.Phys.Med.Biol.58L37(2013).
11. HuangDetal.Science2541178(1991).
12. ShakhovaNMetal.LaserPhys.12617(2002)
13. DeBoerJFetal.IEEEJ.Sel.TopicsQuantumElectron.51200(1999).
14. EsenalievRO,KarabutovAA,OraevskyAAIEEEJ.Sel.Topics. QuantumElectron.5981(1999).
15. WurzingerGetal.Biomed.Opt.Express41380(2013).
16. SubochevPVetal.Dokl.Phys.5959(2014).
17. TuchinVVPhys.Usp.40495(1997).
18. GodavartyAetal.BreastCancerTargetsTherapy7193(2015).
19. TaroniPetal.Phys.Med.Biol.502469(2005).
20. OrlovaAGetal.LaserPhys.Lett.5321(2008).
21. NtziachristosVetal.NatureBiotechnol.23313(2005
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ малоинвазивной низкоэнергетической многолучевой записи информации на поверхности объекта с целью длительного хранения, считывания, диагностики и его реализующее устройство - пучковая система записи-считывания и хранения данных | 2018 |
|
RU2698168C1 |
| Способ оперативного формирования распределенной поглощенной дозы протонов в облучаемом объекте при проведении операций лучевой терапии | 2024 |
|
RU2823897C1 |
| Способ формирования распределений поглощенной дозы протонов в облучаемом объекте при проведении операций лучевой терапии | 2024 |
|
RU2837979C1 |
| СИСТЕМА УСКОРЕНИЯ ИОНОВ ДЛЯ АДРОННОЙ ТЕРАПИИ | 2005 |
|
RU2409917C2 |
| СПОСОБ ПРОВЕДЕНИЯ ОБЛУЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ ПУЧКОМ АДРОНОВ | 2011 |
|
RU2491107C2 |
| СПОСОБ ПРОВЕДЕНИЯ ОБЛУЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ МОЛОЧНОЙ ЖЕЛЕЗЫ ПУЧКОМ АДРОНОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2423156C2 |
| СПОСОБ ПРОВЕДЕНИЯ ОБЛУЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ПИЩЕВОДА ПУЧКОМ АДРОНОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2423157C2 |
| СПОСОБ ПРОВЕДЕНИЯ ОБЛУЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ТРАХЕИ ПУЧКОМ АДРОНОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2423155C2 |
| СПОСОБ ПРОВЕДЕНИЯ ОБЛУЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ЖЕЛУДКА ПУЧКОМ АДРОНОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2424012C2 |
| СПОСОБ ПРОВЕДЕНИЯ ОБЛУЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ЛЕГКИХ ПУЧКОМ АДРОНОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2420332C2 |
Изобретение относится к медицинской технике. Пучковое устройство лучевой терапии (ПУЛТ) избирательно воздействует ориентированно на опухоль или другую патологию пучком заряженных частиц, сформированным в виде прецизионно сфокусированных банчей с обеспечением минимального воздействия на окружающие опухоль здоровые ткани, причем генерацию заряженных частиц осуществляют с помощью возбуждающего многоканального генератора низкоэнергетических ионов на основе высокочастотного лазера, направленного на многослойную структурированную мишень-излучатель заряженных частиц, расположенную в концевой части пучкового устройства лучевой терапии (ПУЛТ), которое неинвазивным методом воздействует на опухоль или другую патологию. Основными элементами системы, пучкового комплекса, являются перемещаемый инструмент воздействия на опухоль, выполненный в виде ПУЛТ, генерирующего банчи заряженных частиц; лазер генератора низкоэнергетических ионов и емкость с вводимым препаратом активно действующего вещества под низким давлением. 3 н.п. ф-лы, 3 ил.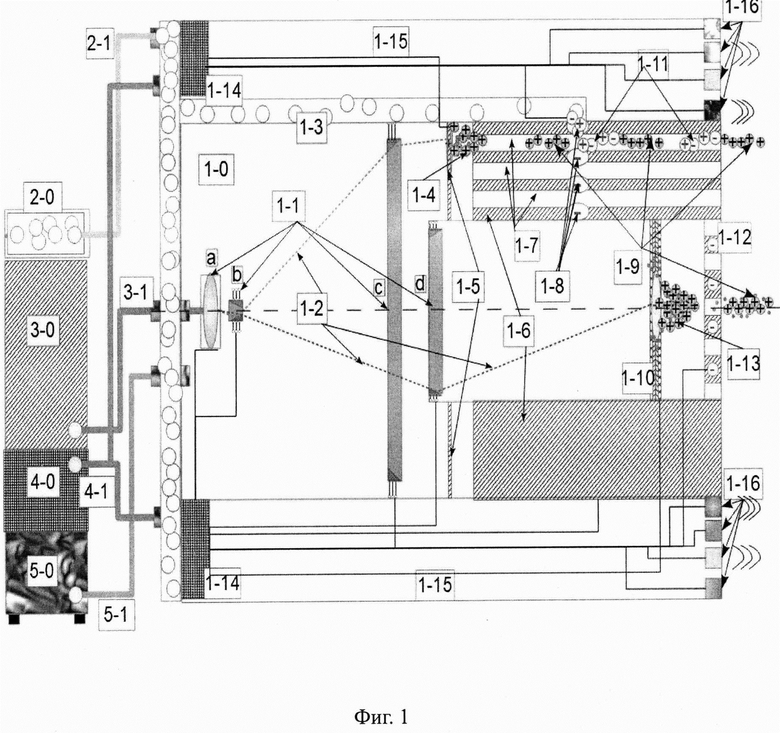
1. Пучковое устройство импульсно-периодического воздействия на биологические ткани и/или агломераты биологических клеток с мониторированием воздействия и дополнительной функцией точечного впрыска действующего вещества с мониторированием, основанное на использовании априорных данных, определении местоположения, оконтуривании области и избирательной локализации сформированного пучка заряженных частиц, пучок заряженных частиц, ориентированный на выбранную область с точностью позиционирования 1-10 мкм, формируется в виде прецизионно сколлимированных банчей ионов с энергией до 50 Мэв/нуклон в сопровождении электронов, позитронов и гамма-квантов, в течение заданного промежутка времени обеспечивает воздействие необходимой дозой ионов со средней интенсивностью 108-1012 ионов/сек с обеспечением минимального воздействия на окружающие выбранную область здоровые ткани, причем генерацию единичного банча заряженных частиц осуществляют с помощью сверхкороткого импульса лазера фемто-атто-секундной длительности, направляемого на одну из многослойных азимутально-структурированных мишеней-излучателей, обеспечивающих создание банча с несколькими типами ионов в сопровождении электронов, позитронов и гамма-квантов для наноинвазивного воздействия на клетки биоткани или агломерата и генерации сигналов отклика на воздействие в режиме «Воздействие», или создание увлекающего потока ионов при точечном впрыске нано-пико-куб. см доз действующего вещества на заданную глубину и генерации сигналов отклика на точечный впрыск в режиме «Впрыск», излучение лазера подводится к пучковому устройству по гибкому световоду, электронное управление позиционированием и фокусировкой лазерных импульсов на мишенях-излучателях осуществляется акустооптическими отклоняющими и фокусирующим элементами лазерной оптики, мониторинг процесса лучевого воздействия и впрыска осуществляется посредством аксиально-расположенных излучателей и датчиков пучкового устройства, содержащих матрицы чувствительных элементов для приема ультрафиолетового, видимого, инфракрасного диапазонов электромагнитного спектра, пьезодатчики для приема ультразвукового излучения с обеспечением возможности приема генерируемых банчем непосредственно и отраженных сигналов, а также матрицы излучателей в ультрафиолетовом, видимом, инфракрасном диапазонах электромагнитного спектра и ультразвуковом диапазоне акустических волн, впрыск действующего вещества с обеспечением прецизионного введения нано-пико-куб. см доз непосредственно в выбранную локальную зону клеток биологической ткани или агломерата осуществляется путем поляризации, захвата, последующего увлечения электромагнитным полем ионных банчей в дрейфовый канал и формирования пучка впрыска в виде следующих друг за другом прецизионно сколлимированных опорных банчей ионов и банчей действующего вещества.
2. Пучковая система, построенная на базе пучкового устройства по п. 1, встроенного в эндоскоп, дополненный троакаром для доступа в закрытые полости, с набором внешних блоков обеспечения функционирования - блок питания, блок вакуумирования, блок сверхкороткоимпульсного лазера, блок низкого давления с действующим веществом для впрыска, блок вычислений и управления с соответствующими гибкими подводящими магистралями.
3. Пучковый комплекс, построенный на базе многократно - до 30-повторенных идентичных пучковых устройств по п. 1, встроенных в эндоскоп, дополненный троакаром для доступа в закрытые полости, с соответствующим набором внешних блоков обеспечения функционирования - блок охлаждения, блок вакуумирования, блоки сверхкороткоимпульсных лазеров, блок низкого давления с действующим веществом для впрыска, блок вычислений и управления с соответствующими гибкими подводящими магистралями.
| Способ скрытого малоинвазивного маркирования объекта с целью его идентификации | 2016 |
|
RU2644121C2 |
| WO 2004054331 A1, 24.06.2004 | |||
| WO 2006081847 A1, 10.08.2006. | |||
Авторы
Даты
2020-06-25—Публикация
2019-06-26—Подача