Область техники, к которой относится изобретение
Изобретение относится к медицине, в частности к торакальной хирургии, и может быть использовано для уменьшения количества послеоперационных осложнений после резекции каудального отдела пищевода и эзофагогастроанастомоза.
Операция резекции каудального отдела пищевода и эзофагогастроанастомоза (Льюиса) - травматичная, инвалидизирующая операция, которая характеризуется выраженными топографоанатомическими изменениями органов грудной клетки и верхнего этажа брюшной полости. Изменения заключаются в латеральном смещении в сторону операции и вращении относительно легочных вен средостения и его органов, прежде всего сердца. Топографоанатомические изменения, происходящие в грудной клетке, сопровождаются функциональными изменениями, прежде всего со стороны дыхательной и сердечно-сосудистой систем. Также возникает выраженная деформация грудной клетки, сколиоз. На стороне операции происходит поднятие купола диафрагмы со смещением органов верхнего этажа брюшной полости (Самойлов П.В. Изменения топографии органов средостения после резекции пищевода с пластикой желудочным трансплантантом (операции типа Льюиса) в отдаленные сроки после операции. / Фундаментальные исследования.-2013.-№5.-с.135-138).
Развитие середчно-сосудистых осложнений при хирургических операциях является нерешенной проблемой на сегодняшний день, поскольку они широко распространены и крайне неблагоприятно влияют на послеоперационный прогноз (Безденежных А.В. Сумин А.Н., 2017; Щукин Ю.В. и др., 2011; Кавайкин А.Г., Чичеватов Д.А., 2013). Известно, что хирургическое вмешательство на пищеводе относится к операциям высокого риска развития сердечно-сосудистых осложнений, частота которых нередко превышает 5% (Kristensen S.D., 2014). В значительной степени развитие послеоперационных осложнений зависит от изменений топографии органов средостения в послеоперационном периоде, что определяет необходимость выявления величины смещения сердца.
Уровень техники.
В литературе описан способ визуального определения смещения сердца после операции Льюиса путем рентгенографии органов грудной клетки до- и после операции (Рентгенография в диагностике заболеваний органов грудной клетки. Под редакцией В.В.Мельникова в 2-х частях, часть 1 2017.-122с.). Способ имеет недостатки: требует рентгеновского оборудования, неоднократного радиационного облучения больного, не дает количественной характеристики смещения сердца.
Известен способ определения основных функциональных показателей миогеодинамики сердца (Способ определения основных показателей миогемодинамики сердца / Бодин О.Н. / Бурукина И.П. / Митин А.А. / Огоньков В.В. / Митрошин А.Н. / Бондаренко Л.А. / Рудакова Л.Е. // Патент РФ № 2264786, МПК А61В 5/0402, 6/00.), заключающийся в том, что регистрируют прямой и левый боковой флюорографические снимки сердца пациента, определяют по снимкам геометрические параметры сердца пациента, осуществляют наложение на них компьютерной модели сердца, осуществляют совмещение и нелинейное масштабирование компьютерной модели сердца. Метод требует участия при диагностике высококвалифицированного специалиста, использования дорогостоящей аппаратуры и значительных затрат времени на проведение одного исследования. Эхокардиография (Функциональная диагностика в кардиологии. Под редакцией Л.А. Бокерия, Е.З. Голуховой, А.В. Иваницкого. В 2-х томах. Т2.-М.: Издательство НЦССХ им. А.Н. Бакулева РАМН, 2005.-296с.) до- и после операции дает полную информацию по изменению внутрисердечных структур и гемодинамики сердца. Однако, наряду с простотой и низкой стоимостью исследования, стандартная процедура не позволяет получить количественную характеристику изменения топографии сердца.
Известен способ построения трехмерной модели сердца (Automaticdelineationofheartbordersandsurfacesfromimages / Richard K.Johnson / JohnAlanMcDonald / Florence H. Sheehan // US 2003038802 от 27.02.2003) при помощи ультразвуковой эхокардиографии, основанный на регистрации отраженных от лоцируемого объекта ультразвуковых волн и дающий возможность визуализации сердечных структур и построения модели поверхности сердца. Однако метод требует участия при диагностике высококвалифицированного специалиста, использования дорогостоящей аппаратуры и значительных затрат времени на проведение одного исследования. Широкое использование эхокардиографического метода при скрининге затруднено также из-за большого количества используемых методик и стандартных проекций, каждая из которых применяется для изучения определенных анатомических отделов сердца и диагностики определенных патологий, так как получаемые изображения сечений сердца зависят от положения датчика. Кроме того, при эхокардиографическом методе невозможно получить достоверную диагностическую информацию при ряде анатомических особенностей сердца пациента.
Прототипом предложенного способа является компьютерная томография органов грудной клетки (Самойлов П.В. Изменения топографии органов средостения после резекции пищевода с пластикой желудочным трансплантантом (операции типа Льюиса) в отдаленные сроки после операции / Фундаментальные исследования.-2013.-№5.-с.135-138). На этапе дооперационного исследования компьютерная томография позволяет получить графическое изображение органов средостения в аксиальной проекции и произвести количественные измерения, характеризующие положение сердца. После операции способ компьютерной томографии позволяет количественно оценить возникшие изменения в положении сердца.
На наш взгляд существенным недостатком данного способа является его ограниченная доступность, дороговизна, облучение больного, сложность количественных измерений.
Раскрытие сущности изобретения
Задача изобретения. Разработать доступный, легко реализуемый способ определения изменения положения сердца после операции Льюиса.
Новизна изобретения заключается в определении ротационного смещения сердца после операции Льюиса путем измерения толщины межжелудочковой перегородки пациента ультразвуковым исследованием до- и после операции.
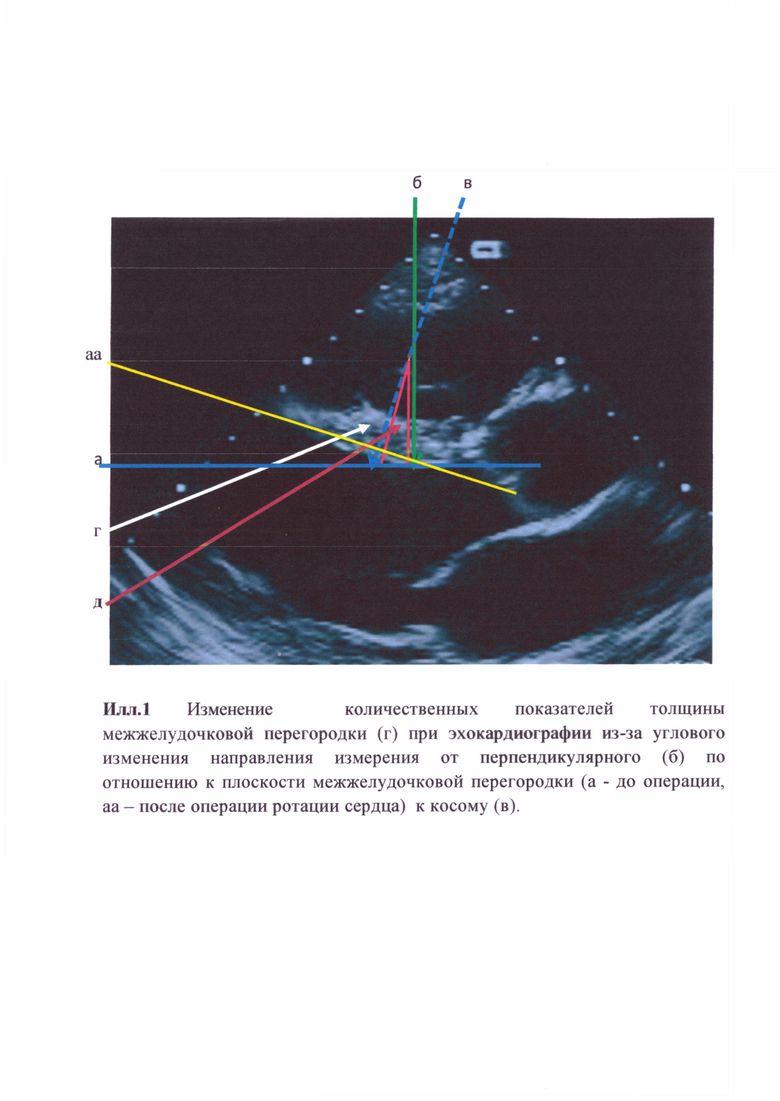
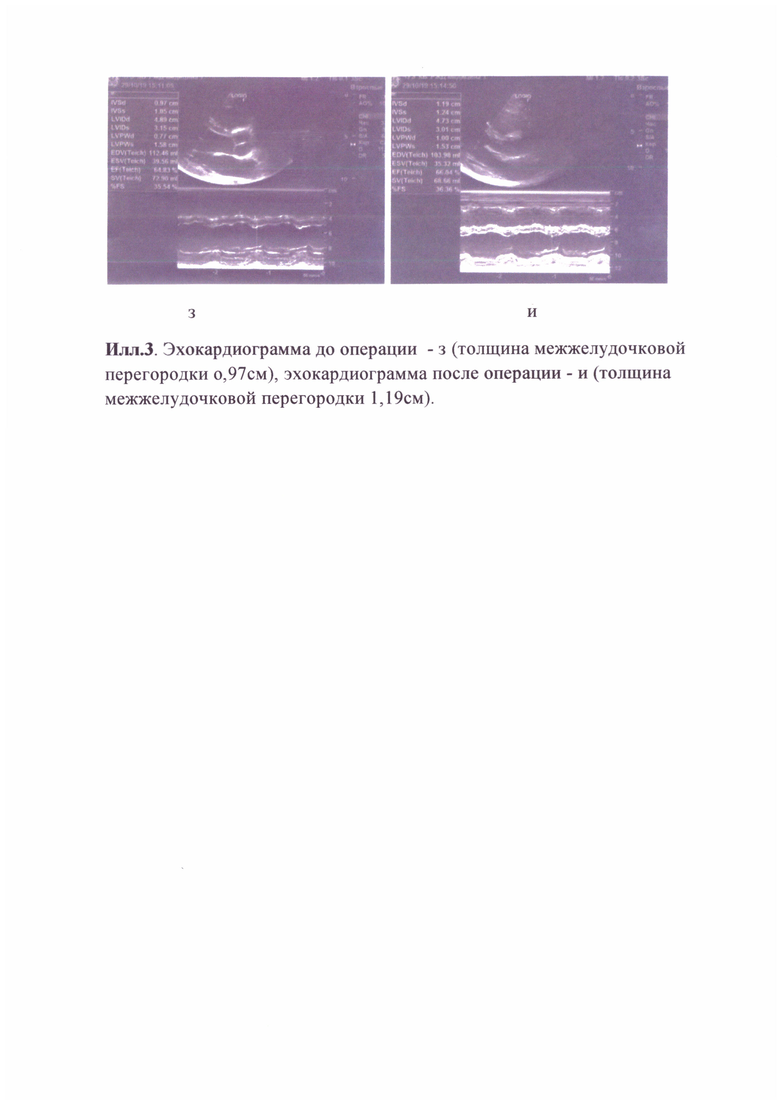
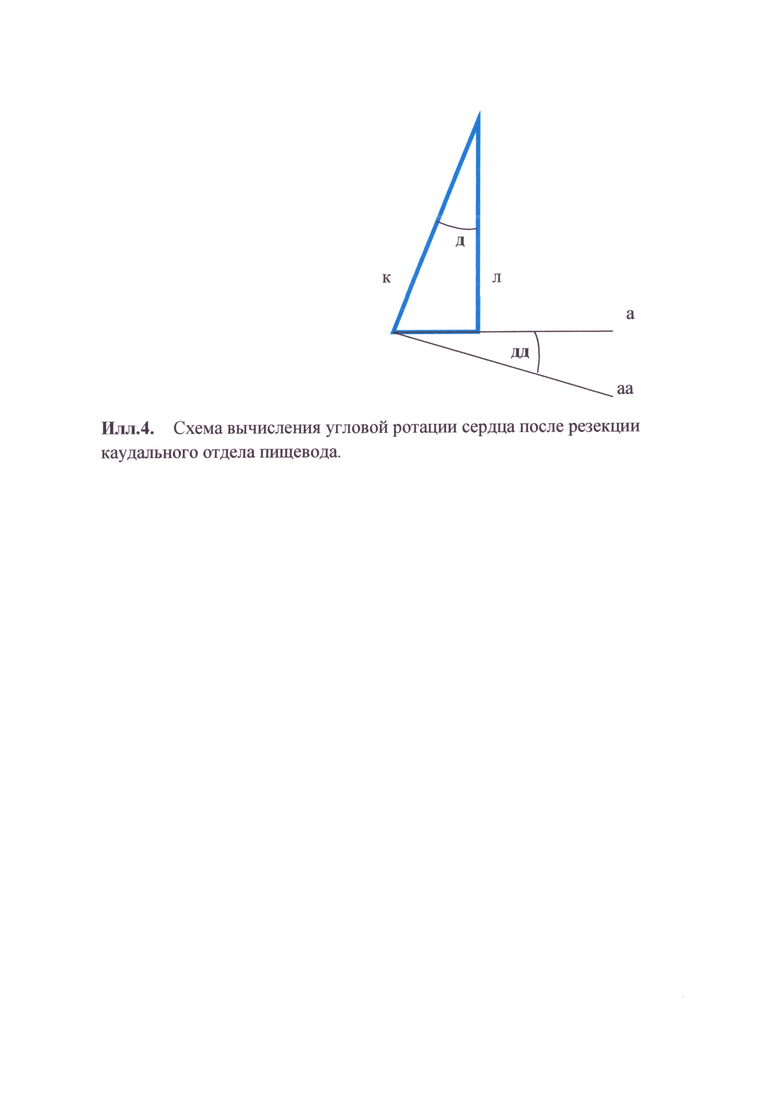
Раскрытие изобретения состоит в том, что количественные показатели толщины межжелудочковой перегородки (илл.1г) при эхокардиографии изменяются из-за углового изменения направления измерения от перпендикулярного (илл.1б, илл.2е) по отношению к плоскости межжелудочковой перегородке (илл.1а - до операции, илл.1аа - после ротации сердца) к косому (илл.1в, илл.2ж). Различия этих величин позволяют вычислить угол дд ротационного смещения сердца (плоскостей а-аа), соответствующий углу д (илл.1д, илл.4). Смещение сердца в послеоперационном периоде происходит в правую половину грудной клетки и к грудине с ротацией против часовой стрелки, соответственно со смещением внутрисердечных структур. Межжелудочковая перегородка имеет наименьшую подвижность во время работы сердца, увеличиваясь в толщине во время систолы при сокращении желудочков и уменьшаясь во время диастолы при расслаблении желудочков сердца. Стандартные измерения межжелудочковой перегородки проводятся в период систолы и в период диастолы в М-режиме из парастернальной позиции длинной оси левого желудочка на уровне нижнего края створок митрального клапана и его хорд. При одинаковом стандартном направлении ультразвукового луча за счет ротации сердца вследствие изменения углового направления измерения будет увеличиваться показатель толщины межжелудочковой перегородки из-за смещения ее плоскости по отношению к ультразвуковому лучу датчика (ил.3з - эхокардиограмма до операции, толщина межжелудочковой перегородки о,97см, ил.3и - эхокардиограмма после операции, толщина межжелудочковой перегородки 1,19 см). Измерение необходимо проводить в период диастолы, поскольку на толщину межжелудочковой перегородки в систолу в большой степени влияет состояние сократительной способности желудочков сердца. Снижение сократительной способности уменьшает толщину межжелудочковой перегородки в систолу, возрастание сократительной способности приводит к ее увеличению. Увеличение толщины межжелудочковой перегородки в диастолу возможно при ее гипертрофии, но за короткий послеоперационный период гипертрофия межжелудочковой перегородки развиться не может (Функциональная диагностика в кардиологии. Под редакцией Л.А. Бокерия, Е.З. Голуховой, А.В. Иваницкого. В 2-х томах. Т2.-М.: Издательство НЦССХ им. А.Н. Бакулева РАМН, 2005.-296с.).
Технический результат достигается тем, что измеряется путем ультразвукового исследования толщина межжелудочковой перегородки в диастолу до и после операции. Вычисляется косинус угла д (ил.1, 4) изменения направления измерения до и после операции, где толщина межжелудочковой перегородки до операции является прилежащим катетом (л), а толщина межжелудочковой перегородки после операции является гипотенузой (к) (ил.4). Угол изменения направления измерения до и после операции определяется по таблице Брадиса и соответствует углу ротации сердца (углу ротации плоскости межжелудочковой перегородки).
Способ осуществляется следующим образом: у больного при эхокардиографии до операции определяется толщина межжелудочковой перегородки в диастолу. В послеоперационном периоде вновь проводится определение толщины межжелудочковой перегородки в диастолу. С учетом значений толщины межжелудочковой перегородки до- и после операции и вычисляется косинус угла измерения направления ультразвукового измерения межжелудочковой перегородки до и после операции (ил.4) по формуле:
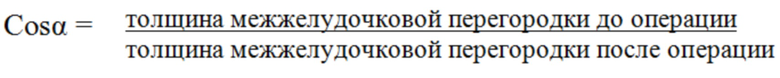
Далее по четырехзначным математическим таблицам Брадиса В.М. (Брадис В.М. Четырехзначные математические таблицы: Для сред.шк. - 57-е изд. - М.: Просвещение, 1990. - 95 с.) определяется угол д, полученный угол соответствует углу поворота плоскости межжелудочковой перегородки дд (ил.1, 4) и характеризует ротационное смещение сердца после операции.
Примеры использования способа
Пример 1. Больной А., 52 года, госпитализирован с жалобами на дисфагию давностью 1 год. При обследовании выявлен кардиоэзофагеальный рак. Проведена расширенная операция типа Льюиса. При эхокардиографическом исследовании до операции толщина межжелудочковой перегородки в диастолу составила 8,6мм. Через 14 дней после операции толщина межжелудочковой перегородки в диастолу составила 10,6мм. С учетом полученных величин вычисляем cosα = 8,6/10,6=0,8113=35°51’.
Угол ротационного смещения сердца после операции равен 35°51’.
Пример 2. Больной П., 61 год, поступил с жалобами на дисфагию в течение последних з-х месяцев. При обследовании был выявлен рак средне-грудного отдела пищевода, по поводу которого больной был прооперирован с использованием комбинированной операции типа Льюиса.
При эхокардиографическом исследовании до операции толщина межжелудочковой перегородки в диастолу составила 9,8 мм. Через 14 дней после операции толщина межжелудочковой перегородки в диастолу составила 11,5 мм. С учетом полученных величин вычисляем cosα = 9,8/11,5=0,8522=31°33’.
Угол ротационного смещения сердца после операции равен 31033’.
Литература, принятая во внимание:
1. Безденежных А.В. Сумин А.Н. Оценка риска сердечно-сосудистых осложнений при внесердечных оперативных вмешательствах: коморбидность и применение шкал клинической оценки // Сибирский медицинский журнал. 2017.- № 5.- С. 90-105.
2. Брадис В.М. Четырехзначные математические таблицы: Для сред.шк. - 57-е изд. - М.: Просвещение, 1990. - 95 с.
3. Кавайкин А.Г., Чичеватов Д.А., Внутриплевральнаяэзофагопластика при раке пищевода и гастроэзофагеальном раке: непосредственные и отдаленные результаты // Известия высших учебных заведений. Поволжский регион. Медицинские науки. 2013. №1(25). С.84-91.
4. Прогнозирование и профилактика кардиальных осложнений внесердечных хирургических вмешательств. Национальные рекомендации / Щукин Ю.В., Хохлунов С.М., Суркова Е.А., Дупляков Д.В., Вачев А.Н., Германов А.В. и др. // Кардиоваскулярная терапия и профилактика. 2011. №10(6). С.1- 28.
4. Рентгенография в диагностике заболеваний органов грудной клетки. Под редакцией В.В.Мельникова в 2-х частях, часть 1 2017.-122с.
5. Самойлов П.В. Изменения топографии органов средостения после резекции пищевода с пластикой желудочнымтрансплантантом (операции типа Льюиса) в отдаленные сроки после операции./ Фундаментальные исследования.-2013.-№5.-с.135-138
6. Способ определения основных показателей миогемодинамики сердца / Бодин О.Н. / Бурукина И.П. / Митин А.А. / Огоньков В.В. / Митрошин А.Н. / Бондаренко Л.А. / Рудакова Л.Е. // Патент РФ № 2264786, МПК А61В 5/0402, 6/00.
7. Функциональная диагностика в кардиологии. Под редакцией Л.А. Бокерия, Е.З. Голуховой, А.В. Иваницкого. В 2-х томах. Т2.-М.: Издательство НЦССХ им. А.Н. Бакулева РАМН, 2005.-296с.
8. Automatic delineation of heart borders and surfaces from images / Richard K. Johnson / John Alan McDonald / Florence H. Sheehan // US 2003038802 от 27.02.2003.
9. 2014 ESC/ESA Guidelines on non-cardiac surgery: cardiovascular assessment and management: The Joint Task Force on non-cardiac surgery: cardiovascular assessment and management of the European Society of Cardiology (ESC) and the European Society of Anaesthesiology (ESA) / Kristensen S.D., Knuutu J., Saraste A. et al. // European Heart Journal. 2014. V. 35, I. 35, P. 2383-2431.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ эхокардиографии у пациентов после операции пневмонэктомии в отдаленном периоде | 2018 |
|
RU2698091C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОБСТРУКЦИИ АОРТОКОРОНАРНЫХ ШУНТОВ | 2003 |
|
RU2255657C2 |
| СПОСОБ КОРРЕКЦИИ ПЛЕВРАЛЬНОЙ ПОЛОСТИ ПРИ РЕЗЕКЦИИ ЛЕГКИХ | 2006 |
|
RU2305503C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГИПЕРТРОФИЧЕСКОЙ ОБСТРУКТИВНОЙ КАРДИОМИОПАТИИ С СОПУТСТВУЮЩЕЙ МИТРАЛЬНОЙ НЕДОСТАТОЧНОСТЬЮ | 1998 |
|
RU2141259C1 |
| СПОСОБ ПРЕДВАРИТЕЛЬНОЙ ДИАГНОСТИКИ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА У БОЛЬНЫХ С ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНЬЮ ПРИ НАЛИЧИИ ГИПЕРТРОФИИ МИОКАРДА ЛЕВОГО ЖЕЛУДОЧКА | 1992 |
|
RU2078538C1 |
| Способ определения операбельности больных раком пищевода | 2019 |
|
RU2718290C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ГИПЕРТРОФИЧЕСКОЙ НЕОБСТРУКТИВНОЙ КАРДИОМИОПАТИИ И ВТОРИЧНЫХ ГИПЕРТРОФИЙ МИОКАРДА | 2014 |
|
RU2567794C1 |
| СПОСОБ УЛЬТРАЗВУКОВОЙ ДИАГНОСТИКИ АНОМАЛИЙ ПОЛОЖЕНИЯ И ВЕТВЛЕНИЯ ДУГИ АОРТЫ У НОВОРОЖДЕННЫХ И ДЕТЕЙ РАННЕГО ВОЗРАСТА | 2024 |
|
RU2830638C1 |
| СПОСОБ ОЦЕНКИ КРОВОСНАБЖЕНИЯ ГРУДИНЫ ПОСЛЕ ОПЕРАЦИЙ НА ГРУДНОЙ КЛЕТКЕ | 2001 |
|
RU2199273C1 |
| Способ выбора хирургического доступа при выполнении супракоронарной миотомии на работающем сердце у пациентов с изолированным миокардиальным мостиком передней межжелудочковой артерии при отсутствии иной кардиальной патологии, требующей оперативного лечения | 2021 |
|
RU2766251C1 |

Изобретение относится к медицине, в частности к торакальной хирургии. До операции посредством эхокардиографии измеряют толщину межжелудочковой перегородки. Затем после операции измеряют толщину межжелудочковой перегородки. На основании полученных величин вычисляют косинус угла ротации плоскости межжелудочковой перегородки (д) как отношение толщины межжелудочковой перегородки до операции к толщине межжелудочковой перегородки после операции. Далее по четырехзначным математическим таблицам Брадиса В.М. определяется угол д, соответствующий углу поворота плоскости межжелудочковой перегородки и характеризующий ротационное смещение сердца после операции. Способ позволяет с высокой точностью определить ротационное смещение сердца при резекции пищевода при операции Льюиса. 4 ил., 2 пр.
Способ определения изменения положения сердца после операции Льюиса путем эхокардиографии до и после операции, отличающийся тем, что до операции посредством эхокардиографии измеряют толщину межжелудочковой перегородки, затем после операции измеряют толщину межжелудочковой перегородки, после чего на основании полученных величин вычисляют косинус угла ротации плоскости межжелудочковой перегородки (д) как отношение толщины межжелудочковой перегородки до операции к толщине межжелудочковой перегородки после операции; и далее по четырехзначным математическим таблицам Брадиса В.М. определяется угол д, соответствующий углу поворота плоскости межжелудочковой перегородки и характеризующий ротационное смещение сердца после операции.
| Самойлов П.В | |||
| Изменения топографии органов средостения после резекции пищевода с пластикой желудочным трансплантантом (операции типа Льюиса) в отдаленные сроки после операции, Фундаментальные исследования, 2013, 5, с.135-138 | |||
| Разрывная застежка | 1930 |
|
SU22635A1 |
| КОРНЯКОВА А | |||
| Р | |||
| и др | |||
| Влияние операции типа Льюиса на функциональное состояние срдечно-сосудтстой | |||
Авторы
Даты
2020-10-01—Публикация
2019-12-04—Подача