Изобретение относится к области медицины, а именно к урологии, касается методики лапароскопической простатэктомии и может быть использовано для радикального хирургического лечения локализованного рака предстательной железы стадий Т1-Т2.
В настоящее время в онкоурологической практике радикальная простатэктомия является основным и самым эффективным методом лечения Т1- и Т2-стадий РПЖ у лиц с ожидаемой продолжительностью жизни более 10 лет. Пораженный орган может быть удален посредством открытого хирургического пособия или с помощью различных методик эндовидеохирургических вмешательств, сопоставимых с открытым методом по своим онкологическим показателям, но менее травматичных для окружающих тканей и органов. Для лапароскопической простатэктомии (ЛРП), по сравнению с открытым методом, характерны меньшие время пребывания в стационаре, частота и выраженность интра- и послеоперационных осложнений (кровопотери, болезненность, недержание мочи, эректильная дисфункция, инфекционно-воспалительные процессы и др.). Так, исходя из данных полученных в ходе многоцентрового ретроспективного исследования, у пациентов, перенесших радикальную простатэктомию открытую (ОРП), лапароскопическую (ЛРП) и робот-ассистированную (РаРП), объем кровопотери был равен в среднем 935 мл, 442 мл и 191 мл, соответственно, необходимость в гемотрансфузии возникала с частотой 19,9%, 6,3% и 4,6%, время нахождения в стационаре составляло 7,8, 6,09 и 3,85 суток, время дренирования мочевого пузыря уретральным катетером Фолея - 1,23-16 суток, 1-12 суток и 1-8 суток, соответственно [Прилепская Е.А., Мальцев Е.Г., Колонтарев К.Б., Говоров А.В., Раснер П.И., Васильев А.О., Садченко А.В., Дьяков В.В., Пушкарь Д.Ю. Сравнительный анализ функциональных и онкологических результатов радикальной простатэктомии - позадилонной, лапароскопической и робот-ассистированной // ОУ. 2015. №4]. Удержание мочи после ЛРП было сохранено в 83,5-95% случаев, после ОРП - в 73-97% случаев [Переверзев А.С., Коган М.И. Рак простаты. Монография / Изд-во «Факт», Харьков, 2004. - 231 с.].
Важнейшим направлением дальнейшего развития и усовершенствования лапароскопической хирургии является снижение уровня инвазивности лапароскопических операций за счет минимизации объема локальной травмы при получении доступа и сокращение времени оперативного вмешательства. Например, применение методики выполнения доступа через мочевой пузырь к оперируемому органу существенно ограничивают хирургическое повреждение околопростатических и околопузырных структур, в том числе и механизма отвечающего за удержание мочи в послеоперационном периоде, дорзального венозного сплетения простаты благодаря чему снижается риск массивного кровотечения, что способствует повышению качества лечебных мероприятий, скорому восстановлению пациентов, сохранению качества жизни в послеоперационном периоде, при этом высокие показатели эффективности и онкологической безопасности остаются на уровне стандартных вмешательств.
Известен способ радикальной простатэктомии, включающий доступ к передней поверхности мочевого пузыря и простаты, удаление простаты, ушивание раны, в котором поочередно формируют два тоннеля справа и слева от проекции шейки мочевого пузыря в слое жировой ткани, расположенном медиальнее сухожильной дуги таза и латеральнее пубовезикального комплекса, до появления семявыносящих протоков и семенных пузырьков, по внутренней поверхности сформированных тоннелей верифицируют и пересекают наружные боковые пучки детрузора и пузырно-простатическую мышцу, освобождая проксимальную уретру по заднебоковой полуокружности, объединяют тоннели, далее продвигаются по контуру основания простаты из глубины наружу от 6 к 12 часам условного циферблата, рассекают краниально передний фартук детрузора, затем пересекают проксимальную часть интрапростатической уретры, выделяют семенной комплекс, проводят заднюю диссекцию простаты, начав медиальнее сухожильной дуги таза, разделяют слой между латеральной перипростатической, внутритазовой фасциями и фасцией мышц, поднимающих задний проход, до обнажения лобково-промежностной мышцы с обеих сторон, после чего, ориентируясь на прослойку жировой ткани между пубовезикальным комплексом и передней перипростатической фасцией, их разделяют до уретрального сфинктера, при этом дорзальный венозный комплекс не прошивают, далее выделяют и пересекают дистальный отдел интрапростатической уретры, предстательную железу перемещают в контейнер для последующего извлечения, накладывают анастомоз между проксимальным и дистальным отделом уретры непрерывным или узловыми швами, сухожильные дуги таза и пубо-везикальный комплекс фиксируются швами к шейке мочевого пузыря (патент РФ №2675171, А61В 17/00, опубл. 17.12.2018). Недостатком этого способа является высокая локальная травматизация, в следствии чего достаточно большое количество пациентов с недержанием мочи в послеоперационном периоде, длительность оперативного вмешательства, что может негативно сказаться на состоянии онкологического пациента.
Классическая технология внебрюшинной лапароскопической радикальной простатэктомии, как частный случай лапароскопической операции, предполагает выполнение внебрюшинного доступа (формируя при этом локальную полость в предпузырном пространстве по средством балонного дилататора) либо через брюшную полость, при этом также формируется локальная рабочая зона в предпузырном пространстве, далее все этапы проводятся аналогичным образом с доступом через брюшную полость. Альтернативным и более щадящим вариантом доступа к предстательной железе, является не имеющий аналогов в онкоурологической практике доступ к предстательной железе посредством рассечения дна мочевого пузыря.
Задачей изобретения явилась создание способа радикального хирургического лечения локализованного рака предстательной железы, имеющего широкие функциональные возможности, позволяющего снизить объем интра- и послеоперационных осложнений, сократить продолжительность операции и предупредить возникновение рецидивов.
Решение поставленной задачи обеспечивается тем, что в способе лапароскопического радикального лечения локализованного рака предстательной железы с доступом через мочевой пузырь, пациент находится под эндотрахеальным наркозом, после чего выполняется укладка на операционном столе и выполненяется трансумбиликальный разрез кожи размером 2,5 см., далее послойно осуществляют доступ в брюшную полость, в которую после установки стандартного 10 мм. троакара вводится лапароскоп и осуществляется инсуфляция СО2 до 12 мм рт. ст., производится осмотр всех отделов брюшной полости. Отступив медиальнее на 2 см от передне-верхней ости гребня подвздошной кости под визуальным контролем размещаются два порта - слева диаметром 10 мм, справа - 5 мм. По латеральному краю передней мышцы живота с обеих сторон на уровне пупка под визуальным контролем устанавливаются два 5 мм троакара для рабочих инструментов оператора и ассистента. После заполнения мочевого пузыря (через уретральный катетер) до 200 мл физиологическим раствором для лучшей визуализации контуров мочевого пузыря. Производится продольный разрез в проекции дна мочевого пузыря, с рассечеинем брюшины, паравезикальной клетчатки и стенки мочевого пузыря. После визуализации устьев мочеточников производится циркулярный разрез с отступом в 1 см. от внутреннего отверстия уретры, далее производится субфасциальное выделение предстательной железы до уровня апекса с использованием аппарата Thunderbeat, отсечение семенных пузырьков. Контроль гемостаза. Простата отсекается от уретры и погружается в контейнер. На ложе простаты накладываются гемостатические швы с использованием нити V-Loc. Повторный контроль гемостаза. Под визуальным контролем устанавливается профилированный уретральный катетер Фолея 18Ch. Баллон катетера раздувается на 15 мл в ложе предстательной железы. Стенка мочевого пузыря ушивается непрерывным швом с использованием нити V-Loc. В мочевой пузырь вводится 150 мл. физиологического раствора, производится контроль герметичности пузыря. Поочередно под контролем зрения удаляются троакары. Предстательная железа эвакуируется с помощью эндоскопического контейнера. Раны послойно ушиваются. Производится обработка йодом и наложение асептической повязки.
Преимуществом способа лапароскопического радикального лечения локализованного рака предстательной железы с доступом через мочевой пузырь являются сохранение каркасного связочного аппарата предстательной железы, мочевого пузыря, уретры, с максимальным сохранением сосудисто-нервных пучков, его широкие функциональные возможности, значительное ускорение времени выполнения вмешательства за счет отсутствия необходимости в прошивании и пересечении дорзального венозного комплекса, а также необходимости в формировании анастомотической связи между мочевым пузырем и уретрой, за счет чего отмечается снижение риска формирования рубцовых изменений в области шейки мочевого пузыря. Для применения способа не являются противопоказанием избыточная масса тела, наличие сосудистых протезов подвздошных артерий и вен, многочисленные операции на органах брюшной полости в анамнезе.
Достижению технического результата способствуют, во-первых -использование трансвезикального доступа, являющегося на наш взгляд наиболее физиологичным и щадящим при вмешательствах подобного рода; во-вторых - соответствие последовательности проведения этапов и хирургических приемов сценарию, предложенному авторами.
В целом, у лиц с локализованными формами рака предстательной железы применение предлагаемого способа позволяет уменьшить вероятность и численность осложнений и рецидивов заболевания, улучшить качество жизни после радикального хирургического лечения, ускорить восстановительный период.
Пример 1. Пациент Е., 64 лет, находился на лечении в урологическом отделении стационара. Клинический диагноз: Основное заболевание: Сr предстательной железы pT1cN0M0. Сопутствующие заболевания: гипертоническая болезнь II ст., артериальная гипертензия 1 ст., риск сердечнососудистых осложнений 3. Хроническая сердечная недостаточность 0 ф.кл. МКБ: С61. Злокачественное новообразование предстательной железы
При поступлении предъявлял жалобы на вялую струю мочи, частые ночные мочеиспускания (до 2-4 раз за ночь). За медицинской помощью обратился самостоятельно.
Анамнез жизни: Наследственность не отягощена. Перенесенные заболевания: детские инфекции, простудные заболевания. Вредные привычки: нет. Операции: аппендэктомия 2014 г. Инвалидности нет. Эпидемиологический анамнез: туберкулез, венерические заболевания, гепатит отрицает. В контакте с больными инфекционными заболеваниями за последние 3 месяца не был. Гемотрансфузий не было. Аллергологический анамнез: реакций на медикаменты, пищевые продукты: отрицает.
Результаты дооперационного обследования.
Общеклинический анализ крови:

Биохимический анализ крови:

Коагулограмма:
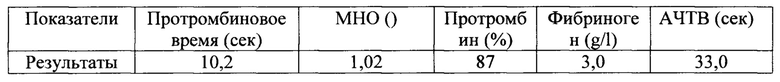
Общий анализ мочи:

Определение общего ПСА: 9,02 нг/мл.
Урофлоуметрия: средняя скорость потока 3,5 мл/с, максимальный поток 5.9 мл/с.
Электрокардиограмма: Синусовый ритм, ЧСС 68 в мин., начальные признаки ГЛЖ, синдром ранней реполяризации желудочков.
Рентгенограмма органов грудной клетки обзорная, выполненная в трех проекциях: очаговых и инфильтративных изменений не выявлено, легочный рисунок усилен за счет сосудистого компонента. Корни структурны, не расширены. Сердце не расширено, аорта не изменена. Диафрагма и синусы без особенностей. Костнодеструктивных изменений не выявлено.
УЗИ почек и мочевого пузыря: даных за нарушение уродинамики не получено.
УЗИ простаты: Объем предстательной железы - 40 см3, структура диффузно неоднородная, с очаговыми гипо и гиперэхогенными участками.
Объем остаточной мочи - 50 мл.
Осмотр терапевта: Диагноз: Осн.: Сr предстательной железы T1cNoMo.
Cоп.: ГБ II ст., АГ I ст., рССО3. ХСН 0 ф.кл.
Проведено хирургическое вмешательство: лапароскопическая радикальная чреспузырная простатэктомия.
Протокол операции, под эндотрахеальным наркозом, выполнен трансумбиликальный разрез кожи размером 2,5 см., далее выполнена минилапаротомия по Хассону, выполнена установка стандартного 10 мм. троакара, инсуфляция СO2 до 12 мм рт. ст., произведен осмотр всех отделов брюшной полости (патологические образования, свободная жидкость не выявлены). Отступив медиальнее на 2 см от передне-верхней ости гребня подвздошной кости под визуальным контролем размещены два порта - слева диаметром 10 мм, справа - 5 мм. По латеральному краю передней мышцы живота с обеих сторон на уровне пупка под визуальным контролем установлено два 5 мм троакара. После заполнения мочевого пузыря до 200 мл. произведен продольный разрез в проекции дна мочевого пузыря, с рассечеинем брюшины, паравезикальной клетчатки и стенки пузыря. После визуализации устьев мочеточников произведен циркулярный разрез отступя на 1 см. от внутреннего отверстия уретры, выполнено субфасциальное выделение предстательной железы до уровня апекса с использованием аппарата Thunderbeat, далее семенные пузырьки отсечены. Контроль гемостаза. Простата отсечена от уретры и погружена в контейнер. На ложе простаты наложено два гемостатических шва с использованием нити V-Loc. Повторный контроль гемостаза. Под визуальным контролем установлен профилированный уретральный катетер Фолея 18Ch. Баллон катетера раздут на 15 мл в ложе предстательной железы. Стенка мочевого пузыря ушита непрерывным швом с использованием нити V-Loc. В мочевой пузырь введено 150 мл. физиологического раствора, контроль герметичности. Поочередно под контролем зрения удалены троакары. Предстательная железа эвакуирована с помощью эндоскопического контейнера. Раны послойно ушивается. Раны обработаны антисептическим раствором. Асептические повязки.
Результаты послеоперационного обследования.
Общеклинический анализ крови:

Электрокардиограмма (заключение): синусовый ритм, ЧСС 80 в мин., косвенные признаки ГЛЖ.
Рентгенография легких (2 проекции): На снимках легких в сравнении с данными предоперационного рентгенологического исследования - свежие очаговые и инфильтративные изменения не выявлены, синусы свободные. Остальные данные прежние, без отрицательной динамики.
Выписан в удовлетворительном состоянии с улучшением. Рекомендовано: 1) наблюдение уролога, онколога, кардиолога, поликлиники по месту жительства; 2) контрольные анализы амбулаторно, в поликлинике по месту жительства: общеклинический анализ крови, общий анализ мочи, биохимический анализ крови амбулаторно в поликлинике по месту жительства; 3) компьютерная томография грудной клетки, брюшной полости через 3 месяца; 4) МРТ органов малого таза через 3 месяца; 4) Омник, по 1 капсуле 1 раз в сутки; 5) Клексан, 0,4 г. в сутки в течение 30 дней.
Способ лапароскопического радикального лечения локализованного рака предстательной железы с чреспузырным доступом был использован нами при лечении рака предстательной железы еще у 12 пациентов, каждому из которых осуществляли вышеописанный доступ к оперируемому органу. Никаких дополнительных инструментов или портов не использовалось. Уретровезикальный анастомоз не накладывался ни в обном из клинических случаев. Во всех случаях оперативные вмешательства были завершены без конверсии на стандартный эндовидеохирургический вариант. Средний объем кровопотери равнялся 105±53 мл, необходимость в переливании крови отсутствовала во всех случаях. Общее время вмешательств составило 75±16 минут, длительность пребывания в стационаре не превышала 5,5 дней. Катетер Фолея у всех пациентов был удален не позднее, чем через 3 дней после операции, интраоперационные осложнения отсутствовали. У всех пациентов без исключения в послеоперационном периоде эректильная функция сохранена, инконтиненция отсутствовала.
Таким образом, применение предлагаемого способа у лиц с имеющимися соответствующими показаниями позволяет получить следующие технические результаты:
1) выполнение в максимально полном объеме всех этапов радикального хирургического лечения локализованного рака предстательной железы;
2) существенное ограничение риска интраоперационного кровотечения, связанного с отсутствием необходимости в пересечении и прошивании дорзального венозного комплекса, уменьшение негативного влияния этого фактора на ход и результаты операции;
3) снижение трудоемкости, продолжительности кривой обучения, облегчение хода оперативного вмешательства, сокращение его продолжительность как минимум на 1 час;
4) сведение до минимума хирургического повреждения тканей и сосудисто-нервных элементов, предупреждение ассоциированных с этим обстоятельством интра- и постоперационных осложнений.
5) более легкое и комфортное для пациента течение послеоперационного периода.
Вывод: простатэктомия выполненная с применением чреспузырного доступа является малоинвазивным хирургическим вмешательством, позволяющим с высокой эффективностью и безопасностью проводить лечение пациентов с локализованным раком предстательной железы.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ внебрюшинной радикальной простатэктомии с использованием эпидуральной анестезии | 2019 |
|
RU2733698C1 |
| Способ монопортового лапароскопического радикального лечения локализованного рака предстательной железы | 2019 |
|
RU2707652C1 |
| Способ эндовидеохирургической трансвезикальной дивертикулэктомии | 2021 |
|
RU2770740C1 |
| Способ эндовидеохирургической аденомэктомии с использованием эпидуральной анестезии | 2019 |
|
RU2713787C1 |
| Способ оперативного лечения пациентов с локализованными формами рака предстательной железы и стриктурами уретры | 2021 |
|
RU2770733C1 |
| Способ комбинированного оперативного лечения пациентов с аденомой предстательной железы с объемом более 250 см | 2021 |
|
RU2766986C1 |
| Комбинированный способ оперативного лечения пациентов с локализованными формами рака предстательной железы и камнями средней и нижней трети мочеточника | 2022 |
|
RU2784592C1 |
| Способ симультанного лечения дивертикулов мочевого пузыря трансвезикальным методом в сочетании с тулиевой лазерной энуклеацией аденомы предстательной железы | 2022 |
|
RU2797275C1 |
| Способ симультанного лечения дивертикулов мочевого пузыря трансвезикальным методом с формированием уретероцистонеоанастомоза | 2022 |
|
RU2794864C1 |
| Способ перкутанной антеградной уретеролитотрипсии с использованием мочеточникового кожуха | 2021 |
|
RU2770669C1 |
Изобретение относится к медицине, а именно к урологии, онкологии. Осуществляют доступ в брюшную полость. Отступив медиальнее на 2 см от передне-верхней ости гребня подвздошной кости размещаются два порта - слева диаметром 10 мм, справа - 5 мм. По латеральному краю передней мышцы живота с обеих сторон на уровне пупка устанавливаются два 5 мм троакара. После заполнения мочевого пузыря до 200 мл физиологическим раствором производится продольный разрез в проекции дна мочевого пузыря. После визуализации устьев мочеточников производится циркулярный разрез с отступом в 1 см. от внутреннего отверстия уретры, далее производится субфасциальное выделение предстательной железы до уровня апекса с использованием аппарата Thunderbeat, отсечение семенных пузырьков. Далее простата отсекается от уретры и погружается в контейнер. На ложе простаты накладываются гемостатические швы с использованием нити V-Loc. Устанавливается профилированный уретральный катетер Фолея 18Ch. Баллон катетера раздувается на 15 мл в ложе предстательной железы. Стенка мочевого пузыря ушивается непрерывным швом с использованием нити V-Loc. В мочевой пузырь вводится 150 мл физиологического раствора, производится контроль герметичности. Удаляются троакары. Предстательная железа эвакуируется с помощью эндоскопического контейнера. Раны послойно ушиваются. Способ позволяет снизить риск интраоперационного кровотечения, связанного с отсутствием необходимости в пересечении и прошивании дорзального венозного комплекса, уменьшить негативное влияние этого фактора на ход и результаты операции; снизить риск хирургического повреждения тканей и сосудисто-нервных элементов, предупредить ассоциированные с этим обстоятельством интра- и постоперационные осложнения; улучшить качество жизни пациента в послеоперационном периоде. 5 табл., 1 пр.
Способ лапароскопического радикального лечения локализованного рака предстательной железы с применением чреспузырного доступа, отличающийся тем, что под эндотрахеальным наркозом выполняют укладку пациента на операционном столе, далее производят трансумбиликальный разрез размером 2,5 см, послойно осуществляют доступ в брюшную полость, в которую после установки 10 мм троакара вводят лапароскоп и осуществляют инсуфляцию СО2 до 12 мм рт. ст., производят осмотр всех отделов брюшной полости; затем, отступив медиальнее на 2 см от передне-верхней ости гребня подвздошной кости, под визуальным контролем размещают два порта - слева диаметром 10 мм, справа - 5 мм; по латеральному краю передней мышцы живота с обеих сторон на уровне пупка под визуальным контролем устанавливают два 5 мм троакара для рабочих инструментов - оператора и ассистента; после заполнения мочевого пузыря через уретральный катетер до 200 мл физиологическим раствором производят продольный разрез в проекции дна мочевого пузыря с рассечением брюшины, паравезикальной клетчатки и стенки пузыря; после визуализации устьев мочеточников производят циркулярный разрез с отступом в 1 см от внутреннего отверстия уретры, далее производят субфасциальное выделение предстательной железы до уровня апекса с использованием аппарата Thunderbeat, отсечение семенных пузырьков; осуществляют контроль гемостаза; далее отсекают простату от уретры и погружают в контейнер; на ложе простаты накладывают гемостатические швы с использованием нити V-Loc и осуществляют повторный контроль гемостаза; под визуальным контролем устанавливают профилированный уретральный катетер Фолея 18Ch, баллон катетера раздувают на 15 мл в ложе предстательной железы; далее стенку мочевого пузыря ушивают непрерывным швом с использованием нити V-Loc; далее в мочевой пузырь вводят 150 мл физиологического раствора, производят контроль герметичности; далее поочередно под контролем зрения удаляют троакары; предстательную железу эвакуируют с помощью эндоскопического контейнера; далее раны послойно ушивают, производят обработку йодом и наложение асептической повязки.
| Способ внебрюшинной радикальной простатэктомии с использованием эпидуральной анестезии | 2019 |
|
RU2733698C1 |
| СПОСОБ ПОЗАДИЛОННОЙ РАДИКАЛЬНОЙ ПРОСТАКТЭКТОМИИ ПРИ РАКЕ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2001 |
|
RU2223042C2 |
| Спринклерная головка (разбрызгиватель) | 1924 |
|
SU2195A1 |
| US 20080262477 A1 23.10.2008 | |||
| КНУТОВ А.В | |||
| Способ приготовления искусственной массы из продуктов конденсации фенолов с альдегидами | 1920 |
|
SU360A1 |
| Первые впечатления | |||
| Оригинальные исследования, 2017, т.7, 4, с.14-21 | |||
| ZHOU X | |||
| et al | |||
| Transvesical robot-assisted radical prostatectomy: initial experience | |||
Авторы
Даты
2021-09-30—Публикация
2020-12-28—Подача