Область применения изобретения
Настоящее изобретение относится по существу к инвазивной абляции с использованием электрических сигналов и, в частности, к необратимой электропорации (НЭП) сердечной ткани.
Предпосылки создания изобретения
Ранее в патентной литературе были предложены методики, в которых применяют медицинский зонд для выполнения необратимой электропорации (НЭП) ткани внутри тела. Например, в публикации заявки на патент США № 2020/0009378 описаны способ, система и устройство для электропорации. Система может включать в себя медицинское устройство со множеством электродов, размещенных на расширяемом элементе, и генератор энергии, соединенный с электродами. У генератора энергии может быть схема обработки, выполненная с возможностью избирательной подачи энергии электропорации по меньшей мере на один из электродов. Схема обработки может определять наличие аварийного состояния и, если это так, прекращать подачу энергии электропорации на один или более электродов, идентифицированных как причина аварийного состояния, и (или) предотвращать подачу энергии электропорации на один или более электродов, идентифицированных как причина аварийного состояния. Генератор энергии также может быть сконфигурирован с возможностью подачи энергии электропорации на каскады множества схем подачи энергии для стимуляции образования поврежденного участка. В одном варианте осуществления изобретения биполярные сигналы прикладывают одновременно на все пары множества электродов, а для предотвращения перегрева определенных электродов в некоторых случаях эти электроды отключены от генератора энергии.
В другом примере в публикации заявки на патент США № 2018/0214202 описаны способы, системы и устройства для повышения коэффициента использования и эффективности подачи энергии и картирования ткани. Одна система включает в себя элемент для обработки, имеющий множество электродов, и генератор энергии, выполненный с возможностью доставки импульсов электрической энергии на электроды в соответствии с различными схемами. Например, электроды могут быть расположены парами, близко друг к другу. Генератор энергии может подавать энергию картирования на каждый электрод в каждой отдельной паре для картирования ткани и может подавать энергию абляции на электроды в каждой паре так, что каждая пара обрабатывается как отдельный электрод для доставки энергии абляции, такой как биполярная абляционная энергия, между смежными парами. Одна система включает в себя по меньшей мере один вогнутый электрод, благодаря конфигурации которого осуществляется концентрация энергии и ее более глубокое проникновение в ткань. Одна система включает нейтральные электроды, расположенные между активными электродами, причем с помощью генератора энергии осуществляется избирательное соединение нейтральных электродов для изменения схемы абляции. В варианте осуществления изобретения для предотвращения перегрева электрода эффективную поверхность электрода увеличивают путем соединения нескольких электродов друг с другом. В другом варианте осуществления изобретения перегретые электроды отключают для снижения нагрева.
В публикации заявки на патент США № 2016/0113709 дано описание селективной клеточной абляции путем электропорации, применимой, например, к основной массе ткани бьющегося сердца. Параметры протокола потенциально вызывают потерю ткани без термического повреждения. Устройство и способ потенциально применимы к абляции ткани миокарда для лечения аритмий, обструктивной гипертрофии и (или) для образования естественных каркасов для восстановления ткани миокарда. В некоторых вариантах осуществления изобретения импульсы доставляются поочередно с помощью различных пар электродов. В некоторых вариантах осуществления изобретения интенсивность (импульсное напряжение, частота, количество и (или) длительность) протокола электропорации ограничена требованием избегать локализованного нагрева, приводящего к термическому повреждению. Таким образом, например, потенциалы электропорации поочередно доставляются (необязательно с разностями потенциалов, соответствующими разностям межэлектродного расстояния, чтобы поддерживать силу электрического поля электропорации) между парами электродов. В такой конфигурации каждый электрод потенциально участвует только в половине активированных пар (т. е. используется половина необходимого времени).
Изложение сущности изобретения
Один вариант осуществления настоящего изобретения, описанный в настоящем документе, представляет способ необратимой электропорации (НЭП), включающий размещение множества электродов катетера, контактирующих с тканью органа. Генерируются биполярные импульсы НЭП. Ткань подвергают абляции путем подачи биполярных импульсов НЭП на пары электродов в соответствии с порядком, в котором последовательные активации данной пары электродов перемежаются с активацией по меньшей мере одной другой пары электродов и разнесены во времени по меньшей мере на предварительно заданный промежуток.
В некоторых вариантах осуществления изобретения приложение биполярных импульсов НЭП включает в себя приложение биполярных импульсов НЭП между соседними электродами.
В некоторых вариантах осуществления изобретения приложение биполярных импульсов НЭП включает в себя приложение по меньшей мере некоторых из биполярных импульсов НЭП между несоседними электродами.
В одном варианте осуществления изобретения приложение биполярных импульсов НЭП включает в себя приложение по меньшей мере некоторых из биполярных импульсов НЭП между парами групп электродов.
В другом варианте осуществления изобретения межэлектродное расстояние между парами электродов является одинаковым.
В некоторых вариантах осуществления изобретения ткань включает в себя сердечную ткань, причем применение биполярных импульсов НЭП включает в себя гейтирование биполярных импульсов НЭП для синхронизации с рефракторными периодами сердечной ткани.
В соответствии с другим вариантом осуществления настоящего изобретения дополнительно предложена система необратимой электропорации (НЭП), включающая в себя катетер, источник энергии для абляции НЭП и процессор. Катетер состоит из множества электродов, выполненных с возможностью осуществления контакта с тканью органа. Источник энергии НЭП для абляции выполнен с возможностью генерирования биполярных импульсов НЭП. Процессор сконфигурирован с возможностью абляции ткани путем подачи биполярных импульсов НЭП на пары электродов в соответствии с порядком, в котором последовательные активации данной пары электродов перемежаются с активацией по меньшей мере одной другой пары электродов и разнесены во времени по меньшей мере на предварительно заданный промежуток времени.
В некоторых вариантах осуществления изобретения система дополнительно включает в себя узел переключения, сконфигурированный для переключения абляционного источника питания НЭП между парами электродов, а также процессор сконфигурирован с возможностью подачи биполярных НЭП импульсов в соответствии с порядком управления с помощью узла переключения.
Краткое описание графических материалов
Настоящее изобретение станет более понятным из следующего подробного описания вариантов осуществления, представленных вместе со следующими графическими материалами, причем
на Фиг. 1 представлена схематическое графическое изображение системы отслеживания положения и необратимой электропорационной абляции с использованием катетера в соответствии с примером осуществления настоящего изобретения;
На Фиг. 2 представлена схематическая графическая боковая проекция гибкой концевой секции многоэлектродного катетера с Фиг. 1 в соответствии с примером осуществления изобретения;
На Фиг. 3 представлен схематический вид спереди последовательного питания пар электродов гибкой концевой секции многоэлектродного катетера, размещенных в форме петли, в соответствии с примером осуществления изобретения; и
На Фиг. 4 представлена блок-схема, схематически иллюстрирующая способ использования пар электродов головки катетера, показанной на Фиг. 2, для последовательной абляции путем необратимой электропорационной (НЭП) абляции в соответствии с примерным вариантом осуществления изобретения.
Подробное описание вариантов осуществления
Общее описание
Необратимая электропорация (НЭП), также называемая абляцией импульсным полем (PFA - Pulsed Field Ablation), может применяться в качестве инвазивного терапевтического средства для уничтожения клеток ткани путем воздействия на них импульсами высокого напряжения. В частности, импульсы НЭП потенциально могут применяться для уничтожения клеток тканей миокарда для лечения сердечной аритмии. Разрушение клеток происходит, когда трансмембранный потенциал превышает пороговое значение, что приводит к гибели клеток и, таким образом, к развитию поражения ткани. Следовательно, особый интерес представляет применение биполярных электрических импульсов высокого напряжения (т.е. с применением пары электродов, контактирующих с тканью) для генерирования высокой напряженности электрического поля (т.е. выше определенного порога) для уничтожения клеток ткани между электродами.
В контексте настоящего описания «биполярный» импульс напряжения означает импульс напряжения, приложенный между двумя электродами катетера (в противоположность, например, однополярным импульсам, приложенным катетерным электродом относительно какого-либо общего заземляющего электрода, не размещенного на катетере).
Для осуществления абляции НЭП на относительно большом участке ткани органа, таком как окружность устья легочной вены (ЛВ), необходимо применять множество пар электродов многоэлектродного катетера. Чтобы сделать генерируемое электрическое поле как можно более равномерным на большом участке ткани, лучше всего выбрать пары электродов с перекрывающимися полями или, по меньшей мере, полями, смежными друг с другом. Однако существует элемент электрического нагрева, который возникает при генерируемых полях НЭП, и этот нагрев может повредить электроды, когда множество пар электродов постоянно применяют для доставки последовательности импульсов НЭП.
Генератор импульсов НЭП выполнен с возможностью подачи пиковой мощности в диапазоне десятков кВт. Однако достаточно интенсивные импульсы НЭП для абляции ткани также могут вызывать нежелательное влияние, имеющее потенциальную клиническую опасность. Например, импульсное напряжение 2 кВ на 200 Ω ткани (оба возможных значения) мгновенно генерирует в ткани между двумя электродами пиковый ток 10 A, т.е. 20 кВт. Это напряжение, приложенное между электродами для формирования последовательности биполярных импульсов НЭП, также может быть достаточно высоким для генерации достаточно сильного электрического нагрева, который, если быстро не рассеивается, может вызвать обугливание.
В вариантах осуществления настоящего изобретения, описанных ниже в настоящем документе, предложены способы абляции НЭП (т.е. применения импульсов НЭП) на относительно большом непрерывном участке ткани, не вызывая теплового повреждения электродов и (или) ткани вследствие перегрева электродов. В некоторых вариантах осуществления изобретения система, содержащая узел переключения, подает питание на различные пары электродов многоэлектродного катетера и обеспечивает синхронизацию пар таким образом, чтобы исключить перегрев во время применения НЭП к ткани, но с обеспечением при этом непрерывной пространственной абляции. В некоторых вариантах осуществления изобретения предлагается блок переключения (т.е., «узел переключения») с процессорным управлением. Во время приложения абляционной мощности НЭП с помощью электродов процессор может, управляя блоком переключения, переключаться между парами электродов.
Подача питания на различные пары электродов (независимо от того, расположены ли они на соседних электродах или несоседних электродах) и время, необходимое для рассеивания электрического нагрева, заданы в протоколе (т.е. с помощью алгоритма). В частности, пара электродов не используется последовательно. Например, протокол может указывать применение биполярных импульсов НЭП к парам электродов в соответствии с порядком, в котором чередуются последовательные активации данной пары электродов. Иными словами, активация по меньшей мере одной другой пары электродов должна происходить между последовательными активациями данной пары электродов. Такой протокол обеспечивает разнесение по времени любых двух активаций одной и той же пары электродов (т.е. с разрывом по времени) по меньшей мере на предварительно заданный промежуток времени. Временной интервал может находиться в диапазоне от 0,2 микросекунд до 20 мс, и, как правило, составляет 5 мс.
В еще одном варианте осуществления протокол оптимизирован для последовательной подачи питания на пары электродов (т. е. активации чередованием) по всей окружности катетера с головкой в виде петли для выполнения абляции НЭП по всей окружности просвета, такой как устье ЛВ.
В настоящем документе термин «приблизительно» в отношении любых числовых значений или диапазонов указывают на приемлемый допуск на размер, который позволяет детали или совокупности компонентов выполнять функцию, предусмотренную для них в настоящем документе. Более точно, термин «приблизительно» может означать диапазон значений ±20% от представленного значения, например фраза «приблизительно 90%» может означать диапазон значений от 71% до 99%.
В другом варианте осуществления изобретения расстояние между электродами в каждой паре является одинаковым для всех пар. Поддерживая одинаковое межэлектродное расстояние в каждой паре электродов, процессор сохраняет приложение равномерной напряженности электрического поля к повреждению до тех пор, пока импульсы одинаковы. Межэлектродное расстояние пары электродов может варьироваться от 0,5 мм до 15 мм, и, как правило, составляет 3,5 мм.
Описанный способ последовательной абляции НЭП применяется ко многим типам многоэлектродных катетеров, включая одноразовые каркасные катетеры, такие как баллонные или корзинчатые катетеры. Способ также применим к петлевым катетерам, таким как катетер Lasso™, и к разветвленным катетерам, таким как катетер PentaRay™ (оба производства компании Biosense Webster, г. Ирвайн, штат Калифорния, США). В рамках описанной методики также можно использовать катетеры с другой формой, например, с гибким кончиком, размещаемые с одномерной матрицей электродов, или плоские катетеры, размещаемые с двухмерной матрицей электродов. Сами электроды могут иметь любую форму, подходящую для биполярной абляции НЭП, например, плоскую или кольцевую форму.
Как правило, процессор запрограммирован с использованием программного обеспечения, содержащего определенный алгоритм, благодаря которому процессор может выполнять каждую из описанных выше стадий и функций, связанных с процессором.
Последовательная биполярная абляции НЭП с использованием пары электродов в соответствии с заранее заданным протоколом (например, алгоритм), описанная последовательная многоэлектродная методика абляции НЭП могут обеспечить более безопасные и эффективные способы абляции НЭП.
Описание системы
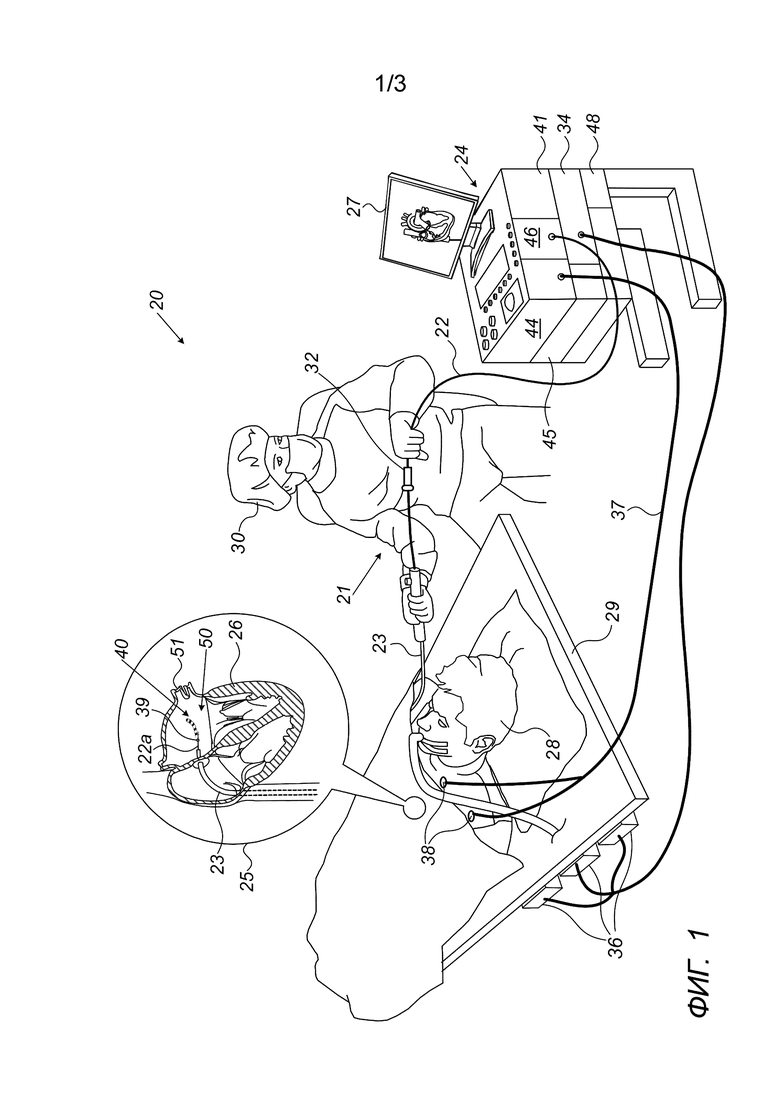
На Фиг. 1 представлено схематическое графическое изображение системы 20 абляции с отслеживанием положения и необратимой электропорацией (НЭП) на основе катетера 21 в соответствии с примером осуществления настоящего изобретения. Система 20 включает в себя гибкую концевую секцию 40, изображенную на вставке 25, которая установлена на дистальном конце 22a шафта 22 катетера 21 с гибкой концевой секцией 40, включающей в себя множество электродов 50 (подробно изображены на Фиг. 2). В варианте осуществления изобретения, описанном в настоящем документе, электроды 50 используются для абляции НЭП ткани левого предсердия сердца 26, такой как абляция НЭП устья 51 легочной вены в сердце 26.
Проксимальный конец катетера 21 соединен с пультом 24 управления, содержащим источник 45 абляционной энергии. Пульт управления 24 включает в себя блок переключения 46 (также называемый узлом переключения), который может осуществлять переключение подачи питания на любую одну или более пар электродов среди электродов 50. Последовательный протокол абляции НЭП с использованием варианта осуществления описанного способа, такого как показанный на Фиг. 3, хранится в памяти 48 пульта управления 24.
Врач 30 вводит дистальный конец 22a ствола 22 через оболочку 23 в сердце 26 пациента 28, лежащего на столе 29. Врач 30 направляет дистальный конец ствола 22 в целевое положение в сердце 26 путем манипулирования стволом 22 с помощью манипулятора 32 возле проксимального конца катетера и/или отклонения от оболочки 23. Во время введения гибкой концевой секции 22a баллон 40 удерживается в выпрямленной и ограниченной конфигурации с помощью оболочки 23. Удерживая концевую секцию 40 в выпрямленной конфигурации, оболочка 23 также обеспечивает минимизацию травмирования сосудов на пути к целевому местоположению.
Как только дистальный конец 22a ствола 22 достигает целевого местоположения, врач 30 втягивает оболочку 23 и отклоняет концевую секцию 40 и дополнительно манипулирует шафтом 22 для размещения электродов 50, расположенных над концевой секцией 40, в контакте с устьем 51 легочной вены.
Электроды 50 соединены проводами, проходящими через ствол 22 к процессору 41, управляющему распределительной коробкой 46 интерфейсных цепей 44 в пульте 24 управления.
В варианте осуществления изобретения процессор 41 принимает сигналы электрического импеданса, измеренные между электродами 50 и поверхностными электродами 38, которые показаны в примере системы и соединены проводами, проходящими по кабелю 37 к грудной клетка пациента 28. Способ отслеживания положений электродов 50 с применением измеренных импедансов реализован в различных медицинских системах, например в системе CARTO™ производства Biosense-Webster (г. Ирвайн, штат Калифорния), и подробно описан в патентах США №№ 7,756,576; 7,869,865; 7,848,787 и 8,456,182, описания которых включены в настоящий документ путем ссылки. Этот способ иногда называют способом определения местоположения выдвинутого катетера (ACL). Пульт управления 24 приводит в действие дисплей 27, на котором демонстрируется отслеживаемое положение гибкой концевой секции 40 внутри сердца 26.
Как дополнительно показано на вставке 25, дистальный конец 22a содержит магнитный датчик 39 положения, находящийся внутри дистального конца 22a непосредственно проксимально по отношению к концевой секции 40. Во время навигации дистального конца 22a в сердце 26 пульт 24 управления принимает сигналы от магнитного датчика 39 в ответ на магнитные поля от внешних генераторов 36 поля, например, с целью определения положения концевой секции 40 в сердце и необязательно представления отслеживаемого положения на дисплее 27. Генераторы 36 магнитного поля размещены в известных положениях вне тела пациента 28, например под столом 29 пациента. Пульт 24 управления также содержит схему 34 запуска, выполненную с возможностью приведения в действие генераторов 36 магнитного поля.
Данный способ определения положения с использованием внешних магнитных полей реализован в различных медицинских системах, например в системе CARTO™ производства Biosense-Webster, и подробно описан в патентах США №№ 5,391,199; 6,690,963; 6,484,118; 6,239,724; 6,618,612 и 6,332,089, в публикации патента PCT WO 96/05768 и в публикациях заявки на патент США №№ 2002/0065455 A1, 2003/0120150 A1 и 2004/0068178 A1, описания которых полностью включены в настоящий документ посредством ссылки.
Процессор 41, показанный в составе пульта управления 24, как правило, представляющий собой компьютер общего назначения с подходящим пользовательским интерфейсом и интерфейсными цепями 44 для приема сигналов от катетера 21, а также для приложения РЧ-энергии для лечения посредством катетера 21 в левом предсердии сердца 26 и для управления другими компонентами системы 20. Процессор 41, как правило, содержит программное обеспечение в памяти 48 системы 20, которая запрограммирована для выполнения функций, описанных в настоящем документе. Программное обеспечение может быть загружено на компьютер в электронном виде, например передано по сети, или в альтернативном или дополнительном варианте осуществления может быть обеспечено и/или может храниться на материальном носителе для долговременного хранения информации, таком как магнитная, оптическая или электронная память. В частности, процессор 41 выполняет специальный алгоритм, описанный в настоящем документе и показанный на Фиг. 4, благодаря которому процессор 41 выполняет стадии, дополнительно описанные ниже.
ВЫБОР ПОСЛЕДОВАТЕЛЬНЫХ ЭЛЕКТРОДОВ ВО ВРЕМЯ НЭП
На Фиг. 2 представлена схематическая графическая боковая проекция гибкой концевой секции 40 многоэлектродного катетера 21 с Фиг. 1 в соответствии с примером варианта осуществления изобретения. Гибкая концевая секция 40, которая показана прямой, но может иметь изогнутую форму или даже форму петли, включает в себя десять электродов 50, расположенных над секцией 40 и обозначенных e1-e10.
Используя узел переключения 46 системы 20, один или более импульсов НЭП могут быть доставлены от абляционного источника питания НЭП 45 системы 20 независимо на каждую пару электродов, выбранную из десяти электродов, как предварительно определено, например, с помощью алгоритма, такого как схематически проиллюстрированный на Фиг. 3. В проиллюстрированном примере осуществления изобретения пары электродов e1-e2 (50a), e4-e5 (50b) и e6-e7 (50c) выбраны для подачи питания для обеспечения доставки импульсов НЭП. Таким образом, вместо последовательной активации пар e1-e2, e2-e3, e3-e4, e4-e5, e5-e6, e6-e7, где на электроды e2, e3, e4, e5, e6 приложен электрический ток, проходящий между ними без времени для охлаждения, для этих пар может быть установлена последовательность e1-e2, e4-e5, e6-e7 и, соответственно, e2-e3, e5-e6, e3-e4 так, что перед повторным использованием для абляции НЭП для каждого электрода 50 предусмотрено время для охлаждения. Пары могут быть запитаны последовательно, или группы электродов могут запитаны вместе (например, e1-e2 и e6-e7; e4-e5 и e2-e3 e5-e6 и e3-e4). В приведенном выше описании предполагается, что на соседние электроды подается питание. Однако электроды могут быть спарены другими способами, например, e1-e4, e2-e5, e3-e6, e4-e7.
На Фиг. 3 представлен схематичный вид спереди последовательного питания пар электродов многоэлектродных гибких концевых секций 40 катетера, размещенных в форме петли 404, в соответствии с примером осуществления настоящего изобретения. На Фиг. 3 схематически представлен вид спереди вышеупомянутого катетера Lasso™, размещенного в устье ЛВ.
На Фиг. 3 каждое концентрическое кольцо 60 представляет собой продолжительность т. е. в течение рефракторного периода сердечного цикла, при котором на избранные электроды подается питание для доставки биполярных импульсов НЭП.
В одном из вариантов осуществления изобретения импульсы регулируются синхронно с биением сердца, т. е. для применения во время рефракторного периода ткани. Электрограммы желудочков и предсердий в местах расположения ткани желудочков или предсердий обычно получают с помощью электродов, контактирующих с тканью на позиционном катетере, т. е. во время электрофизиологического картирования участков ткани стенки каждой из соответствующих камер сердца. Желудочковый или предсердный рефракторный период представляет собой продолжительность паузы нейронной активности в месте расположения ткани после активации ткани любой из указанных выше камер сердца. Как правило, рефракторный период в значительной степени совпадает с частью интервала QRST сердечного цикла, показанной на желудочковой или предсердной электрограмме, полученной для данного местоположения. Рефракторный период можно намеренно вызвать на участке ткани сердца, например, с помощью электростимулирующего катетера для стимуляции ткани в местоположении ткани.
Номер продолжительности от одного до шести (т.е., номера циклов сердечных сокращений 1, 2, 3, 4, 5, 6) и соответствующая особенность пар электродов, запитанных на них во время рефракторного периода каждого цикла сокращений сердца, приведены в таблице I ниже.
Таблица I. Выбор последовательности для пар электродов
Как видно, на каждый электрод подают питание четыре раза в течение шести промежутков времени с паузой каждые два последовательных энергетических периода (т.е. паузы 61 e1, паузы 62 e2, паузы 63 e3, паузы 64 e4, паузы 65 e5, паузы 66 e6, паузы 67 е7, паузы 68 е8, паузы 69 e9, паузы 70 e10).
Темные круговые сегменты (77) представляют собой дугообразные области ткани по окружности устья, в котором проводили абляцию НЭП. Как видно, все устье подвергалось абляции НЭП дважды в течение шестипериодного (сердцебиения) НЭП.
Например, импульс, приложенный при каждом цикле сердцебиения, может быть определен по следующей таблице II:
Таблица II
Графическое изображение вида сбоку, показанное на Фиг. 3, взято для примера, при этом возможны и другие варианты осуществления изобретения. Например, в другом варианте осуществления изобретения дугообразные секции 77 длиннее, т.е. соответствуют величинам биполярного напряжения, приложенного между двумя соседними электродами (т.е. каждый третий электрод), таким как e1-e3, e2-e4, e3-e5 и т.п., которые генерируют частично перекрывающиеся электрические поля.
В другом примере осуществления изобретения в любой момент времени активируется не более одной пары электродов. В этом случае протокол из таблицы I может быть заменен на протокол, приведенный ниже в таблице III, в котором каждый цикл определяет одну пару электродов, которая активируется отдельно:
Таблица III
В еще одном иллюстративном варианте осуществления изобретения, по меньшей мере, некоторые биполярные импульсы НЭП применяются между несоседними электродами. В еще одном иллюстративном варианте осуществления изобретения и по меньшей мере некоторые биполярные импульсы НЭП применяются между группами электродов, закороченных вместе (т.е. между e1, e2, e3, закороченных друг с другом, и e6, e7, e8, закороченных друг с другом, или между e1, e2, e3, e4, закороченных друг с другом и e9), в отличие от пар отдельных электродов, например, между e2 и e3.
На Фиг. 4 представлена блок-схема, схематически иллюстрирующая способ использования пар электродов головки катетера, показанной на Фиг. 2, для последовательной абляции путем необратимой электропорационной (НЭП) абляции в соответствии с примерным вариантом осуществления настоящего изобретения. Алгоритм в соответствии с представленным примером осуществления изобретения обеспечивает процесс, который начинается со стадии 82 выбора протокола НЭП, когда врач 30 выбирает протокол НЭП, содержащий последовательную активацию пар электродов и многоэлектродного катетера, таких как пары электродов 50 катетера 21. Пример протокола представлен выше в таблицах I и II.
Затем врач 30 вводит, направляет и размещает катетер в целевом местоположении внутри просвета органа пациента, например, через устье 51, на этапе 84 размещения баллонного катетера.
Наконец, врач 30 использует систему 20, применяя протокол НЭП, для приложения импульсов НЭП в соответствии с последовательностью, указанной в протоколе (т. е. в соответствии с последовательностью, приведенной в таблице I), для непоследовательной подачи питания на каждую из пар электродов и электродов на стадии 86 последовательной абляции НЭП.
Пример блок-схемы, показанный на Фиг. 4, выбран исключительно для обеспечения концептуальной ясности. В альтернативных вариантах осуществления изобретения могут быть выполнены дополнительные стадии, такие как использование процессора 41, контролирующего измеренную температуру электродов, и при необходимости действия в соответствии со значениями измеренной температуры, такими как отключение перегретой пары электродов от дальнейшего использования в указанном протоколе.
Хотя описанные в настоящем документе варианты осуществления изобретения главным образом касаются изоляции легочной вены, способы и системы, описанные в настоящем документе, также можно использовать в других областях применения, где может потребоваться последовательная абляция, например, при денервации почек и, как правило, при удалении других органов, например, при лечении рака легкого или печени.
Таким образом, следует понимать, что описанные выше варианты осуществления изобретения приведены в качестве примера, и что настоящее изобретение не ограничено вариантами, показанными и подробно описанными выше в настоящем документе. Напротив, объем настоящего изобретения включает в себя как комбинации, так и подкомбинации различных вышеописанных признаков, а также их варианты и модификации, которые будут очевидны специалистам в данной области после ознакомления с приведенным выше описанием и которые не были описаны на предшествующем уровне техники. Документы, включенные в настоящую заявку на патент путем ссылки, следует считать неотъемлемой частью заявки, за исключением того, что, если определение терминов в этих включенных документах противоречит определениям, сделанным явным или неявным образом в настоящем описании, следует учитывать только определения настоящего описания.


Группа изобретений относится к медицине, а именно к способу и системе необратимой электропорации НЭП. Система содержит катетер с электродами, источник питания НЭП для абляции, процессор. При исполнении способа размещают электроды катетера в контакте с тканью органа. С помощью процессора задают протокол приложения импульсов НЭП. При этом протокол задает порядок подачи питания на различные пары электродов и время, необходимое для рассеивания электрического нагрева. Генерируют биполярные импульсы НЭП. Выполняют абляцию ткани путем подачи биполярных импульсов НЭП на пары электродов в соответствии с порядком. При этом обеспечивается разнесение по времени двух активаций одной и той же пары электродов на предварительно заданный промежуток времени так, что перед повторным использованием для НЭП для каждого электрода предусмотрено время для охлаждения. Осуществляется синхронизация пар электродов таким образом, чтобы исключить перегрев во время применения НЭП к ткани. При этом обеспечивается непрерывная пространственная абляция. За счет совокупности синхронизации подачи питания на пары электродов для исключения перегрева во время применения НЭП к ткани и времени, необходимого для рассеивания электрического нагрева, заданного для разнесения по времени двух активаций одной и той же пары электродов на предварительно заданный промежуток времени таким образом, чтобы перед повторным использованием для НЭП для каждого электрода было предусмотрено время для охлаждения, с обеспечением при этом непрерывной пространственной абляции, обеспечивается равномерное генерируемое электрическое поле на участке ткани, при этом исключается электрический нагрев ткани, имеющий клиническую опасность, повышается безопасность и эффективность процедуры для пациента. 2 н. и 11 з.п. ф-лы, 4 ил., 3 табл.
1. Способ необратимой электропорации (НЭП), включающий:
размещение электродов катетера в контакте с тканью органа;
задание протокола приложения импульсов НЭП, задающего порядок подачи питания на различные пары электродов и время, необходимое для рассеивания электрического нагрева;
генерирование биполярных импульсов НЭП; и
абляцию ткани путем подачи биполярных импульсов НЭП на пары электродов в соответствии с порядком, в котором обеспечивается разнесение по времени двух активаций одной и той же пары электродов по меньшей мере на предварительно заданный промежуток времени так, что перед повторным использованием для НЭП для каждого электрода предусмотрено время для охлаждения, и осуществляется синхронизация пар электродов таким образом, чтобы исключить перегрев во время применения НЭП к ткани, но с обеспечением при этом непрерывной пространственной абляции.
2. Способ по п. 1, в котором применение биполярных импульсов НЭП включает в себя применение биполярных импульсов НЭП между соседними электродами.
3. Способ по п. 1, в котором применение биполярных импульсов НЭП включает в себя применение по меньшей мере некоторых из биполярных импульсов НЭП между несоседними электродами.
4. Способ по п. 1, в котором приложение биполярных импульсов НЭП содержит применение по меньшей мере некоторых из биполярных импульсов НЭП между парами групп электродов.
5. Способ по п. 1, отличающийся тем, что межэлектродное расстояние между парами электродов одинаковое.
6. Способ по п. 1, в котором ткань представляет собой сердечную ткань, и причем применение биполярных импульсов НЭП включает в себя гейтирование биполярных импульсов НЭП для синхронизации с рефрактерными периодами сердечной ткани.
7. Система необратимой электропорации (НЭП), включающая:
катетер, имеющий электроды, выполненные с возможностью размещения в контакте с тканью органа;
источник питания НЭП для абляции, выполненный с возможностью генерирования биполярных импульсов НЭП; и
процессор, который сконфигурирован с возможностью задания протокола приложения импульсов НЭП, задающего порядок подачи питания на различные пары электродов и время, необходимое для рассеивания электрического нагрева, для абляции ткани посредством катетера путем подачи биполярных импульсов НЭП на пары электродов в соответствии с порядком, который обеспечивает разнесение по времени двух активаций одной и той же пары электродов по меньшей мере на предварительно заданный период времени так, что перед повторным использованием для НЭП для каждого электрода предусмотрено время для охлаждения, и осуществляется синхронизация пар электродов таким образом, чтобы исключить перегрев во время применения НЭП к ткани, но с обеспечением при этом непрерывной пространственной абляции.
8. Система по п. 7, в которой процессор сконфигурирован для подачи биполярных импульсов НЭП между соседними электродами.
9. Система по п. 7, в которой процессор сконфигурирован для подачи, по меньшей мере, некоторых из биполярных импульсов НЭП между несоседними электродами.
10. Система по п. 9, в которой процессор сконфигурирован с возможностью применения по меньшей мере некоторых из биполярных импульсов НЭП между парами групп электродов.
11. Система по п. 7, в которой межэлектродное расстояние между парами электродов одинаковое.
12. Система по п. 7, в которой ткань представляет собой сердечную ткань, и при этом процессор сконфигурирован с возможностью управления биполярными импульсами НЭП для синхронизации с рефрактерными периодами сердечной ткани.
13. Система по п. 7, содержащая узел переключения, сконфигурированный для переключения абляционного источника питания НЭП между парами электродов, и при этом процессор сконфигурирован с учетом возможности применения биполярных импульсов НЭП в соответствии с порядком управления узлом переключения.
| WO 2019217300 A1, 14.11.2019 | |||
| US 2018311497 A1, 01.11.2018 | |||
| EP 2942023 A2, 11.11.2015 | |||
| WO 2014025394 A1, 13.02.2014 | |||
| АБЛЯЦИОННЫЙ КАТЕТЕР И АБЛЯЦИОННОЕ УСТРОЙСТВО | 2015 |
|
RU2678229C1 |
Авторы
Даты
2022-10-18—Публикация
2021-03-26—Подача