ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ
Изобретение относится к области питания для младенцев, в частности к детским смесям для младенцев.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Человеческое грудное молоко повсеместно считается оптимальным питанием для младенцев в первые месяцы жизни. Грудное молоко вероятно играет несколько взаимодополняющих ролей в формировании микробиоты кишечника и иммунной системы ребенка. Они включают пребиотические действия, с помощью которых питательные компоненты молока селективно влияют на рост специфических видов бактерий, а также прямой перенос бактерий и иммунных компонентов. Однако в некоторых случаях грудное вскармливание является неадекватным или неудачным по медицинским показаниям или из-за решения не кормить грудью. Для таких ситуаций разработаны детские смеси для младенцев или следующие детские смеси. Коммерческие смеси для питания младенцев обычно используются в настоящее время для обеспечения дополнительного или единственного источника питания в раннем возрасте. Такие смеси включают ряд питательных веществ для удовлетворения потребностей растущего ребенка в питании и обычно включают жиры, углеводы, белки, витамины, минералы и другие питательные вещества, полезные для оптимального роста и развития ребенка. Коммерческие смеси для младенцев разработаны таким образом, чтобы настолько, насколько возможно имитировать состав и функции человеческого молока.
Кишечник новорожденного при рождении функционально незрелый и иммунологически наивный. Желудочно-кишечный тракт (ЖКТ (GI)) испытывает быстрый рост и созревание после рождения, при котором развивается адекватная пищеварительная функция, устанавливается функциональный кишечный барьер, развивается кишечная микробиота и развивается иммунная функция. Это означает, что в течение первых недель жизни все млекопитающие имеют незрелый кишечник.
Известно, что питание в раннем возрасте влияет на траекторию развития младенца, включая развитие кишечника, непосредственно путем обеспечения строительных блоков, а также путем регулирования путей передачи сигналов с помощью молекулярных механизмов (Jimenez-Chillaron JC et al., 2012, Biochemie, 94: 2242-2263). В клинических и доклинических исследованиях показано, что по сравнению с материнским молоком концепции смесей изменяют сроки и результаты созревания кишечника (Catassi C. et al., 1995, J. Pediatr. Gastroenterol. Nutr., 21 (4): 383-386).
В технике существует потребность в модуляции созревания кишечника и одновременно иммунного созревания кишечника младенцев на искусственном вскармливании для достижения/поддержания адекватных сроков и результатов, несоблюдение которых может привести к возникновению аутоиммунных или атопических заболеваний.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение направлено на удовлетворение потребности техники в детских смесях для младенцев для использования для модуляции созревания кишечника и улучшения иммунной системы кишечника у младенцев, вскармливаемых смесями, до степени созревания кишечника, более схожей со степенью созревания у младенцев, вскармливаемых грудным молоком.
Авторы изобретения сравнивали послеродовые паттерны экспрессии генов трех групп здоровых мышей, которых рандомизировали в одну группу, получающую грудное вскармливание (вскармливаемых матерью), одну группу, получающую экспериментальную детскую смесь для младенцев, включающую липидный компонент в форме больших липидных глобул, покрытых фосфолипидами (активную), и одну группу, получающую контрольную смесь для младенцев без липидного компонента в форме больших липидных глобул, покрытых фосфолипидами, но в форме стандартных маленьких липидных глобул, покрытых белком (контроль). Обе смеси вводили с 14,5-го по 18,5-й день после рождения. Контрольную и экспериментальную молочные смеси получали для достижения одинакового содержания белка в обоих препаратах с очень схожим содержанием жира и углеводов, а также калорийностью.
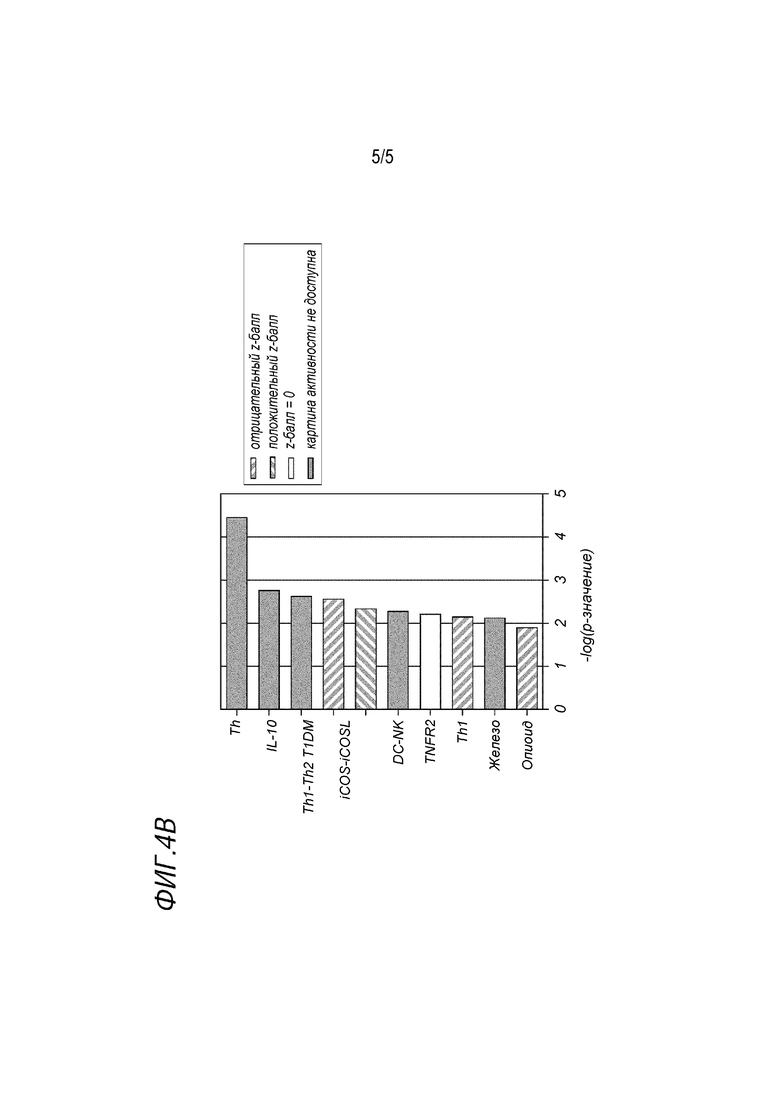
Авторы изобретения неожиданно обнаружили, анализируя экспрессию генов в тонком кишечнике в группах с различным питанием, что экспрессия генов у мышей, которых кормили экспериментальной смесью для младенцев, больше схожа с экспрессией генов у мышей, которых кормила мать, чем с экспрессией генов у мышей, которых кормили контрольной смесью. Мыши, которых кормили экспериментальной смесью для младенцев, имели экспрессию отдельных генов, вовлеченных в регуляцию барьерной функции эпителия и защиты эпителия как части иммунного ответа (включая регенерирующий островковый 3 бета (Reg3b), регенерирующий островковый 3g (Reg3g), протеинтирозинкиназу 6 (Ptk6), TRAF-взаимодействующий белок с доменом, ассоциированным с Forkhead (Tifa)), которая более схожа с экспрессией генов у мышей, вскармливаемых матерью. Кроме того, у мышей, которых кормили экспериментальной смесью для младенцев, паттерны экспрессии генов функциональных наборов генов (канонические пути), участвующих в передаче сигналов иммунитета и клеточного цикла (фигура 4B), меньше отличались от, следовательно, больше походили на группу, которую кормила мать, по сравнению с контрольной группой.
В целом такие результаты показывают, что кормление смесью для младенцев со схожим содержанием калорий и макроэлементов, но имеющей другую структуру липидных глобул, оказывает благоприятное действие на постнатальное созревание кишечника и иммунной системы кишечника в раннем возрасте, придавая такому кормлению предпочтительно большую схожесть по срокам и результатам созревания кишечника у младенцев, вскармливаемых грудным молоком, по сравнению со сроками и результатами созревания кишечника у младенцев, получавших контрольную смесь.
ОПИСАНИЕ ФИГУР
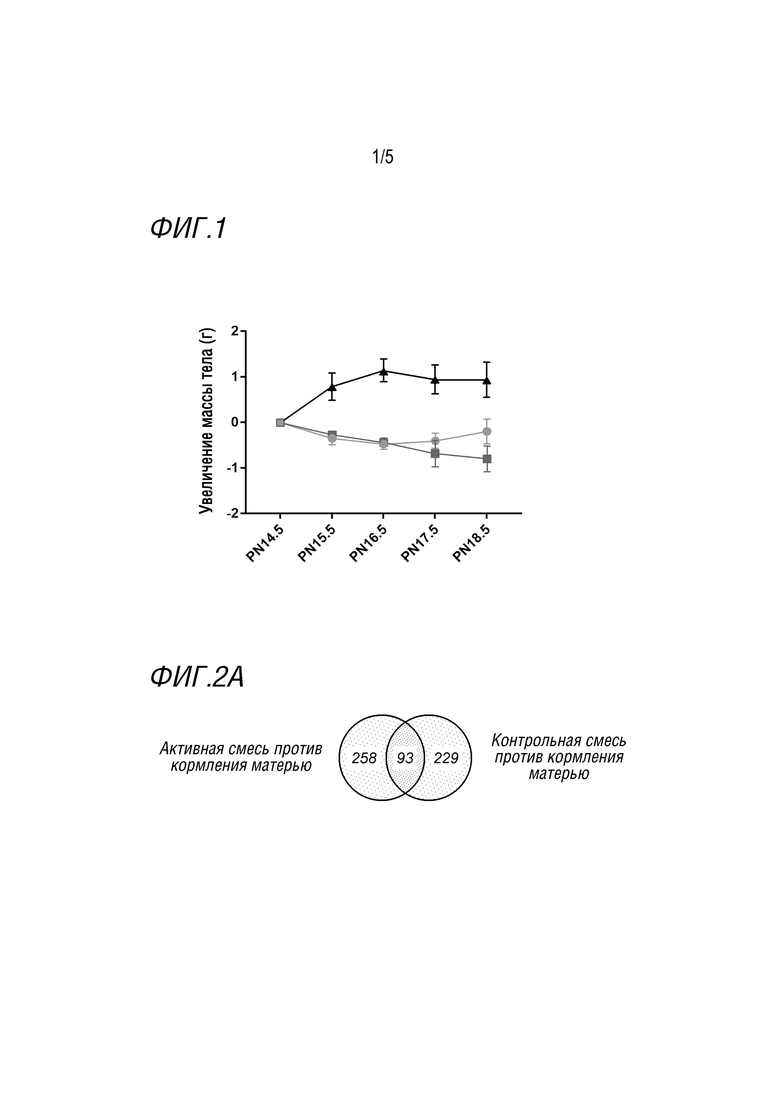
Фигура 1 показывает увеличение массы тела в граммах с 14,5-го послеродового дня и далее у мышей, которых или кормила мать (черные треугольники), или подвергали воздействию активной (светло-серые кружки) или контрольной (темно-серые квадраты) композиции. Показаны средние значения ± SEM; 2-факторный ANOVA с последующим критерием множественного сравнения Тьюки.
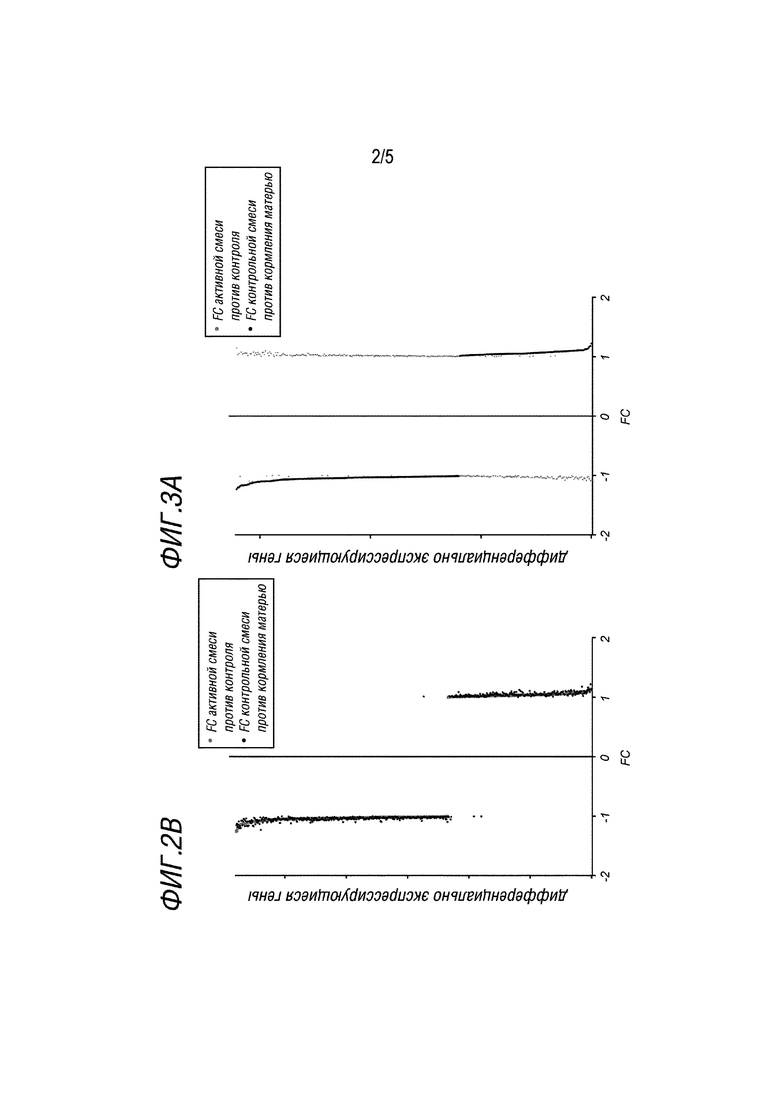
Фигура 2 показывает пересечения наборов генов и различия для различных условий питания, полученные из сравнения дифференциально экспрессирующихся генов после коррекции FDR (q≤0,05) для активной смеси против кормления матерью (n=351) и контроля против кормления матерью (n=322) с использованием диаграммы Венна.
Фигура 2B показывает график изменения сгиба (FC) дифференциально экспрессирующихся генов (q≤0,05) в группах активной против кормления матерью (светло-серый) и контроля против кормления матерью (черный) (всего n=580), указывающий на направленность и нагрузку изменений генов в различных группах сравнения.
Фигура 3А показывает график FC дифференциально экспрессирующихся генов (q≤0,05) в контроле против материнского вскармливания (n=322), указывающий на направленность и нагрузку изменений генов в сравнениях групп контроля против материнского вскармливания и активной против контроля. FC дифференциально экспрессирующихся генов активной группы против контроля показан светло-серым, черным показан FC контроля против материнского вскармливания.
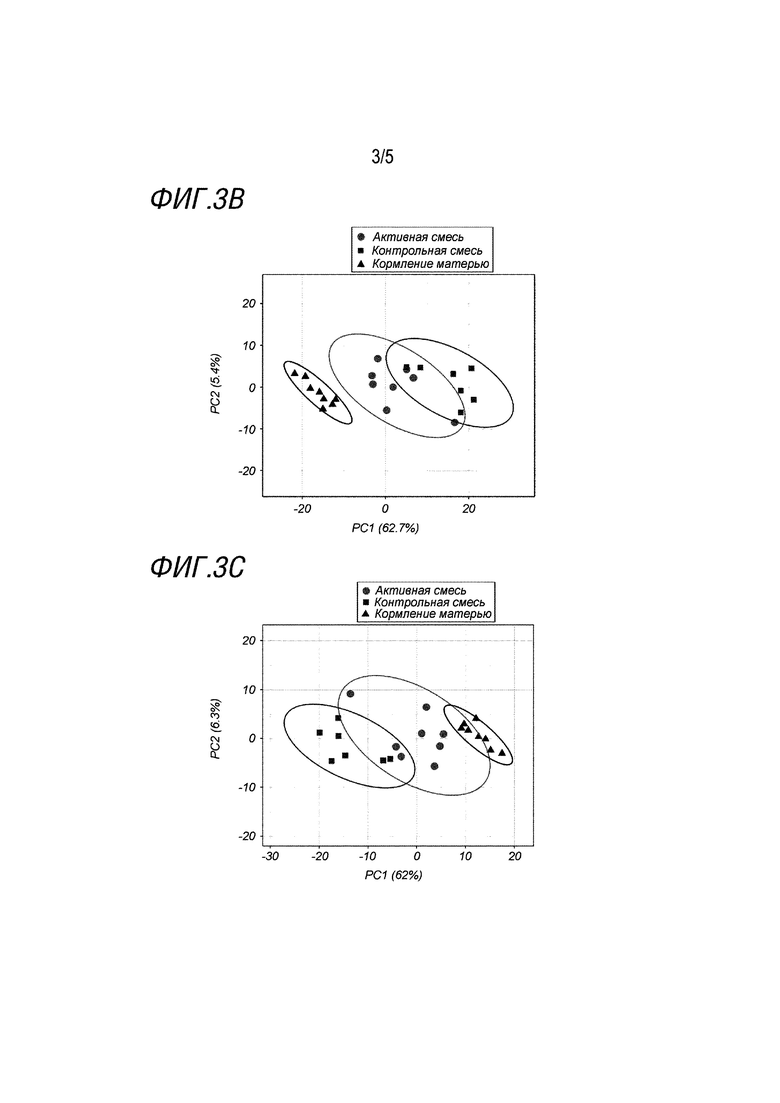
Фигура 3В показывает PCA генов, которые дифференциально экспрессируются в контроле, против кормления матерью (n=322) для всех 3 групп: кормление матерью (черные треугольники), активной смесью (светло-серые кружки), контрольной смесью (темно-серые квадраты). К строкам применяется масштабирование единичной дисперсии; SVD с вменением используют для вычисления основных компонентов. Оси X и Y показывают основной компонент 1 и основной компонент 2, которые объясняют 62,7% и 5,4% общей дисперсии соответственно. Эллипсы прогнозирования таковы, что с вероятностью 0,95 новое наблюдение из той же группы попадет внутрь эллипса. N=23 точки данных.
Фигура 3С показывает PCA генов, которые дифференциально экспрессируются в контроле, против только кормления матерью (n=229), исключая перекрытие для всех 3 групп: кормление матерью (черные треугольники), активной смесью (светло-серые круги), контрольной смесью (темно-серые квадраты). К строкам применяется масштабирование единичной дисперсии; SVD с вменением используется для вычисления основных компонентов. Оси X и Y показывают основной компонент 1 и основной компонент 2, которые объясняют 62% и 6,3% общей дисперсии соответственно. Эллипсы прогнозирования таковы, что с вероятностью 0,95 новое наблюдение из той же группы попадет внутрь эллипса. N=23 точки данных.
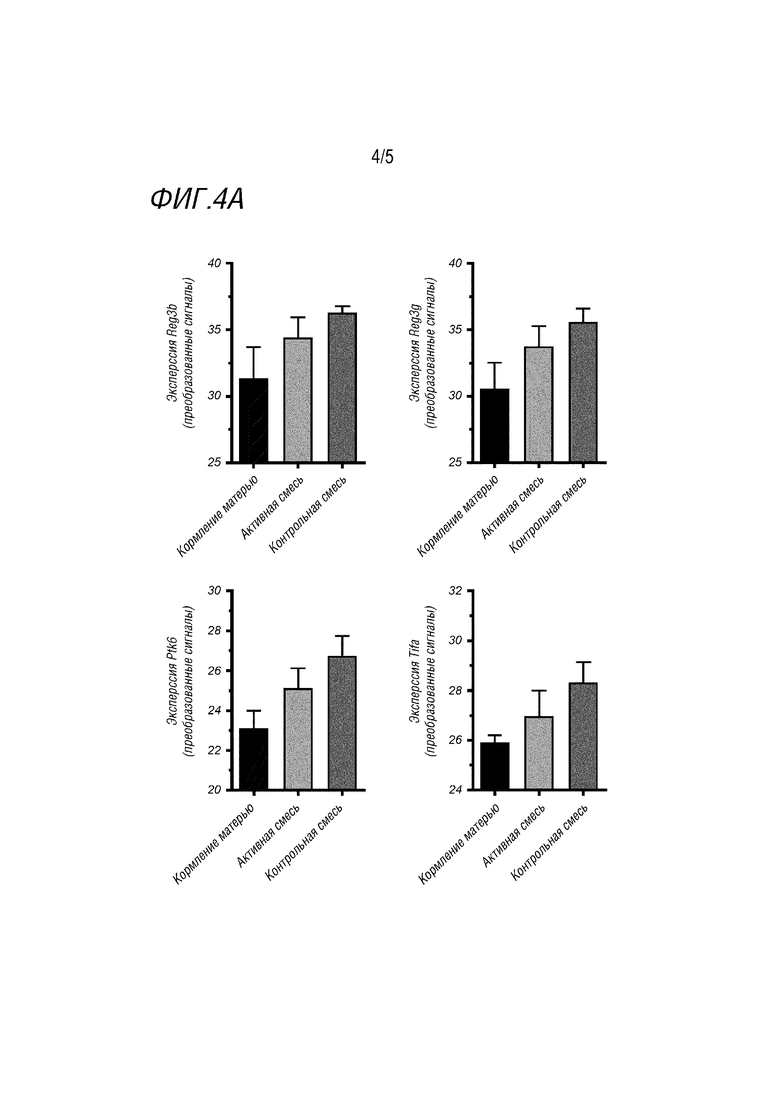
Фигура 4А показывает экспрессию отдельных генов, которые, среди прочего, участвуют в регуляции функции эпителиального барьера и эпителиальной защиты как части иммунного ответа (вкл. Reg3b, Reg3g, Ptk6, Tifa), на которые влияет контроль (темно-серые полосы) по сравнению с материнским кормлением (черные полосы), но не активная смесь (светло-серые полосы).
Фигура 4B показывает топ-10 значимо регулируемых канонических путей для контроля против кормления матерью с использованием n=322 дифференциально экспрессирующихся генов. Показаны следующие топ-10 регулируемых канонических путей для контроля против кормления матерью: Th: дифференцировка Т-хелперных клеток, IL-10: передача сигналов IL-10, Th1-Th2: путь активации Th1 и Th2, T1DM: передача сигналов сахарного диабета I типа, iCOS-iCOSL: передача сигналов iCOS-iCOSL в T-хелперных клетках, DC-NK: перекрестные помехи между дендритными клетками и природными клетками-киллерами, TNFR2: передача сигналов TNFR2, Th1: путь Th1, железо: путь передачи сигнала гомеостаза железа, опиоид: опиоидный путь передачи сигнала.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Таким образом, настоящее изобретение относится к способу модуляции сроков и результатов созревания кишечника у младенца, которые более схожи со сроками и результатами созревания кишечника, наблюдаемыми у младенцев, вскармливаемых грудным молоком, по сравнению со сроками и результатами созревания кишечника у младенца, которому вводят контрольную смесь для младенцев или следующую детскую смесь, включающую липидные глобулы со средним диаметром по объему примерно 0,5 мкм и которые не имеют покрытия из фосфолипидов,
причем указанный способ включает кормление указанного младенца питательной композицией, выбранной из смеси для младенцев и следующей детской смеси, причем смесь для младенцев или следующая детская смесь не является грудным молоком, и причем указанная смесь для младенцев или следующая детская смесь включает липид, белок и легкоусвояемые углеводы, причем липид находится в форме липидных глобул, и в которой
а) липидные глобулы имеют средний диаметр по объему по меньшей мере 1 мкм, и/или
b) по меньшей мере 45 об.% липидных глобул имеют диаметр 2-12 мкм, и
c) липид включает по меньшей мере 0,5 мас.% фосфолипидов относительно всего липида,
и липидные глобулы имеют покрытие, включающее фосфолипид.
Изобретение также можно сформулировать как относящееся к нетерапевтическому способу модуляции сроков и результатов созревания кишечника у младенца путем введения питательной композиции, выбранной из смеси для младенцев и следующей детской смеси, причем смесь для младенцев и следующая детская смесь не являются грудным молоком, и причем указанная смесь для младенцев или следующая детская смесь включает липид, белок и легкоусвояемые углеводы, причем липид находится в форме липидных глобул, и в которой
а) липидные глобулы имеют средний диаметр по объему по меньшей мере 1 мкм, и/или
b) по меньшей мере 45 об.% липидных глобул имеют диаметр 2-12 мкм, и
c) липид включает по меньшей мере 0,5 мас.% фосфолипидов относительно всего липида, и липидные глобулы имеют покрытие, включающее фосфолипид,
причем сроки и результаты созревания кишечника у младенца более схожи со сроками и результатами созревания кишечника, наблюдаемыми у младенцев, вскармливаемых грудным молоком, по сравнению со сроками и результатами созревания кишечника у младенца, которому вводят контрольную смесь для младенцев или следующую детскую смесь, включающую липидные глобулы со средним диаметром по объему примерно 0,5 мкм и которые не имеют покрытия из фосфолипидов.
Иными словами, настоящее изобретение относится к питательной композиции, выбранной из смеси для младенцев и следующей детской смеси, причем смесь для младенцев или следующая детская смесь не является грудным молоком, и причем указанная смесь для младенцев или следующая детская смесь включает углеводы, белок и липид, причем липид находится в форме липидных глобул, и в которой
а) липидные глобулы имеют средний диаметр по объему по меньшей мере 1 мкм, и/или
b) по меньшей мере 45 об.% липидных глобул имеют диаметр 2-12 мкм, и
с) липид включает по меньшей мере 0,5 мас.% фосфолипидов относительно всего липида,
и липидные глобулы имеют покрытие, включающее фосфолипид,
для применения при модуляции сроков и результатов созревания кишечника у младенца, которые больше схожи со сроками и результатами созревания кишечника, наблюдаемыми у младенцев, вскармливаемых грудным молоком, по сравнению со сроками и результатами созревания кишечника у младенца, которому вводят контрольную смесь для младенцев или следующую детскую смесь, включающую липидные глобулы со средним диаметром по объему примерно 0,5 мкм и которые не имеют покрытия из фосфолипидов.
Изобретение также можно сформулировать как относящееся к применению липидных глобул при производстве питательной композиции для использования при модуляции сроков и результатов созревания кишечника у младенца, которые более схожи со сроками и результатами созревания кишечника, наблюдаемыми у младенцев, вскармливаемых грудным молоком, по сравнению со сроками и результатами созревания кишечника у младенца, которому вводят контрольную смесь для младенцев или следующую детскую смесь, включающую липидные глобулы со средним диаметром по объему примерно 0,5 мкм и которые не имеют покрытия из фосфолипидов,
причем питательную композицию выбирают из смеси для младенцев и следующей детской смеси, причем смесь для младенцев или следующая детская смесь не является грудным молоком, и указанная смесь для младенцев или следующая детская смесь включает углеводы, белок и липид в форме липидных глобул, и в которой
а) липидные глобулы имеют средний диаметр по объему по меньшей мере 1 мкм, и/или
b) по меньшей мере 45 об.% липидных глобул имеют диаметр 2-12 мкм, и
c) липид включает по меньшей мере 0,5 мас.% фосфолипидов относительно всего липида,
и липидные глобулы имеют покрытие, включающее фосфолипид.
Термин «младенцы, вскармливаемые грудным молоком», используемый в настоящем описании, относится к младенцам, которые с рождения и по меньшей мере до 4-месячного возраста потребляют исключительно грудное молоко либо непосредственно из груди, либо из бутылочки, включающей сцеженное грудное молоко.
Термин «контрольная смесь для младенцев и/или следующая детская смесь», используемый в настоящем описании, относится к смеси для младенцев или следующей детской смеси, которые
- соответствуют требованиям законодательства (например, правилам ЕС № 609/2013 и № 2016/127) для смесей для младенцев или следующих детских смесей;
- включают липидные глобулы со средним диаметром по объему примерно 0,5 мкм; и
- указанные липидные глобулы не имеют покрытия из фосфолипидов.
В предпочтительном воплощении изобретения сроки и результаты созревания кишечника в первые 12 месяцев жизни младенца, предпочтительнее в первые 6 месяцев жизни младенца, больше схожи со сроками и результатами созревания кишечника, наблюдаемыми в тот же период жизни у младенцев, вскармливаемых грудным молоком.
В предпочтительном воплощении изобретения питательную композицию вводят младенцу, причем младенец, которому вводят питательную композицию, имеет возраст 0-12 месяцев, предпочтительно 0-6 месяцев, предпочтительнее 0-4 месяца.
В предпочтительном воплощении изобретения сроки и результаты созревания кишечника у младенца являются сроками и результатами созревания кишечника у младенца в первые 12 месяцев жизни ребенка.
В контексте настоящего изобретения младенцем предпочтительно является новорожденный младенец. Предпочтительно питательную композицию вводят или используют для доношенного ребенка. Термин «младенец» обозначает младенца, родившегося в гестационном возрасте от 37 до 42 недель. Предпочтительно питательную композицию вводят или используют для здорового младенца.
В контексте настоящего изобретения модуляция сроков и результатов созревания кишечника у младенца предпочтительно включает модуляцию сроков и результатов функции эпителиального барьера и защиты эпителия как части иммунного ответа кишечника, до более схожей с функцией эпителиального барьера и защиты эпителия как части иммунного ответа кишечника, наблюдаемой у младенцев, вскармливаемых грудным молоком.
В контексте настоящего изобретения модуляция сроков и результатов созревания кишечника предпочтительно включает модуляцию иммунного статуса и/или функции кишечника до более схожих с иммунным статусом и/или функцией кишечника, наблюдаемыми у младенцев, вскармливаемых грудным молоком. Иными словами, в одном воплощении модуляция сроков и результатов созревания кишечника является модуляцией сроков и результатов созревания иммунной системы кишечника, предпочтительно модуляцией сроков созревания иммунной системы кишечника.
В контексте настоящего изобретения модуляция сроков и результатов созревания иммунной системы кишечника предпочтительно включает индукцию статуса иммуннологической толерантности для стимулирования пищевой толерантности.
Созревание иммунной системы кишечника предпочтительно включает модуляцию экспрессии генов, участвующих в регуляции функции эпителиального барьера и эпителиальной защиты как части иммунного ответа кишечника (включая, но без ограничения, человеческие гены Reg3b, Reg3g, Ptk6, Tifa), и/или канонических путей, участвующих в передаче сигналов иммунитета кишечника, для большей схожести с младенцами, вскармливаемыми грудным молоком, по сравнению с младенцами, которых кормят контрольной (или стандартной) смесью, включающей липидные глобулы в примерно 0,5 мкм и которые не имеют покрытия из фосфолипидов.
Канонические пути, участвующие в передаче сигналов иммунной системы кишечника, включают, но без ограничения, пути, участвующие в следующих биологических функциях: дифференцировка Т-хелперных клеток (Th), передача сигналов интерлейкина-10 (IL-10), пути активации Th1 и Th2, передача сигналов лигандов iCOS-iCOS в Th-клетках, перекрестные помехи между дендритными клетками и природными клетками-киллерами, передача сигналов рецептора фактора некроза опухоли 2 (TNFR-2), путь Th1 и путь передачи сигналов гомеостаза железа. Канонические пути, участвующие в передаче иммунных сигналов в кишечнике, больше схожие с путями у младенцев, вскармливаемых грудным молоком, существенно различно регулируемыми каноническими путями. Гены, связанные с передачей иммунных сигналов в кишечнике, которые, в частности, регулируются или экспрессируются с большей схожестью с паттерном, наблюдаемым у младенцев, вскармливаемых грудным молоком, представляют собой следующие гены: рецептор костного морфогенетического белка типа 1A (BMPR1A), BRAF, кальций/кальмодулин-зависимая протеинкиназа II дельта (CAMK2D), HCK, гистондеацетилаза 9 (HDAC9), человеческий лейкоцитарный антиген A (HLA-A), HLA-DQB1, ингибитор ДНК-связывания 4 (ID4), рецептор гамма-интерферона 1 (IFNGR1), интерлейкин-18 (IL18), рецептор интерлейкина-2 2B (IL2RB), рецептор интерлейкина 4 (IL4R), митоген-активированная протеинкиназа киназа 3 (MAP2K3), ядерный фактор усилителя гена легкого полипептида каппа в ингибиторе альфа В-клеток (NFKBIA), белок тирозинфосфатаза нерецепторного типа 22 (PTPN22), матери против декапентаплегического гомолога 4 (SMAD4), сфингозинкиназа 1 (SPHK1), преобразователь сигнала и активатор транскрипции 3 (STAT3), активатор NFKB, связанный с членом семейства TRAF (TANK), TRAF-взаимодействующий белок с Forkhead-ассоциированным доменом (TIFA), член суперсемейства рецепторов TNF 1A (TNFRSF1A) и VAV1.
В контексте изобретения модуляция сроков и результатов созревания кишечника предпочтительно включает модуляцию экспрессии генов, участвующих в иммунном развитии, иммунной функции, иммунной активации и иммунной сигнализации.
Размер липидных глобул
Согласно настоящему изобретению питательная композиция включает липидные глобулы. В жидкой форме такие липидные глобулы эмульгированы в водной фазе. С другой стороны, липидные глобулы присутствуют в порошке, и порошок подходит для восстановления водой или другой водной фазой пищевого качества, предпочтительно для получения готовой к употреблению смеси.
Липидные глобулы включают сердцевину и поверхность. Сердцевина предпочтительно включает растительный жир и предпочтительно включает по меньшей мере 90 мас.% триглицеридов и предпочтительнее по существу состоит из триглицеридов. Не все растительные липиды, которые присутствуют в композиции, обязательно должны быть включены в сердцевину липидных глобул, но предпочтительно большая часть составляет, предпочтительно более 50 мас.%, предпочтительнее более 70 мас.%, еще предпочтительнее более 85 мас.%, даже еще предпочтительнее более 95 мас.%, наиболее предпочтительно более 98 мас.% растительных липидов, которые присутствуют в композиции, содержатся в сердцевине липидных глобул. В одном воплощении сердцевина липидных глобул включает по меньшей мере 40 мас.% триглицеридов растительного происхождения, предпочтительнее по меньшей мере 50 мас.%, еще предпочтительнее по меньшей мере 70 мас.% триглицеридов растительного происхождения, предпочтительнее сердцевина липидных глобул включает по меньшей мере 85 мас.%, предпочтительнее по меньшей мере 95 мас.% триглицеридов растительного происхождения.
Липидные глобулы в питательной композиции в способе или применении по настоящему изобретению имеют диаметр, взвешенный по объему, больше 1,0 мкм, предпочтительно больше 3,0 мкм, предпочтительнее 4,0 мкм или больше, предпочтительно от 1,0 до 10 мкм, предпочтительнее от 2,0 до 8,0 мкм, еще предпочтительнее от 3,0 до 8,0 мкм, наиболее предпочтительно от 4,0 мкм до 8,0 мкм. Кроме того или с другой стороны, предпочтительно распределение по размерам таково, что по меньшей мере 45 об.%, предпочтительно по меньшей мере 55 об.%, еще предпочтительнее по меньшей мере 65 об.%, еще предпочтительнее по меньшей мере 75 об.% имеют диаметр от 2 до 12 мкм. Предпочтительнее по меньшей мере 45 об.%, предпочтительно по меньшей мере 55 об.%, еще предпочтительнее по меньшей мере 65 об.%, еще предпочтительнее по меньшей мере 75 об.% имеет диаметр от 2 до 10 мкм. Даже предпочтительнее по меньшей мере 45 об.%, предпочтительно по меньшей мере 55 об.%, еще предпочтительнее по меньшей мере 65 об.%, еще предпочтительнее по меньшей мере 75 об.% имеет диаметр от 4 до 10 мкм. Предпочтительно менее 5 об.% имеет диаметр больше 12 мкм.
Процентное содержание липидных глобул основано на объеме всего липида. Типовой диаметр относится к диаметру, который является наиболее присутствующим по объему всего липида, или пиковому значению при графическом представлении, когда по оси X диаметр, а по Y объем (%).
Объем липидных глобул и их распределение по размерам можно соответствующим образом определить с использованием анализатора размера частиц, такого как Mastersizer (Malvern Instruments, Malvern, UK), например, методом, описанным в Michalski et al., 2001, Lait 81: 787-796.
Фосфолипиды
Питательная композиция, которую вводят в способе или применении согласно настоящему изобретению, включает фосфолипиды, предпочтительнее питательная композиция включает фосфолипиды, полученные от животного, по происхождению не являющегося человеком, наиболее предпочтительно питательная композиция включает фосфолипиды, полученные из молока млекопитающих, не являющихся людьми. Фосфолипиды, полученные из молока млекопитающих, не являющихся людьми, включают фосфолипиды, выделенные из липидов молока, липидов сливок, липидов сыворотки сливок, липидов подсырного масла, бета-липидов сыворотки, липидов сыворотки, липидов сыра и/или липидов пахты. Липид пахты обычно получают во время производства пахты. Липид подсырного масла или бета-липид сыворотки обычно получают во время производства безводного молочного жира из сливок или сливочного масла. Предпочтительно фосфолипиды получают из молочных сливок. Фосфолипиды предпочтительно получают из молока коров, кобыл, овец, коз, буйволов, лошадей и верблюдов, наиболее предпочтительно из коровьего молока. Наиболее предпочтительно использовать липидный экстракт, выделенный из коровьего молока. Подходящим источником фосфолипидов, полученных из молока млекопитающих, не являющихся людьми, является фракция, которую можно выделить из молока, называемая мембраной глобул молочного жира (MFGM). Поэтому в одном воплощении фосфолипиды для использования в питательной композиции в способе или применении согласно настоящему изобретению представлены в виде MFGM. Подходящими коммерчески доступными источниками липидов фосфолипидов молока являются BAEF, SM2, SM3 и SM4 в порошке от Corman, Salibra oт Glanbia и LacProdan MFGM-10 или PL20 от Arla.
Питательная композиция включает по меньшей мере 0,5 мас.% фосфолипидов относительно всего липида, предпочтительно 0,5-20 мас.% фосфолипидов относительно всего липида, предпочтительнее 0,75-10 мас.%, предпочтительнее 1-10 мас.%, еще предпочтительнее 1,5-10 мас.%, еще предпочтительнее 2-8 мас.% фосфолипидов относительно всего липида.
Липидные глобулы, которые присутствуют в питательной композиции для применения согласно настоящему изобретению, по меньшей мере частично покрыты на поверхности фосфолипидами. Под «покрытием» подразумевается, что внешний поверхностный слой липидной глобулы включает фосфолипиды, тогда как такие фосфолипиды практически отсутствуют в сердцевине липидной глобулы. Подходящим способом определения того, расположены ли фосфолипиды на поверхности липидных глобул, является лазерная сканирующая микроскопия.
Обнаружено, что присутствие фосфолипидов в качестве покрытия или наружного слоя липидной глобулы во вводимом питании благоприятно модулирует созревание кишечника, которое более схоже с созреванием у младенцев, вскармливаемых грудным молоком. Не все фосфолипиды, которые присутствуют в композиции, обязательно должны включаться в покрытие, но предпочтительно большая их часть. Предпочтительно более 30 мас.%, предпочтительнее более 50 мас.%, предпочтительнее более 70 мас.%, даже предпочтительнее более 85 мас.%, наиболее предпочтительно более 95 мас.% фосфолипидов, которые присутствуют в композиции, включаются в покрытие липидных глобул.
Согласно настоящему изобретению питательная композиция предпочтительно включает глицерофосфолипиды. Глицерофосфолипиды представляют собой класс липидов, образованных из жирных кислот, этерифицированных по гидроксильным группам у углерода-1 и углерода-2 скелетной части глицерина, и отрицательно заряженной фосфатной группы, присоединенной к углероду-3 глицерина через сложноэфирную связь, и необязательно холиновой группы (в случае фосфатидилхолина, PC), сериновой группы (в случае фосфатидилсерина, PS), этаноламинной группы (в случае фосфатидилэтаноламина, PE), инозитной группы (в случае фосфатидилинозита, PI) или глицериновой группы (в случае фосфатидилглицерина, PG), присоединенной к фосфатной группе. Лизофосфолипиды представляют собой класс фосфолипидов с одной жирной ацильной цепью. Предпочтительно композиция по настоящему изобретению содержит PC, PS, PI и/или PE, предпочтительнее по меньшей мере PC.
Предпочтительно питательная композиция включает сфингомиелин. Сфингомиелины имеют молекулу фосфорилхолина или фосфорилэтаноламина, этерифицированную по 1-гидроксигруппе керамида. Они классифицируются как фосфолипиды, а также сфинголипиды, но не классифицируются ни как глицерофосфолипиды, ни как гликосфинголипиды. Предпочтительно питательная композиция включает 0,05-10 мас.% сфингомиелина относительно всего липида, предпочтительнее 0,1-5 мас.%, еще предпочтительное 0,2-2 мас.%. Предпочтительно фосфолипиды включают по меньшей мере 2 мас.% сфингомиелина, предпочтительнее 5-40 мас.% сфингомиелина и наиболее предпочтительно 10-30 мас.% сфингомиелина относительно всех фосфолипидов.
Согласно настоящему изобретению питательная композиция предпочтительно включает холестерин. Питательная композиция предпочтительно включает по меньшей мере 0,005 мас.% холестерина относительно всего липида, предпочтительнее по меньшей мере 0,01 мас.%, предпочтительнее по меньшей мере 0,02 мас.%, предпочтительнее по меньшей мере 0,05 мас.%, даже предпочтительнее по меньшей мере 0,1 мас.%. Предпочтительно количество холестерина не превышает 10 мас.% относительно всего липида, предпочтительнее не превышает 5 мас.%, даже предпочтительнее не превышает 1 мас.% от всего липида.
Предпочтительно массовое отношение фосфолипидов к белку составляет выше 0,10, предпочтительнее выше 0,20, даже предпочтительнее выше 0,3.
Одновременное использование фосфолипидов, полученных от животного, не являющегося человеком, и триглицеридов, полученных из растительных липидов, позволяет получать липидные глобулы с архитектурой, более схожей со структурой человеческого молока, в то же время обеспечивая оптимальный профиль жирных кислот.
Способы получения липидных глобул увеличенного размера и покрытием из фосфолипидов раскрыты в WO 2010/0027258, WO 2010/0027259 и WO 2013/135738.
Смесь для младенцев и следующая детская смесь
Питательную композицию для введения в способе или применения согласно настоящему изобретению выбирают из смеси для младенцев и следующей детской смеси. Это означает, что питательная композиция по настоящему изобретению не является человеческим молоком. С другой стороны, термин «смесь» означает, что он относится к композиции, которая получена искусственно или, другими словами, является синтетической. Поэтому в одном воплощении питательную композицию выбирают из искусственной смеси для младенцев и искусственной следующей детской смеси или синтетической смеси для младенцев и синтетической следующей детской смеси. В контексте настоящего изобретения смесь для младенцев относится к питательным композициям, полученным искусственным путем, предназначенным для младенцев в возрасте от 0 до примерно 4-6 месяцев и предназначенным в качестве заменителя грудного молока. Как правило, смеси для младенцев подходят для использования в качестве единственного источника питания. Такие смеси также известны как стартовые смеси. Смеси для младенцев, начиная с 4-6 месяцев жизни и до 12 месяцев жизни, предназначены для дополнительного питания младенцев, которых начинают отнимать от груди для других продуктов. Такие смеси также известны как следующие детские смеси. На смеси для младенцев и следующие детские смеси распространяются строгие правила, например, правила ЕС № 609/2013 и № 2016/127. Такие смеси предпочтительно включают другие ингредиенты, такие как минералы, микроэлементы, витамины и другие питательные микроэлементы, как рекомендовано и известно в данной области техники.
Предпочтительно питательную композицию используют по меньшей мере в течение первых 2 месяцев жизни, предпочтительно по меньшей мере в течение первых 3 месяцев жизни младенца, предпочтительнее по меньшей мере в течение первых 4 месяцев жизни младенца. Предпочтительно питательную композицию вводят младенцу в возрасте до 12 месяцев, предпочтительно в возрасте до 6 месяцев, предпочтительнее в возрасте до 4 месяцев.
Питательная композиция предпочтительно включает 3-7 г липида/100 ккал, предпочтительно 4-6 г липида/100 ккал, предпочтительнее 4,5-5,5 г липида/100 ккал, предпочтительно 1,2-5 г белка/100 ккал, предпочтительно 1,4-4 г белка/100 ккал, предпочтительнее 1,6-3 г белка/100 ккал, предпочтительнее 1,8-2,5 г белка/100 ккал, и предпочтительно 6-18 г легкоусвояемого углевода/100 ккал, предпочтительно 8-16 г легкоусвояемого углевода/100 ккал, предпочтительнее 10-15 г легкоусвояемого углевода/100 ккал.
В одном воплощении питательная композиция находится в форме порошка, подходящего для приготовления готовой к употреблению смеси после восстановления водным раствором, предпочтительно водой. Предпочтительно питательная композиция представляет собой порошок, который восстанавливают водой.
Предпочтительно смесь для младенцев или следующая детская смесь, готовая к употреблению, имеет энергетическую плотность 60-75 ккал/100 мл, предпочтительнее 60-70 ккал/100 мл. Такая плотность обеспечивает оптимальный баланс между гидратацией и потреблением калорий.
В контексте настоящего изобретения смесь для младенцев или следующая детская смесь не является натуральным коровьим молоком или человеческим молоком. В контексте настоящего изобретения также контрольная смесь для младенцев или следующая детская смесь не является натуральным коровьим молоком или человеческим молоком.
Липид
В настоящем описании LA относится к линолевой кислоте и/или ацильной цепи (18:2, n6); ALA относится к α-линоленовой кислоте и/или ацильной цепи (18:3, n3); PUFA относится к полиненасыщенным жирным кислотам и/или ацильным цепям; MUFA относится к мононенасыщенным жирным кислотам и/или ацильным цепям; LC-PUFA относится к длинноцепным полиненасыщенным жирным кислотам и/или ацильным цепям, включающим по меньшей мере 20 атомов углерода в жирной ацильной цепи и с 2 или большим числом ненасыщенных связей; DHA относится к докозагексаеновой кислоте и/или ацильной цепи (22:6, n3); EPA относится к эйкозапентаеновой кислоте и/или ацильной цепи (20:5, n3); ARA относится к арахидоновой кислоте и/или ацильной цепи (20:4, n6); DPA относится к докозапентаеновой кислоте и/или ацильной цепи (22:5, n3). Среднецепные жирные кислоты (MCFA) относятся к жирным кислотам и/или ацильным цепям с длиной цепи 6, 8 или 10 атомов углерода.
Липид, который присутствует в питательной композиции согласно изобретению, предпочтительно включает PUFA, предпочтительнее LC-PUFA, так как LC-PUFA дополнительно улучшают картины роста и состав тела во время догоняющего роста, а также развитие мозга и сетчатки. Питательная композиция предпочтительно включает 5-35 мас.% PUFA, предпочтительнее 10-30 мас.% PUFA, наиболее предпочтительно 15-20 мас.% PUFA относительно всего липида. Также предпочтительно, чтобы питательная композиция по настоящему изобретению включала MUFA, предпочтительно 10-80 мас.% MUFA, предпочтительнее 20-70 мас.% MUFA, наиболее предпочтительно 35-55 мас.% MUFA относительно всего липида.
LA предпочтительно присутствует в количестве, достаточном для того, чтобы способствовать здоровому росту и развитию, но в насколько возможно меньшем количестве, чтобы предотвратить нежелательное развитие. Поэтому питательная композиция предпочтительно включает меньше 20 мас.% LA относительно всего липида, предпочтительно 5-16 мас.%, предпочтительнее 10-14,5 мас.%. Предпочтительно питательная композиция включает по меньшей мере 5 мас.% LA относительно всего липида. На 100 ккал питательная композиция предпочтительно включает 350-1400 мг LA. Предпочтительно ALA присутствует в количестве, достаточном для способствования здоровому росту и развитию младенца. Следовательно, композиция по настоящему изобретению предпочтительно включает по меньшей мере 1,0 мас.% ALA относительно всего липида. Предпочтительно композиция включает по меньшей мере 1,5 мас.% ALA относительно всего липида, предпочтительнее по меньшей мере 2,0 мас.%. Предпочтительно композиция включает менее 12,5 мас.% ALA, предпочтительнее менее 10,0 мас.%, наиболее предпочтительно менее 5,0 мас.%. Питательная композиция предпочтительно включает массовое соотношение LA/ALA от 2 до 20, предпочтительнее от 3 до 16, предпочтительнее от 4 до 14, предпочтительнее от 5 до 12.
Для надлежащего роста и развития композиция по настоящему изобретению предпочтительно включает по меньшей мере 3 мас.% MCFA относительно всего липида, предпочтительнее по меньшей мере 9 мас.%, даже предпочтительнее 15 мас.%. Композиция по настоящему изобретению преимущественно включает менее 50 мас.% MCFA относительно всего липида, предпочтительнее менее 40 мас.%, даже предпочтительнее менее 25 мас.%.
Согласно настоящему изобретению питательная композиция предпочтительно включает LC-PUFA, предпочтительнее n-3 LC-PUFA, так как n-3 LC-PUFA способствуют созреванию кишечника. Предпочтительнее питательная композиция включает ЕРА, DPA и/или DHA, еще предпочтительнее DHA. Так как низкая концентрация DHA, DPA и/или EPA уже эффективна, содержание n-3 LC-PUFA в питательной композиции, предпочтительнее DHA, предпочтительно не превышает 15 мас.% от общего содержания жирных кислот, предпочтительно не превышает 10 мас.%, даже предпочтительнее не превышает 5 мас.%. Предпочтительно питательная композиция включает по меньшей мере 0,15 мас.%, предпочтительно по меньшей мере 0,35 мас.%, предпочтительнее по меньшей мере 0,75 мас.% n-3 LC-PUFA, предпочтительнее DHA, от общего содержания жирных кислот. В одном воплощении композиция по настоящему изобретению включает по меньшей мере 0,15 мас.% n-3 LC-PUFA относительно всех жирных кислот, выбранных из группы, состоящей из DHA, EPA и DPA, предпочтительнее DHA.
Так как группа жирных кислот n-6, особенно арахидоновая кислота (ARA), и LA как ее предшественник, противодействует группе жирных кислот n-3, особенно DHA и EPA и ALA как их предшественнику, питательная композиция включает относительно низкие количества ARA. Содержание n-6 LC-PUFA, предпочтительнее ARA, предпочтительно не превышает 5 мас.%, предпочтительнее не превышает 2,0 мас.%, предпочтительнее не превышает 0,75 мас.%, даже предпочтительнее не превышает 0,5 мас.% от всех жирных кислот.
Предпочтительно питательная композиция включает по меньшей мере один источник растительного липида, выбранный из подсолнечного масла, рапсового масла, кокосового масла и пальмового масла. Кроме того, предпочтительно, чтобы кроме растительного липида присутствовал по меньшей мере один источник липида, выбранный из рыбьего жира (предпочтительно рыбьего жира тунца), масла одноклеточных (такого как водорослевое, микробное масло и грибковое масло), масла MCT и яичного липида. Такие источники масла подходят в качестве источников LC-PUFA. Предпочтительно в качестве источника n-3 LC-PUFA используют масло одноклеточных, включая масло водорослей и микробное масло. В предпочтительном воплощении питательная композиция включает по меньшей мере один липид, выбранный из группы, состоящей из подсолнечного масла, рапсового масла, кокосового масла, пальмового масла, масла MCT, яичного липида, соевого лецитина, подсолнечного лецитина, молочного жира, жира пахты, жира подсырного масла, рыбьего жира, жира морских млекопитающих, масла водорослей, грибкового масла и микробного масла.
Белок
Питательная композиция включает белки, предпочтительно в количествах, указанных выше. Источник белка следует выбирать таким образом, чтобы соблюсти минимальные требования к содержанию незаменимых аминокислот и обеспечить удовлетворительный рост. Следовательно, предпочтительными являются источники белка на основе белков коровьего молока, такие как сыворотка, казеин и их смеси, и белки на основе сои, картофеля или гороха. В случае использования сывороточных белков источник белка предпочтительно основан на кислой сыворотке или сладкой сыворотке, изоляте сывороточного белка или их смесях и может включать α-лактальбумин и β-лактоглобулин. Предпочтительнее источник белка основан на кислой молочной сыворотке или сладкой молочной сыворотке, из которой удален казеиногликомакропептид (CGMP). Предпочтительно композиция включает по меньшей мере 3 мас.% казеина относительно сухой массы. Предпочтительно казеин является интактным и/или негидролизованным. В случае настоящего изобретения белок включает пептиды и свободные аминокислоты.
Легкоусвояемые углеводы
Питательная композиция включает легкоусвояемые углеводы, предпочтительно в количествах, указанных выше. Предпочтительными источниками легкоусвояемых углеводов являются лактоза, глюкоза, сахароза, фруктоза, галактоза, мальтоза, крахмал и мальтодекстрин. Лактоза является основным легкоусвояемым углеводом, присутствующим в грудном молоке. Лактоза выгодно имеет низкий гликемический индекс. Питательная композиция предпочтительно включает лактозу. Питательная композиция предпочтительно включает легкоусвояемый углевод, в котором по меньшей мере 35 мас.%, предпочтительнее по меньшей мере 50 мас.%, предпочтительнее по меньшей мере 75 мас.%, даже предпочтительнее по меньшей мере 90 мас.%, наиболее предпочтительно по меньшей мере 95 мас.% легкоусвояемого углевода составляет лактоза. В пересчете на сухую массу композиция по настоящему изобретению предпочтительно включает по меньшей мере 25 мас.% лактозы, предпочтительно по меньшей мере 40 мас.%.
Неперевариваемые углеводы
В одном воплощении питательная композиция включает неперевариваемые олигосахариды. Предпочтительно питательная композиция включает неперевариваемые олигосахариды со степенью полимеризации (DP) от 2 до 250, предпочтительнее от 3 до 60.
Предпочтительно неперевариваемые олигосахариды включают фруктоолигосахариды, инулин и/или галактоолигосахариды, предпочтительнее галактоолигосахариды, наиболее предпочтительно трансгалактоолигосахариды. В предпочтительном воплощении неперевариваемые олигосахариды включают смесь трансгалактоолигосахаридов и фруктоолигосахаридов или инулина. Подходящими неперевариваемыми олигосахаридами являются, например, Vivinal®GOS (FrieslandCampina DOMO), RaftilinHP® или Raftilose® (Orafti).
Предпочтительно питательная композиция включает 80 мг - 2 г неперевариваемых олигосахаридов на 100 мл, предпочтительнее 150 мг - 1,50 г, даже предпочтительнее 300 мг - 1 г на 100 мл. В пересчете на сухую массу питательная композиция предпочтительно включает 0,25 мас.% - 20 мас.%, предпочтительнее 0,5 мас.% - 10 мас.%, даже предпочтительнее 1,5 мас.% - 7,5 мас.%.
В настоящем документе и в формуле изобретения глагол «включать» и его спряжения используются в неограничивающем смысле для обозначения того, что элементы, следующие за словом, включены, но элементы, не упомянутые конкретно, не исключены. Кроме того, ссылка на элемент с неопределенным артиклем «a» или «an» не исключает возможности того, что присутствует более одного элемента, если только контекст не требует явно наличия одного и только одного из элементов. Неопределенный артикль «а» или «ан» обычно означает «по меньшей мере один».
ПРИМЕРЫ
Пример 1. Способ получения IMF с липидными глобулами большего размера
Получают смесь для питания младенцев так, как описано в примере 1 в WO 2013/135738. В частности, смесь для младенцев получают в форме порошка, включающего на кг конечного продукта примерно 4800 ккал, примерно 247 г липида, примерно 540 г легкоусвояемых углеводов, примерно 41 г неперевариваемых олигосахаридов и примерно 97 г белка. Композицию получают с использованием порошка сыворотки от сбивания масла, обогащенной молочными фосфолипидами, смеси растительных масел (липид), порошка деминерализованной молочной сыворотки (белок), лактозы и неперевариваемых олигосахаридов. Также используют витамины, минералы, микроэлементы, известные в данной области техники.
Количество порошка сыворотки от сбивания масла таково, что в конечной композиции присутствуют 1,62 мас.% фосфолипидов относительно всех липидов. Водную фазу, включающую порошок сыворотки от сбивания масла, белок и легкоусвояемые углеводы и другие ингредиенты, за исключением липида и жирорастворимых витаминов, получают как известно в данной области техники и подвергают тепловой обработке для предотвращения бактериального загрязнения, а именно обработке при сверхвысокой температуре (UHT) как известно в данной области техники, после которой применяют стадию выпаривания. Содержание сухого вещества в водной фазе после стадии выпаривания составляет от 30 до 48 мас.%. Смесь нагревают до 50°C.
Липидную фазу получают так, как известно в технике. Смесь растительных масел также нагревают до 50°C и добавляют к водной фазе в соотношении мас./мас. от 15 до 30 путем впрыска и с помощью центробежного бустерного насоса. Общее содержание твердых веществ в смеси липидной и водной фаз составляет от 40 до 60 мас.%. Соответственно, водную и липидную фазы подают в подключенный смеситель (Ystral Z80), включающий одну насадку для смешивания. Конструкция ротора-статора подключенного смесителя имела 3 ряда зубьев. Водную и липидную фазы смешивают со скоростью насадки 20-50 м/с (приводящей к скорости сдвига от 50000 до 100000 с-1) для эмульгирования липидной фазы в водную фазу, и затем перекачивают в нагреватель насосом вытесняющего действия, мононасосом, под давлением примерно 800 кПа (8 бар) на нагреватель.
Затем смесь масла и воды подают через нагреватель концентрата в распылительную сушилку, приводимую в действие насосом, используемым после подключенного смесителя.
Эмульсию распыляют с помощью системы распыления с низким сдвигом, использующей двухжидкостную форсунку Schlick (серии 0/2-0/5), причем давление, используемое для распылительной сушки, ниже 800 кПа (8 бар), и сушат, причем температура сушильного газа на входе составляет 195°C. Размер липидных глобул в конечном порошке после восстановления водой измеряют с помощью Mastersizer 2000 (Malvern Instruments, Malvern UK).
Пример 2. Питание раннего возраста с большими липидными глобулами и молочными фосфолипидами улучшает созревание кишечника у мышей
Выполняют эксперимент на животных in vivo, в котором оценивают влияние питания раннего возраста с большими липидными глобулами, включающими покрытие, включающее фосфолипиды, на экспрессию генов в тонком кишечнике.
Детенышей мышей C57BL/6 рандомизируют в три различные группы по питанию: на 14,5-й день после рождения мыши или остаются на материнском вскармливании (n=8), или начинают получать пероральное кормление в течение 4 дней или смесь (активная, n=8), включающую большие липидные глобулы, покрытые фосфолипидом, со средним диаметром по объему примерно 4 мкм, и в которой объемный % липидных глобул со средним диаметром от 2 до 12 мкм превышает 45 об.%, или контрольную смесью (контроль, n=7), в которой жировой компонент присутствует в форме липидных глобул, покрытых белком, и липидные глобулы имеют диаметр по объему меньше примерно 0,5 мкм, и объемный % липидных глобул типа от 2 до 12 мкм составляет ниже 10 об.%.
Детеныши сами едят такое питание. Активную и контрольную смеси дают мышам в жидкой форме в чашке в клетке. Мышей взвешивают каждый день. Детеныши, вскармливаемые матерью, за период обработки набирают значительно большую массу тела, чем детеныши в активной и контрольной группах. Детеныши, которых кормят активной или контрольной смесью, не отличаются по прибавке массы тела в течение первых дней, но на PN17.5 и PN18.5 детеныши, которых кормят активной смесью, имеют существенно увеличенную прибавку массы тела по сравнению с контролем и, следовательно, демонстрируют тенденцию к росту, как у мышей, вскармливаемых матерью (фигура 1).
В возрасте 18,5 дней мышей умерщвляют, и тонкую кишку мышей собирают и хранят при -80°C до использования.
Состав смеси как активной группы, так и контрольной группы является одинаковым за исключением размера липидных глобул и покрытия на них. В состав смесей входят жир, белок, легкоусвояемые углеводы, неперевариваемый олигосахарид, витамины, микроэлементы и минералы в пропорциях, известных в данной области техники для детских смесей для человека.
Состав контроля и активной композиции приводятся в таблице 1.
Таблица 1. Контрольная и активная композиция
Выделение РНК и анализ микрочипов
Получают общую РНК с использованием мини-набора RNeasy (QIAGEN, Courtaboeuf, France) в соответствии с инструкциями изготовителя, включая дополнительную стадию обработки ДНКазой. Общий выход и качество РНК оценивают на биоанализаторе Agilent 2100 (Agilent Technologies, Massay, France). Для анализа экспрессии генов используют одноцветную цельную мышь (слайды 074809_D_F_20171030) с 60-мерными олигонуклеотидами 8×60k на микрочипах (Agilent Technologies). Маркировку, гибридизацию и детекцию кРНК проводят в соответствии с инструкциями поставщика (Agilent Technologies). Для каждого микрочипа синтезируют меченную цианином 3 кРНК из 50 нг общей РНК с низким расходом с помощью набора для мечения QuickAmp. Во все пробирки добавляют спайк-ин РНК и используют в качестве положительного контроля стадий мечения и амплификации. Меченую кРНК очищают, и затем 600 нг каждой кРНК гибридизируют и промывают, следуя инструкциям изготовителя. Микрочипы сканируют на сканере Agilent G2505C, и извлекают данные с использованием программного обеспечения Agilent Feature Extraction Software© (версия FE 10.7.3.1).
Аннотируют зонды с использованием аннотаций 074809_D_GeneList_SurePrint G3 Mouse v2 от Agilent, получая в результате 45973 аннотированных признака, включая дубликаты символов генов. Чтобы получить 1 признак на символ гена, дубликаты удаляют путем усреднения величин необработанного сигнала по среднему арифметическому по различным зондам на символ гена, получая в результате 26850 уникальных генов. Используя CLC workbench (QIAGEN Bioinformatics), выполняют контроль качества данных, и данные нормализуют и преобразовывают.
Биоинформационный анализ
Используя CLC Main Workbench, версия 8.1, квантильно нормализованные и преобразованные в log2 интенсивности сигналов уникальных генов усредняют для каждой группы, и выполняют статистический анализ с использованием одностороннего дисперсионного анализа (ANOVA) по трем группам и, при необходимости, парных t-критериев для идентификации дифференциально экспрессирующихся генов для различных групповых сравнений активная против контроля, активная против кормления матерью и контроль против кормления матерью и соответствующей значимости изменений (p-значения). Соответствующие изменения сгиба (FC) указывают, во сколько раз больше средняя величина экспрессии одной группы по сравнению с величиной другой группы. Для контроля ложноположительных результатов p-значения корректируют на частоту ложных обнаружений (FDR) с использованием метода Бенджамини и Хохберга (Benjamini and Hochberg 1995), получая в результате q-значения (p-значения с поправкой на FDR). Ожидается, что 5% исправленных FDR признаков с q-значениями ниже 0,05 являются ложноположительными. Квантильно-нормализованные и преобразованные в log2 интенсивности сигналов, FC и q-значения применяют для описательного биоинформационного анализа данных, используя инструменты диаграммы Венна для идентификации пересечений и различий наборов генов для наборов дифференциально экспрессирующихся генов различных групповых сравнений, GraphPad Prism, версия 7.03, для Windows (программное обеспечение GraphPad, La Jolla California USA) для графиков FC и ClustVis (Metsalu and Vilo 2015) для анализа основных компонентов (PCA). Используют анализ путей изобретательности (IPA, Ingenuity Systems, www.ingenuity.com) и базу данных генов NCBI (https://www.ncbi.nlm.nih.gov/gene) для соотнесения данных микрочипов с каноническими путями и биологическими функциями.
Из всех уникальных аннотированных генов из набора данных (n=26849) в общей сложности имеется 1127 генов, экспрессирующихся значимо различно (p≤0,05) между детенышами, получавшими активное питание, и детенышами, получавшими контрольное питание, и 4509 генов, экспрессирующихся значимо различно (p≤0,05) между группами, получавшими активное питание, и получавшими питание от матери, и 5417 генов, экспрессирующихся значимо различно (р≤0,05) между группами контроля и получавшими питание от матери (таблица 2). После поправки на FDR очевидно, что существует схожее количество дифференциально экспрессирующихся генов (q≤0,05) в тонком кишечнике при активном питании и питании от матери (n=351) и при контрольном питании и питании от матери (n=322). Диапазон FC, в свою очередь, показывает, насколько изменяется уровень экспрессии между двумя сравниваемыми группами, показывая в данном случае, что в целом влияние на экспрессию генов в тонком кишечнике относительно невелико.
Таблица 2. Общее представление о количестве дифференциально экспрессирующихся генов
* q-значение=p-значение после коррекции FDR
В целом данные микрочипов показывают, что экспрессия генов тонкого кишечника в группе активного питания ближе к группе, получавшей материнское питание, для наборов дифференциально экспрессирующихся генов в группах, получавших контрольное питание, по сравнению с группами, получавшими материнское питание, причем эффект можно приписать, в частности, иммунной функции и пролиферации.
Перекрытие дифференциально экспрессирующихся генов
Пересечения набора генов и различия для различных условий питания, полученные в результате сравнения дифференциально экспрессирующихся генов после коррекции FDR (q≤0,05) для активной смеси против кормления матерью (n=351) и контроля против кормления матерью (n=322), идентифицируют с помощью диаграммы Венна (фигура 2А). Диаграмма Венна иллюстрирует, что существует 93 перекрывающихся гена, отражающих значимый эффект питания смесями (как контрольной, так и активной) против грудного вскармливания.
Для того, чтобы проверить, следуют ли изменения экспрессии генов одной и той же направленности, наносят на график кратные изменения экспрессии всех дифференциально экспрессирующихся генов (q≤0,05) в тонком кишечнике для активного питания против кормления матерью и контроля против кормления матерью (фигура 2B). Большинство кумулированных дифференциально экспрессирующихся генов (n=580) показывают схожую направленность изменений в обоих сравнениях, в то время как только 6 генов имеют противоположную направленность изменения: рецептор трансферрина 2 (Trf2), заряженный белок мультивезикулярного тела 4B (Chmp4b), регуляторная субъединица протеинфосфатазы 2 B” гамма (Ppp2r3c), 9330133O14Rik и A730063M14Rik, кодирующие RIKEN, пальмитоилированный мембранный белок 7 (Mpp7) и фактор распознавания убиквитина при ER-ассоциированной деградации 1 (Ufd1).
При дальнейшем анализе эффекта активного питания в 322 генах, дифференциально экспрессирующихся у контрольных детенышей по сравнению с детенышами, вскармливаемыми матерью, обнаружено 25 генов, имеющих одинаковую направленность изменений для активного питания против контроля, и 297 генов, имеющих противоположную направленность что касается контроля против вскармливания матерью (фигура 3А). В целом это показывает, что паттерн экспрессии генов в группе активного питания ближе к материнскому для этого набора генов, что также показано на тепловой карте средних значений экспрессии в 3 различных группах для 322 генов (не показано). Анализ основных координат (PCA) на 322 генах, дифференциально экспрессирующихся при контроле и при материнском вскармливании, показывает, что 3 группы в значительной степени разделяются по основному компоненту (PC) 1, при этом материнское вскармливание и контроль кластеризуются отдельно друг от друга, и активная группа находятся между ними по отношению к группе на материнском вскармливании, визуализируя, что активная смесь влияет на экспрессию генов, которые дифференцированно экспрессируются между контрольной группой и группой, вскармливаемой матерью, в сторону экспрессии, более сходной с наблюдаемой в группе, вскармливаемой матерью (фигура 3B). PCA-анализ только n=229 генов, которые специфически дифференциально экспрессируются в контроле и только на материнском вскармливании (без перекрытия n=93 с активными и на материнском вскармливании), показывает схожее разделение и кластеризацию, причем активная группа находится даже ближе к кластеру группы на материнском вскармливании (фигура 3C). На последний вывод о том, что группа, получающая активное питание, группируется ближе к группе, получающей материнское питание, не оказывает влияния отбор генов; когда анализ PCA выполняют для n=351 гена, которые дифференциально экспрессируются в активной группе и вскармливаемой матерью, контрольная группа не группируется ближе к группе, вскармливаемой матерью (данные не приводятся).
Для того, чтобы получить представление о функциональном значении наблюдаемых паттернов экспрессии генов в различных группах, авторы сначала рассмотрели отдельные гены, которые значимо дифференциально экспрессируются в контроле по сравнению с группой материнского питания (q≤0,05), но не в активной группе по сравнению с материнским питанием (q≥0,05), и которые противоположно регулируются в активной группе против контроля, чем в контроле против материнского вскармливанияи, и ранжировали их по межквартильному размаху, представляющему вариабельность экспрессии генов в трех группах. Среди 20 лучших ранжированных генов, соответствующих таким критериям, были гены, участвующие в регуляции функции эпителиального барьера и эпителиальной защиты как части иммунного ответа, вкл. Reg3b (топ-2), Reg3g (топ-4), Ptk6 (топ-9) и Tifa (топ-20), q-значения контроля по сравнению с материнским питанием составили для Reg3b q=0,025, Reg3g q=0,017, Ptk6 q=0,007 и Tifa q=0,005 соответственно (фигура 4A).
Отдельно от отдельных генов авторы также рассматривали функциональные группы генов, так как общепризнано, что довольно небольшие эффекты для различных отдельных генов, которые указаны в одних и тех же функциональных группах, могут иметь биологическую релевантность. Для того, чтобы исследовать, в каких канонических путях и биологических функциях предполагаются n=322 дифференциально экспрессирующихся гена контроля при сравнении с генами при кормлении матерью, и как на эти пути и функции влияет кормление активной смесью, авторы изобретения выполнили анализ путей изобретательности (IPA). В IPA значимость регуляции канонического пути указывается с помощью -log(p-значения), которые вычисляют на основании числа регулируемых генов по отношению к общему числу генов, приписываемых пути - таким образом, -log(p-значение) ~1,3 относится к p-значению 0,05 - и картины активности указываются как z-баллы, если доступна адекватная информация (положительный z-балл=регулируется с повышением, отрицательный z-балл=регулируется с понижением). С помощью IPA обнаружено 43 значимо регулируемых канонических путей с -log(p-значение) >1,3, причем 10 из них в основном участвуют в иммунной передаче сигналов (дифференцировка Т-хелперных клеток, передача сигналов IL-10, путь активации Th1 и Th2, передача сигналов при сахарном диабете I типа, передача сигналов iCOS-iCOSL в Т-хелперных клетках, перекрестные помехи между дендритными клетками и природными клетками-киллерами, путь Th1) и передаче сигналов клеточного цикла и выживания (передача сигналов TNFR2, опиоидный сигнальный путь) (фигура 4B). Регулируемые пути (43) обусловлены 46 генами. Используя описания биологических процессов онтологии генов, авторы обнаружили, что 18 (Bcl2l1, Bmpr1a, Braf, Hck, Hdac9, Id4, Il18, Il2rb, Map2k3, Nfkbia, Ptpn22, Smad4, Sphk1, Stat3, Tank, Tifa, Tnfrsf1b, Vav1) из 49 генов включают один или несколько из следующих элементов: воспаление (n=6) и/или иммунитет (n=6) и/или Т-клетки (n=8) и/или цитокины (n=4) и/или NF-каппа (n=5). Визуализируя среднюю групповую экспрессию 46 генов, указанных в регулируемых путях на тепловой карте (фигура 3B), также обнаружено, что активная группа меньше отличается от группы, вскармливаемой матерью, в то время как группа, вскармливаемая матерью, и контроль действительно отличаются друг от друга. В целом данные показывают, что активная смесь обеспечивает паттерн экспрессии генов, более схожий с паттерном, который наблюдают в группе, вскармливаемой матерью, в частности, в отношении иммунной функции кишечника, что, учитывая условия исследования до отлучения от груди, подразумевает влияние на созревание кишечника и иммунитета.
| название | год | авторы | номер документа |
|---|---|---|---|
| СМЕСЬ ДЛЯ ДЕТЕЙ ПЕРВЫХ МЕСЯЦЕВ ЖИЗНИ ИЛИ СТАРШЕ | 2004 |
|
RU2346448C2 |
| ДЕТСКАЯ СМЕСЬ C МОЛОЧНЫМ ЖИРОМ ДЛЯ СТИМУЛИРОВАНИЯ ЗДОРОВОГО РОСТА | 2016 |
|
RU2728720C2 |
| МОДУЛИРОВАНИЕ ПОСТПРАНДИАЛЬНОГО ПОГЛОЩЕНИЯ ЖИРОВ | 2011 |
|
RU2552940C2 |
| ПИЩА С КРУПНЫМИ ЛИПИДНЫМИ ГЛОБУЛАМИ, ВКЛЮЧАЮЩИМИ РАСТИТЕЛЬНЫЙ ЖИР, С ПОКРЫТИЕМ ИЗ ФОСФОЛИПИДОВ МОЛОКА ДЛЯ УЛУЧШЕНИЯ ВСАСЫВАНИЯ ЖИРА | 2016 |
|
RU2706167C2 |
| ДЕТСКАЯ СМЕСЬ CО СПЕЦИАЛЬНОЙ СТРУКТУРОЙ ЛИПИДА ДЛЯ СТИМУЛИРОВАНИЯ ЗДОРОВОГО РОСТА | 2016 |
|
RU2731641C2 |
| ДЕТСКАЯ СМЕСЬ ДЛЯ УЛУЧШЕНИЯ ПИЩЕВОГО ПОВЕДЕНИЯ | 2018 |
|
RU2761114C2 |
| ДЕТСКАЯ СМЕСЬ ДЛЯ УЛУЧШЕНИЯ ПИЩЕВОГО ПОВЕДЕНИЯ | 2018 |
|
RU2761065C2 |
| ДЕТСКОЕ ПИТАНИЕ ДЛЯ УЛУЧШЕНИЯ СОСТАВА ЖИРНЫХ КИСЛОТ В МЕМБРАНАХ КЛЕТОК МОЗГА | 2011 |
|
RU2692920C2 |
| ДЕТСКОЕ ПИТАНИЕ ДЛЯ УЛУЧШЕНИЯ СОСТАВА ЖИРНЫХ КИСЛОТ В МЕМБРАНАХ КЛЕТОК МОЗГА | 2011 |
|
RU2559113C2 |
| ЭФФЕКТЫ МЕТАБОЛИЧЕСКОГО ИМПРИНТИНГА СПЕЦИАЛЬНО РАЗРАБОТАННОГО ЛИПИДНОГО КОМПОНЕНТА | 2012 |
|
RU2586930C2 |
Изобретение относится к области питания для младенцев. Нетерапевтический способ модуляции сроков и результатов созревания кишечника у младенца предусматривает введение питательной композиции, выбранной из смеси для младенцев и следующей детской смеси, включающей липид, белок и легкоусвояемые углеводы. Причем липид находится в форме липидных глобул, и липидные глобулы имеют средний диаметр по объему по меньшей мере 1 мкм, и/или по меньшей мере 45 об.% липидных глобул имеют диаметр 2-12 мкм, и липид включает по меньшей мере 0,5 мас.% фосфолипидов относительно всего липида. При этом липидные глобулы имеют покрытие, включающее фосфолипид. Изобретение позволяет модулировать сроки и результаты созревания кишечника у младенца. 12 з.п. ф-лы, 8 ил., 2 табл., 2 пр.
1. Нетерапевтический способ модуляции сроков и результатов созревания кишечника у младенца путем введения питательной композиции, выбранной из смеси для младенцев и следующей детской смеси, причем смесь для младенцев или следующая детская смесь не является грудным молоком, и причем указанная смесь для младенцев или следующая детская смесь включает липид, белок и легкоусвояемые углеводы, причем липид находится в форме липидных глобул, и
а) липидные глобулы имеют средний диаметр по объему по меньшей мере 1 мкм, и/или
b) по меньшей мере 45 об.% липидных глобул имеют диаметр 2-12 мкм, и
c) липид включает по меньшей мере 0,5 мас.% фосфолипидов относительно всего липида, и липидные глобулы имеют покрытие, включающее фосфолипид,
причем сроки и результаты созревания кишечника у младенца более схожи со сроками и результатами созревания кишечника, наблюдаемыми у младенцев, вскармливаемых грудным молоком, по сравнению со сроками и результатами созревания кишечника у младенца, которому вводят контрольную смесь для младенцев или следующую детскую смесь, включающую липидные глобулы со средним диаметром по объему примерно 0,5 мкм и которые не имеют покрытия из фосфолипидов.
2. Нетерапевтический способ по п.1, причем младенец, которому вводят питательную композицию, имеет возраст 0-12 месяцев, предпочтительно 0-6 месяцев, предпочтительнее 0-4 месяца.
3. Нетерапевтический способ по п.1 или 2, причем младенец является доношенным ребенком.
4. Нетерапевтический способ по любому из предшествующих пунктов, причем модуляция сроков и результатов созревания кишечника включает модуляцию сроков и результатов созревания иммунной системы кишечника.
5. Нетерапевтический способ по п.4, причем модуляция сроков и результатов созревания иммунной системы кишечника включает модуляцию экспрессии генов, участвующих в регуляции функции эпителиального барьера и защиты эпителия как части иммунного ответа кишечника, до более схожей с функцией у младенцев, вскармливаемых грудным молоком.
6. Нетерапевтический способ по любому из предшествующих пунктов, причем модуляция сроков и результатов созревания кишечника включает регуляцию экспрессии генов, участвующих в иммунном развитии, иммунной функции, иммунной активации и/или иммунной сигнализации.
7. Нетерапевтический способ по п.6, причем гены, участвующие в иммунном развитии, иммунной функции, иммунной активации и/или иммунной сигнализации, являются релевантными отдельными генами и/или генами в значимо дифференциально регулируемых канонических путях.
8. Нетерапевтический способ по любому из предшествующих пунктов, причем липид включает 0,5-20 мас.% фосфолипидов относительно всего липида.
9. Нетерапевтический способ по любому из предшествующих пунктов, причем смесь для младенцев или следующая детская смесь включает 0,25-20 мас.% неперевариваемых олигосахаридов относительно сухой массы смеси.
10. Нетерапевтический способ по п.9, причем неперевариваемые олигосахариды включают галактоолигосахариды и/или фруктоолигосахариды.
11. Нетерапевтический способ по любому из предшествующих пунктов, причем смесь для младенцев или следующая детская смесь представляет собой порошок, пригодный для восстановления водой для предоставления готовой к употреблению смеси.
12. Нетерапевтический способ по любому из предшествующих пунктов, причем липид включает по меньшей мере 0,15 мас.% докозагексаеновой кислоты относительно всех жирных кислот.
13. Нетерапевтический способ по любому из предшествующих пунктов, причем смесь для младенцев или следующая детская смесь включает 1,2-5 г белка/100 ккал, 3-7 г липида/100 ккал, 6-18 г легкоусвояемых углеводов/100 ккал.
| WO 2013191533 A1, 27.12.2013 | |||
| WO 2017064304 A1, 20.04.2017 | |||
| WO 2015065193 A1, 07.05.2015 | |||
| WO 2014160150 A1, 02.10.2014 | |||
| WO 2009082216 A1, 02.07.2009 | |||
| RU 2015157046 A, 06.07.2017. |
Авторы
Даты
2024-07-29—Публикация
2021-02-01—Подача