Изобретение относится к медицине, а именно хирургии и урологии, и может быть использовано для лечения пациентов с солитарными кистами почек и поликистозом почек.
Киста почки - это аномалия структуры почки, характеризующаяся образованием в почке одной или нескольких замкнутых полостей, содержащих серозную жидкость и ограниченных соединительнотканной капсулой. Распространенность заболевания в общей популяции составляет 20-50% [Bas О., Nalbant I., Sener С, Firat Н., Yesil S., Zengin К. et al. Management of Renal Cysts. JSLS. 2015; 19(1): e2014.0 0097. doi: 10.4293/JSLS.2014.00097].
Солитарная киста почки представляет собой ограниченное скопление жидкости, окруженное тонкой стенкой. Солитарные кисты могут быть «простыми» - I стадия по Bosniak, а могут быть представлены другими стадиями по этой же классификации. Образующихся в почке простых кист могут быть одна (солитарная) или несколько (множественные). Простая киста является наиболее часто встречающейся кистой почек [Karen G., Stephen W.L. Simple Renal Cyst // StatPearls Publishing LLC. - 2019. - №88. - P. 52-59].
Аутосомно-доминантный поликистоз почек является одним из наиболее распространенных наследственных заболеваний почек и встречается с частотой 1/ 1000, в то же время аутосомно-рецессивный поликистоз почек встречается значительно реже (от 1/ 10000 до 1/ 40 000 человек) [Norcia L.F., Watanabe Е.М., Hamamoto Filho Р.Т., Hasimoto C.N., Pelafsky L., de Oliveira W.K., Sassaki L.Y. Polycystic Liver Disease: Pathophysiology, Diagnosis and Treatment. Hepat Med. 2022 Sep 29; 14: 135-161. doi: 10.2147/HMER.S377530. PMID: 36200122; PMCID: РМС9528914].
Поликистоз почек является значимой медико-социальной проблемой. Выявлено, что аутосомно-доминантный поликистоз почек - одна из ведущих причин развития терминальной почечной недостаточности. Среди общего числа получающих заместительную почечную терапию доля этих пациентов доходит до 8-10% [Rudenko Т.Е., Bobkova I.N., Stavrovskaya E.V. Ter Arkh. 2019; 91(6): 116-123. Published 2019 Jun 15. doi: 10.26442/00403660.2019.06.000299].
В последние годы, с повсеместным использованием современных методов лучевой диагностики - ультразвуковых исследований, компьютерной и магнитно-резонансной томографии, отмечается увеличение количества диагностированных кист и поликистоза почек. Применение МРТ с использованием гадолиниевого контрастного препарата позволяет повысить разрешение изображения и улучшить характеристику кист почек по сравнению с компьютерной томографией [Prasad S.R., Dalrymple N.C., Surabhi V.R. Cross-sectional imaging evaluation of renal masses. Radio Clin. 2008;46:95-111]. Увеличение частоты использования возможностей визуализирующих методов диагностики является достоверным инструментом для обнаружения кист и поликистоза почек у населения. В настоящее время используется классификация почечных кист по Bosniak, которая определяет гистопатологические особенности строения кист.
Показатель заболеваемости в различных возрастных группах в популяции колеблется от 5% до 40%, но выявляемость простых кист в возрасте от рождения до 18 лет составляет всего 0,2%. У 50% пациентов в возрасте от 50 лет и старше, при проведении аутопсий, обнаруживаются кисты почек [Ravine D., Gibson R.N., Donlan J., Sheffield L.J. An ultrasound renal cyst prevalence survey: specificity data for inherited renal cystic diseases // Am J Kidney Dis. - 1993. - №22. - P. 803-807].
Развитие ультразвуковых методов исследования способствовало как ранней диагностике этого заболевания, так и развитию новых методов лечения. Пункция кисты почки под контролем ультразвукового наведения -малоинвазивная операция, выполняемая в большинстве урологических отделений. В целом хирургическое лечение солитарных кист и поликистоза почек на сегодня включает в себя следующие возможные варианты [Мао X., Xu G., Wu Н., Xiao J. Ureteroscopic management of asymptomatic and symptomatic simple parapelvic renal cysts // BMC Urol. - 2015. - №6. - P. 15-48]:
- традиционная операция (открытый доступ) - в настоящее время применяется редко;
- пункция кисты с аспирацией содержимого + склеротерапия (PAIR, с дренированием или без);
- гибкая уретероскопия (лечение парапельвикальных кист почек);
- лапароскопическое или ретроперитонеальное иссечение стенок кисты с различными модификациями (фенестрация, марсупиализация).
- пересадка почек.
Накопление опыта, улучшение технических характеристик аппаратуры и техники выполнения операций позволили уменьшить количество осложнений и рецидивов, сократить время операции. В случае успешного лечения качество жизни больного улучшается в связи с минимизацией операционной травмы и уменьшением количества осложнений.
Из существующего уровня техники известен способ лечения больших, гигантских и многокамерных кист почек, включающий формирование чрескожного пункционного канала, расширение его с помощью бужей, введение через него в полость кисты нефроскопа, эвакуацию ее содержимого с последующей установкой дренажной трубки, отличающийся тем, что после эвакуации содержимого кисты нефроскоп выводят в забрюшинное пространство, в область спавшейся кисты вводят углекислый газ до 14-16 мм.рт.ст., создавая таким образом "рабочее пространство", в которое через разрез по средней аксиллярной линии вводят троакар для манипуляторов, после чего производят полную мобилизацию и иссечение стенок кисты с использованием электрокоагулятора, отступя 0,5 см от паренхимы почки, (патент РФ№2296527, Публикация: 2007.04.10).
Недостатками данного технического решения являются использование карбоксиретроперитонеума; необходимость наружного дренирования; расширение чрескожного пункционного канала с помощью бужей вслепую, что приводит к увеличению риска кровотечения, остановка которого через пункционный канал может вызвать значительные технические сложности. Способ также ограничен в применении при поликистозной болезни почек. Отдельно нужно отметить, что контроль процедуры выполняется с помощью электронно-оптического преобразователя, что увеличивает лучевую нагрузку на больного и операционную бригаду.
Известен способ однотроакарной ретроперитонеоскопической фенестрации кист почек у детей, включающий фенестрацию кисты почки в наиболее тонком месте, удаление содержимого и обработку внутренней выстилки кисты радиоволновым методом в режиме коагуляции, отличающийся тем, что разрез кожи для установки порта длиной 7-8 мм проводят по средней подмышечной линии между XI и XII ребром отступя 0,5-1 см в обе стороны от условной линии, соединяющей ребра, после обработки полость кисты дренируют катетером с боковыми отверстиями, швы не накладывают (патент РФ№2578186, Публикация: 2016.03.20).
Его недостатки - необходимость применения эндотрахеального наркоза, использование карбоксиретроперитонеума, необходимость наружного дренирования, а также ограничение технической мобильности оператора при использовании однопортовой техники, что может представлять технические сложности при наличии поликистозного поражения почек.
Известен способ чрескожного пункционного лечения больших, гигантских и многокамерных кист почек в жидкой среде из одного доступа, включающий чрескожную пункцию паранефральной клетчатки, выполняемую непосредственно на капсулу кисты под ультразвуковым контролем, отличающийся следующей последовательностью действий: сворачивание дистального кончика проведенной основной струны-проводника в непосредственной близости к стенке кисты, расширение пункционного хода с помощью пластикового бужа диаметром не более 10 Шр. до свернутой части дистального кончика, удаление пластикового бужа, установку двойного металлического бужа, удаление внутренней части двойного металлического бужа, установку страховой струны по просвету наружной части двойного металлического бужа аналогично основной струне, удаление наружной части двойного металлического бужа, бужирование пункционного хода металлическим дилататором тубуса нефроскопа по основной струне, установку по металлическому дилататору металлического тубуса 16,5 Шр., не имеющего замка, удаление металлического дилататора тубуса мини-нефроскопа и основной струны-проводника, осуществление эндоскопической ревизии дистальной части пункционного хода, дном которого является фасция Геррота, вскрытие эндоскопическими ножницами фасции Геррота и капсулы почки, механическое выделение при помощи мини-нефроскопа и эндоскопических щипцов, а также ирригационной жидкости купола кисты почки, рассечение и иссечение с помощью лазера и эндоскопических ножниц стенки кисты, лазерную коагуляцию края стенки кисты с кровоточащими сосудами, установку паранефрально страхового силиконового дренажа 10-12 Шр., удаление тубуса нефроскопа и страховой струны-проводника, фиксацию дренажа швом к коже (патент №2725554, Публикация: 2020.07.02).
Бесспорные преимущества в виде отсутствия использования карбоксиретроперитонеума, рентгеновского излучения, эндотрахеального наркоза выделяют данный способ по сравнению двумя предыдущими. Однако его недостатки аналогичны предыдущим двум способам -необходимость наружного дренирования и ограничение технической мобильности оператора. При поликистозе почек иссечение стенок множественных кист через одиночный доступ представляется технически крайне сложным, что может привести к уменьшению радикальности вмешательства и последующему рецидивированию.
Наиболее близким к заявленному техническому решению является методика чрескожной пункции, аспирации и последующей абляции стенок кисты с помощью повреждающего химического агента (PAIR), которая нашла широкое применение в хирургическом лечении кист различных органов (печень, почка, щитовидная железа). При адекватной деэпителизации происходит превращение истинной кисты в ложную, что ведет к постепенному рубцеванию ее полости. В качестве агентов применялись такие, как этиловый спирт, гипертонический солевой раствор, тетрациклин, уксусная кислота, доксициклин, верографин [Bean W.J. Renal cysts: treatment with alcohol. Radiology. 1981; 138(2): 329-331. doi:10.1148/radiology.l38.2.7455112, Bean W.J. Hepatic cysts: treatment with alcohol / W.J. Bean, B.A. Rodan // AJR Am. J. Roentgenol. - 1985. - Vol.144. - P. 237-241, https://www.ncbi.nlm.nih.gov/pubmed/9311243]. Повреждающее действие на поверхностный слой эпителия у данных веществ основано на разрушении клеточной мембраны химическим действием, дегидратации клеток и денатурации белка, что в конечном итоге приводит к некрозу клеток [Biochemical and cytologic analysis of cystic contents in benign non-parasitic symptomatic hepatic cysts before and after ethanol sclerotherapy / T.B. Larssen, J. Rorvik, A. Horn [et al.] // Acta Radiol. - 2004. - Vol.45, N 5. - P. 504-509]. Данный способ принят нами за прототип.
Недостатками данного технического решения являются ряд обусловленных техническими особенностями ограничений. Во-первых, токсическое влияние склерозанта на окружающие кисту здоровые гепатоциты из-за всасывания, особенно при его длительной экспозиции в полости кисты. В литературных данных зафиксирован случай летального исхода вследствие интоксикации уксусной кислотой [Kim S.R., Lee D.S., Park I.Y. Managements of simple liver cysts: ablation therapy versus cyst unroofing. Korean J Hepatobiliary Pancreat Surg. 2012; 16(4): 134-137. doi:10.14701/kjhbps.2012.16.4.134].
Во-вторых, ограничением метода выступает техническая невозможность контакта склерозанта со всеми клетками эпителиальной выстилки кисты вследствие топографо-анатомических особенностей либо наличия перегородок в просвете, что приводит к продолжающейся секреции и рецидивированию. Указанные причины могут обусловливать невозможность выполнения максимально полной аспирации содержимого кисты, а также невозможность попадания склерозанта в каждую камеру кисты [Kim P.N., Lee Y., Won H.J., Shin Y.M. Radiofrequency ablation of hepatic cysts: evaluation of therapeutic effi cacy. J Vase Interv Radiol 2014 Jan; 25(1): 92-6. doi: 10.1016/j.jvir.2013.09.020].
В-третьих, существенным недостатком PAIR считается техническая невозможность полноценной ревизии полости кисты, поэтому наряду с цитологическим исследованием аспирата при любом сомнении в природе кистозного образования следует выполнить чрескожную биопсию.
Кроме того, методика PAIR, как правило, может потребовать выполнения нескольких сеансов скрерозирования (6±3), а также наружного дренирования кистозной полости, особенно при осложненных крупных и гигантских кистах. Установлено, что прямо пропорционально частоте пункционных сеансов возникают и осложнения (кровотечение, инфицирование) [Третьяк С.И. Хирургическое лечение непаразитарных кист печени / С.И. Третьяк, В.И. Дружинин // Военная медицина. - 2007. - №1. - С.65-69].
Указанные недостатки устраняются в заявляемом техническом решении.
Задачей, на решение которой направлено заявляемое изобретение является разработка способа лечения солитарных кист и поликистоза почек, позволяющего предупредить геморрагические осложнения и рецидивы после пункционного лечения.
Данная задача решается тем, что метод включает чрескожную пункцию полости, аспирацию содержимого кисты и последующую абляцию стенок кисты при этом, после пункции полости и аспирации содержимого кисты под УЗ-наведением, обработку полости кисты осуществляют с использованием радиочастотной абляции, без стандартного водоохлаждения рабочего электрода в ручном режиме, с прогреванием эпителиальной выстилки полости кисты от 60°С до 69°С в течение 5-10 мин, при этом оставляют пункционную иглу в полости кисты на всей продолжительности сеанса радиочастотной абляции, после этого генератор переводят в режим средней мощности и извлекают электрод постепенно с длиной шага 1 см.
Техническим результатом, обеспечиваемым приведенной совокупностью признаков, является снижение осложнений и рецидивов.
Методика чрескожной радиочастотной абляции (РЧА) технически аналогична PAIR, но в качестве повреждающего действия использует электромагнитную волну с частотой около 500 кГц. Под ее действием ионы ткани совершают колебательные движения, передавая свою кинетическую энергию ближайшим атомам, что приводит к увеличению температуры ткани. Радиочастотная абляция получила широкое применение в терапии опухолей из-за минимальной инвазивности и возможности выполнения дозированного эффекта. РЧА оказывает некротизирующее воздействие на опухолевые клетки посредством тепловой энергии, генерируемой высокочастототным электрическим полем. Температура в центре воздействия может достигать 80-110°С и способна приводить к образованию зоны коагуляционного некроза диаметром до 5 см в зависимости от количества доставленной в ткань энергии. Этот метод в основном используется для лечения опухолей печени, легких, костей и почек [Qi, X., Shao, Н., Zhang, J. et al. Radiopharmaceutical study on Iodine-131 -labelled hypericin in a canine model of hepatic RFA-induced coagulative necrosis. Radiol med (2015) 120: 213. https://doi.Org/10.1007/sll547-014-0433-9https://doi. org/10.1007/s11547-014-0433-9].
При выполнении РЧА опухоли первостепенной задачей является максимально радикальная некротизация опухолевых клеток. «Идеальной» - полной РЧА - подразумевается деструкция, представленная зоной коагуляционного некроза, перекрывающей опухоль «с захватом» прилежащей печеночной паренхимы до 8 - 10 мм. [Жаворонкова О.И. Вклад интервенционной сонографии в развитие органосохраняющих технологий института хирургии им. А.В. Вишневского при лечении пациентов с очаговыми поражениями печени и селезенки / О.И. Жаворонкова, А.В Гаврилин, Д.А. Ионкин // Новости хирургии. - 2011. - Т. 19, №1. - С. 94-102].
Распространение тепла в солидной ткани подробно изучено отечественными авторами [Долгушин Б.И., Косырев В.Ю. Радиочастотная термоаблация опухолей. - М.: «Практическая медицина», 2015. - С. 44-45]. В солидной ткани опухоли теплопередача прекращается при высушивании и обугливании прилежащей к электроду ткани, делая дальнейшее распространение термического повреждения невозможным. Таким образом, возникает опасность неполной деструкции опухоли и последующего рецидивирования.
С целью предотвращения указанного эффекта при выполнении сеанса РЧА используется водоохлаждаемый электрод, активный кончик которого постоянно охлаждается водой, поступающей из циркуляционного насоса. Это уменьшает непосредственную передачу термической энергии от кончика электрода к близлежащей ткани, что позволяет избежать резкого чрезмерного повышения температуры, перегрева и обугливания ткани, однако одновременно увеличивает время нагрева ткани до целевой температуры.
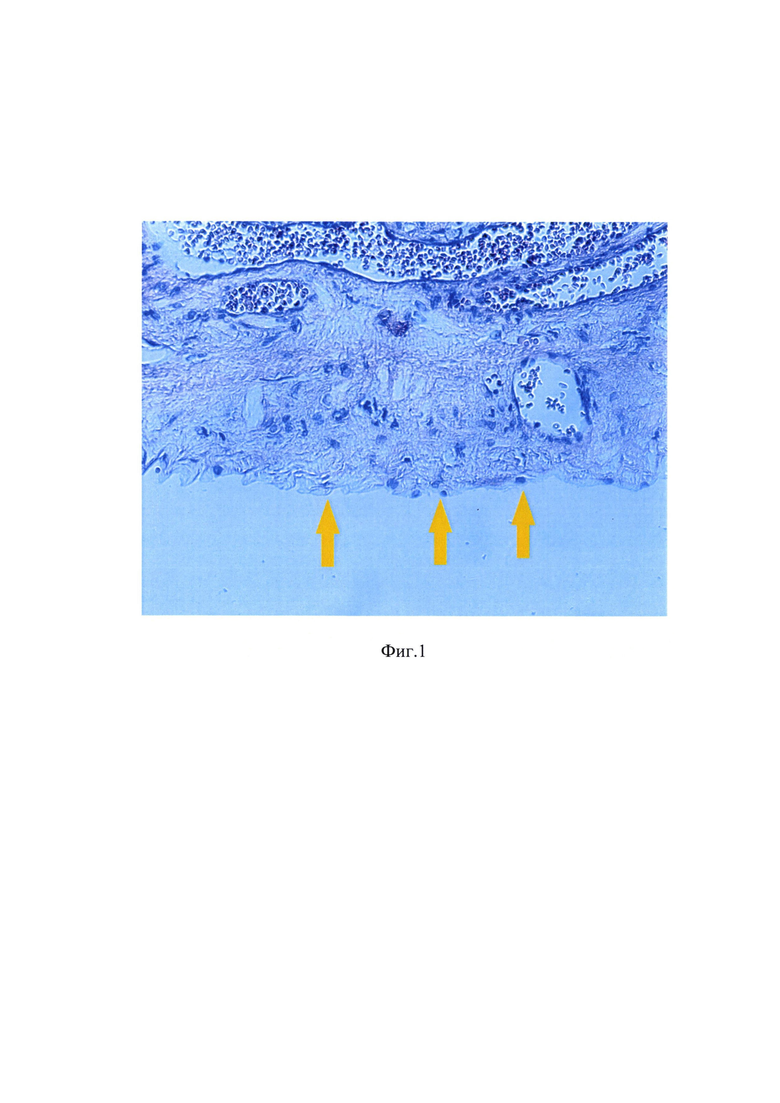
В случае выполнения РЧА кистозной полости преследуется совершенно иная цель, что предполагает выбор принципиально иных параметров вмешательства. Учитывая, что в норме внутренняя стенка кисты покрыта секретирующим жидкость эпителием в один ряд (Фигура), целесообразно выполнять РЧА в таком режиме, когда некрозу подвергается лишь один этот ряд, не допуская избыточного распространения тепловой энергии вглубь здоровой ткани и соседних структур, чтобы одновременно исключить рецидив и минимизировать термическое повреждение здоровой ткани.
Проблема достижения достаточного для некротизирования эпителия кисты прогревания при РЧА тесно пересекается с проблемой избыточного распространения термической энергии в глубину окружающих кистозную стенку тканей и органов. В экспериментальном исследовании Song НТ с соавторами (2001) установили, что РЧА в различных температурных режимах вызывает проникновение термического повреждения на разную глубину окружающих кисту тканей [Radiofrequency Thermal Ablation of Benign Cystic Lesion: An Experimental Pilot Study in a Porcine Gallbladder Model / H. Song, H. Rhim, J.B. Choi [et al.] // J. Korean. Radiol. Soc. - 2001. - Vol. 44, N 5.- P. 571-576].
Экспериментальные модели истинной кисты печени (отключенный желчный пузырь свиньи ex vivo) подвергали РЧА в течение 1 минуты при температурах 70°С, 80°С и 90°С. При последующем морфологическом исследовании все модели продемонстрировали полный коагуляционный некроз стенки «кисты». Однако, средняя глубина повреждения прилегающей паренхимы в группе 90°С составила 9,8 мм, в группе 80°С - 5,4 мм, в то время, как в группе 70°С термического повреждения прилегающей паренхимы отмечено не было. Однако, в группе 70°С наблюдались минимальные изменения окружающих тканей. На основании проведенного исследования авторы сделали вывод, что с помощью РЧА возможно лечение доброкачественных кист печени и почек под контролем УЗИ.
Результаты данного исследования позволяют сделать вывод, что температура абляции 70°С в течение одной минуты достаточна для достижения полного некроза стенки. В то же время, указанная температура являлась пороговой, при которой наблюдались косвенные признаки начального распространения термического повреждения вглубь окружающей паренхимы. Таким образом, для практического использования наиболее приемлемой температурой, как мы установили, является диапазон от 60°С до 69°С. Превышение порога 69°С в течение одной минуты может вызвать распространение термического повреждения за пределы стенки кисты.
Особую актуальность это приобретает при топографической близости капсулы кисты к сосудисто-секреторным структурам и полым органам; существует риск непосредственного термического повреждения, развития тромбоза и рубцовых стриктур [Complications of radiofrequency ablation for hepatocellular carcinoma in a multicenter study: An analysis of 16 346 treated nodules in 13 283 patients / M. Koda, Y. Murawaki, Y. Hirooka [et al.] // Hepatol. Res.-2012.-Vol. 42, N 11.-P. 1058-1064].
Установлено, что при температуре 60°С клетка погибает практически мгновенно [Долгушин Б.И., Косырев В.Ю. Радиочастотная термоаблация опухолей. - М.: «Практическая медицина», 2015. - С. 44-45]. Чтобы достичь полного поверхностного некроза однорядного эпителия, необходимо достижение температуры жидкой среды вблизи него 60°С на короткий период воздействия. Этого будет достаточно для необратимого повреждения клеток эпителия и предотвращения распространения термического повреждения вглубь здоровых тканей.
Достижение и удержание необходимой температуры во время сеанса РЧА кист сопряжено с рядом особенностей. Во-первых, встроенная термопара электрода в реальном времени отображает лишь значения близкорасположенного слоя жидкости, в то время как остальной ее объем прогревается постепенно. Для достоверного достижения целевой температуры у поверхностного слоя выстилки кисты необходимо учитывать разницу температур электрода и среды, и задержку прогревания кистозной среды.
Во-вторых, в отличие от экспериментальных исследований, в клинической практике при выполнении РЧА должен быть учтен такой важный фактор, как «эффект теплоотвода» («heat sink effect»). Поглощение тепла кровотоком окружающих сосудов вызывает охлаждение периферических границ области абляции, что, в совокупности с задержкой прогревания, требует увеличения либо мощности, либо экспозиции.
С учетом вышеизложенного, а также с целью минимизировать время абляции, мы в своей практике не применяли стандартное водоохлаждение электрода циркуляционным насосом во время сеанса РЧА. Это позволяло значительно ускорить время достижения заданной температуры и более оперативно реагировать на ее изменения в ходе вмешательства.
Данные преимущества дают возможность в режиме ручного управления мощностью генератора устанавливать и удерживать в зоне операции необходимую температуру. При РЧА кист почек она рекомендуется не менее 60°С, но не более 69°С.
Использование стандартной методики РЧА с помощью водоохлаждаемого электрода уменьшает непосредственную передачу термической энергии от кончика электрода к близлежащей ткани, что увеличивает время нагрева до целевой температуры и не позволяет оперативно изменять показатели температуры. Применение радиочастотной абляции без стандартного водоохлаждения рабочего электрода позволяет в ручном режиме управления достигать в полости кисты различных управляемых значений требуемой температуры в зависимости от необходимости для оператора и топографо-анатомических особенностей кисты (размеры, объем, локализация). В заявляемом методе: от первоначальной температуры 60°С до 69°С.
Таким образом, выбор меньшей температуры - приводит к меньшему термическому некрозу окружающих здоровых тканей, что особенно важно в хирургии почек. Поддержание температуры 60°С вблизи кистозной стенки в течение короткого периода времени способствовало необратимому повреждению клеток эпителия кисты и, в то же время, минимальному распространению термического повреждения на окружающую ткань, что имеет большое значение при близком расположении кисты к сосудисто-секреторным структурам, и полым органам.
Оставление пункционной иглы в полости кисты на всей продолжительности сеанса абляции способствует стабилизации внутриполостного давления в кисте, а также позволяет осуществить эвакуацию продуктов нагрева кистозного содержимого и окончательную аспирацию после сеанса абляции, что позволяет снизить послеоперационные осложнения.
Постепенное извлечение электрода с длиной шага около 1 см позволяет предотвратить геморрагические осложнения, т.к. меньшая длина шага при извлечении обеспечивает более полное перекрытие коагулируемых зон пункционного канала, что способствует лучшему гемостазу, поскольку по мере извлечения электрода происходит коагуляция пункционного канала.
Изобретение иллюстрируется Фигурой, на которой представлена микрофотография морфологической картины структуры солитарной кисты почки - стрелки указывают на однослойный кубический эпителий внутренней стенки кисты.
Подробное описание способа и примеры его клинического выполнения
Способ лечения солитарных кист и поликистоза почек осуществляют следующим образом.
Операционное вмешательство проводят в асептических условиях операционной как под внутривенной, так и под эндотрахеальной анестезией, в положении пациента на боку или на животе. Основное оборудование включает в себя систему радиочастотной абляции Cool-tip RF Radionics (Tyco Healthcare Group LP, USA), одиночный игольчатый монополярный электрод с длиной активной части 3 см со встроенной термопарой (Cool-tip RF Radionics (Tyco Healthcare Group LP, USA). После обработки кожи раствором йода операционное поле обкладывают стерильным хирургическим бельем. УЗ визуализацию проводят с помощью сканера ProFokus с многочастотным конвексным датчиком (2,5-6 МГц).
Прокол кожи выполняют в месте наиболее оптимального акустического доступа, с учетом предполагаемой траектории движения иглы и с учетом локализации крупных сосудов, и чашечно-лоханочной системы, чтобы избежать их ранения при пункции. Данная манипуляция выполняется под непрерывным У3-контролем, при необходимости применяется цветовое допплер-картирование ткани почек.
В месте предполагаемой пункции выполняют прокол кожи скальпелем длиной 2-3 мм. Для выполнения пункции солитарных кист или поликистоза почек используют нефростомическую иглу типа Chiba 18 G. Под контролем УЗИ производят пункцию кисты иглой, что подтверждается аспирацией из иглы нескольких миллилитров кистозного содержимого. Прохождение иглы через стенку кисты характеризуется ощущением провала в полость. Иглу позиционируют в центре полости кисты, чтобы избежать повреждения сосудов на противоположной стороне стенки кисты. Игла под контролем УЗИ четко визуализируется в виде линейной гиперэхогенной структуры на фоне анэхогенного содержимого кисты.
Под контролем УЗИ через выполненный ранее прокол вводят игольчатый электрод для проведения радиочастотной абляции с рабочей поверхностью 3 см. При подготовке генератора РЧА к работе стандартное водоохлаждение электрода циркуляционным насосом не используют и водоохлаждающие трубки к электроду не подключают с целью минимизировать время абляции.
Электрод позиционируют в центре полости кисты. По игле полностью аспирируют содержимое кисты, отправляют на цитологическое исследование.
После этого выполняют сеанс радиочастотной абляции полости кисты. Переводят генератор токов высокой частоты в режим ручного управления и включают в минимальном режиме, постепенно повышая мощность. Производят прогревание эпителиальной выстилки полости кисты до 60°С. Постепенно путем медленного поворота рукояти управления ручным режимом мощность увеличивают до нужных значений температуры. Достигнув нужного значения температуры - не более 69°С, сеанс радиочастотной абляции, в зависимости от размеров и расположения кисты, проводят в течение 5-10 минут. На всем протяжении сеанса нефростомическая игла находится в полости кисты, что позволяет удалять продукты нагрева.
После окончания сеанса радиочастотной абляции производят аспирацию остаточной жидкости из полости кисты, затем иглу извлекают. После этого генератор переводят в режим средней мощности и электрод постепенно, с длиной шага около 1 см, извлекают. По мере извлечения происходит коагуляция пункционного канала, что позволяет предотвратить геморрагические осложнения. Пункционную иглу извлекают. На место прокола накладывают асептическую наклейку.
Способ эффективно применим как при солитарных кистах, так и при поликистозе почек вследствие возможности обработки сразу нескольких кист с применением пункционного доступа. Возможно поэтапное лечение множественных кист обеих почек через определенные промежутки времени вследствие минимальной травматичности. Способ на практике показал себя возможным к применению после предшествовавшего лапароскопического иссечения кист почек.
Работоспособность заявляемого способа подтверждается следующими клиническими примерами:
Клинический пример 1. Пациентка С, 75 лет, в плановом порядке поступила в хирургическое отделение ГБУ РО «КДЦ «Здоровье» в г. Ростове-на-Дону в 2022 г. с диагнозом: Киста правой почки (Bosniak IIF).
Жалобы на дискомфорт и тяжесть в правой поясничной области. Анамнез в течение нескольких лет. В 2021 г. на МРТ выявлена солитарная киста верхнего сегмента правой почки с экстраренальным расположением, размерами 65×61×56 мм, с тонкими перегородками (Bosniak IIF). Функция почек не нарушена.
Пациентке выполнено миниинвазивное лечение кисты верхнего сегмента правой почки по заявляемой методике. В положении больной на левом боку под внутривенной анестезией под У3-контролем была выполнена пункция с сеансом РЧА кисты верхнего сегмента правой почки. РЧА выполнялась при температуре 69°С, продолжительностью 5 минут. На УЗИ интраоперационно фиксировано изменение состояния полости кисты в виде усиления эхогенности и неоднородности сигнала, появления гиперэхогенных включений в полости кисты.
Послеоперационный период протекал гладко, выписана на четвертые сутки в удовлетворительном состоянии. На контрольном УЗИ через 6 месяцев отмечено уменьшение объема оперированной кисты до 27×15 мм, через 12 месяцев на месте кисты определяется гипоэхогенный участок.
Клинический пример 2. Пациентка Г., 58 лет, в плановом порядке поступила в хирургическое отделение ГБУ РО «КДЦ «Здоровье» в г. Ростове-на-Дону в 2020 г. с диагнозом: Поликистоз почек (Bosniak I-II), лапароскопическое иссечение кист почек, холецистэктомия (2018).
Пациентка предъявляла жалобы на тяжесть в поясничной области. Анамнез заболевания около 20-ти лет. В 2018 г. по поводу данного заболевания была выполнена операция - лапароскопическое иссечение кист почек, холецистэктомия. В 2019 г. на КТ в динамике отмечено незначительное уменьшение части крупных кист по сравнению с картиной 2018 г. (размеры справа до 67×58 мм, слева до 70×72 мм), однако также выявлено увеличение кист средне-нижнего сегментов левой почки, с опущением и ротацией почки вокруг поперечной оси. Функция почек не нарушена.
Пациентка подготовлена к миниинвазивному лечению кист средне-нижнего отдела левой почки. В положении больной на животе под эндотрахеальной анестезией под У3-контролем была выполнена пункция с сеансом РЧА по вышеописанной методике последовательно двух кист средне-нижнего (размеры 60×50 мм и 71×70 мм) отдела левой почки. РЧА каждой кисты выполнялась при температуре 60°С, продолжительностью 5 минут (в совокупности 10 мин). На УЗИ интраоперационно фиксировано изменение состояния полости кисты в виде усиления эхогенности и неоднородности сигнала, появления гиперэхогенных включений в полости кисты. На всем протяжении сеанса нефростомическая игла находилась в полости кисты. После окончания сеанса абляции аспирировано до 1 мл остаточной жидкости из полости кисты, затем нефростомическая игла извлечена. После этого генератор переведен в режим средней мощности и электрод постепенно, с длиной шага около 1 см извлечен.
После вмешательства состояние пациентки стабильное, болезненности нет. При лабораторном контроле увеличения лейкоцитоза, маркеров воспаления не отмечено. На четвертые сутки после операции пациентка выписана в удовлетворительном состоянии.
На контрольной КТ через 6 месяцев отмечено уменьшение объема второй оперированной кисты до 33×31 мм с изменениями в виде утолщения стенок; на месте первой кисты представлен фиброзированный участок в области спавшихся стенок.
В ходе нашего научного исследования проведено изучение воздействия РЧА в различных режимах на кистозную стенку и соседнюю ткань почек. Были созданы имитационные модели простой кисты почки. Для создания модели кисты почки мы использовали 15 неперфузированных желчных пузырей свиней размерами от 5.5 до 6.5 см с толщиной стенки до 2 мм, погруженных в неперфузированную ткань почки свиньи. Желчный пузырь забирали у животных без прилежащей ткани печени. Участок на 4 см от дна желчного пузыря перевязывали лигатурой, создавая замкнутые пустые сферы, имитирующие полость кисты, достижимым объемом до 33.51 см3. Почка широко укладывалась на отводящую пластину пассивного электрода, наиболее массивную ее часть глубоко рассекали. Модели наполнялись дистиллированной водой в равных объемах по 15 мл, затем максимально погружались в разрез почки. В центральную часть модели вводили одиночный игольчатый монополярный электрод Cool-tip RF Radionics с длиной активной части 3 см, избегая контакта со стенкой модели. На расстоянии 2 см параллельно ему вводили иглу контактного цифрового термометра Cem DT-131, позиционируя ее вблизи стенки. После этого модели подверглись воздействию РЧА с температурой от 50 до 70°С с продолжительностью от 1 до 5 минут. Затем проводилась оценка постабляционных изменений препаратов с помощью гистологического исследования.
Исследование показало, что для простых кист с гомогенным прозрачным содержимым объемом 15 мл может быть рекомендована РЧА. Время сеанса РЧА в температурном режиме от 60°С до 69°С рекомендуется в течение 5-10 мин, что позволяет добиться полного некроза эпителиальной выстилки с минимальным повреждением окружающих тканей. Проведенное исследование позволяет сделать вывод, что на достижение полной коагуляции РЧА поверхностного слоя кисты с минимальным распространением вглубь окружающих тканей оказывают влияние следующие факторы: 1) объем и электропроводность кистозной среды; 2) возможность адекватного контроля истинной температуры внутри кисты, которая отличается в различных средах от показаний встроенной термопары электрода (большинство имеющихся в продаже систем РЧА оснащены подобной термопарой); 3) тщательный контроль применяемой температуры и времени воздействия. Полученные данные легли в основу разработки заявленного способа лечения солитарных кист и поликистоза почек.
Заявленным способом пролечено 2 больных с солитарными кистами почек и поликистозом почек. Послеоперационных осложнений и рецидивов в ходе наблюдения в течение 6-9 мес. после лечения - не выявлено.
Следует отметить, что у больных, которым оперативное вмешательство под эндотрахеальным наркозом с вхождением в брюшную полость противопоказано, описанный способ является одним из немногих возможных к применению.
Таким образом, предлагаемый нами способ, в отличие от известных, осуществляют чрескожным доступом через один прокол с использованием внутривенной анестезии, что является более благоприятным для пациента. Метод не требует дренирования или проведения нескольких сеансов.
С использованием предлагаемого нами способа возможно лечение не только солитарных кист и поликистоза почек, а также кист, расположенных рядом с жизненно важными структурами. Результаты нашего клинического исследования показали существенное уменьшение объема кист почек в сроки до 6-9 месяцев.
Использование заявленной технологии, направленной на снижение риска осложнений и числа рецидивов у этой категории больных, позволило существенно повысить выполнимость, эффективность и безопасность пункционных методов диагностики и лечения солитарных кист и поликистоза почек.
Преимущества метода:
Заявленный способ лечения солитарных кист и поликистоза почек легко выполним и малотравматичен. В результате использования данного способа достигается максимально полная обработка полости кисты почки практически любой локализации за счет выбора оптимального температурного режима и времени воздействия.
Заявленный способ не требует вхождения в брюшную полость, создания карбоксиперитонеума, использования потенциально токсичных химических веществ, наружного дренирования, обеспечивает короткий срок пребывания больного в отделении, выполним в «стационаре одного дня».
Заявляемый способ лечения солитарных кист и поликистоза почек показал высокую эффективность при использовании и может быть рекомендован к клиническому применению в профильных стационарах и в «стационарах одного дня».
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ НЕПАРАЗИТАРНЫХ КИСТ ПЕЧЕНИ | 2016 |
|
RU2626692C1 |
| СПОСОБ ОДНОТРОАКАРНОЙ РЕТРОПЕРИТОНЕОСКОПИЧЕСКОЙ ФЕНЕСТРАЦИИ КИСТ ПОЧЕК У ДЕТЕЙ | 2014 |
|
RU2578186C2 |
| СПОСОБ ЧРЕСКОЖНОГО ПУНКЦИОННОГО МИНИ-ПЕРКУТАННОГО ЛЕЧЕНИЯ БОЛЬШИХ, ГИГАНТСКИХ И МНОГОКАМЕРНЫХ КИСТ ПОЧЕК В ЖИДКОЙ СРЕДЕ | 2019 |
|
RU2725554C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬШИХ, ГИГАНТСКИХ И МНОГОКАМЕРНЫХ КИСТ ПОЧЕК | 2004 |
|
RU2296527C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ СОЛИТАРНЫХ НЕПАРАЗИТАРНЫХ КИСТ СЕЛЕЗЕНКИ У ДЕТЕЙ | 2009 |
|
RU2402281C1 |
| СПОСОБ ЛЕЧЕНИЯ КИСТ ПАРЕНХИМАТОЗНЫХ ОРГАНОВ | 1996 |
|
RU2102013C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭХИНОКОККОВОЙ КИСТЫ ПЕЧЕНИ ТИПА СЕ2В, СЕ3В | 2018 |
|
RU2695007C1 |
| Способ лечения полостных образований | 2016 |
|
RU2652750C1 |
| СПОСОБ КОМБИНИРОВАННОЙ ДЕСТРУКЦИИ ДОБРОКАЧЕСТВЕННЫХ СОЛИДНЫХ УЗЛОВ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2009 |
|
RU2426565C2 |
| СПОСОБ ЛЕЧЕНИЯ КИСТ ПОЧЕК | 1997 |
|
RU2115371C1 |
Изобретение относится к медицине, а именно к хирургии и урологии. Выполняют чрескожную пункцию полости кисты почек под УЗ-наведением. Аспирируют содержимое кисты. Обрабатывают полость кисты почек с использованием радиочастотной абляции в ручном режиме, с прогреванием эпителиальной выстилки полости кисты от 60°С до 69°С в течение 5-10 мин, при этом оставляют пункционную иглу в полости кисты на всю продолжительность сеанса радиочастотной абляции. После чего генератор переводят в режим средней мощности и извлекают электрод постепенно с длиной шага 1 см. Способ позволяет предупредить геморрагические осложнения и рецидивы после пункционного лечения солитарных кист и поликистоза почек. 1 ил., 2 пр.
Способ лечения солитарных кист и поликистоза почек, включающий чрескожную пункцию полости, аспирацию содержимого кисты и последующую абляцию стенок кисты, отличающийся тем, что после пункции полости и аспирации содержимого кисты под УЗ-наведением обработку полости кисты осуществляют с использованием радиочастотной абляции в ручном режиме с прогреванием эпителиальной выстилки полости кисты от 60°С до 69°С в течение 5-10 мин, при этом оставляют пункционную иглу в полости кисты на всю продолжительность сеанса радиочастотной абляции, после этого генератор переводят в режим средней мощности и извлекают электрод постепенно с длиной шага 1 см.
| СПОСОБ ЛЕЧЕНИЯ НЕПАРАЗИТАРНЫХ КИСТ ПЕЧЕНИ | 2016 |
|
RU2626692C1 |
| CN 109820593 A, 31.05.2019 | |||
| Глыбочко П.В и др | |||
| / Опыт применения радиочастотной абляции в лечении почечно-клеточного рака / Сеченовский вестник | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| H | |||
| Song, H | |||
| et al | |||
| / Radiofrequency Thermal Ablation of Benign Cystic Lesion: An Experimental Pilot Study in a Porcine Gallbladder Model / J | |||
| Korean | |||
| Radiol | |||
Авторы
Даты
2025-02-11—Публикация
2024-04-16—Подача