Изобретение включает способ получения внеклеточного экзополимера, продуцируемого путем культивирования отобранных штаммов бактерий Bifidobacterium, обладающих иммуномодуляторными свойствами. Способ относится к этому экзополимеру и фармацевтическим веществам, содержащим указанный экзополимер в качестве основного активного агента.
Многочисленные заболевания, такие как аллергии, аутоиммунные болезни, инфекционные болезни и некоторые виды рака, имеют общую черту - первичное или вторичное расстройство иммунной системы. В то время как первичные иммуннодефициты редки и обычно имеют генетическую причину, вторичные иммунодефициты встречаются более часто и их причины главным образом внешние, включающие, например, возвратные инфекции, старение, рак, недоедание, воздействие иммунотоксических веществ и стресса.
Иммунотерапия позволяет устранить симптомы первичного иммунодефицита и восстановить иммунный статус в случае вторичного иммунодефицита.
Было разработано множество иммунотерапевтических агентов в виде иммуностимулянтов или иммуносупрессантов. Иммуномодуляторы - агенты, которые неспецифически улучшают специфичную реактивность хозяина и неспецифические эффекторные механизмы. Иммуномодуляторы можно подразделить на синтетические и биологические. Последние являются микробиальными продуктами и экстрактами животного или даже человеческого происхождения, например гормоны вилочковой железы, способные к диализу лейкоцитарные экстракты, интерфероны и цитокины.
В действительности активирование лимфоцитов или макрофагов и их промежуточных форм значительно изменяется под воздействием структурных молекул микроорганизмов или биологически активных компонентов, продуцируемых микроорганизмами. Многие разные бактерии и бактериальные продукты продемонстрировали свое влияние на иммунную систему. Этот арсенал иммуномодулярных агентов бактериального происхождения включает микобактерии и их продукты, липополисахариды грамотрицательных бактерий, энтеротоксины холерного вибриона, продукты стрептококка, липопротеины и гликопротеины различных грамотрицательных бактерий и полисахариды различного происхождения. В этой области в настоящее время ведутся интенсивные исследования.
Предлагаемое изобретение относится к новому внеклеточному экзополимеру, обладающему крайне интересными иммуномодуляторными свойствами. Точнее изобретение охватывает способ получения указанного экзополимера, а также внеклеточный экзополимер, получаемый при использовании указанного способа.
Экзополимер продуцируется при культивировании отобранных селекцией штаммов недавно выделенного вида Bifidobacterium infantis longum грамположительной бактерии, которая имеет таксономические характеристики между Bifidobacterium infantis и Bifidobacterium longum. Обладая экспериментально продемонстрированными иммуномодуляторными свойствами, этот экзополимер представляет большой интерес для медицины и ветеринарии.
Данный способ характеризуется тем, что бактериальный штамм IBS Bifidobacterium infantis longum, депонированный под номером 1-885 в институте Пастера в национальной коллекции культур микроорганизмов (НККМ), культивируют в анаэробных условиях в подходяшей среде и после удаления микроорганизмов из культуральной среды продуцированный ими экзополимер выделяют и осаждают путем добавления органического растворителя. Полученный путем осаждения продукт лиофилизируют.
Штамм IBS может культивироваться на подходящей среде любого типа, компоненты которой имеют молекулярный вес менее 10 тыс. дальтон, в анэробных условиях предпочтительно при 37оС.
Микроорганизмы удаляют из культуральной среды центрифугированием и экзополимер выделяют, например, ультрафильтрацией на калиброванной пористой мембране с удерживающим порогом выше или равным 10 тыс. дальтон. Изолированный таким образом продукт затем концентрируют, подвергают диализу, осаждают добавлением органического растворителя, предпочтительно этанола, и наконец лиофилизируют. Полученный экзополимер имеет в основном полисахаридную природу, состоит из глюкозы и галактозы в соотношении (1-4):1 и содержит белковую фракцию в количестве до 30 мас.%. Во фракции полисахаридов соотношение глюкозы и галактозы составляет (1-4):1, предпочтительно около 3 : 2.
Экзополимер по настоящему изобретению имеет молекулярный вес в диапазоне 10-100 тыс. дальтон, предпочтительно 20-30 тыс. дальтон. Он может образовывать агрегаты молекулярного веса порядка 106 дальтон в равновесии с частицами более низкого молекулярного веса. Он свободен также от нуклеиновых кислот, жиров и органических кислот. Изолированный таким образом и очищенный экзополимер обладает интересными иммуномодуляторными свойствами и при этом нетоксичен. Опыты, проведенные как "ин-витро", так и "ин-виво", показали, что экзополимер, продуцированный штаммом IBS, ведет себя как иммуномодулятор, и увеличивает неспецифическое сопротивление хозяина. Этот экзополимер также обладает антилейкемическими (противоопухо- левыми) свойствами, происхождение которых может быть связано с его иммуномодуляторными свойствами.
Так, экзополимер, продуцируемый штаммом IBS, может быть с выгодой использован в качестве основного активного начала различных фармацевтических составов, которые могут применяться через рот, парентерально или местно. Эти фармацевтические составы могут быть представлены в виде форм, обычно используемых в медицине и ветеринарии, например, в виде простых или покрытых сахаром таблеток, капсул, маленьких пилюль, растворов, сиропов, суппозиториев, инъецируемых препаратов, пессариев, кремов, помад, лосьонов, капель и глазных мазей. Они все изготавливаются обычными методами.
Основное активное начало (экзополимер) может вводиться в фармацевтические составы самостоятельно или вместе с другими фармакологически активными агентами. Используются обычные носители и вспомогательные вещества, такие как тальк, камедь, маннитол, крахмал, стеарат магния, кокосовое масло, водные или неводные носители, жировые вещества животного или растительного происхождения, производные парафина, гликоли, различные увлажняющие, диспергирующие или эмульси- фицирующие агенты, и консерванты.
У животных заметные иммуномодуляторные эффекты наблюдались на мышах для доз между 4-400 мг на мышь.
Примеры, представленные ниже, касаются, в частности, приготовления экзополимера, называемого РВЗD, и его фармакологического действия.
П р и м е р 1. Получение экзополимера путем культивирования бактериального штамма IBS Bifidobacterium infantis longum.
Стадия А: культивирование штамма IBS.
Штамм IBS культивируют в анаэробных условиях при 37оС (воздух удаляют в начале ферментации) в следующей питательной среде, г/л: Пептон (мол.вес 10 тыс. дальтон) 5 NaCl 3 Глюкоза 10 Цистеин 0,5 Ацетат натрия 2 Na2HPO4 2,87 КH2PO4 1,12 MgSO4 0,09 NaH2PO4 0,15 NaHCO3 2,2 Твин 1 мл/л Витаминный раствор 10 мл/л
Для повышения выхода к этой культуральной среде может быть добавлена твердая основа, такая как СYТODЕX или ее эквивалент. В этих условиях штамм IBS продуцирует экзополимер, количество которого можно установить в надосадочной жидкости с использованием тестового метода ELISA.
10 л указанной культуральной среды помещают в 12-литровый ферментер для ее стерилизации. Ферментер затем засевают 1000 мл культуры штамма IBS, выдержанной предварительно в такой же среде в течение 48 ч. Жидкость барботируют смесью 90% азота и 10% СО2 в течение 20 мин со скоростью 3 л смеси в минуту.
Инкубация осуществляется при 37оС при перемешивании 400 об/мин в атмосфере смеси N2/СО2 в обычном соотношении, которую вводят в среду в течение первых двух часов ферментации. Через 48 ч, по окончании ферментационного процесса, методом ELISA определяют количество продуцированного полисахарида. Минимальный выход составляет 35 мг/мл.
Стадия В: выделение и очистка полученного экзополимера.
После завершения процесса ферментации, клетки отделяют центрифугированием. После осаждения клеток надосадочную жидкость ультрафильтруют с использованием известного аппарата. Сохраняются только молекулы, тяжелее 10000 дальтон. Раствор, содержащий полученный экзополимер, концентрируют десятикратно и затем подвергают диализу.
Концентрированный раствор осаждают спиртом (этанол:вода - 3:1 по объему). Осажденный спиртом продукт лиофилизируют. Таким образом получают беловатый продукт, который выглядит волокнистым.
Из указанной культуры получают 10 л надосадочной жидкости, которые концентрируют до 1 л путем ультрафильтрации. Объем доводят до 10 л дистиллированной водой и затем его снова уменьшают до 1 л ультрафильтрацией. Эту операцию проводят дважды. Полученный таким образом 1 л концентрированного раствора осаждают этанолом (3:1 по объему). Полученный осадок лиофилизируют с получением около 400 г лиофилизата.
Метод ELISA.
Используемый антиген - препарат полисахарида, чистота которого обеспечивается дополнительной депротеинизацией фенолом. Начальную дозу 0,5 мг инъецируют кролику в двух инъекциях: одна внутрибрюшинно и другая подкожно - вместе с полным адъювантом Фрейнда.
Инъекцию повторяют на 15-й день, на этот раз с использованием неполного адъюванта Фрейнда. Пятнадцатью днями позже у кролика берут кровь с получением антисыворотки с высоким уровнем антител, которая позволяет методом ELISA узнать экзополимер, очищенный хроматографией на колонне SEPHADЕХ G 200, и экзополимер, присутствующий в надосадочной жидкости культур B ifidobacterium после осаждения этанолом.
Тест ELISA проводят на микрочашках. Антиген адсорбируется. Затем выемки в оставшихся пустыми участками заполняют сывороточным альбумином и осуществляют инкубацию со специфическими антителами, полученными от кролика. Далее добавляют антитела, направленные против антител кролика. Они конъюгируют к щелочной фосфатазе. Наконец, добавляют субстрат ортонитрофенилфосфат. После инкубации реакцию останавливают с использованием ЗМ раствора NaOH. Оптическая плотность (светопоглощение) измеряется при 405 нм на приборе ЕLISA. Этой процедурой получают достаточно высокие титры антител для получения положительной реакции для 10-4 разведений антисыворотки при концентрации очищенных антигенов 4 мг.
Характеристика экзополимера, продуцированного штаммом IBS.
1) Полученный продукт составит преимущественно из глюцидов (измерено фенольно-сернокислым методом) и белков (измерено методом Лоури) в соотношении 5: 1. Этот продукт не содержит никаких нуклеиновых кислот согласно аналитическим данным, полученным ионно-исключающей хроматографией или газовой хроматографией. Ни в одном из случаев гидролизат не содержит пентоз. Продукт свободен от липидов согласно результатам газовой хроматографии после экстрагирования н-гептаном. В нем нет и органических кислот согласно измерениям, сделанным ионно-исключающей хроматографией;
2) Согласно результатам, полученным высокопроизводительной жидкостной хроматографией (НРLС) на колонне RР-8 300  , продукт имеет гликопротеиновую природу;
, продукт имеет гликопротеиновую природу;
3) Глюцидная часть состоит из глюкозы и галактозы согласно аналитическим данным, полученным ионно-исключающей, тонкослойной и газовой хроматографией;
4) Глюкоза и галактоза присутствуют в соотношении 3:2 согласно результатам газовой хроматографии мономеров, гидролизованных метанолизом и затем ацетилированных трифторацетилированием;
5) Полисахаридная часть имеет разнообразные связи 1-2, 1-3, 1-4 и 1-6 согласно хроматограмме, полученной газовой хроматографией метилированных (метанолизом) и затем ацетилированных (трифторацетилированием) мономеров;
6) Биологическая активность, измеряемая по способности стимулировать увеличение количества клеток, образующих зоны гемолиза (РFC), проистекает из глюцидной части и поддерживается после обработки протеиназой К, повреждающей белковую часть;
7) Примерный молекулярный вес колеблется от 20000 до 30000 дальтон согласно результатам хроматографии на SEPHAD EX G 200 (пик низкомолекулярного веса).
Экзополимер может образовать аггрегаты молекулярного веса порядка 106 дальтон в равновесии с частицами более низкого веса.
П р и м е р 2. Определение иммуномодуляторных свойств экзополимера, продуцируемого штаммом IBS (тест "ин витро").
Пролиферация спленоцитов (селезеночных микрофагов).
Пролиферация спленоцитов в присутствии митогена может быть измерена окислением МТТ [3-(4,5-диметилтиазол-2-ил)- 2,5-дифенил тетразол бромид] с формазанмитохондриальной дегидрогеназой.
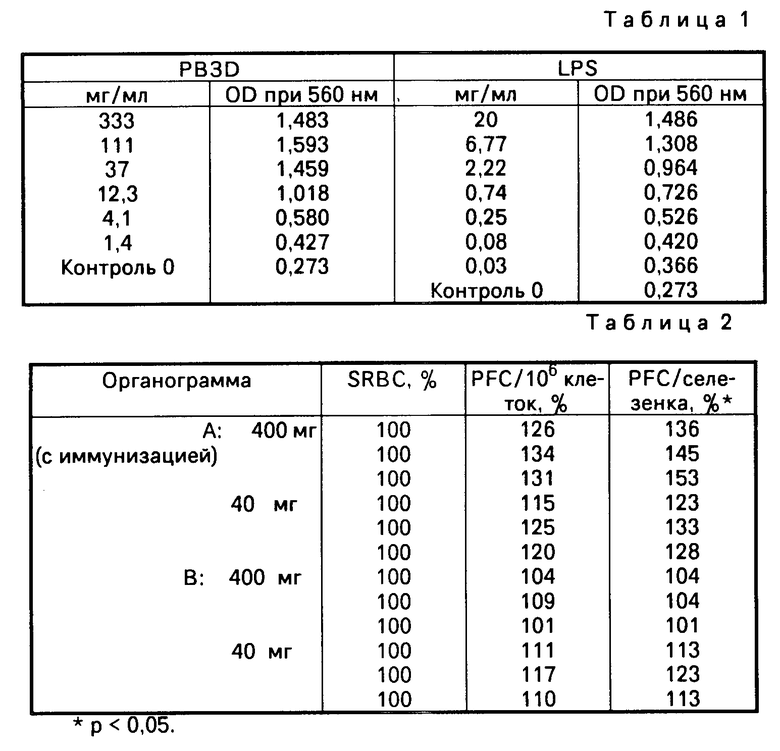
Пролиферация (спленоцитов мыши С57ВL/6) выражается оптической плотностью (светопоглощением) при 560 нм как функция концентрации РВЗD или концентрации LPS, служащей в качестве ссылки (см. табл.1).
РВЗD вызывает пролиферацию, которая немного слабее пролиферации, вызываемой LPS.
П р и м е р 3. Определение иммуномодуляторных свойств экзополимера, продуцируемого штаммом IBS (тест "ин виво").
Стимулирование производства клеток, синтезирующих антитела у мышей. Этот экзополимер неспецифически стимулирует производство клеток, синтезирующих антитела при оральном введении вместе с эритроцитами овцы или внутрибрюшинно без эритроцитов овцы. Экзополимер также нормализует эту способность у мышей, когда она подавлена цилкофосфамидом.
После 5-ти дневного орального введения РВЗD и иммунизирующей дозы на 19-й и 20-й дни (органограмма А) или без иммунизирующей дозы (органограмма В) наблюдается увеличение количества РFC в селезенке мышей, в зависимости от введенных доз (см. табл.2).
После внутрибрюшного введения разовой дозы 4000 мг/на мышь РВЗD наблюдается значительное увеличение количества РFC через 4 дня (cм. табл.3).
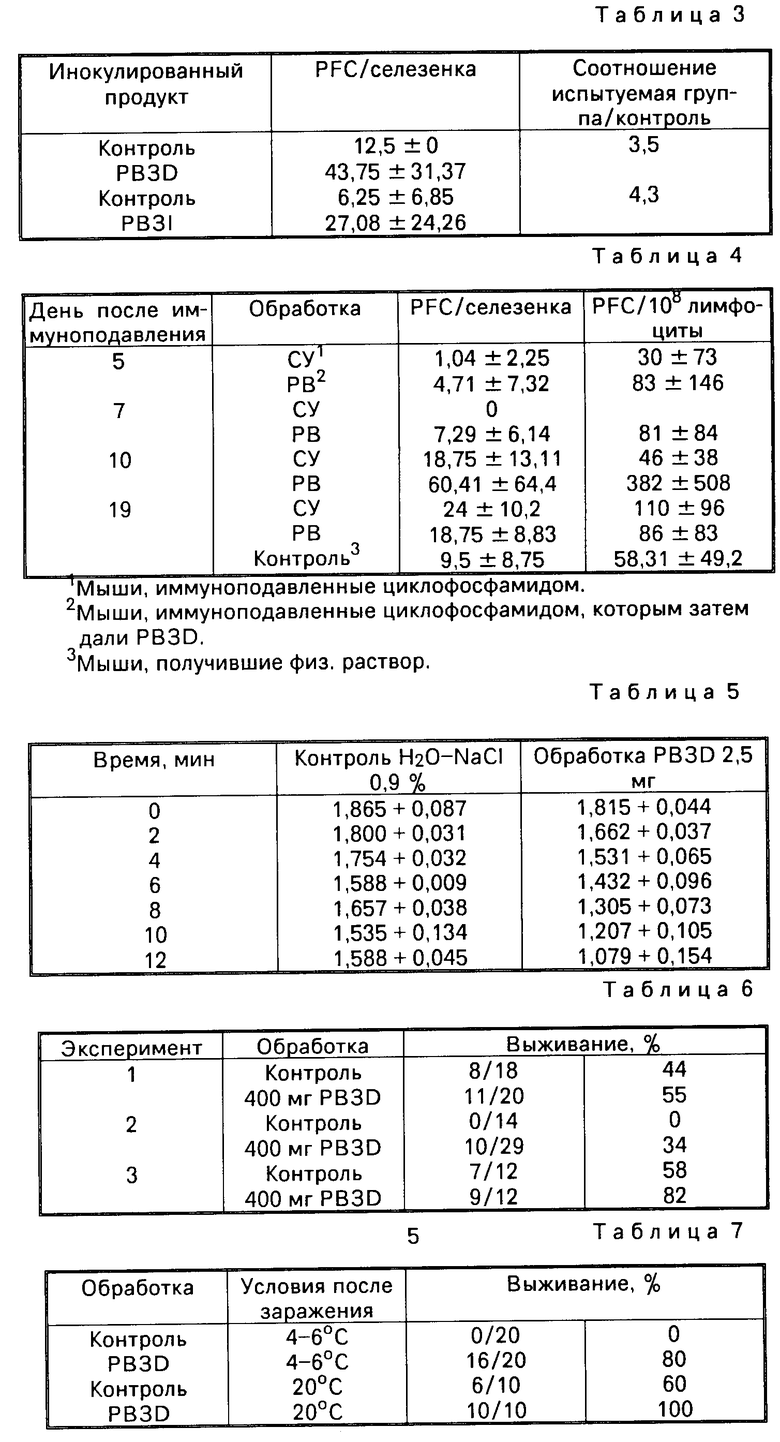
Экзополимер, вводимый мышам, которые были иммуноподавлены циклофосфамидом, позволяет наблюдать у обработанных мышей снижение иммуноподавления или более быстрое восстановление нормального количества РFC по сравнению с необработанными мышами (cм. табл.4).
П р и м е р 4. Влияние на состав сывороточных протеинов.
Различные иммуномодуляторы изменяют иммуноэлектрофоретические характеристики сывороточных протеинов, определенных как Х, LA и LB. Экзополимер по настоящему изобретению вызывает такую модификацию.
Внутрибрюшное введение РВЗI в количестве 400 мг на мышь вызывает через 24 ч и 4 дня модификацию сывороточных протеинов, сравнимую с изменениями, вызываемыми липополисахаридами Escherichia coli (LPS).
Общее введения 400 мг оральным путем с разбивкой на пять последовательных дневных доз по 80 мг вызывает модификацию протеинов, заметную через пять дней после введения экзополимера.
П р и м е р 5. Очищение коллоидного углерода.
Экзополимер вводят внутривенно (по 2,5 мг на мышь) мышам Balb/с. Через 48 ч внутривенно вводят 0,2 мл суспензии коллоидного углерода. Исчезновение коллоидного углерода из крови, называемое очищением, выражается логарифмической кривой уровня углерода во времени. Экзополимер усиливает процесс очищения (см. табл.5).
П р и м е р 6. Увеличение неспецифической резистентности.
У мышей, иммуноподавленных циклофосфамидом и помещенных в холод, можно наблюдать, что экзополимер по настоящему изобретению увеличивает неспецифическую резистентность хозяина к бактериальной инфекции, такой как, например, вызванной Pseudomonas на слизистых оболочках или к вирусной инфекции (вирус Сохsackie B).
Иммуноподавление осуществляют введением внутрибрюшинно 200 мг/кг циклофосфамида. На третий день начинают пятидневную оральную обработку экзополимером (по 80 мг на мышь в день).
Контрольные мыши получают эквивалентное количество физ. раствора. Hесколькими часами позже окончания курса обработки мышей инфицируют интраназально штаммом Pseudomonas aeruginesa, сделанным патогенным для мышей. Процент выживания у обработанных мышей дан в табл.6.
П р и м е р 7. Иммуноподавление создают разовым внутрибрюшным введением 200 мг/кг циклофосфамида.
На третий день начинают пятидневную обработку экзополимером (80 мг на мышь в день). Контрольные мыши получают эквивалентное количество физ. раствора. Через несколько часов после окончания курса обработки мышей инфицируют внутрибрюшинно вирусом Сохsаскiе В5 (0,5 мл с 107 РFИ) и оценивают степень выживания, которая была выше у обработанных мышей.
П р и м е р 8. Тесты на спонтанную и индуцированную лейкемию.
Экзополимер по настоящему изобретению способен задерживать появление лейкемии у мышей АКR (линия инбредных мышей очень часто развивает спонтанную лейкемию). Экзополимер также способен задерживать у мышей RF появление лейкемии, вызванной канцерогенным веществом, таким как метилхолантрен (линия RF является инбредной, у которой метилхолантрен вызывает очень скоро появляющуюся лейкемию).
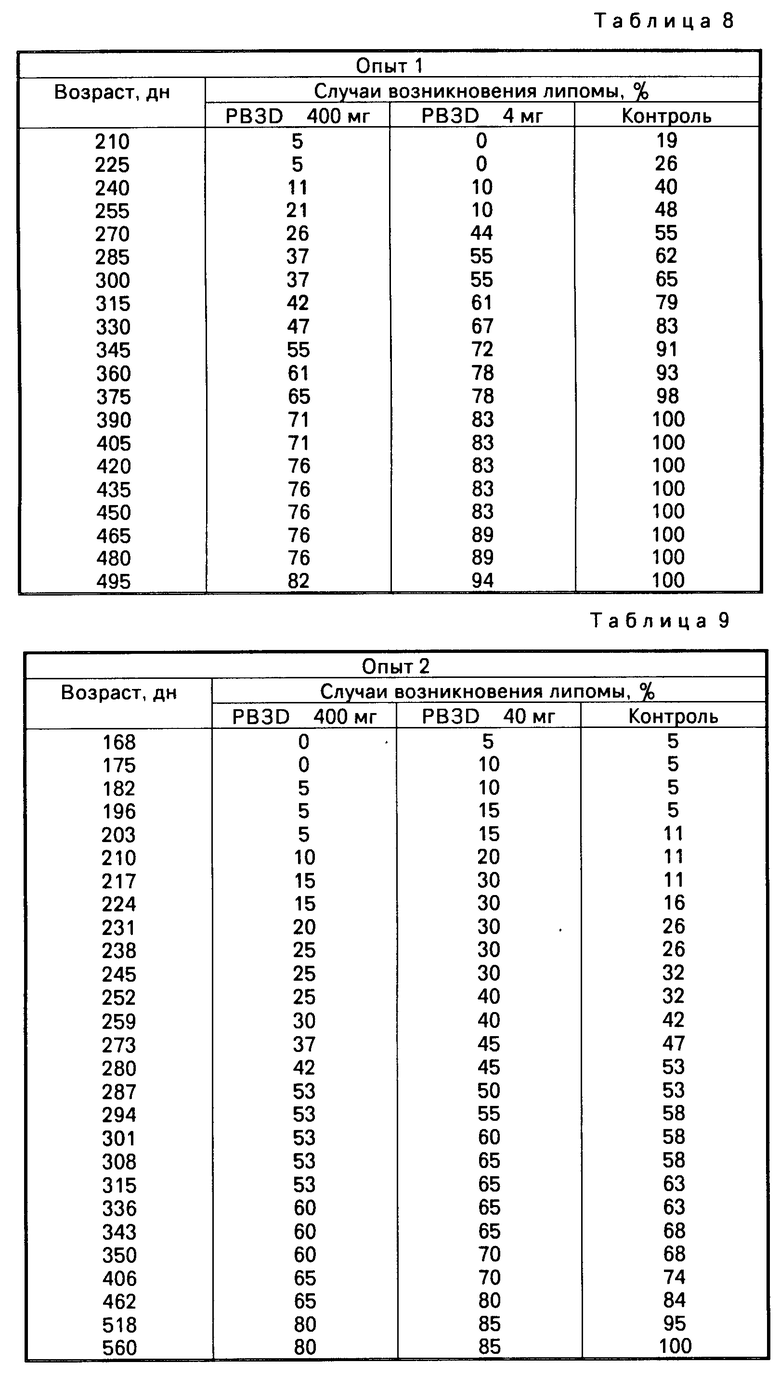
Две группы мышей АКR получали орально пятидневную терапию РВЗD каждый месяц, тогда как третья группа не получала испытываемый продукт и служила в качестве контроля. Из двух обработанных групп одна получала общую месячную дозу в 400 мг (по 80 мг в день на мышь пять последовательных дней), а другая получала общую месячную дозу в 4 мг по 0,8 мг в день на мышь пять последовательных дней).
Полученные результаты показывают задержку появления лейкемии у обработанных мышей. Эта разница была отчетливо видна у группы, получавшей месячную дозу в 400 мг. Эти данные были подтверждены другим опытом, при котором обработанные группы получали по 400 и по 40 мг РВЗD соответственно.
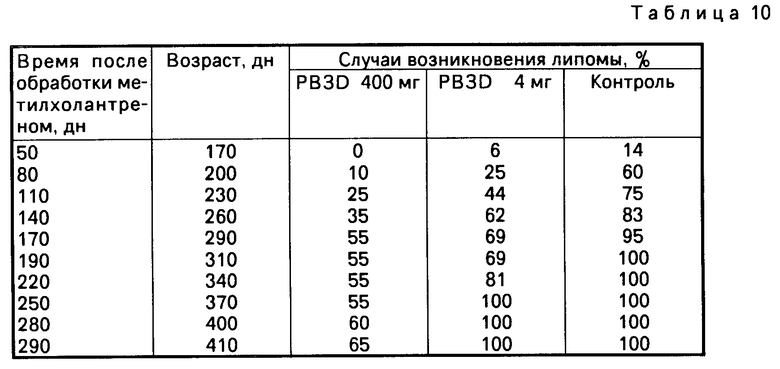
П р и м е р 9. В течение 2 мес до тематического введения метилхолантрена две группы мышей RF получали по два оральных введения с перерывом в три недели.
Одной из групп давали общую месячную дозу 400 мг (80 мг в день на мышь, пять последовательных дней), тогда как другая группа получала общую месячную дозу величиной 4 мг (по 0,8 мг в день на мышь, пять последовательных дней). Контрольную группу не обрабатывали. Лейкемию вызывали кожным применением метилхолантрена на тщательно выбритый участок тела. Введение РВЗD замедлило появление лейкемии. Эта задержка была ясно заметна у группы, получавшей 400 мг РВЗD.
П р и м е р 10. Острая токсичность.
Тесты на острую токсичность проводили путем внутривенного введения экзополимера в следующих дозах: 1, 10, 15, 100, 300, 600 и 1200 мг на мышь в хвостовую вену, по каждой дозе 5 мышам. Ни одна из доз не вызвала негативных реакций у мышей, которые все были живы еще два месяца после инъекции.
Штамм IBS Bifidobacterium infantis longum был депонирован 6 июля 1989 г. в Национальной коллекции культур микроорганизмов (институт Пастера, 25 Rue de Docfeur Roux, 75724, Par 19, Сеdex, France). Он носит депозитарный номер 1-885.
Этот штамм был выделен из сточной воды, содержащей фекалии человека, представляет таксономические характеристики между Bifidobacterium infanfis и Bifidobacterium longum и может быть типирован по профилю структурных компонентов, профилям ферментационных катаболитов D-глюкозы, резистентности к антибиотикам и продуцированию экзополимера по настоящему изобретению.
Использование: биотехнология, иммунотерапия, иммуностимулятор, экзополимер, бифидобактерии. Сущность изобретения: способ получения внеклеточного экзополимера, наделенного иммуномодуляторными свойствами, предусматривает культивирование штамма Bifidobacterium infantis Lonqum, депонированного в институте Пастера под номером 1-885, в подходящей среде в анаэробных условиях. После удаления микроорганизмов из культуральной среды выделяют продуцированный ими экзополимер, концентрируют и затем осаждают добавлением органического растворителя. Далее полученный в результате осаждения продукт лиофилизируют. Полученный экзополимер действует как на клеточный, так и на гуморальный иммунитет и может быть использовано в качестве иммуномодулирующего агента в любом возможном терапевтическом применении. 10 табл.
СПОСОБ ПОЛУЧЕНИЯ ИММУНОМОДУЛЯТОРА, предусматривающий культивирование штамма Bifidobacterium infantis в анаэробных условиях в подходящей среде с последующим выделением целевого продукта, отличающийся тем, что из штаммов Bifidobacterium infantis используют штамм Bifidobacterium infantis lonqum CNCM 1 - 885, культуральную среду центрифугируют, отделяют супернатант, подвергают его ультрафильтрации на калиброванной пористой мембране с порогом удерживания 10000 - 100000 дальтон, полученный продукт концентрируют, выделение осуществляют осаждением смесью этанол-вода в соотношении 1 : 3 и получают целевой продукт, представляющий собой экзополимер полисахаридной природы.
| Патент США N 4645667, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1994-11-30—Публикация
1990-09-28—Подача