Изобретение относится к области спектрофотометрических исследований в медицине и может быть использовано при изучении и дифференциальной диагностике предраковых и раковых состояний в онкологии (в частности, в онкогинекологии) и других областях медицины.
Известен способ функциональной диагностики онкопатологий с помощью люминесцентных микроскопов, основанный на освещении препарата ультрафиолетовыми лучами, при которых в объекте исследования вызывается флюоресценция различных оттенков (см. Мияновский А.И. Методы диагностики в онкогинекологии. К. Выща школа, 1988, с. 35-39). В качестве объекта исследования используются различные биологические объекты, например, эпителий слизистой оболочки матки. Однако данный метод исследования имеет высокую трудоемкость, низкую достоверность и большое время диагностики.
Высокая трудоемкость обусловлена тем, что большая часть биологических объектов не обладает способностью флюоресцировать, поэтому для возбуждения флюоресценции препарат предварительно обрабатывают флюрохромными красителями (акридиновым оранжевым). Этим же фактором обусловлено и большое время диагностики, поскольку необходима предварительная обработка исследуемых препаратов.
Низкая достоверность обусловлена тем, что не исключается возможность химического взаимодействия препарата и красителей, в результате которого изменяется химический состав исследуемого препарата.
Известен способ исследования гистоцитологических препаратов, заключающийся в облучении в оптическом диапазоне исследуемых и эталонных образцов и определении их поглощения в видимом и ИК-диапазонах, при этом о злокачественном характере гуморального образца судят по спаду показателя поглощения по крайней мере до 0,3 см-1 в диапазоне 500-600 нм.
Однако данный способ имеет большое время и низкую достоверность диагностики.
Длительное время диагностики обуславливается тем, что для реализации способа необходимо сравнение гуморальных исследуемого и эталонных образцов (плазма крови), включающее снятие спектра поглощения в диапазоне 500-600 нм для обоих образцов и анализ этих кривых по спаду показателя поглощения по крайней мере до 0,3 см-1.
Низкая достоверность по данному способу обусловлена тем, что для точной диагностики исследуемого образца необходим подбор донорского аналога с соответствующими параметрами (например, группа крови, резус-фактор и др.).
Известно устройство для спектрометрических исследований, которое может быть использовано при реализации предложенного способа, содержащее источник излучения, монохроматор, коллимирующую трубку, блок интегрирования светового пучка, в котором также размещена кювета с исследуемой средой, приемник излучения и блок регистрации. Однако все операции по излучению параметров исследуемой среды, их обработка и сравнение с эталонными производятся вручную, что делает процесс исследования достаточно длительным и трудоемким.
Задача, на решение которой направлено изобретение, заключается в разработке способа для исследования гуморальных сред (ранняя диагностика предраковых и раковых состояний), при котором определяют оптический диапазон для спектрофотометрического анализа гуморальной среды и по характеру спектральной кривой в данном диапазоне устанавливают состояние исследуемой гуморальной среды.
При осуществлении изобретения могут быть получены следующие технические результаты: уменьшение трудоемкости исследований, поскольку все операции, необходимые для проведения исследований согласно данному способу, легко автоматизируются; повышение достоверности и уменьшение времени проведения диагностики, поскольку для реализации способа не нужен подбор донорского аналога (эталонного образца), соответствующего исследуемой гуморальной среде (группа крови, резус-фактор и другие параметры) и, следовательно, не требуется проводить анализ и сравнение двух образцов.
Сущность изобретения заключается в том, что при известном способе исследования злокачественного характера гистоцитологических препаратов облучают в оптическом диапазоне исследуемые образцы и определяют их спектр поглощения, при этом о злокачественном характере гуморальной среды судят по наличию в спектральной области 600-900 нм зоны антистоксовой люминесценции.
Устройство для осуществления способа, содержащее последовательно включенные источник излучения, монохроматор, коллимирующую трубку, блок интегрированного светового пучка, в котором также размещена кювета с исследуемой средой, приемник излучения и блок регистрации, дополнительно содержит последовательно соединенные измерительный преобразователь, блок сопряжения, формирователь управляющего сигнала, исполнительный элемент, выход которого механически соединен с монохроматором, а вход измерительного преобразователя соединен с выходом приемника излучения, причем вход-выход блока сопряжения соединен с входом-выходом блока регистрации.
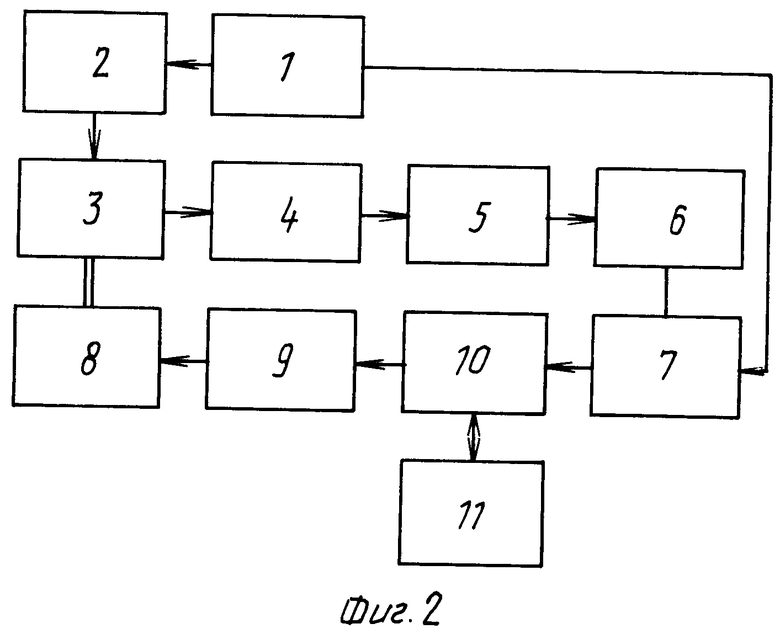
На фиг. 1 изображены спектры гуморальных образцов; на фиг. 2 структурная схема устройства для осуществления способа.
Устройство содержит источник питания 1, источник излучения 2, монохроматор 3, коллимирующую трубу 4, блок 5 интегрирования светового пучка, приемник излучения 6, измерительный преобразователь 7, выполняющий функцию аналого-цифрового преобразователя, исполнительный элемент 8 в виде шагового двигателя, вал которого механически соединен с монохроматором 3 для обеспечения изменения длины волны монохроматического излучения, формирователь управляющего сигнала 9 для исполнительного элемента двигателя 8, блок сопряжения 10 и блок регистрации 11. Кроме того, используется специальная кварцевая кювета, заполняемая исследуемым образцом.
На внутреннюю поверхность блока интегрирования светового пучка наносят окись магния до толщины 1 мм. Указанная толщина нанесенного слоя окиси магния обеспечивает коэффициент отражения около 98% во всем интервале длин волн (600-900 нм).
Реализация способа происходит следующим образом.
С помощью блока регистрации 11, выполненного в виде микропроцессорной системы на основе ЭВМ, формирователя управляющего сигнала 9 и шагового двигателя 8, выходное излучение монохроматора 3 выставляется на начальную длину волны 6000 нм. В центр блока 5 интегрирования светового пучка устанавливается пустая кювета. Монохроматический пучок света, попадая через коллимирующую трубу 4 на кювету и многократно отражаясь от стенок в интегрирующей полости блока 5 интегрирования светового пучка, интегрируется. Результирующий световой сигнал поступает на приемник излучения 6. Информация о величине электрического сигнала на выходе приемника излучения 6, поступающая через измерительный преобразователь 7 и блок сопряжения 10, запоминается в оперативной памяти блока регистрации 11 микропроцессорной системы. Далее посредством подачи сигнала на шаговый двигатель 8 через блок сопряжения 10 и формирователь управляющего сигнала 9 происходит изменение длины волны монохроматического излучения на предварительно заданное фиксированное значение Δ λ с последующим измерением и запоминанием электрического сигнала Х1(λ) на выходе приемника излучения 6. Данный процесс повторяется до достижения на выходе монохроматора 3 излучения с λ= 900 нм.
Затем вместо пустой кюветы в блок 5 интегрирования светового пучка устанавливается кювета с исследуемой жидкой средой и происходит последовательное изменение длины волны монохроматического излучения и регистрация электрического сигнала Х2(λ) на выходе приемника излучения 6 от λ 900 нм до λ= 600 нм при обратном вращении вала шагового двигателя в указанной последовательности.
Таким образом, изменяя длину волны λ монохроматического излучения и регистрируя электрические сигналы на выходе приемника излучения Х1(λ) и Х2(λ), получают объемный коэффициент поглощения исследуемой гуморальной среды
α(λ) 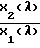 (1) а по нему определяют истинный спектральный показатель поглощения элементарного объема исследуемой гуморальной среды
(1) а по нему определяют истинный спектральный показатель поглощения элементарного объема исследуемой гуморальной среды
mλ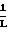 ln(1-α(λ) (2) где L толщина слоя исследуемого образца среды.
ln(1-α(λ) (2) где L толщина слоя исследуемого образца среды.
Анализ графического представления функции m  на фиг. 1 показывает существенные отличия в поглощении гуморальных сред (плазмы крови) онкобольных по сравнению с донорскими гуморальными средами в диапазоне 600-900 нм, а именно: жидкие гуморальные среды онкобольных имеют спектральную зону "отрицательного" поглощения, обусловленного, по-видимому, красным свечением (антистоксовой флюоресценцией) порфиринов.
на фиг. 1 показывает существенные отличия в поглощении гуморальных сред (плазмы крови) онкобольных по сравнению с донорскими гуморальными средами в диапазоне 600-900 нм, а именно: жидкие гуморальные среды онкобольных имеют спектральную зону "отрицательного" поглощения, обусловленного, по-видимому, красным свечением (антистоксовой флюоресценцией) порфиринов.
Для сравнения представлены спектры поглощения плазм крови донора Д-ч А. Г. А(П) Rh+, N 1682 и онкобольной Я-й С.П. А(П)Rh+, и.б. N 97 с диагнозом: рак тела матки инфильтративная форма П. Из анализа сравнительных характеристик следует, что поглощательная способность второго спектра во всей спектральной области (600-900 нм) меньше по сравнению с донорским. Более того, у него в указанной области наблюдается эффект "отрицательного" поглощения.
Отдельные блоки заявленного устройства могут быть выполнены следующим образом.
Блок 5 интегрирования светового пучка, коллимирующая труба 4, источник 2 и приемник 6 излучения могут конструктивно совпадать с известными, например авт. св. СССР N 1681204, кл. G 01 N 21/35, 1991).
Монохроматор 3 и исполнительный элемент 8 в виде шагового двигателя реализованы по известной схеме (см.Алексеев А.Б. Вилесов А.Ф. и др. Вакуумный монохроматор светосильный малогабаритный ВМС. Приборы и техника эксперимента, N 4, 1991, с.244).
Формирователь управляющего сигнала 9 реализован на основании рекомендации, приведенной в кн. Кенио Т. Шаговые двигатели и их микропроцессорные системы управления: Пер. с англ. М. Энергоатомиздат, 1987, с.119-136.
В качестве блока регистрации 11 может быть использована микроЭВМ IBM PC/AT.
Блок сопряжения 10 и измерительный преобразователь 7, представляющий собой аналого-цифровой преобразователь, могут быть выполнены по аналогии с известными устройствами. Сопряжение датчиков и устройств ввода данных с компьютерами IBM PC: пер. с англ./Под ред. У.Томпкинса Дж.Уэбстера. М. Мир, 1992, с.549-551.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ исследования гистоцитологических препаратов | 1989 |
|
SU1681204A1 |
| УСТРОЙСТВО ДЛЯ ОПРЕДЕЛЕНИЯ ВОДОРОДА В МЕТАЛЛАХ | 1992 |
|
RU2027165C1 |
| ОДНОПУЧКОВАЯ МИКРОСПЕКТРОСКОПИЯ КОГЕРЕНТНОГО КОМБИНАЦИОННОГО РАССЕЯНИЯ СВЕТА НА ОСНОВЕ ВОЛОКОННО-ОПТИЧЕСКОГО СИНТЕЗАТОРА УПРАВЛЯЕМЫХ ПОСЛЕДОВАТЕЛЬНОСТЕЙ СВЕРХКОРОТКИХ ИМПУЛЬСОВ | 2007 |
|
RU2360270C1 |
| УСТРОЙСТВО ДЛЯ ДИАГНОСТИКИ ДРАГОЦЕННЫХ КАМНЕЙ В СОСТАВЕ ЮВЕЛИРНЫХ ИЗДЕЛИЙ | 2021 |
|
RU2765213C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЛУБИНЫ ПРОНИКНОВЕНИЯ СВЕТА В КОЖУ И УСТРОЙСТВО ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2012 |
|
RU2521838C1 |
| МЕТОД И УСТРОЙСТВО ДЛЯ РЕГИСТРАЦИИ ИЗОБРАЖЕНИЙ ФАЗОВЫХ МИКРООБЪЕКТОВ В ПРОИЗВОЛЬНЫХ УЗКИХ СПЕКТРАЛЬНЫХ ИНТЕРВАЛАХ | 2016 |
|
RU2626061C1 |
| СПОСОБ ГАЗОВОГО АНАЛИЗА И ГАЗОАНАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2003 |
|
RU2235311C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ СПИРТА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2001 |
|
RU2207564C2 |
| СПОСОБ ОПТИЧЕСКИХ ИЗМЕРЕНИЙ ДЛЯ МАТЕРИАЛА | 2009 |
|
RU2423684C2 |
| СПОСОБ РЕГИСТРАЦИИ МУЛЬТИСПЕКТРАЛЬНОГО ЦИФРОВОГО ГОЛОГРАФИЧЕСКОГО ИЗОБРАЖЕНИЯ | 2019 |
|
RU2713567C1 |

Изобретение относится к области спектрофотометрических исследований в медицине. Сущность изобретения заключается в облучении гуморальных сред в оптическом диапазоне и определении их спектра поглощения. При этом о злокачественном характере исследуемой гуморальной среды судят по наличию в спектральной области 600-900 нм антистоксовой люминисценции. Для реализации изобретения используют спектрофотометрическое устройство, содержащее последовательно включенные источник излучения, монохроматор, коллиминирующую трубку, блок интегрирования светового пучка, в котором также размещена кювета с исследуемой средой, приемник излучения, блок регистрации, измерительный преобразователь, блок сопряжения, формирователь управляющего сигнала, исполнительный элемент, выход которого механически соединен с монохроматором, а вход измерительного преобразователя соединен с выходом приемника излучения, причем вход - выход блока сопряжения соединен с входом-выходом блока регистрации. 2 с. п. ф-лы, 2 ил.
| Способ исследования гистоцитологических препаратов | 1989 |
|
SU1681204A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1995-10-20—Публикация
1994-02-28—Подача