Описаны способ анализа, композиция для количественного определения общего содержания глюкозы в цельной неразбавленной крови и способ ее использования. Образец цельной неразбавленной крови вводят в контакт с композицией в сухой форме, включающей дегидрогеназу глюкозы (ДГГ), одно или несколько веществ из группы, состоящей из диафоразы, феназинметосульфата, феназинэтосульфата, феназинфеносульфата и мелдолового голубого; одно или несколько веществ из группы, состоящей из НАД (никотинамидный динуклеотид). НАДФ, тио-НАД, тио-НАДФ, никотинамидпуринового динуклеотида, никотинамид- метилпуринового динуклеотида, никотинамид-2-хлорметилпуринового динуклеотида; одного или нескольких гемолизирующих веществ, принадлежащих к группе, состоящей из фосфолипазы, гемолизирующих сапонинов и производных гидрофильных моно-, ди- или трисахаридов и алифатических углеводородов, содержащих 10-16 атомов углерода; окислительно-восстановительный индикатор-краситель и возможно дополнительно мутаротазу. Изменения цвета в ходе реакции неразбавленной цельной крови с указанным реактивом регистрируют методом спектрофотометрии (в режиме пропускания).
Изобретение относится к способу определения глюкозы, а более конкретно к количественному определению общего содержания глюкозы в цельной неразбавленной крови. Изобретение предусматривает также способ анализа, композицию и способ ее использования.
Определение содержания глюкозы в крови является важным рутинным анализом в клинической химии. Анализ этого типа используют для диагностики и терапии при диабетах и для диагностирования ряда других метаболических заболеваний. Известен ряд способов количественного определения общего содержания глюкозы в цельной неразбавленной крови.
Один из известных способов основан на ферментативном определении глюкозы с использованием дегидрогеназы глюкозы. Известная композиция для определения глюкозы включает буфер, пиридиновый коэнзим и дегидрогеназу глюкозы. Буфер имеет значение рН в пределах 7,9 9,0.
Известна также композиция для определения глюкозы, которая состоит главным образом из дегидрогеназы глюкозы, к которой предъявляют определенные требования в отношении чистоты и типа, пиридинового коэнзима, например, НАД (никотинамидный динуклеотид), буферной системы для поддержания определенного значения рН в водном растворе композиции (в пределах от 6,5 до 8,5) и мутаротазы. Однако ни в том, ни в другом случае не предусматривается способ или композиция, пригодная для прямого количественного определения общего содержания глюкозы в цельной неразбавленной крови, т.е. без стадии предварительного разбавления или осаждения.
Целью изобретения является разработка способа количественного определения общего содержания глюкозы в цельной неразбавленной крови с использованием спектрофотометрии в режиме пропускания, а также разработка сухой композиции для проведения указанного определения.
Изобретение, в частности, относится к определению общего содержания глюкозы в малых объемах цельной неразбавленной крови (в этом контексте "малый объем" относится к объемам 0,1 0,001 мл, предпочтительно 0,02 0,001 мл).
Согласно изобретению кровь не только не разбавляют, но и не подвергают никакой обработке. Осуществляют контактирование образца цельной неразбавленной крови объемом предпочтительно менее 20 мкл с реагентом в сухом виде, включающим:
дегидрогеназу глюкозы (ДГГ);
одно или несколько соединений из группы, состоящей из диафоразы, феназинметосульфата, феназинэтосульфата, феназинфеносульфата и мелдолового голубого;
одно или несколько соединений из группы, состоящей из НАД (никотинамидный динуклеотид), НАДФ, тио-НАД, тио-НАДФ, никотинамидпуринового динуклеотида, никотинамидметилпуринового динуклеотида, никотинамид-2-хлорметилпуринового динуклеотида;
одного или нескольких гемолизирующих веществ, принадлежащих к группе, состоящей из фосфолипазы, гемолизирующих сапонинов и производных гидрофильных моно-, ди- или трисахаридов и алифатических углеводородов, содержащих 10-16 атомов углерода
окислительно-восстановительный индикатор-краситель;
возможно дополнительно мутаротазу.
Регистрацию изменения окраски в ходе реакции указанного реагента с глюкозой в цельной неразбавленной крови проводят методом спектрофотометрии в режиме пропускания.
Предусматривается композиция для количественного определения общего содержания глюкозы в цельной неразбавленной крови, отличающаяся тем, что она существует в сухом виде и включает:
дегидрогеназу глюкозы (ДГГ);
одно или несколько соединений из группы, состоящей из диафоразы, феназинметосульфата, феназинэтосульфата, феназинфеносульфата и мелдолового голубого;
одно или несколько соединений из группы, состоящей из НАД (никотинамидный динуклеотид), НАДФ, тио-НАД, тио-НАДФ, никотинамидпуринового динуклеотида, никотинамидметилпуринового динуклеотида, никотинамид-2-хлорметилпуринового динуклеотида;
одного или нескольких гемолизирующих веществ, принадлежащих к группе, состоящей из фосфолипазы, гемолизирующих сапонинов и производных гидрофильных моно-, ди- или трисахаридов и алифатических углеводородов, содержащих 10-16 атомов углерода;
окислительно-восстановительный индикатор-краситель;
возможно дополнительно мутаротазу.
Предусматривается способ использования указанной композиции, отличающейся тем, что она включает:
дегидрогеназу глюкозы (ДГГ);
одно или несколько соединений из группы, состоящей из диафоразы, феназинметосульфата, феназинэтосульфата, феназинфеносульфата и мелдолового голубого;
одно или несколько соединений из группы, состоящей из НАД (никотинамидный динуклеотид), НАДФ, тио-НАД, тио-НАДФ, никотинамидпуринового динуклеотида, никотинамидметилпуринового динуклеотида, никотинамид-2-хлорметилпуринового динуклеотида;
одного или нескольких гемолизирующих веществ, принадлежащих к группе, состоящей из фосфолипазы, гемолизирующих сапонинов и производных гидрофильных моно-, ди- или трисахаридов и алифатических углеводородов, содержащих 10-16 атомов углерода;
окислительно-восстановительный индикатор-краситель;
возможно дополнительно мутаротазу; причем указанная композиция берется в сухом виде для количественного определения общего содержания глюкозы в цельной неразбавленной крови с использованием метода спектрофотометрии в пропускании.
Содержание различных компонентов в композиции согласно изобретению находится в приведенных пределах из расчета на образец цельной неразбавленной крови объемом 1 мл:
Дегидрогеназа глюкозы 5-500 ед.
активности
Диафораза или аналоги 1-100 ед.
активности
0,1-30 моль НАД и аналоги 1-100 моль
Фосфолипаза или аналоги 1-1000 ед.
активности/
0,5-70 мг Мутаротаза 0,1-100 ед.
активности
Окислительно-вос-
становительный индикатор-краситель 5-10 ммоль
К основной композиции можно добавлять различные компоненты, оптимизирующие реакционную функциональность при различных применениях. Мутаротазу можно использовать для быстрого перевода альфа-глюкозы и бета-глюкозы, которая и является той формой, которая реагируют с дегидрогеназой глюкозы. Этот вариант представляет особый интерес в том случае, когда анализу подлежит образец, не взятый непосредственно у пациента. Дегидрогеназа глюкозы обладает специфическим воздействием на распад бета-глюкозы. В водных растворах альфа- и бета-глюкоза существуют в равновесии, зависящем от температуры, которое устанавливается относительно медленно. Поскольку температура тела относительно постоянна, мутаротаза, которая ускоряет установленные равновесия, может быть исключена из состава реагента в том случае, когда образцы берут из крови, имеющей температуру тела. Помимо удешевления, преимущества подобного варианта заключаются в уменьшении времени реакции и расширении аналитического диапазона. Недостаток заключается в том, что растворы для калибровки и контрольные растворы должны быть доведены до определенной температуры, что занимает по меньшей мере один час.
К реактиву можно также добавлять вещества, обладающие эффектом стабилизации рН в определенном диапазоне, с целью проведения реакции в диапазоне рН, соответствующем активности ферментов.
К реактиву можно также добавлять вещества, воздействующие на растворимость и устойчивость композиции, что имеет смысл при определенных вариантах использования.
Дегидрогеназа глюкозы может быть получена из различных веществ, имеющих различную молекулярную массу, оптимумы рН и т.п. В данном случае под дегидрогеназой глюкозы понимаются только ферменты, включающие НАД (никотинамидный динуклеотид), или аналоги НАД-зависимые типы; в их число не входят такие типы, как кислород-зависимые и функционирующие с киноидными коэнзимами, которые также называют дегидрогеназами глюкозы.
Диафораза также может быть получена из различных веществ, однако ее можно заменить другими известными веществами, например феназинметосульфат, мелдоловый голубой и т.п. Известны также и другие аналоги НАД (никотинамидный динуклеотид), наиболее известным из числа которых является НАДФ, который может быть восстановлен посредством реакции глюкозы (дегидрогеназы глюкозы и может передать восстановление красителю или цветной системе.
Для облегчения смачивания поверхностей или для других вспомогательных нужд могут потребоваться поверхностно-активные вещества. Вещества, понижающие поверхностное напряжение, могут добавляться для облегчения покрытия гидрофобных поверхностей пластика.
Для адаптирования суспензий к различным типам покрытия оборудования можно изменять их вязкость посредством добавления подходящих высокомолекулярных полимеров. Выбор указанных высокомолекулярных полимеров не является критическим параметром, однако он влияет на скорость растворения сухого реактива. В числе применимых полимеров можно отметить полиэтиленгликоль, поливинилпирролидон, декстран и различные производные целлюлозы. Выбор полимеров также может быть осуществлен с целью стабилизации суспензии. Основываясь на известных способах получения композиций, применяемых, например, в пищевой или косметической промышленности, можно решить практически любые проблемы, связанные с адаптацией реагента к различным поверхностям.
Вещества, уменьшающие поверхностное напряжение, могут обладать также гемолитическим эффектом, как это имеет место, например, в случае деканоил-N-метилглюкамида. Этот факт хорошо известен и, следовательно, можно использовать множество различных комбинаций таких веществ. Существуют также гемолизирующие вещества, котоpые не обладают особой поверхностной активностью, например меллитин и фосфолипазы.
Известны также некоторые типы веществ, изменяющих цвет, которые могут менять цвет при воздействии НАДФ и диафоразы. Предпочтительными являются пpоизводные тетразола, поскольку краситель формазан необратимо образуется при нормальных реакционных условиях. Хорошие результате дает использование в композициях 3-(4,5-диметилтиазол-2-ил)-2,5- дифенил-2Н-тетразолийбромида (ММТ), однако можно использовать и другие производные тетразола. Следует отметить, что группа гемолизирующих соединений содержит только такие вещества, которые не дают нежелательных осадков при взаимодействии с производными тетразола.
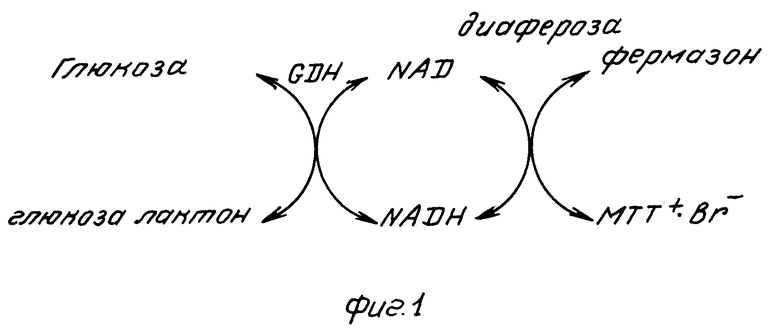
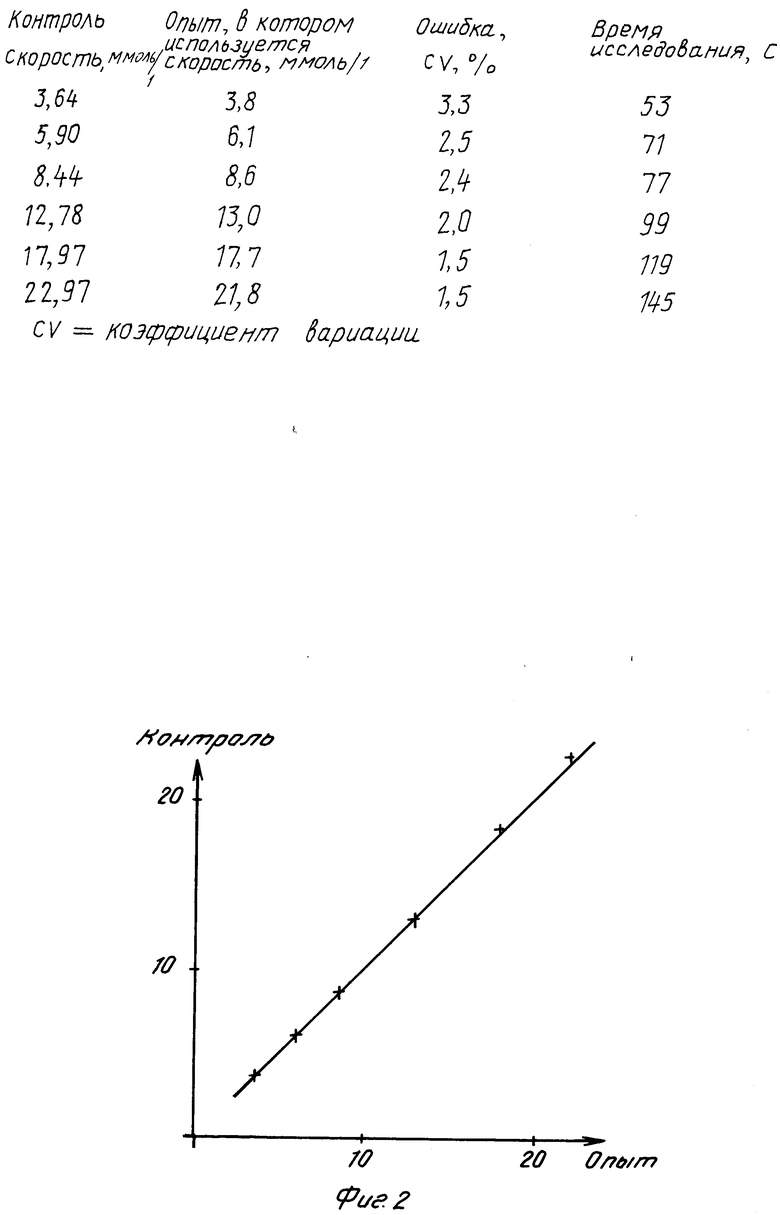
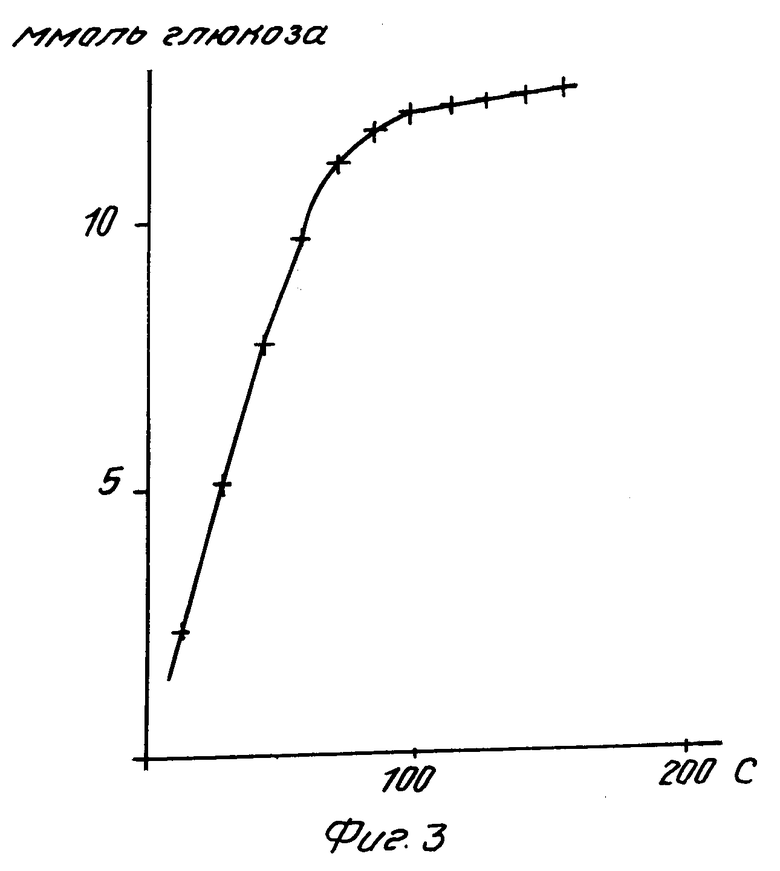
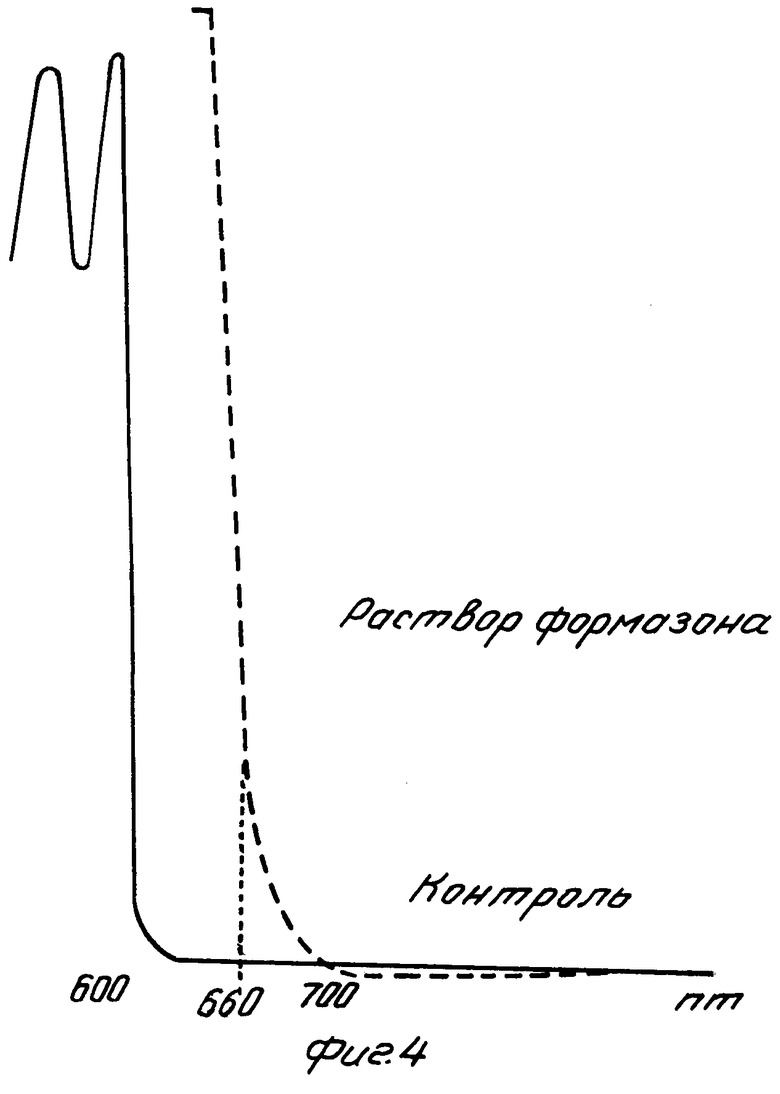
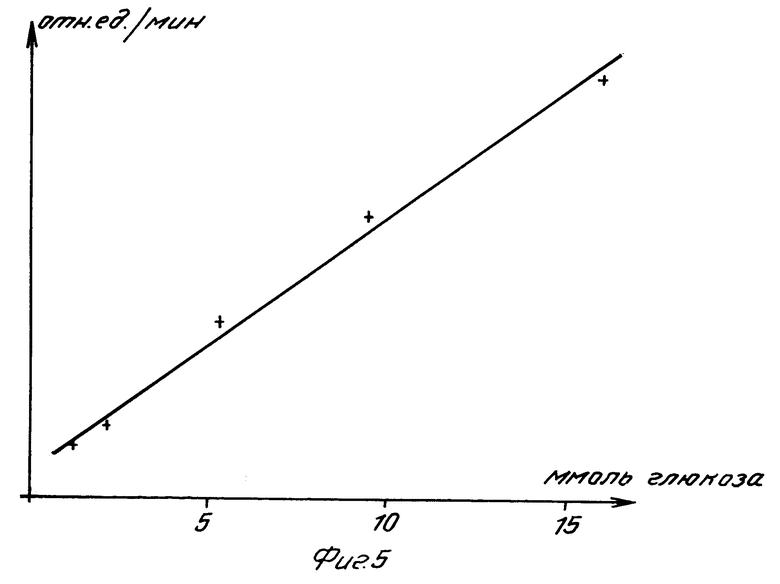
На фиг.1 схематически изображена реакция и формулы соединений; на фиг.2 диаграмма, иллюстрирующая распределение и корреляцию со сравнительным методом и статистической обработкой для определения методом "конечной точки"; на фиг. 3 график для определения "конечной точки"; на фиг.4 спектры гемоглобина и МТТ-формазана, спектр сравнения и длины волн; на фиг.5 диаграмма, иллюстрирующая корреляцию со сравнительным методом в кинетических исследованиях.
Измерения проводят на образцах целой крови, приготовленных с глюкозой с целью получения различных уровней содержания глюкозы. Сравнительный метод представляет собой тестовую систему фирмы "Мерк". На основе дегидрогеназы глюкозы (метод Глюк DH(R), тип 13 886, 13 887). В случае указанного сравнительного метода спектроскопическое определение проводят в УФ-области спектра при 340 нм в соответствии с прилагаемой к набору для тестирования инструкцией. Сравнительный способ является химическим аналитическим способом влажного типа.
П р и м е р 1. Количество композиции реагента 1 мл.
100 ед. активности дегидрогеназы глюкозы (продукт фирмы "Мерк").
20 ед. активности диафоразы (продукт фирмы "Мерк").
22 ммоль НАД (продукт фирмы "Мерк").
30 ммоль МТТ (продукт фирма "Мерк").
25 мг белого сапонина (продукт фирмы "БДН").
5 мг деканоил-N-метилглюкамида.
1 мл воды (после ионообменной обработки).
В результате получают раствор, который пригоден для сушки с замораживанием в микрокюветах, полученных методом инжекционного формования, которые являются промышленным продуктом фирмы "ГемоКуз-АВ". При этом достигается хорошая воспроизводимость и линейность (см. фиг.2). Измерения проводят при 660 нм, используя для сравнения длину волны 880 нм, проводят измерения по методу "конечной точки".
П р и м е р 2. Количество композиции реагента 1 мл.
1000 ед. активности дегидрогеназы глюкозы (продукт фирмы "Мерк").
200 ед. активности диафоразы (продукт фирмы "Мерк").
220 ммоль НАД (продукт фирмы "Мерк").
0,3 ммоль МТТ (продукт фирмы "Мерк").
250 мг белого сапонина (Р) (продукт фирмы "БДН")
50 мг Плюроник Р-85(Р) (продукт фирмы "Серва").
250 мл воды (после ионообменной обработки).
Компоненты композиции мелко измельчают для получения суспензии, пригодной для покрытия поверхностей посредством различных способов печати, например печати на шелке, печати с применением печатных цилиндров и т.д. Данный тип суспензии пригоден для микрокювет с покрытием разделяемого типа.
П р и м е р 3. Микрокюветы, изготовленные из ацетата целлюлозы бутирата целлюлозы глубиной примерно 0,15 мм, покрывают композицией реагента согласно примеру 2 посредством печатного устройства (4 печатных цикла). После сушки и сборки изучалось функционирование кювет для анализа различных образцов целой крови. Гемолиз определяли при длине волны 660 нм; время измерения в пределах 20 40 с, в зависимости от количества эритроцитов. Образование окрашивания изучалось при той же длине волны; для образцов целой крови с концентрацией глюкозы около 12 ммоль/л конечная точка удовлетворительная с точки зрения методики измерений, достигается примерно через 1,5 мин (см. фиг.3). На фиг.4 приведен спектр гемоглобина и спектр красителя для образца целой крови концентрацией глюкозы около 12 ммоль/л в кювете согласно примеру 3. Очевидно, что в этом случае имеются хорошие возможности для измерения образовавшегося формазанового окрашивания без какого-либо нежелательного перекрывания с гемоглобином; имеется также возможность изменения мутности для общей фоновой компенсации вне указанных спектров. В результате изменения толщины покрытия естественно в некоторой степени изменяются время реакции, а также максимальные определяемые концентрации.
П р и м е р 4. Количество композиции реагента 1 мл.
25 ед. активности дегидрогеназы глюкозы с максимальным количеством связанного с ней метилового простого эфира полиэтиленгликольальдегида (750) (продукт фирмы "Мерк") 5 ед. активности диафоразы (продукт фирмы "Мерк").
7 ммоль НАД (продукт фирмы "Мерк").
20 ммоль МТТ (продукт фирмы "Мерк").
25 мг белого сапонина (Р) (продукт фирмы "БДН").
1 мл воды (после ионообменной обработки).
Таким способом получают раствоp, пригодный для сушки при замораживании аналогично примеру 1. Реагент подготавливают для кинетических исследований в противоположность предшествующим примерам, где предусматривалось определение по конечной точке. Относительное большое количество дегидрогеназы глюкозы связано с активностью восстановления, происходящего при сшивке молекул полимера. Сшивка молекул полимера с ферментом увеличивает устойчивость, что является хорошо известным фактом и желательным условием для проведения кинетических измерений. Подбор оптимального типа полимера не производился; данный пример предназначен лишь для иллюстрации возможности использования подобных полимеров. Монометиловый эфир полиэтиленгликоля переводят в альдегид посредством реакции с диметилсульфоксидом и уксусным ангидридом. После связывания с дегидрогеназой глюкозы в хлориде натрия с карбонатным буфером при рН 10 и наличии избытка полимера смесь диализуют и концентрируют. Комплекс фермент-полимер обладает лучшей устойчивостью по сравнению с чистым ферментом. Примеры результатов, полученных из кинетических измерений с реагентом согласно данному примеру, приведены на фиг.5. Измерения проводят при 660 нм в течение 3-3,75 мин при длине волны сравнения 880 нм.
Использование: медицина, для определения глюкозы в цельной крови. Сущность изобретения: образец цельной неразбавленной крови вводят в контакт с композицией в сухой форме, включающий дегидрогеназу глюкозы (ДГГ), одно или несколько веществ из группы, состоящей из диафоразы, феназинметосульфата, феназинэтосульфата, феназинфеносульфата и мелдолового голубого; одно или несколько веществ из группы, состоящей из НАД (никотинамидный динуклеотид), НАДФ, тио-НАД, тио-НАДФ, никотинамидпуринового динуклеотида, никотинамидметитлпуринового динуклеотида, никотинамид-2-хлорметитлпуринового динуклетида; одного или нескольких гемолизирующих веществ, принадлежащих к группе, состоящей из фосфолипазы, гемолизирующих сапонинов и производных гидрофильных моно-, ди- или трисахаридов и алифатических углеводородов, содержащих 10 16 атомов углерода; окислительно-восстановительный индикатор-краситель и возможно дополнительно мутаротазу. Изменения цвета в ходе реакции неразбавленной цельной крови с указанным реактивом регистрируют методом спектрофотометрии (в режимер пропускания). 2 с. и 5 з. п. ф-лы, 5 ил.
дегидрогеназу глюкозы (ДГГ);
одно или несколько соединений из группы, состоящей из диафоразы, феназинметосульфата, феназинэтосульфата, феназинфеносульфата и мелдолового голубого;
одно или несколько соединений из группы, состоящей из НАД (никотинамидный динуклеотид), НАДФ, тио-НАД, тио-НАДФ, никотинамидпуринового динуклеотида, никотинамидметилпуринового динуклеотида, никотинамид-2-хлорметилпуринового динуклеотида;
одного или нескольких гемолизирующих веществ, принадлежащих к группе, состоящей из фосфолипазы, гемолизирующих сапонинов и производных гидрофильных моно-, ди- или трисахаридов и алифатических углеводородов, содержащих 10-16 атомов углерода;
окислительно-восстановительный индикатор-краситель,
и, возможно, дополнительно мутаротазу.
5-500 ед. дегидрогеназы глюкозы,
1-100 ед. диафоразы/аналогов,
1-100 ммоль НАД/аналогов,
1-1000 ед. фосфолипазы/аналогов,
1-10 ед. мутаротазы,
5-100 ммоль красителя-индикатора окислителя-восстановителя из расчета на образец цельной неразбавленной крови объемом в 1 мл.
| Патент США N 4120755, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1995-12-20—Публикация
1990-04-24—Подача