Изобретение относится к способам умягчения жесткой воды и можетбыть использовано в домашних условиях для питьевых и пищевых целей.
Кроме того, данный способ может быть использован на предприятиях пищевой промышленности и т.д.
Известен способ умягчения жесткой воды, в котором на первой стадии используют соединения кальция, например гидроокись кальция, а на второй стадии используют NaOH и (или) Na2CO3 [1, 2]
Недостатком известного способа является непригодность данного способа для пищевых целей и его сравнительная длительность.
Известен способ умягчения воды для пищевых целей, заключающийся в использовании на первой стадии умягчения соединений кальция, на второй - соединений KOH и K2CO3, отстаивании и отделении осадка, нейтрализации умягченной воды пищевой, например, ортофосфорной кислотой [3]
Недостатками способа являются его сравнительная сложность и длительность, что делает его практически невыгодным для использования в домашних условиях.
Целью изобретения является его упрощение и интенсификация процесса умягчения воды, что позволит использовать этот способ в домашних условиях.
Это достигается тем, что в способе умягчения воды путем введения в нее соединений K2CO3 и KOH, отстаивания осадка, отделения отстоявшейся воды и нейтрализации умягченной воды с помощью пищевой, например, фосфорной кислоты до pH≅9, в отличии от прототипа едкий калий и углекислый калий используют в весовом соотношении (0,1-1): (0,9-1) и в количестве, определяемом зависимостью (20-70)•(Жобщ-Жост), где Жобщ общая жесткость воды в мг-эквивалентах на 1 л воды, а Жост требуемая остаточная общая жесткость воды в мг-эквивалентах на 1 л воды, при этом умягчаемую воду перед введением соединений калия нагревают до 50-70oC, затем воду с добавкой доводят до кипения и кипятят ≅3 мин.
В известном способе при использовании для умягчения воды окиси кальция и углекислого калия их вводить одновременно нельзя, так как происходит их взаимная реакция с образованием мела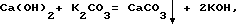
в результате чего происходит нерациональная трата реагентов. Поэтому требуется раздельное введение компонентов, приводящее к значительным затратам времени.
Кроме того, передозировка Ca(OH)2 приводит к дополнительному увеличению жесткости воды, поэтому применение Ca(OH)2 требует очень тщательного анализа воды и точной дозировки этого компонента. Все это вместе взятое усложняет способ и делает его использование в домашних условиях непригодным.
В предлагаемом способе использование смеси едкого калия и углекислого калия позволяет одновременно производить устранение и временной, и постоянной жесткости, так как эти вещества не могут взаимодействовать друг с другом, а каждое выполняет свои функции, поэтому обработка воды значительно ускоряется.
Использование этой смеси не может привести к дополнительному увеличению жесткости, а некоторая передозировка того или иного компонента не страшна, так как избыточная щелочность воды устраняется с помощью пищевой кислоты, например фосфорной, наряду с которой могут быть использованы другие кислоты (например, лимонная).
Содержание иона калия в питьевой воде допускается в количестве до 2000 мг/л [4] При этом следует отметить, что предлагаемый способ не создает возможности получения даже в очень жесткой воде (до 40 мг/л) подобной концентрации калия.
Использование едкого калия и углекислого калия в соотношении (0,1-1): (0,9-1) определяется различными характеристиками жесткости и состава воды в разных источниках.
Так, например, при наличии только временной жесткости и жесткости, определяемой свободным CO2, а также соединениями магния, достаточно использовать только едкий калий.
Если вода имеет только постоянную жесткость, можно использовать для ее умягчения один углекислый калий.
Кроме таких крайних случаев использование отдельно едкого калия или углекислого калия возможно и в тех случаях, когда параметры воды позволяют при использовании только одного из указанных компонентов оставлять остаточную общую жесткость в пределах 3-4 мг-экв./л (независимо от того, какими соединениями она определяется).
При наличии как временной, так и постоянной жесткости воды, необходимо использовать смесь реагентов (имеется в виду смесь гидроокиси калия и углекислого калия). Их весовое соотношение необходимо определять отдельно для каждого конкретного источника воды с учетом колебаний жесткости воды и ее среднегодовой величины.
Использование едкого калия и углекислого калия в количестве (20-70)•(Жобщ- Жост) определяется также различным составом и широкими интервалами соотношений временной и постоянной жесткости воды, а также необходимостью быстрого умягчения воды, имеющей общую жесткость в пределах от 10 до 40 мг-экв./л.
Так, например, для быстрого умягчения воды с жесткостью 10-20 мг-экв./л достаточно использовать указанные вещества в количествах (20-40)•(Жобщ Жост), а при более высокой жесткости требуется (40-70)•(Жобщ- Жост). Предварительный нагрев воды до температуры 50-70oC позволяет интенсифицировать процесс умягчения воды.
При нагревании воды до температуры <50oC процесс умягчения идет медленнее, а при температуре >70oC при умягчении очень жесткой воды определенного состава возможен выброс части жесткости из сосуда из-за быстрого образования в воде большого количества хлопьев и пены.
Последующее доведение воды до кипячения и кипячение в течение до трех минут позволяет довести жесткость умягчаемой воды за это время до требуемой величины.
Анализы воды, умягченной по предлагаемому способу, показывают, что уже через 5 мин после окончания кипячения (5 мин требуется на подготовку пробы к анализу и, соответственно, анализ) жесткость воды снижается до заданной величины.
При этом очень жесткую воду с высокой постоянной жесткостью кипятить нельзя, так она дает много пены, а воду более мягкую можно и достаточно кипятить до 3 мин.
В настоящее время вода во многих регионах страны по жесткости не удовлетворяет требованиям ГОСТа. Решить проблему в масштабах города (даже сравнительно небольшого) при водопотреблении 250 300 л в сутки на человека очень сложно и дорого.
В то же время потребность в питьевой воде на человека составляет 2,5-3 л в день. Умягчение такого количества воды в домашних условиях сравнительно просто осуществимо. Для этого централизованно (для данного конкретного источника воды) готовят концентрат, содержащий соединения калия в таком соотношении и такой концентрации, чтобы умягчить воду до остаточной жесткости, например 3-5 мг-экв./л при добавлении, например, 1 столовой ложки концентрата на три литра подогретой воды с последующим ее кипячением и отстаиванием осадка. Отстаивание осадка происходит очень интенсивно (за 5-10 мин). Осветленную воду сливают декантацией, а оставшуюся воду с осадком отфильтровывают через 1 слой тканевого (например, ситцевого) фильтра. После отделения умягченной воды от осадка к ней добавляют (если в этом будет необходимость) раствор фосфорной или лимонной кислоты.
Концентрат должен быть изготовлен таким образом, чтобы была исключена возможность его передозировки в воду (следовательно, необходимо учесть среднегодовое колебание величины общей жесткости), т.е. его введение в воду не должно снижать ее жесткость ниже, например, 2-2,5 мг-экв./л при минимальном статистическом значении общей жесткости в данном водном источнике.
pH воды в домашних условиях можно определять с помощью универсальной индикаторной бумаги (pH бумага реахим), позволяющей мгновенно определить pH в интервале от 1 до 10. Кроме того, можно воспользоваться органолептическим методом и определять щелочность воды на вкус (при правильной дозировке концентрата и пищевой кислоты вкус обработанной воды не должен отличаться от вкуса мягкой природной воды).
По существующему ГОСТу на воду (ГОСТ 2877-82) pH питьевой воды допустимо в пределах 6,0-9,0, содержание калия в воде и сверхмалое содержание фосфора не ухудшают ее пищевой ценности. Следует отметить, что эти вещества требуются человеческому организму, поэтому в последнее время специально выпускаются препараты, содержащие наряду с витаминами минеральные добавки, в том числе и фосфор (фосфаты) (см. например, поливитаминный препарат "Супрадин Рош", в котором в одной таблетке содержание фосфора составляет 23,8 мг, а содержание кальция 51,3 мг).
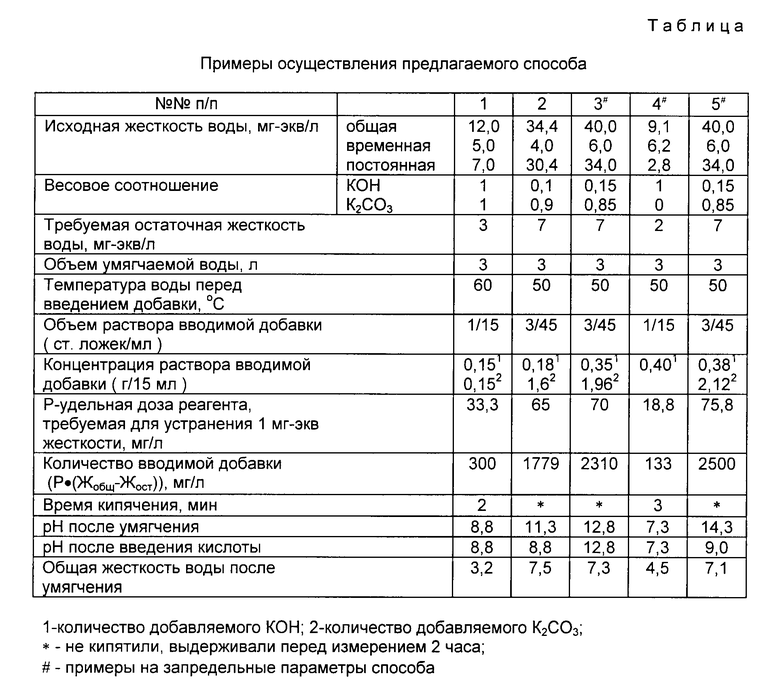
Предлагаемый способ позволяет сравнительно дешево и быстро умягчать воду в домашних условиях не только для пищевых целей, но и для мытья головы, стирки и т.д. (см. таблицу).
При этом резко (не менее, чем в два раза) сокращается расход моющих средств и стиральных порошков, что приносит эколого-экономическую выгоду.
Осадок, образуемый при умягчении воды, не загрязняет природу и может быть использован в качестве удобрения, так как содержит CaCO3, MgCO3, Mg(OH)2, калий.
Источники информации.
1. Краткий справочник химика. Составитель В.И.Перельман, издание 6, Государственное научно-техническое издательство химической литературы, М. 1963, с. 366 370.
2. Ф.И.Белан. Водоподготовка. М. Энергия, 1979.
3. Заявка на патент "Способ умягчения воды" авторов Тарханова О.В. и др. N 93042332 от 25.08.93. (Входящий N 042574/Ла).
4. Я.М.Грушко. Вредные неорганические соединения в промышленных сточных водах. Л. Химия, Ленинградское отделение, 1979, с. 58.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ УМЯГЧЕНИЯ ВОДЫ | 1993 |
|
RU2106316C1 |
| СПОСОБ УМЯГЧЕНИЯ ВОДЫ | 1995 |
|
RU2114072C1 |
| СОСТАВ ДЛЯ УМЯГЧЕНИЯ ВОДЫ | 1994 |
|
RU2109694C1 |
| СОСТАВ ДЛЯ УМЯГЧЕНИЯ ВОДЫ (ВАРИАНТЫ) | 1994 |
|
RU2090521C1 |
| СОСТАВ ДЛЯ УМЯГЧЕНИЯ ВОДЫ | 1994 |
|
RU2093479C1 |
| СПОСОБ УМЯГЧЕНИЯ ВОДЫ ЗАМОРАЖИВАНИЕМ | 2002 |
|
RU2225847C2 |
| СОСТАВ ДЛЯ УМЯГЧЕНИЯ ВОДЫ | 1995 |
|
RU2100293C1 |
| СПОСОБ УМЯГЧЕНИЯ ВОДЫ | 1997 |
|
RU2151746C1 |
| СПОСОБ УМЯГЧЕНИЯ ВОДЫ ОТ СОЛЕЙ ЖЕСТКОСТИ | 2011 |
|
RU2462422C1 |
| Способ умягчения воды | 1979 |
|
SU842034A1 |
Использование: умягчение жесткой воды в домашних условиях для питьевых и пищевых целей. Сущность изобретения: воду обрабатывают соединениями едкого калия и углекислого калия, осадок отстаивают, отделяют умягченную воду и нейтрализуют с помощью пищевой, например фосфорной кислоты. Едкий калий и углекислый калий используют в весовом соотношении (0,1-1):(0,9-1). Количество вводимых добавок определяют зависимостью (20-70)•(Жобщ - Жост), где Жобщ - общая жесткость воды в мг-экв./л, а Жост - требуемая остаточная общая жесткость воды в мг-экв./л. Умягчаемую воду доводят до кипения и кипятят не более 3 мин. 4 з.п. ф-лы, 1 табл.
(20 70)•(Жобщ Жост),
где Жобщ общая жесткость воды, ммоль/л;
Жост требуемая остаточная жесткость воды, ммоль/л.
| Белан Ф.И | |||
| Водоподготовка | |||
| - М.: Энергия, 1979, с | |||
| Халат для профессиональных целей | 1918 |
|
SU134A1 |
Авторы
Даты
1997-09-27—Публикация
1993-12-24—Подача