Изобретение относится к новым производным ненасыщенных 17бета-замещенных 3-карбоксистероидов, к способу их получения, к фармацевтическим композициям, их содержащим, и к использованию вышеназванных соединений в качестве ингибиторов андрогенной активности путем подавления тестестерон-5α-редуктазы.
На определенные ткани, реагирующие на андрогены, действие тестостерона передается главным образом через его метаболит, восстановленный в положении 5α - дигидротестостерон (ДГТ) (Bruchowsky N., Wilson J. D.; j. Biol Chem. 243, 5953, 1968).
Превращение тестостерона в дигидротестостерон катализируется ферментом 5α-редуктазой и, если действие 5α-редуктазы подавляется, образование дигидротестостерона снижается и снижается или предотвращается его специфическое эндрогенное действие.
Ингибиторы 5α-редуктазы могут найти медицинское применение при лечении состояний, связанных с гиперпродукцией мужских половых гормонов, например при определенных заболеваниях простаты, таких, как доброкачественная гиперплазия простаты и рак простаты, и определенных состояниях кожи и волосяного покрова, таких, как акне, себоррея, гирсутизм у женщин и характерное для мужчин облысение (Siiteri P. K. , wilson j. D., J. Chin. Invest. 49, 1737, 1970; Price V. A. Arch. Dermatol. III., 1496, 1975; Sandferg A.A., Urology 17, 34, 1981).
Использование ингибиторов 5α-редуктазы также может быть полезно при лечении рака молочных желез, так как этот вид опухоли прогрессирует, как известно, в присутствии андрогенов. Андрост-4-ен-3-ов-17β-карбоновая кислота и ее метиловый эфир являются одними из первых стероидных соединений, описанных как ингибиторы 5α-редуктазы (Voigt and Hsia, Endocrinology, 92, 1216 (1973); Canadian Patent No. 970, 692).
Два 5,10-секостероида, имеющие 3-кето-4,5-диеновую систему в расширенном кольце, как было обнаружено, являются селективными ингибиторами эпидимической 5α-редуктазы крыс (Robaire et. al.).
Как сообщалось, (20R)-4-диазо-21-гидрокси-2О-метил-5αпрегнан-3-он и его аналоги являются ферментативно активируемыми ингибиторами тестостерон-5α-редуктазы (Blohm et. al., Biochem. Biophys. Res. Comm. 95, 273-80, 1980; US Patent 4.317.817).
Новые серии энзим-управляемых необратимых ингибиторов 5α-редуктазы были получены введением 6-метиленовой замещающей группы в субстраты типа 3-кето-Δ4-прогестинов и андрогенов (Petrow at. al., Steroids 38, 352-53, 1981; United States Patent 4.396.615).
Совсем недавно было сообщено, что 4-азастероиды также являются ингибиторами стероидной 5α-редуктазы (Liang et. al., J. steroid. Biochem. 19, 385-90, 1983; United States Patent 4.377.584 опубликованный European Patent Appl. no. 155096).
И наконец, сообщалось, что ненасыщенные производные 3-карбоксистероидов тоже являются неконкурентными ингибиторами 5α-редуктазы тестостерона (Biolog. Chem. 17, 372-376, 1989; Eur. Pat. Appl. no 0289327).
Изобретение представляет новые производные ненасыщенных 17β-замещенных 3-карбоксистероидов, имеющих следующую формулу: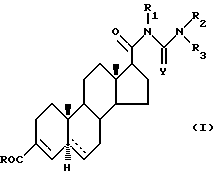
где Y - кислород или сера;
R - группа:
а) -OR4, где R4 - водород или C1-C6 алкильная группа, или
б)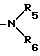 , где каждый из R5 и R6 независимо являются или C1-C6-алкильной группой;
, где каждый из R5 и R6 независимо являются или C1-C6-алкильной группой;
с) 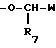 , где R7 - водород или C1-C6 алкильная группа; W является группой:
, где R7 - водород или C1-C6 алкильная группа; W является группой:
(I) 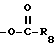 , где R8 - C1-C6 алкильная группа, C5-C6 циклоалкильная группа, C6-C9-циклоалкилалкильная группа, фенильная группа или бензильная группа;
, где R8 - C1-C6 алкильная группа, C5-C6 циклоалкильная группа, C6-C9-циклоалкилалкильная группа, фенильная группа или бензильная группа;
(II) 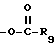 , где R9 - C1-C6-алкильная группа или C5-C6 циклоалкильная группа; или
, где R9 - C1-C6-алкильная группа или C5-C6 циклоалкильная группа; или
(III) 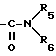 , где R5 и R6 определены выше; или
, где R5 и R6 определены выше; или
д) 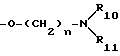 , где каждый из R10 и R11 является независимо водородом или C1-C6 алкильной группой или оба радикала вместе с атомом азота, с которым они связаны, образуют насыщенное гетеромоноциклическое кольцо с 5-ю или 6-ю членами, возможно содержащее по крайней мере один дополнительный гетероатом, выбранный из кислорода и азота; n - целое число 2-4; R1 - водород, C1-C6 алкильная группа, C5-C6- циклоалкильная группа, C6-C9 циклоалкилалкильная группа или арильная группа;
, где каждый из R10 и R11 является независимо водородом или C1-C6 алкильной группой или оба радикала вместе с атомом азота, с которым они связаны, образуют насыщенное гетеромоноциклическое кольцо с 5-ю или 6-ю членами, возможно содержащее по крайней мере один дополнительный гетероатом, выбранный из кислорода и азота; n - целое число 2-4; R1 - водород, C1-C6 алкильная группа, C5-C6- циклоалкильная группа, C6-C9 циклоалкилалкильная группа или арильная группа;
каждый из C2 и C3 независимо выбраны из группы, состоящей из водорода, C1-C6-алкила, C5-C6-циклоалкила, C6-C9-циклоалкилалкила и арила, или R2 и R3, взятые вместе с азотом, с которым они связаны, образуют 5- или 6-членное насыщенное гетеромоноциклическое кольцо, возможно содержащее по крайней мере один дополнительный гетероатом, выбранный из кислорода и азота, символ 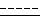 обозначает одинарную или двойную связь при условии, что, когда это двойная связь, водород в 5α-положении отсутствует.
обозначает одинарную или двойную связь при условии, что, когда это двойная связь, водород в 5α-положении отсутствует.
В формулах этого описания линия из точек ("""") показывает заместитель в α конфигурации, т. е. ниже плоскости кольца, а клиновидная линия  обозначает заместитель в β-конфигурации, т.е. выше плоскости кольца.
обозначает заместитель в β-конфигурации, т.е. выше плоскости кольца.
Изобретение включает также фармацевтически применимые соли соединения и формулы I, так же, как и все возможные изомеры формулы I и их смеси.
Кроме того, метаболиты и матаболические предшественники соединений формулы I включаются в объем изобретения.
В этом описании алкильные группы и алкильный заместитель циклоалкильных групп может быть с прямой или разветвленной цепью, а C1-C6 алкильная группа может быть, например, метилом, этилом, изопропилом, н-бутилом, трет-бутилом или трет-бутилметилом (т.е. неопентилом).
C5-C6-циклоалкильная группа является циклопентилом или циклогексилом, предпочтительно циклогексилом.
C6-C9-циклоалкилалкильная группа может быть, например, циклогексилметилом.
Арильная группа может быть, например, фенилом или бензилом.
Когда R является группой -OR4, как определено выше, предпочтительно R4 - водород, метил или этил, наиболее предпочтительно водород;
Когда R является группой 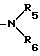 , как определено выше, предпочтительно каждый из R5 и R6 - независимо метил или этил.
, как определено выше, предпочтительно каждый из R5 и R6 - независимо метил или этил.
Когда R является группой 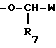 , R7 - предпочтительно водород или метил.
, R7 - предпочтительно водород или метил.
Когда W является группой 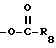 , R8 - предпочтительно метил, этил, пропил, н-бутил, т-бутил, циклогексилметил, фенил или бензил.
, R8 - предпочтительно метил, этил, пропил, н-бутил, т-бутил, циклогексилметил, фенил или бензил.
Когда W является группой 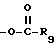 , R9 - предпочтительно метил, этил, н-пропил или циклогексил.
, R9 - предпочтительно метил, этил, н-пропил или циклогексил.
Когда W является группой 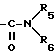 , предпочтительно каждый из R5 и R6 - независимо метил или этил.
, предпочтительно каждый из R5 и R6 - независимо метил или этил.
Когда R является группой 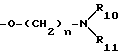 , предпочтительно каждый из R10 и R11 - независимо водород, метил, этил, пропил, изопропил или, когда R10 и R11 вместе с атомом азота, с которым они связаны, образуют пентатомное или гексатомное насыщенное гетеромоноциклическое кольцо, как определено выше, группа
, предпочтительно каждый из R10 и R11 - независимо водород, метил, этил, пропил, изопропил или, когда R10 и R11 вместе с атомом азота, с которым они связаны, образуют пентатомное или гексатомное насыщенное гетеромоноциклическое кольцо, как определено выше, группа 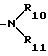 предпочтительно представляет собой
предпочтительно представляет собой 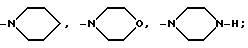 n - предпочтительно 2, 3.
n - предпочтительно 2, 3.
R1 - предпочтительно метил, этил, изопропил, терт-бутил, циклогексил или циклогексилметил.
Предпочтительно каждый из R2 и R3 - независимо водород, метил, этил, изопропил, т-бутил, циклогексил, циклогексилметил фенил, или, когда R2 и R3 вместе с атомом азота, с которым они связаны, образуют 5- или 6-членное насыщенное гетеромоноциклическое кольцо, как определено выше, группа предпочтительно представляет собой 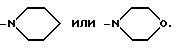
Фармацевтически приемлемые соли соединений этого изобретения - это соли фармацевтически приемлемых оснований, или неорганических оснований, таких, как, например, щелочного металла, например натрия или калия, или щелочно-земельных металлов, например кальция или магния, или цинка или алюминия гидроксидов; или органических оснований, таких, как, например, алифатические амины, например метиламин, триметиламин, этиламин, и гетероциклические амины, например пиперидин.
Предпочтительным классом соединений в соответствии с этим изобретением являются соединения формулы I, где Y - кислород или сера;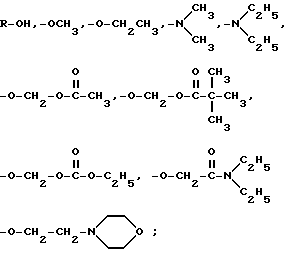
R1 - метил, этил, изопропил, трет-бутил, циклогексил; группа 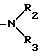 представляет собой
представляет собой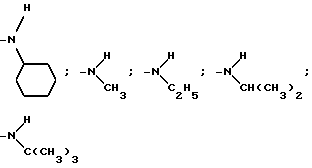
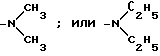
символ 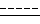 обозначает одинарную или двойную связь, и фармацевтически приемлемые их соли.
обозначает одинарную или двойную связь, и фармацевтически приемлемые их соли.
Примерами специфических соединений, предпочитаемых в рамках этого изобретения являются:
17β-[N-изопропил-N-(N-изопропилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоновая кислота;
17β-[N-циклогексил-N-(N-циклогексилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоновая кислота;
17β-[N-третбутил-N-(N-трет-бутилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоновая кислота;
17β-[N-изопропил-N-(N-изопропилтиокарбамоил)карбамоил] андроста-3,5-диен-3-карбоновая кислота;
17β-[N-циклогексил-N-(N-циклогексилтиокарбамоил)карбамоил] андроста-3,5-диен-3-карбоновая кислота;
17β-[N-метил-N-(N-диэтилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоновая кислота;
метил-17β-[N-изопропил-N-(N-изопропилтиокарбамоил)карбамоил] андроста-3,5-диен-3-карбоксилат;
метил-17β-[N-изопропил-N-(N-изопропилтиокарбамоил)карбамоил] андроста-3,5-диен-3-карбоксилат;
метил-17β-[N-циклогексил-N-(N-циклогексилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоксилат;
метил-17β-[N-циклогексил-N-(N -циклогексилтиокарбамоил)карбамоил] андроста-3,5-диен-3-карбоксилат;
метил-17β-[N-трет-бутил-N-(N-трет-бутилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоксилат;
метил-17β-[N-метил-N-(N, N-диэтилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоксилат;
N, N-диэтил-17β-[N-изопропил-N-(N -изопропилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоксамид;
N, N-диэтил-17β-[N-изопропил-N-(N-изопропилтиокарбамоил)карбамоил] андроста-3,5-диен-карбоксамид;
N, N-диэтил-17β-[N-циклогексил-N-(N-циклогексилкарбамоил)карбамоил] андроста-3,5-диен-карбоксамид;
N, N-диэтил-17β-[N-циклогексил-N-(N-циклогексилтиокарбамоил)карбамоил] андроста-3,5-диен-карбоксамид;
N, N-диэтил-17β-[N-метил-N-(N, N-диэтилкарбамоил)карбамоил] андроста-3,5-диен-карбоксамид;
ацетилоксиметил-17β-[N-изопропил-N-(N-изопропилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоксилат;
Пивалоилоксиметил-17β-[N-изопропил-N-([N-изопропилкарбамоил) карбамоил] андроста-3,5-диен-3-карбоксилат;
Этоксикарбонилоксиметил-17β-[N-изопропил-N-(N-изопропилкарбамоил) карбамоил] андроста-3,5-диен-3-карбоксилат;
(N, N-диэтилкарбамоил)метил-17β-[N-изопропил-N-(N-изопропилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоксилат;
2-(N-морфолино)этил-17β-[N-изопропил-N-(N-изопропилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоксилат;
и, где возможно, их фармацевтически приемлемые соли.
Соединение формулы I могут быть получены с помощью способа, включающего:
А) реакцию соединения формулы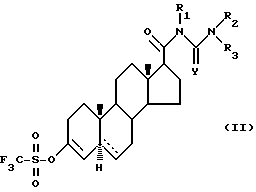
где символ 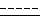 - это одинарная или двойная связь; Y, R1, R2, R3 определены выше, с моноксидом углерода (СО) в присутствии C1-C6-алкилового спирта, таким образом получая соединение формулы I, где символ
- это одинарная или двойная связь; Y, R1, R2, R3 определены выше, с моноксидом углерода (СО) в присутствии C1-C6-алкилового спирта, таким образом получая соединение формулы I, где символ 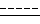 - это одинарная или двойная связь; Y, R1, R2, R3 определены выше, a R является группой OR4, где R4 - C1-C6 алкильная группа; или
- это одинарная или двойная связь; Y, R1, R2, R3 определены выше, a R является группой OR4, где R4 - C1-C6 алкильная группа; или
В) реакцию соединения формулы II, как определено выше, с моноксидом углерода в присутствии амина формулы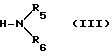
где R5 и R6 определены выше, таким образом получая соединение формулы I, где символ 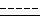 - это одинарная или двойная связь; Y, R1, R2, R3 определены выше, а R является группой
- это одинарная или двойная связь; Y, R1, R2, R3 определены выше, а R является группой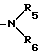
где R5 и R6 определены выше; или
С) Реакцию соединения формулы I, где символы  - это одинарная или двойная связь; Y, R1, R2, R3 определены выше, а R - группа OR4, где R4 - водород, с соединением формулы
- это одинарная или двойная связь; Y, R1, R2, R3 определены выше, а R - группа OR4, где R4 - водород, с соединением формулы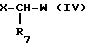
где R7 и W определены выше, а X - атом галогена, таким образом получая соединение формулы I, где символ  - одинарная или двойная связь; Y, R1, R2, R3 определены выше, R является группой
- одинарная или двойная связь; Y, R1, R2, R3 определены выше, R является группой 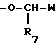 , где R7 и W определены выше; или
, где R7 и W определены выше; или
Д) Реакцию соединения формулы I, где 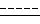 обозначает одинарную или двойную связь; Y, R1, R2, R3 определены выше, R - группа OR4, где R4 - водород, с соединением формулы
обозначает одинарную или двойную связь; Y, R1, R2, R3 определены выше, R - группа OR4, где R4 - водород, с соединением формулы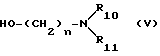
где R10 и R11 определены выше, таким образом получая соединение формулы I, где 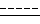 - символ, обозначающий одинарную или двойную связь; Y, R1, R2, R3 определены выше, R - группа
- символ, обозначающий одинарную или двойную связь; Y, R1, R2, R3 определены выше, R - группа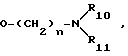
где n, R10 и R11 определены выше; если желательно, превращая соединение формулы I, где символ 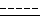 - это одинарная или двойная связь; Y, R1, R2, R3 определены выше, R - группа OR4, где R4 - C1-C6-алкильная группа, путем селективного гидролиза в соответствующее соединение формулы I, где символ
- это одинарная или двойная связь; Y, R1, R2, R3 определены выше, R - группа OR4, где R4 - C1-C6-алкильная группа, путем селективного гидролиза в соответствующее соединение формулы I, где символ 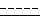 - это одинарная или двойная связь; Y, R1, R2, R3 определены выше, R - группа OR4, где R4- водород, и/или, если желательно, превращая соединение формулы I в его соль, или превращая соль соединения формулы I в соответствующее свободное соединение, и/или, если желательно, разделение смеси изомеров соединения формулы I на отдельные изомеры.
- это одинарная или двойная связь; Y, R1, R2, R3 определены выше, R - группа OR4, где R4- водород, и/или, если желательно, превращая соединение формулы I в его соль, или превращая соль соединения формулы I в соответствующее свободное соединение, и/или, если желательно, разделение смеси изомеров соединения формулы I на отдельные изомеры.
Реакция соединения формулы II с моноксидом углерода в присутствии C1-C6-алкилового спирта в соответствии со способом по варианту А может быть проведена, например, путем взаимодействия раствора соединения формулы II в подходящем органическом растворителе, предпочтительно диметилформамиде (ДМФ), с органическим основанием, таким, как, например, триэтиламин (ТЭА), и палладиевым комплексом, таким, как, например, бис (трифенилфосфин)-палладий (II)-ацетат или бис(трифенилфосфин)-палладия (II)-хлорид, и C1-C4-алкильным спиртом.
По желанию палладиевые комплексы могут быть получены in situ путем добавления, каждого отдельно, фосфина, такого, как трифенилфосфин, и соли палладия, такой, как, например, палладия, такой как, например, палладия (II) ацетат или палладия (II) хлорид.
Затем реакционная смесь продувается моноксидом углерода (CO) в течение нескольких минут и затем перемешивается в атмосфере CO в течение 1-48 ч при температуре 0-40oC (аналогичный процесс описан, например, в Jetr. Lett. 26(8), 1109-12, 1985).
Реакция соединения формулы II с моноксидом углерода и амином формулы III в соответствии с процессом по варианту В может быть проведена аналогично такой же процедуре, о которой сообщено выше, причем вместо алкилового спирта используется амин формулы III.
Атом галогена X в соединении формул IV и V является предпочтительно атомом хлора, брома, йода, наиболее предпочтительно хлора или брома.
Реакция соединения формулы I с соединением формулы IV в соответствии со способом варианта C может быть осуществлена в растворителе, таком, как, например, диметилформамид, диметилацетамид, ацетонитрил, в присутствии основания, такого, как, например, гидрид щелочного металла, предпочтительно гидрид натрия, или щелочного металла алкоксид, предпочтительно метоксид натрия, этоксид натрия, терт-бутоксид калия, или амин, предпочтительно пиридин или триэтиламин, по желанию, когда X не йод, в присутствии иодида щелочного металла, предпочтительно иодида натрия, при температуре в пределах от около 0oC до примерно комнатной температуры в течение времени варьирующего от около 2 ч до около 24 ч, предпочтительно, в нейтральной атмосфере азота.
Реакция соединения формулы I с соединением формулы V в соответствии со способом варианта D может быть проведена в растворителе, таком, как, например, этилацетат, диметилформамид, диметилацетамид, ацетонитрил, в присутствии основания, такого, как, например, гидрид щелочного металла, предпочтительно гидрид натрия, или алкоксид щелочного металла, предпочтительно метоксид натрия, этоксид натрия, терт-бутоксид калия, или амин, предпочтительно пиридин или триэтиламин, по желанию, когда X не йод, в присутствии йодида щелочного металла, предпочтительно йодида натрия, при температуре в интервале от около 0oC до около 80oC, в течение 1-8 ч.
Превращение вещества формулы I, где символ 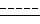 - это одинарная или двойная связь; Y, R1, R2, R3 определены выше и R - группа OR4, где R4 - C1-C4 алкильная группа, в соответствующее соединение формулы I, где символ
- это одинарная или двойная связь; Y, R1, R2, R3 определены выше и R - группа OR4, где R4 - C1-C4 алкильная группа, в соответствующее соединение формулы I, где символ 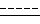 - это одинарная или двойная связь, Y, R1, R2, R3 определены выше, R - группа OR4, где R4 является водородом, может быть проведена, например, в подходящем растворителе, таком, как, например, метанол, этанол, тетрагидрофуран, диоксан, в присутствии водного концентрированного раствора гидроксида щелочного металла, такого, как, например, гидроксид калия, гидроксид натрия или, предпочтительно гидроксида лития, в течение времени, варьирующего от нескольких часов до нескольких дней, при температуре, изменяющейся в пределах от около 0oC до температуры перегонки растворителя, желательно в инертной атмосфере азота.
- это одинарная или двойная связь, Y, R1, R2, R3 определены выше, R - группа OR4, где R4 является водородом, может быть проведена, например, в подходящем растворителе, таком, как, например, метанол, этанол, тетрагидрофуран, диоксан, в присутствии водного концентрированного раствора гидроксида щелочного металла, такого, как, например, гидроксид калия, гидроксид натрия или, предпочтительно гидроксида лития, в течение времени, варьирующего от нескольких часов до нескольких дней, при температуре, изменяющейся в пределах от около 0oC до температуры перегонки растворителя, желательно в инертной атмосфере азота.
Для превращения соединения формулы I в его фармацевтически приемлемую соль, также как для получения свободного соединения из соответствующей соли и для разделения смеси изомеров формулы I на отдельные изомеры, могут быть использованы стандартные процедуры.
Соединение формулы II, где символ  обозначает одинарную связь, Y, R1, R2, R3 определены выше, может быть получено из соединения формулы
обозначает одинарную связь, Y, R1, R2, R3 определены выше, может быть получено из соединения формулы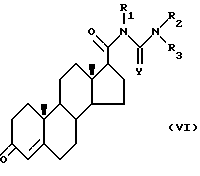
где Y, R1, R2, R3 охарактеризованы выше, следующим способом.
Соединение формулы VI растворяется в подходящем органическом растворителе, таком, как, например, тетрагидрофуран (ТГФ), в присутствии подходящего органического донора протонов, такого, как, например, трет-бутанол или анилин. Затем к полученной смеси добавляется восстанавливающий металл-аминовый раствор, например раствор лития/жидкого аммиака, и затем реакционная смесь перемешивается при температуре, изменяющейся в пределах от около -100oC до около -30oC, предпочтительно при около -78oC, в течение около 2-3 ч. Затем реакция останавливается с помощью органического литиевого акцептора, такого, как, например, бромобензол, дибромоэтан или, предпочтительно, изопрена, и растворитель удаляется под вакуумом. Твердый осадок снова растворяется в органическом растворителе, таком, как, например, тетрагидрофуран или диэтиловый эфир, и обрабатывается N-арилтрифторалкилсульфонимидом, предпочтительно N-фенилтрифторметилсульфонимидом, при температуре от около -20oC до около -30oC, в течение от примерно 2 ч до примерно 24 ч (об этом методе сообщено, например, в Jetr. Lett. 1983, 24, 579-982).
Соединение формулы II, где символ  - это двойная связь, Y, R1, R2, R3 определены выше, может быть получено из соответствующего соединения формулы VI, где R1, R2 и R3 определены выше и
- это двойная связь, Y, R1, R2, R3 определены выше, может быть получено из соответствующего соединения формулы VI, где R1, R2 и R3 определены выше и  - это одинарная связь, например добавляя к раствору, содержащему соединение формулы VI, как определено выше, и слабое органическое основание, такое, как, 2,6-ди-третбутил-4-метилпиридин, в подходящем органическом растворителе, таком, как, например, метиленхлорид, трифторсульфоновый ангидрид, предпочтительно трифторметансульфоновый ангидрид, в соответствии с методом, опубликованном в Synthesis. 438-440, 1979.
- это одинарная связь, например добавляя к раствору, содержащему соединение формулы VI, как определено выше, и слабое органическое основание, такое, как, 2,6-ди-третбутил-4-метилпиридин, в подходящем органическом растворителе, таком, как, например, метиленхлорид, трифторсульфоновый ангидрид, предпочтительно трифторметансульфоновый ангидрид, в соответствии с методом, опубликованном в Synthesis. 438-440, 1979.
Соединение формулы VI может быть в свою очередь синтезировано с использованием известных методов, например тремя путями а), b) и с), приведенными в следующей схеме: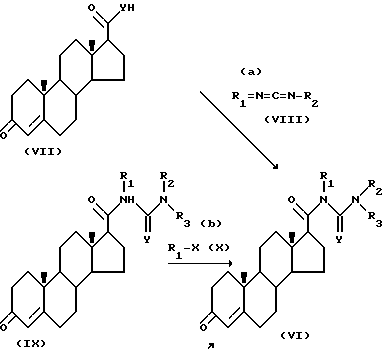
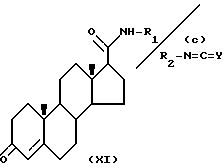
По реакции (а), соединение формулы VI, где Y, R1, R2, R3 определены выше, причем R1 и R2 - неводородные атомы, a R3 - водород, может быть получено при реакции соединения формулы VI, где Y охарактеризован выше, с карбодиимидом формулы VIII, где R1 и R2 определены выше.
Согласно реакции (b), соединение формулы VI, где R1 определено выше, причем это не водород; Y, R1, R2, R3 определены выше, может быть получено из соединения формулы IX, где R2 и R3 охарактеризованы выше, путем алкилирования соединением формулы X, где R1 определено выше, причем это не водород, а X - атом галогена, например йод.
В соответствии с реакцией (с) соединение формулы VI, где R3 - водород, Y, R1, R2, R3 определены выше, причем R2 не водород, может быть получено из соединения формулы XI, где R1 охарактеризован выше, путем реакции с соединением формулы XII, где R2 и Y определены выше, причем R2 - не водород.
Соединения формулы VII, где Y - S, формулы IX и формулы XI могут быть получены реакцией соединения формулы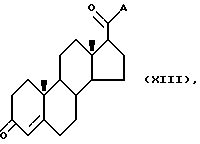
где A может быть любой подходящей активирующей карбоксильную функцию группой, которая пригодна для образования амидных и пептидных связей, с соответствующим реагентом, как показано далее.
Подходящей активирующей группой может быть, например, одна из следующих групп: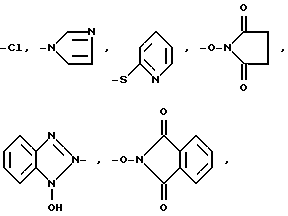
Конкретно, соединение формулы VII, где Y - сера, может быть, например, получено из соединений формулы XIII в соответствии с известными методами.
Один метод может включать, например, взаимодействие вещества формулы XIII, где А - хлор, с газообразным сероводородом в присутствии диметилтиоформамида в растворителе, таком, как, например, CH2Cl2, при комнатной температуре в течение времени от примерно 10 мин до нескольких часов при энергичном перемешивании по методике, описанной в Synthesis, 671-2, 1985.
Другой метод может включать, например, взаимодействие соединения формулы XIII, где А -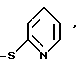 который является S-2-пиридилтиоатным производным, с избытком бисульфида натрия моногидрата. Реакция может быть выполнена в растворителе, таком, как, например, метиленхлорид, тетрагидрофуран, ацетонитрил, при температуре, например, от около 0oC до около 50oC в течение времени, например, от около 1 ч до около 48 ч.
который является S-2-пиридилтиоатным производным, с избытком бисульфида натрия моногидрата. Реакция может быть выполнена в растворителе, таком, как, например, метиленхлорид, тетрагидрофуран, ацетонитрил, при температуре, например, от около 0oC до около 50oC в течение времени, например, от около 1 ч до около 48 ч.
Соединение формулой VII, где Y - сера, может также быть синтезировано в соответствии с основными методами, описанными в литературе по синтезу тиокарбоновых кислот, например путем, аналогичным описанному у Houben Weyl, Bd E5, 832 - 842, или у Duns F. in Barton and Ollis, Comprehen. sive Organic Chemistry, Vol. 3, Pergamon Press, Oxford, 1979 p. 420-432.
Соединение формулы IX, как определено выше, может быть получено взаимодействием соединения формулы XIII, как определено выше, с мочевиной формулы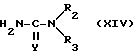
где R2 и R3 определены выше.
Соединение формулы XI может быть получено взаимодействием соединения формулы XIII с амином формулы
R1 - NH2 (XV)
где R1 определено выше.
Соединение формулы XIII может быть получено из соединения формулы VII, где Y - кислород, хорошо известными методами.
Соединения формулы III, IV, V, VII, где Y - кислород, соединения формул VIII, X, XII, XIV и XV являются коммерчески доступными или могут быть получены известными методами из известных веществ.
Соединения по изобретению специфически подавляют фермент тестостерон-5α-редуктазу и поэтому могут быть полезны для лечения состояний, зависящих от уровня андрогенов. Для примера подавляющее действие соединений этого изобретения на 5α-редуктазу было определено in virto в соответствии с методикой, описанной далее.
Подавление 5α-редуктазы оценивалось с использованием фракции плотных частиц, содержащей ядра, микросомы и митохондрии, из гомогенатов доброкачественной гипертрофированной ткани простаты человека в качестве источника фермента.
Фракцию плотных частиц получали центрифугированием гомогената простаты при 140000•g. Полученный осадок отмывался несколько раз, ресуспендировался в буфере и хранился при -80oC в порциях, содержащих 10 мг протеина в 1 мл.
Исследование на 5α-редуктазу выполнялось в окончательном объеме 0,5 мл, содержащем 1 ммоль дитиотрептола, 40 ммоль Трис-HCl буфера pH 5,5, 5 ммоль НАДФ, 1 мкмоль 4-14C тестостерона, 0,3 мг протеина фракции плотных частиц простаты и различные концентрации ингибиторов. После 30 мин инкубации при 37oC реакция останавливалась путем добавления 2,0 мл диэтилового эфира и органическая фаза отделялась, выпаривалась в атмосфере N2 и ресуспендировалась в этилацетате. Метаболиты тестосторона из этого экстракта выделялись путем ТСХ на силикагельных пластинках F 254 (Merck) с использованием хлороформа, ацетона и н-гексана (2:1:2) в качестве проявляющей системы растворителей. Радиоактивность на пластинке сканировалась и анализировалась с помощью количественных графиков, напечатанных ТСХ-анализатором (Berthold).
Фракционное 5α-восстановление тестостерона подсчитывалось по соотношению 14С-радиоакnивности в полосах 5α-восстановленных метаболитов (5α-дигидротестостерона, 3α- и 3β-андростандиолов) к общей радиоактивности в полосах тестостерона и 5α- восстановленных метаболитов.
Концентрацию каждого соединения, необходимую для снижения активности контрольной 5α-редуктазы на 50 % (ПК50), определяли по графику зависимости процента подавления от логарифма концентраций ингибитора.
Таким образом, например, при вышеприведенном исследовании было установлено, что соединение, представляющее данное изобретение, а именно 17β-[N-изопропил-N-(N-изопропилкарбамоил)карбамоил] андрост-3,5-диен-3-карбоновая кислота, вызывает 50 %-ное подавление активности человеческой простатической 5α- редуктазы в дозе 3 нМ.
Ввиду показанной выше активности соединения этого изобретения могут быть терапевтически пригодны в случаях заболеваний, при которых желательно снижение андрогенного действия путем подавления 5α-редуктазы, при таких, например, как доброкачественная гиперплазия простаты, рак простаты и молочных желез и определенных состояниях кожи и волосяного покрова, таких, как, например, себоррея, гирсутизм у женщин и облысение у мужчин.
Они пригодны как для фармацевтического производства, так и для лечения гиперплазии простаты в ветеринарии.
Токсичность соединений этого изобретения совершенно незаметна, так что они могут быть безопасно использованы для терапии.
Соединения этого изобретения могут применяться в виде ряда дозированных лекарственных форм, например перорально, в форме таблеток, капсул, таблеток, покрытых сахаром или пленкой, растворов и суспензий, ректально в виде свечей, парентерально, например внутримышечно или внутривенно в виде инъекций или вливаний, местно, например в форме кремов.
Дозировка зависит от возраста, веса, состояния больного и способа введения, например дозы для перорального применения у взрослых людей могут изменяться в пределах от около 0,2 до около 100 мг на одну дозу 1-3 раза в день.
Изобретение включает фармацевтические композиции, состоящие из соединения этого изобретения в смеси с фермацевтически приемлемым наполнителем, который может быть носителем или растворителем.
Фармацевтические композиции, содержание вещества данного изобретения, обычно получают следующими общепринятыми методами и применяются в удобной фармацевтической форме.
Например, твердые пероральные формы могут содержать вместе с активным веществом разбавители, например лактозу, декстрозу, сахарозу, целлюлозу, кукурузный или картофельный крахмал, скользящие вещества, например кремнезем, тальк, стеариновую кислоту, стеарат магния или кальция, и/или полиэтиленгликоли, связывающие агенты, например крахмалы, аравийскую кемедь, желатин, метилцеллюлозу, карбоксиметилцеллюлозу или поливинилпирролидон, разрыхляющие агенты, например крахмал, альгиновую кислоту, альгинаты или крахмал-гликолят натрия, шипучие смеси красители, подслащивающие вещества, увлажняющие агенты, такие, как лецитин, полисорбаты, лаурилсульфаты, и, в общем, нетоксичные и фармакологически неактивные вещества, используемые в технологии приготовления лекарственных средств.
Вышеназванные фармацевтические препараты могут быть произведены известными способами, например путем смешивания, гранулирования, таблетирования, дражирования с нанесением карамельного или пленочного покрытия.
Жидкими дисперсиями для перорального применения могут быть, например, сиропы, эмульсии и суспензии.
Сиропы могут содержать в качестве носителя, например, сахарозу или сахарозу с глицерином и/или маннитол, и/или сорбитол; в частности, сироп, который будут принимать диабетические больные, может содержать в качестве носителя (основы) только вещества, не метаболизирующиеся до глюкозы или метаболизируемые до глюкозы в очень малых количествах, например сорбитол.
Суспензии и эмульсии могут содержать в качестве носителя, например, природную камедь, агар, альгинат натрия, пектин, метилцеллюлозу, карбоксиметилцеллюлозу или поливиниловый спирт.
Суспензии или растворы для внутримышечных инъекций могут содержать вместе с активным веществом фармацевтически приемлемый носитель, например стерильную воду, оливковое масло, этилолеат, гликоль, например пропиленгликоль и, если желательно, соответствующее количество лидокаина гидрохлорида.
Растворы для внутривенных инъекций или вливаний могут содержать в качестве носителя, например, стерильную воду или, предпочтительно, они могут быть в форме стерильного, водного, изотонического солевого растворов.
Свечи могут содержать вместе с активным веществом фармацевтически приемлемый носитель (основу), например масло какао, полиэтиленгликоль, сурфактант (ПАВ), представляющий собой эфир полиоксиэтилен-сорбитана и жирной кислоты, или лецитин.
Общепринятые носители могут быть использованы для получения лекарственных форм для местного применения.
Выражения "фармацевтический" и т.п., использованные в описании, подразумевают включение и значения "ветеринарный и т.н.".
Следующие примеры иллюстрируют, но не ограничивают изобретение, в спектрах ЯМР приняты следующие обозначения: s- синглет, d -дублет, t -триплет, m -мультиплет, b - широкий сигнал, q - квартет.
Пример 1. 1-(3-оксоандрост-4-ен-17β-карбонил)-1,3-диизопропилмочевина [(VI): Y = 0, R1 = iPr, R2 = iPr, R3 = H].
К перемешиваемому раствору андрост-4-ен-3-он-17β-карбоновой кислоты (50 г) в этилацетате (1,5 л) и триэтиламине (33 мл) каплями добавляется N,N-диизопропилкарбодиимид (32,4 мл) в течение 5 мин и затем реакционная смесь нагревается в колбе с обратным холодильником на протяжении 1 ч. Реакционная смесь охлаждалась и отфильтровывалась на воронке Бюхнера, фильтрат промывался 1 н. HCl, 0,5 н. NaHCO3, соляным раствором и высушивался сульфатом натрия и концентрировался до примерно 150 мл, путем охлаждения продукт, указанный в названии, осаждается и отфильтровывается фильтрацией с отсосом, промывается изопропиловым эфиром, оставляя таким образом 54 г белого кристаллического вещества (т. пл. 172-175oC), [α]D + 89oC(с = 1, ДМФ).
Следуя аналогичной методике, могут быть получены ниже перечисленные вещества:
1-(3-оксоандрост-4-он-17β-карбонил)-1,3-дициклогексилмочевина (т. пл. 178-180oC, [α]D +77oC (с = 1, ДМФ);
1-(3-оксоандрост-4-ен-17β-карбонил)-1,3-дитретбутилмочевина (т. пл. 175-177oC), [α]D + 53oC (с = 0,5, ДМФ).
Пример 2. 1-(3-оксоандрост-4-ен-17β-карбонил)-1,3-диизопропилтиомочевина [(VI): Y = S, R1 = iPr, R2 = iPr].
Раствор 2-пиридил-3-оксоандрост-4-ен-17β-карботионата [(XIII) 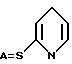 ] (3,0 г) в тетрагидрофуране (70 мл) обрабатывали 70 % сульфида натрия моногидрата (3,9 г) и смесь нагревали с обратным холодильником в течение 2 ч. После подкисления 1 н. соляной кислотой смесь тщательно экстрагировали метиленхлоридом.
] (3,0 г) в тетрагидрофуране (70 мл) обрабатывали 70 % сульфида натрия моногидрата (3,9 г) и смесь нагревали с обратным холодильником в течение 2 ч. После подкисления 1 н. соляной кислотой смесь тщательно экстрагировали метиленхлоридом.
Объединенные органические экстракты отмывались водой до нейтральной реакции, высушивались сульфатом натрия и выпаривались до сухого состояния.
Дальнейшая очистка тонкослойной хроматографией на силикагеле (элюент - метиленхлорид: ацетон 95: 5) дает 3,5 г 3-оксоандрост-4-ен-17β-карботиоевой кислоты [(VII) Y = S].
ЯМР (CDCI3) δ: 5,70 (S, 1H, H (4)), 1,2 (s, 3H, CH3 (19)), 0,75 (s, 3H, CH3 (18)).
MC (м/з): 332 М+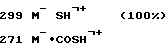
Раствор тиокислоты (2,54 г), полученной таким образом, в этилацетате (59 мл) обрабатывали сначала триэтиламином (1,6 мл) и затем N,N'-диизопропилкарбодиимидом (1,54 мл) и смесь перемешивали в течение 5 ч при комнатной температуре.
Реакционная смесь сразу же подвергалась хроматографии на колонке с силикагелем с элюированием метиленхлоридом/этилацетатом 90:10, получая таким образом вещество, указанное в названии (2,03 г, рекристаллизованного из метиленхлорида/этилацетата; т. пл. 180-183oC) [α]D + 146oC (с = 1, ДМФ).
ЯМР (CDCl3) δ: 6,8 (d, 1H, H), 5,75 (s, 1H, H(4)), 4,2-4,8 (m, 2Н, NH-CH(CH3)2, 1,3 (2d, 12H, 4 изопропиловая CH3), 1,2 (s, 3H, CH3 (19)), 0,85 (s, 3H, CH3 (18)).
МС (м/з) : 458 М+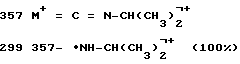
Следуя аналогичной методике, могут быть получены соединения, перечисленные ниже:
1-(3-оксоандрост-4-ен-17β-карбонил)-1,3-дициклогексилтиомочевина (т. пл. 209-212oC);
1-(3-оксоандрост-4-ен-17β-карбонил)-1,3-дитертбутилтиомочевина.
Пример 3. 3-{[(трифторметил)сульфонил]окси}-17β[N-изопропил-N-(N-изопропилкарбамоил)карбамоил)] андроста-3,5-диен [(II), Y = 0, R1 = iPr, R1 = iPr, R3 = H, 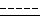 - двойная связь].
- двойная связь].
К перемешиваемому раствору 17β-[N-изопропил-N-(N -изопропилкарбамоил) карбамоил] андрост-4-ен-3-она (6,0 г) и 2,6-дитретбутил-4-метилпиридин (3,63 г) в метиленхлориде (54 мл), выдерживаемому в атмосфере азота при комнатной температуре, добавляли по каплям трифторуксусный ангидрид (2,54 мл) в течение 10 мин.
После перемешивания в течение 30 мин реакционная смесь разводилась метиленхлоридом и отмывалась насыщенным водным раствором бикарбоната натрия, 1 н. HCl, водой до нейтральной реакции и высушивалась сульфатом натрия.
Полученная пена очищалась с помощью флэш-хроматографии на силикагеле (элюент: н-гексан/этилацетат 75: 25) с получением таким образом 4,6 г соединения, указанного в названии (т. пл. 135-140oC).
ЯМР (CDCl3) δ: 5:80 (m, 1H, H(4)), 5,45 (m, 1H, H(6)).
МС (м/з) 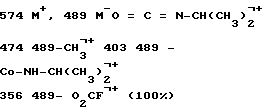
Следуя аналогичной методике, могут быть получены нижеперечисленные соединения:
3-{ [(трифторметил)сульфонил] окси} -17β-[N-изопропил-N(N-изопропилтиокарбамоил)карбамоил] андроста-3,5-диен;
3-{ [(трифторметил)сульфонил] окси} -17β-[N-циклогексил-N(N-циклогексилкарбамоил)карбамоил] андроста-3,5-диен (т. пл. 140-145oC);
3-{ [(трифторметил)сульфонил] окси} -17β-[N-циклогексил-N(N-циклогексилтиокарбамоил)карбамоил] андроста-3,5-диен;
3-{ [(трифторметил)сульфонил] окси} -17β-[N-трет-бутил-N-трет-бутилкарбамоил) карбамоил] андроста-3,5-диен (т. пл. 123-124oC);
3-{ [(трифторметил)сульфонил] окси} -17β-[N-метил-N(N,N-диэтилкарбамоил) карбамоил] андроста-3,5-диен.
Пример 4. Метил-17бета-[N-изопропил-N-(N-изопропилкарбамоил) карбамоил] андроста-3,5-диен-3-карбоксилат [(I): Y=0, R1 = iPr, R2 = iPr, R3 = H, 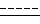 - двойная связь, R = OR4, R4 = CH3].
- двойная связь, R = OR4, R4 = CH3].
К раствору 3-{ [(трифторметил) сульфонил]окси}-17β-[N-изопропил-N(N-изопропилкарбамоил)карбамоил] андроста-3,5-диена (4,6 г) в диметилформамиде (17 мл), метаноле (17 мл) и триэтиламине (2,23 мл) добавляли бис(трифенилфосфин) палладий (II) ацетат (180 мг), смесь продували моноксидом углерода в течение 5 мин и затем перемешивали в течение ночи при комнатной температуре в атмосфере моноксида углерода, поддерживаемой в закрытой стеклянной колбе.
Затем добавляли этилацетат и органический раствор промывался водой до нейтральной реакции, высушивался сульфатом натрия и растворитель удалялся под вакуумом. Сырой продукт очищали с помощью флэш-хроматографии на силикагеле (элюент: н-гексан/этилацетат 75:25), получая таким образом 3,5 г указанного в названии продукта (т. пл. 15О-155oC)
ЯМР (CDPCl3) δ: 7,05 (m, 1H, H (4)), 5,80 (m, 1H, H (6)), 3,75 3Н, COOCH3).
МС (м/з) 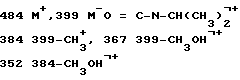
Следуя аналогичной методике, могут быть получены перечисленные ниже вещества:
Метил-17β-[N-изопропил-N-(N-изопропилтиокарбамоил) карбамоил]андроста-3,5-диен-3-карбоксилат;
Метил-17β-[N-изопропил-N-(N-циклогексилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоксилат;
Метил-17β-[N-изопропил-N-(N-циклогексилтиокарбамоил) карбамоил] андроста-3,5-диен-3-карбоксилат;
Метил-17β-[N-терт-бутил-N-(N-терт-бутилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоксилат (т. пл. 110-115oC);
Метил-17β-[N-метил-N-(N-изопропилтиокарбамоил) карбамоил] андроста-3,5-диен-3-карбоксилат.
Пример 5. Метил-17β-[N-изопропил-N-(N-изопропилкарбамоил) карбамоил] андроста-3,5-диен-3-карбоновая кислота [(I): Y = 0, R1 = iPr, R2 = iPr, R3 = H, 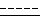 - двойная связь, R = OR4, R4 = H].
- двойная связь, R = OR4, R4 = H].
Смесь метил-17бета-[N-изопропил-N-(N-изопропилтиокарбамоил) карбамоил] андроста-3,5-диен-3-карбоксилата (3,29 г), метанола (136 мл) и водного гидроксида лития (1,424 г в 36 мл воды) перемешивалась при комнатной температуре в течение 5 дней. Метанол испарялся под вакуумом и добавлялась вода, смесь подкислялась 1 н. HCl и экстрагировалась метиленхлоридом, органические слои промывались насыщенным соляным раствором, водой до нейтральной реакции, высушивались сульфатом натрия и растворитель удалялся под вакуумом.
Полученный желтый твердый осадок очищался с помощью флэш-хроматографии на силикагеле (элюент: метиленхлорид/ацетон 9:1), таким образом получали 1,66 г белого твердого вещества, которое кристаллизовалось из метиленхлорида/этилацетата (1,15 г, т. пл. 173-175oC дец.), [α]D = -132oC (с = 1, CHCl3).
ЯМР (CDCl3) δ: 7,13 (m, 1H, H(4)), 6,50 (b m, 1H, CONH), 5,82, (m, 1H, H(6)), 4,48 (м, 1H, 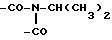 ), 3,98 (m, 1H, CONH-CH(CH3)2), 2,69 (t, 1H, CH(17 α)), 1,15-1,35 (4d - 12H, 4 изопропиловый CH3), 0,90 (s, 3H, CH3(19)), 0,80 (s, 3H, CH3(18)).
), 3,98 (m, 1H, CONH-CH(CH3)2), 2,69 (t, 1H, CH(17 α)), 1,15-1,35 (4d - 12H, 4 изопропиловый CH3), 0,90 (s, 3H, CH3(19)), 0,80 (s, 3H, CH3(18)).
MC (м/з): 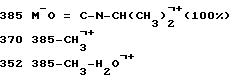
Следуя аналогичной методике могут быть получены перечисленные ниже вещества:
17β-[N-изопропил-N-(N-изопропилтиокарбамоил)карбамоил] андроста-3,5-диен-3-карбоновая кислота (т. пл. 125-130oC);
17β-[N-циклогексил-N-(N-циклогексилкарбамоил)карбамоил] (т. пл. 253-255oC, AcOEt) [α]D - 110oC (с = 1, CHCl3);
17β-[N-циклогексил-N-(N-циклогексилтиокарбамоил)карбамоил] андроста-3,5-диен-3-карбоновая кислота;
17β-[N-трет-бутил-N-(N-трет-бутилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоновая кислота (т. пл. 118-120oC), 134oC (с = 0,5, ДМФ);
17β-[N-метил-N-(N-диэтилкарбамоил) карбамоил] андроста-3,5-диен-3-карбоновая кислота.
Пример 6. N,N-диэтилкарбамоил-17β-[N-изопропил-N-(N-изопропилкарбамоил) карбамоил] андроста-3,5-диен-3-карбоксамид [(I): Y = 0, R1 = iPr, R2 = iPr, R3 = H,  R4 = R5 = Эт].
R4 = R5 = Эт].
Смесь 3-{ [(трифторметил) сульфонил]окси}-17β-[N-изопропил-N-(N-изопропилкарбамоил)карбамоил]андроста-3,5-диена (574 мг), ацетата палладия (6 мг), трифенилфосфина (16 мг) и диэтиламина (4,2 мл) в диметилформамиде (4 мл) продували моноксидом углерода в течение 10 мин и затем перемешивали в течение ночи при комнатной температуре в атмосфере моноксида углерода, поддерживаемой в закрытой колбе.
Затем добавляли этилацетат и органический раствор промывали водой до нейтральной реакции, высушивали сульфатом натрия и растворитель удаляли под вакуумом.
Сырой продукт очищали с помощью флэш-хроматографии на силикагеле (элюент: н-гексан/этилацетат 60:40), получая таким образом 310 мг вещества, указанного в названии.
Следуя аналогичной методике, могут быть получены перечисленные ниже вещества:
N, N-диэтил-17β-[N-изопропил-N-(N-изопропилтиокарбамоил) карбамоил] андроста-3,5-диен-3-карбоксамид;
N, N-диэтил-17β-[N-циклогексил-N-(N-циклогексилкарбамоил)карбамоил] андроста-3,5-диен-3-карбоксамид;
N, N-диэтил-17β-[N-циклогексил-N-(N-циклогексилтиокарбамоил) карбамоил] андроста-3,5-диен-3-карбоксамид;
N,N-диэтил-17β-[N-метил-N-(N-диэтилкарбамоил)карбамоил]андроста-3,5-диен-3-карбоксамид.
Пример 7. 2-(N-морфино)этил-17β-[N-изопропил-N-(N-изопропилкарбамоил) карбамоил] андроста-3,5-диен-3-карбоксилат [(I): Y = 0, R1 = iPr, R2 = iPr, R3 = H,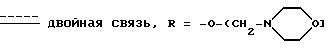
К раствору 17β-[N-изопропил-N-(N-изопропилкарбамоил) карбамоил]андроста-3,5-диен-3-карбоновой кислоты (235 мг) в метиленхлориде (2,5 мл) медленно добавляли 4-(2-гидроксиэтил)-морфолин (7,4 мкл) и 4-пирролидинопиридина (3,7 мг), а после них дициклогексилкарбодиимид (124 мг). Спустя несколько минут, прозрачный раствор становился мутным. Перемешивание продолжали при комнатной температуре в течение 3 ч. Смесь фильтровали через бумажный фильтр и твердый осадок промывался метилен-хлоридом, фильтрат выпаривался до сухости. Полученное таким образом сырое маслянистое вещество (394 мг) очищали с помощью флэш-хроматографии на силикагеле (элюент: метиленхлорид/ацетон 8:2), получая 170 мг соединения, указанного в названии.
ЯМР (CDCl3) δ: 7,00 (m, 1H, H (4)), 6,50 (b m, 1H, CONH), 5,78 (m, 1H, H(6)), 4,48 (m, 1H, 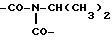 ), 4,27 (m, 2Н,
), 4,27 (m, 2Н, 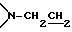 OCO-), 3,98 (m, 1H, CONCH (CH3)2), 3,68 (m, 4Н,
OCO-), 3,98 (m, 1H, CONCH (CH3)2), 3,68 (m, 4Н, 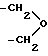 ), 2,65 (m, 4Н
), 2,65 (m, 4Н 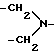 ), 2,50 (m, 2Н,
), 2,50 (m, 2Н, 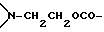 ), 1,35-1,15 (4d, 12Н, 4 изопропиловая CH3), 0,50 (s, 3Н, CH3 (19)), 0,80 (s, 3Н, CH3(18)).
), 1,35-1,15 (4d, 12Н, 4 изопропиловая CH3), 0,50 (s, 3Н, CH3 (19)), 0,80 (s, 3Н, CH3(18)).
МС (м/з): 583 М+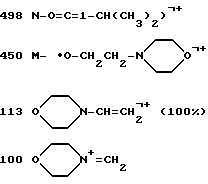
Пример 8. Ацетилоксиметил 17бета-[N-изопропил-N-(N-изопропилкарбамоил) карбамоил] андроста-3,5-диен-3-карбоксилат [(I): Y = 0, R1 = iPr, R2 = iPr, R3 = H, 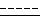 - двойная связь, R = -O-CH2O-COMe]
- двойная связь, R = -O-CH2O-COMe]
К раствору 17β-[N-изопропил-N-(N-изопропилкарбамоил) карбамоил]андроста-3,5-диен-3-карбоновой кислоты (500 мг) в безводном диметилформамиде (15 мл), выдерживаемому в атмосфере азота и охлаждаемому до 0oC на ледяной бане, добавляют гидрид натрия (47,8 мг, 80 % суспензии в минеральном масле) и смесь перемешивают при 0oC в течение 1 ч. Каплями добавляют бромометилацетат (0,31 мл) и раствор перемешивают при комнатной температуре в течение 3 ч. Затем смесь льют в ледяную воду и экстрагируют толуеном (3 х 50 мл), объединенные органические экстракты промывают водой, насыщенным соляным раствором и обезвоживают сульфатом натрия. Растворитель удаляется под вакуумом, причем остается 500 мг сырого материала, который очищают с помощью флэш-хроматографии на силикагеле (элюент: н-гексан/этилацетат 65:35), получая таким образом 270 мг вещества, указанного в названии, в виде белого твердого осадка (т. пл. 183-185oC).
Элементарный анализ для C31H46N2O6:
Вычислено, %: C 68,61; H 8,54; N 5,16.
Найдено, %: C 68,34; H 8,76; N 5,08.
ЯМР (CDCl3), δ: 7,05 (m, 1H, H(4)), 6,40 (b m, 1H, CONH), 5,80 (m, 1H, H (6)), 5,75 (s, 2H, CH3COOCH2OCO-), 4,48 (m, 1H,  (CH3)2), 3,98 (m, 1H, -CONHCH(CH3)2), 2,08 (s, 3H, CH3CO), 1,35 -1,15 (4d, 12H, 4 изопропиловая CH3), 0,90 (s, 3H, CH3 (19)), 0,80 (s, 1H, CH3(18)).
(CH3)2), 3,98 (m, 1H, -CONHCH(CH3)2), 2,08 (s, 3H, CH3CO), 1,35 -1,15 (4d, 12H, 4 изопропиловая CH3), 0,90 (s, 3H, CH3 (19)), 0,80 (s, 1H, CH3(18)).
MC (м/з) 542 M+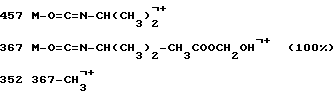
Следуя аналогичной методике и используя соответствующие исходные материалы, могут быть получены перечисленные ниже вещества:
пивалоилоксиметил 17β-[N-изопропил-N-(N-изопропил-карбамоил) карбамоил] андроста-3,5-диен-3-карбоксилат;
этоксикарбонилоксиметил 17β-[N-изопропил-N-(N-изопропил-карбамоил) карбамоил]андроста-3,5-диен-3-карбоксилат.
Пример 9. N, N-диэтилкарбамоилметил 17β-[N-изопропил-N-(N-изопропил-карбамоил) карбамоил]андроста-3,5-диен-3-карбоксилат [(I): Y = 0, R1 = iPr, R2 = iPr, R3 = H,
К раствору 17β-[N-изопропил-N-(N-изопропил-карбамоил) карбамоил] андроста-3,5-диен-3-карбоновой кислоты (480 мг) в безводном диметилформамиде (13 мл), выдерживаемому в атмосфере азота и охлаждаемому до около 0oC на ледяной бане, добавляли гидрид натрия (41,1 мг, 80 % суспензии в минеральном масле) и смесь перемешивали при около 0oC в течение 1 ч.
Добавляли N,N-диэтил-2-хлорацетамид (409,8 мг) и иодид натрия (410,6 мг) при 0oC и затем смесь перемешивали при комнатной температуре в течение 3 ч.
Так как некоторое количество исходного материала еще не прореагировало, добавляли дополнительное количество N,N-диэтил-2-хлорацетамида (132,9 мг) и йодида натрия (136,8 мг) и смесь дополнительно перемешивали в течение 3 ч при комнатной температуре.
Реакционную смесь выливали в ледяную воду (250 мл) и экстрагировали толуеном (4 х 50 мл), объединенные органические экстракты обрабатывали триэтиламином (1 мл) и промывали водой (3 х 20 мл), 0,1 н. тиосульфатом натрия, насыщенным соляным раствором и обезвоживали сульфатом натрия.
После удаления растворителя под вакуумом полученный сырой темный маслянистый продукт (500 мг) очищали с помощью флэш-хроматографии на силикагеле (элюент: н-гексан/этилацетат 40: 60), получая таким образом желтоватый твердый материал, который растирают с эфиром в порошок, что дает 320 мг соединения, указанного в названии, в виде белого порошкообразного материала (т. пл. 103-105oC).
Элементарный анализ для C34H53N2O5:
Вычислено, %: C 69,35; H 9,15; N 7,20.
Найдено, %: C 69,42; H 9,41; N 7,03.
ЯМР (CDCl3) δ: 7,17 (m, 1H, H(4)), 6,51 (d 1H, CONH), 5,85 (m, 1H, H(6)), 4,80 (s, 1H, COOCH2СО) 4,48 (m, 1H,  (CH3)2), 3,98 (m, 1H, CONHCH(CH(CH3)2), 3,38 (q, 4H, 2 CH2CH3), 1,35-1,15 (4d , 12H, 4 изопроииловая CH3), 0,90 (s, 3Н, CH3(19)), 0,80 (S 3H, CH3(18)).
(CH3)2), 3,98 (m, 1H, CONHCH(CH(CH3)2), 3,38 (q, 4H, 2 CH2CH3), 1,35-1,15 (4d , 12H, 4 изопроииловая CH3), 0,90 (s, 3Н, CH3(19)), 0,80 (S 3H, CH3(18)).
МС (м/з): 498 M - O=C=N-CH(CH3)2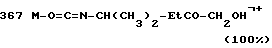
Пример 10. 1-(3-оксоандрост-4-он-17β-карбонил)-3-третбутилмочевина [соединение (VI): Y = 0, R1 = H, R2 = tBu, R3 = H].
К смеси 3-оксо-андрост-4-ен-17β-карбоновой кислоты (284 мг) в безводном толуоле (6,0 мл) по каплям добавляли оксалилхлорид (0,72 мл).
Смесь перемешивали при комнатной температуре в течение 1,5 ч и затем летучие компоненты удаляли под вакуумом, таким образом получая желтоватый твердый остаток 3-оксоандрост-4-ен-17β-карбонилхлорида.
К раствору полученного ацилхлорида в пиридине (4,1 мл) добавляли порошкообразную третбутилмочевину (105 мг). После перемешивания в течение 2 ч реакционная смесь выливалась в ледяную воду (60 мл) и экстрагировалась метиленхлоридом, объединенные органические экстракты промывали 1 н. соляной кислотой, насыщенным соляным раствором, водой и обезвоживали сульфатом натрия.
После выпаривания растворителя остается 330 мг темного твердого вещества, которое хроматографировали на силикагеле (элюент: н-гексан/этилацетат 50: 50), таким образом получается 230 мг соединения, указанного в названии (т. пл. 210-217oC).
ЯМР (CDCl3) δ: 8,5 (s, 1H, -CONH-), 8,1 (s, 1H, -CONH-), 5,7 (m, 1H, H(4)). 1,35 (s, 3Н, тВ), 1,1 (s, 3Н, CH3(19)), 0,8 (s, 3Н, CH3(18)).
Следуя аналогичной методике и используя соответствующие исходные материалы, можно получить перечисленные ниже соединения:
(3-оксоандрост-4-он-17β-карбонил)мочевина (т. пл. 242-245oC);
1-(3-оксоандрост-4-ен-17β-карбонил)-3-н-бутилмочевина.
Пример 11. 1-(3-оксоандрост-4-ен-17β-карбонил)-3,3-диэтилмочевина. [соединение (VI): Y = 0, R1 = H, R2 = R3 = Et].
К суспензии гидрида калия (275 мг) в безводном тетрагидрофуране (2 мл) в атмосфере азота добавляют порошкообразную (твердую) N,N -диэтилмочевину (110 мг), смесь перемешивают при комнатной температуре в течение 10 мин, затем нагревают с обратным холодильником в течение 2 ч.
После охлаждения при комнатной температуре ацилхлорид, полученный из 95,0 мг 3-оксоандрост-4-ен-17β-карбоновой кислоты по методике, описанной в примере 10, растворенный в безводном тетрагидрофуране (2 мл), добавляют по каплям.
Смесь перемешивают при комнатной температуре в течение 2 ч. Летучие компоненты удаляли при сниженном давлении и остаток растворяют в этилацетате и воде.
После подкисления 1 н. HCl органический слой отделяется, а водный дважды экстрагируется этилацетатом. Объединенные органические экстракты промывают водой, обезвоживают сульфатом натрия и выпаривают под вакуумом.
Полученный таким образом сырой продукт (180 мг) очищают с помощью флэш-хроматографии на силикагеле (элюент: н-гексан/этилацетат 75:25), имея выход 80 мг указанного в названии соединения (т. пл. 187-190oC).
ЯМР (CDCl3: 7,1 (s, 1H, -CONHCO-), 5,7 (m, 1H, H (4)), 3,3 (q, 4H 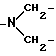 ), 1,15 (t, 6Н, 2N-CH2CH3), 1,1 (s, 3H, CH3 (19)), 0,8 (s, 3H, CH3(18)).
), 1,15 (t, 6Н, 2N-CH2CH3), 1,1 (s, 3H, CH3 (19)), 0,8 (s, 3H, CH3(18)).
Следуя аналогичной методике и используя соответствующие исходные материалы, получают 1-(3-оксоандрост-4-ен-17β-карбонил)-3,3-диметилмочовину.
Пример 12. 1-метил-1-(3-оксоандрост-4-он-17β-карбонил)-3,3-диэтилмочевина [соединение (VI): Y = 0, R1 = CH, R2 = R3 = Et].
К суспензии гидрида калия (275 мг) в безводном тетрагидрофуране (2 мл) в атмосфере азота добавляли твердую N,N-диэтилмочевину (33 мг), смесь перемешивали при комнатной температуре в течение 10 мин и затем нагревали с обратным холодильником в течение 2 ч.
После охлаждения при комнатной температуре по каплям в течение 5 мин добавляли ацилхлорид, приготовленный из 95,0 мг 3-оксоандрост-4-ен-17β-карбоновой кислоты, следуя методике, описанной в примере 10.
Смесь перемешивали при комнатной температуре в течение 1,5 ч и добавляли метилиодид (0,168 мл) по каплям.
После перемешивания при комнатной температуре в течение 1,5 ч реакционную смесь охлаждали до около 0oC и медленно добавляли воду.
Экстракция этилацетатом, обезвоживание сульфатом натрия и выпаривание растворителя под вакуумом обеспечивают 115 мг сырого желтого маслообразного продукта, который очищали с помощью флэш-хроматографии на силикагеле (элюент: н-гексан/этилацетат 65:35), получая таким образом 52 мг вещества, указанного в названии (т. пл. 142-145oC).
ЯМР (CDCl3): 5,7 (m, 1H, (H (4)), 3,3 (q, 4Н, 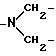 ), 2,98 (s, 3H, N-CH3), 1,15 (т, 6Н, 2N-CH2CH3), 1,1 (s, 3H, CH3(13)), 0,8 (S, 3H, CH3 (18)).
), 2,98 (s, 3H, N-CH3), 1,15 (т, 6Н, 2N-CH2CH3), 1,1 (s, 3H, CH3(13)), 0,8 (S, 3H, CH3 (18)).
По аналогичной методике и используя соответствующие исходные материалы, получают перечисленные ниже вещества:
1-этил-1-(3-оксоандрост-4-ен-17β-карбонил)-3,3-диэтилмочевина;
1-метил-1-(3-оксоандрост-4-ен-17β-карбонил)-3,3-диметилмочевина;
1-этил-1-(3-оксоандрост-4-ен-17β-карбонил)-3,3-диметилмочевина.
Пример приготовления лекарственной формы.
Таблетки для перорального применения с риском с содержанием в каждой 250 мг активного вещества были получены следующим образом.
Состав (на 10000 таблеток), г:
17β-N-изопропил-N-(N-изопропилкарбамоил)карбамоиландрост-3,5-диен-3-карбоновая кислота - 2500
Кукурузный крахмал - 275
Тальк - 187
Стеарат кальция - 38
Активное вещество гранулировали с 4 мас. %/об. водным раствором метилцеллюлозы.
К высушенным гранулам добавляли остальные ингредиенты и окончательную смесь прессовали в таблетки соответствующей массы.
Изобретение относится к ингибиторам стероидной 5альфа-редуктазы, имеющим следующую формулу: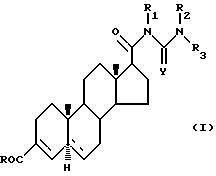
где Y - кислород или сера; R - группа: а) -OR4, где R4 - водород или C1-С6 алкильная группа; б) 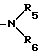 , где каждый из R5 и R6 независимо водород или C1-C6 алкильная группа; в)
, где каждый из R5 и R6 независимо водород или C1-C6 алкильная группа; в) 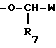 , где R7 - водород или C1-C6 алкильная группа, W - группа; (I)
, где R7 - водород или C1-C6 алкильная группа, W - группа; (I) 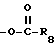 , где R8 - C1-C6 алкильная группа, C5-C6 циклоалкильная группа, C6-C9 циклоалкилалкильная группа, фенильная группа или беннзильная группа; или (II)
, где R8 - C1-C6 алкильная группа, C5-C6 циклоалкильная группа, C6-C9 циклоалкилалкильная группа, фенильная группа или беннзильная группа; или (II) 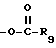 , где R9 - C1-C6 алкильная группа или C5-C6 циклоалкильная группа, или (III)
, где R9 - C1-C6 алкильная группа или C5-C6 циклоалкильная группа, или (III) 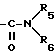 , где R5 и R6 определены выше; г)
, где R5 и R6 определены выше; г) 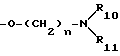 , где каждый из R10 и R11 - независимо водород или C1-C6 алкильная группа или оба вместе с атомом азота, с которым они связаны, образуют пентатомное или гексатомное насыщенное гетеромоноциклическое кольцо, по желанию включающее по крайней мере один дополнительный гетероатом, выбранный из кислорода и азота; n - целое число от 2 до 4; R1 - водород, C1-C6 алкильная группа, C5-C6 циклоалкильная группа, C6-C9 циклоалкилалкильная группа или арильная группа; каждая из R2 и R6 независимо выбраны из группы, состоящей из водорода, C1-C6 алкила, C5-C6 циклоалкила, C6-C9 циклоалкилалкила и арила или R2 и R3 вместе с атомом азота, с которым они связаны, образуют пентатомное или гексатомное насыщенное гетеромоноциклическое кольцо, по желанию включающее по крайней мере один дополнительный готероатом, выбранный из кислорода и азота; символ
, где каждый из R10 и R11 - независимо водород или C1-C6 алкильная группа или оба вместе с атомом азота, с которым они связаны, образуют пентатомное или гексатомное насыщенное гетеромоноциклическое кольцо, по желанию включающее по крайней мере один дополнительный гетероатом, выбранный из кислорода и азота; n - целое число от 2 до 4; R1 - водород, C1-C6 алкильная группа, C5-C6 циклоалкильная группа, C6-C9 циклоалкилалкильная группа или арильная группа; каждая из R2 и R6 независимо выбраны из группы, состоящей из водорода, C1-C6 алкила, C5-C6 циклоалкила, C6-C9 циклоалкилалкила и арила или R2 и R3 вместе с атомом азота, с которым они связаны, образуют пентатомное или гексатомное насыщенное гетеромоноциклическое кольцо, по желанию включающее по крайней мере один дополнительный готероатом, выбранный из кислорода и азота; символ 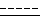 обозначает одинарную или двойную связь, при условии, что, когда это двойная связь, водород в 5α-положении отсутствует, и его фармацевтически приемлемые соли. Благодаря их ингибирующей активности в отношении 5α-редуктазы, вещества этого изобретения могут быть пригодны при лечении состояний, зависящих от уровня андрогенов, 2 с. и 4 з.п. ф-лы.
обозначает одинарную или двойную связь, при условии, что, когда это двойная связь, водород в 5α-положении отсутствует, и его фармацевтически приемлемые соли. Благодаря их ингибирующей активности в отношении 5α-редуктазы, вещества этого изобретения могут быть пригодны при лечении состояний, зависящих от уровня андрогенов, 2 с. и 4 з.п. ф-лы.
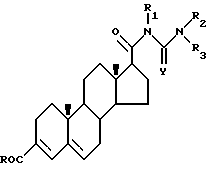
где Y кислород или сера;
R группа: a) -OR4, где R4 водород или С1 - С6-алкильная группа,
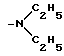
b) -NR5R6, где каждый из R5, R6 независимо - водород или С1 С6-алкильная группа;
c) -O-CHR7-W, где R7 водород или С1 - С6-алкильная группа и W группа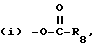
где R8 C1 C6-алкильная группа или С5 - С6-циклоалкильная группа, или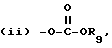
где R9 C1 C6-алкильная группа или С5 - С6-циклоалкильная группа;
или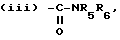
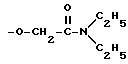
где R5 и R6 имеют указанные значения;
или d) -O-(CH2)n-NR1 0R1 1, где каждый из R1 1 и R1 1 независимо водород или С1 С6-алкильная группа или взятые вместе с атомом азота, к которому они присоединены, образуют 5- или 6-атомное насыщенное гетеромоноциклическое кольцо, необязательно содержащее по крайней мере один дополнительный гетероатом, выбранный из кислорода и азота, n 2, 3, 4;
R водород, С1 С6-алкильная группа или С5 - С6-циклоалкильная группа;
R2 и R3 каждый независимо выбран из группы, состоящей из водорода, С1 С6-алкильной группы или С5 - С6-циклоалкильной группы, или R2 и R3, взятые вместе с атомом азота, к которому они присоединены, образуют 5- или 6-атомное насыщенное гетеромоноциклическое кольцо, необязательно содержащее по крайней мере один дополнительный гетероатом, выбранный из кислорода и азота,
или его фармацевтически приемлемые соли.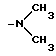
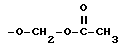
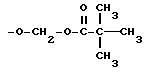
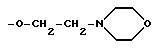
R1 метил, этил, изоприл, трет-бутил, циклогексил;
Группа -NR2R3 представляет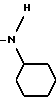
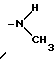
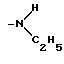
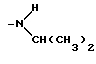
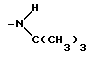
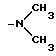
или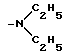
и его фармацевтически приемлемые соли.
и в соответствующих случаях его фармацевтически приемлемые соли.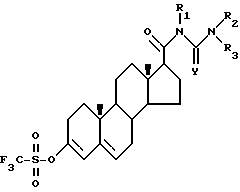
где Y, R1 R3 имеют значения, определенные в п.1,
подвергают взаимодействию с моноокисью углерода (СО) в присутствии С1 С6-алкилового спирта и, если необходимо, соединение формулы I, полученное таким образом, в котором R4 C1 - C6-алкильная группа, превращают с помощью селективного гидролиза в соответствующее соединение формулы I, где R4 водород, и/или, если необходимо, превращают соединение формулы I в его соль, или превращают соль соединения формулы I в соответствующее свободное соединение, и/или, если необходимо, разделяют смесь изомеров соединение формулы I на индивидуальные изомеры.
| EP, 0427434, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| EP, 0289327, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| US, патент 4377584, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1998-02-10—Публикация
1992-05-22—Подача