Извлечение ионов тяжелых металлов из водных растворов относится к области извлечения веществ из водных растворов с использованием сорбентов и/или флокулянтов при реагентном осаждении, способ может быть использован в цветной и черной металлургии, а также для очистки промышленных и бытовых стоков.
Известен способ ионообменной очистки сточных вод [1], в котором для очистки сточных вод используют глинистые алюмосиликатные минералы, в основном, бентонитовые глины.
Недостатком данного способа является отсутствие оптимальных условий использования глин для извлечения катионов, что приводит к повышенному расходу реагентов.
Наиболее близким техническим решением является способ извлечения ионов тяжелых металлов с помощью бентонитовых глин [2], в котором использовали модельные растворы сульфатов меди, цинка, кадмия и кальция с концентрацией исходных растворов по металлу 16 - 80 мг/дм3, временем перемешивания 30 мин, отстаивания - 2 ч, расходом бентонитовых глин без дополнительного использования нейтрализатора не менее 15 - 20 г/дм3, при этом бентонитовые глины медленно отстаивались.
С целью повышения степени осветления растворов использовали активированную глину, полученную обработкой последней в гидротермальных условиях 10% раствором щелочи при 105 - 110oC в течение 5 - 6 ч.
Расход активированной глины составил 10 г/дм3, время перемешивания 30 мин, отстаивания - 2 ч. Степень очистки от ионов меди, цинка и кадмия составила соответственно, %: 99,8; 99,7; 98,8. Растворы полностью осветляются после отстаивания в течение 30 мин, при этом степень очистки от взвешенных веществ составляет 95 - 98%.
Недостатками способа являются сложность предварительной подготовки активированной глины, большие расходы глины и других реагентов, неизменность соотношения составов глины и нейтрализатора - щелочи, последняя содержится в составе активированной глины.
Задачей изобретения является создание оптимальных условий извлечения ионов тяжелых металлов из водоемких стоков с солесодержанием, способствующим образованию коллоидных, мелкодисперсных систем с трудноосаждаемыми взвесями.
Технический результат, который может быть достигнут при осуществлении изобретения, заключается в экономичности процесса за счет сокращения расхода реагентов и количества технологических стадий, а также за счет получения плотного осадка с низким влагосодержанием.
Этот технический результат достигается тем, что в известном способе, включающем введение в исходный раствор бентонитовой глины с нейтрализатором, бентонитовую глину вводят разово в количестве не более 5,0 г/дм3, при этом осветленную водную фазу отделяют декантацией, а осадок многократно подвергают контакту со следующими порциями исходного раствора с последующей декантацией осветленной водной фазы. Контакт осадка со следующими порциями исходного раствора осуществляют до соотношения Ж:Т≤2:1. Введение нейтрализатора осуществляют до величины pH, лежащей в пределах значений 4,0≤pH≤12,0.
Сущность способа поясняется технологической схемой процесса, изображенной на чертеже.
Примеры конкретного осуществления способа.
В качестве исходного раствора использовали сточную воду промышленного предприятия, состав которой по основным компонентам представлен в табл. 1.
Исходный раствор пропускали через тщательно отмытый кварцевый песок для удаления взвешенных веществ.
Бентонитовая глина содержала в качестве основных компонентов алюминий, кремний, железо, магний, кальций, а в качестве примесей - натрий, барий, марганец, титан.
В глине содержались кварц, кальцит, пирит и другие минералы.
Глина набухала значительно в щелочной среде и незначительно - в кислой.
Состав глины по фракциям приведен в табл. А.
Пример 1 (табл. 2, опыты 1.1. - 1.5).
В соответствии с технологической схемой процесса, изображенной на фиг., в 200 см3 исходного раствора добавили 0,5 г бентонитовой глины (Cглины = 2,5 г/дм3), и одновременно с этим при непрерывном перемешивании проводили нейтрализацию раствора 10% раствором щелочи NaOH до оптимальной величины pH осаждения ионов тяжелых металлов, равной для данного раствора значению 9,5 - 10,5. За время перемешивания 10 мин, отстаивания 15 мин возникала четкая граница раздела между раствором и осадком. Объем осадка оценивали в процентах ко всему объему системы. Осветленную водную фазу отделяли от осадка декантацией, к осадку приливали новую порцию исходного раствора до объема 200 см3, проводили нейтрализацию до pH = 9,5 - 10,5 при непрерывном перемешивании и последующем отстаивании, как было описано выше. Подобную процедуру повторяли пять раз, при этом всякий раз измеряли объемы осадка и осветленной водной фазы, в последнем определяли концентрацию ионов тяжелых металлов. На всех этапах проведения экспериментов контролировали величину pH с помощью pH-метра и расход нейтрализатора.
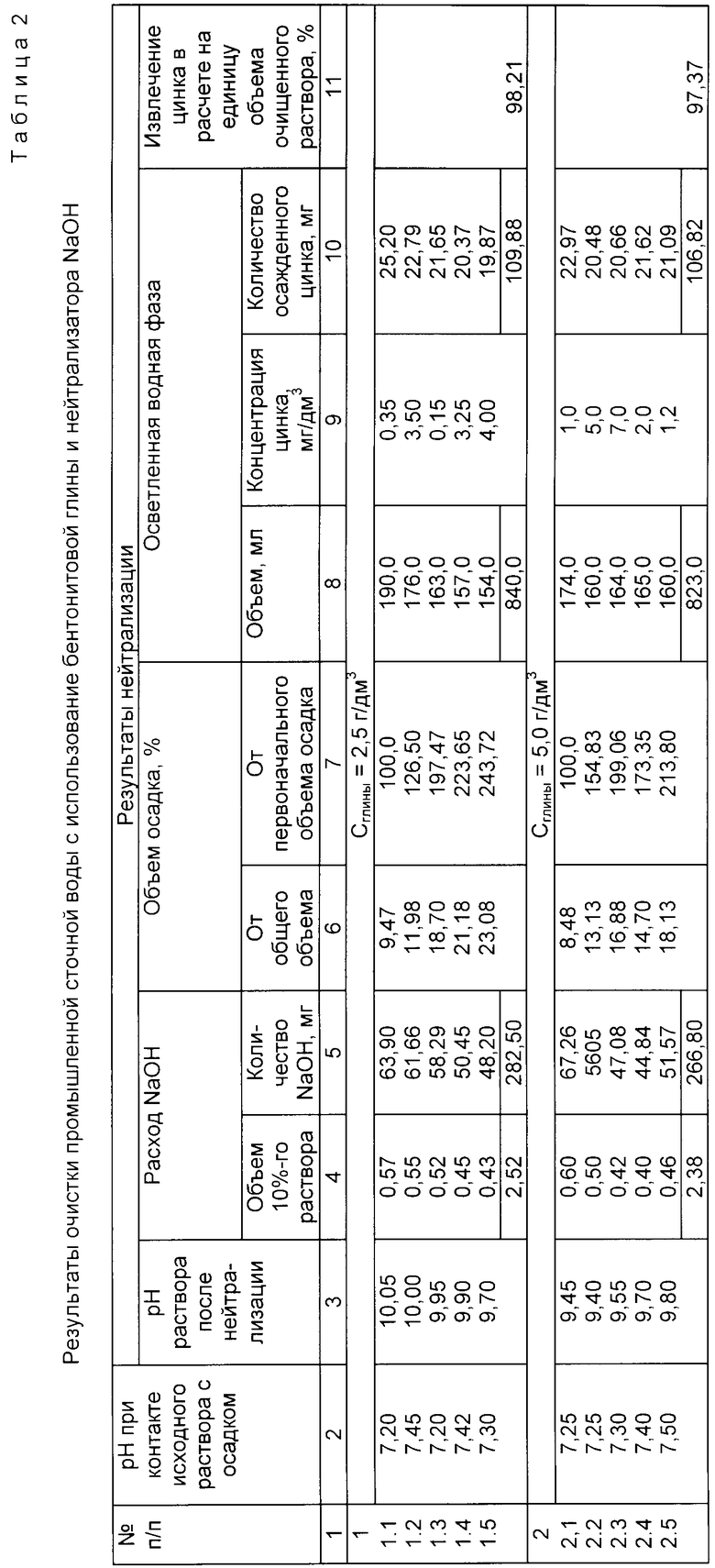
В табл. 2 даны результаты очистки промышленной сточной воды с использованием бентонитовой глины и нейтрализатора NaOH, причем концентрация и извлечение ионов тяжелых металлов даны по основному компоненту исходного раствора - цинку.
Из данных табл. 2 (опыты 1.1 - 1.5) можно сделать следующие выводы:
1. Извлечение цинка из раствора составляет 98,2%.
2. Осадки, полученные в предыдущих стадиях нейтрализации, способствуют нейтрализации исходного раствора.
Многократный контакт осадка с новыми порциями очищаемого раствора повышает величину pH последнего, что способствует удалению примесей и сокращает расход реагентов.
Пример 2 (табл. 2, опыты 2.1 - 2.5).
Эксперименты проводили аналогично опытам 1.1 - 1.5 табл. 2 с той лишь разницей, что к 200 см3 раствора добавляли 1,0 г бентонитовой глины (Cглины = 5 г/дм3), т.е. в два раза больше.
Из данных табл. 2 (опыты 1.1 - 1.5 и 2.1 - 2.5) следует, что увеличение количества добавляемой глины приводит к образованию более плотных осадков и сокращает расход нейтрализатора.
Пример 3 (табл. 3, опыты 1.1 - 1.5).
Эксперименты проводили аналогично опытам 1.1 - 1.5 табл. 2, но в качестве нейтрализатора использовали более дешевый по сравнению со щелочью - гашеную известь Ca(OH)2 в виде известкового раствора с концентрацией 1,496 г/дм3 по CaO.
Сравнение данных опытов 1.1 - 1.5 табл. 2 и 3 свидетельствует о том, что при использовании в качестве нейтрализатора CaO образуются более плотные осадки.
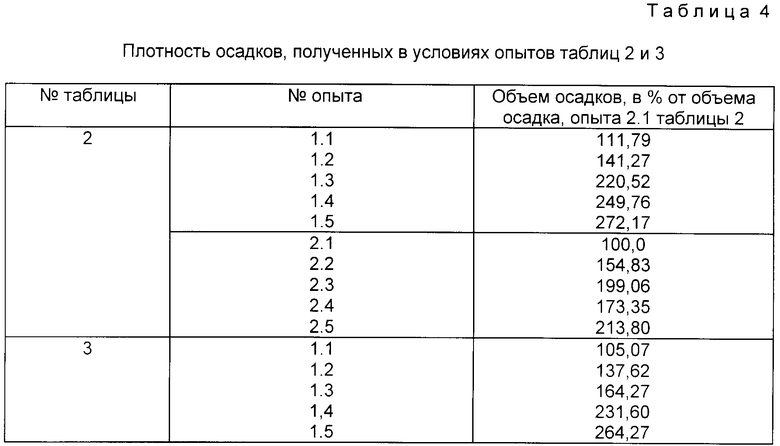
В табл. 4 представлены данные о плотности осадков, полученных в условиях опытов табл. 2 и 3.
Для сравнения плотность всех осадков определялась по отношению к наиболее плотному осадку, полученному в опыте 2.1 табл. 2, его плотность принята за 100%.
Из данных табл. 4 следует, что наиболее плотные осадки образовались в опытах 2.1, 1.1 (табл. 2) и 1.1 (табл. 3).
В табл. 5 дана характеристика осадков, полученных в условиях опытов табл. 2 и 3.
Из данных табл. 5 следует, что глина способствует уменьшению влажности осадков и увеличению их плотности, использование в качестве нейтрализатора CaO по сравнению со щелочью дает более плотные с меньшей влажностью осадки.
В табл. 6 дан расход реагентов в расчете на 1 м3 очищенного раствора, полученный по данным опытов табл. 2 и 3.
Из данных табл. 6 следует, что увеличение количества глины снижает расход нейтрализатора, особенно, если в качестве нейтрализатора используется известь.
Опытами установлено, что в присутствии глины снижается содержание кальция в растворе, из раствора удаляются соединения серы низших степеней окисления, возрастает извлечение металлов.
Осветленная водная фаза отделяется от осадка декантацией, минуя трудоемкую операцию фильтрации обычно влагоемких гидрофильных осадков, образующихся из больших объемов очищаемых растворов.
Осветленная водная фаза может быть использована в технологических целях, а осадки различными способами переработаны в полезные продукты.
Очистка, особенно больших объемов, загрязненных производственных растворов предлагаемым способом экологически безвредна и экономически выгодна.
Количество контактов данного осадка с новыми порциями исходного раствора определяется составом и объемом очищаемого раствора, однако с технологической и экономической точек зрения отвечает оптимуму Ж:Т≤2:1.
Диапазон величины pH осаждения ионов тяжелых металлов определяется качественным и количественным составами очищаемого раствора и зависит от величины pH полного осаждения удаляемых ионов, для многих технологических сточных вод этот диапазон находится в пределах 4,0≤pH≤12,0.
В технологической схеме, представленной на фигуре, нейтрализатор и бентонитовая глина введены одновременно на стадии перемешивания и нейтрализации раствора до оптимальных значений pH. Однако, как показали эксперименты, введение глины на стадии отстаивания после нейтрализации раствора не ухудшает результаты очистки производственных сточных вод.
По сравнению с прототипом предлагаемый способ упрощает технологический процесс, нет необходимости в предварительной сложной обработке бентонитовой глины, многократный контакт осадка с новыми порциями исходного раствора сокращает расход нейтрализатора и бентонитовой глины, позволяет получать плотные осадки, которые содержат меньше влаги и быстро теряют ее на открытом воздухе.
Более 50% влаги удаляется из осадка сушкой на воздухе в течение суток, более 90% влаги удаляется при сушке на воздухе в течение двух суток или прокаливанием при 200oC не более двух часов.
Образование более плотных осадков способствует сокращению времени и повышению степени осветления раствора, что позволяет отказаться от трудоемкой стадии фильтрации труднофильтрующихся гидрофильных осадков, перейдя к отделению осветленной водной фазы от осадка декантацией.
Предлагаемый способ позволяет реализовать безотходную, экологически безвредную, экономически выгодную технологию с переработкой осадка в полезные продукты и возвратом очищенной осветленной водной фазы в технологический процесс.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОСАЖДЕНИЯ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ ИЗ ВОДНЫХ РАСТВОРОВ | 1996 |
|
RU2113519C1 |
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД | 1995 |
|
RU2107039C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ ИЗ ВОДНЫХ РАСТВОРОВ | 1996 |
|
RU2106415C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ МЕТАЛЛОВ ИЗ ВОДНЫХ РАСТВОРОВ | 2004 |
|
RU2256710C1 |
| СПОСОБ СОВМЕСТНОГО ИЛИ СЕЛЕКТИВНОГО ИЗВЛЕЧЕНИЯ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ ИЗ ВОДНЫХ РАСТВОРОВ | 2004 |
|
RU2263718C1 |
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ЭМУЛЬГИРОВАННОЙ ОГРАНИЧЕСКОЙ ФАЗЫ | 1995 |
|
RU2091325C1 |
| СПОСОБ ЭКСТРАКЦИИ МЕДИ ИЗ ВОДНОГО РАСТВОРА | 1996 |
|
RU2104315C1 |
| СПОСОБ УДАЛЕНИЯ ДИСПЕРГИРОВАННЫХ И ЭМУЛЬГИРОВАННЫХ МАСЕЛ ИЗ СТОЧНЫХ ВОД | 1994 |
|
RU2093241C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ НИКЕЛЯ ИЗ ВОДНЫХ РАСТВОРОВ С ВЫСОКИМ СОДЕРЖАНИЕМ СОЛЕЙ СУЛЬФАТА НАТРИЯ | 2001 |
|
RU2221883C2 |
| СПОСОБ АДСОРБЦИИ ИОНОВ ИЗ РАСТВОРОВ | 1994 |
|
RU2091317C1 |




Использование: очистка промышленных и бытовых стоков от ионов тяжелых металлов. Сущность: исходный раствор подвергают нейтрализации до величины pH, лежащей в пределах значений 4,0≤pH≤12,0, одновременно с этим в исходный раствор разово вводят бентонитовую глину в количестве не более 5,0 г/дм3, осветленную водную фазу отделяют декантацией, а осадок многократно подвергают контакту со следующими порциями исходного раствора до соотношения Ж: Т≤2: 1 с последующей декантацией осветленной водной фазы. 2 з.п. ф-лы, 7 табл., 1 ил.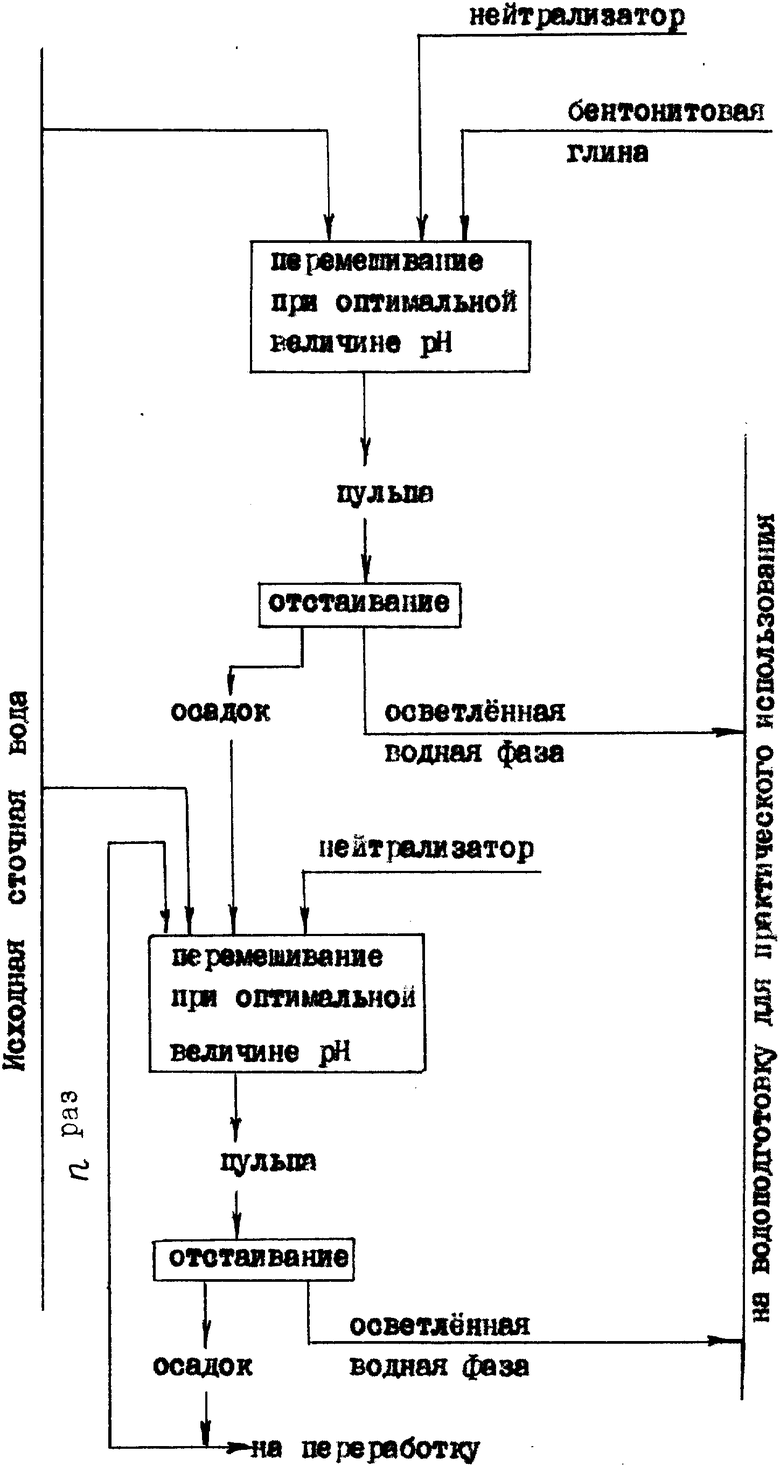
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Аширов А.А | |||
| Ионообменная очистка сточных вод, растворов и газов | |||
| - Л.: Химия, Ленинградское отделение, 1983 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Водооборот, очистка промышленных сточных вод и эксплуатация хвостохранилищ | |||
| - Алма-Ата: Институт "Казмеханобр", 1983, с | |||
| Огнетушитель | 0 |
|
SU91A1 |
Авторы
Даты
1998-02-10—Публикация
1996-08-15—Подача