Изобретение касается нового способа получения соединения общей формулы I.
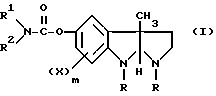
где
R - низший алкил,
R1 - атом водорода,
R2 - низший алкил, низший циклоалкил, низший циклоалкил-низший алкил, низший бициклоалкил, арил или арил-низший алкил, или
R1 и R2 - образуют вместе с атомом азота, с которым они связаны, группу 3,4-дигидро-2(1Н)-изохинолина,
X - низший алкил, низший алкокси, атом галогена или трифторметильная группа,
m - равняется 0,1 или 2,
который включает взаимодействие соединения общей формулы II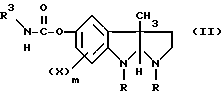
где
R, X и m имеют значения, указанные выше, а R3 - низший алкил, с алкиллитием или алкоголятами щелочных металлов, а затем с карбоновой кислотой общей формулы R5COOH, в которой R5 - низший алкил, с получением в результате соединения общей формулы III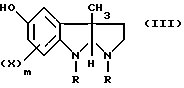
где
R, X и n имеют значения, указанные выше;
b) взаимодействие реакционной смеси, содержащей соединение общей формулы III,
с изоцианатом общей формулы; R2NCO и выделение соединения общей формулы I.
Другим аспектом изобретения является новый способ получения соединения общей формулы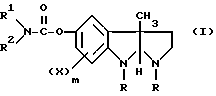
где
R - низший алкил,
R1 - атом водорода,
R2 - низший алкил, низший циклоалкил, низший циклоалкил-низший алкил, низший бициклоалкил, арил или арил-низший алкил, или
R1 и R2 - образуют вместе с атомом азота, с которым они связаны, группу 3,4-дигидро-2(1Н)-изохинолина,
X- низший алкил, низший алкокси, атом галогена или трифторметильная группа,
m - равняется 0, 1 или 2,
который включает взаимодействие соединения общей формулы II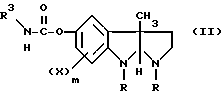
где
R, X и m имеют значения, указанные выше, а R3 - низший алкил, с алкиллитием или алкоголятами щелочных металлов, а затем с карбоновой кислотой общей формулы R5COOH, в которой R5 - низший алкил, с получением в результате соединения общей формулы III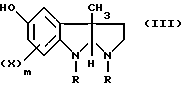
где
R, X и m имеют значения, указанные выше, с последующим взаимодействием реакционной смеси, содержащей соединение общей формулы III, с соединением общей формулы IV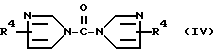
где
R4 - атом водорода или низший алкил, в присутствии карбоновой кислоты общей формулы R5 COOH, в которой R5 имеет значение, указанное выше, и получение соединения общей формулы V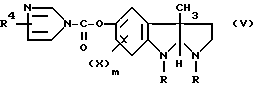
где
R, R4, X и m имеют значения, указанные выше, и контактирование полученной реакционной смеси, содержащей соединение общей формулы V, с соединением общей формулы R1R2NH, в которой R1 и R2 имеют значения, указанные выше, и выделение соединения общей формулы I.
Полученные соединения могут быть пригодными для использования в качестве улучшающих память и обезболивающих агентов.
Если иное не оговаривается и не обозначается, понятие "низший алкил" подразумевает прямую или разветвленную алкильную группу, имеющую от 1 до 6 атомов углерода. Примерами таких алкильных групп являются метильная, этильная, н-пропильная, изо-бутильная, пентильная и гексильная.
Если иное не оговаривается и не обозначается, понятие "циклоалкил" подразумевает насыщенное кольцо, содержащее от 3 до 7 атомов углерода. Примерами таких циклоалкильных групп являются циклопропильная, циклогексильная и циклогептильная.
Если иное не оговаривается и не обозначается, понятие "бициклоалкил" подразумевает группу, содержащую от 7 до 11 атомов углерода.
Если иное не оговаривается и не обозначается, понятие "галоген" подразумевает атом фтора, хлора, брома или йода.
Если иное не оговаривается и не обозначается, понятие "арил" подразумевает незамещенную фенильную или ароматическую гетероциклическую группу или фенильную или ароматическую гетероциклическую группу, замещенную 1, 2 или 3 заместителями, каждый из которых может независимо быть низшей алкильной группой, низшей алкоксильной группой, атомом галогена, гидроксильной группой, трифторметильной группой, феноксигруппой или бензилоксигруппой.
Другие способы получения производных физостигмина карбамата известны. См. , например, Хамер, патент США 3.791.107 и Брафани, патент США 4.831.155. Однако остается необходимость повышения выхода и снижения стоимости продукта.
Способ по настоящему изобретению обеспечивает более высокий выход целевого продукта. В предпочтительном варианте осуществления изобретения также обеспечивается "однообъемный" процесс, в котором промежуточные продукты не выделяются, что позволяет избежать дополнительных расходов и временных затрат, связанных с выделением промежуточных соединений.
Было найдено, что реакцию получения соединения общей формулы III выгодно выполнять, используя в качестве основания алкиллитий, например н-бутиллитий, предпочтительно в алифатическом углеводороде как растворителе, например в смеси гексанов, или алкоголят щелочных металлов, например трет-бутилат калия, и предпочтительно трет-бутилат калия. Обычно реакцию выполняют в органическом растворителе, таком как тетрагидрофуран, диметилформамид, 1,2-диметоксиэтан, 2-метоксиэтиловый эфир, диоксан или диэтиловый эфир, предпочтительно тетрагидрофуран, при температуре от приблизительно 0oC до приблизительно 50oC, предпочтительно от приблизительно 10oC до приблизительно 30oC.
Добавляют приблизительно один эквивалент низшей алкил-карбоновой кислоты, такой как, например, уксусная кислота, для доведения значения pH от приблизительно 13 до приблизительно 8, предпочтительно от приблизительно 9 до приблизительно 10, наиболее предпочтительно до приблизительно 9,5.
Затем к реакционной смеси добавляют или алкилизоцианат, или замещенный алкилизоцианат для образования соединения общей формулы I (в котором R1 - атом водорода), или карбамоилирующий агент, такой как карбонилдиимидазол для образования соединения общей формулы V.
В том случае, когда добавляют алкилизоцианат для получения соединения общей формулы I, реакцию проводят обычно при температуре между приблизительно 0oC и приблизительно 25oC, предпочтительно от приблизительно 5oC до приблизительно 10oC. Условия реакции контролируют и поддерживают значение pH между приблизительно 9 и 10 добавлением основания, такого как, например, трет-бутилат калия, или кислоты, такой как, например, уксусная кислота.
В том случае, когда добавляют карбонилдиимидазол для получения соединения общей формулы IV, то его добавление осуществляют при температуре от приблизительно -30oC до приблизительно 25oC, предпочтительно в пределах от -20oC до -30oC, когда трет-бутилат калия используют как основание.
Реакционную смесь, содержащую соединение общей формулы IV, затем предпочтительно подкисляют до величины от приблизительно 4 до приблизительно 6, более предпочтительно от приблизительно 4,5 до приблизительно 6, наиболее предпочтительно приблизительно до 5,5, кислотой, такой как, например, уксусная кислота, и добавляют амин, такой как тетрагидроизохинолин, для обеспечения хорошего выхода соединения общей формулы I.
Добавление амина обычно проводят при температуре от приблизительно -15oC до приблизительно 25oC, предпочтительно от приблизительно 10 до 20oC.
Свободное основание - исходный материал общей формулы II, такой как физостигмин, может быть получен из его соли, такой как салицилат, обработкой ее основанием, таким как карбонат натрия, в смеси воды и несмешивающегося органического растворителя, такого как, например, дихлорметан, этилацетат или толуол, и используется в способе по настоящему изобретению без дальнейшей очистки.
Следующие примеры лишь иллюстрируют изобретение, но не ограничивают его. Все значения температуры даны в градусах Цельсия, если не указывается иное.
Пример 1. (3aS-цис) -1,2,3,3a,8,8a-гексагидро- 1,3а,8-триметилпирроло [1,3-b]индол-5-ил3,4-дигидро-2(1Н)-изохинолинкарбоксилат.
К раствору физостигмина (1 г) в сухом тетрагидрофуране (10 мл) в атмосфере азота при температуре 10oC добавляют 2,5 М н-бутиллития в гексане (1,5 мл) в течение 0,25 часа. После 0,5 часа выдерживания при температуре 20oC смесь содержит физостигмин (II) и эзеролин (III) в виде фенолята лития (pH 12) в соотношении 2/98, определенном методом высокоэффективной жидкостной хроматографии (ВЭЖХ). Добавление ледяной уксусной кислоты (0,22 г, pH 9,5), а затем 1,1'-карбонилдиимидазола (0,59 г) и выдерживание реакционной смеси при температуре 20oC в течение 0,25 часа приводит к соотношению в смеси имидазолкарбонильного промежуточного продукта (V) и эзеролина 96/4, определенному ВЭЖХ. Добавление 1,2,3,4-тетрагидроизохинолина (0,6 мл, 1,3 эквивалента) приводит после 0,5 часа выдержки при температуре 25oC к получению смеси, содержащей (3aS-цис)-1,2,3,3а, 8,8а-гексагидро-1,3а,8-триметилпирроло[2,3-b] индол-5-ил 3,4- дигидро-2(1Н)-изохинолинкарбоксилат и эзеролин в соотношении 75/25, определенном методом ВЭЖХ.
Пример 2. (3aS-цис) -1,2,3,3а,8,8а-гексагидро-1,3а,8- триметилпирроло [2,3-b]индол-5-ил 3,4-дигидро-2 (1Н) - изохинолинкарбоксилат.
К раствору физостигмина (1 г) в сухом тетрагидрофуране (10 мл) в атмосфере азота при температуре 10oC добавляют 2,5 М н-бутиллития в гексане (1,5 мл) в течение 0,25 часа. После 0,5 часа выдерживания при температуре 20oC смесь содержит физостигмин (II) и эзеролин (III) в виде фенолята лития (pH 11,5) в соотношении 2/98, определенном методом ВЭЖХ. Добавление 1,1'-карбонилдиимидазола (0,59 г, 1,0 эквивалента) и выдерживание реакционной смеси при температуре 20oC в течение 0,25 часа приводит к соотношению в смеси имидазолкарбонильного промежуточного продукта (V) и эзеролина 98/2, определенному методом ВЭЖХ. Добавление 1,2,3,4-тетрагидроизохинолина (0,6 мл, 1,3 эквивалента, pH 11,5) приводит после 0,5 часов выдержки при температуре 25oC к получению смеси, содержащей (3aS-цис)-1,2,3,3а,8,8а-гексагидро-1,3а, 8- триметилпирроло[2,3-b]индол-5-ил 3,4-дигидро-2(1Н)- изохинолинкарбоксилат и эзеролин в соотношении 55/45, определенном методом ВЭЖХ.
Пример 3. (3aS-цис) -1,2,3,3а, 8,8а-гексагидро-1, За,8-триметилпирроло[2,3-b]индол-5-ил 3,4-дигидро-2 (1Н) - изохинолинкарбоксилат.
К раствору физостигмина (6,88 г) в сухом тетрагидрофуране (69 мл) в атмосфере азота при температуре 15oC добавляют 2,5 М н-бутиллития в гексане (10,5 мл) в течение 0,25 часа. После 0,5 часа выдерживания при температуре 20oC смесь содержит физостигмин (II) и эзеролин (III) в виде фенолята лития (pH 11) в соотношении 2/98, определенном методом ВЭЖХ. Добавление ледяной уксусной кислоты (1,5 мл, 1 эквивалент, pH 9,5), а затем 1,1'-карбонилдиимидазола (4,25 г, 1,05 эквивалента) и выдерживание реакционной смеси при температуре 20oC в течение 1 часа приводит к соотношению в смеси имидазолкарбонильного промежуточного продукта и эзеролина 99/1, определенному методом ВЭЖХ. Добавление ледяной уксусной кислоты (7,15 мл, 5 эквивалентов, pH 5), а затем 1,2,3,4-тетрагидроизохинолина (3,7 г, 1,1 эквивалента, добавление в течение 5 минут) приводит после 15 часов выдержки при температуре 25oC к получению смеси, содержащей (3aS-цис)-1,2,3,3a,8,8a- гексагидро-1,3a,8-триметилпирроло[2,3-b] индол-5-ил 3,4-дигидро-2 (1Н)-изохинолинкарбоксилат и эзеролин в соотношении 96/4, определенном методом ВЭЖХ.
Пример 4. (3aS-цис) -1,2,3,3a, 8,8a-гексагидро-1,3a,8- триметилпирроло[2,3-b]индол-5-ил 3,4-дигидро-2(1Н)-изохинолинкарбоксилат.
К раствору физостигмина (68,8 г) в сухом тетрагидрофуране (690 мл) в атмосфере азота при температуре 15oC добавляют 2,5 М н-бутиллития в гексане (102 мл) в течение 0,25 часа. Выдерживают смесь 0,5 часа при температуре 15oC, обрабатывают ледяной уксусной кислотой (14,6 мл, 1 эквивалент, pH 10). Полученная смесь содержит физостигмин (II) и эзеролин (III) в соотношении 1/99, определенном методом ВЭЖХ. Добавление 1,1'-карбонилдиимидазола (44,6 г, 1,1 эквивалент) и выдерживание реакционной смеси при температуре 20oC в течение 1 часа приводит к соотношению в смеси имидазолкарбонильного промежуточного продукта (V) и эзеролина 89/1, определенному методом ВЭЖХ. Добавление ледяной уксусной кислоты (85,9 мл, 6 эквивалентов, pH 5), а затем 1,2,3,4-тетрагидроизохинолина (37 г, 1,1 эквивалента, добавление в течение 5 минут) приводит после 15 часов выдержки при температуре 25oC к получению смеси, содержащей (3aS-цис)-1,2,3,3a,8,8a-гексагидро-1,3a,8-триметилпирроло[2,3-b] индол-5-ил 3,4-дигидро-2 (1Н)-изохинолинкарбоксилат и эзеролин в соотношении 98/2, определенном методом ВЭЖХ.
Пример 5. (3aS-цис) -1,2,3,3a, 8,8a-гексагидро-1,3a,8- триметилпирроло[2,3-b]индол-5-ил 3,4-дигидро-2 (1Н)-изохинолинкарбоксилат.
К раствору физостигмина (2,75 г) в сухом тетрагидрофуране (28 мл) в атмосфере азота при температуре 25oC добавляют трет-бутилат калия (1,28 г) в течение 0,25 часа. Смесь выдерживают 0,5 часа при температуре 25oC и обрабатывают ледяной уксусной кислотой (0,6 мл, 1 эквивалент, pH 10). Полученная смесь содержит физостигмин (II) и эзеролин (III) в соотношении 1/99, определенном методом ВЭЖХ. Добавление 1,1'-карбонилдиимидазола (1,92 г, 1,2 эквивалента) порциями в 1,0-0,05-0,05-0,1 эквивалента при интервалах в 0,25 часа при температуре 20oC давало спустя 10 минут после добавления каждой порции следующие соотношения в смеси имидазолкарбонильного промежуточного продукта (V) и эзеролина: 95/5, 96/4, 97/3 и 98/2, определенные методом ВЭЖХ. Последующее добавление ледяной уксусной кислоты (3,4 мл, 6 эквивалента, pH 5), а затем 1,2,3,4-тетрагидроизохинолина (1,6 г, 1,2 эквивалента, добавление в течение 0,5 часа при температуре 15oC), приводит после 15 часов выдержки при температуре 25oC к получению смеси, содержащей (3aS-цис) -1,2,3,3a,8,8a-гексагидро-1,3a,8-триметилпирроло [2,3-b]индол-5-ил 3,4-дигидро-2 (2Н) - изохинолинкарбоксилат, и эзеролина в соотношении 97/3, определенном методом ВЭЖХ.
Пример 6. (3aS-цис)-1,2,3,3a, 8,8a-гексагидро-1,3a, 8-триметилпирроло [2,3-b]индол-5-ил 3,4-дигидро-2 (1Н)-изохинолинкарбоксилат.
К раствору физостигмина (2,75 г) в сухом тетрагидрофуране (28 мл) в атмосфере азота при температуре 25oC добавляют трет-бутилат калия (1,28 г) в течение 0,25 часа. Смесь выдерживают 0,5 часа при температуре 25oC и добавляют ледяную уксусную кислоту (0,6 мл, 1 эквивалент, pH 10). Полученная смесь содержит физостигмин (II) и эзеролин (III) в соотношении 1/99, определенном методом ВЭЖХ. Добавление 1,1'-карбонилдиимидазола (1,7 г, 1,05 эквивалента) порциями в 1,0-0,05 эквивалентов с интервалом 1,25 часа при температуре -20oC давало спустя 1 час после добавления соответствующей порции следующие соотношения в смеси имидазолкарбонильного промежуточного продукта (V) и эзеролина 97/3 и 99/1, определенном методом ВЭЖХ. Последующее добавление ледяной уксусной кислоты (3,4 мл, 6 эквивалентов, pH 5), а затем 1,2,3,4- тетрагидроизохинолина (1,5 г, 1,1 эквивалента, добавление в течение 0,5 ч при температуре 15oC) приводит после 4 часов выдержки при температуре 25oC к получению смеси, содержащей (3aS-цис)-1,2,3,3a,8,8a-гексагидро-1,3а,8-триметилпирроло[2,3-b]индол-5-ил 3,4-дигидро-2(1Н)-изохинолинкарбоксилат и эзеролин в соотношении 98/2, определенном методом ВЭЖХ.
Пример 7. (3aS-цис) -1,2,3,3a, 8,8a-гексагидро-1,3a,8- триметилпирроло[2,3-b]индол-5-ил 3,4- дигидро-2 (1Н)-изохинолинкарбоксилат.
К раствору физостигмина (290 г) в сухом тетрагидрофуране (2,3 л) в атмосфере азота при температуре 15oC добавляют трет-бутилат калия (126,4 г) в течение 0,5 часа. Смесь выдерживают 0,5 часа при температуре 15oC и добавляют ледяную уксусную кислоту (64,1 мл, 1 эквивалент, pH 10). Полученная смесь содержит физостигмин (II) и эзеролин (III) в соотношении 1/99, определенном методом ВЭЖХ. Добавление 1,1'-карбонилдиимидазола (195,8 г, 1,15 эквивалента) 10 порциями по 0,1 эквивалента и 3 порциями по 0,05 эквивалента при температуре -30oC в течение 2 часов приводит к следующим соотношениям в смеси имидазолкарбонильного промежуточного продукта (V) и эзеролина после добавления соответственно 1,0-1,1-1,5 эквивалентов: 92/8, 98/2, 99/1, определенным методом ВЭЖХ. Последующее добавление ледяной уксусной кислоты (482 мл, 8 эквивалентов, pH 5), а затем 1,2,3,4-тетрагидроизохинолина (175 г, 1,25 эквивалента, добавление в течение 1,5 часа при температуре -10oC), и доведение до температуры 20 градусов в течение 15 часов приводит к получению смеси, содержащей (3aS-цис)-1,2,3,3a,8,8a-гексагидро-1,3a,8-триметилпирроло[2,3-b] индол-5-ил 3, 4,-дигидро-2(1Н)-изохинолинкарбоксилат и эзеролин в соотношении 99/1, определенном методом ВЭЖХ. Добавляют воду (500 мл), охлаждают смесь до температуры -10oC, частично нейтрализуют ее до pH 8 с помощью 50%-ного раствора гидроксида натрия (471 г, 0,7 эквивалента по уксусной кислоте), концентрируют тетрагидрофуран при температуре 30oC, экстрагируют остаток толуолом (одной порцией в 1 л и двумя порциями по 0,5 л), промывают экстракт водой (500 мл) 5%-ным раствором хлорида натрия (500 мл) и концентрируют при пониженном давлении при 50oC, получая в итоге 370 г сырого продукта. Этот материал затем очищают хроматографией на силикагеле, используя систему этилацетат/метанол, и получают 346 г продукта 99%-ной чистоты с выходом в 89% от исходного количества физостигмина. Перекристаллизация из системы метанол/вода позволяет получить 321 г кристаллического продукта 99%-ной чистоты, определенной методом ВЭЖХ, с выходом 84%.
Пример 8. Превращение физостигмина салицилата в свободное основание физостигмина.
К гетерогенной смеси физостигмина салицилата (450 г) в дихлорметане (1,35 л) и воде (1,35 л) прибавляют карбонат натрия (150 г) в течение 0,5-1,0 часа, поддерживая температуру на уровне 18-20oC. В процессе добавления значение pH водной фазы увеличивается от 5,5 до 9,5. После перемешивания при температуре 18-20oC в течение 0,5 часа водную фазу отделяют и экстрагируют дихлорметаном (дважды по 112 мл). Объединенную дихлорметановую фазу обрабатывают водой (500 мл) и карбонатом натрия (23 г) при температуре 18-20oC и перемешивании в течение 0,5 часа. Водную фазу отделяют, экстрагируют дихлорметаном (дважды по 112 мл) и объединенную дихлорметановую фазу промывают водой (450 мл), высушивают над карбонатом калия (20 г) и концентрируют при пониженном давлении и при температуре ниже 30oC, получая 302 г свободного основания кристаллического физостигмина (выход 100,8% от теоретического, степень чистоты 99,0%, определенная методом ВЭЖХ).
Пример 9. (3aS-цис) -1,2,3,3а, 8,8а-гексагидро-1,3а,8- триметилпирроло[2,3-b]индол-5-ол циклогексилкарбамат эфир.
Физостигмин (550 мг) и метилат натрия (108 мг) помещают в сосуд, в котором создают разряжение (5-10 мм рт. ст.). Малыми порциями при взбалтывании в течение 2 часов добавляют абсолютный этанол (70 мл) при внешней температуре 25oC. Затем отгоняют этанол, добавляют бензол (50 мл) и смесь выпаривают досуха. Реакционная смесь в этот момент содержит физостигмин (II) и эзеролин (III) в соотношении 12/88, определенном методом ВЭЖХ. К остатку добавляют бензол (50 мл), содержащий циклогексилизоцианат (0,5 г) и смесь выдерживают при температуре 25oC. Через 3 ч соотношение физостигмина, эзеролина и (3aS-цис)-1,2,3,3a,8,8a- гексагидро-1,3a,8-триметилпирроло [2,3-b]индол-5-ол циклогексилкарбамата (эфира) составляет 11/61/28, что было определено методом ВЭЖХ. Последующие подкисление и обработка не привели к изменению состава полученного сырца.
Пример 10. (3aS-цис) -1,2,3,3a,8,8a-гексагидро-1,3a,8-триметилпирроло [2,3-b]индол-5-ол 3-хлорфенилкарбамата эфир.
К раствору физостигмина (25 г) в сухом тетрагидрофуране (250 мл) содержащемуся в атмосфере азота при температуре 25oC, порциями добавляют трет-бутилат калия (11,5 г) в течение 0,25 ч, поддерживая температуру в пределах 25-30oC. Через 0,5 ч смесь охлаждают до температуры 5oC и обрабатывают ледяной уксусной кислотой (6,0 мл, 1,1 эквивалента, pH 9,5), добавляя ее в течение 0,25 часа. Полученная смесь содержит физостигмин (II) и эзеролин (III) в соотношении 1/99, определенном методом ВЭЖХ. Добавляют 3-хлорфенилизоцианат (25,8 г) в течение 1 ч при температуре 5oC, а затем трет-бутилат калия (5 порций по 0,05 эквивалента) в течение 0,5 часа, поддерживая значение pH в пределах от 9,5 до 10,0. Смесь содержит эзеролин и (3aS-цис) -1,2,3,3а, 8,8а-гексагидро-1,3а, 8- триметилпирроло [2,3-b] индол-5-ол 3-хлорфенилкарбамат (эфир) в соотношении 1/99, определенном методом ВЭЖХ. После промывания смеси водой, концентрирования при пониженном давлении, хроматографической очистки на силикагеле с помощью этилацетата, подкисления очищенного свободного основания в этилацетате (300 мл) фумаровой кислотой (1 эквивалент) был выделен продукт (31,6 г) в виде соли фумаровой кислоты с выходом 71,3%.
Пример 11. (3aS-цис) -1,2,3,3a,8,8a-гексагидро-1,3a,8- триметилпирроло[2,3-b]индол-5-ол, 3-хлорфенилкарбамат эфир.
К раствору физостигмина (10 г) в сухом тетрагидрофуране (100 мл), содержащемуся в атмосфере азота при температуре 25oC, порциями добавляют трет-бутилат калия (4,4 г) в течение 0,25 часа, поддерживая температуру в пределах 25-30oC. Через 0,5 ч смесь охлаждают до температуры 5oC и обрабатывают ледяной уксусной кислотой (2,5 мл, 1,2 эквивалента, pH 8,5). Полученная смесь содержит физостигмин (II) и эзеролин (III) в соотношении < 1/99, определенном методом ВЭЖХ. Добавляют 3-хлорфенилизоцианат (5,6 г, 1 эквивалент) в течение 5 минут при температуре -5oC.
Через 0,25 ч реакционная смесь, имеющая pH 7,0, содержит эзеролин, (3aS-цис) -1,2,3,3a, 8,8a-гексагидро-1,3a,8-триметил- пирроло[2,3-b]индол-5-ол 3-хлорфенилкарбамат (эфир) и побочный продукт (образовавшийся в результате pH-зависимого обратимого присоединения второго остатка изоцианата к продукту) в соотношении 39/3/39, определенном методом ВЭЖХ. Корректировка значения PH путем добавления трет-бутилата калия (0,5 г, 0,1 эквивалента, до pH 8,5) изменяет это соотношение до 12/50/5.
Пример 12. (3aS-цис)- [3aα,5(R*)8aα] -1,2,3,3a,8,8a-гексагидро-1,3a,8- триметилпирроло[2,3-b]индол-5-ил (1-фенилэтил) карбамат.
К раствору физостигмина (55,1 г) в сухом тетрагидрофуране (600 мл), содержавшемуся в атмосфере азота при температуре 10-20oC, порциями в течение 0,5 часа добавляют трет-бутилат калия (26,8 г), поддерживая температуру в пределах 10-20oC. Через 0,5 часа смесь охлаждают до температуры 10oC и обрабатывают ледяной уксусной кислотой (12,6 мл, 1,1 эквивалента, pH 9,5). Полученная смесь содержит физостигмин (II) и эзеролин (III) в соотношении 1/99, определенном методом ВЭЖХ. Добавляют (S)-(-)- α -метилбензил-изоцианат (29,0 г, 1 эквивалент) в течение 1,5 часов при температуре 10oC. В процессе добавления pH реакционной смеси остается постоянным на уровне 9,5. Через 0,5 часа реакционная смесь содержит эзеролин и (3aS-цис)- [3aα,5(R*)8aα] -1,2,3,3a,8,8a-гексагидро-1,3a,8-триметилпирроло[2,3-b]индол-5-ил, (1-фенилэтил) карбамат (эфир) в соотношении 2/98, определенном методом ВЭЖХ. После промывания реакционной смеси водой (300 мл), концентрирования тетрагидрофурановой фазы, хроматографической очистки на нейтральной окиси алюминия с использованием дихлорметана как элюента и перекристаллизации из диизопропилового эфира был выделен целевой продукт (63 г) с выходом 86% и степенью чистоты 99,5% определенной методом ВЭЖХ.
Пример 13. [3aS- [3aα,5(R*)8aα]]-1,2,3,3a,8,8a- гексагидро-1,3a,8- триметилпирроло[2,3-b]индол-5-ил (1- фенилэтил) карбамат.
К раствору физостигмина (55,1) в сухом тетрагидрофуране (600 мл), содержащемуся в атмосфере азота при температуре 8-12oC, порциями в течение 0,5 часа добавляют трет-бутилат калия (26,8 г), поддерживая температуру в пределах 10-18oC. Через 0,5 часа смесь охлаждают до температуры 5oC и обрабатывают ледяной уксусной кислотой (12,6 мл, 1,1 эквивалента, pH 9,5). Полученная смесь содержит физостигмин (II) и эзеролин (III) в соотношении 1/99, определенном методом ВЭЖХ. Добавляют (R)(+)- α -метилбензилизоцианат (29,0 г, 1 эквивалент) в течение 0,5 часа при температуре 10oC. Через 10 мин после добавления изоцианата при значении pH 10,0 реакционная смесь содержит эзеролин и [3aS- [3aα,5(R*)8aα]]-1,2,3,3a,8,8a-гексагидро-1,3a,8-триметилпирроло[2,3-b] индол-5-ил (1-фенилэтил)карбамат в соотношении 3/97, определенном методом ВЭЖХ. Через 0,5 часа содержание эзеролина увеличивается до 4%. Доведение значения pH до 9,5 уксусной кислотой (0,4 мл, 0,03 эквивалента) и добавление 0,05 эквивалента изоцианата привело к соотношению эзеролина и продукта 1/99, определенному методом ВЭЖХ. После промывания реакционной смеси водой (300 мл), концентрирования тетрагидрофурановой фазы, хроматографической очистки на нейтральной окиси алюминия с использованием дихлорметана как элюента и перекристаллизации из диизопропилового эфира был выделен целевой продукт (69 г) с выходом 95% и степенью чистоты 98%, определенной методом ВЭЖХ.
Пример 14. (3aS-цис) -1,2,3,3a,8,8a-гексагидро-1,3а,8- триметилпирроло[2,3-b]индол-5-ил циклогексилкарбамат (эфир).
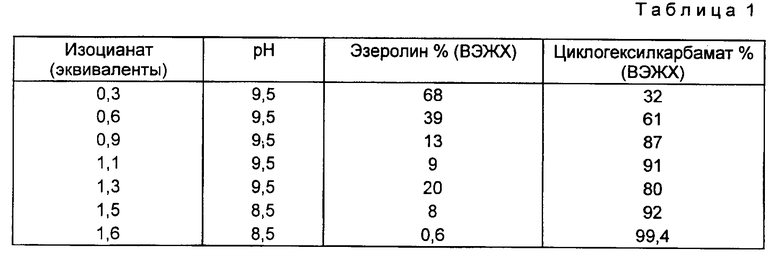
К раствору физостигмина (75 г) в сухом тетрагидрофуране (700 мл), содержавшемуся в атмосфере азота при температуре 8-12oC, порциями в течение 1,0 часа добавляют трет-бутилат калия (39,9 г), поддерживая температуру в пределах 19-23oC. Через 0,5 ч смесь охлаждают до температуры 10oC и обрабатывают ледяной уксусной кислотой (17,1 мл, 1,1 эквивалента, pH 9,0-9,5). Полученная смесь содержит физостигмин (II) и эзеролин (III) в соотношении 1/99, определенном методом ВЭЖХ. Добавляют циклогексилизоцианат (54,5 г, 1,6 эквивалента) в течение 3,0 часов при температуре 10-20oC. В процессе добавления циклогексилизоцианата значение pH доводилось от 9,5 до 8,5 добавлением ледяной уксусной кислоты. Определенное методом ВЭЖХ соотношение эзеролина и (3aS-цис)-1,2,3,3a, 8,8a-гексагидро-1,3a,8- триметилпирроло[2,3-b]индол-5-ол циклогексилкарбамата (эфир) было следующим (см. таблицу).
После промывания реакционной смеси водой (2•100 мл), концентрирования тетрагидрофурановой фазы и перекристаллизации из гексана был выделен целевой продукт (85,6 г) с выходом 86% и степенью чистоты 99,0%, определенной методом ВЭЖХ.
Изобретение касается новых способов получения соединения общей формулы (I), где R - низший алкил, R1 - атом водорода, R2 - низший алкил, низший циклоалкил, низший циклоалкил-низший алкил, низший бициклоалкил, арил или арил - низший алкил, или R1 и R2 - образуют вместе с атомом азота, с которым они связаны, группу 3,4-дигидро-2(1H)-изохинолина, X - низший алкил, низший алкокси, атом галогена или трифторметильная группа, m - равняется 0,1 или 2, взаимодействием соединения общей формулы (II), где R, X и m имеют значения, указанные выше, а R3 - низший алкил, с алкиллитием или алкоголятом щелочного металла, а затем с карбоновой кислотой общей формулы R5COOH, в которой R5 - низший алкил, и получением в результате соединения общей формулы (III), где R, X и m имеют значения, указанные выше, взаимодействием реакционной смеси, содержащей соединение общей формулы III, с изоцианатом общей формулы R2NCO с получением соединения общей формулы I, где R1 - атом водорода, или с соединением общей формулы (IV), где R4 - атом водорода или низший алкил, в присутствии карбоновой кислоты общей формулы R5COOH, в которой R5 имеет значение, указанное выше, с получением соединения общей формулы (V), где R, R4, X и m имеют значения, указанные выше, контактированием реакционной смеси, содержащей соединение общей формулы (V), с соединением общей формулы R1R2NH, в которой R1 и R2 имеют значения, указанные выше, и выделением соединения общей формулы I. 2 c. и 17 з.п. ф-лы, 1 табл.
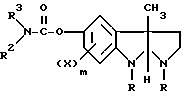
где R - низший алкил;
R1 - атом водорода;
R2 - низший алкил, низший циклоалкил, низший циклоалкил - низший алкил, низший бициклоалкил, арил или арил-низший алкил, или R1 и R2 - взятые вместе, образуют вместе с атомом азота, с которым они связаны, группу 3,4-дигидро-2(1H)-изохинолина;
X - низший алкил, низший алкокси, атом галогена или трифторметильная группа;
m = 1 или 2,
отличающийся тем, что осуществляют взаимодействие соединения общей формулы II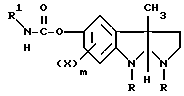
где R, X и m имеют значения, указанные выше,
R3 - низший алкил;
с алкиллитием или алкоголятом щелочного металла, а затем с карбоновой кислотой общей формулы R5COOH, в которой R5 - низший алкил, с получением в результате соединения общей формулы III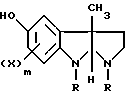
где R, X и m имеют значения, указанные выше,
с последующим взаимодействием полученной реакционной смеси, содержащей соединение общей формулы III, с изоцианатом общей формулы R2NCO с получением соединения общей формулы I.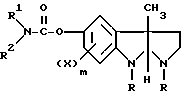
где R, R1, R2, X и m имеют значения, указанные в п.1, отличающийся тем, что осуществляют
a) реакцию соединения формулы II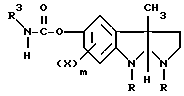
где R, X и m имеют значения, указанные выше,
R3 - низший алкил,
с алкиллитием или алкоголятом щелочного металла и затем с карбоновой кислотой формулы R5COOH, где R5 представляет низший алкил, с получением соединения формулы III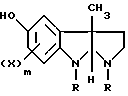
где R, X и m имеют значения, указанные выше,
b) взаимодействие полученной реакционной смеси, содержащей соединение формулы III, с соединением общей формулы IV: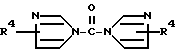
где R4 - атом водорода или низший алкил,
в присутствии карбоновой кислоты общей формулы R5COOH, в которой R5 имеет значение, указанное выше, с получением соединения общей формулы V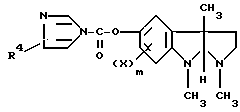
R, R4 и X и m имеют значения, указанные выше,
c) контактируют реакционную смесь, содержащую соединение общей формулы V, с соединением общей формулы R1R2NH, в которой R1 и R2 имеют значения, указанные выше, и выделяют соединение формулы I.
| SU, 4831155, C 07 D 487/04, 1989. |
Авторы
Даты
1998-07-27—Публикация
1993-07-20—Подача