Изобретение относится к химическим средствам контактного действия для борьбы с бытовыми насекомыми и может быть использовано для уничтожения кератофагов: моли и коврового жука.
Для уничтожения кератофагов применяются химические средства как фумигационного, так и контактного действия. Более предпочтительным следует считать последние, т.к. они могут быть использованы для защиты шерстяных изделий, находящихся как в открытом, так и закрытом хранении.
Известны средства контактного действия для уничтожения кератофагов, представляющие собой растворы в органических растворителях фосфорорганических инсектицидов, например дихлорфоса (см. Авторское свидетельство N 1544335, приор. 12.06.88, публ. в Бюл. N 7, 23.02.90) или фоксима (см. Сборник тезисов докладов конференции "Современные направления медицинской дезинсекции и дератизации", состоявшейся 17-18 октября 1981 г., Всесоюзный научно-исследовательский институт дезинфекции и стерилизации. - М.: 1981, стр. 92-94 "Средства борьбы с синантропными кератофагами"). В последние годы стали известны более эффективные и менее опасные для теплокровных животных средства контактного действия для уничтожения кератофагов, представляющие собой растворы в органических растворителях синтетических пиретроидов, например перметрина (см. Авторское свидетельство N 1701226, приор. 29.09.89, публ. в Бюл. N 48, 30.12.91).
Наиболее эффективным и в то же время наиболее безопасным для человека и других теплокровных животных следует считать средство контактного действия для уничтожения кератофагов, представляющее собой раствор относительно нового синтетического пиретроида-дельтаметрина (IR-цис-3-(2,2-дибромвинил)-2,2-диметилпропанкарбоновой кислоты (S)-3-фенокси-α- цианбензилового эфира) в органических растворителях, в частности в диацетоновом спирте или нефрасах (в воде дельтаметрин практически нерастворим).
Это средство, принимаемое в качестве прототипа, имеет коммерческое название "Дефен" и содержит 0,002% дельтаметрина (см. Перечень N 0017-94 отечественных и зарубежных дезинфекционных средств, разрешенных к применению на территории Российской Федерации. Раздел "Средства дезинсекции". Стр. 3, п. 7. Опубликован Минздравом РФ в 1994 г., г. Москва).
Описанному средству-прототипу присущи, однако, существенные недостатки. Во-первых, это средство как при хранении в полимерной таре, так и после нанесения на субстрат, не обладает достаточно высокой стабильностью, что снижает длительность его инсектицидного действия. В частности, после нанесения средства на шерстяную ткань (25 см3 на 1 м2 поверхности) 100%-ная гибель гусениц моли и личинок кожееда обеспечивается на протяжении соответственно 6 и 4 месяцев, после чего инсектицидная активность средства резко снижается. Кроме того, при хранении средства в полимерной таре его острая инсектицидная активность начинает заметно падать по истечении 10 месяцев.
Во-вторых, вследствие того, что около 99% массы средства приходится на органические растворители, применение препарата в жилых помещениях нельзя считать полностью безопасным для человека и других теплокровных животных. Сочетание диацетонового спирта или нефрасов с дельтаметрином приводит к тому, что средство при попадании в желудок квалифицируется как умеренно опасное.
Целью данного изобретения является повышение длительности инсектицидного действия средства, содержащего 0,002% дельтаметрина, а также снижение его токсичности для теплокровных животных. Это достигается тем, что средство на основе дельтаметрина содержит микроколичества О-ксилола, алкил-(C10-C18) бензолсульфоната кальция и бутилгидрокситолуола, а также дополнительно ингредиенты, ранее применявшиеся в антимольных средствах, в частности, цитраль и полигликолевый эфир алкилфенола, этоксилированный 9-12 молями этиленоксида, в котором алкильная группа представлена тримером пропилена. Приведенное сочетание ингредиентов позволяет растворить "нерастворимый" дельтаметрин в дистиллированной воде, которой и заменяют относительно токсичные органические растворители. Предложенное средство характеризуется следующим соотношением ингредиентов мас.%:
Дельтаметрин (IR-цис-3-(2,2-дибромвинил) -2,2-диметилпропанкарбоновой кислоты (S)-3-фенокси-α- цианбензиловый эфир - 0,0018-0,0022
O-ксилол - 0,0620-0,0670
Алкил (C10-C18) бензолсульфонат кальция - 0,0048-0,0052
Бутилгидрокситолуол - 0,0028-0,0032
Цитраль - 0,4900-0,5100
Этоксилированный 9-12 молями этиленоксида алкилфенол, в котором алкильная группа представлена тримером пропилена
Вода дистиллированная - До 100,0000
Пример. Для проведения энтомологических испытаний и токсикологических исследований в полупромышленных условиях готовили 100 кг предлагаемого средства. Приготовление осуществляли в стальном эмалированном реакторе, оборудованном пропеллерной мешалкой (60 мин-1). В реактор при комнатной температуре заливали 99,125 кг дистиллированной воды. Затем при работающей мешалке и комнатной температуре в реактор последовательно добавляли 300 г этоксилированного 9-12 молями этиленоксида алкилфенола (в котором алкильная группа представлена тримером пропилена), 500 г цитраля, 5 г алкил (C10-C18) бензолсульфоната кальция, 3 г бутилгидрокситолуола, 65 г O-ксилола и 2 г дельтаметрина. Ингредиенты перемешивали до получения прозрачного раствора, который затем пропускали через фильтр из стекловолокна и разливали во флаконы.
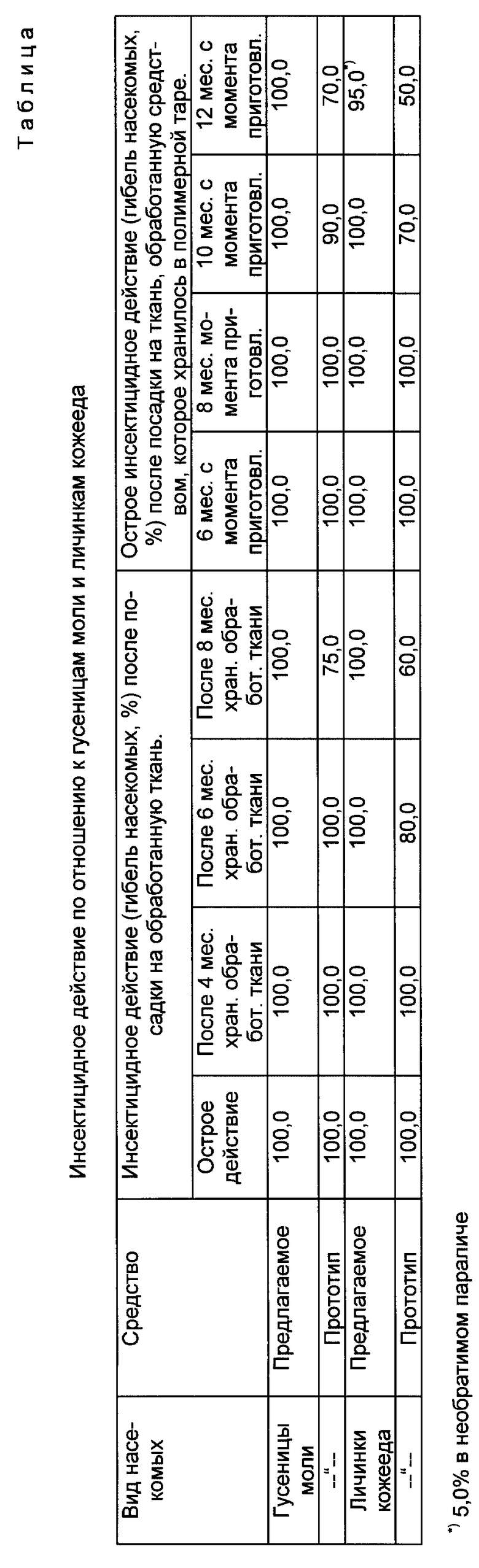
Энтомологические испытания предложенного средства проводили в лабораторных условиях на культурах моли Tineola bisseelliella Hum и кожееда Attadenus smirnovi. В опытах использовали 3-4-недельных гусениц моли и 11-12-недельных личинок кожееда инсектарного разведения. В качестве субстрата применяли образцы чисто шерстяной ткани (арт. 1134) размером 40х40 мм. Образцы ткани обрабатывали предложенным средством и средством - прототипом, залитых в полимерные флаконы, снабженные клапанами - распылителями. Норма расхода жидкости составляла 25 см3 на 1 м поверхности. После обработки образцы ткани высушивали при температуре 20oC на протяжении 24 часов. На каждый из высушенных образцов ткани подсаживали по 30 гусениц моли или по 30 личинок кожееда. Опыты вели в трехкратной повторности. Образцы ткани с помещенными на них насекомыми закладывали в стеклянные стаканчики диаметром 40 и высотой 50 мм. Сверху стаканчики накрывали хлопчатобумажной тканью, после чего их помещали в термостат, где выдерживали при 20oC. Учет гибели насекомых (острой инсектицидной активности) производили через сутки после подсадки насекомых. Для оценки длительности остаточного инсектицидного действия образцы обработанной ткани хранили на свету при комнатной температуре, отбирая их для испытаний через 4, 6 и 8 месяцев после обработки. Оценку инсектицидной активности производили так же, как в остром опыте. Кроме того, инсектицидное действие оценивали и после хранения предлагаемого средства и средства - прототипа в полимерных флаконах. Из флаконов производили опрыскивание образцов ткани по истечении 6; 8; 10 и 12 месяцев после приготовления. Обработку образцов ткани и оценку острой инсектицидной активности производили, как описано выше. Результаты описанных испытаний приведены в таблице.
Как следует из этой таблицы, предлагаемое средство позволяет существенно повысить длительность инсектицидного действия в сравнении со средством-прототипом. В частности, для гусениц моли - до 8 месяцев, вместо 6, а для личинок кожееда - до 8 месяцев, вместо 4. Одновременно показано, что при хранении предложенного средства его острая инсектицидная активность сохраняется 12 месяцев, вместо 8 - у средства - прототипа.
Токсикологические исследования предложенного средства приведены по стандартным методикам. В частности, в остром опыте на белых крысах и белых мышах была определена токсичность при пероральном введении в организм. В обоих случаях гибель животных не наступала даже при введении 10000 мг на кг веса (ДЛ50 для средства-прототипа составляет 3000 мг/кг белых мышей и 2600 мг/кг у белых крыс).
При ингаляционных затравках животных предлагаемым средством никаких отклонений от нормы (в сравнении с группой контрольных животных) у подопытных животных не обнаружено. При затравках средством-прототипом (как на диацетоновом спирте, так и на нефрасе) отмечены явные симптомы наркотического отравления.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРЕПАРАТ ДЛЯ БОРЬБЫ С НАСЕКОМЫМИ-КЕРАТОФАГАМИ | 2016 |
|
RU2630316C1 |
| СПОСОБ СВЧ-ДЕЗИНСЕКЦИИ МАТЕРИАЛОВ И/ИЛИ ИЗДЕЛИЙ ИЗ ШЕРСТИ | 2011 |
|
RU2477147C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНСЕКТИЦИДНОГО ПРЕПАРАТА "ЦИПАМ" | 1997 |
|
RU2121833C1 |
| ЖИДКОЕ ГЕРБИЦИДНОЕ СРЕДСТВО В ВИДЕ ЭМУЛЬСИИ И СПОСОБ БОРЬБЫ С НЕЖЕЛАТЕЛЬНОЙ РАСТИТЕЛЬНОСТЬЮ | 2006 |
|
RU2307503C1 |
| ИНСЕКТОАКАРИЦИДНАЯ СУБСТАНЦИЯ ДЛЯ БОРЬБЫ С ЭКТОПАРАЗИТАМИ СОБАК И КОШЕК | 2006 |
|
RU2312100C1 |
| РЕПЕЛЛЕНТНОЕ СРЕДСТВО ДЛЯ ЗАЩИТЫ ДЕТЕЙ ОТ УКУСОВ ЛЕТАЮЩИХ КРОВОСОСУЩИХ НАСЕКОМЫХ | 1996 |
|
RU2116782C1 |
| МОЮЩЕЕ СРЕДСТВО ТЕХНОСОЛ | 2010 |
|
RU2439205C2 |
| МОЮЩЕЕ ДЕЗИНФИЦИРУЮЩЕЕ СРЕДСТВО | 1998 |
|
RU2142499C1 |
| СПОСОБ ИНСЕКТИЦИДНОЙ ОБРАБОТКИ И ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ "ПЕШКА" ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2318385C2 |
| ГИПОТАЛАМО-ГИПОФИЗАРНОЕ СРЕДСТВО, ВЫЗЫВАЮЩЕЕ НЕОБРАТИМУЮ СТАДИЮ ТОРМОЖЕНИЯ И/ИЛИ ПОКОЯ У СОБАК И СТАДИЮ ПОКОЯ У КОШЕК (АНЭСТРУС) | 1999 |
|
RU2139057C1 |
Изобретение относится к химическим средствам контактного действия для уничтожения бытовых насекомых - кератофагов (моли и кожееда). В состав средства входят: дельтаметрин (IR-цис-3-(2,2-дибромвинил-2,2-диметилциклопропанкарбоновой кислоты (S)-3-фенокси-α-цианбензиловый эфир), микроколичества О-ксилола, алкил (С10 - C18)-бензолсульфоната кальция, бутилгидрокситолуола, а также цитраль и этоксилированный 9 - 12 молями этиленоксида алкилфенол, в котором алкильная группа представлена тримером пропилена. В качестве растворителя используют дистиллированную воду. Перечисленные ингредиенты берут в определенных количественных соотношениях. Предложенное средство позволят существенно увеличить длительность инсектицидного действия и снизить токсичность по отношению к человеку и другим теплокровным животным. 1 табл.
Средство контактного действия для уничтожения кератофагов на основе синтетического пиретроида - дельтаметрина (1R-цис -3-(2,2-дибромвинил)-2,2-диметилциклопропанкарбоновой кислоты (S)-3-фенокси -α- цианбензилового эфира в растворителе, отличающееся тем, что оно содержит микроколичества О-ксилола, алкил-(C10 - C18) бензолсульфоната кальция и бутилгидрокситолуола, цитраль и этоксилированный 9 - 12 молями этиленоксида алкилфенол, в котором алкильная группа представлена тримером пропилена, а в качестве растворителя содержит дистиллированную воду, при соотношении ингредиентов, мас.%:
Дельтаметрин (1R-цис-3-(2,2-дибромвинил)-2, 2-диметилциклопропанкарбоновой кислоты (S)-3-фенокси-α-цианбензиловый эфир - 0,0018 - 0,0022
О-Ксилол - 0,0620 - 0,0670
Алкил (C10 - C18) бензолсульфонат кальция - 0,0048 - 0,0052
Бутилгидрокситолуол - 0,0028 - 0,0032
Цитраль - 0,4900 - 0,5100
Этоксилированный 9 - 12 молями этиленоксида алкилфенол, в котором алкильная группа представлена тримером пропилена - 0,2800 - 0,3200
Вода дистиллированная - До 100,0000ю
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Средство борьбы с кератофагом | 1989 |
|
SU1701226A1 |
| Средство для уничтожения кератофагов | 1988 |
|
SU1544335A1 |
| Тезисы докладов | |||
| Современные направления медицинской дезинсекции и дератизации | |||
| - М.: ВНИИ дезинфекции и стерилизации, 1981, с.92-94 | |||
| Антимольное средство | 1985 |
|
SU1259988A1 |
| DE 4220161 A1, 1993 | |||
| DE 3734341 A1, 1989 | |||
| GB 1592615 A2, 1981 | |||
| DE 3508643 A1, 1986 | |||
| DE 3343092 A1, 1985 | |||
| DE 3529693 A1, 1987. | |||
Авторы
Даты
1998-09-27—Публикация
1996-07-19—Подача