Изобретение относится к области медицины и может быть использовано при диагностике онкологических заболеваний.
Известен способ диагностики онкологических новообразований, основанный на облучении подозреваемого участка ультрафиолетовым облучением и анализе вторичного люминесцентного излучения пораженных тканей в видимом участке видимого спектра [1].
Наиболее близким к изобретению является способ диагностики заболеваний в онкологии, включающий ультрафиолетовое воздействие на орган с известной патологией и на исследуемый орган и регистрацию путем визуального наблюдения или фотографирования вторичного люминесцентного излучения от этих органов, а вид патологии определяют путем визуального сопоставления результатов регистрации вторичного люминесцентного излучения от органов с известной патологией и исследуемого [2].
Недостатком этого способа являются:
субъективность результатов диагностики, т.к. они являются зависимыми от уровня квалификации лица, осуществляющего диагностику;
недостаточная достоверность диагностики из-за существенной зависимости спектрального (цветового) образца обследуемого участка от плотности потока мощности ультрафиолетового излучения на поверхности наблюдаемого органа. Спектральный (цветовой) образ при одной и той же мощности источника ультрафиолетового излучения будет изменяться в зависимости от расстояния между концом световода и поверхностью наблюдаемого участка. Различие в цветовом выражении вследствие разной яркости цветовых тонов вторичного излучения обследуемого участка будет приводить к ошибочной диагностике.
Задача, на решение которой направлено изобретение, заключается в разработке способа диагностики заболеваний в онкологии, обладающего более высокими характеристиками.
Технический результат от использования изобретения заключается в повышении объективности диагностики и повышении достоверности результатов диагностики.
Этот результат достигается тем, что способ диагностики заболеваний в онкологии, включающий воздействие ультрафиолетового излучения заданной мощности на органы с известной патологией и на исследуемый орган, последующий анализ спектров вторичного люминесцентного излучения освещенных ультрафиолетовым излучением тканей, отличается тем, что предварительно измеряют совокупности значений уровней спектральных составляющих вторичного люминесцентного излучения от образцов тканей с известной патологией, нормируют полученные отсчеты спектральных составляющих мощности вторичного люминесцентного излучения по отношению к максимальному уровню, совокупности полученных относительных значений уровней спектральных составляющих по каждому виду патологии и норме являются диагностическими критериями, при каждом обследовании подозреваемых участков с неизвестной патологией аналогично измеряют совокупность уровней спектральных составляющих вторичного люминесцентного излучения от подозреваемого участка, нормируют полученные отсчеты спектральных составляющих мощности вторичного люминесцентного излучения по отношению к максимальному уровню, полученную совокупность относительных значений уровней спектральных составляющих в качестве спектрального образа обследуемого участка поочередно сопоставляют с предварительно полученными диагностическими критериями нормы и характерных видов патологии, находят наибольшее приближение к одному из диагностический критериев, которое и определяет вид патологии обследуемого участка.
Сущность способа состоит в следующем. В основу способа положено известное свойство возникновения вторичного люминесцентного излучения при воздействии на обследуемый участок ультрафиолетовым излучением.
При этом в материале клеток ткани возникает вторичное люминесцентное излучение, охватывающее область желто-зеленого участка видимого спектра и более длинноволновую область. Возникшее свечение неоднородно по своей интенсивности, а распределение его интенсивности по спектру (спектральный образ) зависит от состава и состояния облучаемых клеток. Это распределение (спектральный образ) будет различным у клеток здоровых тканей, а также у клеток тканей с различными отклонениями, обусловленными разной патологией. У клеток очагов язвенной болезни, полипов и очагов раковых новообразований распределение интенсивности вторичного люминесцентного излучения (спектральный образ) отличается по спектру.
Так, например, при люминесцентных исследованиях желудка у практически здоровых лиц спектральный образ нормальных тканей характеризуется слабо-желтым свечением с зеленоватым оттенком, у больных с доброкачественными изъязвлениями спектральный образ изъязвленных участков содержит вторичное излучение ярко-желтого цвета, у больных со злокачественной язвой - темно-зеленое в очаге и ярко-желтое на краях язвы, а у больных раком желудка спектральный образ представляет увеличение ярко-желтой люминесценции с зеленоватым оттенком [2, с. 43-50].
Для выделения этой информации и формирования сопоставимых спектральных образов, спектр желто-зеленой области, где наблюдается вторичные излучение, разделяют на более узкие спектральные участки. Каждый из этих участков характеризуется некоторой полосой пропускания Δλi(Δλi= λimax-λimin) и характеризуется средним значением длины волны λi. На этих частотах первоначально осуществляется измерение абсолютного значения интенсивности вторичного излучения. Однако измеренное значение уровня мощности спектральной составляющей будет зависеть не только от вида патологии обследуемого участка, но и от мощности ультрафиолетового излучения, чувствительности фотометрических датчиков, используемых для измерения вторичного излучения, расстояния от входа фотометрического канала до обследуемой поверхности, расстояния между концом канала подачи ультрафиолетового облучения и обследуемой поверхности и интервала времени, прошедшего с момента ультрафиолетового облучения до момента измерения вторичного излучения. Суммарное воздействие этих факторов приводит к тому, что при каждом последующем обследовании абсолютное значение уровня мощности измеряемого вторичного излучения в одних и тех же участках спектра для одного и того же обследуемого участка обследуемого органа будут отличаться друг от друга. Данное изменение уровней мощности спектральных составляющих носит случайный характер и затрудняет непосредственное использование результатов измерений врачом, осуществляющим диагностику.
Для исключения случайного влияния на результаты диагностики после измерения абсолютных значений уровней мощности спектральных составляющих P(λi) определяют максимальный уровень Pmax(λi) мощности среди совокупности всех составляющих P(λi) по спектру измерений (λ1,..., λi,..., λn), определяют относительное значение мощности вторичного излучения спектральных составляющих Pотн(λi) путем нормирования абсолютных значений всех спектральных составляющих P(λi) по отношению к максимально измеренному значению Pmax(λi).
Совокупности относительных значений спектральных составляющих представляют устойчивый спектральный образ обследуемого участка, который зависит только от физиологического состояния тканей обследуемого участка. Эти спектральные образы и используются при диагностике.
На фиг. 1 приведен график, характеризующий результаты измерения абсолютных значений спектральных составляющих P(λi) уровней вторичного излучения во всех участках наблюдаемого диапазона и показан характер случайного изменения результатов измерения в зависимости от указанных факторов.
На фиг. 2 приведены графики, показывающие наиболее характерные распределения измеренных значений спектральной мощности вторичного излучения. Цифрами обозначены: 1 - норма, 2 - язва, 3 - полипы, 4 - рак, 5 - результаты измерений исследуемого органа.
На фиг. 3 приведены спектральные образцы (диагностические критерии) для тех же видов патологии, которые представляют собой совокупности относительных значений мощности вторичного излучения исследуемого органа для характерных видов патологии и для нормы.
Последовательность действий способа состоит в следующем.
Перед началом применения способа по назначению производится определение диагностических критериев (характерных спектральных образов для каждого состояния тканей обследуемого органа). Для этого в качестве диагностических образцов используются ткани с установленной патологией, принадлежащие органам различного вида и имеющие различную степень поражения (различные виды патологии), причем вид патологии подтвержден гистологическими исследованиями. Эти ткани облучаются ультрафиолетовым излучением. На длительность и мощность облучения накладывается лишь одно ограничение - они не должны превышать предельно допустимые значения, установленные нормативными документами.
Авторами в своей практике использован источник ультрафиолетового излучения с мощностью на выходе 10-3...2•10-3 Вт. Продолжительность облучения в зависимости от мощности составляла 3...10 мин.
Для каждого исследуемого вида патологии в качестве диагностических спектральных образцов берется совокупность отсчетов амплитуд спектральных составляющих на всех частотах λi. Авторами при практической реализации способа использовался четырехканальный спектроанализатор, желто-зеленый участок спектра делился на четыре полосы пропускания: Δλ1=400...450 нм, Δλ2=460...550 нм, Δλ3=550. . .600 нм, Δλ4=600...650 нм. Им соответствуют средние значения длин волн: λ1=425 нм, λ2=500 нм, λ3=575 нм, λ4=625 нм.
Полученные результаты измерений сводятся в таблицу для каждого вида патологии или представляются в виде графиков. На фиг. 2 результаты измерений представлены в графической форме для четырех исследуемых случаев: норма, язва, полип, рак.
При измерении вторичного излучения на чувствительность используемых фотометрических датчиков (измерительных преобразователей) накладывается лишь одно ограничение - она должна быть достаточной для регистрации вторичного люминесцентного излучения. Авторами использовались первичные фотометрические преобразователи с чувствительностью 10-4...10-3 Вт.
Как было показано выше, результаты измерений имеют случайную составляющую, приводящую к их нестабильности. Для исключения этого недостатка для каждого вида патологии определяют максимальное значение измеренной мощности и на это значение делятся все отсчеты. Тем самым осуществляется нормирование результатов измерений уровней мощности - спектральных составляющих по отношению к максимальному уровню. Нормированные значения результатов измерений совокупности спектральных составляющих и представляют диагностические критерии (диагностический спектральный образ) для данного вида патологии. Они также могут быть представлены в виде таблицы или графика. На фиг. 3 они представлены в виде графиков для тех же видов патологии.
Полученные таким образом диагностические критерии (диагностические спектральные образы) для всех образцов биологических тканей соответствуют характерным состоянием, включая норму, язвенные заболевания, полипы и раковые новообразования.
Они определяются только один раз, а в дальнейшем могут использоваться многократно как критерии для сравнения со спектральными образами от обследуемых участков с неизвестным состоянием.
Последующее применение способа заключается в получении от обследуемого участка органа вторичного люминесцентного излучения, измерении совокупности уровней спектральных составляющих этого излучения и нормировании результатов измерений относительно максимального (получение спектрального образца исследуемого участка). Нормированные результаты измерений уровней мощности спектральных составляющих вторичного излучения во всем диапазоне и являются устойчивой объективной оценкой состояния тканей подозреваемого участка исследуемого органа. Они также могут быть представлены в табличном, графическом или ином виде. На фиг. 2 и 3 показано, как спектральные образы (совокупности измеренных значений спектральных составляющих мощности вторичного излучения) могут быть сопоставлены с диагностическими критериями (диагностическими спектральными образцами).
В основе диагностики лежит нахождение близкого диагностического образца по отношению к измеренному спектральному образцу исследуемого органа.
Эта сопоставительная оценка может быть произведена визуально. Но это не исключает субъективности результатов оценки, особенно в случаях, когда визуальное отождествление с одним из диагностических критериев затруднено. Этот случай и приведен на фиг. 3.
Поэтому для повышения достоверности оценки и исключения ее субъективности применяется один из известных методов принятия решения по результатам сравнения выборок: максимального правдоподобия, наименьших квадратов, экспертных оценок, корреляционного или дисперсионного анализа и т.п. Это обеспечивает возможность автоматизации диагностики онкологических заболеваний рассматриваемым способом.
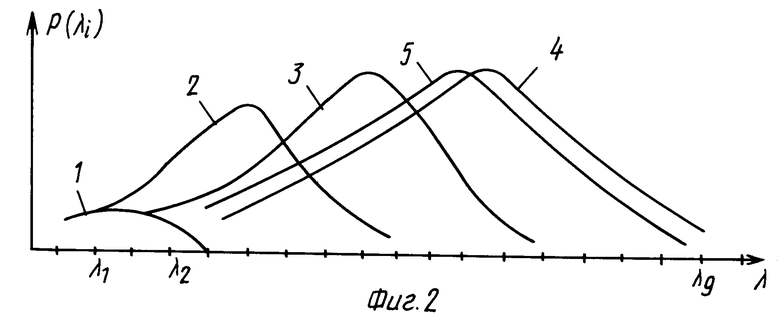
Для примера на фиг. 3, используя метод наименьших квадратов, сформулируем решающее правило в виде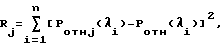
где
Rj - сумма квадратов отклонений j-го диагностического критерия от уровня мощности спектральных составляющих исследуемого органа;
n - число частотных участков (поддиапазонов);
j - вид состояния, которому соответствует диагностический критерий (1 - норма, 2 - язва, 3 - полип, 4 - рак);
Pотнj(λi) - значение, j-го диагностического критерия на i-й частоте;
Pотн(λi) - значение уровня мощности вторичного излучения исследуемого органа на i-й частоте;
Решение о виде состояния выбирается по минимальному значению Rj.
В условиях рассматриваемого примера R1 = 3,370; R2 = 2,206; R3 = 0,966; R4 = 0,361.
В соответствии с полученными результатами делается вывод, что у исследуемого органа раковые новообразования.
Таким образом из материалов заявки видно, что технический результат при использовании способа достигается.
Источники информации
1. Заявка Японии N 63-23776, кл. A 61 B 5/00.
2. Сорокин И. С. Значение люминесцентной эндоскопии в дифференциальной диагностике изъявлений желудка. - Дисс. на соискание ученой степени канд. мед.наук. - М., 1984, с. 38-39.

Изобретение может быть использовано в медицине, в частности в онкологии. На органы с известной патологией и исследуемый орган воздействуют ультрафиолетовым излучением заданной мощности, анализируют спектры вторичного люминесцентного излучения. Предварительно измеряют совокупности значений уровней спектральных составляющих мощности вторичного люминесцентного излучения от образцов тканей с известной патологией, нормируют полученные отсчеты, определяют совокупности полученных относительных значений уровней спектральных составляющих по каждому виду патологии и норме в виде диагностических критериев. Аналогично измеряют совокупность уровней подозреваемого участка. Полученные отсчеты нормируют, а совокупность относительных значений сопостовляют с предварительно полученными диагностическими критериями нормы и характерных видов патологии. Находят наибольшее приближение к одному из диагностических критериев, которое и определяет вид патологии обследуемого участка. При этом повышается объективность диагностики и достоверность ее результатов. 3 ил.
Способ диагностики заболеваний в онкологии, включающий воздействие ультрафиолетового излучения заданной мощности на органы с известной патологией и на исследуемый орган, последующий анализ спектров вторичного люминесцентного излучения освещенных ультрафиолетовым излучением тканей, отличающийся тем, что предварительно измеряют совокупности значений уровней спектральных составляющих вторичного люминесцентного излучения от образцов тканей с известной патологией, нормируют полученные отсчеты спектральных составляющих мощности вторичного люминесцентного излучения по отношению к максимальному уровню, определяют совокупности полученных относительных значений уровней спектральных составляющих по каждому виду патологии и норме в виде диагностических критериев, при каждом обследовании подозреваемых участков органов с неизвестной патологией аналогично измеряют совокупность уровней спектральных составляющих вторичного люминесцентного излучения от подозреваемого участка, нормируют полученные отсчеты спектральных составляющих мощности вторичного люминесцентного излучения по отношению к максимальному уровню, полученную совокупность относительных значений уровней спектральных составляющих в качестве спектрального образа обследуемого участка поочередно сопоставляют с предварительно полученными диагностическими критериями нормы и характерных видов патологии, находят наибольшее приближение к одному из диагностических критериев, которое и определяет вид патологии обследуемого участка.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Сорокин И.С | |||
| Значение люминесцентной эндоскопии в дифференциальной диагностике изъявлений желудка: Дисс | |||
| на соискание ученой степени канд.мед.наук | |||
| Колосниковая решетка с чередующимися неподвижными и движущимися возвратно-поступательно колосниками | 1917 |
|
SU1984A1 |
| Способ сужения чугунных изделий | 1922 |
|
SU38A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| JP 6323776 B (оримпасу Когаку Коге К.К.), 18.05.88, A 61 B 5/00 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Плетнев С.Д | |||
| Диагностика злокачественных опухолей | |||
| - М., 1979, 70 с. | |||
Авторы
Даты
1998-09-27—Публикация
1995-11-30—Подача