Изобретение относится к аккумуляции металла и, в частности оно касается удаления металлов из воды, содержащей такие металлы, например, для одной или нескольких из следующих целей:
(a) очистки воды,
(b) извлечения металлов из воды, которую используют при промывке или в другом процессе, например из воды, которую используют при обработке руд благородных металлов, и
(c) аккумуляции тяжелых металлов из воды, которую используют для обработки почв с целью удаления тяжелых металлов из таких почв.
Ранее в работе L.E. Macaskie J. Chem. Technol. Biotechnol. 49, 357 - 379 (1990) "Animmobilised cell bioprocess for the removal of heavy metals from aqueous flows" предлагалось осуществлять удаление тяжелых металлов при использовании Citrobacter ps., в этом способе биомассу культивировали, используя глицерол-2-фосфат, для получения биомассы клеток в физиологическом состоянии, подходящем для удаления металла.
Полагали, что удаление металлов происходит, благодаря совместному присутствию металла и глицерол-2-фосфата (C2P) в количестве до 5 мМ, являющегося донором фосфата при аккумуляции металла посредством иммобилизованных клеток. G2P ферментативно расщепляется до глицерола (источника потенциальной энергии для клеток) и неорганического фосфата, истечение которого мешает поступлению металла и приводит к осаждению кристаллического фосфата тяжелого металла. Хотя такой способ является эффективным при удалении тяжелых металлов из раствора, он обладает недостатком, который состоит в использовании дорогостоящего глицерол-2-фосфата.
Целью настоящего изобретения является обеспечение методики, в которой не предполагается использование такой дорогостоящей среды как глицерол-2-фосфат.
По одному из его аспектов, настоящее изобретение предлагает использование одного или нескольких микроорганизмов, аккумулирующих полифосфат, для аккумуляции полифосфата, который затем ферментативно расщепляется в присутствии воды, содержащей один или несколько металлов, для продуцирования фосфат-ионов, которые взаимодействуют с металлом(ами) в воде для осаждения фосфата металла. Такой фосфат металла может быть кристаллическим или может быть смешан с другими осажденными разновидностями, например гидроксидом.
По другому из его аспектов, настоящее изобретение предлагает использование фосфат-ионов, полученных при расщеплении полифосфата, для удаления металла(ов) из раствора путем осаждения в виде фосфата(ов) металла.
Металлами, которые поддаются методикам настоящего изобретения, являются такие, которые имеют фосфаты, обладающие низкой растворимостью в воде, например кадмий, свинец, медь, марганец, кобальт, никель, кальций, иттрий, стронций, уран, лантан, лантаниды, плутоний, америций и нептуний.
В предпочтительном способе микроорганизм, аккумулирующий полифосфат, культивируют в культуральной среде при таких условиях когда микроорганизм может синтезировать и использовать аденозинтрифосфат (АТФ), и затем синтез/использование АТФ модифицируют для того, чтобы микроорганизм использовал полифосфат в качестве альтернативного источника энергии, что приводит к получению вышеупомянутых фосфат-ионов, которые затем взаимодействуют с ионами металла для осаждения фосфата металла.
Микроорганизмом предпочтительно является бактерия, аккумулирующая полифосфат, и им может быть, например, бактерия Acinetobacter, аккумулирующая полифосфат. Из работы (смотри Y. Comeau et al., Wat. Res. vol. 20, N 12, pp. 1511 - 1521) известно, что: (a) определенные микроорганизмы способны аккумулировать при аэробных условиях резервы полифосфата и использовать такой полифосфат при анаэробных условиях для получения фосфата, и что: (b) это может быть применено для того, чтобы вызвать биологическое удаления фосфора при обработке активированного ила путем обеспечения анаэробной обработки зоны восходящего потока обычного аэробного процесса. Однако насколько известно, ранее никогда не предлагалось использовать полифосфат, аккумулированный такими микроорганизмами, в качестве источника фосфата для удаления тяжелых металлов из раствора. Таким образом, настоящее изобретение основано на использовании полифосфата в качестве главного источника фосфата при аккумуляции металла через ферментативно опосредованную биоаккумуляцию или биоминерализацию металла.
Особым примером известных бактерий Acinetobacter, аккумулирующих полифосфат, являются Acinetobacter calcoaceticus АТСС 23055 (NCIMB 10694). Другим примером известного микроорганизма, аккумулирующего полифосфат, является Klebsiella pneumoniae АТСС 12658 (=NCIMB 8806).
В случае Acinetobacter синтез/использование АТФ возможен при аэробных условиях, а изменение направления использования энергии АТФ возможно путем переключения в анаэробные условия. При анаэробных условиях использование АТФ задерживается за счет ингибирования синтеза АТФ, так как обычно он происходит при нормальных (аэробных условиях). Однако, в область настоящего изобретения входит изменение направления использования АТФ путем добавления несвязующего (несочетающего) вещества, которое мешает синтезу АТФ, например 2,4-динитрофенола или DCCD (дициклогексилкарбодиимида).
Предпочтительными бактериями являются Acinetobacter sp. W6 и Acinetobacter sp. W9, которые выделены из активного ила, что будет описано в дальнейшем, и которые были депонированы по условиям Будапештского соглашения " The National Collection of Indastrial and Marine Bacteria Limited" (NCIMB) 23 st. Machar Drive, Aberdeen AB2 1RV, Scotland, под соответствующими новыми добавочными номерами NCIMB 40594 и NCIMB 40595 5 ноября 1993.
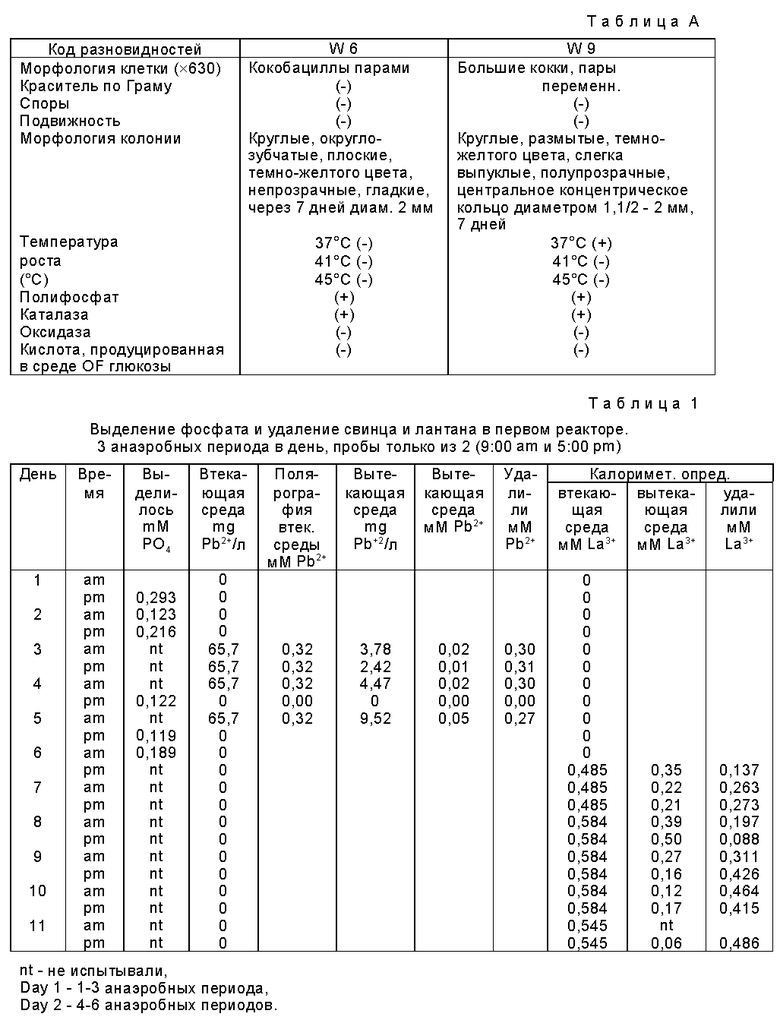
Пригодными показателями этих бактерий (которые наблюдали при росте на питательном агаре Lab M и инкубировали при 25oC) были следующие (см. в конце описания).
Было также обнаружено, что настоящее изобретение не требует того, чтобы микроорганизм, аккумулирующий полифосфат, выделяли из среды, в которой он встречается. В частности, было обнаружено, что активный ил, содержащий микроорганизмы, аккумулирующие полифосфат, может быть использован в настоящем изобретении сам по себе. Подходящим видом активного ила является такой, который используют на установке для удаления ионов фосфора из вытекающих (сточных) вод (например путем так называемого способа "Phostrip" или "Phoredox" перед сливом в окружающую среду.
Следует принять во внимание, что методики настоящего изобретения основаны на подаче фосфора. Такая подача может быть обеспечена по крайней мере частично, путем осторожного добавления ассимилируемого источника фосфора. Однако понятно, что настоящее изобретение применимо к удалению металла(ов) из воды, которая уже содержит ассимилируемый источник фосфора в виде примеси, но который не находится в той форме, в которой он может непосредственно взаимодействовать с примесью металла(ов), также присутствующей в воде, или в которой примесь металла не находится в той форме, в которой она может взаимодействовать с фосфором.
Рабочими условиями на аэробной и анаэробной стадиях способа являются обычные условия, которые используют для аэробной и анаэробной обработок, включающих использование микроорганизмов. Однако предпочтительно использовать низкие концентрации нитрата на анаэробной стадии, так как восстановление нитрата в нитрит может заменить кислород и может затем тормозить необходимое превращение полифосфата в фосфат.
Обычно температура находится в диапазоне от 0 до 36oC, наиболее предпочтительно от 15 до 30oC. Средой, используемой при аэробном культивировании микроорганизма, является соответствующая питательная среда, содержащая ассимилируемый углерод, азот, фосфор и другие необходимые для оптимального роста микроэлементы. Такая среда может быть отходами от другого процесса. Нет необходимости использовать дорогостоящие источники углерода и фосфора, например G2P.
В анаэробных условиях не является необходимым обеспечение таких питательных веществ, которые нужны только для создания соответствующих анаэробных условий путем обеспечения отсутствия растворенного кислорода и окисленного азота (нитрита и нитрата).
Далее будет описан типичный способ удаления тяжелых металлов из сточных вод в соответствии с настоящим изобретением.
Типичных представителей штаммов Acinetobacter sp., аккумулирующих полифосфат, выращивают аэробно и иммобилизуют на твердом носителе (например открытопористом пенополиуретане, стеклянной дроби, песке или материалах типа гравия) в биореакторе с использованием водной питательной среды, которую циркулируют через биореактор. Газообразный кислород вводят через подачу сжатого воздуха и приспособление для разрушения пузырьков. Питательная среда содержит отходы ферментации и отработанный фосфат из сточных вод, обогащенных фосфатом, в качестве источников ассимилируемого углерода, азота и фосфора.
Аэробную обработку осуществляют при температуре от примерно 20oC, при pH 7,0 в течение 24 - 48 часов, с тем, чтобы аккумулировать полифосфат.
После этого условия в биореакторе переключают на анаэробные условия, когда питательные вещества или ассимилируемый кислород не подают.
Сточные воды, содержащие тяжелые металлы, которые необходимо удалить, пропускают через биореактор с тем, чтобы осуществить контактирование с иммобилизованными бактериями, содержащими аккумулированный полифосфат.
При анаэробных условиях, бактерии лишают подачи АТР и, таким образом, начинают использовать в качестве источника энергии аккумулированный полифосфат. Результатом этого является то, что полифосфат ферментативно расщепляют для получения фосфата, который взаимодействует с тяжелыми металлами для осаждения фосфата тяжелого металла, что приводит к удалению таким образом тяжелых металлов или по крайней мере уменьшению концентрации тяжелых металлов в воде.
Затем биореактор можно переключить обратно, для того, чтобы он работал в аэробных условиях, с тем, чтобы способ можно было осуществлять циклически с периодическим выключением для замены микроорганизма, когда он становится нежизнеспособным.
Во время каждой анаэробной стадии микроорганизм может также продуцировать аккумулированных карбополимер, полигидроксибутират (PHB) при соответствующей подаче углерода, который может быть использован в качестве источника запасного углерода для роста и для генерирования АТР до топлива при дальнейшем аккумулировании полифосфата во время последующего аэробного цикла.
Настоящее изобретение будет описано более подробно в следующих экспериментах.
Описание чертежей.
Фиг. 1a представляет график, на котором концентрации фосфат-иона и иона лантана в растворе представлены в виде функции времени во время неорганического осаждения фосфата лантана в растворе, не содержащем клетки.
Фиг. 1b представляет график, на котором концентрации фосфат-иона и иона уранила в растворе представлены в виде функции времени во время культивирования в растворе, не содержащем клетки.
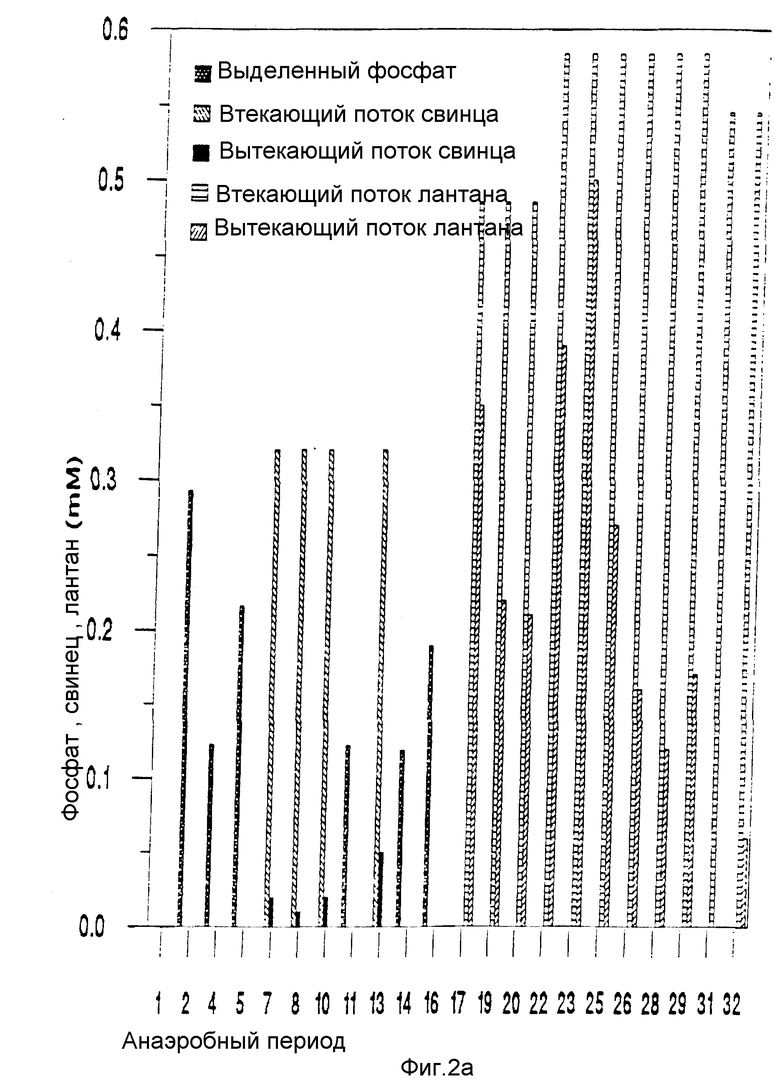
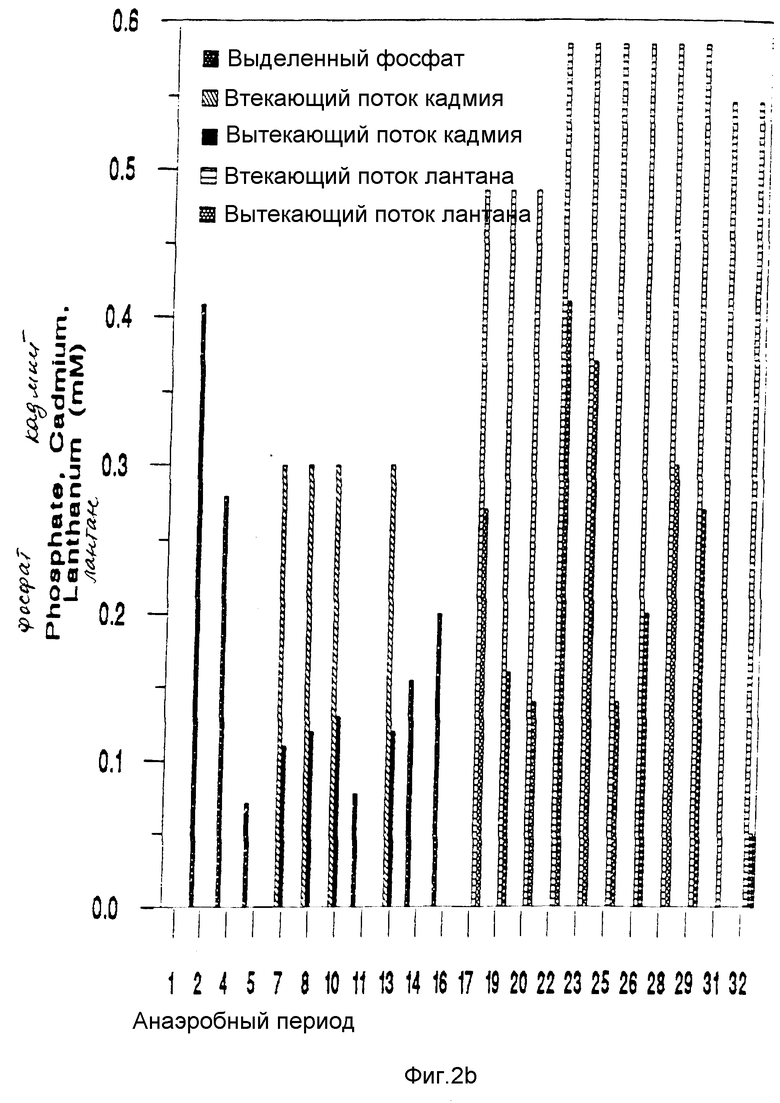
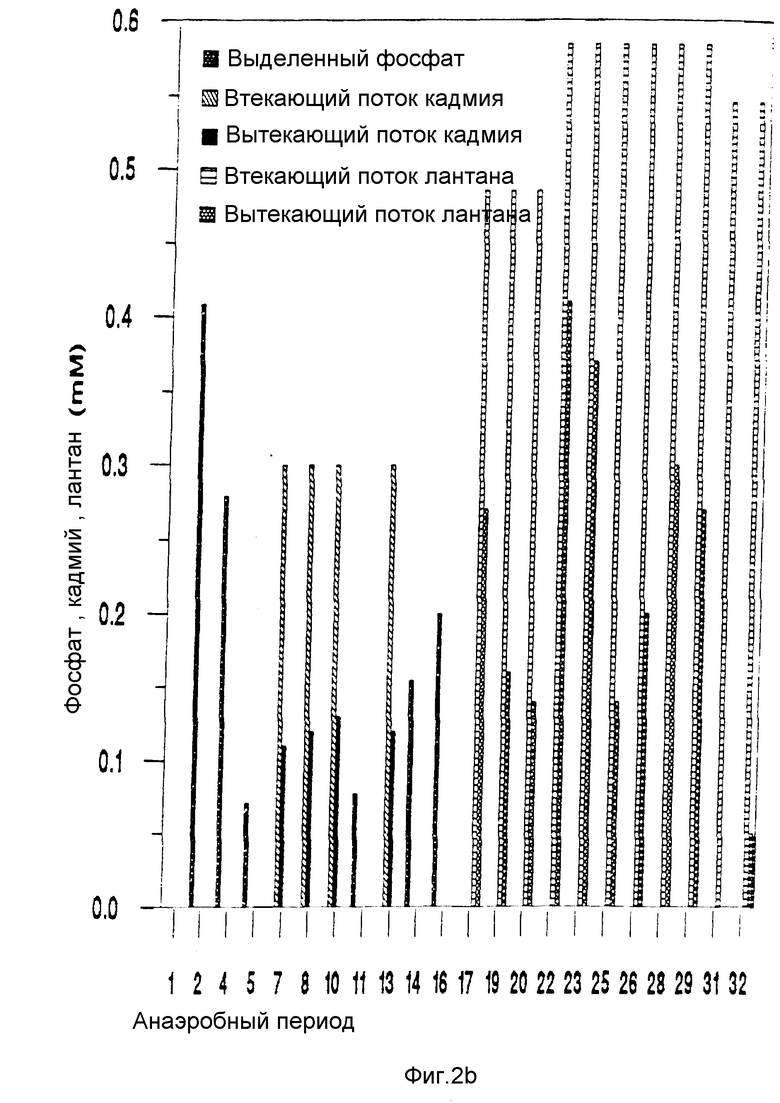
Фиг. 2a и 2b являются диаграммами, показывающими результаты, представленные соответственно в таблицах 1 и 2.
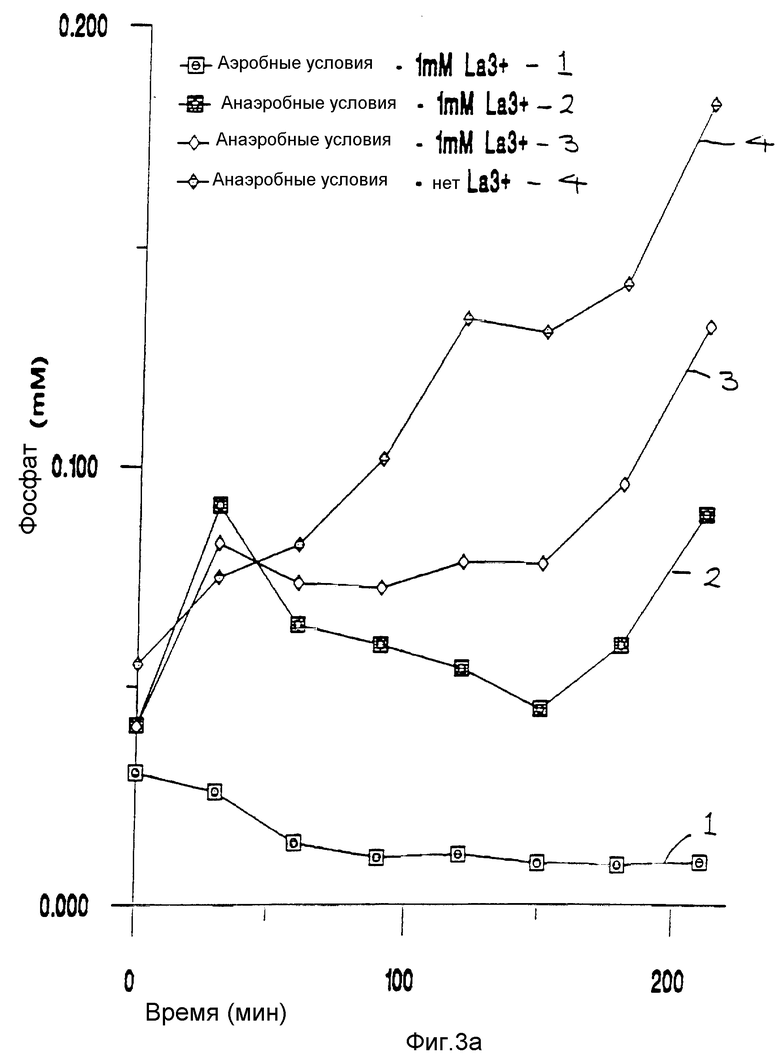
Фиг. 3a представляет график, показывающий выделение фосфата с помощью Acinetobacter calcoaceticus NCIMB 10694, на котором концентрация фосфата выражена в виде функции времени.
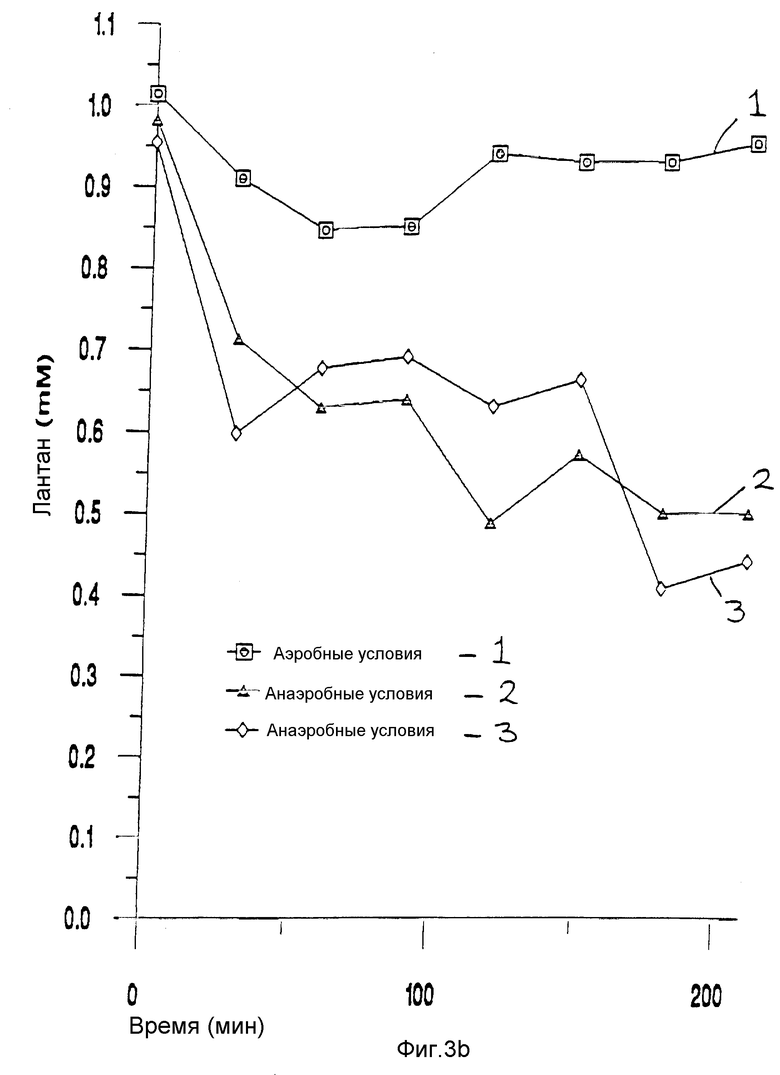
Фиг. 3b представляет график, показывающий удаление лантана с помощью Acinetobacter calcoaceticus NCIMB 10694, на котором концентрация лантана выражена в виде функции времени.
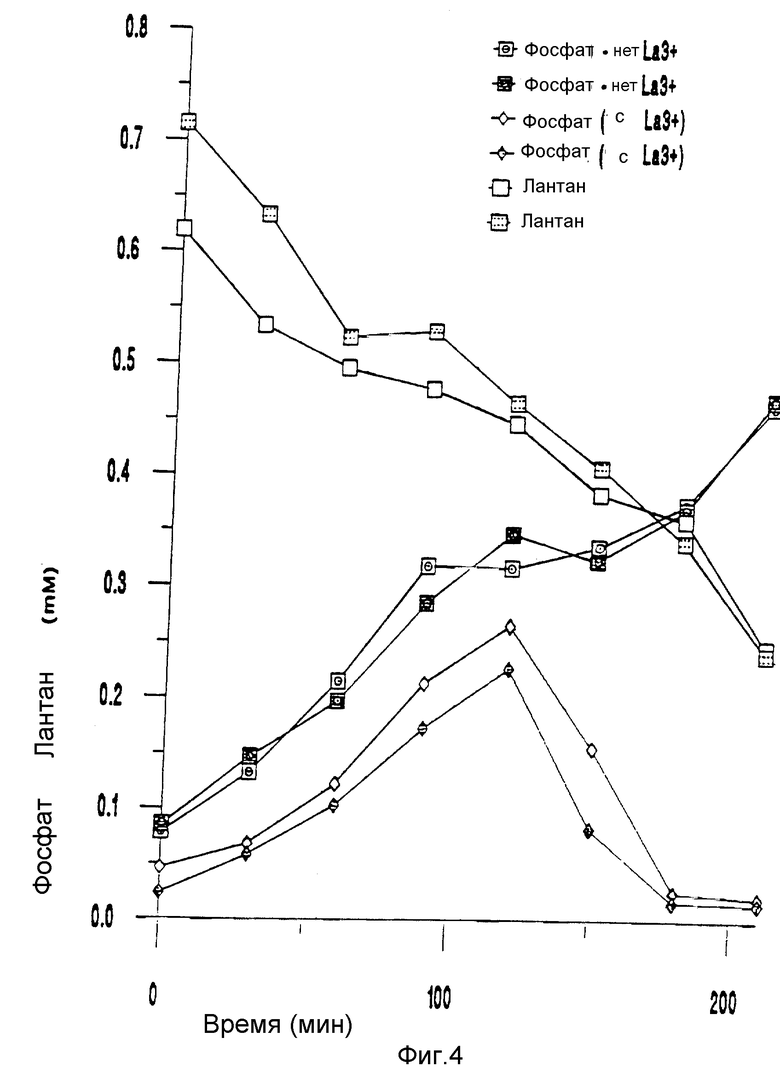
Фиг. 4 представляет график, показывающий выделение фосфата с помощью штамма W9 при анаэробных условиях в присутствии и отсутствии La3+ и удаление лантана, на котором концентрации фосфата и лантана выражены в виде функции времени.
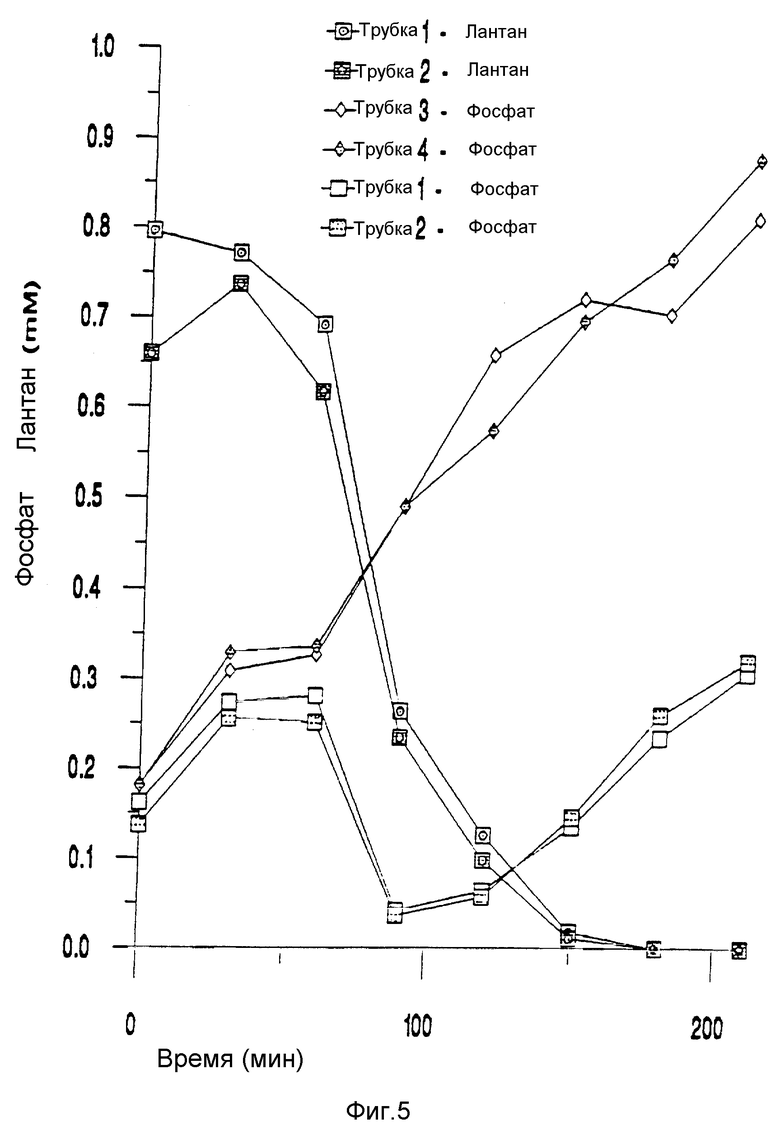
Фиг. 5 представляет график, показывающий удаление лантана и выделение фосфата с помощью клеточных суспензий штамма W6, инкубированных при анаэробных условиях, на котором концентрации фосфата и лантана представлены в виде функции времени.
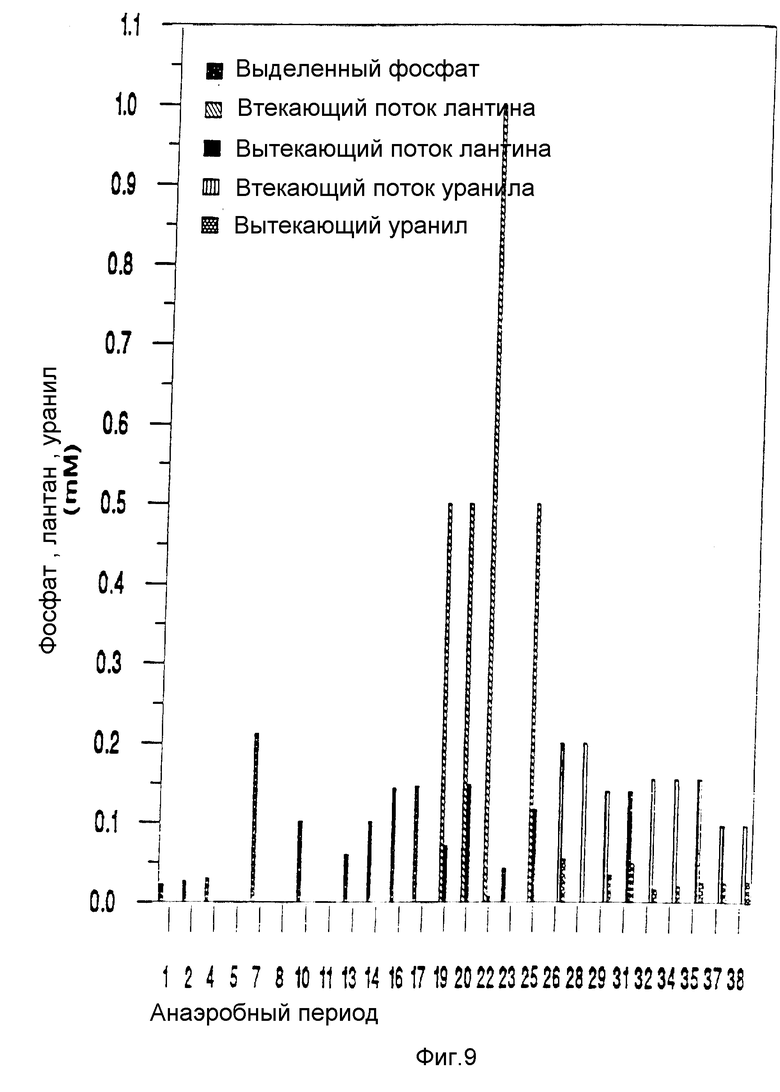
Фиг. 6-9 являются диаграммами, показывающими результаты, представленные ниже соответственно в таблицах 3-5.
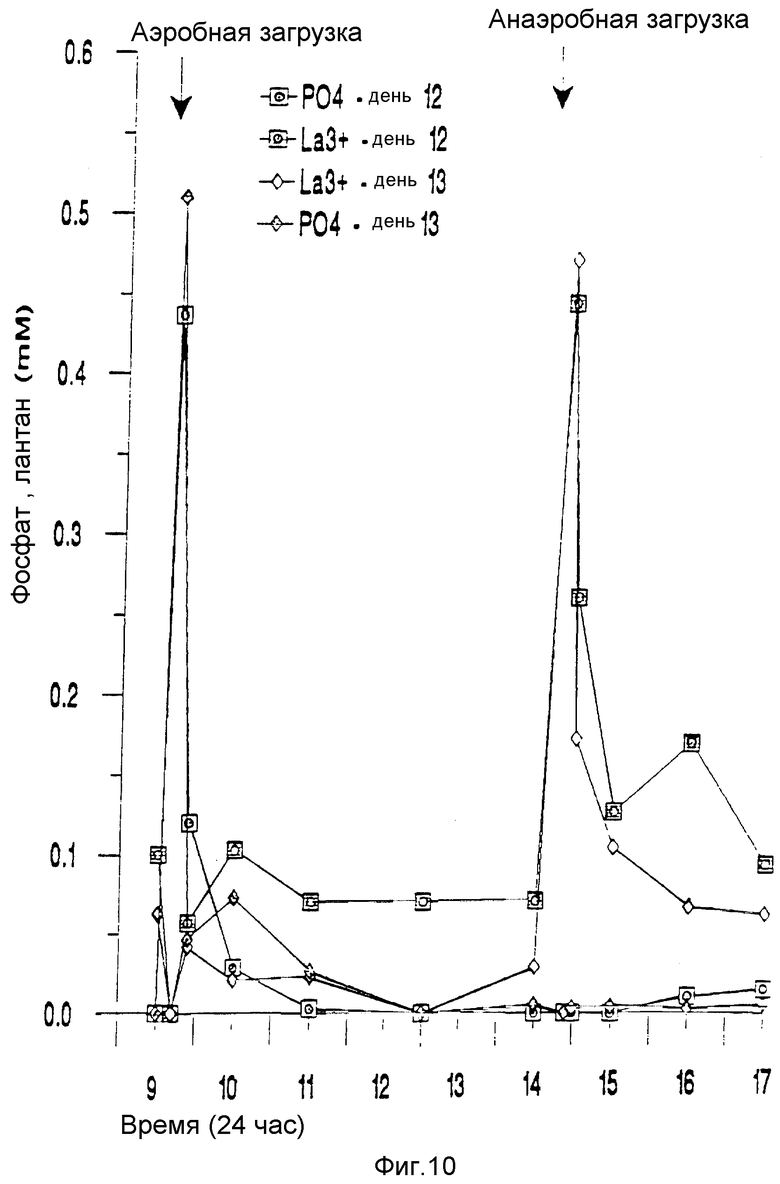
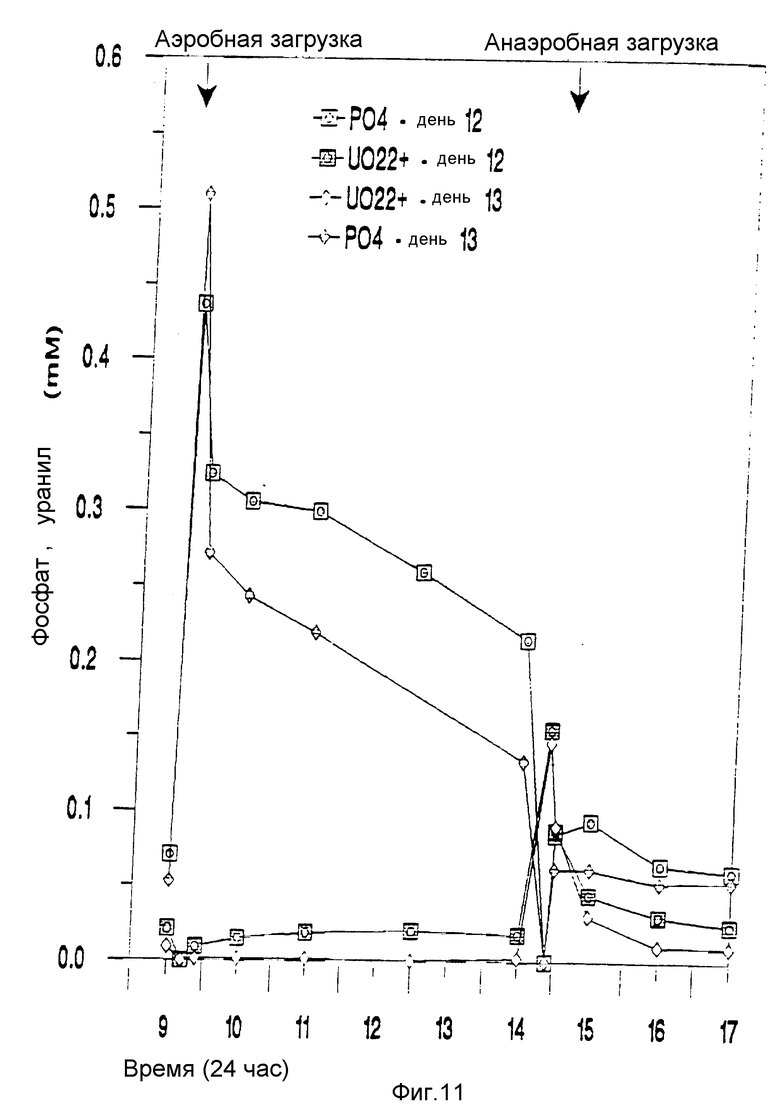
Фиг. 10 и 11 показывают концентрации фосфата и металла соответственно в первом и втором реакторах во время одного аэробного и одного анаэробного периода в течение двух последовательных дней в опыте 8, приведенном ниже, и
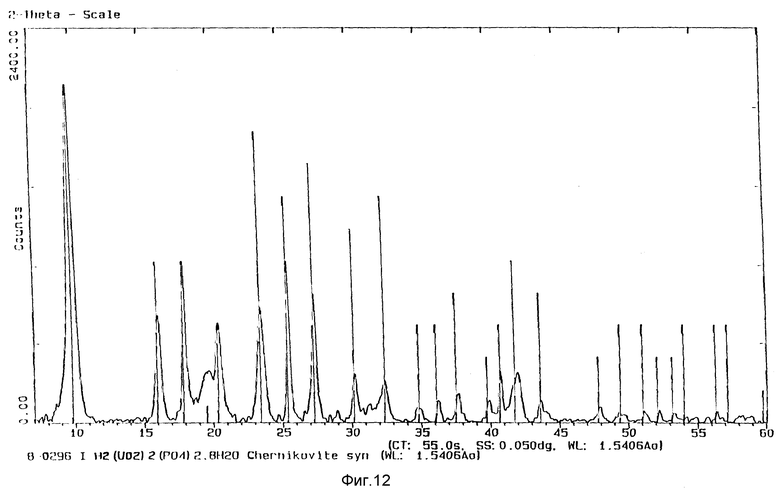
Фиг. 12 представляет рентгеновский дифракционный спектр пробы, полученной из второго реактора, используемого в опыте 8, по сравнению с таковым для чистого H2 (UO2)2(PO4)2•8H2O.
В экспериментах, представленных ниже, использовали следующие питательные среды:
Среда 1 - питательная среда, г/л
Трис - 6,0
Ацетат натрия - 5,0
(NH4)2SO4 - 1,5
MgSO4•7H2O - 0,16
CaCl2•2H2O - 0,08
KCl - 0,6
Раствор микроэлементовa, мл - 1,0
Раствор солей двухвалентного железа и EDTAb, мл - 0,25
С помощью HCl установили pH 7,1 и среду стерилизовали с помощью автоклавной обработки. Нижеприведенное стерилизовали отдельно и добавили после охлаждения:
10%-ный Дрожжевой экстракт, мл - 1
K2HPO4•3H2O, г - 0,16
a Раствор микроэлементов содержал, мг/л
ZnSO4 • 7H2O - 10
MnCl2 • 4H2O - 3
H3BO3 - 30
CoCl2 • 6H2O - 20
CuCl2 • 2H2O, мкг - 1
NiCl2 • 6H2O - 2
Na2MoO4 • 2H2O - 3
b Раствор солей двухвалентного железа и EDTA содержал (гептагидрат) сернокислого железа (II) и динатриевую соль этилендиаминтетрауксусной кислоты (коммерчески полученная смесь) 1,0 г/л]
Среда 2 - питательная среда, ограничивающая азот.
Подобна среде 1, но содержит (на л) 10 г ацетата натрия и 0.23 г K2HPO4 • 3H2O.
Среда 3 - среда аэробной стадии, содержащая, г/л:
Трис - 6,0
Ацетат натрия - 0,36
(NH4)2SO4 - 0,02
MgCl2 • 6H2O - 0,03
CaCl2 • 2H2O - 0,02
KCl - 0,012
K2HPO4 • 3H2O (подвергнутый обработке в автоклаве отдельно) - 0,136
С помощью HCl установили pH 7,1 и среду стерилизовали обработкой в автоклаве.
Среда 4 - Среда анаэробной стадии (конечные концентрации).
MOPS (3-(N-морфолино)пропансульфокислота), мМ:
Буферный раствор NaOH pH 7,0 - 40
Буферный раствор лимонный кислоты/тринатрийцитрата, pH 7,0 - 2
Ацетат натрия (стерилизованный путем обработки в автоклаве) - 10
В некоторых опытах MOРS заменили буферным раствором Трис/HCl при том же самом значении pH и концентрации. В опытах с уранил-ионами, ацетат натрия заменили 10 мМ ацетатом аммония.
Если не указано иным образом, во всех опытах осуществляли при 30oC.
Выделение микробных штаммов W6 и W9.
Смешанный раствор активного ила получили от обработки сточных вод Severn Frent (расположенной в Wimborne, Англия). Приготовили гомогенную суспензию каждой жидкости и последовательные разбавления (в стерильном солевом растворе, 0,85% вес./об) нанесли на питательный агар (Difco Laboratiries, Detroit, USA). Через 2 недели инкубации при комнатной температуре (20oC) отобрали колонии с отчетливо различными морфологиями, удалили из 10-4 - 10-6 разбавлений и покрыли полосами до чистоты тона на питательном агаре. После осуществления опытов с красителем по Граму и оксидазой, выделенные штаммы микроорганизмов (W6 и W9) пробно идентифицировали, используя полосы для идентификации API 20E и 20 NE (Система API, bio-Merieux, SA, Франция) в виде рода Acinetobacter. Штаммы W6 и W9 депонировали по условиям Будапештского соглашения "The National Collection of Industrial and Marine Bacteria Limited (NCIMB) под соответствующими новыми добавочными номерами NCIMB 40594 и NCIMB 40595 5 ноября 1993.
Методы.
(a) Опыты со свободными клетками.
50 мл исходную культуру среды 1 инокулировали и инкубировали в течение 1-2 дней. 20 мл ее использовали для инокуляции 2 л среды 2 и культуру инкубировали аэробно при принужденной аэрации сжатого воздуха в течение 24 - 36 часов. Клетки собрали посредством центрифугирования (4500 оборотов в минуту, 4oC, 30 минут). Всплывшее наверх (супернатант) слили, и часть его использовали для повторного суспендирования клеток. Каждую суспензию опять подвергли центрифугированию. Гранулы клеток опять повторно суспендировали в порции всплывшего наверх, суспензии клеток соединили и перед использованием охладили на льду.
Смешанную клеточную суспензию использовали для инокуляции среды 4 при добавлении и без добавления солей металлов, как описано в отдельных экспериментах. Воздух или газообразный азот, (не содержащий кислорода) барботировали через среду в зависимости от того, какие были необходимы условия, аэробные или анаэробные.
Время от времени удаляли 1 мл инкубационной смеси, и клетки быстро осаждали путем центрифугирования (12000 оборотов в минуту, 5 минут). Всплывшее наверх анализировали на содержание фосфата и металла.
(b) Опыты с иммобилизованными клетками.
Вырастали культуры до 4 л и собрали как описано для опытов со свободными клетками. Гранулы клеток взвесили, повторно суспендировали в 0,85% NaCl и соединили в аликвоты. Клетки иммобилизовали по-разному в агар-агаре или агарозе (конечная концентрация 3% вес./об., конечная концентрация клетки составила приблизительно 5% вес/об.) при образовании, в некоторых опытах, бусинок (со средним диаметром 1 мм) в соответствии с методом Нильсона et al. (Eur.). Appl. Microbiol. Biotechnol 17:319-326), при этом для гидрофобной фазы использовали соевое масло. В других опытах желатинированную клеточную суспензию поместили в форму и отвержденный гель раздробили путем пропускания через стальное сито для получения прессованных частиц с площадью поперечного сечения 1 мм и длиной до 10 мм. Частицы геля или бусинки промыли в солевом растворе для удаления неиммобилизованных клеток и/или прилипшего масла и поместили в предварительно стерилизованный реактор или колонну.
Здесь их инкубировали на чередующихся анаэробных и аэробных стадиях (соответственно среда 4 или 3) с металлом или без металла на анаэробной стадии как описано ниже.
Химические анализы.
Кадмий и свинец обнаруживали с помощью ASV (анодной стриппинговой вольтрамперометрии) с электродом в виде висячей ртутной капли при использовании полярографического и вольтампрометрического анализатора Metrohm 693 VA. Лантан и уранил обнаружили путем калориметрического определения с помощью соединения машьяка (III) в кислом растворе (M.R.Tolley, D.Phil. Thesis Univ. of Oxford. 1993). Фосфат определили калориметрически путем его взаимодействия с подкисленным молибдатом (Pierpont 1957 Biochem. J. 65:67-76). Данные рентгеноструктурного анализа порошка получили на дифрактометре Picker Precision с монохроматором падающего луча (германий 3 плоскости), дифрактометрической контрольной установкой Phillips PN 1710 и программным обеспечением Siemens/Socabin DIFFRAC/AT. Длительность воздействия составила 16 часов 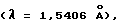 CuKα излучение.
CuKα излучение.
Подробное описание реакторов.
1) Автоматизированные реакторы.
Использовали два реактора с максимальным объемом 500 мл, содержащие 150 гр стеклянных бус диаметром 4 мм, действующих для частиц в качестве фильтра. Насосы и электрически работающие клапаны обеспечили автоматическую работу системы наполнения и всасывания с чередующимися аэробными и анаэробными периодами, и их работу регулировали посредством таймеров, при этом реакторы подвергали трем 8-ми часовым циклам в день.
Втекающую среду и реакторы перед использованием подвергали автоклавной обработке, пока трубы и клапаны стерилизовали 70%-ным этанолом и промывали дистиллированной водой. Каждый 8-ми часовой цикл выглядел следующим образом:
Время (минуты).
0-150 Инкубация на анаэробной стадии (среда 4, газообразный азот барботировали через среду с низкой скоростью для поддержания верхней части пространства бескислородным).
150-161 Стадия всасывания - среду 4 устраняли, пропускали азот.
161-166 Стадия наполнения - заполнение средой 3 (аэробная среда), азот устраняли через среду с высокой скоростью барботировали воздух.
166-464 Инкубация на аэробной стадии, пропускали воздух.
464-476 Стадия всасывания - среду 3 устраняли, пропускали воздух.
476-480 Стадия наполнения - заполняли средой 4, воздух устраняли/пропускали азот.
Ежедневно было 3 анаэробных периода в следующее время:
06.30-9.00, 14.30-17.00, 22.30-01.00. Пробы брали на анализ ежедневно в конце первого и второго анаэробных периодов, и, если подходило, в продолжение всей первой аэробной и второй анаэробной стадии (09.00-17.00). Во время третьей анаэробной стадии пробы не отбирали.
Приблизительный объем, поставляемый в каждый реактор, состоял из 200 мл среды 4 для анаэробной стадии и 250 мл среды 3 для аэробной стадии (скорость втекающего потока = 50 мл/минуту, скорость вытекающего потока = 20,8 мл/минуту).
Для анализа фосфата и металла в продолжении всей аэробной и анаэробной стадии шприцом посредством пробоотборной трубки отбирали 2-4 мл пробы. Перед анализом металла среде дали возможность отстояться, а для анализа фосфата ее центрифугировали для удаления суспендированных клеток, и всплывшее наверх анализировали. Выделение фосфата во время анаэробной стадии определяли как разницу между пробами в начале и в конце анаэробной стадии. Для вычисления удаления металла, пробам вытекающего потока дали возможность отстояться в течение 5 минут и концентрацию металла сравнили с концентрацией втекающей среды.
2) Колонные реакторы.
Насос с переменной скоростью, имеющий обратное действие ручного управления и вручную управляемые клапаны, обеспечивал асептическое изменение среды между аэробной и анаэробной стадиями. Колонные реакторы были подвергнуты двум анаэробным стадиям, каждая из которых продолжалась по 2,5 часа приблизительно в одно и то же время каждый день - 9.30-12.00 и 16.00-18.30). В качестве фильтра в основании каждой колонны использовали стеклянные бусы (диаметром 2 мм). Общий объем на каждой стадии составил 250 мл. Во время изменения между стадиями одну среду сливали, а другую среду заполняли в колонну менее чем за 5 минут. Для анализа металла, отстоявшийся вытекающий поток сравнили со втекающей средой. К пробе остаточного фосфата в колонне в начале анаэробной стадии посредством первого слива 10-15 мл среды через пробоотборную трубу отобрали пробу среды для обеспечения смыва застоявшейся жидкости в пробоотборной трубке, затем взяли еще 5 мл пробы и подвергли центрифугированию и анализу всплывшего вверх, последнее сравнили с фосфатом в отстоявшемся (супернатанте) вытекающего потока.
Опыт 1. Сравнение-неорганическое осаждение фосфатов металла в растворе, не содержащем клетки.
Нитрат лантана (1 мМ) и нитрат уранила (1 мМ) инкубировали в присутствии 0,5 мМ неорганического фосфата (в виде K2HPO4) в среде 4 при барботаже азота для обеспечения анаэробных условий. Время от времени пробы удаляли, центрифугировали (12000 оборотов в минуту, 5 минут) и всплывшее наверх анализировали на оставшийся фосфат и ионы металла.
Фиг. 1a показывает быструю потерю лантана из раствора из-за осаждения фосфата лантана. Однако, осадок мелкозернистый и остается в суспензии без центрифугирования.
Фиг. 1b показывает, что ион уранила (UO2 2+) с трудом дает осадок, который может быть удален из суспензии путем центрифугирования.
Опыт 2. Выделение фосфата и удаление металла с помощью активного ила, удаляющего фосфат.
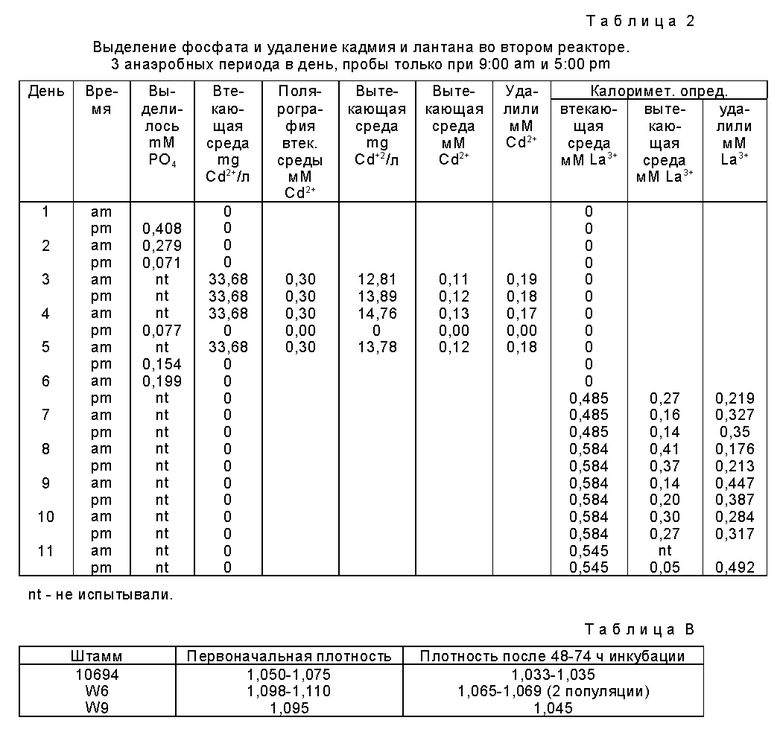
Необработанный активный ил или так называемую "смешанную жидкость" получили из питательной установки, работающей по способу "Phostrip". Общее суспендированное твердое вещество смешанной жидкости составило 6.43 г/л. 350 мл смешанной жидкости использовали для инокуляции каждого из двух автоматизированных реакторов. Ее покрыли (долили) 50 мл среды 4 (без добавленного металла) и начали первоначальную инкубацию анаэробной фазы. Реакторы первоначально работали без металла во втекающей среде 4, затем, как показано ниже в таблицах 1 и 2, добавили ацетат кадмия или свинца (0,2 мМ) или нитрат лантана (0,5 мМ).
Результаты, данные выше в таблицах 1 и 2, представлены в виде диаграммы, приложенных соответственно на фиг. 2a и 2b.
Опыт 3. Сравнение накопительной емкости полифосфата в штаммах W6 и W9, выделенных из активного ила, по сравнению с культурой штамма Acinetobacter calcaoceticus NCIMB 10694.
Клетки вырастили и собрали, как описано ранее. Клеточную суспензию, содержащую приблизительно 1,0 г клеток (мокрый вес) загрузили на предварительно сформированные градиенты плотности PercoII и центрифугировали в течение 30 минут со скоростью 9000 оборотов в минуту. Клетки образовали полосу в соответствии с их плотностью (удельной плотностью), которую определяли по отношению к маркировочным бусам (шарикам) известной плотности (чем больше полифосфата, тем выше плотность клетки), во время последующей инкубации при 30oC полифосфат подвергся деструкции и было видно, что полоса клеток продвигается к градиенту, по мере того как клетки становились менее плотными. Уменьшение плотности является мерой полифосфата с короткой цепью, который может быть легко подвержен деструкции при анаэробных условиях.
Опыт 4. Удаление лантана клеточными суспензиями Acinetobacter calcoaceticus NCIMB 10694.
Культуру Acinetobacter calcoaceticus NCIMB 10694 собрали после 24-х часов развития при оптической плотности клетки (OD600) 0.370. Мокрый вес полученной гранулы клетки составил 2.243 г и ее повторно суспендировали в общем объеме 6 мл 1 мл суспензии добавили в трубки, содержащие 10 мл каждого из следующих растворов:
Трубка 1: Среда 4 с 1 мМ нитрата лантана, инкубированная аэробно
Трубка 2 и 3: Среда 4 с 1 мМ нитрата лантана, инкубированная анаэробно.
Трубка 4: Среда 4 без металла, инкубированная анаэробно.
Пробы анализировали как описано ранее.
Фиг. 3a показывает, что фосфат выделяется при анаэробных условиях, а не при аэробных условиях, меньше фосфата выделится, по-видимому, в трубках, содержащих лантан. Фиг. 3b также показывает потерю лантана в трубках 2 и 3, которой сопутствует выделение фосфата. Значительное удаление лантана не наблюдалось в трубке 1 при аэробных условиях, что указывало на то, что существует незначительная пассивная биосорбция металла.
Опыт 5. Удаление лантана клеточными суспензиями штамма W9.
Культуру штамма W9 собрали после 24-х часов развития при плотности клетки (OD600) 1.000. Мокрый вес полученной гранулы клетки составил 5.329 г и ее повторно суспендировали в общем объеме 6 мл. 1.5 мл суспензии добавили в трубки, содержащие 20 мл каждого из следующих растворов:
Трубки 1 и 2: Среда 4 с 0.7 мМ нитрата лантана, инкубированная анаэробно.
Трубки 3 и 4: Среда 4 без металла, инкубированная анаэробно.
Пробы анализировали как описано выше.
Фиг. 4 показывает выделение фосфата и удаление лантана при анаэробных условиях с сопутствующей потерей лантана и явное уменьшение выделения фосфата в присутствии лантана, сопровождаемое внезапной потерей выделенного фосфата через 120 минут. Уменьшение концентрации лантана (0.4-0.5 мМ), наблюдаемое через 210 минут, совмещалось с выделением 0.4-0.5 мМ фосфата в контрольных трубках.
Опыт 6. Удаление лантана клеточными суспензиями выделенного штамма W6.
Культуру штамма W6 собрали после 24-х часов развития при плотности клетки (OD600) 0.790. Мокрый вес полученной гранулы клетки составил 3.80 г и ее повторно суспендировали в общем объеме 6 мл. 1.5 мл суспензии добавили в трубки, содержащие 20 мл каждого из следующих растворов:
Трубки 1 и 2: Среда 4 с 0.8 мМ нитрата лантана, инкубированная анаэробно.
Трубки 3 и 4: Среда 4 без металла, инкубированная анаэробно.
Пробы анализировали как описано выше.
Фиг. 5 показывает выделение фосфата и удаление лантана при анаэробных условиях при потере лантана и внезапной потере выделенного фосфата, начавшейся через 60 минут. Следует отметить, что полное удаление 0.7-0.8 мМ лантана произошло, когда в контрольных трубках (в отсутствии металла) обнаружили 0.7-0.8 мМ фосфат.
Опыт 7. Удаление кадмия и свинца в колонных реакторах иммобилизованными клетками штамма W9.
Культуру штамма W9 вырастили и собрали, как описано ранее, и иммобилизовали в агарозовых бусах со средним диаметром 1 мм. Бусы поместили в предварительно стерилизованную первую и вторую колонну с нагрузкой биомассы, приблизительный мокрый вес клеток которой составил 5 г (100 г желатированного материала) на колонну, хотя из-за диффузионных ограничений ожидали, что не все клетки в бусах способствуют наблюдаемой физиологии иммобилизованной культуры, например диффузионные ограничения для кислорода на поверхности обычно составляют 50 мкм. Перед тем как ввести металл, колонны подвергали анаэробному/аэробному циклу в течение 8-и дней в отсутствии металла: в первую колонну ввели в течение 7-и последовательных дней приблизительно 0.2 мМ ацетата свинца, а во вторую колонну приблизительно 0.2 мМ ацетата кадмия на анаэробный период. Пробы анализировали как описано выше.
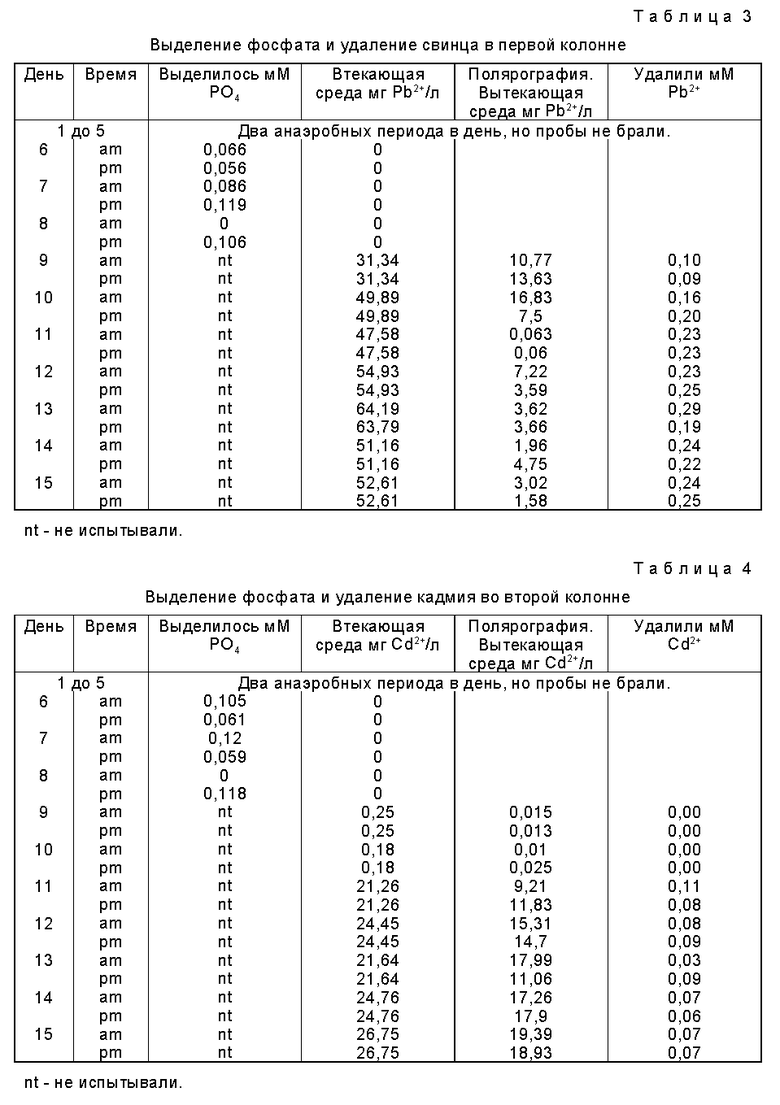
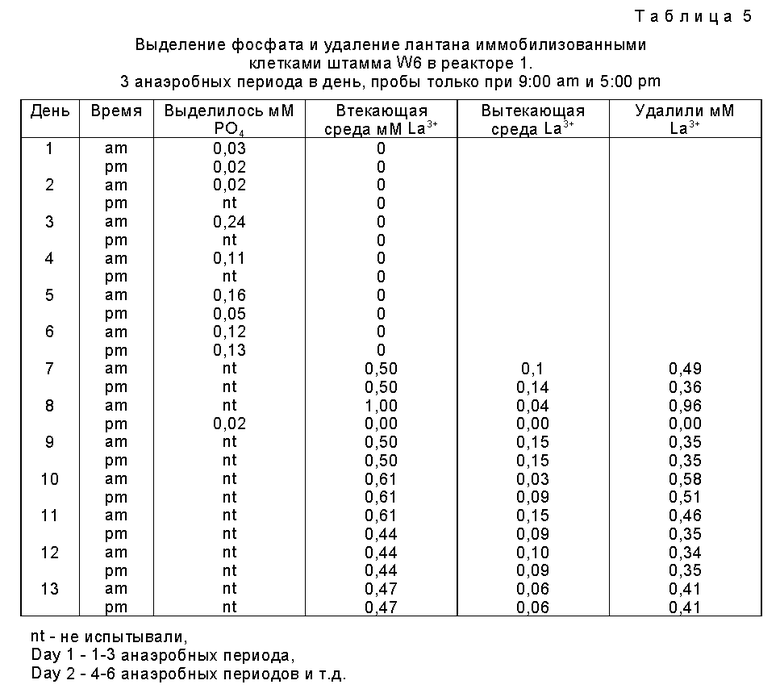
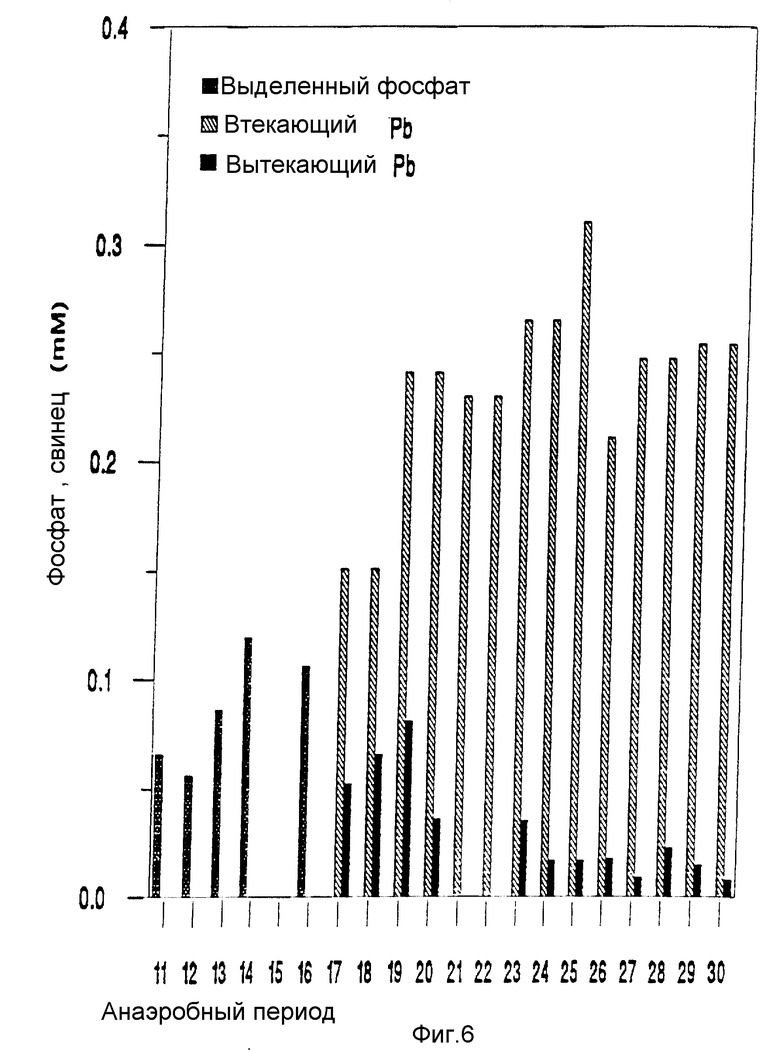
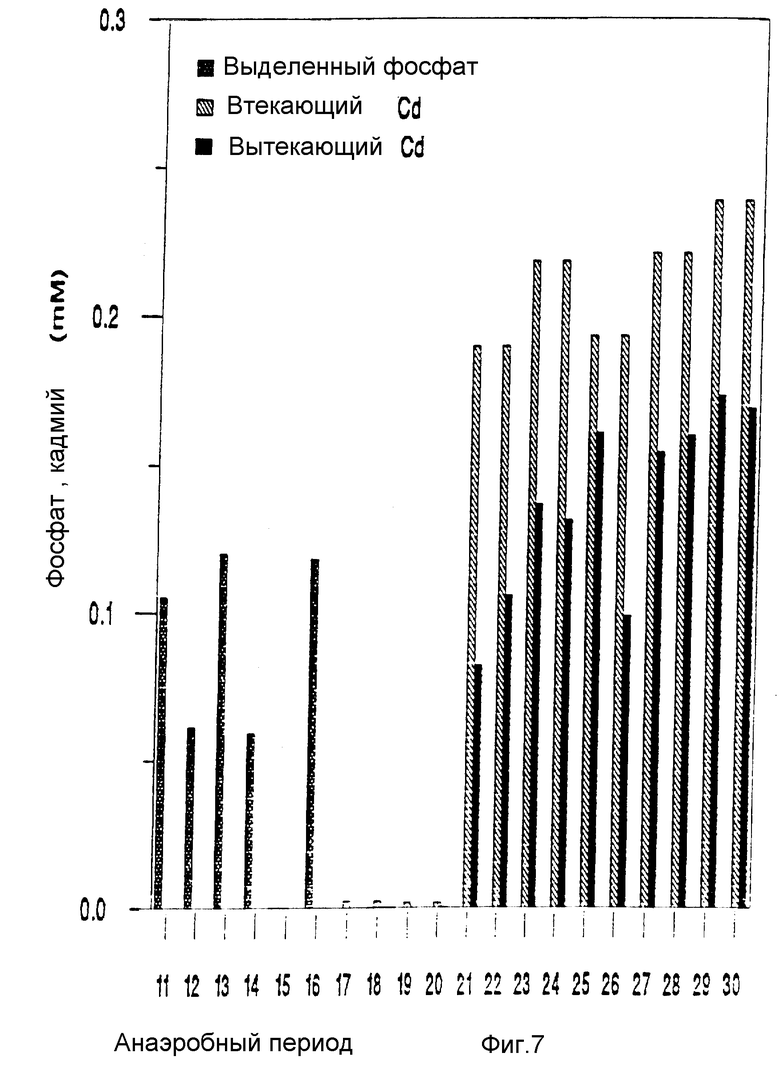
Таблица 3, приведенная ниже, и фиг. 6 показывают выделенный фосфат и определенный свинец во втекающем и вытекающем потоке первой колонны. Таблица 4, приведенная ниже, и фиг. 7 показывают выделенный фосфат и определенный кадмий во втекающем и вытекающем потоке второй колонны.
Опыт 8. Удаление лантана и урана в автоматизированных реакторах иммобилизованными клетками штамма W6.
Культуру штамма W6 вырастили и собрали как описано выше, иммобилизовали в агаре и гель раздробили до получения частиц размером приблизительно 1 мМ х 1 мм х 10 мм. Частицы поместили в предварительно стерилизованные первый и второй колонные реакторы с нагрузкой биомассы, приблизительный мокрый вес клеток который составил 5 г (100 г желатированного материала) на колонну. Перед тем как ввести металл, колонны подвергали анаэробному/аэробному циклу в течение 7 дней в отсутствии металла: первоначально в оба реактора ввели 0.5 мМ нитрат лантана, затем в первый реактор продолжали вводить лантан, в то время как во второй реактор ввели 0.2 мМ нитрат уранила. Пробы анализировали как описано выше.
В конце опыта, когда реакторы осушали, заметили, что на стеклянных бусах на основании реакторов образовалась биопленка. Пробы желатированного материала и биопленка на бусах во втором реакторе имели бледно-желтый цвет (фосфат уранила имеет желтый цвет) и было видно, что они флуоресцируют в ультрафиолетовом свете (как это делают чистые кристаллы фосфата уранила). Часть желатированного материала и стеклянные бусы сильно встряхнули в ацетоне для удаления поверхностных бактерий и кристаллического осадка. Пробу обезвожили в ацетоне, выпарили и анализировали с помощью дифракции рентгеновских лучей.
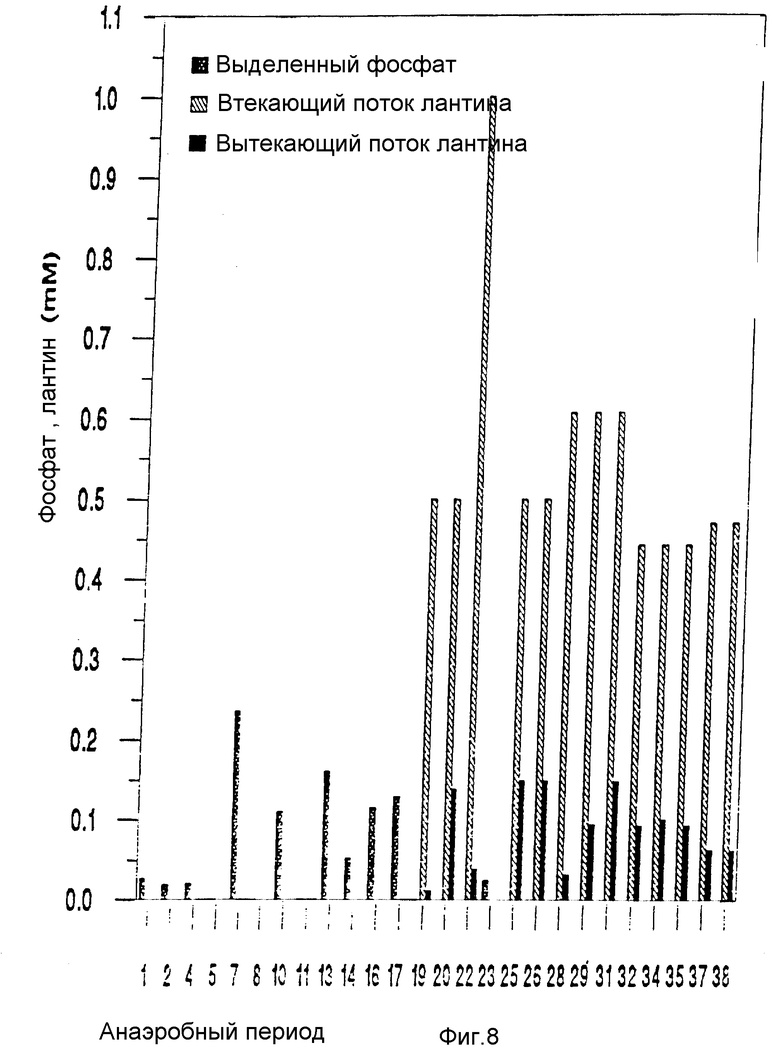
Таблица 5, приведенная ниже, и фиг. 8 показывают выделенный фосфат и определенный лантан во втекающем и вытекающем потоке первого реактора. Таблица 6 и фиг. 9 показывают выделенный фосфат и определенные лантан и уранил во втекающем и вытекающем потоке второго реактора. Фиг. 10 и 11 показывают, что не существует заметной солюбилизации осажденных металлов на аэробной стадии.
Фиг. 12 показывает, что спектр, полученный дифракцией рентгеновских лучей образца пробы из второго реактора совместим с таковым, полученным для H2(UO2)2(PO4)2 • 8H2O (Ross (1955) Am. Mineral 40, 917-919). Значения d для 10-ти самых сильных дифракционных пиков находятся соответственно в пределах 0.03 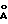 таких значений для H2(UO2)2(PO4)2 • 8H2O. Это указывает, что проба содержит кристаллический материал H2(UO2)2(PO4)2 • 8H2O.
таких значений для H2(UO2)2(PO4)2 • 8H2O. Это указывает, что проба содержит кристаллический материал H2(UO2)2(PO4)2 • 8H2O.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЕРЕРАБОТКИ ОТРАБОТАННОГО ЯДЕРНОГО ТОПЛИВА | 1997 |
|
RU2182379C2 |
| СПОСОБ И МАТЕРИАЛ ДЛЯ ОБНАРУЖЕНИЯ ИОНИЗИРУЮЩЕГО ИЗЛУЧЕНИЯ | 1994 |
|
RU2139555C1 |
| СПОСОБ ВИЗУАЛИЗАЦИИ ИЗЛУЧЕНИЯ ИЗ СЪЕМОЧНОГО ПЛАНА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1994 |
|
RU2147754C1 |
| СПОСОБ ОБРАБОТКИ ПОВЕРХНОСТИ ОБЪЕКТА, ЗАГРЯЗНЕННОГО РАДИОНУКЛИДАМИ | 1992 |
|
RU2120677C1 |
| СОРБЕНТ НА ОСНОВЕ СИЛИКАТА СУРЬМЫ ДЛЯ УДАЛЕНИЯ ИОНОВ МЕТАЛЛОВ | 1999 |
|
RU2219996C2 |
| ЗАЩИТНЫЙ КОЖУХ | 1999 |
|
RU2216059C2 |
| СПОСОБ ОБРАБОТКИ ЗАГРЯЗНЕННОГО МАТЕРИАЛА | 1995 |
|
RU2133632C1 |
| СПОСОБ СЕЛЕКТИВНОГО ИЗВЛЕЧЕНИЯ ФОСФОРА В ФОРМЕ БИОМАССЫ ИЗ ТВЕРДЫХ МАТЕРИАЛОВ | 2009 |
|
RU2531751C2 |
| ШТАММ RHODOCOCCUS RHODOCHROUS NCIMB 41164 И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ ПРОДУЦЕНТА НИТРИЛГИДРАТАЗЫ | 2004 |
|
RU2403280C2 |
| РАЗДЕЛЕНИЕ ИЗОТОПОВ ПУТЕМ ИОНИЗАЦИИ ДЛЯ ОБРАБОТКИ МАТЕРИАЛОВ ДЛЯ ЯДЕРНОГО ТОПЛИВА | 1997 |
|
RU2216390C2 |


Изобретение относится к биотехнологии и экологии. Способ заключается в удалении из воды ряда металлов путем взаимодействия с фосфатом, полученным путем ферментативного расщепления полифосфата, аккумулируемого одним или несколькими микро- организмами, которые способны аккумулировать полифосфат. К удаляемым металлам относятся кадмий, свинец, уран, лантан. Используются бактерии рода Acinetobacter. Микроорганизмы культивируют в аэробных условиях. При изменении условий на анаэробные микроорганизм использует накопленный полифосфат. Получаемые фосфат-ионы, вступая в реакцию с ионами металлов, обуславливают осаждение фосфатов металлов. Технический результат обеспечивается за счет упрощения технологии очистки воды и повышения технологической безопасности процесса. 6 з.п.ф-лы. 6 табл., 15 ил.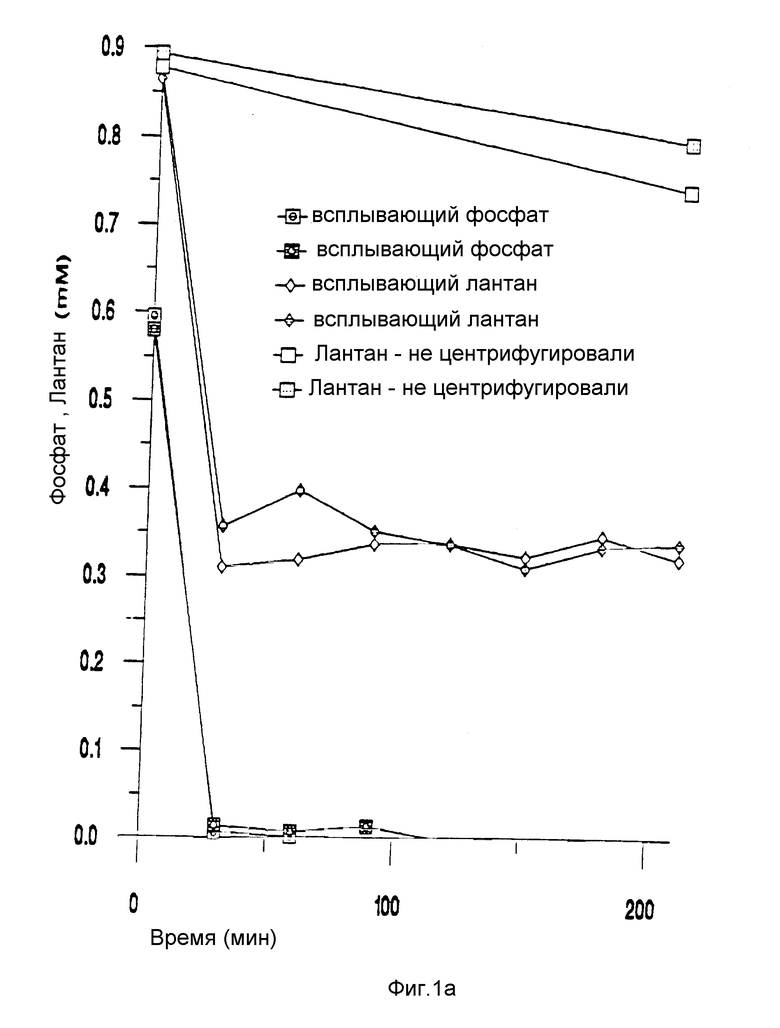
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Y.Comeau et.al | |||
| "Biochemical model for enhanced biological phosphorus removal", "Water Research", vd.20, N 12, 1986, p | |||
| Прибор для питания паровых котлов помощью резервуара, расположенного выше котла и сообщающегося то с котлом, то с атмосферой | 1925 |
|
SU1511A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| L.Macaskie, "An Immobiliged Cell Bioprocess for the Removal of Heavy Metals from Aqueous Flows", "J.of Chemical Technoloqy and Biotechnoloqy", vol.49, N 4, 1990, p | |||
| Клапан | 1919 |
|
SU357A1 |
Авторы
Даты
1999-08-27—Публикация
1993-11-12—Подача