Изобретение относится к медицине и предназначено для тепловой деструкции избирательно раковых клеток на основании большей их чувствительности к повышенной температуре по сравнению с нормальными клетками.
Известны различные способы тепловой избирательной деструкции раковых клеток с помощью лазерного испарения (сжигания) опухоли излучением 20 - 30 Вт мощности и длиной волны 1,06 мкм (см. Доценко А.П., Грубник В.В., Мельниченко Ю. А. , Шипулин П. П. Способ деструкции опухолей. Авт. св. СССР N 1383554, приоритет 22.01.86 г.).
Однако эти способы достаточно сложны из-за необходимости вводить в опухолевую ткань световод. Кроме того, они не обеспечивают избирательной деструкции только опухолевых клеток.
Известны методы лазерной фотодинамической деструкции опухолей, использующие для введения в опухолевую ткань специальные красители фотосенсибилизаторы фотогем или фотосенс, которые увеличивают поглощение и тепловое разрушение опухоли при меньших мощностях порядка 1 Вт (см. Странадко Е.Ф., Скобелкин О. К. и др. Пятилетний опыт клинического применения фотодинамической терапии. // Фотодинамическая терапия злокачественных новообразований. Материалы 2-го Всероссийского симпозиума с межд. участием. М., 1997, с. 7-19 и Ромоданов А. П., Савенко А.Г. и др. Способ лечения злокачественных опухолей головного мозга. Авт. св. СССР N 1259532, приоритет 18.05.83 г.).
Однако эти методы используют лазеры в красной области спектра (0,67 мкм), который не может проникать глубоко и используется только для деструкции поверхностных опухолей кожи и слизистых оболочек. Кроме того, эти методы не обеспечивают достаточной локальности и избирательности, так как краситель может накапливаться и в окружающих нормальных клетках или проникать не во все клетки опухоли.
Недостатками этого способа являются также трудоемкость и сложность, связанные с необходимостью введения в ткань красителя, стоимость которого относительно высока.
Известные способы фотодинамической терапии злокачественных опухолей не учитывают колебания теплоемкости и теплопроводности ткани в связи с ритмами кровенаполнения ткани. Это снижает избирательность и локальность деструкции раковых клеток относительно нормальных.
Наиболее близким к предлагаемому является способ избирательной деструкции раковых клеток, включающий нагрев ткани опухоли в диапазоне 42 - 45oC в моменты выдоха и диастолы сердца пациента в течение времени, определяемого видами опухоли, ее размерами и локализацией (см. Загускин С.Л., Ораевский В. Н. , Рапопорт С.И. Способ избирательной деструкции раковых клеток. Патент РФ N 2106159, приоритет 27.09.96 г.).
По этому способу для избирательной деструкции раковых клеток используют индукционный нагрев вводимых в опухоль ферромагнитных частиц и лазерное облучение в моменты диастолы и выдоха пациента. По известному способу с помощью СВЧ - термометра контролируют степень нагрева ткани опухоли, а компьютерное автоматическое регулирование нагрева в диапазоне 42 - 45oC синхронизировано с колебаниями теплоемкости и теплопроводности ткани, определяемыми колебаниями кровенаполнения ткани и регистрируемыми датчиками пульса и дыхания, устанавливаемыми на теле больного.
Недостатками данного способа являются трудоемкость и сложность, связанная с введением в ткань ферромагнитных частиц, недостаточная локальность нагрева.
Техническим результатом является упрощение процедуры фотодинамической деструкции раковых клеток, увеличение локальности и избирательности деструкции раковых клеток без введения красителя или ферромагнитных частиц.
Поставленная задача достигается тем, что в способе избирательной деструкции раковых клеток, включающем нагрев ткани опухоли в диапазоне 42 - 45oC в моменты выдоха и диастолы сердца пациента в течение времени, определяемого видами опухоли, ее размерами и локализацией, нагрев ткани опухоли производят с помощью лазерного облучения с длиной волны (1,264 ± 0,01) мкм и частотой следования импульсов (22,5 ± 1) кГц при средней плотности мощности излучения 0,5 - 2 Вт/см2.
Сущность изобретения заключается в том, что использование длины волны лазерного излучения (1,264 ± 0,01) мкм, соответствующей максимуму поглощения синглетного кислорода, и частоты следования импульсов (22,5 ± 1) кГц, соответствующей максимуму образования синглетного кислорода, обеспечивает максимальное выделение при данной мощности тепла и максимальную избирательную деструкцию опухолевых клеток за счет их большей чувствительности в диапазоне нагрева 42-45oC (см. Иванов А.В. О роли эндогенного кислорода в биологическом действии низкоэнергетического оптического излучения. Фундаментальные науки и альтернативная медицина. Пущино, 1997 г., с. 56).
Оптимальная для образования синглетного кислорода частота инфракрасного излучения лазера (22,5 ± 1) кГц установлена экспериментально по образованию перекиси водорода в водных растворах.
Сравнение предлагаемого способа с ближайшим аналогом позволяет утверждать о соответствии критерию "новизна", а отсутствие в известных аналогах отличительных признаков предлагаемого изобретения говорит о соответствии критерию "изобретательский уровень".
Способ осуществляют следующим образом.
После полного клинико-рентгенологического и инструментального обследования, гистологического подтверждения рака и установления невозможности проведения хирургического удаления опухоли осуществляют лазерное воздействие в следующем порядке. На теле больного устанавливают датчики пульса (например, в виде прищепки на палец, фотодиод напротив светодиода) и дыхания (например, на область диафрагмы в виде пояса, при растяжении которого меняется сопротивление, или в виде терморезистора возле носа). Сигналы с датчиков включают лазерный нагрев опухоли только в благоприятные моменты выдоха и диастолы сердца. Нагрев обеспечивается максимальным образованием синглетного кислорода при выбранной частоте следования импульсов (22,5 ± 1) кГц и максимальным поглощением при выбранной длине волны (1,264 ± 0,01) мкм синглетным кислородом фотонов лазерного излучения при средней плотности мощности 0,5 - 2 Вт/см2. Воздействие только во время диастолы сердца во время фазы выдоха, когда уменьшается кровенаполнение ткани и, следовательно, уменьшаются теплоемкость и теплопроводность, увеличивает локальность нагрева и уменьшает его инерционность. Это облегчает удержание температуры нагрева в пределах коридора 42-45oC, в котором гибнут избирательно только раковые клетки. Контроль за температурным диапазоном осуществляют путем компьютерного автоматического управления мощностью и длительностью сеанса лазерного облучения с использованием СВЧ или ультразвукового измерения температуры облучаемой ткани.
На чертеже представлена распечатка экрана компьютера при осуществлении испытаний предлагаемого способа.
Лазерный нагрев указанных параметров контролировали методами ультразвуковой и дифференциальной термометрии на больных с опухолями. Для этого использовались 3 лазерных излучателя с указанными параметрами при фокусировке лазерных лучей в месте локализации опухоли. Сеансы осуществлялись при управлении лазерным нагревом с помощью компьютера, в которой вводятся сигналы датчиков пульса и дыхания, учитывается инерционность нагрева и охлаждения с помощью разработанной программы на основании проведенных расчетов колебания теплоемкости и теплопроводности и экспериментов с контактным ультразвуковым и СВЧ-термометрами (см. распечатку экрана компьютера, представленную на чертеже). Результаты показали, что при осуществлении предлагаемого способа отпадает необходимость в использовании красителей или ферромагнитных частиц и их введения в опухолевую ткань, увеличивается глубина воздействия за счет длины волны (1.264 ± 0,01) мкм по сравнению с лазером в красной области, возможно воздействие на более глубоколежащие опухоли. Увеличение образования синглетного кислорода при использовании лазерного излучения с частотой (22,5 ± 1) кГц и длине волны (1,264 ± 0,01) мкм обеспечивает нагрев ткани за счет синглетного кислорода, не требует введения красителя и обеспечивает избирательность деструкции раковых клеток относительно нормальных при данном способе воздействия и контроле температурного диапазона нагрева.
Диапазон средней плотности мощности излучения 0,5 - 2 Вт/см2 определяется в зависимости от глубины нахождения опухоли.
Пример 1. Больной Ш.В.И., 65 лет. Диагноз: меланома кожи в области правой лопатки на спине. Размеры 2,4х3,2. Диагноз подтвержден гистологическим анализом. Проведено 16 сеансов лазерной терапии по разработанному способу с длительностью облучения одновременно всей опухоли в течение 69 мин в каждом сеансе. Уменьшение опухоли заметно на 4-й день (после 4 сеансов). После 14 сеансов визуально опухоль не наблюдалась. Гистологический анализ биопсийного материала подтвердил полное рассасывание опухоли.
Пример 2. Больной Г.Р.М., 67 лет. Диагноз: рак прямой кишки с множественными метастазами в печени и в лимфоузлах. Размер опухоли в подмышечном лимфоузле 3 - 4 мм. Гистологический анализ биопсийного материала подтвердил диагноз. Проведена лазерная терапия в режиме биоуправления с параметрами разработанного способа. 15 сеансов по 60 мин каждый. По данным обследования (пальпация, УЗИ) опухоль резко уменьшилась, практически рассосалась.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СЕЛЕКТИВНОЙ ДЕСТРУКЦИИ РАКОВЫХ КЛЕТОК | 1999 |
|
RU2147848C1 |
| СПОСОБ ИЗБИРАТЕЛЬНОЙ ДЕСТРУКЦИИ РАКОВЫХ КЛЕТОК | 1996 |
|
RU2106159C1 |
| СПОСОБ РЕАБИЛИТАЦИОННОЙ ИЗБИРАТЕЛЬНОЙ ХРОНОФОТОТЕРАПИИ | 2007 |
|
RU2341307C1 |
| СПОСОБ ПРОВЕДЕНИЯ АДАПТИВНОЙ ЛИМФОТРОПНОЙ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2022 |
|
RU2815182C1 |
| СИСТЕМА БИОСИНХРОНИЗАЦИИ ФИЗИОТЕРАПЕВТИЧЕСКИХ И ДЕСТРУКТИВНЫХ ПРОЦЕССОВ ВОЗДЕЙСТВИЯ | 2001 |
|
RU2186584C1 |
| СПОСОБ ЛЕЧЕНИЯ НАРУШЕНИЙ ФУНКЦИЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1999 |
|
RU2175874C2 |
| СПОСОБ РЕГУЛЯЦИИ СИНТЕЗА МЕЛАТОНИНА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1999 |
|
RU2149044C1 |
| СПОСОБ КОМПЕНСАЦИИ ДЕКАЛЬЦИНИЗАЦИИ КОСТНОЙ ТКАНИ | 1996 |
|
RU2141852C1 |
| СПОСОБ ЛОКАЛЬНОГО РАЗРУШЕНИЯ ОПУХОЛЕЙ С ПОМОЩЬЮ СВЧ-НАГРЕВА МАГНИТНЫХ НАНОЧАСТИЦ | 2008 |
|
RU2382659C1 |
| СПОСОБ УПРАВЛЕНИЯ ДАВЛЕНИЕМ В СЕКЦИЯХ МАНЖЕТЫ ПНЕВМОМАССАЖА | 1996 |
|
RU2103974C1 |
Изобретение относится к онкологии. Способ включает воздействие на опухоль лазерным излучением с плотностью мощности 0,5-2 Вт/см2, с длиной волны (1,264 ± 0,01)мкм и с частотой следования импульсов (22,5 ± 1)кГц во время фаз выдоха и диастолы сердца. Способ позволяет увеличить локальность и избирательность деструкции. 1 ил.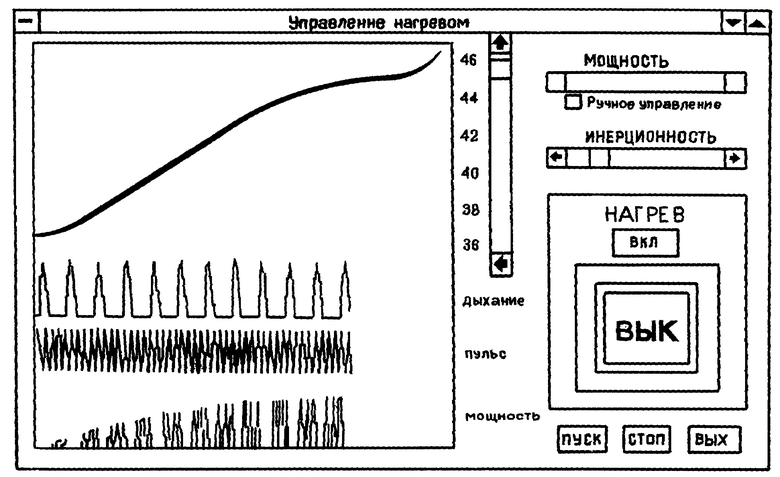
Способ избирательной деструкции раковых клеток, включающий нагрев ткани опухоли в диапазоне 42 - 45oC в моменты выдоха и диастолы сердца пациента в течение времени, определяемого видами опухоли, ее размерами и локализацией, отличающийся тем, что нагрев ткани опухоли производят с помощью лазерного облучения с длиной волны (1,264±0,01) мкм и частотой следования импульсов (22,5±1) кГц при плотности мощности излучения 0,5 - 2 Вт/см2.
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С ГЛИАЛЬНЫМИ ОПУХОЛЯМИ ГОЛОВНОГО МОЗГА | 1995 |
|
RU2067014C1 |
| МЕДИЦИНСКОЕ ЛАЗЕРНОЕ УСТРОЙСТВО | 1992 |
|
RU2045298C1 |
| СПОСОБ ЛЕЧЕНИЯ НОВООБРАЗОВАНИЙ | 1997 |
|
RU2122452C1 |
| Лазеры в клинической медицине/ Под ред | |||
| С.Д.ПЛЕТНЕВА | |||
| - М.: Медицина, 1996, с.147 - 182. | |||
Авторы
Даты
2000-04-27—Публикация
1999-05-06—Подача