Изобретение относится к способу превращения 2,4-дихлорпиридинов в 2-арилокси-4-хлорпиридины. Этот способ может быть использован для получения 3,6-ди-(C1-C4)алкил-4-хлор-2-(2,4,6-тризамещенный-фенокси) пиридинов, которые являются промежуточными соединениями в синтезе фармацевтически активных производных 2-феноксипиридина, проявляющих активность как антагонисты кортикотропин рилизинг-фактора (CRF) и являются полезными при лечении некоторых неврологических заболеваний. Такие фармацевтически активные соединения, способы их получения и неврологические заболевания, при лечении которых они полезны, описаны в находящейся одновременно на рассмотрении патентной заявке США N 08/255514, поданной 8 июня 1994. Эта заявка на патент в полном своем объеме включена в описание в качестве ссылки.
Настоящее изобретение относится к способу получения соединения формулы I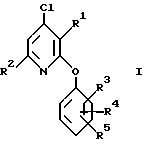
где R1 представляет собой (C1-C4)алкил;
R2 представляет метил или этил; и
R3, R4 и R5 выбирают независимо из (C1-C4)алкила и (C1-C4)алкокси;
или его фармацевтически приемлемой соли;
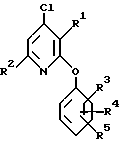
включающему взаимодействие соединения формулы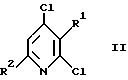
где R1 и R2 определены выше, с соединением формулы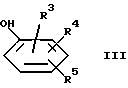
где R3, R4 и R5 определены выше, в присутствии основания, способного к депротонированию соединения формулы III, необязательно в присутствии металлоорганического галогенида или оксида и подходящего растворителя, и затем необязательно превращение полученного соединения формулы I в фармацевтически приемлемую соль такого соединения.
Подходящие основания для данной реакции включают гидрид натрия, гидрид калия, карбонат калия, карбонат цезия, гидроксид аммония, н-бутиллитий и литий, (C1-C4)алкоксид натрия или калия. Примерами подходящих металлоорганических галогенидов и оксидов являются бромид, иодид или хлорид меди (I), оксид меди (II), оксид меди (I), металлическая медь и триалкилхлорид олова. Примеры подходящих растворителей представляют собой тетрагидрофуран (ТГФ), диметилсульфоксид (ДМСО), ацетонитрил, метилен хлорид (CH2Cl2), 1-метил-2-пирролидинон, пиридин, хинолин, N,N-диалкилацетамид, 2,4,6-триметилпиридин, N, N-диалкилацетамид, N,N-диалкилформамид (например, N,N-диметилформамид), гексаметил фосфорамид и толуол. Температура реакции может изменяться в интервале от примерно 0oC до примерно 180oC и предпочтительно находится между примерно комнатной температурой и примерно 150oC.
Предпочтительное воплощение настоящего изобретения относится к вышеуказанному способу, в котором образующееся соединение формулы I является соединением, в котором все из R1, R2, R3, R4 и R5 представляют собой метил, растворитель является пиридином, металлоорганический галогенид или оксид представляют иодид меди (I) и основание является трет-бутоксидом калия.
Другое воплощение настоящего изобретения относится к вышеописанной реакции соединения формулы II с соединением формулы III, в которой растворитель выбирают из диметилсульфоксида (ДМСО), пиридина, 2,4,6-триметилпиридина, хинолина и смеси упомянутых выше растворителей, основание выбирают из гидрида калия, гидрида натрия, метилата натрия, трет-бутоксида калия и трет-бутоксида натрия, и металлоорганический галогенид или оксид выбирают из бромида меди (I), хлорида меди (I) и иодида меди (I).
Другие воплощения настоящего изобретения относятся к вышеописанной реакции соединения формулы II с соединением формулы III, в которой:
(а) растворитель является пиридином, ДМСО или смесью пиридина и ДМСО или
(b) основание является гидридом натрия или трет-бутоксидом калия или
(с) металлоорганический галогенид или оксид представляют собой иодид меди (I), бромид меди (I) или хлорид меди (I);
(d) растворитель является пиридином, R1 и R2 в соединении формулы II оба являются метилом, и R3, R4 и R5 в соединении формулы III все являются метилом;
(е) растворитель является пиридином, R1 - R2 в формулах II и III все являются метилом, и основание представляет собой трет-бутоксид калия; или
(f) растворитель является пиридином R1 - R5 в формулах II и III, все являются метилом, и металлоорганический галогенид или оксид представляют собой иодид меди (I), бромид меди (I) или хлорид меди (I).
Соединения формулы I полезны как промежуточные соединения при синтезе производных 2-феноксипиридина, являющихся антагонистами кортикотропин рилизинг-фактора (CRF) и полезными при лечении заболеваний, для которых лечение антагонизированием CRF может быть результативным или облегчающим состояние. Примерами таких заболеваний являются заболевания, выбранные из воспалительных заболеваний, таких как ревматический артрит и остеоартрит, боли, астма, псориаз и аллергии; состояние, вызванное страхом; паника; фобии; навязчиво-компульсивное расстройство; пост-травматический стресс; нарушения сна, вызванные стрессом; болевые ощущения, такие как фибромиалгия; расстройства настроения, такие как депрессия, включая глубокую депрессию, единичные случайные депрессии, повторяющуюся депрессию, депрессию, вызванную чрезмерным общением с ребенком, и послеродовую депрессию; дистимия; биполярные расстройства; циклотимия; синдром усталости; головная боль, вызванная стрессом; рак; слизистый колит; болезнь Крона; синдром раздраженной толстой кишки; инфекции вирусом иммунодефицита человека (ВИЧ); нейродегенеративные заболевания, такие как болезнь Альцгеймера, болезнь Паркинсона и болезнь Гентингтона; желудочно-кишечные заболевания; нарушения пищеварения, такие как анорексия и невротическая булимия; геморрагический стресс; химическая зависимость и наркомания (например, зависимость от алкоголя, кокаина, героина, бензодиазепина или других наркотиков); синдром отвыкания от наркотиков и алкоголя; психотические случаи, вызванные стрессом; синдром недостаточности щитовидной железы; синдром несоответствующего антидиарейного гормона (ADH); ожирение: бесплодие; травмы головы, травма спинного мозга; ишемическое нейронное повреждение (т.е. церебральная ишемия, такая как церебральная гиппокампальная ишемия); возбуждающе-токсические нейронные повреждения; эпилепсия; паралич (удар); иммунные дисфункции, включая иммунные дисфункции, вызванные стрессом (например, синдром свиного стресса, вызванное погрузкой нервное возбуждение у быков, лошадиная пароксизмальная фибрилляция, и дисфункции, вызванные ограничением у цыплят, стресс у отбившихся овец, или взаимодействие человек-животное, относящееся к стрессу у собак); спазмы мускулатуры; недержание мочи; старческое слабоумие типа Альцгеймера; мультиинфарктное слабоумие; боковой амиотрофический склероз (болезнь Шарно) и гипогликемия у млекопитающих, включая человека.
Фармацевтически активные CRF-антагонисты, которые могут быть получены с использованием промежуточных соединений формулы I, получаемых способом настоящего изобретения, указаны ниже.
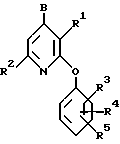
В этих соединениях B представляет собой -NR6R7, -NHCHR6R7, -OCHR6R7 или -SCHR6R7;
R1 - R5 принимают значения, как определено выше;
R6 является C1-C6-алкилом, который может быть необязательно замещен одним или двумя заместителями R8, независимо выбранными из группы, состоящей из гидрокси, фтора, хлора, брома, иода, CF3 и C1-C4-алкокси, и где вышеупомянутый C1-C6-алкил и (C1-C4)алкильная часть вышеуказанного C1-C4-алкокси могут необязательно содержать одну двойную или тройную углерод-углеродную связь; и
R7 представляет собой C1-C12-алкил, арил или -(C1-C4-алкилен)арил, где указанный арил представляет собой фенил, нафтил, тиенил, бензотиенил, пиридил, хинолил, пиразинил, пиримидил, имидазолил, фуранил, бензофуранил, бензотиазолил, изотиазолил, бензизотиазолил, бензизоксазолил, бензимидазолил, ипдолил или бензоксазолил; 3-8-членный циклоалкил или -(C1-C6-алкилен)циклоалкил, где один или два кольцевых углерода указанного циклоалкила, имеющего по меньшей мере 4 кольцевых члена, и циклоалкильная часть вышеуказанного -(C1-C6-алкилен)циклоалкила, имеющего, по меньшей мере, 4 кольцевых члена, могут быть необязательно замещены атомом кислорода или серы, или N-R9, где R9 представляет водород или C14-C4-алкил; и где каждая из упомянутых выше R7 групп может быть необязательно замещена от одного до трех заместителями, выбранными независимо из хлора, фтора и C1-C4-алкила, или одним заместителем, выбранным из брома, иода, C1-C6-алкокси, -O-CO-(C1-C6-алкил), O-CO-N(C1-C4-aлкил)(C1-C2-алкил), -S(C1-C6-алкил), CN, NO2, -SO(C1-C4-aлкил), и -SO2(C1-C4-алкил), где вышеуказанный C1-C12-алкил и C1-C4-алкиленовая часть указанного -(C1-C4-алкилен)арила могут необязательно содержать одну углерод-углерод двойную или тройную связь;
или -NR6R7 может образовывать насыщенное 5-8-членное карбоциклическое кольцо, которое может необязательно содержать одну или две углерод-углеродные двойные связи, и в котором один или два кольцевых углерода могут быть необязательно замещены атомом кислорода или серы.
Фармацевтически активные соединения, указанные выше, описаны в находящейся одновременно на рассмотрении патентной заявке США N 08/255514, поданной 8 июня 1994, которая полностью включена в описание в виде ссылки. Способы получения таких соединений и их фармацевтически приемлемых солей (в дальнейшем совместно ссылаются как на "активные агенты") также излагаются в этой заявке.
Активные агенты могут вводиться сами по себе или в комбинации с фармацевтически приемлемыми носителями в единичной или многократных дозах. Подходящие фармацевтические носители включают инертные твердые разбавители или наполнители, стерильные водные растворы и различные органические растворители. Фармацевтические композиции, образованные сочетанием соединений формулы I и фармацевтически приемлемых носителей, могут легко вводиться в разнообразных дозировочных формах, таких как таблетки, порошки, пастилки, сиропы, растворы для инъекций и т.п. Эти фармацевтические композиции могут, если желательно, содержать дополнительные ингредиенты, такие как ароматизаторы, связующие вещества, эксципиенты и т.п. Таким образом, для целей перорального введения таблетки, содержащие различные эксципиенты, такие как цитрат натрия, карбонат кальция и фосфат кальция, могут использоваться с различными разрыхлителями, такими как крахмал, метилцеллюлоза, альгиновая кислота и некоторые комплексные силикаты, вместе со связующими агентами, такими как поливинилпирролидон, сахароза, желатин и аравийская камедь. Дополнительно часто полезны в целях таблетирования смазывающие агенты, такие как стеарат магния, лаурилсульфат натрия и тальк. Твердые композиции подобного типа могут также использоваться в качестве наполнителей в мягких и твердых наполненных желатиновых капсулах. Предпочтительные материалы для этого включают лактозу или молочный сахар и полиэтиленгликоли высокого молекулярного веса. Когда для перорального введения желательны водные суспензии или эликсиры, то необходимый активный ингредиент в них может быть объединен с различными подсластителями или ароматизирующими агентами, красящими материалами или красителями и, если желательно, эмульгирующими или суспендирующими агентами вместе с разбавителями, такими как вода, этанол, пропиленгликоль, глицерин и их комбинации.
Для парентерального введения могут применяться растворы, содержащие активные агенты в кунжутном или арахисовом масле, водном пропиленгликоле или стерильном водном растворе. Если необходимо, такие водные растворы могут быть забуферены подходящим образом, и жидкий разбавитель сначала превращен в изотонический посредством достаточного количества солевого раствора или глюкозы. Эти специфические водные растворы особенно пригодны для внутривенного, внутримышечного, подкожного и внутрибрюшинного введения. Используемые стерильные водные среды все легко получить стандартными методами, известными специалистам.
Эффективные дозировки для активных агентов будут зависеть от назначенного пути введения и таких факторов, как возраст, вес и состояние пациента, обычно известных врачу. Доза будет также зависеть от особенностей болезни, которую лечат. Дневная доза для болезней, вызванных стрессом, воспалительных заболеваний, болезни Альцгеймера, желудочно-кишечных заболеваний, анорексического невроза, геморрагического стресса и синдрома отвыкания от наркотиков и алкоголя будут обычно изменяться от примерно 0,1 до примерно 50 мг/кг веса тела пациента, которого лечат.
Следующий экспериментальный пример иллюстрирует новый способ настоящего изобретения, но не ограничивает его объем.
Пример 1
4-хлор-3,6-диметид-2-(2,4,6-триметилфенокси)пиридин
В 2-х литровую колбу, снабженную механической мешалкой, дефлегматором и вводом для азота, загружают 250 мл пиридина. Колбу охлаждают на ледяной бане и загружают в нее 42,5 г (0,312 ммоль) 2,4,6-триметилфенола и 35,1 г (0,313 моль) трет-бутоксида калия. Колбу нагревают до комнатной температуры и загружают 50,0 г (0,284 моль) 2,4-дихлор-3,6-диметилпиридина и 13,5 г (0,071 моль) иодида меди (I). Реакционную смесь нагревают до флегмы в течение двух часов и затем охлаждают до 0oC. Реакцию разбавляют 500 мл гексана, затем смешивают с 1000 мл насыщенного хлорида аммония (NH4Cl). После нагревания до комнатной температуры смесь перемешивают в течение ночи. Слои разделяют и органический слой промывают 3 х 125 мл 1 М гидроксида аммония (NH4OH), 2 х 250 мл 3N гидроксида натрия (NaOH), 1 х 250 мл IN соляной кислоты (HCl) и 1 х 250 мл воды. После сушки над сульфатом натрия (Na2SO4) твердые вещества удаляют посредством фильтрации и промывают гексаном. Фильтрат концентрируют в вакууме до коричневого масла. Остаток смешивают с 250 мл метанола и перемешивают в течение ночи. Полученную суспензию фильтруют в вакууме. Не совсем белое твердое вещество промывают метанолом и затем сушат, получая 31,6 г (40,4%) названного соединения.
1H-ЯМР (CDCl3): 6,88 (с, 2H), 6,78 (с, 1H), 2,40 (с, 3H), 2,30 (с, 3H), 2,20 (с, 3H), 2,04 (с, 6H) м.д.
Фильтрат концентрируют в вакууме до масла и остаток смешивают с 50 мл метанола. После перемешивания в течение ночи полученную суспензию охлаждают до 0oC и фильтруют в вакууме. Твердое вещество промывают минимальным количеством метанола и сушат, получая дополнительно 16,1 г (20,5%) вещества.
Изобретение относится к способу получения производных 2-арилокси-4-хлорпиридина ф-лы (I), где R1 - (C1 - C4)алкил, R2 - метил или этил, R3, R4 и R5 - (C1 - C4)алкил или (C1 - C4)алкокси, или их фармацевтически приемлемых солей взаимодействием соединения ф-лы (II) с фенолом ф-лы (III), где R1 - R5 имеют указанные значения, в присутствии основания, способного к депротонированию соединения ф-лы (III), и в присутствии металлического галогенида и пиридина с последующим переводом в случае необходимости полученного соединения в фармацевтически приемлемую соль. Соединения ф-лы (I) могут быть использованы в качестве промежуточных соединений при получении производных 2-феноксипиридина, которые являются антагонистами кортикотропин рилизингфактора (GRF) и используются при лечении различных заболеваний, например воспалительных заболеваний. 5 з.п. ф-лы.
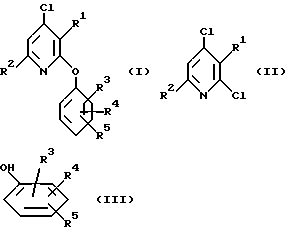
где R1 - (С1-С4) алкил;
R2 - метил или этил;
R3, R4 и R5 выбирают независимо из (С1-С4) алкила и (С1-С4) алкокси,
или их фармацевтически приемлемых солей, отличающийся тем, что включает взаимодействия соединения формулы II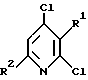
где R1 и R2 принимают значения, определенные выше,
с соединением формулы III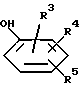
где R3, R4 и R5 принимают значения, определенные выше,
в присутствии основания, способного к депротонированию соединения формулы III, в присутствии бромида меди (I), хлорида меди (I) или иодида меди (I) и пиридина, и затем необязательно превращение получающегося соединения формулы I в фармацевтически приемлемую соль такого соединения.
| US 3637720 А, 25.01.72 | |||
| СПОСОБ АВТОМАТИЧЕСКОГО ОБМЕРА ДЛИН БРЕВЕН НА ПРОДОЛЬНЫХ ТРАНСПОРТЕРАХ | 0 |
|
SU315916A1 |
| СУППОРТНЫЙ ТОКАРНЫЙ РЕЗЕЦ ДЛЯ ОБТАЧИВАНИЯ ПРЕССОВАННОЙ ДРЕВЕСИНЫ И ПЛАСТМАСС | 0 |
|
SU385720A1 |
| Цилиндрический сушильный шкаф с двойными стенками | 0 |
|
SU79A1 |
| Способ получения сложных эфиров пиридинилоксифеноксипропановой кислоты | 1984 |
|
SU1373319A3 |
Авторы
Даты
2000-07-20—Публикация
1995-06-06—Подача