Изобретение относится к области теплофизических измерений и может быть использовано для прецизионных измерений теплот сгорания природного газа, при метрологической аттестации образцовых мер в виде индивидуальных компонентов или многокомпонентных смесей, а также при разработке новых видов топлив и в прецизионных измерениях термодинамических свойств газообразных и легколетучих органических соединений с целью получения ключевых термохимических величин, таких как энтальпия сгорания и энтальпия образования.
Повышение стоимости природного газа имело и имеет своим следствием повышение требований к точности определения его калорийности. Так, в США энергия сгорания природного газа должна быть установлена на основании принятого Конгрессом США в 1978 г. "Положения о политике в области природного газа" (так называемый "Gas Act") с погрешностью не более 0,1% [1]. В результате этого на смену газовым калориметрам, имевшим погрешность измерения не менее 1%, пришли газовые хроматографы, которые на основании анализа состава природного газа позволяли рассчитывать его теплоту сгорания. Этот метод определения калорийности природного газа является в настоящее время основным при его добыче, транспортировке и распределении [2]. Благодаря усилиям международной организации по стандартизации (ISO) он был в течение ряда лет тщательно отработан и в версии 1996 г. позволяет, при определенных допущениях, производить расчет энергии сгорания природного газа с погрешностью, равной 0,1%, определяющей современный уровень требований к точности определения калорийности природного газа. Для этого одновременно был стандартизован в международном масштабе и хроматографический метод анализа природного газа [3].
Указанная погрешность расчета (0,1%) получается при допущении, что значения энергий сгорания индивидуальных компонентов, входящих в состав природного газа, известны с такой высокой точностью, что их неопределенность не оказывает уже влияния на суммарную погрешность расчета. В действительности это допущение не выполняется.
Установлено, что при современном уровне газохроматографического анализа природного газа, когда воспроизводимость результатов анализа достигает 0,02-0,04%, если принять всю суммарную погрешность расчетного метода за 100%, то более 50% этой погрешности составляет вклад, обусловленный погрешностями, с которыми прямыми калориметрическими методами измерены энергии сгорания отдельных его компонентов [4]. При этом наибольший вклад вносит погрешность измерения энергии сгорания метана, являющегося основным компонентом природного газа с концентрацией не менее 80%.
В настоящее время известны всего три работы по прецизионному измерению энергии сгорания метана [5-7], две из них [5, 6] были положены в основу рекомендаций при проведении расчетов [2]. Погрешность этого рекомендованного значения составляет по оценкам, приведенным в [2], 0,12%.
Учитывая, что недостаточная точность определения значений энергии сгорания индивидуальных компонентов природного газа становится тормозом в достижении требуемого уровня погрешности расчета калорийности природного газа, еще в 1986 г. специалистами Национального Бюро Стандартов США было высказано предложение о необходимости проведения новых исследований с целью снижения этой погрешности. Так, для метана предлагалось уменьшить погрешность не менее чем в 5 раз [8]. При этом там же подчеркивалось, что решение этой задачи требует создания совершенно новой методики и аппаратуры, существенно отличающихся от известных.
Известен способ, предназначенный для достаточно точного измерения теплоты сгорания газообразных видов топлив, основанный на измерении теплового потока, выделяющегося при кристаллизации калориметрического вещества, расплавленного перед этим в результате поглощения тепла, выделившегося при сгорании измеренной порции газа [9]. Недостатком этого способа является весьма продолжительное время, необходимое для определения теплоты сгорания. При этом продолжительность этого времени экспоненциально возрастает с повышением требований к точности измерений теплового потока, обусловленного кристаллизацией калориметрического вещества. Так, например, для измерения теплоты кристаллизации с погрешностью 0,1% требуются 8 часов.
Наиболее близким из известных в настоящее время способов измерения теплоты сгорания горючих газов и легколетучих органических соединений является уже упомянутый выше способ Россини, который и был выбран за прототип. Этот способ реализуется главным образом с помощью изопериболического калориметра [5].
Есть описание данного способа и калориметра, относящееся к 1997 г., однако, этот источник литературы труднодоступен [7], поэтому воспользуемся более ранними публикациями [10, 11], тем более, что никаких существенных изменений не претерпели ни способ, ни конструкция калориметра, начиная с пионерской работы Россини [5], опубликованной в 1931 г. Об этом можно судить по описаниям как способа, так и калориметра, содержащимся в опубликованных в последнее время монографиях [12 - 14].
Главное отличие последних модификаций данного способа связано с методом определения количества сгоревшего газа. Если Россини основывал свой расчет на измерениях количества воды, образовавшейся в результате сгорания газа, то в более поздних работах [6, 11] для этой цели определяли количество образовавшегося углекислого газа, а в работе 1997 г. [7] - количество сгоревшего газа измеряли непосредственно как разницу в массе баллона с газом до и после опыта.
Известный изопериболический калориметр [5-7, 10, 11], реализующий выбранный за прототип способ, состоит из изотермической оболочки в виде водяного термостата, размещенного в нем калориметрического сосуда, наполненного калориметрическим веществом. В калориметрическом сосуде размещены камера сгорания, снабженная газовой горелкой, и теплообменник, погруженный в калориметрическое вещество.
Известный способ реализуется следующим образом [5-7, 10, 11]:
Калориметрический сосуд, заполненный калориметрическим веществом, размещают в нише термостата, устанавливают температуру термостата равной 28,2oC, продувают камеру сгорания, зажигают исследуемый газ, определяют теплоту сгорания газа. Расчет теплоты сгорания выполняется по уравнению:
n•ΔH = C•ΔT, (1)
где ΔH - удельная энтальпия сгорания газа [кДж/моль],
n - количество сгоревшего газа [моль],
C - энергетический эквивалент калориметра, устанавливаемый предварительно в результате градуировки [кДж/К],
ΔT - исправленный подъем температуры, т.е. изменение температуры калориметрического сосуда с учетом поправки на теплообмен [К].
В калориметрическом опыте выделяют три периода:
1. Начальный, обычно продолжительностью 20 мин, в котором устанавливается начальный ход калориметра.
2. Главный, как правило, продолжительностью около 40 мин, из которых 15-20 мин приходятся на сжигание газа, в результате чего температура калориметрического сосуда возрастает примерно на 3oC, а оставшееся время идет на достижение стационарного равновесия между калориметрическим сосудом и оболочкой.
3. Конечный период продолжительностью также около 20 мин для установления хода калориметра после окончания главного периода.
В течение всех трех периодов производится измерение температуры калориметрического сосуда платиновым термометром сопротивления. Полученные данные используются для установления точного значения исправленного подъема температуры.
Если количество сгоревшего газа или паров легколетучих органических соединений определяют либо по количеству образовавшейся при сгорании воды, либо по количеству образовавшегося при этом углекислого газа, то очень важно, чтобы все поступающие в камеру сгорания газы, включая кислород и аргон, были тщательно осушены и не содержали следов углекислого газа.
Если же количество сгоревшего газа устанавливается из изменения массы баллона с газом, то эти факторы не играют такой важной роли.
Детальное описание обработки данных и способа выполнения измерений приведено в [12].
На точность измерений теплоты сгорания газов известным способом оказывает влияние ряд факторов, которые можно разделить на две группы:
I. Факторы, обусловленные способом измерения.
II. Факторы, обусловленные инструментальными погрешностями.
К факторам первой группы относятся следующие:
1. Различие между температурой газов, поступающих в калориметрический сосуд, и температурой самого сосуда.
2. Изменение разности температур, отмеченной в п.1, в течение калориметрического опыта.
3. Изменение температуры газов, выходящих из калориметрического сосуда, вследствие изменения температуры самого сосуда в ходе опыта.
4. Испарение части воды, образующейся при сгорании, и ее унос из калориметрического сосуда.
Факторы первой группы (I) определяют преимущественно величину возможной систематической погрешности известного способа измерения теплоты сгорания газов. Последнее, конечно, относится к случаю, когда условия проведения измерений сохраняются неизменными для всей серии опытов. Ряд этих факторов учитывается введением соответствующих поправок [5, 11].
Факторы второй группы (II) зависят от точностных характеристик приборов, используемых для измерения подъема температуры, массы воды и углекислого газа, образовавшихся при сгорании.
Анализ уравнения (1) показывает, что повышение точности измерения известным способом, в принципе, возможно за счет:
1. применения еще более точных приборов для измерения температуры и массы продуктов сгорания, или массы сжигаемого газа;
2. увеличения количества сжигаемого газа.
Повышение точности определения исправленного подъема температуры достигается как за счет применения более точных средств измерения температуры, так и за счет сокращения времени между измерениями.
Однако уже в пионерской работе Россини (1931 г.) чувствительность измерения температуры с помощью 25-омного термометра сопротивления и термометрического моста (Jeeds & Northsup N 47609) составляла примерно 2•10-5 К. При подъеме температуры в пределах (2,8 ± 0,2) К этой чувствительности соответствует инструментальная погрешность измерения подъема температуры, равная 1•10-3%. В работе Пильчера [11] при измерении подъема температуры с использованием термометрического моста (Tinsley, Type 4162-B) эта погрешность составила 3•10-4%. При этом важно отметить, что случайная погрешность измерения теплоты сгорания (СКО) составила у Россини 0,015%, а у Пильчера - 0,027%. В работе [7] промежуток времени между измерениями температуры с 2-х минут (как в работах Россини) или с 30 сек (как в работах [6, 11]) был сокращен до 3-х секунд.
На основании анализа методик измерений, применяемых при реализации известного способа, можно утверждать, что погрешность измерения температуры не является доминирующей в данном способе.
По-видимому, этим обстоятельством можно объяснить применение в ряде более поздних работ относительно менее точных кварцевых термометров, которые, однако, более удобны именно для калориметрических измерений.
Справедливость данного положения подтверждается последней работой [7], в которой повышение точности измерения теплоты сгорания метана достигнуто исключительно за счет повышения точности измерения подъема температуры в результате сокращения промежутка времени между измерениями температуры, с одной стороны, и массы сгоревшего метана с другой.
Наибольшую сложность для прецизионных измерений теплоты сгорания газа представляет определение количества сгоревшего газа. Именно поэтому основные попытки совершенствования способа Россини сводились, как это уже отмечалось выше, к повышению точности определения количества сгоревшего газа.
Если в исходном способе Россини неисключенный остаток погрешности измерения количества газа составлял 4•10-3%, то Пильчеру удалось уменьшить эту погрешность до 4•10-4%.
Однако при измерении калорийности природного газа не представляется возможным воспользоваться ни первым, ни вторым способом определения количества сгоревшего газа. Все дело в том, что оба эти способа рассчитаны на определение количеств только индивидуальных соединений и не пригодны для смесей, к которым относится природный газ. Для природного газа остается измерение либо его объема, либо его массы. При этом предпочтение следует отдать измерению массы как потенциально более точному способу.
В работе [7] измерение количества сгоревшего газа (метана) осуществлялось по изменению массы баллона с газом. Как правило, для проведения одного опыта использовалось около 1 г газа, что соответствовало нормируемому подъему температуры калориметрического сосуда ΔT ≅ 3 К. При измерении массы баллона с погрешностью 1,4•10-5 г, соответственно, погрешность определения массы газа (НСП) составит 1,4•10-3%.
Увеличение количества газа, используемого для проведения калориметрического опыта, также должно способствовать повышению точности определения массы сжигаемого газа и представляется перспективным направлением.
Однако, данный путь повышения точности невозможен при сохранении неизменной методики и аппаратуры, используемых в известном наиболее прецизионном способе Россини.
Увеличение количества сжигаемого газа приведет в этом случае к пропорциональному увеличению подъема температуры калориметрического сосуда и, тем самым, к возрастанию систематических погрешностей, обусловленных указанными выше факторами первой группы.
Анализ изложенного выше показывает, что для повышения точности измерения теплоты сгорания природного газа необходимо создание такого способа, который бы позволял производить измерения с применением, с одной стороны, большего количества газа, а с другой стороны, это не сопровождалось бы соответствующим увеличением подъема температуры калориметрического сосуда. Кроме того, необходимо обеспечить снижение влияния факторов, определяющих и другие источники систематических погрешностей.
Случайную погрешность измерения можно при любом способе измерений уменьшить до желаемого предела, увеличив число опытов в каждой серии измерений. Поэтому в первую очередь следует стремиться уменьшить вклад погрешностей, обусловленных влиянием факторов первой группы (см. стр. 6 пп. 1-4).
Задачей, на решение которой направлено заявляемое изобретение, является создание способа, обладающего более высокой точностью (правильностью) измерений теплот сгорания газообразных топлив, в первую очередь теплоты сгорания метана как основного компонента природного газа.
Для решения этой задачи заявляемые технические решения обеспечивают измерение теплоты сгорания существенно больших количеств газообразных видов топлив с одновременным уменьшением тепловых потерь, вызывающих систематические погрешности (см. стр. 6 пп. 1-4).
В предлагаемом способе прецизионного измерения теплоты сгорания газообразных топлив, заключающемся в том, что калориметрический сосуд с установленной в нем камерой сгорания, заполненный калориметрическим веществом с заданной температурой плавления, размещают в нише термостата, устанавливают температуру термостата равной температуре плавления калориметрического вещества, продувают камеру сгорания кислородом, зажигают исследуемый газ и определяют теплоту сгорания газа в отличие от известного способа, выделяющееся при сгорании газа тепло используют для полного плавления калориметрического вещества, при этом процесс плавления проводят в заданном температурном интервале, симметричном относительно температуры плавления калориметрического вещества, а удельную теплоту сгорания вычисляют по формуле: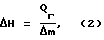
где ΔH - удельная теплота сгорания [кДж/кг],
Qг - градуировочная характеристика [кДж],
Δm - масса сгоревшего природного газа [кг].
При этом в качестве калориметрического вещества используют эвтектику Ga-Zn, имеющую температуру плавления 25,2oC, а все газы, подаваемые в калориметрический сосуд, термостатируют при температуре, равной температуре плавления калориметрического вещества.
Технический результат, получаемый при осуществлении изобретения, заключается в поглощении тепла, выделенного при сгорании больших количеств газа, без существенного повышения температуры калориметрического сосуда, что обеспечивает уменьшение тепловых потерь даже при одновременном увеличении количества сжигаемого газа. Применение в качестве калориметрического вещества эвтектики Ga-Zn, имеющей температуру плавления 25,2oC, ограничивает возможный подъем температуры калориметрического сосуда. Термостатирование всех подаваемых в горелку газов при температуре плавления эвтектики также уменьшает тепловые потери, обусловливаемые разностью температур этих газов и температурой калориметрического сосуда.
Преимущество предлагаемого способа по сравнению с известным наиболее четко проявляется уже при сравнении уравнений (2) и (1), используемых для расчета теплоты сгорания в каждом из этих способов.
Если в известном способе измеряемой величиной является прежде всего подъем температуры калориметрического сосуда ΔT и градуировочный коэффициент "C" в виде теплоемкости калориметра ("энергетический эквивалент"), то в предлагаемом способе определяемой величиной является тепловая энергия Qг, необходимая для плавления заданного количества калориметрического вещества и подъема температуры сосуда на заданный интервал (2ΔT).
На фиг. 1 представлено устройство калориметрической установки для реализации предлагаемого способа.
На фиг. 2 представлено устройство калориметрического сосуда установки для реализации предлагаемого способа.
На фиг. 3 показан разрез калориметрического сосуда по сечению А-А.
Устройство для реализации предлагаемого способа (см. фиг. 1, фиг. 2 и фиг. 3) состоит из калориметрического сосуда 1, наполненного известным количеством калориметрического вещества 2 (см. фиг. 2). В калориметрическом сосуде размещена камера сгорания 3 (фиг. 2) с электродами 4 для зажигания газа, снабженная системой трубопроводов для подачи сжигаемого газа 5; первичного кислорода 6; вторичного кислорода 7, аргона 8. Для подачи газов в камеру сгорания предусмотрены электронные регуляторы расхода газа 9-12, сосуды 13 для насыщения кислорода водой и склянки 14 для предотвращения попадания воды в регуляторы расхода кислорода. В термостатируемой оболочке 15 (водяной термостат) размещены четыре спирали 16 (по одной на каждый подаваемый в камеру сгорания 3 газ). Калориметр содержит два платиновых термометра сопротивления 17 (фиг. 1) и 18 (фиг. 2) и два электрических нагревателя 19 (фиг. 1) и 20 (фиг. 3). Нагреватель 20, состоящий из двух элементов (см. фиг. 3), размещен в калориметрическом сосуде 1, а нагреватель 19 в водяном термостате 15. Кроме того термостат 15 снабжен мешалкой 21. Между калориметрическим сосудом 1 и термостатируемой оболочкой 15 расположен массивный, из металла с высокой теплопроводностью, блок 22. Сверху калориметрический сосуд 1 закрыт крышкой 23, имеющей пазы для трубопроводов 5-8 и выводов электрических проводов к блоку управления и измерения 24. Между металлическим блоком 22 и внешней стенкой калориметрического сосуда 1 расположена батарея дифференциальных термопар 25. Трубки 26 (фиг. 2) и (фиг. 3) предназначены для вывода продуктов сгорания в камеру для сбора конденсата 27 (фиг. 2). Трубка 28 (фиг. 2) и (фиг. 3) служит для выхода газообразных продуктов сгорания из калориметра.
В качестве калориметрического вещества выбрана эвтектика Ga-Zn, т.к. ее температура плавления равна 25,2oC, т.е. максимально близка к стандартной термодинамической температуре, к которой приводятся результаты измерений энтальпии сгорания.
Предлагаемый способ реализуется следующим образом. Калориметрический сосуд 1 заполняется жидкой эвтектикой Ga-Zn 2 так, что она полностью покрывает камеру сгорания 3.
Затем калориметрический сосуд 1 охлаждают в холодильнике до полной кристаллизации эвтектики 2. После этого калориметрический сосуд 2 вынимают из холодильника и выдерживают при комнатной температуре около одного часа, пока калориметрический сосуд 1 не примет температуру окружающей среды, но не более 24oC.
Температура водяного термостата 15 устанавливается равной температуре плавления эвтектики (25,2oC) и поддерживается постоянной с погрешностью ±0,002oC. Помещают калориметрический сосуд с твердой эвтектикой в термостат.
С помощью термометра сопротивления 18, находящегося в хорошем тепловом контакте с калориметрическим веществом 2, регистрируют температуру калориметрического сосуда 1. С помощью электрического нагревателя 20 доводят температуру калориметрического сосуда 1 до 25oC и начинают измерения разности температур между калориметрическим сосудом 1 и термостатом 15 с помощью батареи диффтермопар 25.
Как только установится постоянный ход температуры калориметрического сосуда, свидетельствующий о достижении стационарного состояния, и температура калориметрического сосуда 1 (T1) будет на 0,1oC ниже температуры плавления эвтектики 2, фиксируют величину разности температур, измеренную батареей диффтермопар 25, и подают с помощью электрического нагревателя 20 постоянную электрическую мощность порядка 30 Вт, которую измеряют с погрешностью, не превышающей 0,01%. Подачу электрической мощности продолжают до тех пор, пока разность температуры, регистрируемая батареей диффтермопар, не достигнет того же исходного значения, но противоположного знака, т.е. температура жидкой эвтектики станет выше температуры плавления эвтектики на 0,1oC.
Определяют величину электрической энергии Qг, затраченной на плавление всего калориметрического вещества 2 и нагрев калориметрического сосуда от исходного значения (T1), находящегося на 0,1oC ниже температуры плавления калориметрического вещества 2, до ее конечного значения (T2), превышающего температуру плавления на 0,1oC.
Определенное таким образом значение тепловой энергии Qг является главной ключевой величиной и служит в дальнейшем в качестве градуировочной характеристики для расчета теплоты сгорания газа при проведении всех последующих измерений теплоты сгорания газов.
Измерения теплоты сгорания природного газа производят следующим образом.
Для повышения точности измерения количества сгоревшего газа по предлагаемой методике используют взвешивание баллона с газом до и после сжигания подобно тому, как это выполняется в работе [7]. Чтобы обеспечить минимальную погрешность взвешивания, следует использовать баллоны, масса которых не превышает 200 г. В этом случае современные аналитические весы позволяют производить взвешивание таких баллонов с погрешностью не более 0,1 мг.
При загрузке в калориметрический сосуд 1 250 см3 (или 1350 г) эвтектики (с учетом теплоты плавления эвтектики, равной 81,5 Дж/г, и теплоемкости калориметрического сосуда для плавления всей эвтектики и подъема температуры сосуда на 0,2oC) для проведения одного опыта потребуется примерно 3 л или примерно 2 г природного газа.
Сжигаемый газ из баллона, а также первичный и вторичный кислород и аргон подаются в газовую горелку через систему насыщения и термостатирования, как это представлено на фиг. 1. Расход сжигаемого газа регулируется таким образом, чтобы тепловыделение при его сгорании составляло примерно 30 Вт. Расход первичного и вторичного кислорода выбирается таким образом, чтобы обеспечить не только полноту сгорания газа, но и избежать при этом образования заметного количества окислов азота. Контроль полноты сгорания проверяется с помощью индикатора на окись углерода при пропускании через него продуктов сгорания. Снижения образования окислов азота добиваются уменьшением температуры пламени. С этой целью количество первичного кислорода обычно выбирают не более 20% от эквивалентного по реакции сгорания, а суммарное количество кислорода составляет при этом 150% от эквивалентного, как это рекомендовано в работе [6]. Расход аргона выбирается таким образом, чтобы предотвратить конденсацию избыточного количества паров воды, связанную с уменьшением объемов газов в результате реакции сгорания. Так, например, при сжигании метана расход аргона выбирается равным расходу метана.
Первичный и вторичный кислород в количествах, установленных в соответствии с рекомендацией [6] , подают в камеру сгорания с самого начала опыта. Подача сжигаемого газа в камеру сгорания 3 производится, как только температура калориметрического сосуда достигнет величины T1. При этом разность температур между сосудом и термостатом будет равна той же величине, что и при градуировке. Одновременно с подачей сжигаемого газа производят его зажигание, пропуская электрический разряд между электродами 4.
Подачу газообразного топлива прекращают, как только разность температур, регистрируемая с помощью батареи диффтермопар 30, поменяв свой знак, достигнет исходной величины.
При соблюдении указанных условий проведения опытов сжигания и градуировки количество теплоты, выделившейся при сгорании газа, будет точно равно количеству теплоты Qг, измеренному при градуировке. Поэтому удельная теплота сгорания газа определяется из уравнения (2):
Для повышения точности измерения количества сгоревшего газа по предлагаемой методике используют, как уже было отмечено выше, взвешивание баллона с газом до и после сжигания.
Современные аналитические весы позволяют производить взвешивание баллонов весом до 200 г с погрешностью до 0,01 мг [7]. Таким образом для Δmг, равной 2 г, погрешность измерения количества сгоревшего газа составит 7•10-4%.
Используемое в предлагаемом способе количество метана в два раза больше потребляемого в известном способе. Сжигание такого количества метана по известному способу привело бы к подъему температуры, равному 6 К, что совершенно недопустимо по причинам, изложенным выше.
Условия, обеспечивающие повышение точности измерения теплоты сгорания природного газа и других видов газообразных топлив по предлагаемому способу, заключаются, в первую очередь, в существенном уменьшении систематической погрешности, обусловленной влиянием факторов первой группы.
Рассмотрим эти факторы в той последовательности, в которой они были приведены выше (см. стр. 6).
1. Так как термостатирование всех газов, поступающих в калориметрический сосуд 1 (см. фиг. 1), производится при температуре, равной температуре плавления эвтектики, то практически вся масса газов поступает в калориметрический сосуд при температуре, равной температуре калориметрического сосуда.
Теплоемкость калориметрического сосуда, загруженного указанным количеством эвтектики, составляет примерно 1 кДж/К. (Интересно отметить, что теплоемкость калориметрических сосудов, используемых при реализации способа, выбранного за прототип, более чем на один порядок выше и составляет 15-17 кДж/К] ). Соответственно, для подъема его температуры на 0,2oC потребуются 200 Дж. Это составляет около 0,2% от величины теплоты сгорания 3 л природного газа, т.к. Qг составляет, в свою очередь, около 110 кДж.
При постоянном расходе каждого из газов 0,2% всего их количества будет поступать в калориметр при температуре последнего, отличающейся максимум на 0,1oC от температуры калориметрического сосуда. Однако даже эта малая величина сведется практически к нулю, если принять во внимание, что первая половина от этого количества газа будет вносить дополнительное количество тепла, обусловленное разностью температур оболочки и калориметрического сосуда, а вторая будет отводить по той же причине такое же количество тепла, компенсируя тем самым эффект, вызываемый первой половиной.
Таким образом измерение теплоты сгорания 99,8% всего количества газа производится в адиабатических условиях, при которых потери тепла вследствие сведения теплообмена к нулю практически исключены.
2. Отклонение температуры калориметрического сосуда 1 от температуры изотермической оболочки 15 происходит от -0,1oC до +0,1oC и продолжается в течение 0,2% времени подачи электрической мощности или сжигания газа. Как и в случае, рассмотренном в п.1, и здесь имеет место компенсация тепловых эффектов, обусловленных противоположно направленными отклонениями температуры калориметрического сосуда.
3. Изменение температуры выходящих газов (продуктов сгорания) происходит аналогично изложенному в п.1. Систематическая погрешность, обусловленная отклонением температуры выходящих газов от 25,2oC, также пренебрежимо мала. Во-первых, из-за небольшой величины как самого теплового эффекта (0,006 Дж), так и данного отклонения (максимально 0,1oC), а, во-вторых, из-за взаимной компенсации влияния данного отклонения в начале и в конце опыта.
В качестве комментария к пп. 1 и 3 уместно заметить следующее. В известном способе [5], принятом за прототип, отмечается, что для выходящих газов отклонением температуры в пределах ±0,1oC от температуры калориметрического сосуда можно пренебречь.
4. Дополнительное преимущество предлагаемого способа заключается также и в том, что ни один из газов не проходит дополнительную осушку. Более того первичный и вторичный кислород насыщаются водой при температуре 25,2oC, соответствующей температуре калориметрического сосуда. Благодаря присутствию соответствующего количества аргона, вся образующаяся при сгорании газа вода выделяется в виде конденсата и никакого уноса паров воды не происходит, так как все газообразные продукты сжигания оказываются уже насыщенными теми парами воды, которые поступили с кислородом.
Преимуществом такого способа подготовки газов является также обеспечение возможности производить измерения теплоты сгорания реального газообразного топлива, а не специально осушенного, что имеет большое значение при расчетах за газ.
Применение батареи дифференциальных термопар для измерения подъема температуры позволяет использовать преимущества измерений разности температур перед нахождением той же разности из абсолютных измерений температуры. Данное обстоятельство особенно важно, когда измеряют небольшие разности температур.
Располагая батареей диффтермопар из хромель-алюмеля, имеющей даже 60 спаев, можно с помощью цифрового вольтметра с чувствительностью 1•10-7 В определить разность температуры 0,2oC с погрешностью не более 2,8•10-2%.
Измерение количества электрической энергии, составляющего примерно 110 кДж, возможно без особых усилий произвести с погрешностью, не превышающей 5•10-3%.
Таким образом, суммируя выполненные оценки реально достижимой погрешности измерения теплоты сгорания, можно констатировать, что предлагаемый способ позволяет, располагая даже не самой прецизионной аппаратурой для измерения температуры и электрической мощности, производить измерения теплоты сгорания с инструментальной погрешностью не более 0,03%.
Предлагаемый способ обеспечивает возможность в значительной мере устранить систематические погрешности, обусловленные тепловыми эффектами из-за разности температур в течение опыта между калориметрическим сосудом, газами, подаваемыми в горелку, и продуктами сгорания. Тем самым достигается повышение достоверности (правильности) определения теплоты сгорания газов.
Библиографические данные
1. J.C. Shapiro, G.R. Burkett, W.A. Crowley in the "Gas Quality" ed. by G. I. van Rossum. Proc. Cong. Gas Quality. "Cross reference service of natural gas standard in the United States." Groningen. 22-26 April 1986. - Elsevier, Amsterdam, 1986, P. 739 - 748.
2. International Standard ISO 6976:1996. Natural Gas - Calculation of calorific value, density, relative density and Wobbe index from composition. International Organisation for Standartization. 1996.
3. International Standard ISO/ DIS 6974: 1995. Natural Gas. Determination of composition with defined uncertainty by gas chromatography. Part 1 - 5. International Organisation for Standartization. 1995.
4. R. Kenter, M. Struis and A.L.C. Smit // Process control and quality, 1991,V. I, p. 127-136. "Uncertainty of the gas chromatographic determination of the calorific value of natural gas".
5. F. D. Rossini // J. Res. NBS., 1931, V. 6, P. 37 - 49; ibid 1931, V. 7, P. 329 - 330. "The heat of combustion of methane and carbon monoxide."
6. D.A. Pittam, G. Pilcher // J. Chem. Soc. Faraday Trans., I, 1972, V. 68, P. 2224 - 2229. "Masurements of heats of combustion by flame calorimetry. Part 8: Methane, Ethane, Propane, n-Butane."
7. A. Dale, Luthall Ch., Aucott J., Sayer C., // Brennwertbestimmung von Gasen im geschaftlichen Verkehr. Vortrage des 129. PTB-Seminars am 19. /20.3.1996. Braunschweig, April 1997. PTB-Bericht ThEx-1, S. 55-68. "High precision calorimetry to determine the enthalpy of combustion of methane."
8. D. Garvin, E.S. Domalski, R.C. Wilhoit et al. in "Gas Quality", Ed. by G. J. van Rossum, Elsevier Pub., Amsterdam, 1986, P. 59-73. "Physical properties of pure components of natural gas."
9. Ю.И. Александров // Патент N 2122187. Калориметрический способ измерения энергии сгорания газообразного топлива и других легколетучих органических соединений и устройство для его осуществления. Бюллетень изобретений 1998, N 32.
10. E. J. Prosen, F.W. Maron, F.D. Rossini // J., Res., NBS., 1949, V. 42, P. 269-277. "Heat of isomerization of two butadienes."
11. G. Pilcher, H.A. Skinner, A.S. Pell, A.E. Pope // Transactions of the Faraday Soc., 1963, N 482, V. 59, P. 316 - 330. "Measurement of heat of combustion by flame calorimetry.
12. В.П. Колесов, Основы термохимии. М., Изд. МГУ, 1996, С. 134-153.
13. С.Н. Гаджиев, Бомбовая калориметрия. М., Химия, 1988, 192 с.
14. В. Хеммингер, Г. Хене, Калориметрия. Теория и практика. М., Химия, 1989, 176 с.


Изобретение относится к области теплофизических измерений. Согласно способу измерения тепловую энергию, выделившуюся в калориметрическом сосуде при сгорании газообразного топлива, используют для полного плавления введенного в сосуд калориметрического вещества, процесс плавления проводят в заданном температурном интервале, симметричном относительно температуры плавления калориметрического вещества, поддерживая при этом температуру оболочки калориметра равной температуре плавления калориметрического вещества. Теплота сгорания газообразного топлива равна тепловой энергии, необходимой для нагревания калориметрического вещества в заданном температурном интервале и установленной в процессе электрической градуировки калориметра. Технический результат - повышение точности. 2 з.п.ф-лы, 3 ил.
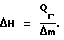
2. Способ по п.1, отличающийся тем, что в качестве калориметрического вещества используют эвтектику Ga-Zn, имеющую температуру плавления 25,2oС.
| КАЛОРИМЕТРИЧЕСКИЙ СПОСОБ ИЗМЕРЕНИЯ ЭНЕРГИИ СГОРАНИЯ ГАЗООБРАЗНОГО ТОПЛИВА И ДРУГИХ ЛЕГКОЛЕТУЧИХ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1994 |
|
RU2122187C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТЕПЛОТЫ СГОРАНИЯ ПРИРОДНОГО ГОРЮЧЕГО ГАЗА | 1995 |
|
RU2091779C1 |
| US 4613482 A, 23.09.1986 | |||
| DE 3720340 C1, 22.09.1988 | |||
| JP 91057630 A2, 22.04.1997. | |||
Авторы
Даты
2001-06-20—Публикация
1999-11-22—Подача