Настоящее изобретение относится к соединениям формулы I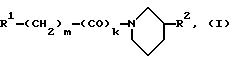
в которой R1 обозначает незамещенный либо одно- или двукратно замещенный группами Hal, CN, А, АО, ОН, CONH2, CONHA, СОМА2, СООН и/или СООА 2- или 3-индолил, 5Н-1,3-диоксоло[4,5-f]-7-индолил,
R2 обозначает незамещенный либо одно-, дву- или трехкратно замещенный группами А, АО, ОН, Hal, CN, NO2, NH2, NHA, NA2, CF3, COA, CONH2, COOH, CONHA, CONA2, OSO2A и/или ОSО2СFз бензил или фенилгидроксиметил,
Hal обозначает F, C1, Вr или J,
А обозначает прямоцепной либо разветвленный алкил с 1-10 С-атомами, который может быть замещен 1-5 F- и/или Cl-атомами, или циклоалкил с 3-10 С-атомами,
k обозначает 0 или 1 и
m обозначает 1, 2, 3 или 4,
а также к их физиологически приемлемым солям и сольватам.
Соединения подобной структуры известны, например, из международных заявок WO 95/02592 или WO 95/33743.
В основу настоящего изобретения была положена задача получить новые соединения с ценными свойствами, в частности такие соединения, которые могли бы использоваться для изготовления лекарственных средств.
Как было установлено, соединения формулы I и их соли наряду с хорошей совместимостью обладают особенно ценными фармакологическими свойствами. Они оказывают воздействие на центральную нервную систему и проявляют высокую антиэпилептическую и прежде всего антиишемическую эффективность (что было подтверждено на модели временной (неустойчивой) окклюзии центральной церебральной артерии у крыс и уменьшении неврологической симптоматики). Указанные субстанции представляют собой высокоэффективные лиганды σ-рецептора с нейропротективными свойствами (см. M. O'Neill и др., European Journ. Pharmacol. 283 (1995), стр. 217-225). Соединения, обладающие действием в качестве лигандов σ-рецептора, оказывают также влияние на NMDA-ионный канал, где NMDA (N-метил-D-аспартат) образует комплекс с соответствующими ионами (см. также H.Yamamoto и др., Journ. Neuroscience (1995), 15(1), стр. 731-736). Агонисты σ-рецептора дополнительно оказывают благотворное воздействие на возрастные нарушения памяти (ср. Maurice и др., Brain Research 733 (1996), стр. 219-230. Некоторые соединения формулы I проявляют далее сильное ингибирующее действие в отношении обратного захвата 5-НТ. От таких соединений правомерно ожидать особенно высокую антидепрессантную, анксиолитическую эффективность, а также положительное воздействие на невроз навязчивых состояний (обессивно-компульсивное расстройство (ОКР)), на нарушения в пищевом поведении, таких как булимия, на замедленную дискинезию, расстройства в процессе обучения, возрастные нарушения памяти и на психотические состояния.
Соединения формулы I и их физиологически приемлемые кислотно-аддитивные соли наряду с хорошей совместимостью обладают особенно ценными фармакологическими свойствами. Эти соединения могут применяться для лечения шизофрении, нарушений познавательной способности, состояний страха, депрессий, тошноты, замедленной дискинезии, нарушений функций желудочно- кишечного тракта или паркинсонизма. Они оказывают воздействие на центральную нервную систему и прежде всего ингибирующее в отношении обратного захвата 5-НТ действие. Для подтверждения ex-vivo ингибирования обратного захвата серотонина можно использовать метод ингибирования этого захвата на синаптическом и соматическом уровнях (см. Wong и др., Neuropsychopharmacol. 8 (1993), 23-33) антагонизм в отношении п-хлорамфетамина (см. Fuller и др., Journ. Pharmacol. Exp. Ther. 212 (1980), стр. 115-119).
Так как указанные субстанции в качестве лигандов σ-рецептора обладают нейропротективным действием, они пригодны также для применения прежде всего в качестве терапевтических средств для лечения последствий апоплексического удара, для лечения травм головного мозга и спинного мозга, равно как и для лечения ишемических состояний после остановки сердца.
Таким образом, соединения формулы I могут применяться как в ветеринарии, так и в медицине для лечения функциональных расстройств центральной нервной системы, а также воспалений. Они могут использоваться для профилактики и лечения последствий инсульта (apoplexia cerebri), таких как апоплексический удар и церебральная ишемия, а также для лечения экстрапирамидально-моторных побочных действий нейролептических средств (транквилизаторов) и болезни Паркинсона, для акутной и симптоматической терапии болезни Альцгеймера и для лечения бокового амиотрофического склероза. В равной степени они пригодны для лечения травм головного мозга и спинного мозга. В то же время они могут применяться в качестве активных веществ в таких лекарственных средствах, как анксиолитики, антидепрессанты, средства для предупреждения психотических состояний, транквилизаторы, гипотензивные средства и/или для положительного воздействия на невроз навязчивых состояний, нарушения сна, замедленную дискинезию, расстройств в процессе обучения, возрастных нарушений памяти, нарушений в пищевом поведении, в частности булемии, и/или половых расстройств.
С учетом вышеизложенного объектом изобретения являются соединения формулы I, а также их физиологически приемлемые соли.
Объектом изобретения являются в первую очередь соединения формулы I, выбранные из группы, включающей
а) 3- [4-(3-бензилпиперидин-1-ил)бутил]индол;
б) 3- [4-(3-фенилгидроксифенилпиперидин-1-ил)бутил] индол;
в) 3- [4-(3-бензилпиперидин-1-ил)бутил] -5-фториндол;
г) 3-бензил-1- [4-(5-фториндол-3-ил)бутаноил] пиперидин;
д) 3-бензил-1-14-(5-хлориндол-3-ил)бутаноил] пиперидин;
е) 3- [4-(3-бензилпиперидин-1-ил)бутил] -5-карбоксииндол;
ж) метиловый эфир 3-[4-(3-бензилпиперидин-1-ил)бутил]индол-5-карбоновой кислоты;
з) метиловый эфир (-)-3-{4-[3-(3R')-бензилпиперидин-1-ил]бутил}индол-5-карбоновой кислоты;
и) метиловый эфир (+)-3-{ 4-[3-(3S')-бензилпиперидин-1-ил] бутил} индол-5-карбоновой кислоты;
к) 3-{4- [3-(3R')-бензилпиперидин-1-ил]бутил]-6-метоксииндол;
л) 3- {4- [3-(3S')-бензилпиперидин-1-ил] бутил]-6-метоксииндол;
м) (+)-3-[4-(3-бензилпиперидин-1-ил) бутил]индол;
н) (-)-3-[4-(3-бензилпиперидин-1-ил)бутил]индол;
о) 3- [4-(3-бензилпиперидин-1-ил)бутил]-5-хлориндол;
п) 3- [4-(3-бензилпиперидин-1-ил)бутил]-5-метоксииндол;
р) 3- [4- [3-(4-фторбензил) пиперидин-1-ил]бутил]-5-фториндол;
с) 7-{4-[(3R)-3-бензилпиперидин-1-ил]бутил]-5Н-1,3-диоксоло[4,5-
f] индол;
т) 7- {4-[(35)-3-бензилпиперидин-1-ил]бутил]-5Н-1,3-диоксоло[4,5- индол;
у) 3- [4-[(3R)-3-бензилпиперидин-1-ил]бутил] -5-фториндол;
ф) 3- {4- [(3S)-3-бензилпиперидин-1-ил]бутил]-5-фториндол;
х) 3-{4-[(3R)-3-бензилпиперидин-1-ил]бутил}индол-5-карбонитрил;
ц) 3-{4-[(3S)-3-бензилпиперидин-1-ил]бутил}индол-5-карбонитрил;
ч) 3- [4- [3-(4-фторфенилгидроксиметил)пиперидин-1-ил] бутил] индол-5-карбонитрил;
а также их соли и сольваты.
Соединения (г), (д) и (е) служат промежуточными продуктами.
Касательно всех остатков, присутствующих в соединениях, как например, А, следует указать, что их значения не зависят друг от друга.
Сольваты представляют собой, например, полу-, моно- либо дигидраты или, например, продукты присоединения со спиртами.
Остаток А обозначает алкил и имеет 1-10, предпочтительно 1, 2, 3, 4, 5 или 6 и прежде всего 1 или 2 С-атома, поэтому его главным значением является, например, метил, кроме того он обозначает этил, н-пропил, изопропил, н-бутил, втор-бутил либо трет-бутил, а также пентил, 1-, 2- либо 3-метилбутил, 1,1-, 1,2- либо 2,2-диметилпропил, 1-этилпропил, гексил, 1-, 2-, 3- либо 4-метилпентил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- либо 3,3-диметилбутил, 1- либо 2-этилбутил, 1-этил-1-метилпропил, 1-этил-2-метилпропил, 1,1,2- либо 1,2,2-триметилпропил, далее также фторметил, дифторметил, трифторметил, 1,1,1-трихлорэтил или пентафторэтил.
Циклоалкил представляет собой прежде всего, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или 1-адамантил.
ОА представляет собой предпочтительно метокси, а также этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси или трет-бутокси. NHA представляет собой предпочтительно метиламино, далее этиламино, изопропиламино, н-бутиламино, изобутиламино, втор-бутиламино или трет-бутиламино. NA2 обозначает предпочтительно диметиламино, далее N-этил-N-метиламино, диэтиламино, ди-н-пропиламино, диизопропиламино или ди-н-бутиламино. Исходя из этого, CO-NHA обозначает предпочтительно N-метилкарбамоил или N-этилкарбамоил; a CO-NA2 обозначает предпочтительно N,N-диметилкарбамоил или N,N-диэтилкарбамоил.
Hal обозначает фтор, хлор, бром или иод, прежде всего фтор или хлор, k обозначает 0 или 1, предпочтительно 0. Если k обозначает 1, то имеются в виду промежуточные продукты для синтеза собственно активных веществ.
m обозначает 1, 2, 3 или 4, прежде всего 3 или 4.
Остаток R1 представляет собой предпочтительно незамещенный либо одно- или двукратно замещенный, но прежде всего однократно замещенный группой Hal, CN, А, АО, ОН, CONH2, CONHA, CONA2, СООН и/или СООА 2- либо 3-индолил, а также 5Н-1,3-диоксоло[4,5-П-7-индолил, который также может быть незамещенным, одно- или двукратно замещенным группой Hal, CN, А, АО или ОН, но прежде всего этот остаток является незамещенным. Предпочтительными значениями R1 являются поэтому следующие: 2- либо 3-индолил, 5- либо 6-метилиндол-2-ил, 5- либо 6-метилиндол-3-ил, 5- либо 6-метоксииндол-2-ил, 5- либо 6-метоксииндол-3-ил, 5- либо 6-гидроксииндол-2-ил, 5- либо 6-гидроксииндол-3-ил, 5- либо 6-фториндол-2-ил, 5- либо 6-фториндол-3-ил, 5- либо 6-цианиндол-2-ил, 5- либо 6-цианиндол-3-ил, 5- либо 6-хлориндол-2-ил, 5- либо 6-хлориндол-3-ил, 5- либо 6-карбоксииндол-2-ил, 5- либо 6-карбоксииндол-3-ил, 5- либо 6-метоксикарбонилиндол-2-ил, 5- либо 6-метоксикарбонилиндол-3-ил, 5Н-1,3-диоксоло[4,5-f] индол-7-ил, далее 5-либо 6-броминдол-2-ил, 5- либо 6-броминдол-3-ил, 5- либо 6-этилиндол-2-ил, 5- либо 6-этилиндол-3-ил, 5- либо 6-трифторметилиндол-2-ил, 5- либо 6-трифторметилиндол-3-ил, 5- либо 6-изопропилиндол-2-ил, 5- либо 6-изопропилиндол-3-ил, 5- либо 6-диметиламиноиндол-3-ил или 5- либо 6-диметиламиноиндол-2-ил, 5- либо 6-этоксииндол-3-ил или 5- либо 6-этоксииндол-2-ил.
Остаток R2 представляет собой предпочтительно незамещенный либо одно-, дву- или трехкратно замещенный группой Hal, ОН, ОА, A, NH2, NHA, NA2, CONH2, CONHA, CONA2, СООН, COA, CF3, CN, OSO2A, OSO2CF3 и/или NO2 бензил или фенилгидроксиметил. В соответствии с этим R2 обозначает прежде всего предпочтительно бензил, фенилгидроксиметил и однократно замещенный группой Hal бензил или фенилгидроксиметил, т. е., например, п-фторбензил или п-фторфенилгидроксиметил, п-метилбензил или п-метилфенилгидроксиметил, п-хлорбензил или п-хлорфенилгидроксиметил. Предпочтительными значениями R2 являются далее п-аминобензил, п-метиламинобензил, п-диметиламинобензил, п-этиламинобензил, п-цианобензил, м-фторбензил, м-метилбензил или м-метилфенилгидроксиметил, п-нитробензил или п-нитрофенилгидроксиметил.
Для изобретения в целом справедливо, что все остатки, которые могут неоднократно присутствовать в молекуле, могут иметь идентичные либо разные значения, т.е. независимо друг от друга.
В соответствии с этим объектом изобретения являются прежде всего такие соединения формулы I, в которых по меньшей мере один из названных остатков имеет одно из вышеуказанных предпочтительных значений. Некоторые предпочтительные группы соединений могут быть представлены нижеследующими формулами la-Ik, подпадающими под формулу I и где не расшифрованные более подробно остатки имеют то же значение, что и в формуле I, однако имеются и определенные отличия, а именно:
в 1а R1 обозначает незамещенный 3-индолил;
в Ib R1 в положении 5 обозначает замещенный 3-индолил;
в 1с к обозначает 0, a m обозначает 4;
в Id к обозначает 1, а m обозначает 3;
в Ie R1 имеет значение, указанное в Ib, а заместителем является Hal, и обозначает также метоксикарбонил, CN или карбоксигруппу;
в If R1 обозначает 5Н-1,3-диоксоло[4,5-г]индол-7-ил;
в Ig R2 обозначает незамещенный бензил;
в Ih R2 имеет значение, указанное в Ig, но бензильное кольцо при этом является однократно замещенным;
в Ii R2 имеет значение, указанное в Ih, а заместителем является Hal;
в Ij R2 представляет собой незамещенный либо однократно замещенный фенилгидроксиметил;
в Ik R2 имеет значение, указанное в Ij, а заместителем является Hal.
Объектом изобретения является далее способ получения соединений формулы I, а также их солей и сольватов. Способ отличается тем, что соединение формулы II
в которой R2 имеет указанное выше значение, подвергают взаимодействию с соединением формулы III
R1-(CH2)m-(CO)k-L (III)
в которой L обозначает С1, Вr, I, ОН, ОСОА, OCOPh, OSO2A, OSO2Ar, где Ar представляет собой фенил либо толил и А обозначает алкил, или какую-либо другую реакционноспособно этерифицированную ОН-группу, или легко нуклеофильно замещаемую уходящую группу, а R1, m и k имеют значения, указанные в п.1 формулы, или путем восстановительного аминирования соединение формулы IV
R1-(CH2)m-1-CHO (IV)
в которой R1 и m имеют значения, указанные в п.1 формулы, подвергают взаимодействию с соединением формулы II, или что какое-либо соединение, подпадающее под формулу I, но содержащее вместо одного или нескольких атомов водорода одну или несколько восстанавливаемых групп, таких как С=O, и/или одну или несколько дополнительных С-С- и/или C-N-связей, обрабатывают восстановителем, или что какое-либо соединение, подпадающее под формулу I, но содержащее вместо одного или нескольких атомов водорода одну или несколько сольволизуемых групп, обрабатывают средством сольволиза, и/или что при определенных условиях остаток R1 и/или R2 превращают в другой остаток R1 и/или R2, например, путем расщепления ОА-группы с образованием ОН-группы и/или путем дериватизации CN-, СООН-, СООА-группы и/или путем алкилирования, например, первичного либо вторичного N-атома, и/или путем превращения полученных основания либо кислоты формулы I за счет обработки кислотой либо основанием в одну из их солей.
Процесс получения соединений формулы I осуществляют в принципе по известным методам, описанным в литературе ((например, в основополагающих публикациях, таких как Houben-Weyl, Methoden der Organischen Chemie, изд-во Georg Thieme Verlag, Штутгарт; Organic Reactions, изд-во John Wiley & Sons, Inc. , Нью-Йорк; DE-OS 4101686), а именно, при соблюдении условий, известных и пригодных для проведения вышеуказанных обменных реакций. При этом можно использовать и такие варианты, которые в настоящем описании не упомянуты более подробно.
Исходные вещества, требуемые для осуществления предлагаемого способа, при необходимости можно получить также in situ, а именно не выделяя их из реакционной смеси, а непосредственно используя для последующего превращения в соединения формулы I.
Соединения формулы I предпочтительно получают взаимодействием соединений формулы II с соединениями формулы III. Исходные вещества формул II и III, как правило, известны; не известные же соединения формул II и III могут быть легко получены аналогично известным соединениям.
Производные пиперидина формулы II большей частью известны. Если же их нельзя приобрести коммерческим путем или если они не известны, то их можно получить с помощью известных методов.
Производные индола формулы III в основном известны и частично также являются коммерчески доступными продуктами. Кроме того, эти соединения можно получить из известных соединений путем электрофильного, а в определенных случаях также путем нуклеофильного ароматического замещения. В качестве исходной субстанции используют предпочтительно соответствующую индол-3-алкановую кислоту (получаемую аналогично синтезу индола по Фишеру (тип Яппа-Клингеманна), ср. Böttcher и др., Journ. Med. Chem. 1992, 35, стр. 4020-4026 или Iyer и др., Journ. Chem. Soc. Perkin Trans. II 1973, стр. 872-878). Кислотную группу затем за счет введения реакционноспособной уходящей группы L, необязательно после предварительного восстановления кислотной группы по известным методам, например, с помощью гидрида литийалюминия в тетрагидрофуране, до ОН-группы, подготавливают для взаимодействия с производным пиперидина.
Взаимодействие соединений формул II и III осуществляют по известным из литературы методам, используемым для алкилирования, соответственно ацилирования аминов. Компоненты можно расплавлять совместно в отсутствие растворителя, при определенных условиях в трубке либо в автоклаве. Но можно также превращать соединения в присутствии нейтрального растворителя. В качестве растворителей пригодны среди прочих, например, углеводороды, такие как бензол, толуол, ксилол; кетоны, такие как ацетон, бутанон; спирты, такие как метанол, этанол, изопропанол, н-бутанол; простые эфиры, такие как тетрагидрофуран (ТГФ) или диоксан; амиды, такие как диметилформамид (ДМФ) или N-метилпирролидон (N-МП); нитрилы, такие как ацетонитрил, при определенных условиях можно использовать также смеси этих растворителей между собой либо смеси с водой. Целесообразным может оказаться добавление связывающего кислоту агента, например гидроксида, карбоната либо бикарбоната щелочного или щелочно-земельного металла или же какой-либо другой соли слабой кислоты щелочных или щелочно-земельных металлов, предпочтительно калия, натрия или кальция, или добавление органического основания, такого, как триэтиламин, диметиланилин, пиридин либо хинолин, или же добавление избыточного количества производного пиперидина формулы II. Продолжительность реакции в зависимости от условий ее проведения составляет от нескольких минут до 14 дней, а температура реакции находится в интервале от приблизительно 0 до 150, обычно от 20 до 130oС.
При определенных условиях до осуществления этой реакции необходимо перед процессом алкилирования или ацилирования защищать другие содержащиеся аминогруппы, вводя соответствующие защитные группы. Понятие "аминозащитные группы" общеизвестно и относится к группам, способным защищать аминогруппу от химических превращений, но легко удаляемым по завершении требуемой химической реакции в другом месте молекулы. Поскольку такие защитные группы, равно как и методика их введения и отщепления, в принципе известны специалисту в данной области техники из многочисленных литературных источников и учебников, необходимость в более подробных пояснениях отпадает.
Соединения формулы I могут быть получены далее путем восстановительного аминирования соединений формулы IV соединениями формулы II. Исходные вещества формул IV и II частично известны. Если же они не известны, их можно получить с помощью известных методов. Восстановительное аминирование можно осуществлять в присутствии восстановителей, таких например, как NaBH3CN и NаВН(ОАс)3.
Еще одна возможность получения соединения формулы I состоит в том, что форпродукт, который вместо атомов водорода содержит одну либо несколько восстанавливаемых групп и/или одну либо несколько дополнительных С-С- и/или C-N-связей, обрабатывают восстановителем, предпочтительно при температурах в интервале от -80 до +250oС в присутствии по меньшей мере одного инертного растворителя. Восстанавливаемыми (заменяемыми на водород) группами являются в первую очередь кислород в карбонильной группе, гидроксил, арилсульфонилокси (например, п-толуолсульфонилокси), N-бензолсульфонил, N-бензил либо О-бензил.
В принципе соединения, которые содержат только одну либо две или более вышеуказанных групп, соответственно дополнительных связей, можно переводить путем восстановления в соединение формулы I; при этом одновременно могут восстанавливаться заместители в группе I, содержащиеся в исходном соединении. Предпочтительно использовать в этих целях выделяющийся водород или комплексные гидриды металлов, кроме того можно проводить восстановление по Вольфу-Кишнеру, а также с помощью газообразного водорода при катализе переходными металлами.
Если в качестве восстановителя предусматривается использовать выделяющийся водород, то последний можно образовать, например, за счет обработки металлов слабыми кислотами или основаниями. Так, например, можно использовать смесь цинка с едким щелоком или железа с уксусной кислотой. Приемлемы для использования также натрий или какой-либо другой щелочной металл, растворенные в спирте, таком как этанол, изопропанол, бутанол, амиловый либо изоамиловый спирт или фенол. Кроме того, может использоваться сплав алюминия с никелем в щелочно-водном растворе, необязательно с добавками этанола. Для образования выделяющегося водорода пригодна также амальгама натрия или алюминия в водноспиртовом либо в водном растворе. Реакцию можно проводить также в гетерогенной фазе, при этом целесообразно использовать водную и бензольную либо толуоловую фазу.
Наряду с указанными особенно предпочтительно использовать в качестве восстановителей комплексные гидриды металлов, такие как LiAlH4, NaBH4, гидрид диизобутилалюминия или NaAl(OCH2CH2OCH3)2H2, а также диборан, при необходимости с добавлением катализаторов, таких как BF3, АlСl3 или LiBr. В качестве растворителей пригодными в указанных целях являются прежде всего простые эфиры, в частности диэтиловый эфир, ди-н-бутиловый эфир, ТГФ, диоксан, диглимы или 1,2-диметоксиэтан, а также углеводороды, в частности бензол. При восстановлении с помощью NaBH4 предпочтительны в качестве растворителей в первую очередь спирты, такие как метанол или этанол, далее вода, а также водные растворы спиртов. Восстановление по этим методам проводят предпочтительно при температурах в интервале от -80 до +150, прежде всего от приблизительно 0 до приблизительно 100oС. Особенно предпочтительно способны восстанавливаться -СО-группы в амидах кислоты до СН2-групп с помощью LiAlH4 в ТГФ при температурах в интервале от приблизительно 0 до 66oС.
Другая возможность заключается в том, чтобы одну или несколько карбонильных групп восстанавливать по методу Вольфа-Кишнера до СН2-групп, например, путем обработки безводным гидразином в абсолютном этаноле под давлением при температурах в интервале от 150 до 250oС. В качестве катализатора предпочтительно использовать алкоголят натрия. Возможен и вариант восстановления по методу Хуанга-Минлона, который заключается в том, что реакцию осуществляют, используя гидрат гидрозина в высококипящем, смешиваемым с водой растворителе, таком как диэтиленгликоль или триэтиленгликоль, в присутствии щелочей, в частности гидроксида натрия. Реакционную смесь кипятят при этом, как правило, в течение примерно 3-4 часов. Затем воду отгоняют и образовавшийся гидразон разлагают при температурах до порядка 200oС. Восстановление по Вольфу-Кишнеру можно проводить и при комнатной температуре в диметилсульфоксиде с помощью гидразина.
Кроме того, некоторые реакции по восстановлению можно осуществлять, используя газообразный Н2 при катализе переходными металлами, такими как никель Ренея или Pd. При такой технологии, например, Cl, Br, I, SH, а в определенных случаях и ОН-группы можно заменять на водород. В равной степени можно нитрогруппы путем каталитического гидрирования с помощью Pd/H2 в метаноле превращать в NH2-группы.
Соединения, подпадающие в принципе под формулу I, но содержащие вместо одного или нескольких Н-атомов одну или несколько сольволизуемых групп, могут подвергаться сольволизу и прежде всего гидролизу с получением в результате соединений формулы I.
Кроме того, одно соединение формулы I по известным методам можно превращать в какое-либо другое соединение формулы I.
Соединения формулы I, в которых R1 обозначает остаток, замещенный CONH2, CONHA или CONA2, могут быть получены путем дериватизации соответствующих замещенных соединений формулы I за счет частичного гидролиза. Другая возможность состоит в том, что цианзамещенные соединения формулы I сначала гидролизуют до кислот, которые затем амидируют первичными либо вторичными аминами. Предпочтительно свободную карбоновую кислоту подвергать взаимодействию с амином в условиях синтеза пептидов. Эту реакцию целесообразно проводить предпочтительно в присутствии агента дегидратации, например карбодиимида, такого как дициклогексилкарбодиимид или N-(3-диметиламинопропил)-N-этилкарбодиимид; в этих целях могут использоваться также ангидрид пропанфосфоновой кислоты (ср. Angew. Chem. 92, 129 (1980)), дифенилфосфорилазид или 2-этокси-N-этоксикарбонил-1,2-дигидрохинолин в инертном растворителе, например в галоидированном углеводороде, таком как дихлорметан, в простом эфире, таком как ТГФ или диоксан, в амиде, таком как ДМФ или диметилацетамид, в нитриле, таком как ацетонитрил, при температурах в интервале от приблизительно -10 до +40, предпочтительно от 0 до 30oС. Но особенно предпочтительно работать в обратной последовательности, т.е. получать нитрилы за счет отщепления воды, исходя из амидов, например с помощью трихлорацетилхлорида /Et3 [см. Synthesis (2), 184 (1985)] или РОСl3 (см. Journ. Org. Chem. 26. 1003 (1961)).
Полученное основание формулы I можно переводить с помощью кислоты в соответствующую кислотно-аддитивную соль. Для осуществления этой реакции пригодны кислоты, образующие физиологически приемлемые соли. Так, в частности, можно использовать неорганические кислоты, например серную кислоту, галогенводородные кислоты, такие как хлористоводородная кислота либо бромистоводородная кислота, фосфорные кислоты, такие как ортофосфорная кислота, азотную кислоту, сульфоаминовую кислоту, а также органические кислоты, конкретно алифатические, алициклические, аралифатические, ароматические или гетероциклические одно- либо многооснбвные карбоновые, сульфо- или серные кислоты, такие как муравьиная кислота, уксусная кислота, пропионовая кислота, пивалиновая кислота, диэтилуксусная кислота, малоновая кислота, янтарная кислота, пимелиновая кислота, фумаровая кислота, малеиновая кислота, молочная кислота, винная кислота, яблочная кислота, бензойная кислота, салициловая кислота, 2-фенилпропионовая кислота, лимонная кислота, глюконовая кислота, аскорбиновая кислота, никотиновая кислота, изоникотиновая кислота, метан- либо этансульфокислота, этандисульфокислота, 2-гидроксиэтансульфокислота, бензолсульфокислота, п-толуолсульфокислота, нафталинмоно- и -дисульфокислоты, лаурилсерная кислота.
Свободные основания формулы I при необходимости могут высвобождаться из их солей за счет обработки сильными основаниями, такими как гидроксид натрия или калия, карбонат натрия или калия, в тех случаях, когда в молекуле отсутствуют другие кислотные группы. В тех же случаях, когда соединения формулы I имеют свободные кислотные группы, за счет обработки основаниями также можно образовывать соли. В качестве таких оснований пригодны гидроксиды щелочных и щелочно-земельных металлов или органические основания в виде первичных, вторичных либо третичных аминов.
Соединения формулы I согласно изобретению благодаря их молекулярной структуре могут быть хиральными и в соответствии с этим могут быть представлены в двух энантиомерных либо в нескольких диастереомерных формах. Поэтому благодаря наличию одного или нескольких хиральных центров они могут быть представлены в рацемической или в оптически активной форме.
Поскольку фармацевтическая эффективность рацематов, соответственно стереоизомеров соединений по изобретению, может быть различной, может оказаться целесообразным применять именно диастереомеры или энантиомеры.
В этих случаях конечный продукт или уже промежуточные продукты с помощью известных специалисту химических или физических операций можно разделять на энантиомерные соединения либо непосредственно применять их как таковые для синтеза.
В случае рацемических аминов из смеси взаимодействием с оптически активным разделяющим агентом можно образовывать диастереомеры. В качестве таких разделяющих агентов пригодны, в частности, оптически активные кислоты, как, например, R- и S-формы винной кислоты, диацетилвинной кислоты, дибензоилвинной кислоты, миндальной кислоты, яблочной кислоты, молочной кислоты, приемлемы и N-защищенные аминокислоты или различные оптически активные камфорсульфоновые кислоты. Предпочтительно также хроматографическое разделение на энантиомеры с помощью оптически активного разделяющего агента (как, например, динитробензоилфенилглицин, триацетат целлюлозы либо другие производные углеводородов или же фиксированные на силикагеле хирально дериватизированные метакрильные полимеры). В качестве элюентов пригодными для указанных целей являются водные либо спиртовые смеси растворителей.
В случае рацемических кислот аналогичным образом могут использоваться оптически активные основания, как, например, R- и S-форма 1-фенилэтиламина, 1-нафтилэтиламина, дигидроабиэтиламина, цинхонина или цинхонидини.
При соблюдении особых условий уже в процессе синтеза возможно также применение соответствующих промежуточных продуктов в виде чистых энантиомеров, полученных по одному из вышеуказанных способов. При этом хиральность сохраняется в ходе проведения последующих стадий синтеза.
Объектом изобретения является далее применение соединений формулы I и их физиологически приемлемых солей для получения фармацевтических композиций, прежде всего нехимическим путем. При этом из них совместно с по меньшей мере одним твердым, жидким и/или полужидким носителем или вспомогательным веществом и необязательно в сочетании с одним либо несколькими другими активными веществами может изготавливаться соответствующая дозированная форма.
Еще одним объектом изобретения являются средства, прежде всего фармацевтические композиции, содержащие в своем составе по меньшей мере одно соединение формулы I и/или одну из его физиологически приемлемых солей. Эти композиции могут применяться в качестве лекарственных средств в медицине и в ветеринарии. В качестве субстанций-носителей в них приемлемы органические или неорганические вещества, пригодные для энтерального (например, орального), парентерального либо местного введения и не вступающие в реакцию с новыми соединениями, например вода, масла растительного происхождения, бензиловые спирты, полиэтиленгликоли, желатин, углеводороды, такие как лактоза или крахмал, стеарат магния, тальк, вазелины. Для энтерального введения могут назначаться прежде всего таблетки, драже, капсулы, сиропы, микстуры, капли или суппозитории, для парентерального введения предназначены растворы, предпочтительно масляные либо водные растворы, далее суспензии, эмульсии или имплантаты, для местного применения могут назначаться мази, кремы или пудра. Новые соединения можно также подвергать лиофилизации и полученные лиофилизаты использовать, например, для изготовления препаратов для инъекций. Указанные композиции можно стерилизовать и/или они могут содержать в своем составе такие вспомогательные вещества, как замасливатели, консерванты, стабилизаторы и/или смачиватели, эмульгаторы, соли для регуляции осмотического давления, буферные субстанции, красители, вкусовые добавки и/или ароматизаторы. При необходимости в их составе можно предусмотреть несколько других активных веществ, например один или несколько витаминов.
Соединения формулы I и их физиологически приемлемые соли могут применяться в терапевтических целях для лечения человека и животных и для борьбы с болезнями. Они пригодны для лечения заболеваний центральной нервной системы, таких как состояния напряженности, депрессии, состояния страха, шизофрения, нарушения функций желудочно-кишечного тракта, тошнота, замедленная дискинезия, паркинсонизм и/или психозы, и для устранения побочных действий при лечении гипертонии (например, α-метилдопамином). Наряду с этим предлагаемые соединения могут найти применение в эндокринологии и гинекологии, например для терапии акромегалии, гипогонадизма, вторичной аминореи, предменструального синдрома, нежелательной пуэрперальной (послеродовой) лактации, кроме того для профилактики и терапии расстройств, связанных с сосудами головного мозга (например, мигреней), прежде всего в гериатрии, подобно некоторым эрготалкалоидам.
Особенно предпочтительно они могут применяться также в качестве терапевтических средств для борьбы с последствиями инсульта (apoplexia cerebri), в частности апоплексического удара и церебральной ишемии и для лечения травм головного мозга и спинного мозга.
Предлагаемые в изобретении субстанции назначают при этом, как правило, аналогично известным препаратам, обладающим подобным действием, предпочтительно в дозировках от порядка 0,1 до 500 мг, прежде всего от 0,2 до 300 мг на одну унифицированную дозу. Суточная доза составляет предпочтительно от порядка 0,001 до 250 мг/кг веса пациента. Однако назначаемая тому или иному пациенту доза зависит от целого ряда факторов, в частности от эффективности применяемого соединения, от возраста пациента, веса тела, общего состояния его здоровья, пола, от особенностей питания, от времени и методики введения препарата, от скорости выделения, комбинации лекарственных средств и степени тяжести соответствующего заболевания, для лечения которого предназначается данная терапия. Предпочтительно оральное введение.
Выше и в последующем все температуры указаны в градусах Цельсия. Под используемым в нижеследующих примерах понятием "обычная переработка" имеются в виду следующие операции: при необходимости добавляют воду, при необходимости в зависимости от структурных особенностей конечного продукта устанавливают рН на значения от 2 до 10, экстрагируют этилацетатом или дихлорметаном, фазы разделяют, органическую фазу сушат над сульфатом натрия, фильтруют, упаривают и очищают посредством хроматографии на силикагеле, разделяя при этом описанные ниже изомеры, и/или путем кристаллизации. Значения Rf определяли с помощью тонкослойной хроматографии на силикагеле. Значения М+ +1 выявляли посредством FAB-масс-спектрометрии (FAB - бомбардировка ускоренными атомами). Указанные значения удельного вращения оптически активных соединений измеряли в каждом случае на растворах свободных оснований.
Пример 1
а) Раствор 4-(5-фториндол-3-ил)бутановой кислоты [получаемой, например, диазотированием соответственно замещенного анилина, конденсацией соли диазония с этиловым эфиром 1-оксоциклогексан-2-карбоновой кислоты по методу Яппа-Клингеманна с получением в результате соответствующей 4-(5-фтор-2-этокси-карбонилиндол-3-ил)бутановой кислоты и последующим омылением и декарбоксилированием этоксикарбонильной группы] в ТГФ подвергают восстановлению с помощью гидрида литийалюминия. После обычной переработки получают 4-(5-фториндол-3-ил)бутанол, который затем взаимодействием с хлорангидридом метансульфокислоты переводят в реакционноспособный 4-(5-фториндол-3-ил)бутиловый эфир метансульфокислоты.
б) Смесь из 2,80 г (0,0098 моля) 4-(5-фториндол-3-ил)бутилового эфира метансульфокислоты, 3,20 г (0,0097 моля) (S)-(+)-(миндальной кислоты/3-бензилпиперидина), 3,80 г (0,0294 моля) этилдиизопропиламина нагревают в 100 мл ацетонитрила в течение приблизительно 96 часов на паровой бане. Затем реакционную смесь фильтруют и концентрируют, остаток растворяют в этилацетате и экстрагируют водой. Органическую фазу перерабатывают и остаток хроматографируют в этилацетате на силикагельной колонке. Фракции концентрируют, остаток растворяют в этилацетате и с помощью НСl в этаноле осаждают гидрохлорид 3- {4-[(38)-3-бензилпиперидин-1-ил]бутил} -5-фториндола, который подвергают дальнейшей переработке, tпл 152,0-153,0oС, α
Аналогичным путем взаимодействием 4-(5-фториндол-3-ил)бутилового эфира метансульфокислоты с (R)-(-)-(3-бензилпиперидин)манделатом получают соответствующий гидрохлорид 3- {4- [(3R)-3-бензилпиперидии-1-ил] бутил] -5-фториндола с tпл 153,0-154,0oС. α
Аналогичным путем получают:
(+)-3-[4-(3-бензилпиперидин-1-ил)бутил] индол, tпл 74-75o, α
(-)-3-[4-(3-бензилпиперидин-1-ил)бутил] индол, tпл 73-74o, α
метиловый эфир (+)-3- {4- [3-(3S')-бензилпиперидин-1-ил]бутил}индол-5-карбоновой кислоты, α
метиловый эфир (-)-3- {4-[3-(3R')-бензилпиперидин-1-ил}бутил]индол-5-карбоновой кислоты, α
3-{ 4-[(3R')-3-бензилпиперидин-1-ил] бутил}-6-метоксииндол, гидрохлорид, tпл 218-221o, α
3-{ 4- [(3S')-3-бензилпиперидин-1-ил}бутил]-6-метоксииндол, гидрохлорид, tпл 217-220o, α
Пример 2
Аналогично примеру 1а) и б), но без добавления предусмотренной на стадии б) миндальной кислоты, исходя из 4-(5-фториндол-3-ил)бутановой кислоты через 4-(5-фториндол-3-ил)бутиловый эфир метансульфокислоты взаимодействием с 3-бензилпиперидином получают 3-[4-(3-бензилпиперидин-1-ил)бутил]-5-фториндол, гидрохлорид, tпл 163-165oС.
Аналогичным путем взаимодействием 4-(индол-3-ил)бутилового эфира метансульфокислоты с 3-бензилпиперидином получают 3-[4-(3-бензилпиперидин-1-ил) бутил] индол, гидрохлорид, tпл 134-136oС;
взаимодействием 4-(5-хлориндол-3-ил)бутилового эфира метансульфокислоты с 3-бензилпиперидином получают 3-[4-(3-бензилпиперидин-1-ил)бутил]-5-хлориндол, малонат, tпл 127-129oC;
взаимодействием 4-(5-фториндол-3-ил)бутилового эфира метансульфокислоты с 3-(4-фторэнзил) пиперидином получают 3-[4-[3-(4-фторбензил)пиперидин-1-ил] бутил}-5-фториндол.
Пример 3
Раствор из эквивалентных количеств 3-бензилпиперидина и 3-(4-хлорбутил)-5-цианиндола (получаемого, например, галоидированием соответствующего спиртового соединения, которое можно получить аналогично примеру 1а) восстановлением из 4-(5-цианиндол-3-ил)бутановой кислоты) в ацетонитриле перемешивают при комнатной температуре в течение приблизительно 6 часов. После обычной переработки и разделения хиральных соединений получают 3- {4- [(3S)-3-бензилпиперидин-3-ил]бутил}-5-цианиндол, α
Аналогичным путем могут быть получены:
7-{ 4-[(3R)-3-бензилпиперидин-1-ил] бутил]-5Н-1,3-диоксоло[4,5-f] индол, Rf 0,4 (в СНСl3: МеОН 95:5);
7- {4-[(3S)-3-бензилпиперидин-1-ил]бутил]-5Н-1,3-диоксоло[4,5-f] индол, Rf 0,4 (в СНСl3: МеОН 95:5).
Пример 4
Эквимолярные количества 3-бензилпиперидина и 4-(5-метоксииндол-3-ил)бутановой кислоты (получение аналогично примеру 1а) подвергают в ТГФ при комнатной температуре взаимодействию между собой, добавляя при этом 2-хлор-1-метилпиридинийиодид. После обычной переработки получают 3-бензил-1-[4-(5-метоксииндол-3-ил)бутаноил] пиперидин.
Аналогичным путем получают:
3-бензил-1-[4-(5-фториндол-3-ил)бутаноил]пиперидин;
3-бензил-1-[4-(5-хлориндол-3-ил)бутаноил]пиперидин;
3-бензил-1-[4-(6-хлориндол-3-ил)бутаноил]пиперидин;
3-бензил-1-[4-(6-фториндол-3-ил)бутаноил]пиперидин;
3-бензил-1-[4-(6-метоксииндол-3-ил) бутаноил]пиперидин;
3-бензил-1-[4-(6-этоксииндол-3-ил)бутаноил]пиперидин;
3-бензил-1-[4-(5-этоксииндол-3-ил) бутаноил]пиперидин;
3-бензил-1-[4-(5-цианиндол-3-ил)бутаноил]пиперидин;
3-бензил-1-[4-(6-цианиндол-3-ил)бутаноил]пиперидин;
3-бензил-1-[4-(5-фториндол-2-ил)бутаноил]пиперидин;
3-бензил-1-[4-(5-хлориндол-2-ил)бутаноил]пиперидин;
3-бензил-1-[4-(6-хлориндол-2-ил)бутаноил]пиперидин;
3-бензил-1-[4-(6-фториндол-2-ил)бутаноил]пиперидин;
3-бензил-1-[4-(6-метоксииндол-2-ил)бутаноил]пиперидин;
3-бензил-1-[4-(6-этоксииндол-2-ил)бутаноил]пиперидин;
3-бензил-1-[4-(5-этоксииндол-2-ил)бутаноил]пиперидин;
3-бензил-1-[4-(5-цианиндол-2-ил)бутаноил]пиперидин;
3-бензил-1-[4-(6-цианиндол-2-ил)бутаноил]пиперидин.
Пример 5
3-бензил-1- [4- (5-метоксииндол-3-ил)бутаноил]пиперидин подвергают в ТГФ взаимодействию с гидридом литийалюминия. После обычной переработки получают 3- [4-(3-бензилпиперидин-1-ил)бутил-5-метоксииндол, гидрохлорид, tпл 222-224oС.
Аналогичным путем могут быть получены:
3- [4-(3-бензилпиперидин-1-ил)бутил]-5-фториндол;
3- [4-(3-бензилпиперидин-1-ил)бутил]-5-хлориндол;
3- [4-(3-бензилпиперидин-1-ил)бутил]-6-хлориндол;
3- [4-(3-бензилпиперидин-1-ил)бутил]-6-фториндол;
3- [4-(3-бензилпиперидин-1-ил)бутил]-6-метоксииндол;
3- [4-(3-бензилпиперидин-1-ил)бутил]-6-этоксииндол;
3- [4-(3-бензилпиперидин-1-ил)бутил]-5-этоксииндол;
3-[4-(3-бензилпиперидин-1-ил)бутил]-5-цианиндол;
3-[4-(3-бензилпиперидин-1-ил)бутил]-6-цианиндол;
2-[4-(3-бензилпиперидин-1-ил)бутил]-5-фториндол;
2-[4-(3-бензилпиперидин-1-ил)бутил]-5-хлориндол;
2-[4-(3-бензилпиперидин-1-ил)бутил]-6-хлориндол;
2-[4-(3-бензилпиперидин-1-ил)бутил]-6-фториндол;
2-[4-(3-бензилпиперидин-1-ил)бутил]-6-метоксииндол;
2-[4-(3-бензилпиперидин-1-ил)бутил]-6-этоксииндол;
2-[4-(3-бензилпиперидин-1-ил)бутил]-5-этоксииндол;
2-[4-(3-бензилпиперидин-1-ил)бутил]-5-цианиндол;
2-[4-(3-бензилпиперидин-1-ил)бутил]-6-цианиндол.
Пример 6
3-[4-(3-бензоилпиперидин-1-ил)бутил] индол взаимодействием в ТГФ с борогидридом натрия подвергают реакции восстановления. После обычной переработки получают 3-[4-(3-фенилгидроксиметилпиперидин-1-ил) бутил] индол, гидрохлорид, tпл 181-183oC.
Аналогичным путем получают:
3-[4-(3-фенилгидроксиметилпиперидин-1-ил)бутил]-5-фториндол;
3-{4-[3-(3R')-фенилгидроксиметилпиперидин-1-ил]бутил]-6-метоксииндол;
3-t4-13-(3S')-фенилгидроксиметилпиперидин-1-ил]бутил]-6-метоксииндол;
3-[4-(3-фенилгидроксиметилпиперидин-1-ил)бутил]-5-хлориндол;
3-[4-(3-фенилгидроксиметилпиперидин-1-ил)бутил]-5-метоксииндол;
3-{4-[3-(4-фторфенилгидроксиметил)пиперидин-1-ил]бутил]-5-фториндол;
3-{4-[(3R)-3-фенилгидроксиметилпиперидин-1-ил]бутил]-5-фториндол;
3-{4-[(3S)-3-фенилгидроксиметилпиперидин-1-ил]бутил}-5-фториндол;
3-{ 4-[(3R)-3-фенилгидроксиметилпиперидин-1-ил] бутил}-индол-5-карбонитрил;
3-{ 4-[(3S)-3-фенилгидроксиметилпиперидин-1-ил] бутил]-индол-5-карбонитрил;
3-{ 4-[3-(4-фторфенилгидроксиметил)пиперидин-1-ил] бутил]-индол-5-карбонитрил, tпл 157-159o.
Пример 7
Смесь из 0,0098 моля 4-(метиловый эфир 5-карбоновой кислоты-индол-3-ил) бутилового эфира метансульфокислоты (получение аналогично примеру 1а) и 0,0097 моля 3-бензилпиперидина нагревают аналогично примеру 16) в ацетонитриле в течение приблизительно 96 часов на паровой бане. Затем реакционную смесь по описанной в указанном примере технологии перерабатывают и очищают. В результате получают метиловый эфир 3-[4-(3-бензилпиперидин-1-ил)бутил]индол-5-карбоновой кислоты, гидрохлорид, tпл 181-183oС.
Аналогичным путем могут быть получены:
метиловый эфир 3-{4-[3-(4-фторбензил)пиперидин-1-ил]бутил]индол-5-карбоновой кислоты;
метиловый эфир 3-{4-13-(4-цианбензил)пиперидин-1-ил]бутил}индол-5-карбоновой кислоты;
метиловый эфир 3-{4-[3-(4-этилбензил)пиперидин-1-ил]бутил}индол-5-карбоновой кислоты;
метиловый эфир 3-{4-[3-(4-метилбензил)пиперидин-1-ил]бутил]индол-5-карбоновой кислоты;
метиловый эфир 3-{4-[3-(4-метоксибензил)пиперидин-1-ил]бутил]индол-5-карбоновой кислоты;
метиловый эфир 3-{4-[3-(4-фторбензил)пиперидин-1-ил]бутил]индол-6-карбоновой кислоты;
метиловый эфир 3-{4-[3-(4-фторбензил)пиперидин-1-ил]бутил}индол-5-карбоновой кислоты;
метиловый эфир 3-[4-(3-бензилпиперидин-1-ил)бутил]индол-6-карбоновой кислоты;
метиловый эфир 3-{4-[3-(4-цианбензил)пиперидин-1-ил]бутил}индол-6-карбоновой кислоты;
метиловый эфир 3-{4-[3-(4-метилбензил)пиперидин-1-ил]бутил}индол-6-карбоновой кислоты.
Пример 8
Смесь из метилового эфира 3-[4-(3-бензилпиперидин-1-ил)бутил]индол -5-карбоновой кислоты и КОН нагревают в этаноле с обратным холодильником. После обычной переработки получают 3-[4-(3-бензилпиперидин-1-ил)бутил]-5-карбоксииндол, гидрат, tпл 144-147oС.
Пример А: Склянки для инъекционных растворов
Раствор из 100 г активного вещества формулы I и 5 г гидрофосфата динатрия в з л дважды дистиллированной воды с помощью 2 н. соляной кислоты устанавливают на рН 6,5, стерильно фильтруют, заполняют склянки, лиофилизуют в стерильных условиях и стерильно укупоривают. В каждой склянке содержится 5 мг активного вещества.
Пример Б: Суппозитории
Смесь из 20 г активного вещества формулы I, 100 г соевого лецитина и 1400 г масла какао расплавляют, разливают в формы и дают застыть. Каждый суппозиторий содержит 20 мг активного вещества.
Пример В: Раствор
Приготавливают раствор из 1 г активного вещества формулы I, 9,38 г NaH2PO4•2H2O, 28,48 г Na2HPO4•12H2O и 0,1 г хлорида бензалкония в 940 мл дважды дистиллированной воды. Затем устанавливают на рН 6,8, доводят до объема 1 л и стерилизуют облучением. Этот раствор может применяться в виде глазных капель.
Пример Г: Мазь
При соблюдении асептических условий приготавливают смесь из 500 мг активного вещества формулы I и 99,5 г вазелина.
Пример Д: Таблетки
Смесь из 1 кг активного вещества формулы I, 4 кг лактозы, 1,2 кг картофельного крахмала, 0,2 кг талька и 0,1 кг стеарата магния таблетируют по обычной технологии, получая таблетки, каждая из которых содержит 10 мг активного вещества.
Пример Е: Драже
Аналогично примеру Д прессуют таблетки, которые затем по обычной технологии покрывают оболочкой из сахарозы, картофельного крахмала, талька, траганта и красителя.
Пример Ж: Капсулы
Из 2 кг активного вещества формулы I по обычной технологии изготавливают капсулы с твердожелатиновым покрытием, каждая из которых содержит 20 мг активного вещества.
Пример З: Ампулы
Раствор из 1 кг активного вещества формулы I в 60 л дважды дистиллированной воды стерильно фильтруют, разливают в ампулы, в стерильных условиях лиофилизуют и стерильно укупоривают. В каждой ампуле содержится 10 м г активного вещества.
ОТЧЕТ О ФАРМАКОЛОГИЧЕСКИХ ИСПЫТАНИЯХ
В отчете о фармакологических испытаниях приведены тестируемые соединения, их температура плавления, значения показателей IС50 или Ki для этих соединений, испытанных в трех различных тестах, а также номер примера, страницы и номера строк (см. русский перевод описания), где эти соединения описаны.
В таблице 1 представлены константы ингибирования для ряда типичных соединений;
значения показателей IC50 или Ki даны в М х литр-1, tпл в oС.

Изобретение относится новым 3-бензилпиперидинам ф-лы (I)
где R1 обозначает незамещенный либо замещенный группами Hal, CN, AO, COOH или СООА 2 - или 3-индолил, 5H-1,3-диоксоло [4,5-f]- индолил, R2 обозначает незамещенный либо замещенный группами А, АО, Hal или CN бензил или фенилгидроксиметил, Hal обозначает F, Cl, Br или J, А обозначает С1-С10 алкил, k обозначает 0 или 1, m обозначает 1, 2, 3 или 4 в форме рацемических смесей или отдельных стереоизомеров, а также их физиологически приемлемым солям и сольватам. Соединения формулы (I) оказывают воздействие на центральную нервную систему, представляют собой высокоэффективные лиганды σ - рецепторов и проявляют сильное ингибирующее действие в отношении обратного захвата 5-НТ. 3 c. и 2 з.п. ф-лы, 1 табл.
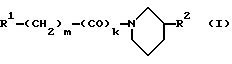
в которой R1 обозначает незамещенный либо замещенный группами Hal, CN, АО, СООН или СООА 2- или 3-индолил, 5Н-1,3-диоксоло[4,5-f] -7-индолил;
R2 обозначает незамещенный либо замещенный группами А, АО, Hal или CN бензил или фенилгидроксиметил;
Hal обозначает F, Cl, Вr или J;
А обозначает алкил с 1-10 С-атомами;
k обозначает 0 или 1;
m обозначает 1, 2, 3 или 4,
в форме рацемических смесей или отдельных стереоизомеров, а также их физиологически приемлемые соли и сольваты.
а) 3-[4-(3-бензилпиперидин-1-ил)бутил] индол;
б) 3-[4-(3-фенилгидроксиметилпиперидин-1-ил)бутил] индол;
в) 3-[4-(3-бензилпиперидин-1-ил)бутил] -5-фториндол;
г) 3-бензил-1-[4-(5-фториндол-з-ил)бутаноил] пиперидин;
д) 3-бензил-1-[4-(5-хлориндол-3-ил)бутаноил] пиперидин;
е) 3-[4-(3-бензилпиперидин-1-ил)бутил] -5-карбоксииндол;
ж) метиловый эфир 3-[4-(3-бензилпиперидин-1-ил)бутил] индол-5-карбоновой кислоты;
з) метиловый эфир (-)-3-{ 4-[3-(3R')-бензилпиперидин-1-ил] бутил} индол-5-карбоновой кислоты;
и) метиловый эфир (+)-3-{ 4-[3-(3S')-бензилпиперидин-1-ил] бутил} индол-5-карбоновой кислоты;
к) 3-{ 4-[3-(3R')-бензилпиперидин-1-ил] бутил} -6-метоксииндол;
л) 3-{ 4-[3-(3S')-бензилпиперидин-1-ил] бутил} -6-метоксииндол;
м) (+)-3-[4-(3-бензилпиперидин-1-ил)бутил] индол;
н) (-)-3-[4-(3-бензилпиперидин-1-ил)бутил] индол;
о) 3-[4-(3-бензилпиперидин-1-ил)бутил] -5-хлориндол;
п) 3-[4-(3-бензилпиперидин-1-ил)бутил] -5-метоксииндол;
р) 3-{ 4-[3-(4-фторбензил)пиперидин-1-ил] бутил} -5-фториндол;
с) 7-{ 4-[(3R)-3-бензилпиперидин-1-ил] бутил} -5Н-1,3-диоксоло[4,5-f] индол;
т) 7-{ 4-[(3S)-3-бензилпиперидин-1-ил] бутил} -5Н-1,3-диоксоло[4,5-f] индол;
у) 3-{ 4-[(3R)-3-бензилпиперидин-1-ил] бутил} -5-фториндол;
ф) 3-{ 4-[(3S)-3-бензилпиперидин-1-ил] бутил} -5-фториндол;
х) 3-{ 4-[(3R)-3-бензилпиперидин-1-ил] бутил} индол-5-карбонитрил;
ц) 3-{ 4-[(3S)-3-бензилпиперидин-1-ил] бутил} индол-5-карбонитрил;
ч) 3-{ 4-[3-(4-фторфенилгидроксиметил)пиперидин-1-ил] бутил} индол-5-карбонитрил,
а также их соли и сольваты.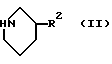
в которой R имеет значение, указанное в п. 1, подвергают взаимодействию с соединением формулы III
R1-(CH2)m-(CO)k-L, (III)
в которой L обозначает Cl, Вr, I, ОН, ОСОА, OCOPh, OSO2A, OSO2Ar, где Ar представляет собой фенил либо толил и А обозначает алкил, или какую-либо другую реакционноспособную этерифицированную ОН-группу или легко нуклеофильно замещаемую уходящую группу, a R1, m и k имеют значения, указанные в п. 1,
и при необходимости полученное соединение формулы I, содержащее вместо одного или нескольких атомов водорода одну или несколько восстанавливаемых групп, обрабатывают восстановителем, с получением соединения формулы I, содержащего один или несколько атомов водорода; и/или остаток R1 и/или R2 в полученном соединении формулы I превращают в другой остаток R1 и/или R2 путем расщепления ОА-группы с образованием ОН-группы, и/или полученное соединение формулы I переводят в одну из его солей путем обработки кислотой либо основанием.
| Резистивный материал | 1974 |
|
SU518805A1 |
| US 5116846 А, 25.05.1992 | |||
| US 4251538 А, 17.02.1981 | |||
| Экономайзер | 0 |
|
SU94A1 |
| RU 94019972 А1, 20.12.1995. | |||
Авторы
Даты
2002-12-10—Публикация
1998-06-08—Подача