Изобретение относится к детской офтальмологии и предназначено для хирургического лечения врожденной глаукомы у детей.
Врожденная глаукома (ВГ) - группа тяжелых инвалидизирующих заболеваний детского возраста, в основе которых лежит наличие структурных аномалий угла передней камеры (УПК) врожденного, и как правило наследственного, характера. Наличие препятствия оттоку внутриглазной жидкости (ВГЖ) приводит к повышению внутриглазного давления (ВГД) и, при несвоевременно начатом лечении, к необратимым глаукоматозным изменениям нейрорецепторного аппарата глаза.
Учитывая органический характер препятствия оттоку ВГЖ, лечение врожденных глауком хирургическое; медикаментозное лечение имеет только вспомогательное значение. Цель операции при врожденной глаукоме - устранение препятствия и/или создание новых путей оттока ВГЖ. В настоящее время большинство офтальмологов мира считают трабекулэктомию (ТЭ) и ее модификации наиболее эффективным, безопасным и универсальным методом лечения всех форм глауком детского возраста (Хватова А.В., Арестова Н.Н. Двадцатилетний опыт лечения врожденной глаукомы у детей. // Актуальные вопросы детской офтальмологии.: Матер, науч. - практ. конф. МНИИ ГБ им.Гельмгольца. - М., 1997. - С.61-64; Fulcher Т. et al. Long-term follow up of primary trabeculectomy for infantile glaucoma. // Br-J-Ophthalmol. 1996 Jun; 80(6): 499-502; Khaw PT. What is the best primary surgical treatment for the infantile glaucomas? // Br-J-Ophthalmol. 1996 Jun; 80(6): 495-6).
Однако несмотря на то, что данный метод обеспечивает непосредственный гипотензивный эффект практически в 100% первичных операций, лишь около половины из них сохраняют свою эффективность в сроки более 6 мес - 2 лет. Причиной нестойкости гипотензивного эффекта операций ТЭ считается рубцовая облитерация созданных путей оттока внутриглазной жидкости (Сидоров Э.Г. и др. // Врожденная глаукома и ее лечение. - М.: Медицина, 1991; Molteno A.C. et al. Surgical technique for advanced juvenile glaucoma. //Arch-Ophthalmol. 1984 Jan; 102(1): 51-7).
До настоящего времени основным методом профилактики избыточного рубцевания после операций ТЭ на глазах детей с врожденной глаукомой является использование медикаментозных антипролиферативных и цитостатических средств - 5-фторурацила (5-ФУ) и митомицина С (ММС) (Полуторнов А.Л. и др. Противорубцовая терапия 5-фторурацилом после антиглаукоматозных операций в молодом возрасте. // Тез. докл. 3 Всеросс. конф. по акт. вопр. детск. офтальмол. - М., 1989. - С. 344-345; Susanna R. Jr. et al. Mitomycin as adjunct chemotherapy with trabeculectomy in congenital and developmental glaucoma. // J Glaucoma 1995: 4: 151-7). Однако применение данных средств сопряжено с повышенным риском таких осложнений, как: расхождение краев конъюнктивального разреза с наружной фильтрацией ВГЖ, выраженная гипотония, вторичные гипотонические дистрофические изменения, кистозное перерождение фильтрационной подушки; возможны также - осложненная катаракта, отслойка сетчатки, эндофтальмит. Данные, полученные разными авторами в отдаленные сроки, свидетельствуют о недостаточно высоком повышении эффективности трабекулэктомии при использовании 5-ФУ и ММС, что при возможности развития вышеперечисленных осложнений ставит под сомнение целесообразность применения 5-ФУ и ММС у детей. Поиск новых путей профилактики избыточного рубцевания с целью повышения эффективности хирургического лечения детей с врожденной глаукомой остается одним из основных направлений современных исследований.
Одним из новых перспективных способов профилактики избыточного рубцевания в хирургии глауком стало использование низкочастотного ультразвука. Использование микрохирургических инструментов, колеблющихся с ультразвуковой частотой 44 кГц и амплитудой 10-15 мкм, обеспечивает легкость и бескровность разрезов (причем коагулирующий и гемостатический эффекты достигаются без термического ожога тканей), а также прямое антипролиферативное действие, что в комплексе значительно снижает травматичность операции, предупреждает избыточное рубцевание в зоне антиглаукоматозного вмешательства, создавая условия для продолжительной компенсации ВГД в послеоперационном периоде (Кодзов М. Б. и др. Применение ультразвуковых инструментов при некоторых офтальмохирургических вмешательствах. // Тезисы докладов III Всероссийского съезда офтальмологов. - М., 1975. - С.272-274).
Одним из известных ультразвуковых способов хирургического лечения открытоугольной (ОУГ) и закрытоугольной (ЗУГ) глауком у взрослых является Ультразвуковая синусотрабекулоэктомия (синоним: Ультразвуковая трабекулэктомия, УТЭ) (Супрун А. В. и др. Применение низкочастотного ультразвука в микрохирургии глаукомы. // Методич. реком. МНИИ ГБ им. Гельмгольца. - М., 1986. - С.7).
Данный способ представляет УЗ-модификацию стандартной микрохирургической трабекулэктомии по Cairns (Cairns J.E. Trabeculectomy: preliminary report of a new method. //Am. J. Ophth. -1968. - vol. 66. - 4. -Р.673-679) с использованием ультразвукового офтальмохирургического аппарата УЗХ-201. Способ УТЭ включает: 1) выделение и отсепаровку склерального лоскута УЗ-круглым ножом УЗН-202 (1 положение ручки регулировки амплитуды = 10-15 мкм); 2) иссечение УЗ-микроскальпелем УЗС-202 блока глубоких слоев склеры 1х4 мм в проекции дренажной зоны (2 положение ручки регулировки амплитуды = 15-20 мкм). Несмотря на наличие разработанных рекомендаций по методике и режимам УЗ-воздействия, операция УТЭ не нашла широкого применения в хирургии глауком у взрослых. Это обусловлено значительной гиперфильтрацией ВГЖ с выраженной гипотонией, наблюдавшейся после УТЭ, что у взрослых больных связано с повышенным риском осложнений - экссудативными отслойками сосудистой и сетчатой оболочек. В сравнении, в хирургии глауком детского возраста такие осложнения чрезвычайно редки. Однако использование УТЭ при врожденной глаукоме у детей в таком виде не представляется возможным, поскольку: 1) способ УТЭ не учитывает чрезвычайную вариабельность физических свойств склеры у детей с врожденной глаукомой, необходимость индивидуального подбора оптимальной амплитуды УЗ-колебаний и недопустимость работы на фиксированных режимах УЗ-колебаний; 2) "озвучивание" внутриглазных структур рассеянным ультразвуком и эффект кавитации, наблюдающийся при контакте рабочего конца УЗ-инструмента с влагой передней камеры, является для детского глаза нежелательным и потенциально травматизирующим фактором, т.к. развивающийся детский глаз значительно более чувствителен к любым повреждающим воздействиям, чем глаз взрослого человека.
Сведения о применении способа ультразвуковой трабекулэктомии (УТЭ) при врожденной глаукоме у детей отсутствуют.
Ближайшим аналогом предлагаемого изобретения является способ лечения врожденной глаукомы у детей - Ультразвуковая склерогониотомия (УСГТ) (Способ лечения врожденной глаукомы у детей, SU 695666, 1975), единственная ультразвуковая антиглаукоматозная операция, применявшаяся до настоящего времени у детей. Способ УСГТ заключается в том, что проводят перфорацию наружной стенки Шлеммова канала и трабекулы ультразвуковым микроскальпелем при частоте колебаний 39-44 кГц и амплитуде 10-15 мкм в виде двух разрезов склеры длиной 2-3 мм по линии проекции задней половины трабекулы. Однако данный метод, несмотря на высокую эффективность (компенсация ВГД в 100% операций в сроки более 6 мес), имеет достаточно узкие показания, являясь ультразвуковым аналогом гониопунктуры по Брошевскому, т.е. паллиативным вмешательством, проводимым только на глазах с терминальными стадиями врожденной глаукомы с органосохранной целью. Применение способа УСГТ у основного контингента детей с начальной и далекозашедшей стадиями врожденной глаукомы невозможно.
Задачей данного изобретения является создание способа хирургического лечения врожденной глаукомы у детей, сочетающего в себе полезные свойства УЗ-операции (атравматичность, качественный гемостаз без ожога тканей, отсутствие необходимости в дополнительном диатермокоагуляционном гемостазе, профилактика избыточного рубцевания, др.) без нежелательного воздействия рассеянным ультразвуком на внутриглазные структуры детского глаза, с микрохирургической техникой операции трабекулэктомии (ТЭ), имеющей наиболее широкие показания в хирургии врожденных глауком.
Техническим результатом предлагаемого изобретения является профилактика избыточного рубцевания с продолжительной компенсацией ВГД.
Технический результат достигается за счет сочетания ультразвуковых приемов выделения и обработки поверхностей склерального лоскута и механического удаления полоски глубоких слоев склеры и трабекулы, а также приемов ушивания поверхностных тканей в зоне вмешательства.
Предлагаемый способ характеризуется следующим:
1) На этапах выкраивания склерального лоскута УЗ-скальпелем и его отсепаровки УЗ-круглым ножом, рабочую, "минимальную эффективную" амплитуду ультразвуковых колебаний инструмента подбирают индивидуально: с постепенным повышением амплитуды от "0" до достижения достаточных эффектов: сначала а) режущего, а затем, с продолжением увеличения амплитуды, б) коагулирующего, - но не превышая амплитуды 15 мкм (2 положение ручки регулировки амплитуды).
В отличие от глаз взрослых больных с глаукомой, физические свойства детской склеры глаз с врожденной глаукомой (плотность, толщина, эластичность, др. ) отличаются чрезвычайной индивидуальностью. Это обусловлено, с одной стороны, возрастными особенностями склеры на различных этапах незавершенного развития; с другой - степенью выраженности вторичных изменений, растяжения и истончения склеры вследствие глаукоматозного процесса. Во избежание серьезных операционных осложнений (перфорация, др.) работа при фиксированной амплитуде УЗ-колебаний недопустима. Подбор оптимальной амплитуды проводят индивидуально, от "0", с постепенным повышением амплитуды до достижения достаточного режущего, а затем коагулирующего, эффекта, но не превышая максимально допустимой для данного типа операции амплитуды (15 мкм).
2) Плоской частью УЗ-круглого ножа проводят выравнивание внутренней поверхности склерального лоскута дополнительным УЗ-воздействием (однократно "проглаживают" 4-мя - 5-ю поперечными движениями всю внутреннюю поверхность склерального лоскута) при амплитуде УЗ-колебаний 10 мкм. Дополнительная УЗ-обработка внутренней поверхности склерального лоскута обеспечивает формирование под ним пространства (внутренней склеральной фистулы) с гладкими стенками, полностью обработанными УЗ-воздействием, что создает благоприятные условия заживления для всех стенок внутренней фистулы с меньшим риском их рубцовой облитерации. В то время как при стандартной микрохирургической ТЭ в течение отсепаровки лоскута на его внутренней поверхности происходит формирование множественных полукружных микробороздок с неровными краями, параллельных направлению движения инструмента), и являющихся субстратом избыточного рубцевания.
3) Полоски глубоких слоев склеры 1х4 мм в зоне проекции Шлеммова канала иссекают исключительно стандартными микрохирургическими инструментами (лезвие - сталь, алмаз, др.), без использования ультразвука.
Выполнение данного этапа операции без использования ультразвука принципиально важно: предупреждается контакт УЗ-инструмента с ВГЖ, что исключает нежелательное "озвучивание" внутренних структур глаза ребенка (цилиарное тело, радужка, хрусталик, эндотелий роговицы) рассеянным ультразвуком, что исключает риск возможных осложнений. Такой подход не снизит общую эффективность УЗ-операции, т.к. в большинстве неуспешных фистулизирующих операций, выполненных стандартными микрохирургическими инструментами, органическое препятствие оттоку ВГЖ локализуется интрасклерально и субконъюнктивально, внутренняя фистула функционально состоятельна, что подтверждается и нашими гониоскопическими данными. Таким образом, обработку внутренней фистулы ультразвуком можно исключить из методики, как необязательный этап УЗ-операции, связанный с нежелательным воздействием рассеянного ультразвука.
4) На этапе наложения конъюнктивальных швов накладывают дополнительные 3-4 узловых шва нижнего этажа - на тенонову капсулу и субконъюнктиву.
В послеоперационном периоде у детей нередко наблюдается расхождение конъюнктивального разреза (как правило, минимальное), вследствие выраженной фильтрации ВГЖ с формированием высокой распространеной фильтрационной подушки (что наиболее характерно для УЗ-операций), беспокойного поведения, других факторов. Наложение дополнительных швов на тенонову капсулу и субконъюнктиву необходимо для обеспечения герметичности фильтрационной подушки с качественной, анатомически правильной поэтажной адаптацией краев конъюнктивального разреза, предупреждения возможных осложнений, связанных с расхождением конъюнктивального разреза (врастание эпителия, наружная фильтрация ВГЖ с выраженной гипотонией, др.).
Способ осуществляется следующим образом:
1. Под общей анестезией проводят обычную подготовку операционного поля. Устанавливают векорасширитель, накладывают уздечный шов-держалку на верхнюю прямую мышцу.
2. Под визуальным биомикроскопическим контролем (операционный микроскоп) проводят разрез конъюнктивы микрохирургическими ножницами в верхне-наружном квадранте в 8 мм от лимба, параллельно ему, протяженностью 10-15 мм; отсепаровывают ("тупым способом", раздвигая бранши ножниц) конъюнктивальный лоскут до зоны проекции лимба. Соблюдают исключительно щадящую тактику по отношению к субконъюнктиве и эписклере (очистку поверхности склерального лоскута скребцом и диатермокоагуляцию сосудов не проводят). При стандартной микрохирургической трабекулэктомии необходимость такой очистки склерального лоскута являлась, в первую очередь, этапом гемостатических мероприятий для предупреждения кровотечения из сосудов эписклеры при формировании склерального лоскута. Однако в настоящее время доказано, что массивное иссечение субконъюнктивы и эписклеры над склеральным лоскутом нежелательно, т.к. ведет к его последующей ишемизации, образованию значительной раневой поверхности, стимулируя формирование грубоволокнистой соединительной ткани в зоне вмешательства и рубцовую облитерацию созданной фильтрационной подушки (Wessels I. F. et al. Avoiding Tenon's capsule. // Ophthalmology. 1998 Jun; 105(6): 942).
Нетермическая УЗ-коагуляция, одновременная с рассечением ткани (см. ниже), обеспечивает качественный гемостаз при пересечении сосудов среднего калибра, не вызывая при этом термического ожога тканей с массированным выбросом медиаторов воспаления из термически разрушенных тканей. Необходимости в дополнительной диатермокоагуляции при выполнении нашей методики нет.
Выполнение данного этапа по предлагаемой методике значительно снизит травматичность операции, сохранит эписклеру, как единственный источник физиологического кровоснабжения склеры, что вместе с прямым антипролиферативным действием низкочастотного ультразвука обеспечит профилактику избыточного рубцевания в зоне вмешательства.
3. Визуально в перилимбальной области производят выбор прямоугольного участка локализации будущего склерального лоскута, размерами 4х5 мм, предпочтительно лишенный крупных сосудов, а также располагающийся вне зон предшествовавших антиглаукоматозных операций (если проводились).
4. С помощью УЗ-микроскальпеля (см. фиг.1 - поз.1) аппарата УЗХ-201 выкраивают П-образный лоскут склеры 4х5 мм (поз.2), основанием к лимбу, на 2/3 толщины склеры. Минимальную эффективную амплитуду УЗ-колебаний подбирают индивидуально: от "0", с постепенным повышением амплитуды (путем поворота ручки регулировки амплитуды УЗ-колебаний аппарата УЗХ-201) до достижения достаточного режущего, а затем коагулирующего, эффекта, но не превышая максимально допустимой для данного типа операции амплитуды (15 мкм).
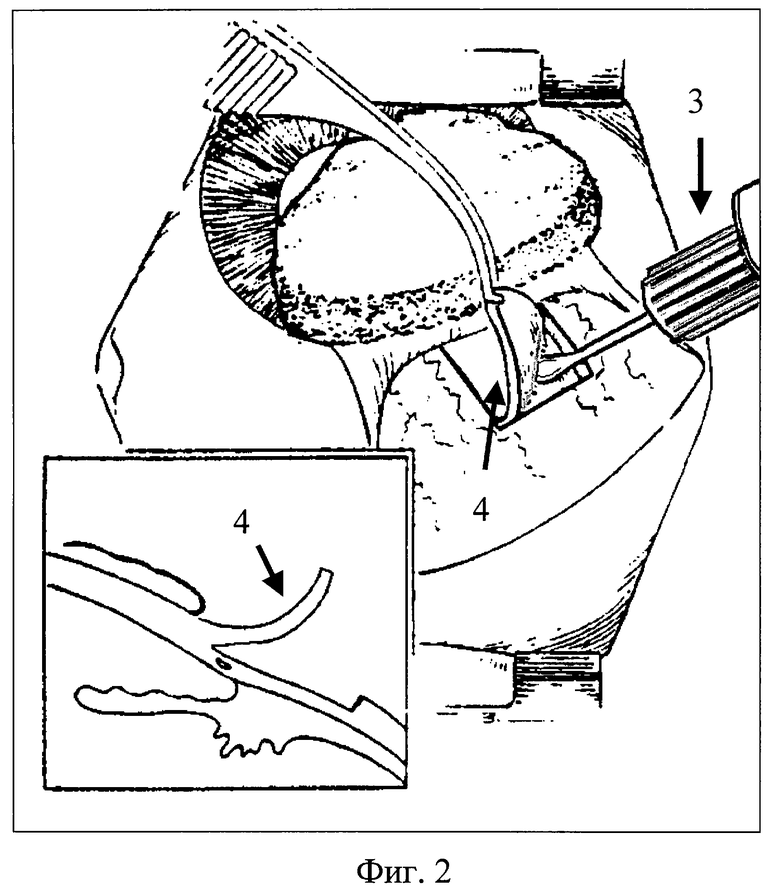
5. УЗ-круглым ножом (см. фиг.2 - поз.3) аппарата УЗХ-201 отсепаровывается склеральный лоскут (поз.4) толщиной приблизительно в 2/3 склеры. Амплитуду УЗ-колебаний подбирают по принципу, описанному выше.
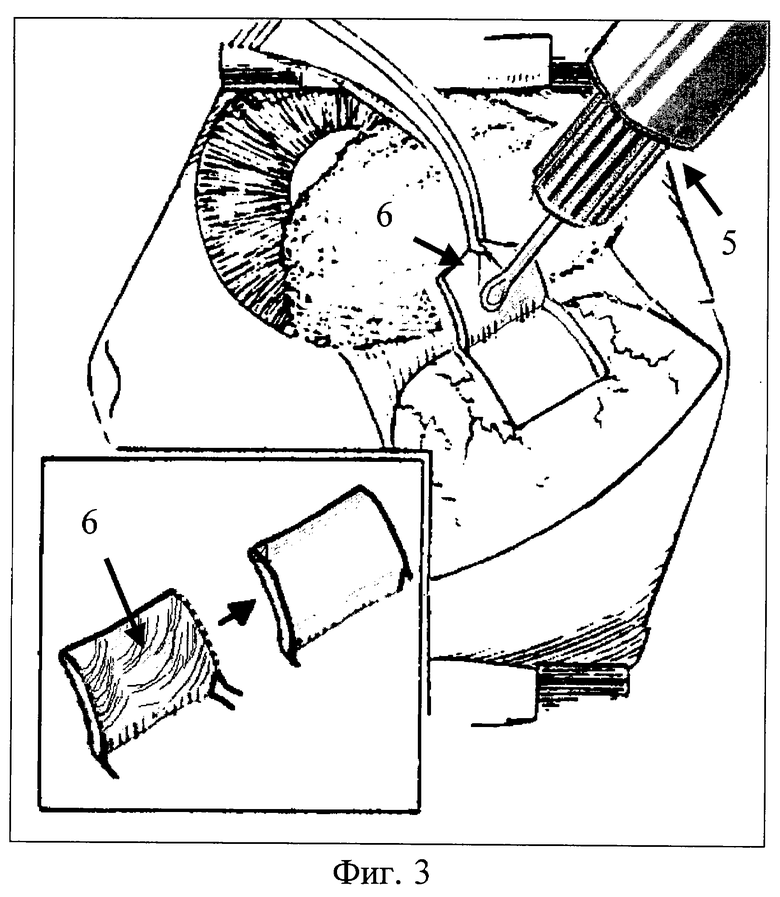
6. Плоской частью УЗ-круглого ножа (см. фиг.3. - поз. 5) проводят выравнивание внутренней поверхности склерального лоскута (поз.6) дополнительным УЗ-воздействием (однократно "проглаживают" 4-мя - 5-ю поперечными движениями всю внутреннюю поверхность склерального лоскута) при амплитуде УЗ-колебаний 10 мкм. При значительном истончении склеры данный этап может не проводиться.
7. Диафаноскопически уточняют локализацию УПК и корнеосклеральной трабекулы. Диафаноскопия проводится путем приложения к роговице стерильного апланационного наконечника световода диафаноскопа при выключенном коаксиальном освещении хирургического микроскопа.
Данный этап исключительно важен при операциях на глазах с врожденной глаукомой, когда зачастую наблюдается значительное растяжение роговицы и лимба, непредсказуемое изменение соотношений структур дренажной зоны.
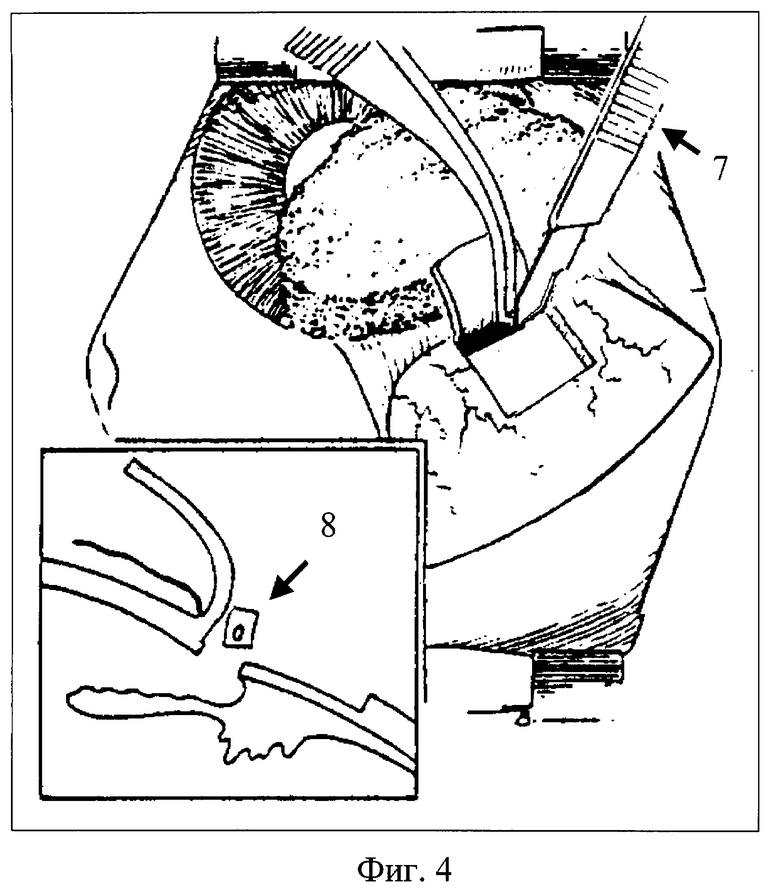
8. Стандартным микрохирургическим лезвием (сапфир, сталь, др.; см. фиг. 4. - поз.7) иссекают полоску глубоких слоев склеры и корнеосклеральной трабекулы 0,5х4 мм (поз. 8). При вставлении радужки в операционный разрез (и/или ее переднем прикреплении) производят базальную иридэктомию микрохирургическими ножницами.
9. П-образный склеральный лоскут репонируют, фиксируют 2 узловыми швами по углам (Викрил, 8-0). При резком сокращении лоскута, что встречается на глазах с терминальными стадиями врожденной глаукомы со значительным растяжением оболочек, целесообразно наложение дополнительных 1-2 узловых швов для достижения равномерного натяжения склерального лоскута.
10. Накладывают швы на разрез конъюнктивы: 3-4 дополнительных узловых шва на нижний этаж - на субконъюнктиву и тенонову капсулу (Викрил, 7-0); непрерывный наружный шов на конъюнктиву (Викрил, синтетика 7-0).
Операцию завершают стандартным путем (вводят раствор Дексазона 0,3 и Гентамицина 0,2 под конъюнктиву; закладывают Альбуцидовую мазь 30% за веки; накладывают бинокулярную стерильную повязку).
Пример 1. Больной А., возраст 5 мес. Диагноз OD: врожденная начальная некомпенсированная глаукома; врожденная колобома радужки и сосудистой оболочки; OS: группа риска по врожденной глаукоме (гониодисгенез 1 ст.). Общие заболевания: ПЭП, с-м мышечной дистонии.
При поступлении: роговица OD вытянутой формы, 12х11 мм (превышает возрастную норму на 1-2 мм), с незначительным отеком и опалесценцией стромы; диаметр роговицы OS соответствует возрасту (10 мм). OD - на 6 ч - полная колобома радужки, зрачок имеет форму "замочной скважины". Хрусталик и ст. тело оптически прозрачны. На глазном дне - обширная колобома сосудистой оболочки, занимающая нижние 2/5 глазного дна, ДЗН в пределах колобомы, бледно-розовый, с сероватым оттенком, границы четкие, с незначительным сдвигом сосудистого пучка в носовую сторону. OS - оптические среды прозрачны, на гл. дне без патологии.
Гониоскопия: OU - высокое прикрепление (на уровне 1/2 трабекулы) радужки. Участки истончения корня радужки, чередующиеся с участками черного пигмента, корень с неоваскуляризацией, напластование эмбриональной полупрозрачной вуалеподобной ткани. Значительной разницы в гониоскопической картине OU не выявлено.
vis OD ≥ 0,05; vis OS ≥ 0,01 (более точно определить по возрасту невозможно; субъективно - вынужденное положение головы, следит за яркими предметами с 25-50 см предпочтительно левым глазом). ВГД OD - 24 мм рт.ст; OS - 19 мм рт. ст. (в наркозе, по Маклакову, на максимальном медикаментозном режиме OD - Пилокарпин 1%х3 р.д., Арутимол 0,25%х2 р.д., Трусопт 2%х2 р.д., Диакарб 0,04 внутрь 1 р.д.).
Топография (ТНЦ-100): OD - Ро=29 мм рт.ст., С=0,15; F=2,8; КВ=196; OD - Ро=47 мм рт.ст., С=0,21; F=2,73; KB=110 (OD - Ро некомпенсировано, умеренная ретенция оттоку ВГЖ).
Эхография. ПЗО/ ПК: OD = 22,8 мм/2,9 мм; OS=20,4 мм/3,8 мм (ПЗО OD превышает размеры парного глаза на 2,4 мм и возрастную норму на 3 мм).
Общая ЭРГ. А/В/бс/кс OD - 50 мкВ/90 мкВ/40 Гц/30 Гц; OS - 50 мкВ/90 мкВ/40 Гц/30 Гц (OD - субнорм. ЭРГ, умерен, патизмен. сетчатки; OS - норма).
Отсутствие компенсации ВГД OD на максимальном возможном гипотензивном режиме при гониоскопически определяемом органическом препятствии оттоку ВГЖ, наличие сочетанной аномалии развития (колобома радужки и сосудистой), патогномоничной одной из форм врожденной глаукомы, и начальных глаукоматозных изменений глаза, - являлись абсолютным показанием к хирургическому антиглаукоматозному лечению OD.
Учитывая достаточно своевременное обращение родителей ребенка за помощью, начальную стадию глаукоматозного процесса OD, наличие начальных анатомических и функциональных глаукоматозных изменений, прогноз по зрению и заболеванию у данного ребенка был расценен как более благоприятный. Прогноз, особенно в данном случае, напрямую зависел от способности фистулизирующей антиглаукоматозной операции обеспечить продолжительную компенсацию ВГД с профилактикой избыточного рубцевания фильтрационной подушки в послеоперационном периоде.
Проведена операция на OD - Комбинированная ультразвуковая трабекулэктомия:
Общая анестезия. На правый глаз установлен векорасширитель, наложен уздечный шов-держалка на верхнюю прямую мышцу. Произведен разрез конъюнктивы микрохирургическими ножницами в верхне- наружном квадранте в 8 мм от лимба, параллельно ему, протяженностью 10 мм; отсепарован тупым способом. Намечен прямоугольный участок склеры 4х5 мм, основанием к лимбу, лишенный крупных сосудов. Очистка эписклеры скребцом не проводилась. УЗ-микроскальпелем аппарата УЗХ-201 выкроен П-образный лоскут склеры 4х5 мм, основанием к лимбу, на 2/3 толщины склеры. Рабочая амплитуда УЗ-колебаний подобрана путем постепенного повышения амплитуды УЗ-колебаний от "0" до появления достаточного режущего и коагулирующего эффекта и составила 8-10 мкм). УЗ-круглым ножом аппарата УЗХ-201 отсепаровыван склеральный лоскут толщиной приблизительно в 2/3 склеры (амплитуда УЗ-колебаний подобрана по описанному выше принципу, составила 10-12 мкм). Отмечена легкость и бескровность разрезов при выделении и отсепаровке склерального лоскута, характерная для УЗ-инструментов. УЗ-коагуляция краев разрезов обеспечила качественный гемостаз, дополнительная диатермокоагуляция не проводилась. Плоской поверхностью УЗ-круглого ножа проведено выравнивание внутренней поверхности склерального лоскута дополнительным УЗ-воздействием (амплитуда УЗ-колебаний 10 мкм). Диафаноскопически уточнена локализация УПК и корнеосклеральной трабекулы. В зоне проекции УПК микрохирургическим лезвием иссечена полоска глубоких слоев склеры и корнеосклеральной трабекулы 0,5х4 мм. Проведенными в ПК микрохирургическими ножницами проведена базальная иридэктомия. П-образный склеральный лоскут репонирован, фиксирован 2 узловыми швами по углам (Викрил, 8-0). На нижний этаж разреза конъюнктивы (тенонова капсула, субконъюнктива) наложены 3 дополнительных узловых шва (Викрил, 7-0); снаружи на конъюнктиву наложен непрерывный шов (синтетика 7-0). С/к инъекция Дексазона 0,3 и Гентамицина 0,2; за веки закладывают Альбуцидовую мазь 30%; наложена бинокулярная стерильная повязка. В течение операции и послеоперационном периоде без осложнений. Отмечена спокойность клинической картины, ареактивность тканей глаза в первые 4 суток после операции (конъюнктива отечна незначительно, нет выраженных отека и гиперемии фильтрационной подушки (ФП) и краев разреза конъюнктивы, желтоватого гемолитического ее оттенка, наблюдающихся при ТЭ с диатермокоагуляционным гемостазом. В день выписки, через 10 дней после операции, наружный конъюнктивальный шов снят; края разреза хорошо адаптированы; формируется толстостенная распространенная, хорошо васкуляризированная ФП; наружной фильтрации ВГЖ нет (флюоресцеиновая проба отрицательная. ВГД OD при выписке - 1 пальп. (без медик. режима).
При контрольном обследовании под наркозом (через 7 мес после операции) обнаружено: OD - спокоен, сформирована распространенная ФП, диаметр роговицы и стабилизирован, отек роговицы отсутствует. Отмечено улучшение зрения OD: vis OD ≥ 0,04; vis OS ≥ 0,04 (более точно определить по возрасту невозможно; нет ранее наблюдавшегося вынужденного положения головы; предпочтительный характер зрения левым глазом не так очевиден).
ВГД OD - 16 мм рт.ст; OS - 19 мм рт.ст. (в наркозе, на медикаментозном режиме OU - Пилокарпин 1%х1 р.д., - профилактически, учитывая гониодисгенез и переднее прикрепление радужки на OU).
Топография (ТНЦ-100): OD - Ро=14,4 мм рт.ст., С=0,37; F= 1,69; КВ=36; OD - Ро= 17,5 мм рт.ст., С-0,27; F=1,97; KB=64.
Эхография. ПЗО/ ПК: OD= 20,9 мм/2,56 мм; OS= 21,2 мм/3,81 мм.
Общая ЭРГ. А/В/бс/кс OD - 60 мкВ/100 мкВ/40 Гц/40 Гц; OS - 70 мкВ/200 мкВ/40 Гц/40 Гц.
Т. о. , по данным исследований через 7 мес после операции отмечена качественная компенсация ВГД оперированного глаза; диаметр роговицы, ПЗО стабилизированы, полностью исчез роговичный синдром, наблюдается некоторое улучшение функций OD, что свидетельствует о компенсации глаукоматозного процесса.
При последнем амбулаторном обследовании ребенка через 1,5 года после операции сохраняется стойкая компенсация ВГД на OD. Хорошее состояние фильтрационной подушки (распространенная, толстостенная, хорошо васкуляризированная) и гониоскопически подтвержденная состоятельность внутренней фистулы свидетельствуют об отсутствии клинических признаков избыточного рубцевания в зоне вмешательства и о принципиальной возможности значительно более продолжительной компенсации ВГЖ с благоприятным прогнозом для данного больного.
Таким образом, предлагаемый способ позволяет добиться более продолжительной компенсации ВГД с профилактикой избыточного рубцевания на глазах детей с врожденной глаукомой за счет сочетания приемов ультразвукового и механического воздействия в зоне операции.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ГЛАУКОМЫ | 1998 |
|
RU2158570C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГЛАУКОМЫ | 2013 |
|
RU2535510C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЛАУКОМЫ | 1998 |
|
RU2161024C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОСТТРАВМАТИЧЕСКОЙ ГЛАУКОМЫ | 1999 |
|
RU2164119C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГЛАУКОМЫ | 2000 |
|
RU2181273C2 |
| СПОСОБ ЛЕЧЕНИЯ ВТОРИЧНОЙ ГЛАУКОМЫ | 1997 |
|
RU2132178C1 |
| СПОСОБ ЛЕЧЕНИЯ ВТОРИЧНОЙ ГЛАУКОМЫ | 1995 |
|
RU2131236C1 |
| Способ лечения врожденной глаукомы | 2022 |
|
RU2790760C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОСЛОЖНЕНИЙ ПОСЛЕ АНТИГЛАУКОМАТОЗНОЙ ОПЕРАЦИИ ПРИ ВРОЖДЕННОЙ ГЛАУКОМЕ | 2003 |
|
RU2242003C1 |
| СПОСОБ ЛЕЧЕНИЯ ВТОРИЧНОЙ ГЛАУКОМЫ | 1999 |
|
RU2164122C2 |
Изобретение относится к офтальмологии и предназначено для лечения врожденной глаукомы у детей. Производят проникающую синусотрабекулэктомию. Поверхностный склеральный лоскут выкраивают и отсепаровывают с помощью УЗ-скальпеля и УЗ-круглого ножа с постепенным повышением амплитуды, достаточной для получения необходимого режущего и коагулирующего эффекта. После отсепаровки лоскута выравнивают внутреннюю поверхность дополнительным УЗ-воздействием. Полоску глубоких слоев склеры и корнеосклеральной трабекулы иссекают лезвием. При ушивании конъюнктивы накладывают дополнительные узловые швы на субконъюнктиву и тенонову капсулу. 4 ил.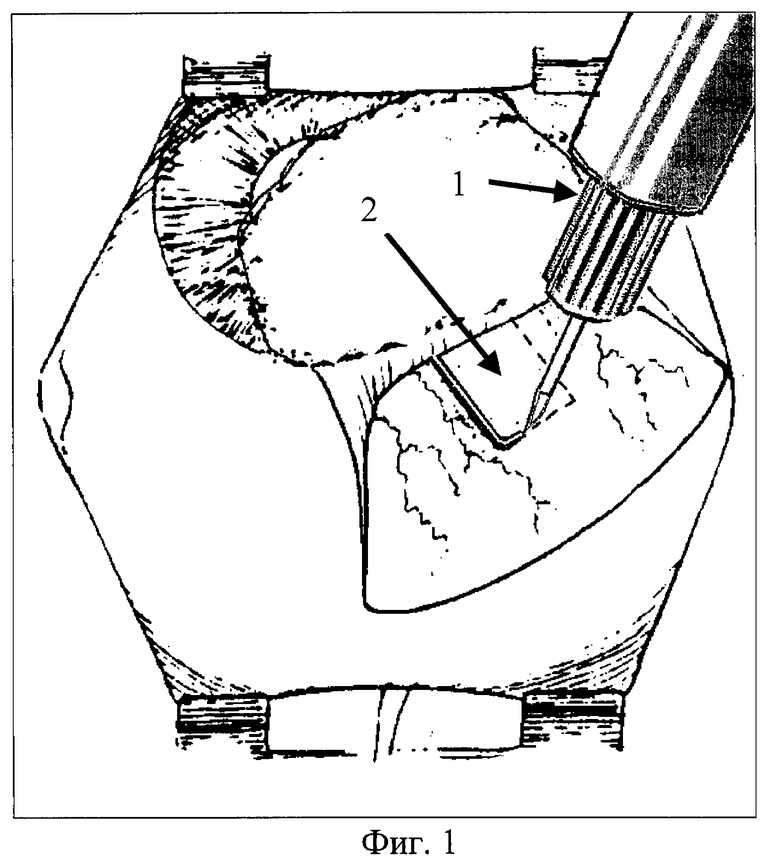
Способ хирургического лечения врожденной глаукомы у детей, включающий ультразвуковое воздействие, отличающийся тем, что производят проникающую синусотрабекулэктомию, при этом поверхностный склеральный лоскут выкраивают и отсепаровывают с помощью УЗ-скальпеля и УЗ-круглого ножа с постепенным повышением амплитуды УЗ-колебаний от 0 до минимальной величины амплитуды, достаточной для получения необходимого режущего и коагулирующего эффекта, после отсепаровки этого лоскута выравнивают его внутреннюю поверхность дополнительным УЗ-воздействием, а полоску глубоких слоев склеры и корнеосклеральной трабекулы иссекают лезвием, при ушивании конъюнктивы накладывают дополнительные узловые швы на субконъюнктиву и тенонову капсулу.
| Способ лечения глаукомы | 1975 |
|
SU695666A1 |
| СПОСОБ ЛЕЧЕНИЯ ВТОРИЧНОЙ ГЛАУКОМЫ | 1997 |
|
RU2132178C1 |
| СПОСОБ ЛЕЧЕНИЯ ВТОРИЧНОЙ ГЛАУКОМЫ У ДЕТЕЙ | 1992 |
|
RU2018289C1 |
| УСТРОЙСТВО ДЛЯ КРИОХИРУРГИИ | 1996 |
|
RU2118514C1 |
| ФРИДМАН Ф.Е | |||
| и др | |||
| Ультразвук в офтальмологии | |||
| - М.: Медицина, 1989, с.156-162. | |||
Авторы
Даты
2003-02-27—Публикация
2000-05-03—Подача