Изобретение относится к медицине, в частности к неврологии, и может быть использовано при лечении больных рассеянным склерозом.
В настоящее время для лечения больных рассеянным склерозом применяют противовоспалительные, сосудистые и общеукрепляющие препараты, а также средства, стимулирующие обменные процессы в организме (Карлов В.А. Терапия нервных болезней. М.: Медицина, 1987, 508 с.).
Все указанные средства могут временно улучшить состояние больного, но не приводят к выздоровлению, так как они не влияют на патогенетические механизмы заболевания.
Учитывая, что рассеянный склероз является заболеванием иммунологически неоднородным и что в его патогенезе часто играют роль аутоиммунные реакции (Матвеева Т.В., Дьяконова И.Н., Гуревич Е.П. Современные теоретические представления об иммунопатологии при рассеянном склерозе // Обзор МРЖ 2, 1985/247/ с. 19-23), современным патогенетическим способом лечения рассеянного склероза являются кортикостероидные гормоны и цитостатические препараты.
Известен способ лечения рассеянного склероза, который заключается в пероральном или внутривенном применении больших доз кортикостероидных гормонов (Гусев Е. И., Демина Т.Л., Бойко А.Н. Рассеянный склероз. М., 1997. 463 с.; Машковский М.Д. Лекарственные средства. М. Медицина. 1993; Рассеянный склероз. Избранные вопросы теории и практики / Под ред. И.А. Завалишина, В.И. Головкина, М., 2000. 639 с.; Хондкариан О.А., Завалишин И.А., Невская О.М. Рассеянный склероз. М. : Медицина, 1987, 245 с.). При среднем весе больного 60-70 кг он вынужден применять 9-10 мг дексаметазона в сутки. При этом способе регресс неврологических симптомов происходит очень медленно (от нескольких недель до нескольких месяцев). Это вынуждает применять длительные курсы лечения (1-1,5 года).
Однако известно, что длительное применение кортикостероидных гормонов в больших дозах вызывает целый ряд серьезных осложнений: снижение функции надпочечников, возникновение гормональной зависимости, артериальной гипертензии, стероидного диабета, образование эрозий и язв на слизистой желудочно-кишечного тракта, возникновение стероидных психозов и т.п. Но самым тяжелым побочным действием кортикостероидный терапии является элиминация предшествеников Т- и В-лимфоцитов, что приводит к усилению уже имеющегося у больных рассеянным склерозом иммунодефицита (Качарова Л.А. Рассеянный склероз: клинико-иммунологические исследования // Диссертация на соискание ученой степени к. м. н. М., 1985). Коррекция этого состояния крайне затруднительна. Кроме того, кортикостероидные гормоны обеспечивают только временный регресс неврологических симптомов, не предотвращают последующих обострений, в некоторых случаях лечение этими препаратами является неэффективным. Поэтому применение такого способа лечения у людей молодого возраста нежелательно.
В последнее время для лечения больных рассеянным склерозом применяют иммуномодуляторы, например бета-интерферон (IFN-beta-1b). Однако лечение рекомбинантными препаратами бета-интерферона является очень дорогим и длительным. Медицинское обслуживание, необходимое пациенту с прогрессирующим рассеянным склерозом, превосходит 35 тысяч долларов США в год (Burt R.K. Immune ablation and hematopotetic stem cell rescne for severe autoimmune diseases (SADS)). Кроме того, частые внутримышечные инъекции препарата (через один день в течение 1-2 лет) создают целый ряд осложнений и неудобств (местные кожные и подкожные инфильтраты, грипп-подобные симптомы с повышением температуры тела, усталость, лейкопения, усиление головной боли и депрессия) - (Huber S., Spycher M., Lechner-Scott J., Bellaiche Y., Steck A.J., Kappos L. Multiple sclerosis: therapu with rekombinant beta-1b interferon = imtial results with 30 muitiple sclerosis patients in northwest Switzerland // Schweiz Med/ Wochenschr. - 1996 Ang.31. - 126 = 35. - 1475-1481, Neilley L. K., Goodiy D.S., Goodkin D.E., Hanser S.L. Side effekt profile of interferon beta-1b in MS: result of an open label trial // Nevrologu. - 1996 Feb. - 46: 2. - p. 552-554). Поэтому, несмотря на снижение частоты обострений заболевания, до 63% пациентов предпочитают прервать курс лечения бета-интерфероном (Neilley L.K., Goodiy D.S., Goodkin D.E., Hanser S.L. Side effekt profile of interferon beta-1b in MS: result of an open label trial // Nevrologu. - 1996 Feb. - 46:2 - p.552-554). Известно также, что введение бета-интерферона повышает секрецию провоспалительного цитокина интерлейкина-6, что вызывает системные побочные эффекты и перекрывает положительный иммуномодулирующий эффект препарата на основе бета-интерферона (Brod S.A., Marshall G.D., Henninger E. M. , Sriram S., Khan M., Wolinsku I.S. Interferon-beta 1b treatment decreases tumor necrosis factor-alpha and increases interlenkin-6 production in multiple sclerosis // Nevrology. - 1996 Iun. - 46:6. - p.1633-1638).
Ранее на кафедре неврологии и нейрохирургии Санкт-Петербургского Государственного медицинского университета им. Акад. И.П. Павлова применялась гемосорбция (Патент РФ 1466675), но гемосорбция может дать серьезные осложнения, как собственно перфузионные, так и связанные с медикаментозным обеспечением процедур. Также на кафедре был разработан новый патогенетический способ лечения больных рассеянным склерозом путем приема гранулированного или волокнистого угольного сорбента в дозе 50-100 мг на 1 кг массы тела пациента три раза в день в двух часовых промежутках между приемами пищи в течение трех-четырех недель. Волокнистый угольный сорбент применяют в чистом виде (Морозова А.А., Барбас И.М., Скоромец А.А. и др.Способ лечения рассеянного склероза. Авторское свидетельство СССР 1680192) или импрегнированный иммуностимуляторами (нукленат натрия, метилурал, витамин В12 (Патент РФ 2016568). Данный способ выбран нами за прототип.
Этот способ был применен, учитывая, что у больных рассеянным склерозом во время обострения обычно имеет место значительный иммунодефицит в периферической крови как со стороны клеточного, так и гуморального иммунитета. Часто стойкий иммунодефицит развивается после курса лечения иммунодепрессантами. Способ энтеросорбции не влечет никаких осложнений и чрезвычайно прост в клинической практике. Применение этого способа позволило сократить срок пребывания пациентов в стационаре на 20-25%, быстро купировать обострение заболевания, улучшение начинается на 3-4 день с начала приема сорбента и прдолжается в течение всего курса лечения, срок ремиссии удлиняется.
Однако прием волокнистого угольного сорбента корригирует содержание Т- и В-лимфоцитов в крови, увеличивая их, но только к концу курса лечения, примерно через 3 недели.
Поэтому требуется разработка нового, более эффективного и быстродействующего способа лечения больных рассеянным склерозом с выраженным иммунодефицитом. У пациентов с рассеянным склерозом, особенно в период обострения заболевания, кроме иммунодефицита продемонстрирован дефицит интерлейкина-2, ключевого противовоспалительного цитокина (Wandinger K.P., Wessel К., etc. Diminished production of tupe-1 interferons and interlenkin-2 in patients with multiple sclerosis // I. Nevrol Sci. - 1997 Iul. - 149 = 1 - p.87-93).
Из опытов in vitro известно, что человеческий интерлейкин-2 (ч-ИЛ-2) является цитокином, который в основном продуцируется Т-лимфоцитами. Его считают веществом, которое играет центральную регуляторную роль в иммунном ответе. В опытах in vitro установлены некоторые его свойства, которые приводят, например, к тому, что ч-ИЛ-2 стимулирует пролиферацию Т-клеток, обуславливает цитоцикличность, усиливает продукцию фактора роста В-клеток, усиливает индукцию рецепторов ч-ИЛ-2 и продукцию гамма-интерферона (Barry G.W. Arnason, etc. Gell-Mediated Immunity and Nevrologie Disease. Diseases of the Nervons System Clinical Nevrobiology. - p.1380-1381 - W.B. Saundges Company. - 1992).
Описано применение ч-ИЛ-2 для усиления антиинфекционной компетентности хозяина. В этом случае ч-ИЛ-2 вводится пациенту с исходно нормально функционирующей иммунной системой для усиления ее борьбы с инфекцией. Все компоненты такой иммунной системы, на которые воздействует при этом ч-ИЛ-2 (в частности лимфоциты), находятся в количестве, характерном для здоровой иммунной системы, и активность их не угнетена. В этом случае ч-ИЛ-2 воздействует непосредственно на рецепторы активных лимфоцитов, что ведет к усилению их активности и пролиферации, а терапевтический эффект достигается тем, что активность иммунной системы еще более стимулируется. (ЕР 0315500)
Известно также применение ч-ИЛ-2 для воздействия на иммунную систему через конкурентное подавление выработки фактора некроза опухолей (ФНО), обнаруживаемого у пациентов, страдающих, в частности, инфекционными болезнями и другими катаболическими нарушениями. При этом у таких пациентов отмечено значительное повышение уровня ФНО, обусловливающее развитие лихорадки и истощение организма, а уровень продукции ИЛ-2 недостаточен для того, чтобы конкурентно подавить выработку этого фактора. Терапевтический эффект обусловлен здесь, в основном, снижением в результате введения ч-ИЛ-2 концентрации в крови ФНО, ответственного за механизм поддержания интоксикации, сопровождающей, в частности, инфекции. (WO 91/14444)
Очевидно, что для медицинских целей целесообразно использовать рекомбинантный ч-ИЛ-2, продуцируемый непатогенными микроорганизмами, клетки которых не содержат эндоксинов типа липополисахаридов. Таковыми являются, например, пекарские дрожжи - сахаромицеты. В частности, представляет интерес дрожжевой рекомбинантный ч-ИЛ-2, получаемый из рекомбинантного штамма дрожжей Saccaharomyces cerevisiae, депонированного во Всероссийской коллекции промышленных микроорганизмов под номером ВКМГ-791.
Задачей, на решение которой направлено данное изобретения, является коррекция содержания Т- и В-лимфоцитов в периферической крови пациентов с рассеянным склерозом в стадии обострения, снижение количества осложнений, вызванных приемом иммунодепресантов, ускорение регресса неврологических симптомов, сокращение сроков лечения больных и увеличение периода ремиссии.
Эта задача решена тем, что больным рассеянным склерозом в стадии обострения заболевания вводят внутривенно, капельно препарат интерлейкина-2 человека (ч-ИЛ-2), например Ронколейкин, в дозе не менее 1 млн. ME.
Согласно п. 2 формулы изобретения препарат ч-ИЛ-2 вводят с интервалом, достаточным для восстановления лейкоцитов.
В доступной литературе нет работ, касающихся применения ч-ИЛ-2 при рассеянном склерозе. Более того, известно, что ч-ИЛ-2 вызывает пролиферацию провоспалительных цитокинов путем активации Т-лимфоцитов. Таким образом, для специалиста явным образом не ясно было о возможности лечения рассеянного склероза ч-ИЛ-2. Результат оказался неожиданным.
Препарат ч-ИЛ-2 вводили больным рассеянным склерозом внутривенно капельно в дозе 1 млн. ME (международных единиц), предварительно растворяя ч-ИЛ-2 в 400 мл изотонического раствора хлорида натрия. Части пациентов препарат вводили 1 раз в 2-3 дня, части - 1 раз в 7 дней.
Наблюдения за больными показали, что при введении препарата с интервалом 1 раз в 7 дней достигается более высокий эффект. Это выражается в быстром регрессе неврологических симптомов, вызванных обострением заболевания, который наступает уже на следующие сутки после введения. Быстро достигается иммунокоррекция Т-лимфоцитов в периферической крови, на 2-3 день уменьшается иммунодефицит Т-клеточного иммунитета. Начавшийся регресс неврологических симптомов продолжается в течение всего курса лечения. Сроки лечения пациентов в стационаре сокращаются на 20-25%. Урежаются рецидивы заболевания (продлевается период ремиссии).
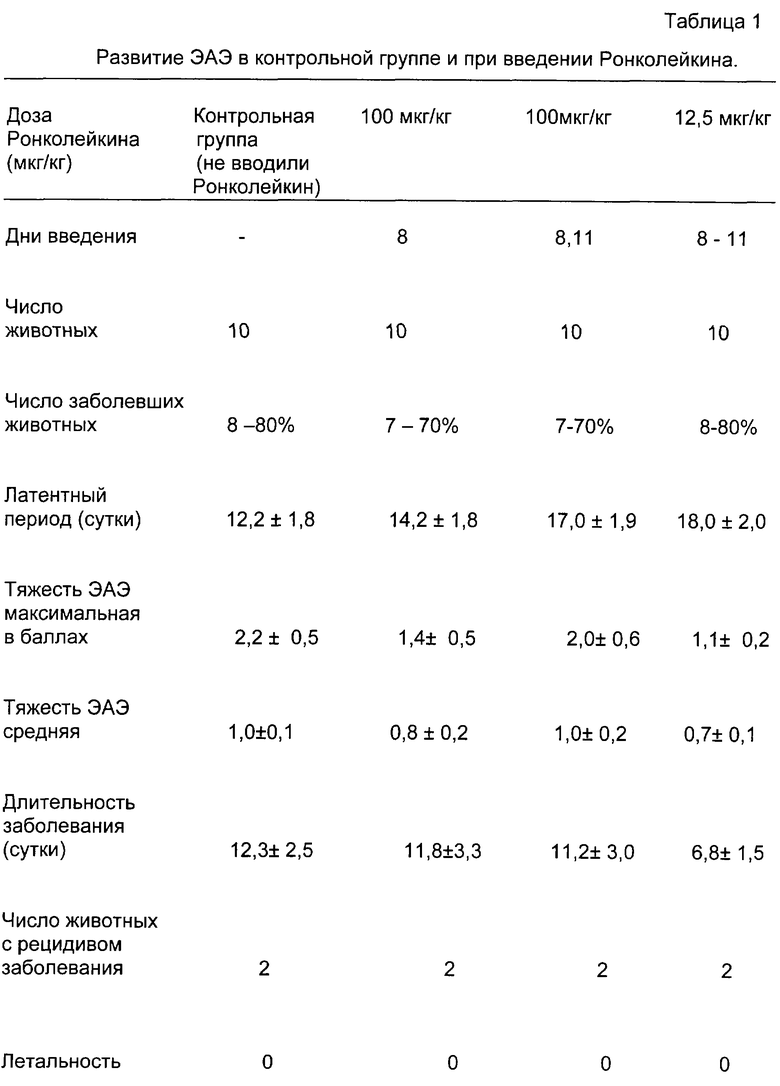
Для изучения влияния Ронколейкина на развитие экспериментального аллергического энцефаломиелита (ЭАЭ) были проведены опыты на 40 крысах самках Spraguc Dawley (SD) массой тела 170-200 г. (см. табл. 1).
Животным однократно подкожно вводили 90 мг гомогената изологичного нативного спинного мозга, смешанного с 0,15 мл изотонического раствора NaCl и эмульгированного в 0,2 мл полного адъюванта Фрейнда. Для своевременного выявления неврологических расстройств ежедневно наблюдали за сенсибилизированными животными: регистрировали время начала заболевания, его продолжительность и тяжесть. Последняя выражалась суммой баллов, соответствующих двигательным нарушениям и мозжечковой атаксии, возникшими у крыс во время заболевания.
Баллы оценивали следующим образом:
0 - отсутствие клинических проявлений ЭАЭ;
0,5 - парез одной лапы или хвоста, гипертонус, незначительный тремор;
1,0 - паралич одной лапы или хвоста, выраженный тремор и т.д.
Суммарный показатель тяжести заболевания был пропорционален тяжести и распространенности симптомов.
Подопытные животные были разделены на 4 группы по 10 крыс в каждой. Животным первой группы (контрольная группа) Ронколейкин не вводили, они получали только физиологический раствор внутрибрюшинно. Животным второй, третьей и четвертой групп вводили Ронколейкин, разведенный в физиологическом растворе также внутрибрюшинно в различных дозах и в разные дни. Ронколейкин или физиологический раствор вводили 1 раз в сутки.
Животные второй группы получали Ронколейкин в дозе 100 мкг/кг массы тела однократно на 8-ой день после сенсибилизации, животным третьей группы вводили Ронколейкин в дозе 100 мкг/кг массы тела двукратно: на 8-ой и 11-ый день, животные четвертой группы получали Ронколейкин в дозе 12,5 мкг/кг массы тела четырехкратно - с 8-ого по 11-ый день.
Результаты опытов.
Клинические признаки заболевания появились у крыс через 9 и более дней от начала сенсибилизации. Как видно из табл. 1, показатель заболеваемости составил 80% в контрольной и четвертой группе животных и 70% во второй и третьей. Продолжительность латентного периода составила 12 суток в контрольной группе и варьировала в сторону увеличения в остальных группах с максимальным показателем у крыс четвертой группы (p<0,05).
Показатели максимальной и средней тяжести оказались меньшими во всех опытных группах по сравнению с контрольной (р<0,05). Особенно это видно у животных четвертой группы, получавших Ронколейкин в дозе 12,5 мкг/кг массы тела с 8-ого по 11-ый день.
Длительность заболевания в этой группе животных снизилась в 1,8 раза и незначительно уменьшилась у крыс второй и третьей групп.
В частоте случаев рецидивов заболевания различий не выявлено. Летальных исходов не было.
Таким образом, в настоящем эксперименте внутрибрюшное введение Ронколейкина не повлекло за собой ухудшения показателей развития и течения ЭАЭ. Более того, назначение Ронколейкина в дозе 12,5 мкг/кг массы тела и ежедневное его введение (с 8-ого по 11-ый день латентного периода) привело к развитию более позднего и коротко текущего заболевания с менее тяжелыми симптомами.
В табл. 1 представлены данные: "Развитие ЭАЭ в контрольной группе и при введении Ронколейкина.
В клинике неврологии и нейрохирургии СПбГМУ им. Академика И. П. Павлова проведена монотерапия Ронколейкином 31-му пациенту в стадии обострения рассеянного склероза в возрасте от 19-ти до 54-х лет. Женщин было 19, мужчин 12. У всех больных при исследовании неврологического статуса отмечался пирамидно-мозжечковый синдром, смешанная стаксия. У большинства пациентов были расстройства чувствительности, зрительных и глазодвигательных нервов и функции тазовых органов. Неврологический статус оценивался по шкале (Sipe et.al. , 1984) (Sipe I. C. , Rnobler R.S., Brahery S.L. et.al. Nevrologie rating Scale (NRS) for use in multiple sclerosis // Nevrology (Clevelend). - 1984. - v.34. - 10. - р.1368 - 1372). Нормальный неврологический статус оценивался 100 баллами. У 5-ти больных был обнаружен лимфоцитарный плеоцитоз в церебро-спинальной жидкости до 40/3, у одного из них было одновременное повышение белка до 0,8 %. После двукратного введения Ронколейкина у 23-х больных (71%) отмечалось значительное уменьшение неврологического дефицита, у пациентов с лимфоцитарным плеоцитозом в церебро-спинальной жидкости, отмечено снижение цитоза до нормы.
По шкале (Sipe et.al., 1984) неврологический статус, определявшийся в среднем 54-мя баллами, возросл до 70-ти баллов.
Высокая эффективность заявляемого способа лечения рассеянного склероза в стадии обострения проиллюстрирована нижеследующими примерами.
Пример 1.
Больная Л. Т. В. , 44 года, находилась в клинике неврологии СПбГМУ им. акад. И.П. Павлова с 18.11.1997 по 11.12.1997 (номер истории болезни 17053).
Жалобы на снижение остроты зрения, затруднение речи, слабость в ногах, шаткость при ходьбе, особенно в темное время суток. Считает себя больной с 1985 года, когда появилось концентрическое сужение полей зрения. Лечилась амбулаторно с улучшением.
В январе 1993 года появилось снижение остроты зрения на оба глаза, чувство онемения кистей с обеих сторон. Получала курс гормонотерапии, после чего зрение восстановилось. В конце января 1997 года после перенесенного гриппа появилась слабость в ногах, шаткость при ходьбе. Проводилось общеукрепляющее лечение без эффекта. В феврале 1997 года вновь появилось снижение остроты зрения на оба глаза, в апреле 1997 года - затруднение речи. Лечилась стационарно гормонотерапией без эффекта.
Неврологический статус при поступлении в клинику: некоторая эйфория, сменяющаяся депрессией. Локальных нарушений корковых функций нет. Гемианопсии нет. Зрачки среднего диаметра без разницы сторон с живой реакцией на свет и аккомодацию. Движение глазных яблок в полном объеме. Горизонтальный нистагм при взгляде в обе стороны. Сглажена левая носогубная складка. Мягкое небо поднимается хорошо, отклонение uvulae влево, глоточный рефлекс вялый. Язык по средней линии, речь несколько скандированная. Объем активных движений в конечностях полный. Мышечная сила снижена в левой кисти, в сгибателях бедра и разгибателях стоп с двух сторон до 3 баллов. Мышечный статус в ногах повышен, глубокие рефлексы высокие S>d. Симптомы Россолимо-Вендеровича, Якобсон-Ласка, Бабинского и Штрюмпеля с двух сторон. Брюшные рефлексы отсутствуют. Левосторонняя гемигипестезия. Вибрационная чувствительность на лодыжках 1-2 с. Интенционный тремор при координаторных пробах, адиадохокинез слева, неустойчива в позе Ромберга, особенно с закрытыми глазами. Походка спастико-атактическая.
По шкале (Sipe et.al., 1984) неврологический статус оценен 38 баллами (при норме 100 баллов).
На глазном дне частичная атрофия зрительных нервов с двух сторон. Анализы крови и мочи в норме. В церебро-спинальной жидкости содержание белка 0.16%, 2/3 лимфоцитов. По данным МРТ головного мозга от 23.04.1997 - демиелинизирующее заболевание нервной системы.
Иммунограмма от 19.11.1997:
CD3 - 44% (норма 60-85%)
CD4 - 31 % (норма 25-55%)
CD8 - 26% (норма 15-35%)
CD4/CD8 - 1.2 (норма 1.7-2.0)
CD16 - 8% (норма 8-20%)
CD25 - 15% (норма 13-24%)
Нейтрофильный фагоцитоз - 80% (норма 20-30%)
Комплемент - 21.56 ед (норма 20.0-23.0 ед CH5O)
Циркулирующие иммунные комплексы - 0.075 (норма 0.06-0.08)
За время пребывания в клинике больная получила две инфузии интерлейкина-2 человека (ч-ИЛ-2) в дозе 1 млн. ME внутривенно капельно, растворенного в 400 мл изотонического раствора хлорида натрия с интервалом в семь дней. Неврологический статус после окончания курса лечения: настроение в норме. Эйфории и депрессии не наблюдалось. Нистагм при взгляде в обе стороны уменьшился. Речь улучшилась: выговаривание слов стало более четким, темп речи возрос. Мышечная сила в ногах наросла до 4 баллов, мышечный тонус в ногах уменьшился. Глубокие рефлексы без разницы сторон, высота их снизилась, симптом Бабинского держится с двух сторон. Вибрационная чувствительность в ногах 3 с. Интенционный тремор при координаторных пробах уменьшился, в позе Ромберга проявляется неустойчивость только с закрытыми глазами. По шкале (Sipe et al., 1984) неврологический статус - 66 баллов.
Иммунограмма от 01.12.1997:
CD3 - 61%
CD4 - 36%
CD8 - 19%
CD4/CD8 - 1.9
CD16 - 22%
CD25 - 19%
Нейтрофильный фагоцитоз - 92%
Комплемент - 17.66 ед
Циркулирующие иммунные комплексы - 0.06
Итак, у больной 44 лет, страдающей рассеянным склерозом с ремиттирующим течением на протяжении 12 лет, после очередного курса гормонотерапии во время последнего обострения не произошло изменения неврологического статуса, неврологический дефицит остался прежним. В то же время до терапии ч-ИЛ-2 имел место иммунодефицит клеточного иммунитета. После курса лечения ч-ИЛ-2 неврологический статус значительно улучшился: с 38 баллов до 66 баллов по шкале (Sipe et al., 1984). Больная стала лучше ходить, значительно улучшилась речь, что имеет большое значение для больной (больная работает адвокатом). Увеличились показатели клеточного иммунитета, нормализовался индекс CD4/CD8. Больная работоспособна.
Пример 2. Более тяжелое течение заболевания.
Больная Х. Т.М. 42 лет, инвалид II группы, находилась в неврологической клинике СПбГМУ им.акад.И.П.Павлова с 26.04.96 по 18.05.1996 (номер истории болезни 10115).
Жалобы на головные боли, головокружение, двоение при взгляде в обе стороны, чувство онемения левой половины лица и тела, слабость ног и шаткость при ходьбе, нарушение функции тазовых органов в виде задержки, частичного недержания мочи и императивных позывов.
Считает себя больной с 1987 года, когда после родов появилось снижение остроты зрения на правый глаз.
Лечилась с применением энтеросорбции волокнистого угольного сорбента, в результате чего острота зрения полностью восстановилась.
Повторное обострение заболевания - в 1992 году, ощущала слабость левых конечностей. Вновь лечилась энтеросорбцией с улучшением. С 1994 года отмечает более частые обострения заболевания - примерно два раза в год. Неоднократно получала курсы лечения стероидными гормонами. Последнее обострение с 19.04.1996.
Неврологический статус при поступлении: депрессия. Локальные корковые функции не нарушены. Зрачки среднего диаметра (d=s), реакция на свет и аккомодацию сохранена. Правое глазное яблоко направлено кнутри, левое - кнаружи. Вправо глазные яблоки ведет только до средней линии, влево - почти до конца. Диплопия при взгляде в обе стороны и вниз. Слабость мышц жевателей с двух сторон, нижнечелюстной рефлекс отсутствует. Лагофталм справа, сглаженность правой носогубной складки. Мягкое небо при фонации поднимается плохо, дисфагия. Девиация языка влево, дизатрия. Объем активных движений снижен в ногах, больше в левой. Мышечная сила снижена в ногах во всех группах мышц, в левой ноге - до двух баллов. Мышечный тонус в руках снижен, в ногах повышен. Глубокие рефлексы высокие S>d. Патологические стопные рефлексы с двух сторон. Левосторонняя гемигипестезия. Вибрационная чувствительность в ногах отсутствует. Пальценосовая проба с мимопопаданием, адиадохокинез с двух сторон. Неустойчива в позе Ромберга. Походка спастико-атактическая. Анализы крови и мочи в норме. Глазное дно: атрофия зрительных нервов с двух сторон. Люмбальная пункция от 06.05.1996: белок 0.33%, цитоз 55/3 (нейтрофилы+лимфоциты). На МРТ головного мозга картина демиелинизирующего процесса.
По шкале (Sipe et al., 1984) неврологический статус оценен 16 баллами.
Иммунограмма от 06.05.1996:
CD3 - 44% (норма 60-85%)
CD4 - 27% (норма 25-55%)
CD8 - 32% (норма 15-35%)
CD4/CD8 - 0.84 (норма 1.7-2.0)
CD16 - 25% (норма 8-20%)
CD25 - 20% (норма 13-24%)
Больная получила 2 инфузии по 1 млн. ME интерлейкина-2 человека внутривенно капельно с семидневным промежутком между инфузиями. После первой инфузии общее состояние улучшилось: уменьшилось двоение, наросла сила в ногах, уменьшилась шаткость при ходьбе.
Неврологический статус на следующий день после введения интерлейкина-2: глазные яблоки в среднем положении, движение их влево в полном объеме, вправо - до средней линии. Диплопия только при взгляде вправо. Значительно наросла сила мышц жевателей, уменьшился парез мимических мышц справа. Язык по средней линии. Дизартрии почти нет. Значительно наросла мышечная сила в ногах: в левой ноге с 2 до 4 баллов. Глубокие рефлексы без четкой разницы сторон, патологических стойких симптомов нет. Улучшилась устойчивость в позе Ромберга и при ходьбе. Тазовые расстройства держатся. По шкале (Sipe et al., 1984) неврологический статус 22 балла.
Иммунограмма от 13.05.1996:
CD3 - 51%
CD4 - 39%
CD8 - 34%
CD4/CD8 - 1.15
CD16 - 37%
CD25 - 33%
Иммунограмма от 26.05.1996 (после второй инфузии ч-ИЛ-2):
CD3 - 49%
CD4 - 22%
CD8 - 23%
CD4/CD8 - 1.8
CD16 - 18%
CD25 - 16%
Неврологический статус к моменту выписки: движение глазных яблок влево в полном объеме, вправо немного не доводит только правое глазное яблоко, диплопия при взгляде вправо значительно меньше. Функция мышц жевателей, мимических мышц в норме. Дисфагии и дизартрии нет. Легкий центральный парез нижних конечностей, гипестезия в пальцах ног, походка значительно улучшилась, уменьшилось расстройство функции тазовых органов. По шкале (Sipe et al., 1984) неврологический статус 63 балла.
Люмбальная пункция от 21.05.1996: белок 0.33%, цитоз 13/3 (лимфоциты).
Итак, у больной, страдающей ремиттирующей формой рассеянного склероза в течение 10 лет, во время очередного обострения обнаруживались нарушения функции III, V, VI, VII, IX, XII пар черепных нервов, нарос нижний спастический парапарез (мышечная сила до 2 баллов слева), увеличилась смешанная атаксия и расстройство функции тазовых органов.
Обострение заболевания подтвердилось смешанным цитозом в церебро-спинальной жидкости 55/3.
Иммунограмма показала снижение Т-лимфоцитов, снижение коэффициента CD4/CD8, повышение CD72 и CD16.
После двукратной инфузии ч-ИЛ-2 с интервалом 7 дней значительно улучшился неврологический статус по шкале (Sipe et.al., 1984) с 16 до 63 баллов (при норме 100 баллов), нормализовалась церебро-спинальная жидкость, уменьшился Т-клеточный иммунодефицит, нормализовался показатель CD4/CD8, CD16 и CD25. Больная выписалась из клиники в удовлетворительном состоянии. В течение последующих 1,5 лет обострений заболевания не было.
Таким образом, лечением ч-ИЛ-2 достигается быстрой регресс неврологических симптомов, вызванных обострением заболевания, который наступает уже на следующие сутки после введения. Быстро достигается иммунокоррекция Т-лимфоцитов в периферической крови, на 2-3 день уменьшается иммунодефицит Т-клеточного иммунитета. Начавшийся регресс неврологических симптомов продолжается в течение всего курса лечения. Сроки лечения пациентов в стационаре сокращаются на 20-25%. Урежаются рецидивы заболевания (продлевается период ремиссии).
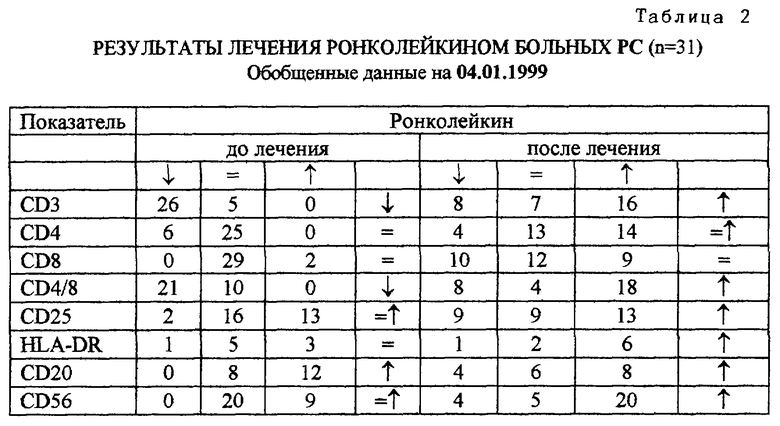
В табл. 2 представлены результаты лечения больных Ронколейкином, где обозначено:
- уменьшение количества иммунных клеток в периферической крови;
- увеличение количества иммунных клеток в периферической крови;
= - нормальное содержание количества иммунных клеток в периферической крови.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ТЕРАПИИ РЕМИТТИРУЮЩЕГО РАССЕЯННОГО СКЛЕРОЗА | 2012 |
|
RU2523058C2 |
| СПОСОБ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА | 1991 |
|
RU2016568C1 |
| Способ лечения рассеянного склероза | 1988 |
|
SU1821214A1 |
| СПОСОБ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА У ДЕТЕЙ | 2015 |
|
RU2596792C1 |
| СПОСОБ ПРОФИЛАКТИКИ РЕЦИДИВА ХРОНИЧЕСКОГО ВИРУСНОГО ГЕПАТИТА С ПОСЛЕ ДОСТИЖЕНИЯ ВИРУСОЛОГИЧЕСКОЙ РЕМИССИИ | 2007 |
|
RU2348412C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ СТАДИИ РАССЕЯННОГО СКЛЕРОЗА С УЧЕТОМ ПОКАЗАТЕЛЕЙ ИММУНОЛОГИЧЕСКОГО СТАТУСА | 2013 |
|
RU2528882C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ РАССЕЯННОГО СКЛЕРОЗА С УЧЕТОМ ИММУНО-МЕТАБОЛИЧЕСКИХ ПОКАЗАТЕЛЕЙ | 2013 |
|
RU2528879C1 |
| ЛЕЧЕНИЕ РАССЕЯННОГО СКЛЕРОЗА ПО МЕТОДУ И.КРИВОПАЛОВА-МОСКВИНА | 2018 |
|
RU2702120C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗАТЯЖНЫХ, РЕЦИДИВИРУЮЩИХ ФОРМ ПСЕВДОТУБЕРКУЛЕЗА И ЕГО СПЕЦИФИЧЕСКИХ ОСЛОЖНЕНИЙ У ДЕТЕЙ | 2000 |
|
RU2189249C2 |
| СПОСОБ ПОЛУЧЕНИЯ КЛЕТОЧНОЙ КУЛЬТУРЫ ДЛЯ ЛЕЧЕНИЯ СОСУДИСТЫХ И ДЕМИЕЛИНИЗИРУЮЩИХ ЗАБОЛЕВАНИЙ НЕРВНОЙ СИСТЕМЫ И КЛЕТОЧНАЯ КУЛЬТУРА, ПОЛУЧЕННАЯ ЭТИМ СПОСОБОМ (ВАРИАНТЫ) | 2007 |
|
RU2347579C1 |
Изобретение относится к медицине, в частности к неврологии, и может быть использовано при лечении больных рассеянным склерозом. Больным в стадии обострения вводят внутривенно капельно препарат интерлейкина-2 человека (ч-ИЛ-2), например Ронколейкин, в дозе не менее 1 млн ME 1 раз в 7 дней. Способ позволяет значительно сократить сроки лечения больных рассеянным склерозом с выраженным иммунодефицитом, добиться урежения рецидивов заболевания, продлить период трудоспособности пациентов. 1 з. п. ф-лы, 2 табл.
| СПОСОБ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА | 1991 |
|
RU2016568C1 |
| RACKE M.K | |||
| et al | |||
| Intravenous antigen administration as a therapy for autoimmune demyelinating disease (USA) // Ann.-Neurol., 1996, Jan; 39(1):46-56 [Medline, CD-ROM, 1996] | |||
| ДЕМИНА Т.Л | |||
| и др | |||
| Роль цитоксинов в определении стадии активности иммунопатологического процесса и их использование при лечении рассеянного склероза // Диагностика и лечение демиелинизирующих заболеваний нервной системы | |||
| Сб | |||
| науч | |||
| тр | |||
| - Ярославль, 1998, с.26-35. | |||
Авторы
Даты
2003-02-27—Публикация
2001-02-23—Подача