Изобретение относится к области прикладной электрохимии и может быть использовано для очистки природной пресной воды от микроорганизмов, ионов тяжелых металлов, токсичных органических соединений и коллоидных взвесей.
Предшествующий уровень техники
В настоящее время очистка и кондиционирование воды осуществляются с помощью процессов коагуляции, сорбции, флотации, фильтрации, ионного обмена, обеззараживания, регулирования минерализации, рН, состава растворенных газов. Все эти процессы реализуются с применением различных методов - химических (ввод коагулянтов, флокулянтов, дезинфектантов, окислителей, регуляторов рН и др. ), электрохимических (электродиализ, электрокоагуляция, электролитическое получение гипохлорита натрия), физических (ультразвук, ультрафиолетовое облучение, обработка высоковольтным искровым разрядом), механических (отстой, аэрация, фильтрация, очистка в гидроциклонах) [1].
Многообразие методов очистки воды объясняется тем, что природная вода имеет сложный физико-химический состав и обычно содержит ионы неорганических соединений (Na+, К+, Са2+, Мg2+, Fe3+, Fe2+, Al3+, NH4 +, Сl-, НСО3 -, SO4 2-, NO3 -, NO2 -, F-, SiO3 2-, HS-, СО3 2- и др.), растворенные газы (O2, CO2, N2, H2S), мельчайшие частицы твердых примесей, органические вещества природного и искусственного происхождения, микроорганизмы и продукты их жизнедеятельности. Таким образом, природная вода представляет собой водный раствор веществ в различном агрегатном состоянии сложного химического состава и содержит нежелательные примеси, которые имеют отличающиеся в десятки и сотни тысяч раз линейные размеры, разнообразную физическую и химическую природу (гидрофильные, гидрофобные, заряженные, незаряженные).
Для очистки и кондиционирования воды в каждом конкретном случае необходимо определять комбинацию известных приемов для достижения положительного результата. Промышленные системы для очистки воды являются сложными гидротехническими сооружениями, включают оборудование и системы для стадий водоподготовки, а также склады химических реагентов, устройства для их ввода в обрабатываемую воду и удаления продуктов реакций из технологического цикла после завершения химических процессов очистки. Кроме того, подобные стационарные системы ориентированы на очистку воды определенного типа, весьма инерционны (т. е. требуют значительного времени на оптимизацию работы системы при изменении физико-химических показателей воды), нуждаются в большом количестве реагентов, не позволяют регулировать окислительно-восстановительные характеристики воды, т.е. не способны влиять на ее физиологически функциональные свойства.
Известно применение в практике очистки воды технологических процессов, связанных с получением электрохимически активированной воды и растворов [2].
В отличие от известных методов электрохимическая активация (ЭХА) направленно изменяет активность электронов в воде и водных растворах, что существеннейшим образом влияет, соответственно, на параметры практически всех физико-химических процессов на границе раздела фаз "вода - объект". Это изменение является временным и после самопроизвольного рассеяния (диссипации) избыточной электрической энергии, введенной в воду в процессе ЭХА, может сохраняться, постепенно убывая (процесс релаксации), в зависимости от внешних условий - от нескольких минут до нескольких десятков и даже сотен часов. Сущность очистки воды с применением ЭХА состоит в использовании избыточной энергии воды после завершения ЭХА, т. е. в период релаксации или возвращения возмущенных коротким интенсивным униполярным электрохимическим воздействием параметров воды к равновесным значениям, в процессах, где эта энергия трансформируется в направленное физико-химическое воздействие, которое способствует устранению (уничтожению, разрушению, удалению, преобразованию, необратимому при обычных условиях физико-химическому связыванию) вредных примесей.
Наиболее близким по технической сути и достигаемому результату является способ, использующий технологию ЭХА и реализуемый в устройстве для обработки воды и/или водных растворов [3].
Устройство для обработки содержит реактор, выполненный по крайней мере из одного электрохимического модульного элемента, представляющего собой компактный диафрагменный электролизер с вертикальными цилиндрическими электродами и цилиндрической керамической диафрагмой, разделяющей межэлектродное пространство на электродные камеры со входом в нижней и выходом в верхней частях реактора. Электроды и диафрагма коаксиально установлены в диэлектрических втулках. В устройстве линия подачи воды соединена через регуляторы расхода со входами электродных камер. Способ обработки воды в указанном устройстве включает обработку исходной воды в катодной камере диафрагменного электрохимического реактора ( где происходит повышение рН, снижение окислительно-восстановительного потенциала (ОВП), насыщение воды водородом, свободными гидроксильными группами, перевод ионов тяжелых металлов в нерастворимые гидроксиды), очистку воды в герметичном флотационном реакторе с удалением части потока воды вместе с газами и коллоидными частицами гидроксидов тяжелых металлов и последующую обработку в анодной камере диафрагменного электрохимического реактора, в которой осуществляется регулирование рН, повышение ОВП, насыщение воды оксидантами, в том числе, пероксидными соединениями водорода, озоном, кислородом, что обеспечивает обеззараживание воды.
Недостатком известного решения является то, что во флотационном реакторе невозможно полностью очистить воду от образовавшихся при обработке в катодной камере коллоидных частичек гидроксидов тяжелых металлов в силу их малых размеров. Некоторая часть гидроксидов тяжелых металлов поступает в анодную камеру, где может вновь превратиться в растворимые в воде соли. Другим недостатком известного способа является наличие в обработанной воде оксидантов, представленных соединениями активного хлора. Их содержание в питьевой воде регламентировано санитарными нормами и не должно превышать 0,3 мг/л, в то время как при электрохимической анодной обработке из хлоридов, содержащихся в обрабатываемой воде, может быть синтезировано гораздо большее количество соединений активного хлора, чем допускается. Кроме того, не все органические соединения, представляющие опасность для человека и находящиеся в воде, могут быть разрушены полностью при обработке воды описанным способом.
Раскрытие изобретения
Техническим результатом использования настоящего изобретения является повышение степени очистки воды от растворенных примесей, в частности металлов, исключение повышенного содержания активного хлора, расширение функциональных возможностей способа за счет возможности использования унифицированных приемов обработки воды в зависимости от ее состава и повышение качества воды за счет придания ей оптимальных, не зависящих от исходного состава, значений рН и ОВП.
Указанный результат достигается тем, что способ обработки воды включает обработку исходной воды в катодной камере диафрагменного электрохимического реактора, очистку воды в герметичном флотационном реакторе с удалением части потока воды вместе с газами и коллоидными частицами гидроксидов тяжелых металлов и последующую обработку в анодной камере диафрагменного электрохимического реактора, причем обработку ведут с использованием одного или нескольких электрохимических диафрагменных реакторов, обработку воды в катодной и анодной камерах ведут в соответствующих камерах одного и того же или разных реакторов, а перед обработкой в анодной камере поток воды обрабатывают в основном каталитическом реакторе, выполненном в виде герметичной, работающей под избыточным давлением емкости, заполненной гранулами гидрофильного минерального вещества с протоком воды сверху вниз, а после обработки в анодной камере воду дехлорируют.
Использование одного или нескольких электрохимических реакторов осуществляется в зависимости от исходного состава обрабатываемой воды.
Обработка воды в катодной камере при удельном расходе электроэнергии 0,5-2,0 Вт•ч/л производится с целью образования нерастворимых гидроксидов из ионов тяжелых металлов, насыщения воды водородом, величения рН и снижения окислительно-восстановительного потенциала воды.
В катодной камере вода очищается за счет образования нерастворимых гидроксидов тяжелых металлов. Кроме того, в катодной камере происходит прямое электролитическое восстановление (на поверхности электрода), а также электрокаталитическое восстановление (в объеме воды с участием катализаторов-переносчиков и гидратированных электронов) многозарядных катионов тяжелых металлов.
Указанные процессы снижают токсичность воды, обусловленную наличием ионов тяжелых металлов, за счет перевода их в естественную устойчивую, биологически неактивную форму существования в природе.
Обработка воды в анодной камере при удельном расходе электроэнергии 0,5-2,0 Вт•ч/л производится с целью окисления органических веществ и уничтожения микроорганизмов как непосредственно на аноде, так и продуктами анодного разложения воды и растворенных в ней солей. Позволяет уменьшать рН воды на 0,5-2 ед. рН, а также увеличивать ее ОВП на 100 - 500 мВ.
Основными процессами при униполярной электрохимической анодной обработке воды являются электролитическое, а также гетерофазное и жидкофазное электрокаталитическое окисление воды и содержащихся в ней веществ. В анодной камере вода насыщается высокоактивными окислителями. Процессы прямого электролитического окисления (на поверхности электрода) и электрокаталитического окисления (на каталитически активных центрах поверхности электрода и в объеме воды с участием катализаторов-переносчиков) обеспечивают деструкцию органических примесей и уничтожение микроорганизмов. При обработке воды в указанном интервале расхода электроэнергии вода приобретает аномально высокое значение окислительно-восстановительного потенциала воды непосредственно в анодной камере (свыше +2000 мВ при измерении платиновым электродом относительно хлорсеребряного электрода сравнения - х.с.э.), что, наряду с наличием метастабильных соединений активного хлора и активного кислорода, участвующих в реакциях, исключает образование токсичных хлорорганических веществ.
Так как электрохимическую обработку ведут в диафрагменном реакторе, то регулируемый электромиграционный перенос ионов через диафрагму электрохимического реактора позволяет удалять из воды избыточное количество ионов, в том числе ионов тяжелых металлов, нитратов, нитритов. Регулирование скорости и селективности электромиграционного переноса достигается изменением плотности электрического тока, перепадом давления на диафрагме, выбором оптимальных физико-химических и фильтрационных ее характеристик.
Повышение степени очистки воды от гидроксидов тяжелых металлов, в том числе железа и других коллоидных взвесей, достигается за счет обработки в основном каталитическом реакторе, где создаются условия для электростатического удерживания коллоидных частиц в зоне диффузионных слоев электрохимически активированных поверхностей минеральных кристаллов. Работа каталитического реактора основана на использовании электрокинетических явлений - электроосмоса, электрофореза, электрофильтрации.
В каталитический реактор, представляющий собой герметичную работающую под избыточным давлением емкость, заполненную сравнительно крупными (средний размер 2,0-5,0 мм) зернами кварца, или оксида алюминия, или оксида циркония, или их смесью, сверху вниз подается вода с окислительно-восстановительным потенциалом -200. . . -600 мВ (х.с.э.). Столь высокий восстановительный потенциал индуцирует значительный отрицательный заряд поверхности кварцевых кристаллов, что приводит к резкому увеличению толщины диффузного слоя противоионов, окружающих зерна кварца. Диффузные слои соседних зерен кварца взаимно перекрываются, создавая в каналах протока-воды электрические поля с постоянным во времени градиентом электрического потенциала.
Поток воды протекает между зернами кварца, оказываясь в электростатическом поле диффузной части ионных слоев Гуи-Чэпмена. Микроколлоидные частицы гидроокисей железа и тяжелых металлов имеют значительно меньший электрический заряд, чем заряд поверхности зерен кварца, поэтому под действием градиента электрического потенциала приближаются к поверхности кристаллов и удерживаются там первоначально за счет электростатического взаимодействия, а затем - за счет хемосорбционного. При этом они теряют значительную часть гидратационной воды и резко уменьшаются в объеме, не оказывая препятствия протекающей воде и не десорбируясь при остановке работы реактора.
Таким образом, процессы, протекающие в каталитическом реакторе, могут быть охарактеризованы как микроэлектрогидродинамичесие, а его работу в процессе очистки воды можно сравнить с работой электрофильтра для очистки газа от взвешенных частиц.
Обработку в катодной камере ведут до достижения значений рН 9,5-10,5 и окислительно-восстановительного потенциала -250. . . -600 мВ относительно хлорсеребряного электрода сравнения.
При более низких значения рН и более высоких значениях окислительно-восстановительного потенциала (ОВП) не обеспечивается образование устойчивого диффузионного слоя на поверхности кристаллов, что снижает степень очистки, а повышение значений рН свыше 10,5 и уменьшение ОВП ниже минус 600 мВ ведет к перерасходу энергии.
При флотационной очистке из герметичного флотационного реактора удаляют от 1 до 10% от общего потока воды, обработанного в катодной камере. Вода после катодной обработки в электрохимическом реакторе насыщена электрически активными микропузырьками водорода, размеры которых находятся в пределах 0,2-10 мкм. На границе раздела фаз "газ-жидкость" концентрируются нерастворимые гидроксиды металлов и другие коллоидные частицы. Удаление всех микропузырьков газа в обычном флотационном реакторе требует большого времени вследствие низкой скорости их всплывания. Поэтому в зависимости от состава исходной воды удаление 1-10% общего потока воды позволяет отделить до 90% всех флотируемых частиц.
В качестве гранул гидрофильного минерального вещества в основном каталитическом реакторе используют частицы кварца, или оксида алюминия, или оксида циркония, или их смесь, причем размер частиц составляет от 2 до 5 мм.
Перечисленные материалы имеют гидрофильную поверхность и способность к адсорбции как положительно, так и отрицательно заряженных частиц в зависимости от величины окислительно-восстановительного потенциала водной среды. Применение частиц меньшего размера приводит к увеличению гидравлического сопротивления, а увеличение частиц более 5 мм уменьшает поверхность контакта и снижает степень очистки воды.
Обработку в анодной камере ведут до достижения значений рН 6,1-7,1 и окислительно-восстановительного потенциала +400..,+600 мВ относительно хлорсеребряного электрода сравнения. Обработка до более низких значений рН и ОВП не обеспечивает эффективного удаления активного хлора и, как и более высокие значения, отрицательно сказывается на качестве воды.
Дехлорирование воды ведут с использованием катализатора, например углеродсодержащего. При этом осуществляют гетерофазную каталитическую деструкцию соединений активного хлора и гетерофазное каталитическое окисление органических веществ. Гранулы углеродсодержащего катализатора не требуют замены и регенерации.
Активные частицы, образующиеся в процессе каталитического разложения соединений активного хлора, обеспечивают деструктивное окисление широкой гаммы органических веществ, в том числе фенолов, хлорфенолов, диоксинов.
После обработки воды в анодной камере и перед дехлорированием поток воды выдерживают в течение 0,1-10,0 с в реакторе смешения и/или обрабатывают в дополнительном каталитическом реакторе с частицами гидрофильного минерального вещества, причем размер частиц в дополнительном реакторе составляет от 0,5 до 2,0 мм.
В реакторе смешения проводят жидкофазное каталитическое окисление органических соединений, необходимое для завершения окислительных реакций после обработки воды в анодной камере электрохимического реактора. Окисление органических веществ протекает с участием промежуточных окислителей (медиаторов). Этими веществами являются акцепторы электронов, синтезированные у анода, или доноры электронов, образующиеся при катодных электрохимических реакциях. Общим для реакций жидкофазного каталитического окисления или восстановления является то, что непосредственный окислитель или восстановитель генерируется и регенерируется на электроде электрохимического реактора.
Конечными продуктами этих реакций являются совершенно нетоксичные, безвредные и безопасные для человека соединения.
Обработка воды в дополнительном каталитическом реакторе с частицами гидрофильного минерального вещества, размер которых составляет от 0,5 до 2,0 мм, имеет своей целью интенсифицировать процессы деструкции органических веществ. Она основана на использовании процесса микрокавитации при фазовых переходах, который протекает на границе раздела фаз в пористой среде во время протока воды с высоким окислительным потенциалом и растворенными в ней газами, причем наибольшая интенсивность этого процесса проявляется на двухфазной ("газ-жидкость") и трехфазной ("газ-жидкость-твердое тело") границах в момент возникновения газовой фазы, т.е. в момент зарождения газового микропузырька.
Материалом, обеспечивающим организацию процесса микроэлектрофизической деструкции органических веществ, являются зерна или гранулы электрохимически активного минерального вещества, например кварца, оксида алюминия, оксида циркония или других твердых минеральных частиц, имеющих гидрофильную поверхность и способность к адсорбции как положительно, так и отрицательно заряженных частиц в зависимости от величины окислительно-восстановительного потенциала водной среды.
Другим важным условием, при котором возможен процесс микроэлектрофизической деструкции органических соединений, является наличие в протекающей через слой твердых частиц воде растворенных газов - кислорода, озона, водорода, полученных в результате предварительной катодной, а затем анодной электрохимической обработки воды, высокое значение окислительного потенциала воды с растворенными газами (более +400 мВ в шкале платинового и хлорсеребряного электродов), а также определенная скорость протока воды, при которой начинается выделение растворенных в воде газов в местах наибольших возмущений потока - гидродинамических (места локального изменения давления, скорости, направления течения) и электрохимических (места резкого изменения напряженности электрического поля двойного электрического слоя на поверхности твердых частиц, области электрически активных центров кристаллов).
При использовании частиц размером менее 0,5 мм возрастает гидравлическое сопротивление, и при увеличении размера частиц более 2 мм увеличивается скорость движения потока воды, что снижает возможность выделения газовых пузырьков, а, кроме того, уменьшается активная поверхность и снижается степень очистки.
В гетерогенной системе, представленной кристаллами кварца или других подобных веществ, вблизи границ раздела фаз на молекулярных расстояниях существует область особого энергетического состояния - очень больших и неоднородных силовых полей. Области действия электростатических сил, возникающих вблизи различных участков твердой фазы, могут перекрываться, если вода имеет достаточно высокое значение окислительно-восстановительного потенциала. В итоге ход химических процессов у поверхности является весьма нестандартным.
На молекулы воды оказывает сильное структурирующее воздействие заряд гидрофильной поверхности раздела. Наличие сетки водородных связей между молекулами воды приводит к тому, что изменение во взаимном расположении молекул в граничном слое (оно навязывается, в частности, потенциалопределяющими ионами поверхности раздела) затухает с удалением от межфазной границы достаточно медленно, сохраняясь на расстоянии до 10 нм, а иногда и более.
Сильные электрические поля в области межфазных границ в сочетании с гидродинамическими возмущениями способны инициировать фазовые переходы первого рода, т. е. вызывать генерацию газовых микропузырьков. Внутри микропузырька, особенно в начальные моменты его зарождения, создается электрическое поле очень высокой напряженности (более 10000 В/см), что обусловлено его малыми размерами, а также значительной разностью электрических потенциалов на его противоположных поверхностях, где сосредоточены заряженные частицы - продукты предшествующих электрохимических реакций.
В зависимости от условий решаемой задачи обработку воды ведут с использованием основного и дополнительного электрохимических диафрагменных реакторов. Обработку воды ведут в катодной камере основного реактора, флотационном реакторе, основном каталитическом реакторе и анодной камере основного электрохимического реактора с последующим дехлорированием, и поток воды перед дехлорированием обрабатывают в дополнительном каталитическом реакторе с размером частиц гидрофильного минерального вещества 0,5-2,0 мм, а после дехлорирования поток воды последовательно обрабатывают в катодной камере дополнительного диафрагменного электрохимического реактора и втором дополнительном каталитическом реакторе.
При этом обработку воды в анодной камере дополнительного диафрагменного электрохимического реактора ведут при расходе электричества 20-500 Кл/л, а в катодную камеру дополнительного электрохимического реактора подают ту часть потока, которая удалена из флотационного реактора.
Также возможно обработку воды вести с использованием основного и двух дополнительных электрохимических диафрагменных реакторов, при этом исходную воду обрабатывают в катодной камере основного реактора, во флотационном реакторе, из которого удаляют часть потока обработанной воды, в основном каталитическом реакторе, в анодной камере первого дополнительного элетрохимического реактора, в дополнительном каталитическом реакторе, в котором размер частиц составляет 0,5-2,0 мм, с последующим дехлорированием и обработкой в катодной камере второго дополнительного электрохимического реактора и втором дополнительном каталитическом реакторе.
В этом случае обработку в основном и двух дополнительных диафрагменных электрохимических реакторах ведут при расходе электричества соответственно 40-350, 50-200 и 70-150 Кл/л, а та часть потока обрабатываемой воды, которая удалена из флотационного реактора, последовательно подается в анодную камеру основного, в катодную камеру первого дополнительного и анодную камеру второго дополнительного диафрагменных электрохимических реакторов.
При осуществлении способа целесообразно использовать проточные электрохимические модульные реакторы, описанные в патенте РФ 2078737 или патенте США 5635040. Эти реакторы, известные как элементы ПЭМ, представляют собой компактные диафрагменные электролизеры, выполненные из вертикальных цилиндрического и стержневого электродов, коаксиально установленных в диэлектрических втулках, керамической диафрагмы, также коаксиально установленной во втулках между электродами и разделяющей межэлектродное пространство на электродные камеры, причем камеры имеют вход в нижней и выход в верхней частях ячейки. Электролизеры выполнены по модульному принципу, что позволяет реализовать способ с обеспечением заданной производительности.
При обработке в электрохимической ячейке целесообразно использовать ультрафильтрационную или нанофильтрационную диафрагму из керамики. Керамические диафрагмы не изменяют свои характеристики при перепаде давления и в процессе обработки, что обеспечивает стабильность параметров обработки.
Состав керамики выбирают исходя из условий решаемой задачи, предпочтительно использование керамики на основе оксида циркония или керамики на основе оксида циркония с добавками оксидов алюминия и иттрия, которые обладают оптимальным сочетанием характеристик.
Вспомогательные устройства - реакторы каталитические, флотационные, смесительные, дехлораторы и ряд других узлов - специально сконструированы с учетом работы совместно с элементами ПЭМ (одиночными или в виде реакторов, включающих в зависимости от производительности от 2 до 20 элементов ПЭМ), что унифицирует и упрощает конструктивное оформление способа, а также позволяет оперативно применять ту или иную разновидность способа в зависимости от условий решаемой задачи.
Краткое описание фигур чертежей
Способ реализуется с помощью установок, схемы которых представлены на фиг.1-5.
На фиг. 1 приведена схема установки для реализации способа по изобретению, содержащая один электрохимический диафрагменный реактор.
Установка содержит электрохимический диафрагменный реактор 1, межэлектродное пространство которого разделено диафрагмой 2 на анодную 3 и катодную 4 камеры. Установка также содержит герметичный флотатор 5, основной каталитический реактор 6, заполненный гранулами гидрофильного минерального вещества, и дехлоратор 7. Линия подвода обрабатываемой воды 8, линия отвода обработанной воды 9 и линия отвода 10 части потока из флотатора 5, а также обвязка узлов, могут быть выполнены в виде трубопроводов, гибких или жестких, а также в любом другом виде, обеспечивающем движение гидравлических потоков в соответствии с предложенным способом. Линия 10 содержит также регулятор расхода 11.
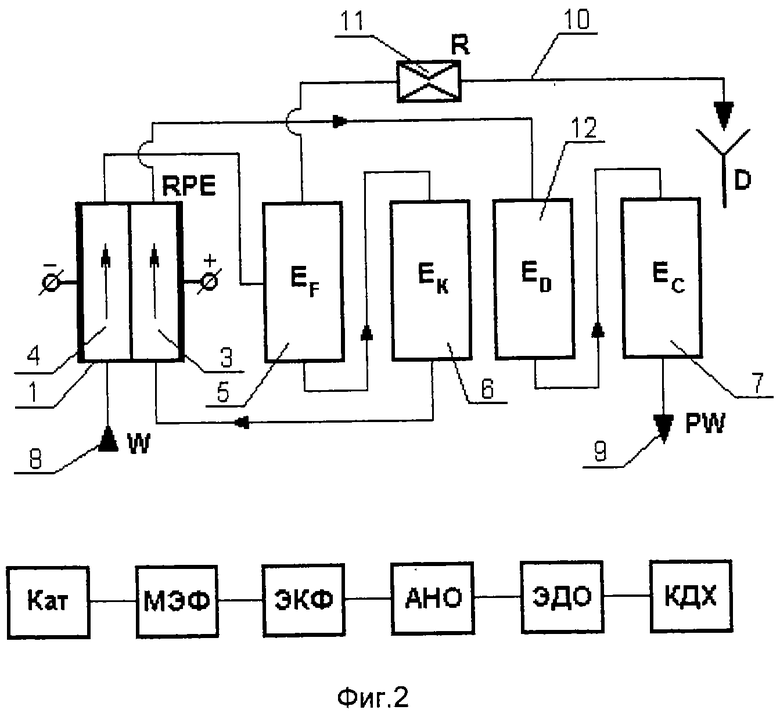
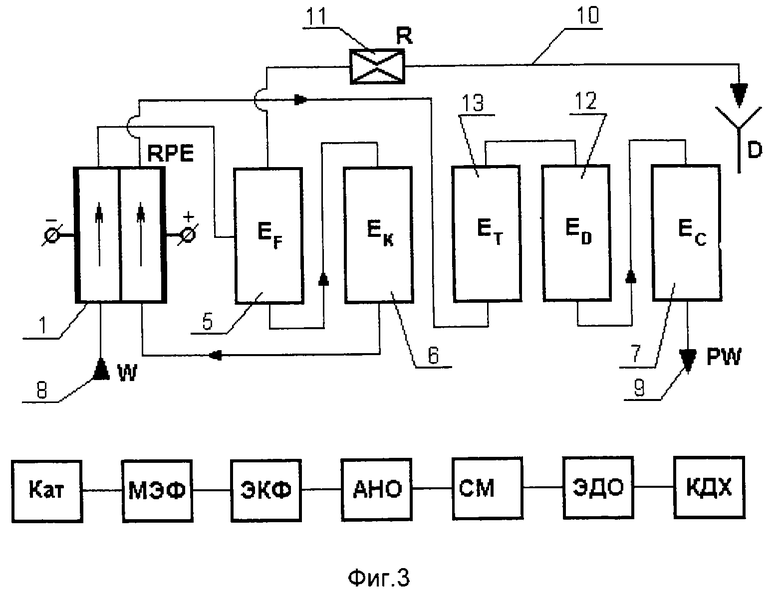
Установка также может содержать реактор смешения 12 (фиг.2) или последовательно соединенные реактор смешения 12 и дополнительный каталитический реактор 13 (фиг.3).
Установка для реализации способа также может содержать несколько электрохимических реакторов.
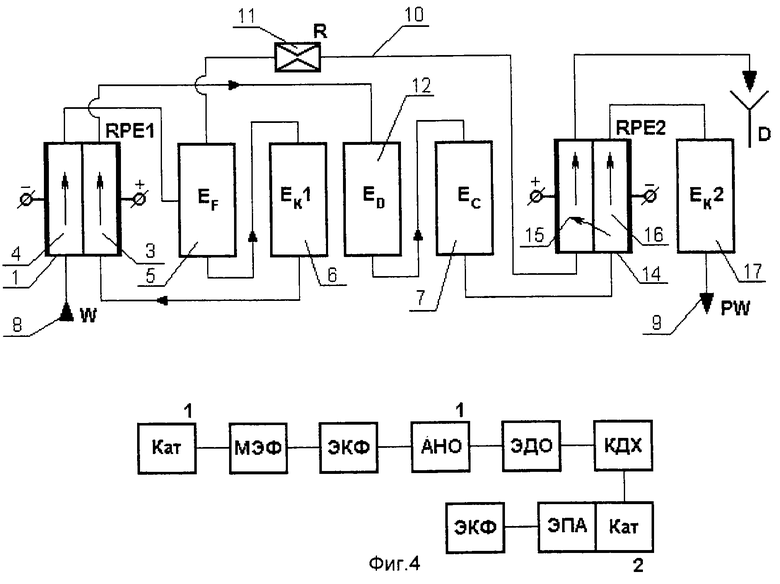
Так на фиг.4 изображена установка, содержащая диафрагменный реактор 1, межэлектродное пространство которого разделено диафрагмой 2 на анодную 3 и катодную 4 камеры, герметичный флотатор 5, основной каталитический реактор 6, заполненный гранулами гидрофильного минерального вещества, и дехлоратор 7. Линия подвода обрабатываемой воды 8, линия отвода обработанной воды 9 и линия 10 с регулятором расхода 11 для отвода части потока из флотатора 5, а также дополнительный диафрагменный электрохимический реактор 14 с анодной 15 и катодной 16 камерами, дополнительные каталитические реакторы 12 и 17.
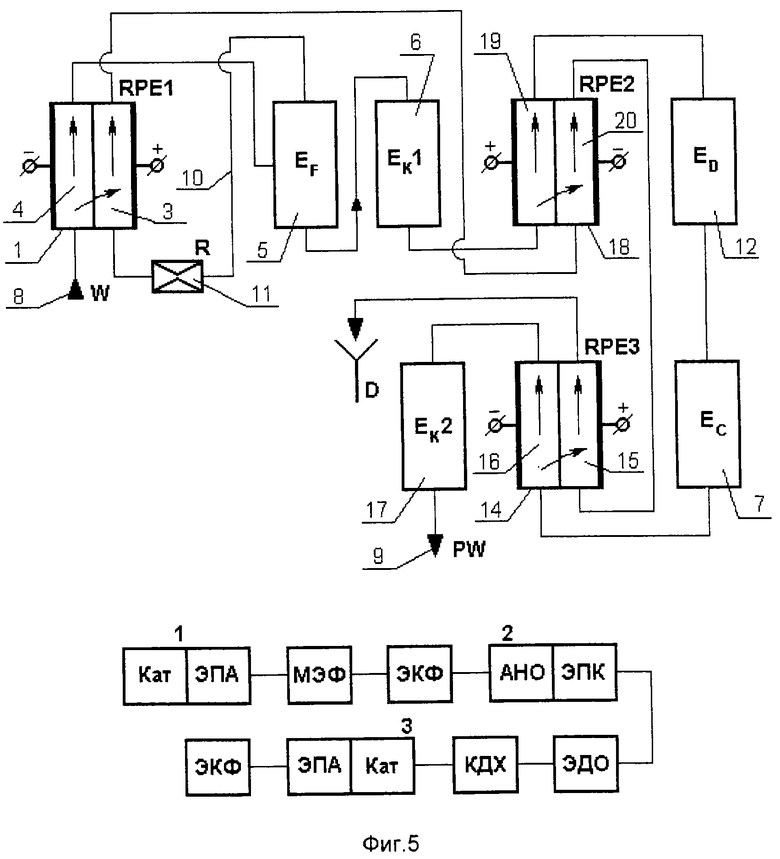
Или установка (фиг.5) может содержать диафрагменный реактор 1, межэлектродное пространство которого разделено диафрагмой 2 на анодную 3 и катодную 4 камеры, герметичный флотатор 5, основной каталитический реактор 6, заполненный гранулами гидрофильного минерального вещества, и дехлоратор 7. Линия подвода обрабатываемой воды 8, линия отвода обработанной воды 9 и линия 10 с регулятором расхода 11 для отвода части потока из флотатора 5, а также дополнительный диафрагменный электрохимический реактор 14 с анодной 15 и катодной 16 камерами, дополнительный диафрагменный электрохимический реактор 18 с анодной 19 и катодной 20 камерами и дополнительные каталитические реакторы 12 и 17.
Способ осуществляют следующим образом (см. фиг.1).
Исходная вода по линии 8 подается в нижнюю часть катодной камеры 4 реактора 1. В процессе обработки потока воды в катодной камере 4 происходит насыщение воды водородом, увеличение рН снижение значения окислительно-восстановительного потенциала до величин минус 600 мВ относительно хлорсеребряного электрода сравнения.
Основными процессами при катодной обработке воды являются электролитическое, а также гетерофазное и жидкофазное электрокаталитическое восстановление в катодной камере электрохимического реактора воды и содержащихся в ней веществ. При катодной обработке вода насыщается высокоактивными восстановителями: ОН-, H2O2, НО2 -, O2 -, eaq. Это приводит к образованию нерастворимых гидроксидов тяжелых металлов (Men++nОН- --> Ме(ОН)n). Кроме того, в катодной камере происходит прямое электролитическое восстановление (на поверхности электрода), а также электрокаталитическое восстановление (в объеме воды с участием катализаторов-переносчиков и гидратированных электронов) многозарядных катионов тяжелых металлов: Men++е --> Меo, например, Hg2 2++2е --> 2Нg; Pb2++2е --> Рb; Cu(NH3)2 ++е --> Сu+2NН3.
Указанные процессы снижают токсичность воды, обусловленную наличием ионов тяжелых металлов, за счет перевода их в естественную устойчивую, биологически неактивную форму существования в природе. Такая вода не представляет опасности, поскольку при попадании в желудок гидроксиды легко связываются энтеросорбентами (белками, полисахаридами), которые предохраняют их от растворения в кислой среде желудочного сока. Таким образом, они не растворяются в желудке и выводятся из организма естественным путем. Аналогичным образом внутренние сорбенты связывают хлопья солей жесткости, гидроксидов железа. Эти компоненты практически безвредны для организма. Однако их присутствие в питьевой воде меняет ее вкус и иногда нежелательно по органолептическим показателям, и в соответствии с предложенным способом вода, обработанная в катодной камере 4, отводится из ее верхней части и подается в среднюю часть герметичного флотатора 5.
Во флотационном реакторе, в который поступает вода после катодной обработки в электрохимическом реакторе, насыщенная электрически активными микропузырьками водорода, происходит отделение основной части нерастворимых примесей. Размеры микропузырьков водорода находятся в пределах 0,2-10 мкм. Электрическая активность пузырьков водорода обусловлена тем, что на границе раздела фаз "газ-жидкость" сосредоточены электрохимически активные неустойчивые продукты катодных реакций, такие, как Н2О2 -, НO2 -, O2 -, eaq. На этой же границе концентрируются нерастворимые гидроксиды металлов и другие коллоидные частицы. Из верхней части флотатора 5 по линии 10 отводится флотошлам и часть обработанного потока воды. Количество отводимого потока устанавливается с помощью регулятора 11. Во флотаторе 5 отделяют до 90% всех флотируемых частиц.
Из нижней части флотатора 5 осветленный поток подают на обработку при протоке сверху вниз в основной каталитический реактор 6.
В реакторе 6 проводят финишную очистку воды от гидроксидов тяжелых металлов, в том числе железа, и других коллоидных взвесей за счет электростатического удерживания коллоидных частиц в зоне диффузионных слоев электрохимически активированных поверхностей минеральных кристаллов.
В реактор 6, представляющий собой герметичную работающую под избыточным давлением емкость, заполненную крупными (средний размер 2,0-5,0 мм) зернами кварца, подается вода с окислительно-восстановительным потенциалом -200... -600 мВ (х.с.э.).
Поток воды протекает между зернами кварца, оказываясь в электростатическом поле диффузной части ионных слоев Гуи-Чэпмена. Микроколлоидные частицы гидроокисей железа и тяжелых металлов имеют значительно меньший электрический заряд, чем заряд поверхности зерен кварца, поэтому под действием градиента электрического потенциала приближаются к поверхности кристаллов и удерживаются там первоначально за счет электростатического взаимодействия, а затем - за счет хемосорббционного. При этом они теряют значительную часть гидратационной воды и резко уменьшаются в объеме, не оказывая препятствия протекающей воде и не десорбируясь при остановке работы реактора. После того как процесс хемосорбционной иммобилизации коллоидных частиц завершится вследствие заполнения свободных участков поверхности кварцевых зерен коллоидными частицами гидроксидов, резко возрастает гидравлическое сопротивление реактора, поскольку удерживаемые электростатическими силами коллоидные частицы гидроксидов не теряют гидратационную воду и быстро заполняют каналы протока воды. Данный момент фиксируется по возрастанию давления воды на входе в реактор и является сигналом к необходимости регенерации кварцевой загрузки реактора 6. Регенерация активной массы реактора 6 осуществляется путем снятия зарядов с поверхностей минеральных кристаллов и удаления коллоидных взвесей промывкой слабым раствором кислоты.
После обработки в основном каталитическом реакторе 6 вода подается на обработку в анодную камеру 3 реактора 1.
Обработка потока воды в анодной камере осуществляется при удельном расходе электроэнергии 0,5-2,0 Вт•ч/л. В процессе обработки происходит окисление органических веществ и уничтожение микроорганизмов как непосредственно на аноде, так и продуктами анодного разложения воды и растворенных в ней солей. Также уменьшается рН воды на 0,5-2 ед. рН и увеличивается ее ОВП на 100-500 мВ.
В анодной камере вода за время протока насыщается высокоактивными окислителями: HClO, ClO2, ClO2 -, О3, O2 -, H2O2, ОН*, НO2*. Их концентрация в зависимости от режима электрохимической обработки может изменяться от 1 до 10 мг/л. Процессы прямого электролитического окисления (на поверхности электрода) и электрокаталитического окисления (на каталитически активных центрах поверхности электрода и в объеме воды с участием катализаторов-переносчиков) обеспечивают деструкцию органических примесей и уничтожение микроорганизмов. Аномально высокое значение окислительно-восстановительного потенциала воды непосредственно в анодной камере (свыше +2000 мВ при измерении платиновым электродом относительно хлорсеребряного электрода сравнения - х.с.э.) и метастабильные соединения активного хлора и активного кислорода, участвующие в реакциях, исключают образование токсичных хлорорганических веществ.
При переходе электронов из органических соединений на анод обычно возрастает число (или кратность) кислородсодержащих связей (С-O, N-O, S-O и т.п. ), либо уменьшается число водородсодержащих связей (С-Н, N-H, S-H и т.п.), например: RCHO --> RCOOH; R2CHCHR2 --> R2C=CR2.
Процессы окисления органических веществ являются первой стадией детоксикации в живых организмах. Например, в ответ на попадание в организм человека или животных ксенобиотиков в клетках печени повышается концентрация определенных форм фермента цитохорма Р-450, осуществляющего окисление ксенобиотиков. Продукты окисления органических веществ-ксенобиотиков, как правило, безвредны для организма, поскольку превращаются в гидрофильные хорошо растворимые в воде соединения и легко выводятся экскреторными органами. В простейшем детоксицирующем цикле работают всего два типа биомолекул - альбумин и цитохром Р-450. Альбумин выполняет транспортную функцию, цитохром Р-450 - окислительную. Попавшие в организм гидрофобные токсины (RH) образуют с альбумином комплекс (RHA), который и переносится в печень. Там этот комплекс (или свободный токсин) окисляется на цитохроме Р-450 с образованием гидрофильных продуктов (ROHA) или (ROH).
Анодная униполярная электрохимическая обработка по окислительному воздействию на много порядков превосходит природные процессы детоксикации.
Ниже приведены некоторые реакции окислительной деструкции органических соединений в анодной камере в процессе очистки воды.
Разрушение формальдегида (НСНО), метилового спирта (СН3ОН), карбамида ((NH2)2 CO) происходит до простых нетоксичных веществ в соответствии со следующими реакциями:
НСНО+2Н2O - 4е --> СО3 2-+6Н+;
СН3ОН+2Н2O -6е --> СО3 2-+8Н+;
(NH2)2CO+Н2O- 6е --> N2+СO2+6H+
Образующиеся в ходе реакций промежуточные продукты также разлагаются до простых нетоксичных соединений, например
НСОО-+Н2O -2е --> CO3 2-+3H+
Аммиак (NН3), нитриты (NO2 -), сероводород (H2S) в анодной камере элемента ПЭМ-3 разрушаются в соответствии с реакциями
2NH3-6e --> N2+8H+
NO2 -+2OН- -2е --> NО3 -+Н2O
H2S-2е --> S+2H+
Если в воде присутствуют цианид-ионы (СN- ) или комплексные ионы цианидов ([Сu(СN)3] 2-, [Zn(CN)4] 2-, [Cd(CN)4]2- и др.), то в процессе анодной обработки они распадаются с образованием цианат-ионов
СN-+2OН-- 2е --> СNО-+Н2O
[Сu(СN)3]2-+6OН- - 6е --> Сu++3CNO-+3Н2O
Дальнейшее окисление приводит к образованию совершенно безопасных продуктов
2CNO-+4OН-- 6е --> 2СO2+N2+2H2O
Деструкция фенолов при анодной обработке происходит с образованием нетоксичного продукта - малеиновой кислоты
C6H5OH+16OН-- 16е --> НO2ССН=СНСО2Н (цис)+2СО2+5H2О
При полном окислении фенолов конечными продуктами являются углекислый газ и вода.
После обработки в анодной камере 3 реактора 1 поток воды поступает на дехлорирование в дехлораторе 7.
В дехлораторе 7 проводят гетерофазную каталитическую деструкцию соединений активного хлора и гетерофазное каталитическое окисление органических веществ на поверхности гранул, не требующего замены и регенерации углеродсодержащего катализатора, где происходит разрушение соединений активного хлора (HClO, ClO2*, HClO*, ClO*) с образованием высокоактивных короткоживущих частиц: О*, О, Сl*, ОН*. Некоторые реакции каталитического разложения соединений активного хлора приведены ниже.
2HClO --> 2Сl-+2O+2H+
ClO-+HClO --> 2Cl-+2O+H+
ClO*+ClO-+ОН- --> 2Cl-+2O+ОН*
2ClO* --> 2Cl-+2O
О+О --> O2
После дехлорирования очищенная вода по линии 9 подается потребителю.
При условии наличия в исходной воде повышенного содержания органических примесей и в соответствии с изобретением способ может быть реализован в установках, изображенных на фиг.2 и 3. В этом случае после обработки воды в анодной камере 3 реактора 1 и перед дехлорированием поток воды обрабатывается в реакторе смешения 12 (фиг.2) или последовательно в реакторе смешения 12 и дополнительном каталитическом реакторе 13 (фиг.3)
В реакторе смешения 12 проводят жидкофазное каталитическое окисление органических соединений. В реакторе 12 завершаются окислительные реакции после обработки воды в анодной камере 3 электрохимического реактора 1, и окисление органических веществ протекает с участием промежуточных окислителей (медиаторов). Этими веществами являются акцепторы электронов, синтезированные у анода, или доноры электронов, образующиеся при катодных электрохимических реакциях.
Некоторые реакции, протекающие в жидкой фазе в реакторе 12, приведены ниже. Элементоорганические соединения разрушаются озоном, образовавшимся в ходе предшествующих анодных реакций
Рb(С2Н5)4+2O3 --> PbO2+4СН3СНО;
SiR4+О3 --> R3SiOOН --> SiO2.
Пероксид водорода, который образуется как при анодных, так и при катодных реакциях обработки воды, участвует в реакциях разрушения сероводорода, других вредных и придающих воде неприятный запах веществ
H2S+H2O2 --> S+2H2O
Na2S+4H2O2 --> Na2SO4+4H2O
SО3 2-+H2O2 --> SO4 2-+H2O
S2O3 2-+4H2O2+2OН- --> 2SO4 2-+5H2O
2RSH+H2O2 --> RSSR+2H2O
RSR+H2O2 --> R2SO+H2O
RSSR+5H2O2+2OН- --> 2RSO3 -+6H2O
С6Н5ОН+14H2O2 --> 6СO2+17H2O
СН3ОН+3H2O2 --> СO2+5H2O
НСНО+H2O2 --> НСООН+H2O
RCHO+H2O2 --> RCOOH+H2O
НСООН+H2O2 --> СO2+H2O
R3N+H2O2 --> R3NО+H2O
N2H4+2H2O2 --> N2+2H2O
Конечными продуктами этих реакций являются совершенно нетоксичные, безвредные и безопасные для человека соединения.
В реакциях разрушения фенолов в воде после анодной обработки принимают также участие гипохлорит-ионы
С6Н5ОН+8ClO- --> HO2ССН=СНСO2Н (цис)+8Сl-+2СO2+Н2O.
В дополнительном каталитическом реакторе 13, в отличие от основного реактора 6, обработке подвергается вода с другими характеристиками, а именно с более высоким рН и имеющая существенно другие, положительные значения окислительно-восстановительного потенциала. Эта обработка воды имеет своей целью интенсифицировать процессы деструкции органических веществ.
Процесс микроэлектрофизической деструкции органических соединений протекает при наличии в протекающей через слой твердых частиц воде растворенных газов - кислорода, озона, водорода, полученных в результате предварительной катодной, а затем анодной электрохимической обработки воды, и высоком значении окислительного потенциала воды с растворенными газами (более +400 мВ в шкале платинового и хлорсеребряного электродов), а также при поддержании скорости протока воды, при которой начинается выделение растворенных в воде газов в местах наибольших возмущений потока - гидродинамических (места локального изменения давления, скорости, направления течения) и электрохимических (места резкого изменения напряженности электрического поля двойного электрического слоя на поверхности твердых частиц, области электрически активных центров кристаллов).
Характерными реакциями при микроэлектрофизической обработке воды является взаимодействие органических соединений с синглетным кислородом, например, присоединение к триметилэтилену с последующим его распадом на нетоксичные соединения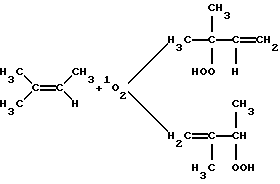
Другой возможной реакцией в процессе очистки воды является превращение антрацена в антрахинон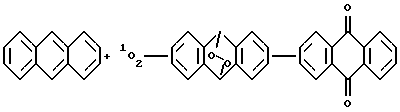
Возможно также окисление как в газовой фазе микропузырьков, так и в водной среде сернистых соединений (сульфидов и меркаптанов)
2R2S+1O2 --> 2R2SO
При наличии в воде цианидов происходит процесс их окисления озоном, который протекает в несколько стадий, причем на одной из них образуются мочевина, азот и углекислый газ
CN-+О3 --> ОСN-+O2
OCN-+2H++Н2O --> СO2+NH4 +
NH4 +OCN- --> NH2CONH2
NH2CONH2+ 2Н2O --> (NH4)2CO3
NH2CONH2+О3 --> N2+СO2+2Н2O
Существенное значение имеет очистка воды от ионов тяжелых металлов. Железо и марганец часто присутствуют в природной воде, как правило в виде органических комплексов, которые придают воде цветность. Очистка состоит в том, что соответствующие металлы окисляются и переводятся в нерастворимый осадок, который удаляется на последующих стадиях очистки. Озон в процессах микроэлектрофизической обработки окисляет Fe(II) до Fe(III), Mn(II) до Mn(IV)
Mn2++Оз+Н2О --> МnO2+О2+2H+
2Fe2++О3+3Н2O --> 2Fе(ОН)3.
Также весьма эффективно в процессе микроэлектрофизической обработки разрушаются металлоорганические токсические соединения, например, тетраметил- и тетраэтилсвинца
Рb(СН3)4+O3 --> СН2Рb(СН3)3+ОН+O2
Pb(C2H5)4+O3 --> СН3СНРb(С2Н5)3+ОН+О2
Осуществление способа в соответствии со схемами, представленными на фиг. 2 и 3 позволяет эффективно очищать воду с высоким содержанием органических примесей.
В случае наличия в исходной воде токсичных органических веществ в повышенной концентрации целесообразно использовать для реализации способа установки, содержащие несколько электрохимических реакторов, и изображенные на фиг.4 (два электрохимических реактора) и 5 (три электрохимических реактора).
При осуществлении способа с двумя электрохимическими ректорами (см. фиг. 4), исходная вода по линии 8 подается на обработку в катодную камеру 4 реактора 1, затем во флотатор 5, в котором отделяется часть потока вместе с флотошламом, а осветленный поток подвергается обработке в основном каталитическом реакторе 6 с частицами гидрофильного кристаллического материала размером 2-5 мм, а затем поступает на обработку в анодную камеру 3 реактора 1.
После анодной обработки вода поступает на обработку в первый дополнительный каталитический реактор 12 с частицами гидрофильного кристаллического материала размером 0,5-2,0 мм, а затем поступает на дехлорирование в дехлоратор 7, после чего поток воды подвергается обработке в катодной камере 16 дополнительного электрохимического реактора 14, во втором дополнительном каталитическом реакторе 17 с частицами гидрофильного кристаллического материала размером 0,5-2,0 мм, и затем обработанная вода по линии 9 подается потребителю. При этом поток из флотатора по линии 10 подается в анодную камеру 15 реактора 14, что позволяет снизить расход энергии. Из анодной камеры 15 раствор направляется в дренаж.
При осуществлении способа с тремя электрохимическими ректорами (см. фиг. 5) исходная вода по линии 8 подается на обработку в катодную камеру 4 реактора 1, затем во флотатор 5, в котором отделяется часть потока вместе с флотошламом, а осветленный поток подвергается обработке в основном каталитическом реакторе 6 с частицами гидрофильного кристаллического материала размером 2-5 мм, а затем поступает на обработку в анодную камеру 19 дополнительного реактора 18.
После анодной обработки вода поступает на обработку в первый дополнительный каталитический реактор 12 с частицами гидрофильного кристаллического материала размером 0,5-2,0 мм, а затем поступает на дехлорирование в дехлоратор 7, после чего поток воды подвергается обработке в катодной камере 16 дополнительного электрохимического реактора 14, во втором дополнительном каталитическом реакторе 17 с частицами гидрофильного кристаллического материала размером 0,5-2,0 мм, и затем обработанная вода по линии 9 подается потребителю. При этом поток из флотатора по линии 10 подается в анодную камеру 3 реактора 1, затем этот же поток проходит катодную камеру 20 реактора 18 и анодную камеру 15 реактора 14, что позволяет снизить расход энергии. Из анодной камеры 15 раствор направляется в дренаж.
Варианты конкретного осуществления
Изобретение иллюстрируется следующими примерами, которые, однако, не исчерпывают всех возможных вариантов осуществления способа.
Во всех примерах использовался электрохимический реактор по патенту РФ 2078737 с коаксиально установленными цилиндрическим и стрежневым электродами и коаксиально же установленной между ними керамической ультрафильтрационной диафрагмой из керамики на основе смеси окислов циркония, алюминия и иттрия (соответственно 60, 37 и 3 мас.%) и толщиной 0,7 мм. В качестве электродов использовались титан с покрытием из смеси оксидов рутения и иридия (анод) и титан с пироуглеродным покрытием (катод). Длина активных участков электродов реактора равняется 200 мм, а объемы электродных камер составляют 10 мл - катодной камеры и 7 мл - анодной. В качестве гранул гидрофильного материала в основном и дополнительных каталитических реакторах использовались частицы кварца соответственно размером 3 мм и 0,5 мм. В качестве катализатора дехлорирования использовался активированный уголь.
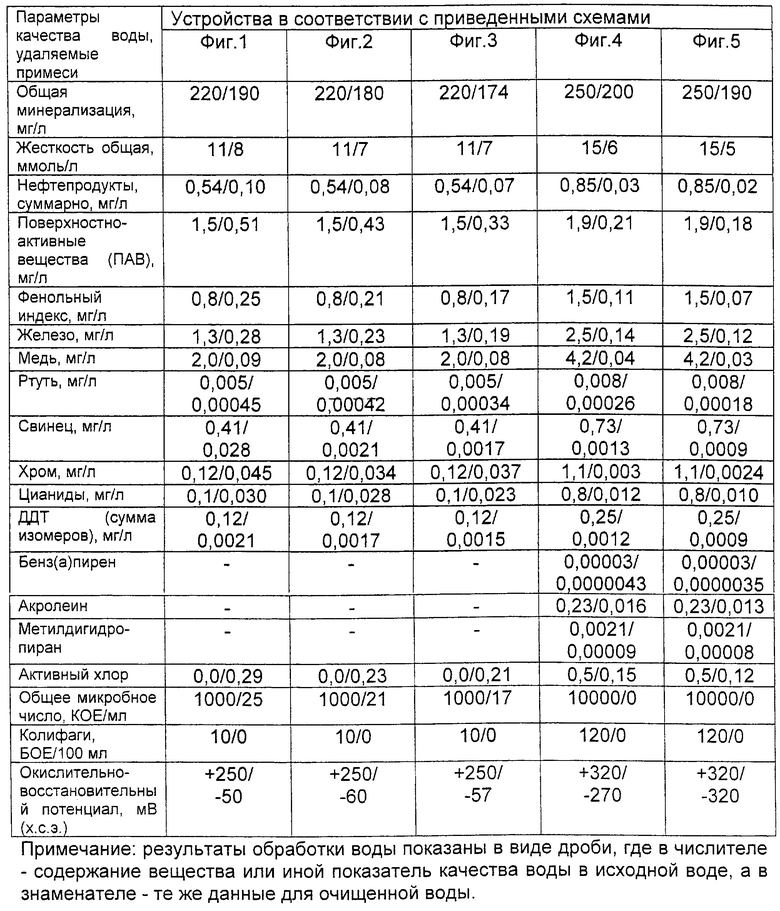
Данные по обработке воды представлены в таблице.
Промышленная применимость
По сравнению с известным решением, как следует из представленных данных, изобретение позволяет повысить степень очистки воды от растворенных примесей, в частности металлов, исключить повышенное содержание активного хлора, а также расширить функциональные возможности путем использования унифицированных приемов обработки воды в зависимости от ее состава и повысить качество воды за счет придания ей оптимальных, не зависящих от исходного состава, значений рН и ОВП.
Источники информации
1. Л.А. Кульский и др. "Технология очистки природных вод", Киев, Высшая школа, 1981, стр. 22-25.
2. В.М. Бахир. Современные технические системы для обеззараживания, очистки и активирования воды. М., ВНИИИМТ, 1999, 84 с.
3. Патент РФ 2091320, C 02 F 1/461, 1997 (прототип).
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТАНОВКА ДЛЯ ОБРАБОТКИ ПИТЬЕВОЙ ВОДЫ | 2006 |
|
RU2322394C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕЗИНФИЦИРУЮЩИХ РАСТВОРОВ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2001 |
|
RU2207983C2 |
| ПЕРЕНОСНОЕ УСТРОЙСТВО ДЛЯ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ ЖИДКОСТИ | 2001 |
|
RU2204530C2 |
| УСТАНОВКА ДЛЯ ОЧИСТКИ И СТЕРИЛИЗАЦИИ ЭНДОСКОПОВ | 1996 |
|
RU2113859C1 |
| СПОСОБ ОЧИСТКИ И СТЕРИЛИЗАЦИИ ЭНДОСКОПОВ | 1996 |
|
RU2115435C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕЗИНФИЦИРУЮЩЕГО РАСТВОРА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2001 |
|
RU2208589C2 |
| СПОСОБ ОБРАБОТКИ ПИТЬЕВОЙ ВОДЫ | 1999 |
|
RU2149835C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕЗИНФИЦИРУЮЩЕГО РАСТВОРА - НЕЙТРАЛЬНОГО АНОЛИТА | 1999 |
|
RU2157793C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕЗИНФИЦИРУЮЩЕГО РАСТВОРА - НЕЙТРАЛЬНОГО АНОЛИТА АНД | 1999 |
|
RU2148027C1 |
| УСТАНОВКА ДЛЯ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ И ОЧИСТКИ ВОДЫ И/ИЛИ ВОДНЫХ РАСТВОРОВ | 1996 |
|
RU2091320C1 |
Изобретение относится к очистке природной пресной воды от микроорганизмов, ионов тяжелых металлов, токсичных органических соединений и коллоидных взвесей. Воду обрабатывают в катодной камере диафрагменного электрохимического реактора. После этого воду очищают в герметичном флотационном реакторе с удалением части потока воды вместе с газами и коллоидными частицами гидроксидов тяжелых металлов. Осветленный поток обрабатывают в анодной камере диафрагменного электрохимического реактора, причем обработку ведут с использованием одного или нескольких электрохимических диафрагменных реакторов, и обработку воды в катодной и анодной камерах ведут в соответствующих камерах одного и того же или разных реакторов. Перед обработкой в анодной камере поток воды обрабатывают в основном каталитическом реакторе, заполненном гранулами гидрофильного минерального вещества с протоком воды сверху вниз, а после обработки в анодной камере воду дехлорируют. После обработки воды в анодной камере и перед дехлорированием поток воды может быть выдержан в реакторе смешения и/или обработан в дополнительном каталитическом реакторе с частицами гидрофильного минерального вещества, причем размер частиц в дополнительном реакторе составляет от 0,5 до 2,0 мм. Технический эффект - повышение степени очистки воды от растворенных примесей, в частности ионов тяжелых металлов и железа, исключение повышенного содержания активного хлора, расширение функциональных возможностей способа за счет возможности использования унифицированных приемов обработки воды в зависимости от ее состава и повышение качества воды за счет придания ей оптимальных, не зависящих от исходного состава, значений рН и ОВП. 10 з.п.ф-лы, 5 ил., 1 табл.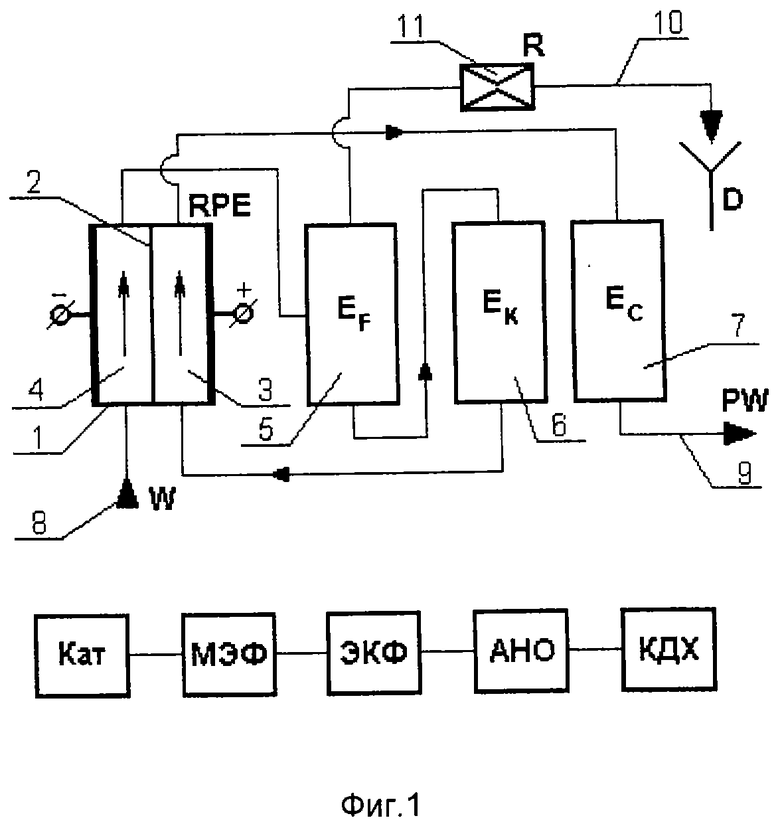
| УСТАНОВКА ДЛЯ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ И ОЧИСТКИ ВОДЫ И/ИЛИ ВОДНЫХ РАСТВОРОВ | 1996 |
|
RU2091320C1 |
| УСТАНОВКА ДЛЯ ЭЛЕКТРОХИМИЧЕСКОЙ ОЧИСТКИ ВОДЫ И/ИЛИ ВОДНЫХ РАСТВОРОВ | 1996 |
|
RU2096337C1 |
| US 5427667 А1, 27.06.1995 | |||
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| ЕР 0100538 А, 15.02.1984. | |||
Авторы
Даты
2003-07-10—Публикация
2001-07-05—Подача