Изобретение относится к медицине, в частности к фармакологии, и касается лекарственной композиции, обладающей цереброваскулярным и нейропротекторным действием, которая может применяться для лечения ишемических поражений мозга.
Известно, что пусковыми факторами ишемического поражения являются снижение мозгового кровотока, нейротоксичность, внутриклеточное накопление кальция, активация внутриклеточных ферментов, повышение синтеза оксида азота и развитие оксидативного стресса.
В настоящее время для лечения больных с ишемическим инсультом и другими ишемическими поражениями мозга применяются блокаторы кальциевых каналов нимодипин и циннаризин, а также кавинтон (М.Д. Машковский, 2000, Д.А. Харкевич, 1999). Указанные соединения недостаточно эффективны при лечении больных в остром периоде ишемического поражения. Вместе с тем выраженный в различной степени гипотензивный эффект цереброваскулярных препаратов существенно ограничивает их применение в этом периоде, так как понижение перфузионного давления вызывает дальнейшее уменьшение церебральной гемодинамики.
Выявление роли глутаматных рецепторов в развитии нейротоксичности способствовало расширению наших представлений о патогенезе ишемического инсульта и направленному поиску средств для лечения этого заболевания. Однако блокаторы глутаматных, в особенности NMDA-рецепторов, такие как дизоцилпин (МК-801) и другие, не получили применения в клинической практике. Это связано с тем, что клинические испытания этих соединений выявили их нежелательные психотропные эффекты.
Анализ современной литературы, посвященной фармакологической регуляции ишемических поражений мозга, указывает на два основных направления в лечении ишемических поражений мозга: улучшение мозгового кровообращения и нейропротекторное действие.
Вышеизложенное свидетельствует о необходимости разработки новых эффективных препаратов с цереброваскулярной и нейропротекторной активностью.
Сущность изобретения заключается в создании лекарственной композиции, состоящей из известных веществ - пироглутаминовой кислоты и пирролидона. Основанием для создания указанной композиции явились результаты исследования каждого из компонентов лекарственной композиции на кровоснабжение и метаболизм мозга. Показано, что наиболее выраженное влияние на мозговое кровообращение оказывает пирролидон, который увеличивает церебральную гемодинамику, понижает тонус сосудов мозга. Пироглутаминовая кислота оказывает более выраженное положительное влияние на энергетический обмен мозга. Лекарственная композиция, состоящая из пироглутаминовой кислоты и пирролидона обладает цереброваскулярным и нейропротекторным действием в условиях ишемического поражения мозга. Установлен выраженный терапевтический эффект лекарственной композиции у крыс с локальной ишемией мозга при использовании в соотношении 1:1. Необходимо отметить, что при изменении соотношения в композиции каждого из компонентов ее положительное влияние на неврологический компонент ослабевает.
Фармакологическая активность лекарственной композиции исследовалась по тестам, принятым для оценки цереброваскулярной и нейропротекторной активности ("Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ", Москва, 2000). При этом изучалось влияние лекарственной композиции и ее отдельных фрагментов на церебральную гемодинамику и состояние сердечно-сосудистой системы. Исследовано влияние пироглутаминовой кислоты и пирролидона на метаболизм ткани мозга. В частности, регистрировали влияние указанных веществ на захват и утилизацию глюкозы срезами и гомогенатами мозга, на активность сукцинат- и лактатдегидрогеназ ткани мозга. Изучено влияние указанной композиции на неврологический дефицит и морфологические изменения ткани мозга в условиях локальной ишемии мозга, вызванной перевязкой средней мозговой артерии.
В качестве препарата сравнения при изучении фармакологической активности использован нимодипин, который обладает выраженной цереброваскулярной активностью и широко применяется в неврологической практике (Д.А. Харкевич "Фармакология", 1999, М.Д. Машковский "Лекарственные средства", 2000).
Для изучения мозгового кровообращения использовались следующие методики: количественного определения локального кровотока с помощью водородного клиренса, определение состояния микроциркуляции в коре головного мозга лазерным допплеровским флоуметром ALF-21 ("Transonic Systems Inc.", США), регистрация притока крови в мозг с помощью ультразвукового расходомера Т-106 ("Transonic Systems Inc.", США).
Опыты, проведенные на крысах и кошках, позволили установить, что лекарственная композиция обладает способностью существенно усиливать кровоснабжение мозга. Необходимо отметить, что пирролидон в большей степени по сравнению с пироглутаминовой кислотой понижает тонус церебральных сосудов, увеличивает объемную скорость мозгового кровотока.
Исходя из того что как пироглутаминовая кислота, так и пирролидон принимают участие в обменных процессах мозга, представляло интерес исследовать влияние указанных веществ на метаболизм ткани мозга. Для этой цели изучалось влияние пироглутаминовой кислоты и пирролидона на захват и утилизацию глюкозы срезами и гомогенатами мозга, а также на активность сукцинат- и лактатдегидрогеназ в ткани мозга. Проведенные опыты позволили установить, что пироглутаминовая кислота и в меньшей степени пирролидон стимулируют захват глюкозы мозговой тканью и одновременно усиливают ее окисление до углекислоты и воды. Следовательно, указанные соединения оказывают стимулирующее влияние на энергетический обмен мозга.
Пироглутаминовая кислота и, в меньшей степени, пирролидон повышают активность сукцинатдегидрогеназы. Что касается лактатдегидрогеназы, то исследованные соединения у интактных животных понижают активность указанного фермента. Вместе с тем в условиях ишемии мозга, вызванной перевязкой общей сонной артерии, пироглутаминовая кислота и пирролидон повышают активность лактатдегидрогеназы. Следовательно, указанные соединения в условиях ишемии и недостатка кислорода стимулируют анаэробный гликолиз, поддерживая на необходимом уровне энергетический обмен ткани мозга.
Вышеизложенное явилось основанием для комбинированного применения пироглутаминовой кислоты и пирролидона в условиях локальной ишемии мозга, вызванной перевязкой средней мозговой артерии.
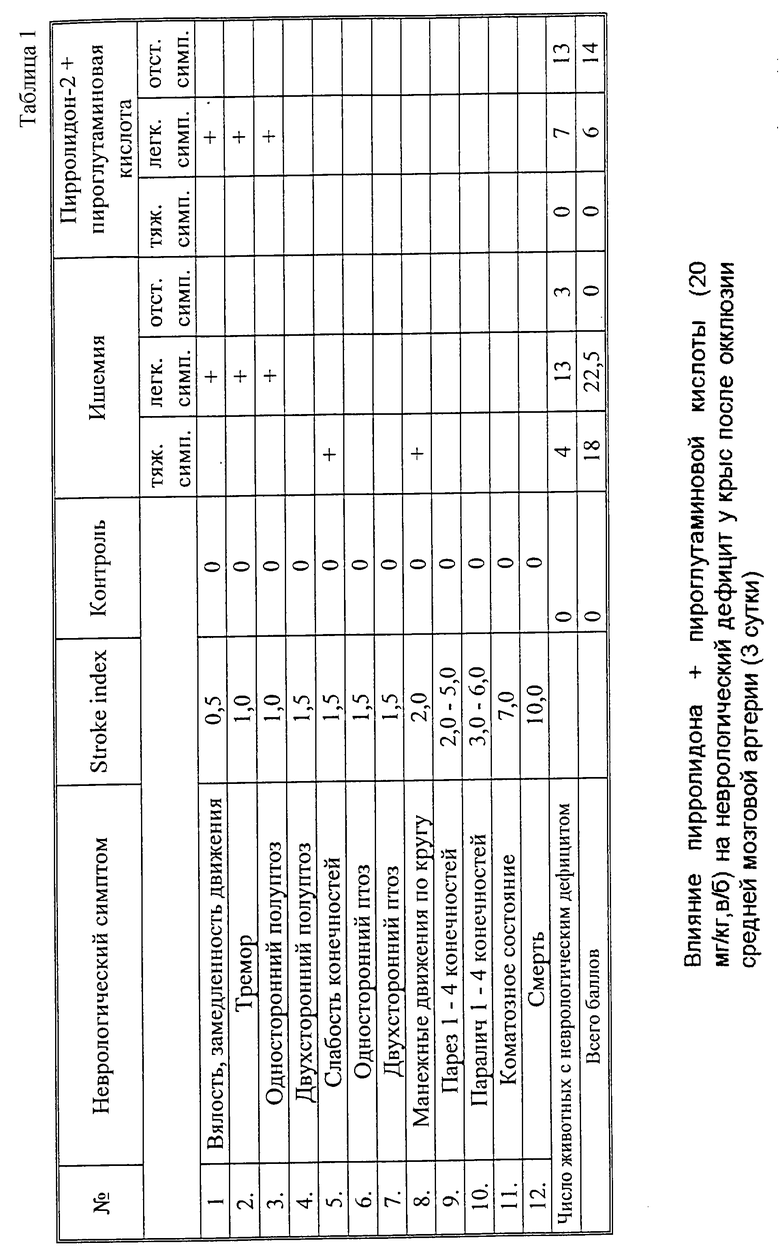
Изучение неврологического дефицита по Mc Grow показало, что лекарственная композиция, состоящая из пироглутаминовой кислоты и пирролидона по 20 мг/кг, внутрибрюшинно два раза в день после окклюзии средней мозговой артерии в первые сутки не вызывает тяжелых симптомов неврологического дефицита (в контроле 20%), у 55% животных наблюдался неврологический дефицит средней тяжести (контроль 65%) и у 45% животных симптомы неврологического дефицита отсутствовали (контроль 15%). На 3 сутки после лечения животных указанной лекарственной композицией наблюдалось уменьшение симптомов средней тяжести до 35% и увеличение до 65% животных с отсутствием симптомов неврологического дефицита. На 6 и 9 сутки у леченых животных это соотношение достигло 30% и 70% соответственно соответственно (см. чертеж).
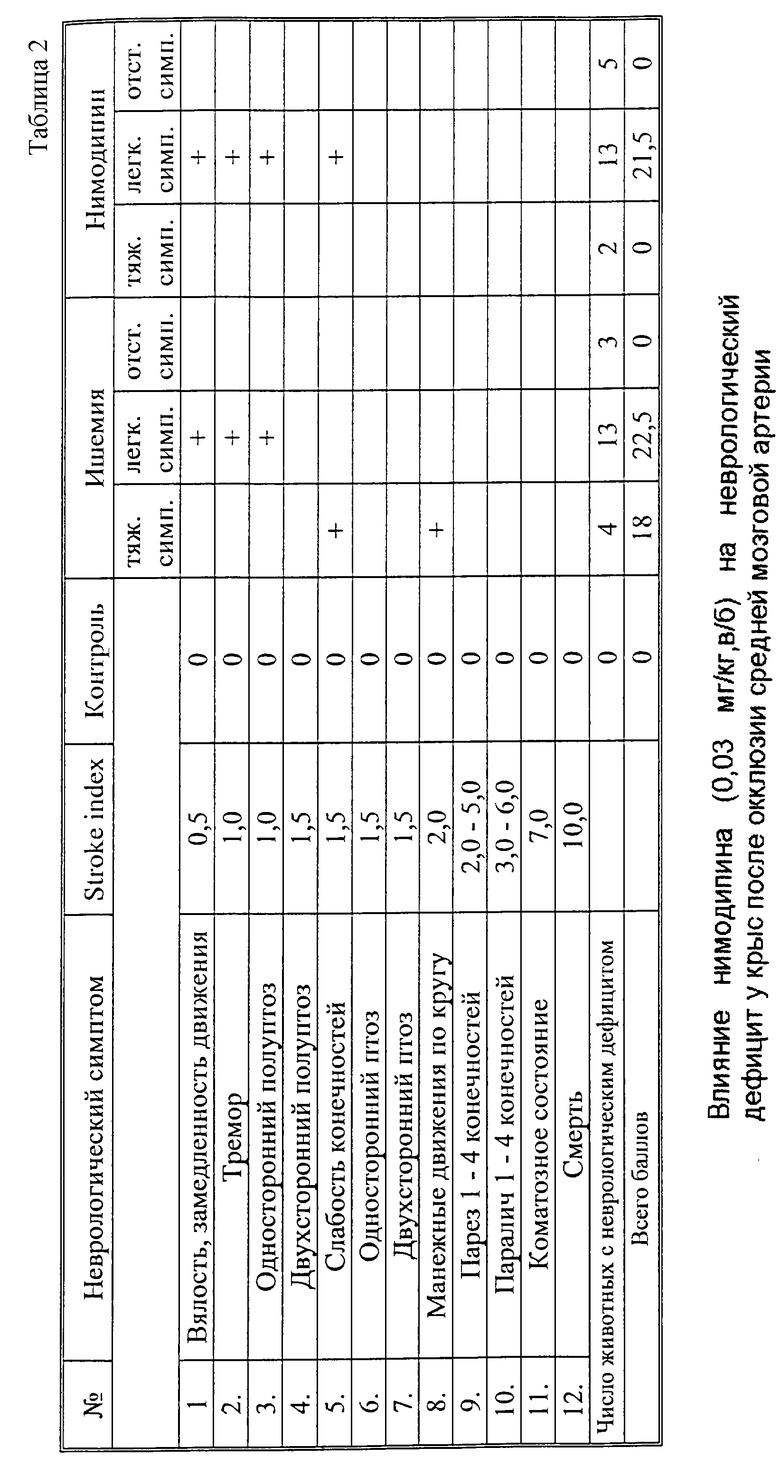
Следует отметить, что соотношение процента животных с явлениями неврологического дефицита у контрольных животных с локальной ишемией мозга в течение 9 суток не претерпевало существенных изменений. Как уже отмечалось выше, в качестве препарата сравнения использовали блокатор кальциевых каналов нимодипин. Поэтому в серии опытов изучили влияние нимодипина в дозе 0,03 мг/кг внутрибрюшинно два раза в день после перевязки средней мозговой артерии. Проведенные опыты показали, что в отличие от лекарственной композициии нимодипин не оказывал влияния на неврологический статус животных, нарушенный после окклюзии средней мозговой артерии (табл. 1, 2).
Далее исследовалось влияние лекарственной композиции на динамику морфологических изменений тканей головного мозга через 6 и 30 суток после необратимой окклюзии левой средней мозговой артерии.
На 6 сутки после необратимой окклюзии левой средней мозговой артерии и введения крысам лекарственной композиции, состоящей из пироглутаминовой кислоты и пирролидона, в дозах по 20 мг/кг внутрибрюшинно два раза в день отмечаются выраженные процессы организации. Участок коагуляционного некроза весьма ограниченный, но по периметру его замечается спонгиоз, умеренный глиоз и обильное количество сосудистых почек. В новообразованных сосудах выявляются форменные элементы крови, т.е. происходит ранняя реваскуляризация (реперфузия) зоны ишемии. Во всех случаях отмечается хорошая сохранность ипсилатеральной хвостатого ядра (Срu). В ипсилатеральном полушарии, вне зоны некроза, нейроциты хорошо сохранены, повреждения проявляются в виде наличия единичных гиперхромных, пикнотичных нейроцитов. Сохранные нейроциты характеризуются высоким содержанием рибонуклеопротеина и белка. На всем протяжении, в том числе и над зонами ишемического некроза, мягкая мозговая оболочка тонкая, нежная. Пиальные сосуды содержат умеренное количество форменных элементов крови.
На 30 сутки после необратимой окклюзии левой средней мозговой артерии на фоне применения лекарственной композиции только в одном случае из 15 замечаются умеренно выраженные спонгиоз и глиоз межпучковой ткани и нерезко выраженная деструкция пучков ипсилатеральной Срu. Во всех остальных случаях Срu хорошо сохранена. Лишь в двух случаях из 15 обнаруживается организация ишемического некроза коры в области 1 и 2 теменной коры (Par, Par) и латерального зрительного тракта (lо). Зона организации имеет вид четко ограниченного участка спонгиоза и рыхлой глиальной реакции. В зоне выявляется большое количество функционирующих сосудов и сосудистых почек. По периметру зон организации обнаруживаются хорошо сохранные нейроциты. В отличие от нелеченных животных пикноморфные и ишемические гомогенизирующие изменения нейроцитов превалируют в ипсилатеральном поле 1,2 поясной коры (Cg1, Cg2), в то время как в симметричных контралатеральных участках коры замечается хорошая сохранность нейроцитов. Нейроциты базальных и гипоталамических ядер хорошо сохранены в обоих полушариях и характеризуются наличием крупнодисперсного хроматофильного вещества, равномерно распределенного по всей цитоплазме. Во всех случаях, в том числе с наличием участков организации ишемического некроза коры, мягкая мозговая оболочка тонкая, нежная, с нерезко выраженным полнокровием пиальных вен.
Во всех случаях как через 6 суток, так и спустя 30 суток в головном мозге леченых животных не обнаруживались признаки дистонии сосудов и извилистости хода артерий коры.
Результаты проведенных исследований по изучению влияния сочетанного применения лекарственной композиции свидетельствуют об их выраженном защитном (протективном) эффекте на структурные компоненты головного мозга крыс с локальной необратимой окклюзией средней мозговой артерии. В первую очередь следует отметить хорошую сохранность Срu, т.е. стриопаллидарной системы мозга крыс, которая более всего страдала у крыс с перевязкой средней мозговой артерии. Кроме того, под влиянием лекарственной композиции зона ишемического некроза коры четко ограничена (пенубра практически отсутствует) и характеризуется ранней реперфузией.
Необходимо отметить, что под влиянием исследуемой лекарственной композиции происходит нормализация мозгового кровообращения в обоих полушариях. Можно полагать, что лекарственная композиция оказывает влияние на нейротрансмиттерную систему, в результате чего предотвращаются расстройства мозгового кровообращения в виде дистонии, полнокровия и тромбоза мозговых сосудов, развитие "васкулитов".
Следовательно, лекарственная композиция, представляющая собой сочетание пироглутаминовой кислоты с пирролидоном-2, оказывает выраженный защитный эффект на все структурные компоненты головного мозга крыс при его локальной ишемии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИШЕМИЧЕСКИХ ПОРАЖЕНИЙ МОЗГА | 2004 |
|
RU2288714C2 |
| СРЕДСТВО, УЛУЧШАЮЩЕЕ КРОВОСНАБЖЕНИЕ ИШЕМИЗИРОВАННОГО МОЗГА | 2019 |
|
RU2747202C2 |
| ИНЪЕКЦИОННАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ЛЕЧЕНИЯ ОСТРОГО ИНСУЛЬТА, СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ И ПРИМЕНЕНИЕ | 2005 |
|
RU2330680C2 |
| Эфиры янтарной кислоты 5-гидроксиадамантан-2-она, улучшающие кровоснабжение ишемизированного мозга | 2017 |
|
RU2658833C1 |
| АНТИГИПОКСИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИШЕМИЧЕСКИХ НАРУШЕНИЙ МОЗГОВОГО КРОВООБРАЩЕНИЯ | 1990 |
|
RU2016579C1 |
| НЕЙРОПРОТЕКТОРНОЕ СРЕДСТВО | 2009 |
|
RU2406488C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ S-АМЛОДИПИНА НИКОТИНАТ И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ЦЕРЕБРОВАСКУЛЯРНЫХ НАРУШЕНИЙ | 2012 |
|
RU2516922C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ИШЕМИИ ГОЛОВНОГО МОЗГА С ЯВЛЕНИЯМИ МЕЖПОЛУШАРНОЙ АСИММЕТРИИ | 1993 |
|
RU2083000C1 |
| ПРИМЕНЕНИЕ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ, СОДЕРЖАЩЕЙ ХОЛИНА АЛЬФОСЦЕРАТ И 2-ЭТИЛ-6-МЕТИЛ-3-ГИДРОКСИПИРИДИНА СУКЦИНАТ, В КАЧЕСТВА НЕЙРОПРОТЕКТОРНОГО СРЕДСТВА ПРИ ИШЕМИИ ГОЛОВНОГО МОЗГА | 2023 |
|
RU2819828C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НЕЙРОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ В УСЛОВИЯХ ИШЕМИЧЕСКОГО НАРУШЕНИЯ МОЗГОВОГО КРОВООБРАЩЕНИЯ | 2015 |
|
RU2586301C1 |
Изобретение может быть использовано в медицине для лечения ишемического поражения мозга, в частности, как лекарственная композиция, состоящая из пироглутаминовой кислоты и пирролидона. Лекарственная композиция улучшает кровообращение и обменные процессы в ткани мозга. 1 з.п. ф-лы, 1 ил., 2 табл.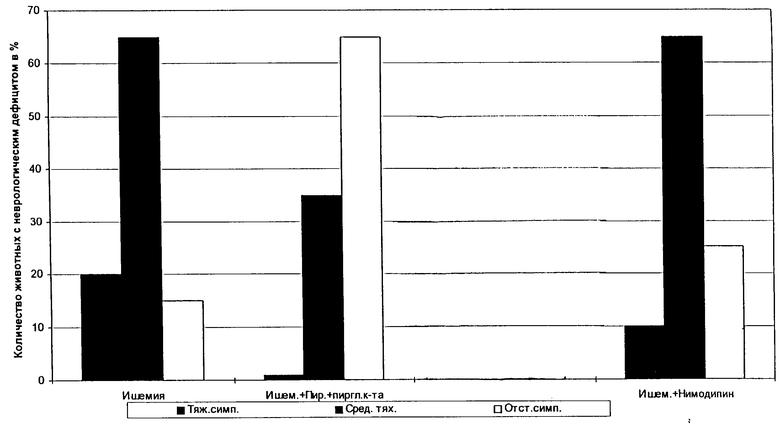
| СПОСОБ ПОЛУЧЕНИЯ ЭНАНТИОМЕРНО ЧИСТЫХ СОЕДИНЕНИЙ ИМИДАЗОЛИЛА, ЭНАНТИОМЕРНО ЧИСТАЯ КИСЛАЯ АДДИТИВНАЯ СОЛЬ ИМИДАЗОЛИЛА И D- ИЛИ L-ПИРОГЛУТАМИНОВОЙ КИСЛОТЫ, МОНОГИДРАТ ГИДРОХЛОРИДА ЭНАНТИОМЕРНО ЧИСТЫХ СОЕДИНЕНИЙ ИМИДАЗОЛИЛА | 1996 |
|
RU2162085C2 |
| СРЕДСТВО ДЛЯ СНИЖЕНИЯ АЛКОГОЛЬНОГО ОПЬЯНЕНИЯ, ПРЕДУПРЕЖДЕНИЯ И СНЯТИЯ АЛКОГОЛЬНОЙ ИНТОКСИКАЦИИ И ПОХМЕЛЬНОГО СИНДРОМА И СПОСОБ СНИЖЕНИЯ АЛКОГОЛЬНОГО ОПЬЯНЕНИЯ, ПРЕДУПРЕЖДЕНИЯ И СНЯТИЯ АЛКОГОЛЬНОЙ ИНТОКСИКАЦИИ И ПОХМЕЛЬНОГО СИНДРОМА С ИСПОЛЬЗОВАНИЕМ ЭТОГО СРЕДСТВА | 2000 |
|
RU2160589C1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| КРЫЛОВ Ю.Ф | |||
| Энциклопедия лекарств | |||
| - М.: изд | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
Авторы
Даты
2003-10-10—Публикация
2001-03-14—Подача