Изобретение относится к медицине, а именно к педиатрии, и может найти применение для оценки состояния здоровья детей, проживающих в районах с высокой экологической нагрузкой тяжелыми металлами.
В частности, способ предназначен для прогнозирования экологически детерминированной патологии почек у детей, а также направлен на оценку вероятности возникновения патологии почек, обусловленную экологическими факторами (ксенобиотическое воздействие тяжелых металлов).
В связи с ухудшением экологической ситуации и изменениями среды обитания человека возникла проблема экологической патологии как следствия воздействия физических, биологических и химических факторов. Важнейшую опасность для здоровья представляет загрязнение биосферы химическими соединениями, обладающими токсическими, мутагенными и канцерогенными свойствами. Экологический риск, т.е. опасность разрушительного воздействия на человека и окружающую среду, способствует отрицательному воздействию на здоровье прежде всего детского населения (1). Состояние детского здоровья - весьма чувствительный индикатор экологического неблагополучия. Химические агенты, поступающие в организм ребенка с воздухом, водой, пищей, воздействуют на различные системы организма. В экологически неблагополучных территориях статистически достоверно повышена частота хронической патологии органов мочевой системы, дыхания и пищеварения (2).
В силу функциональных и анатомических особенностей почки являются одним из основных органов - мишеней для действия ксенобиотиков, особенно тяжелых металлов. Высокой нефротоксичностью обладают такие металлы, как кадмий, ртуть, свинец, хром, мышьяк, железо, висмут, бор, литий, что связано с их способностью депонироваться в паренхиматозных органах, особенно в корковом веществе почки (7). Имеются данные о том, что влияние тяжелых металлов приводит к формированию нефропатий, фенотипически проявляющихся в виде различных симптомокомплексов: дизметаболической нефропатий, тубулоинтерстициального нефрита, пиелонефрита, мочекаменной болезни, синдрома Фанкони (2). Экологический прессинг, связанный с накоплением солей тяжелых металлов (стронция, хрома, свинца, кадмия) является важнейшим фактором формирования нефропатий в условиях высокой нагрузки тяжелыми металлами (1, 3).
Возможность диагностики эконефропатий существует. Она основана на выявлении наличия в регионах высокого уровня экотоксикантов в окружающей среде и, соответственно, высоком уровне патологии органов мочевой системы, по сравнению с общепопуляционными данными; увеличении частоты заболеваний почек у детей, проживающих в непосредственной близости от места производства, загрязняющего среду обитания, по сравнению с районами без промышленных объектов; увеличении частоты патологии с возрастом; наличии у большинства обследуемых сходной клинико-лабораторной характеристики поражения почек, а также выявлении множественных стигм дизэмбриогенеза, анатомических аномалий органов мочевой системы; наличии у большинства больных мембранопатологического процесса. Кроме того, имеет диагностическое значение наличие повышенной экскреции с мочой тяжелых металлов и гиперчувствительность к ним (реакция лейкоцитолиза), выявление морфологических изменений в почечной ткани при гистологическом исследовании нефробиоптатов в виде тубулоинтерстициального нефрита, признаков почечного дизэмбриогенеза (4, 5).
Существует беспороговая модель действия низких концентраций ксенобиотиков, при этом доказано, что опасны даже малые концентрации и дозы, но для контингентов, проявляющих повышенную чувствительность к конкретным химическим агентам. По мере повышения концентраций ксенобиотиков возрастает число детей в популяции, реагирующих на их присутствие (2). При массовом развитии экопатологии оценивается индивидуальная чувствительность организма ребенка на воздействие неблагоприятных экологических факторов, для чего используется определяемая in vitro реакция лейкоцитолиза (6, 7).
Ранняя диагностика экологически детерминированной патологии почек (ЭДПП) традиционными методами вызывает определенные сложности.
Существующие критерии диагностики, указанные выше, основаны на демографических показателях, клинической идентичности симптомов патологии почек, некоторых общепринятых в нефрологии лабораторных показателях. При этом диагностика экологически детерминированных нефропатий затруднена в связи с проблемой непосредственного обнаружения тяжелых металлов в почечной ткани как истинного этиологического фактора. Исследование почечной ткани без выявления депонированных в паренхиме тяжелых металлов методом нефробиопсии не решает этого вопроса, поскольку подтверждает лишь возможное следствие опосредованного воздействия тяжелых металлов на организма ребенка. Метод нефробиопсии проводится по строгим показаниям, дорогостоящ и требует согласия на проведение со стороны родителей. Другие методы, в частности лабораторной диагностики, выявляют общие тенденции в нарушении здоровья, в том числе и в мочевой системе в виде мембранопатологических процессов, нарушения перекисного окисления липидов, подтверждая патологические изменения в почечной ткани, не указывая на детерминированность заболевания экологическими факторами.
Кроме того, при обследовании детей с нефропатиями не учитываются индивидуальные особенности реакции организма ребенка на длительное ксенобиотическое воздействие тяжелыми металлами с позиций “стресс-реакции”, развивающейся в организме в ответ на неадекватное влияние химических факторов в виде нарушения системы “гипоталамус-гипофиз-надпочечники” (10).
Применяемая реакция лейкоцитолиза (7) проста в исполнении. Это микрометод, предусматривающий использование малого количества венной крови, основанный на учете количества лизированных клеток при действии специфического фактора. Авторы используют этот метод в качестве прототипа. Однако проба на лейкоцитолиз не позволяет количественно определить степень выраженности сенсибилизации у детей, подвергшихся воздействию ксенобиотиков, что существенно затрудняет динамическое наблюдение и контроль за лечением экологически детерминированной патологии почек.
Существующие методы обследования детей направлены на уже больного ребенка, у которого имеются изменения в почках, патологический мочевой синдром. При этом дети группы риска (с наследственной отягощенностью по патологии органов мочевой системы, наличием профессиональных вредностей, связанных с контактом с тяжелыми металлами на производстве родителей, со стажем проживания в регионе с высокой экологической нагрузкой тяжелыми металлами более пяти лет) не наблюдаются с позиций ранней диагностики экопатологии, приводящей к нарушению в различных органах и системах, в том числе и в органах мочевой системы. Возникают определенные трудности в наблюдении этой группы детей в силу отсутствия единого прогностического алгоритма.
Новизной предлагаемого способа является прогнозирование патологии почек у детей группы риска, проживающих в регионе с высокой нагрузкой тяжелыми металлами, в основу которого положен комплексный подход с позиций оценки активности гормонов надпочечников (кортизола) в условиях “химического стресса”, степени выраженности сенсибилизации к тяжелым металлам с учетом их накопления в биосредах (волосы, моча) у здоровых детей из группы риска по экопатологии, длительно проживающих в регионе с высокой нагрузкой тяжелыми металлами.
Существенные отличия способа заключаются в том, что при повышении цитотоксического индекса к тяжелым металлам свыше 0,15 и снижении уровня кортизола в сыворотке крови более чем в два раза в сочетании с накоплением нефротоксичных тяжелых металлов в биосредах и подсчетом суммы диагностических коэффициентов, равной результату алгоритма +70 и более, судят о риске формирования патологии почек у детей.
У детей группы риска, проживающих более пяти лет в регионе с высокой экологической нагрузкой тяжелыми металлами, необходимо определить их содержание в биосредах (волосах, моче) атомно-эмиссионным методом. При накоплении тяжелых металлов в биосредах определяется степень сенсибилизации к каждому металлу по реакции повреждения гранулоцитов с подсчетом цитотоксического индекса. При выявлении высокой степени сенсибилизации (цитотоксический индекс свыше 0,15), исследуют уровень гормонов “химического стресса” - кортизола в сыворотке крови методом иммуноферментного анализа.
Для определения прогностических критериев проведена оценка информативности комплекса анамнестических и кпинико-лабораторных показателей с использованием меры Кульбака (11). В результате проведенного анализа установлена информативность каждого признака, отобраны наиболее информативные из них и рассчитаны диагностические коэффициенты.
С учетом дифференцирующего порога для суммы диагностических коэффициентов (+70 и более) определяется риск возможного возникновения экологически детерминированной патологии почек. Наиболее информативные признаки составляют алгоритм прогнозирования патологии почек у детей, проживающих в регионе с высокой экологической нагрузкой тяжелыми металлами (см. таблицу).
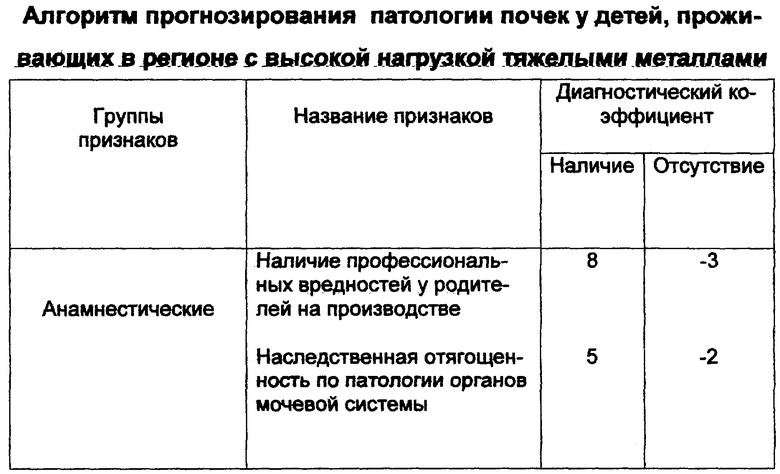
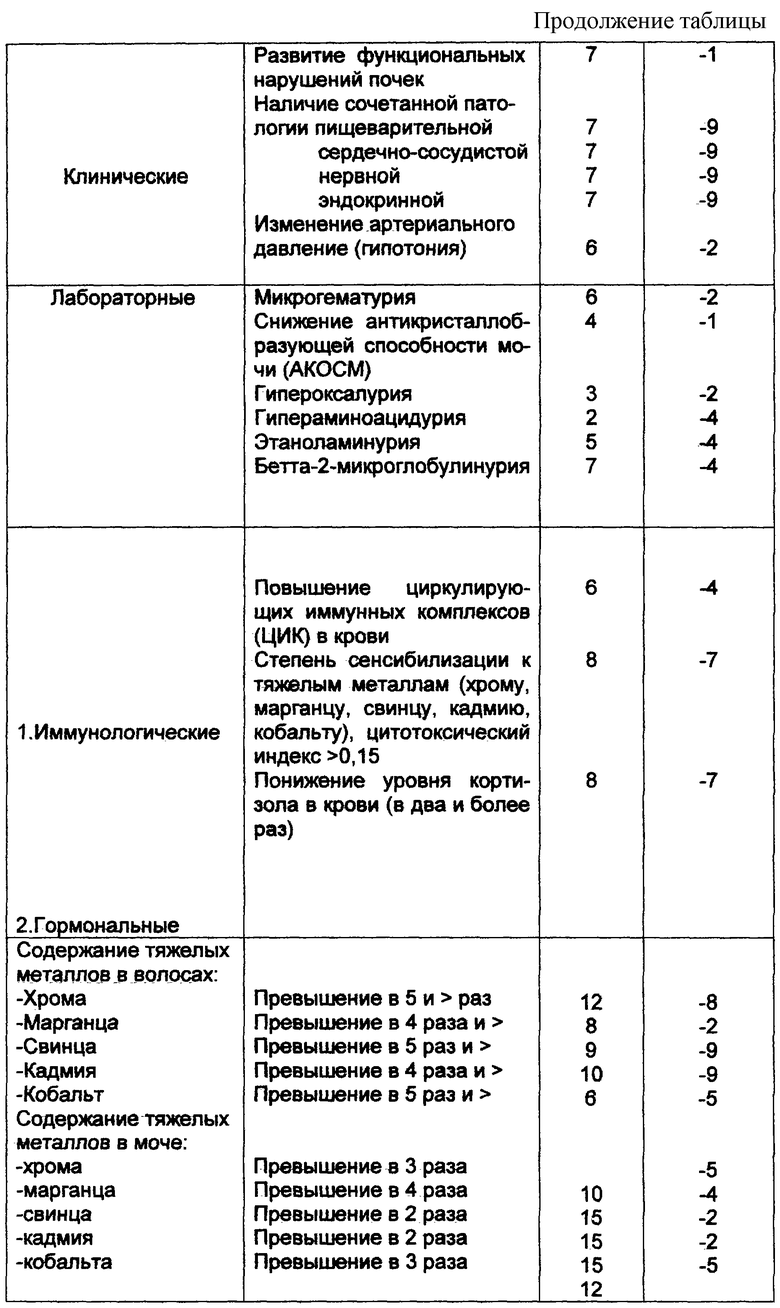
Для определения вероятности прогноза патологии почек, обусловленных экологическими факторами, необходимо суммировать диагностические коэффициенты (ДК).
Оценка. 1. При определении у ребенка суммы баллов ДК более или равную +70 результат алгоритма расценивается как высокая (87%) вероятность экологически детерминированной патологии почек.
Использование прогностического алгоритма позволяет существенно упростить наблюдение детей из группы риска по экопатологии, с высокой вероятностью ранней диагностики отклонений в состоянии органов мочевой системы. Кроме того, данный способ прогнозирования эконефропатий позволит в дальнейшем провести своевременную программу медико-экологической реабилитации и предупредить развитие и прогрессирование патологии органов мочевой системы у детей, длительно проживающих в регионе с высокой нагрузкой тяжелыми металлами.
Пример №1. Больная М., 13 лет, наблюдается в детской поликлинике г.Новотроицка с рождения.
Анамнестические данные: наличие профессиональных вредностей на производстве отца (контакт со свинцовыми добавками) (8 баллов); клинически выявлено наличие тубулярной дисфункции почек (7 баллов), патология со стороны пищеварительной системы - гепатоз, эрозивный гастродуоденит (7 баллов), артериальная гипотония (6 баллов); лабораторные изменения в виде персистирующей гематурии (6 баллов), снижения АКОСМ (4 балла), бетта-2-микроглобулинемия (7 баллов) повышение ЦИК (6 баллов), цитотоксический индекс к хрому составляет 0,23, марганцу 0,33, свинцу 0,50, кадмию 0,82, кобальту 0,65 (8 баллов). Выявлено снижение уровня кортизола в сыворотке крови в 3,2 раза по сравнению с возрастной нормой (8 баллов). Содержание тяжелых металлов в волосах: превышение содержания хрома в 11 раз по сравнению с нормой (12 баллов), марганца - в 2 раза (- 2 балла), свинца в 5 раз (9 баллов), кадмия - в 5 раз (10 баллов), кобальта - в 6,5 раз (6 баллов). Содержание ТМ в моче: хрома - в 12 раз (10 баллов), марганца - в 3 раза (- 4 балла), свинца - в 5 раз (15 баллов), кадмия - в 4 раза (15 баллов), кобальта - в 4 раза (12 баллов).
Оценка результатов обследования: 1. Отсутствие признаков в сумме составляет (- 45) баллов.
2. Присутствие признаков в сумме составляет (+149) баллов.
Итоговая сумма баллов: (+104) балла, т.е. вероятность возникновения эконефропатии высокая. Ребенок должен быть отнесен в группу риска по патологии почек и наблюдаться педиатром совместно с врачом - нефрологом. Показан комплекс профилактических мероприятий.
Пример №2. Больной С., 7 лет, наблюдается у педиатра по месту жительства с рождения (г.Новотроицк). Анамнестические ланные: мать ребенка работает на металлургическом комбинате (8 баллов). Клинические данные: ребенок с признаками церебрастении (7 баллов), артериальной гипотонии (6 баллов). Лабораторные изменения: патологический мочевой синдром в виде микрогематурии (6 баллов), гипераминоацидурия (3 балла), бетта-2-микроглобулинурия (7 баллов). Повышение в крови ЦИК (6 баллов), высокая степень сенсибилизации к свинцу, кадмию, марганцу (8 баллов). Выявлено снижение уровня кортизола в крови в 3,5 раза (8 баллов). Содержание в волосах тяжелых металлов: отмечалось превышение уровня свинца в 7 раз (9 баллов), хрома в 5 раз (12 баллов), марганца в 5 раз (8 баллов). В моче выявлено повышенное содержание хрома в 5 раз (10 баллов), свинца (15 баллов), кадмия (15 баллов), кобальта (12 баллов).
Оценка результатов обследования: 1. Отсутствие признаков в сумме составляет (- 55) балла.
2. Наличие признаков в сумме составляет (+140) баллов.
Итоговая сумма баллов: (+85), т.е. у данного ребенка риск возникновения патологии почек высокий. Показано наблюдение нефролога и проведение профилактических мероприятий (назначение энтеросорбентов и др. медикаментозных средств).
Таким образом, положительный результат, полученный при использовании заявляемого способа, выступает в виде высокой вероятности прогнозирования патологии органов мочевой системы у детей, длительно проживающих в регионе с высокой нагрузкой тяжелыми металлами. В дальнейшем при выявлении детей с высоким риском развития почечной патологии необходимо проведение превентивных мероприятий, что позволит снизить риск развития и уменьшить прогрессирование эконефропатий. Следовательно, конечным результатом использования заявляемого способа является повышение качества наблюдения детей, проживающих в регионе с высокой нагрузкой тяжелыми металлами, а также уменьшение риска развития патологии органов мочевой системы и ее прогрессирования.
Способ расширяет спектр применения существующих методов обследования детей из экологически неблагополучных регионов, применим в практическом здравоохранении в виду простоты пользования в виде алгоритма прогнозирования с выходом на раннюю диагностику патологии почек у детей.
Преимущества данного способа прежде всего в доступности методов, применяемых при проведении обследования детей группы риска, а также в возможности их использования при массовом обследовании детей, проживающих в регионе с высокой нагрузкой тяжелыми металлами. Способ направлен на оценку вероятности возникновения патологии почек у детей, длительно проживающих в регионе с высокой нагрузкой тяжелыми металлами.
Список литературы
1. Вельтищев Ю.Е., Фокеева В.В. Экология и здоровье детей. Химическая экопатология, Москва, 1996, с.57.
2. Студеникин М.Я, Ефимова А.А. Экология и здоровье детей, Москва, Медицина, 1998, с.384.
3. Османов И.М. Кпинико-патогенетические особенности и тактика лечения поражений почек у детей в экологически неблагополучных регионах // Автореф. дис. д-ра мед. наук, Москва, 1996, 48 с.
4. Макарова Т.П. Роль нарушений обмена микроэлементов на этапах развития нефропатий у детей // Автореф. дис. д-ра мед. наук, Н.Новгород, 2001, 48 с.
5. Игнатова М.С.. Османов И.М., Аксенова М.Е. и соавт. Экологически обусловленные заболевания почек у детей и использование для их лечения препаратов из морских водорослей. Рос. вести, перинатол.и педиатр. 1996; 6:48-53.
6. Османов И.М. Нефропатий у детей из регионов, отягощенных солями тяжелых металлов и пестицидами (патогенез, синдромология, лечение) // Автореф. дис. д-ра мед. наук. М, 1996; 38 с.
7. Юрьева Э.А., Османов И.М., Яковлева И.И., Сафронова О.Н. Цитологические критерии гиперчувствительности к ксенобиотикам у детей. Практическая нефрология, 1998; 2657-58.
8. Аксенова М.Е. Тяжелые металлы: механизмы нефротоксичности (обзор литературы). Нефрология и диализ, 2000; Т.1-2:39-43.
9. Inglis I.A., Henderson D.A., Emmerson B.T. The pathology and pathogenesis of chronic lead nephropaty occurring in Queensland. J. Pathol. 1978; 124; 65-73.
10. Немых В.Н., Пашков А.Н., Неретина А.Ф. Экологическая обусловленность нарушений здоровья у детей (аналитический обзор), Воронеж, 1996, с.115.
11. Гублер Е.В. Вычислительные методы анализа и распознавания патологических процессов. -Л.: Медицина, 1978, с.294.
Изобретение относится к медицине, а именно к педиатрии. Сущность способа: у детей определяют комплекс анамнестических и клинико-лабораторных показателей: наличие профессиональной вредности у родителей на производстве, наследственную отягощенность по патологии органов мочевой системы, развитие функциональных нарушений почек, наличие сочетанной пищеварительной, сердечно-сосудистой, нервной, эндокринной патологии, гипотонии, микрогематурии, снижение антикристаллобразующей способности мочи, гипероксалурии, гипераминоацидурии, этаноламинурии, бетта-2-микроглобулинурии, повышения циркулирующих иммунных комплексов в крови, степень сенсибилизации к тяжелым металлам, понижение уровня кортизола в крови, содержание хрома, марганца, свинца, кадмия и кобальта в волосах и моче, рассчитывают сумму диагностических коэффициентов. При повышении цитотоксического индекса к тяжелым металлам свыше 0,15 и снижении уровня кортизола в сыворотке крови более, чем в 2 раза в сочетании с накоплением нефротоксических тяжелых металлов в биосредах и суммой диагностических коэффициентов, равной +70 и более, определяют риск формирования нефропатий. Способ позволяет своевременно выявить детей с высоким риском развития почечной патологии и провести превентивные мероприятия. 1 табл.
Способ прогнозирования экологически детерминированной патологии почек у детей группы риска, проживающих в регионе с высокой антропогенной нагрузкой тяжелыми металлами, путем определения степени сенсибилизации к тяжелым металлам, отличающийся тем, что определяют комплекс анамнестических и клинико-лабораторных показателей: наличие профессиональной вредности у родителей на производстве, наследственную отягощенность по патологии органов мочевой системы, развитие функциональных нарушений почек, наличие сочетанной пищеварительной, сердечно-сосудистой, нервной, эндокринной патологии, гипотонии, микрогематурии, снижение антикристаллобразующей способности мочи, гипероксалурии, гипераминоацидурии, этаноламинурии, бетта-2-микроглобулинурии, повышения циркулирующих иммунных комплексов в крови, степень сенсибилизации к тяжелым металлам, понижение уровня кортизола в крови, содержание хрома, марганца, свинца, кадмия и кобальта в волосах и моче, рассчитывают сумму диагностических коэффициентов и, при повышении цитотоксического индекса к тяжелым металлам свыше 0,15 и снижении уровня кортизола в сыворотке крови более чем в два раза в сочетании с накоплением нефротоксических тяжелых металлов в биосредах и суммой диагностических коэффициентов, равной +70 и более, определяют риск формирования нефропатий.
| ЮРЬЕВА Э.А | |||
| и др | |||
| Цитологические критерии гиперчувствительности к ксенобиотикам у детей | |||
| Практическая нефрология, 1998, с.2657-2658 | |||
| СПОСОБ ДИАГНОСТИКИ ЭКОЛОГИЧЕСКИ ОБУСЛОВЛЕННОЙ ПАТОЛОГИИ У НАСЕЛЕНИЯ | 1998 |
|
RU2137422C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ДЕЙСТВИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ НА ОРГАНИЗМ | 1997 |
|
RU2138816C1 |
| СПОСОБ ОЦЕНКИ СТЕПЕНИ РИСКА ТОКСИЧЕСКОГО ДЕЙСТВИЯ РТУТИ У ДЕТЕЙ | 1999 |
|
RU2179317C2 |
| СПОСОБ МЕДИКО-СОЦИОЛОГИЧЕСКОЙ ОЦЕНКИ ЗДОРОВЬЯ НАСЕЛЕНИЯ, НЕТРУДОСПОСОБНОГО ПО ВОЗРАСТУ | 2001 |
|
RU2193353C1 |
| ПЕРЕПЕЛКИНА Н.Ю | |||
| Распространенность, структура и факторы риска нефропатий у детей в условиях экологически неблагоприятного региона | |||
| Автореф | |||
| дисс | |||
| канд | |||
| мед.н | |||
| - Оренбург, 1995. | |||
Авторы
Даты
2004-08-20—Публикация
2003-02-12—Подача