Область техники
Изобретение относится к средствам для лучевой терапии злокачественных и незлокачественных новообразований и некоторых других заболеваний.
Предшествующий уровень техники
В настоящее время воздействие ионизирующими излучениями широко применяется для лечения не только злокачественных новообразований, но и доброкачественных опухолей, а также ряда воспалительных и других заболеваний неопухолевого характера (Аспекты клинической дозиметрии. Под ред. Р.В.Ставицкого. Москва, “МНПИ”, 2000 [1]).
Известны устройства для лучевой терапии, содержащие рентгеновский источник, ориентируемый с целью направления создаваемого им излучения в область расположения патологического очага. Для уменьшения облучения здоровых тканей, окружающих патологический очаг, такие устройства могут содержать несколько рентгеновских источников. Создаваемое ими излучение направляется в область расположения патологического очага с разных сторон (Лучевая терапия злокачественных опухолей. Руководство для врачей. Под ред. проф. Е.С.Киселевой. Москва, “Медицина”, 1996 [2]).
Известно также устройство для лучевой терапии, содержащее несколько рентгеновских источников, излучение которых, направляемое в область расположения патологического очага с разных сторон, фокусируется с помощью рентгеновских линз (международная заявка PCT/RU 00/00273, WO 01/29845A1, 26.04.2001 [3]). Благодаря указанному фокусированию излучение каждой из линз, проходя через здоровые ткани, имеет в них меньшую концентрацию, чем в патологическом очаге.
Более радикальным путем уменьшения облучения здоровых тканей, окружающих патологический очаг, является облучение его не извне, а изнутри.
Такой путь реализуется, в частности, путем имплантации непосредственно в патологический очаг капсулы с радиоактивным материалом [2]. Недостатками такого метода являются необходимость хирургического вмешательства и связанная с этим сложность управления продолжительностью облучения.
К предлагаемому устройству наиболее близко известное устройство, реализующее другой путь, предлагаемый в патенте США №5153900 [4] (российский патент - аналог №2155413) и ряде других патентов фирмы Photoelectron Corporation. Это известное устройство имеет зонд для введения непосредственно в патологический очаг или приближения к нему. Зонд в данном устройстве является частью рентгеновской трубки. Ее анод расположен в дистальном конце зонда. Проксимальный конец зонда примыкает к выходу средства для формирования электронного луча, который направлен по продольной оси зонда в сторону анода.
В зонде этого устройства (как и внутри всякой рентгеновской трубки) должен поддерживаться вакуум. Данное обстоятельство в сочетании с необходимостью подачи высокого напряжения на анод, находящийся в дистальном конце тонкого протяженного зонда, и необходимостью контроля положения электронного луча обусловливает конструктивную сложность устройства. При этом энергия излучения определяется, в основном, материалом анода. Невозможность замены анода в вакуумированном зонде приводит к тому, что для каждой желаемой энергии излучения необходимо иметь отдельное устройство. То же самое относится к изменению пространственной диаграммы излучения путем подбора соотношения рентгенопрозрачности различных участков дистального конца зонда. На работу устройства, использующего электронный луч, влияют внешние магнитные поля, что вынуждает принимать меры по соответствующему экранированию. Выполнение зонда как части рентгеновской трубки существенно затрудняет его стерилизацию. Преодоление этого недостатка путем снабжения зонда съемной оболочкой увеличивает его диаметр и связано с повышением травматичности при использовании устройства. Поэтому преимущественной областью применения данного устройства является не требующее пунктирования лечение опухолей полых органов, имеющих непосредственное сообщение с внешней средой, таких как мочевой пузырь, прямая кишка и др. Кроме того, данное устройство, в котором зонд является составной частью рентгеновской трубки, применимо для лечения только рентгеновским излучением.
Раскрытие изобретения
Целью предлагаемого изобретения является получение технического результата, заключающегося в:
- возможности применения для терапии с помощью не только рентгеновского, но и других видов излучений в виде потока нейтральных частиц,
- конструктивном упрощении и удешевлении благодаря исключению использования вакуума и высокого напряжения, исключению средств управления электронным лучом и магнитного экранирования,
- легкой трансформируемости путем замены зонда, в частности, для изменения его размеров, изменения энергии и диаграммы направленности излучения, воздействующего на патологический очаг,
- простоте стерилизации зонда, возможности применения сменных или одноразовых зондов,
- возможности отсоединения зонда от остальной части устройства, сохранения его в теле пациента и использования в это время устройства совместно с другим зондом.
Для достижения названных видов технического результата предлагаемое устройство для лучевой терапии, как и названное выше известное, содержит зонд для введения внутрь тела пациента и приближения его дистального конца к патологическому очагу или введения непосредственно в него, источник излучения и средство формирования пучка частиц этого излучения, ориентированного по продольной оси зонда.
Отличие предлагаемого устройства от известного заключается в том, что указанный источник излучения является источником нейтральных частиц в виде рентгеновских или гамма-квантов либо нейтронов. При этом средство формирования пучка частиц указанного излучения, ориентированного по продольной оси зонда, выполнено в виде коллиматора или линзы, представляющей собой совокупность изогнутых каналов транспортировки излучения с полным внутренним отражением.
При такой конструкции предлагаемого устройства, в отличие от известного, на патологический очаг воздействует непосредственно излучение используемого источника нейтральных частиц, поступающее по тонкому зонду к патологическому очагу или внутрь него. Указанное излучение, несмотря на то, что оно создается источником, находящимся вне тела больного, не воздействует на здоровые ткани, находящиеся на пути к патологическому очагу. Это обеспечивается благодаря распространению их внутри зонда.
Благодаря отсутствию вакуума и высокого электрического напряжения в зонде он может быть выполнен съемным, что делает несложной его стерилизацию. Устройство может быть снабжено набором зондов различных размеров.
Зонд, за исключением его дистального конца или отдельных его участков, может быть выполнен непрозрачным для частиц, создаваемых источником излучения и предназначенных для воздействия на патологический очаг.
Средство для формирования пучка частиц, ориентированного по продольной оси зонда, может быть расположено как вне зонда - между ним и источником нейтральных частиц высоких энергий, так и частично или полностью внутри зонда.
В случае, когда средство для формирования пучка частиц, ориентированного по продольной оси зонда, расположено полностью внутри зонда и представляет собой коллиматор, последний может иметь единственный канал.
В случае, когда средство для формирования пучка частиц, ориентированного по продольной оси зонда, выполнено в виде линзы, представляющей собой совокупность изогнутых каналов транспортировки излучения с полным внутренним отражением, такая линза может быть, в частности, фокусирующей линзой с фокусом, расположенным вне зонда на продолжении его продольной оси. В этом случае фокус находится в теле пациента вблизи или внутри патологического очага.
Указанная линза может быть также линзой для формирования квазипараллельного пучка, проходящего внутри зонда и выходящего из его дистального конца.
В случае, когда источник излучения является рентгеновским источником, последний может быть выполнен с секционированным анодом для оперативного изменения энергии частиц.
В дистальном конце зонда может быть расположена вторичная мишень. В этом случае для лучевого воздействия используется рассеянное вторичной мишенью излучение источника или возбужденное излучение вещества вторичной мишени.
В случае, когда средство для формирования пучка частиц, ориентированного по продольной оси зонда, выполнено в виде линзы, представляющей собой совокупность изогнутых каналов транспортировки излучения с полным внутренним отражением, такая линза может быть, в частности, фокусирующей линзой с фокусом, расположенным на вторичной мишени.
Для изменения характеристик рассеянного и возбужденного в веществе вторичной мишени излучения дистальный конец зонда может быть выполнен разъемным с возможностью смены установленной в нем вторичной мишени. При этом в дистальном конце зонда установлена одна из нескольких входящих в комплект устройства вторичных мишеней, например, выполненных из разных металлов.
Для оперативного изменения желаемой диаграммы направленности излучения, выходящего из дистального конца зонда и воздействующего на патологический очаг, дистальный конец зонда может быть выполнен съемным. В этом случае зонд имеет один из нескольких входящих в комплект устройства дистальных концов, выполненных с различными соотношениями прозрачности участков поверхности дистального конца зонда для рассеянного и возбужденного в веществе вторичной мишени излучения.
С целью обеспечения по завершении лечебной процедуры коагуляции раневого канала, возникшего при осуществлении пункции с помощью зонда, последний может быть выполнен электропроводящим и имеющим снаружи, за исключением наиболее удаленной части дистального конца, изоляционное покрытие. В этом случае зонд должен иметь возможность подключения к электрокоагулятору.
Краткое описание фигур чертежей
Предлагаемые изобретения иллюстрируются чертежами, на которых показаны:
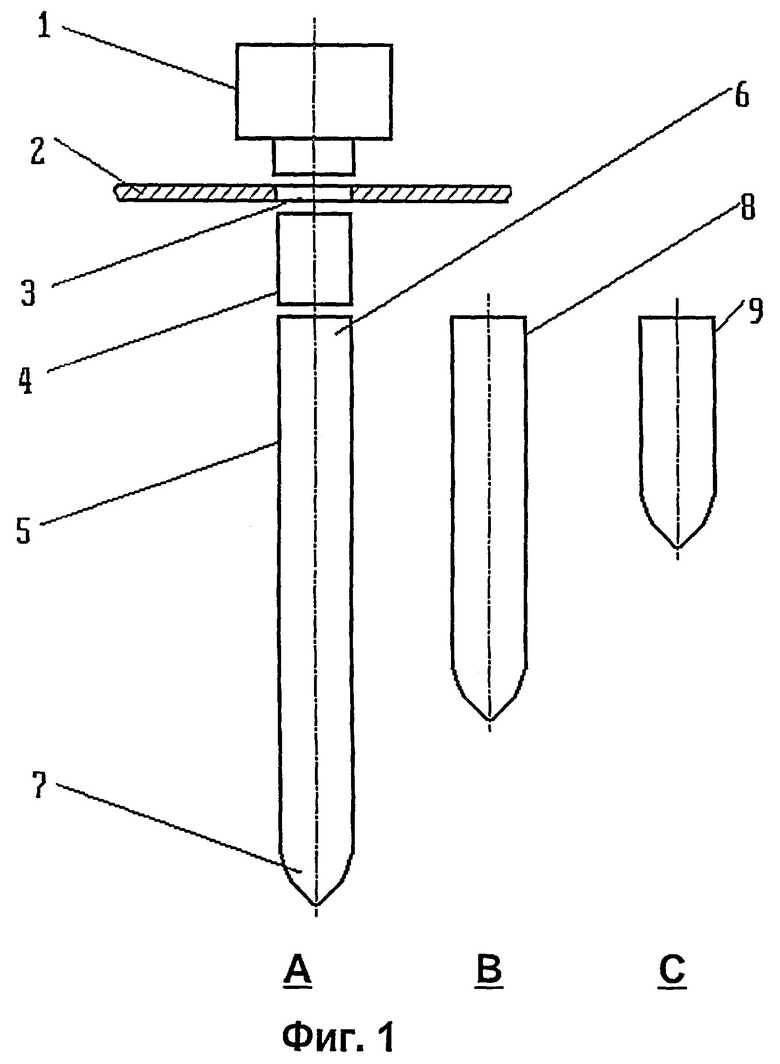
на фиг.1 - схематическое изображение устройства в целом с несколькими прилагаемыми к нему зондами;
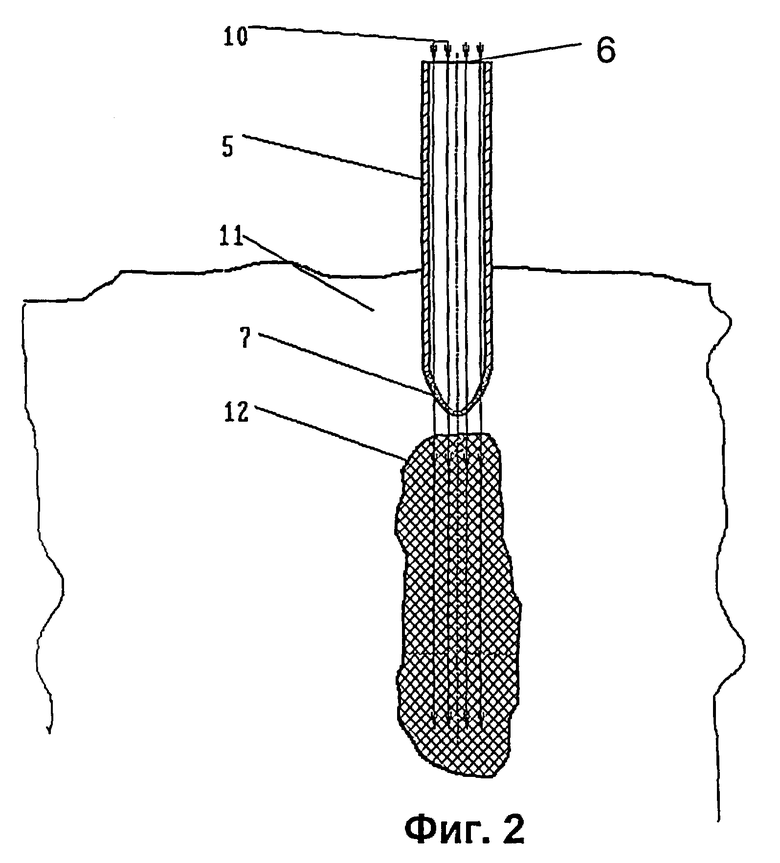
на фиг.2 - использование устройства для облучения протяженной опухоли;
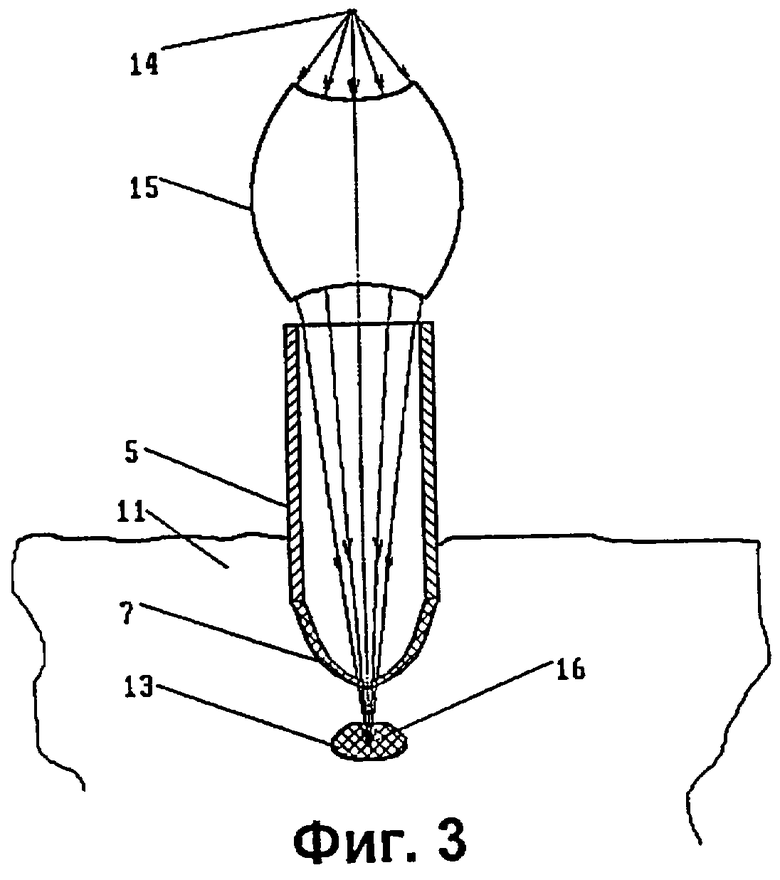
на фиг.3 - использование устройства с расположением линзы вне зонда для облучения небольшой опухоли;
на фиг.4 - расположение линзы частично внутри зонда;
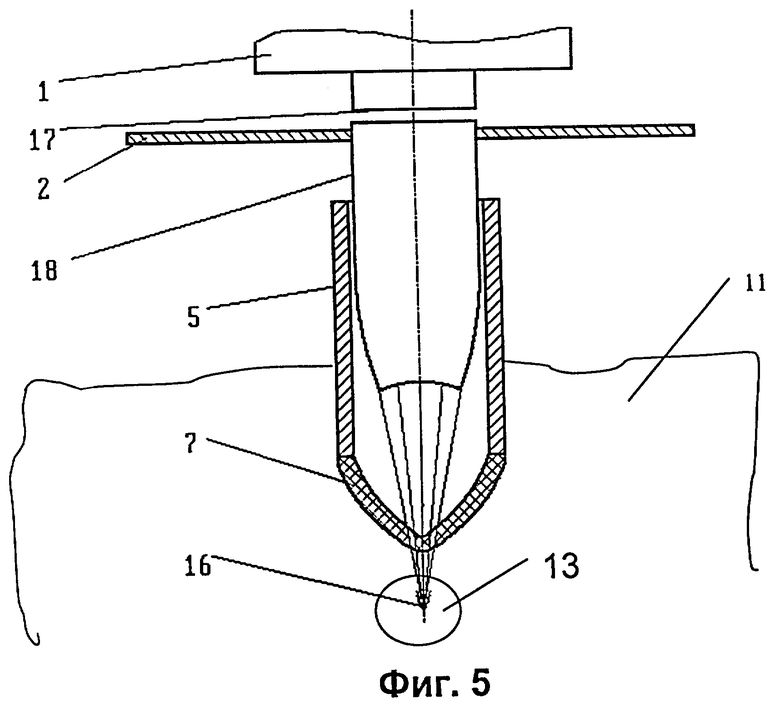
на фиг.5 - устройство с линзой, осуществляющей коллимирование и фокусирование излучения источника;
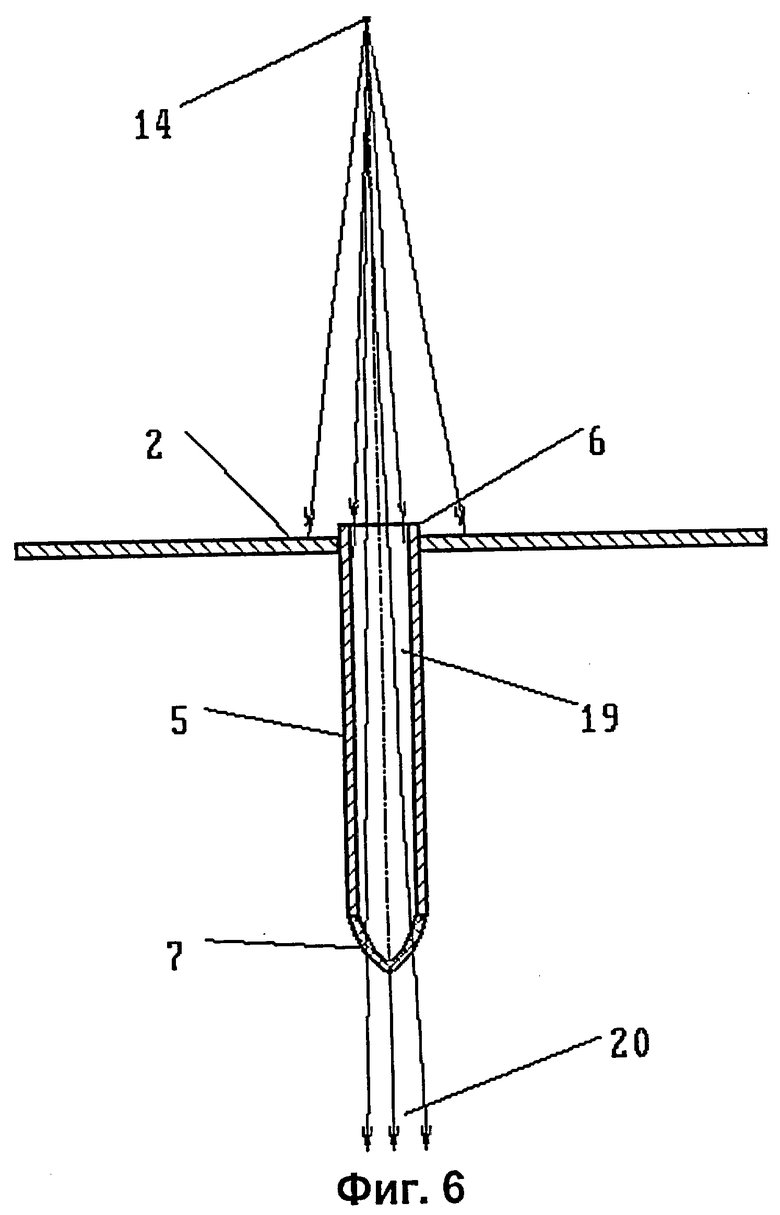
на фиг.6 - зонд, выполняющий одновременно функцию коллиматора с единственным каналом;
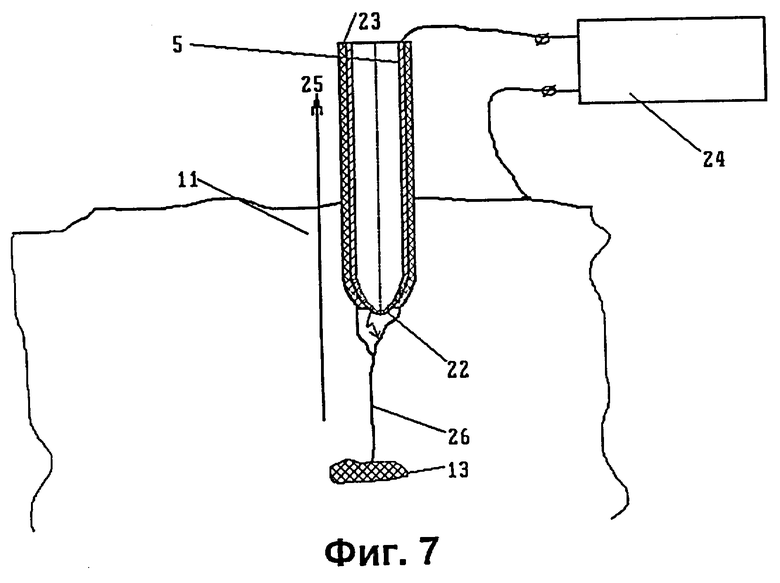
на фиг.7 - использование устройства совместно с коагулятором;
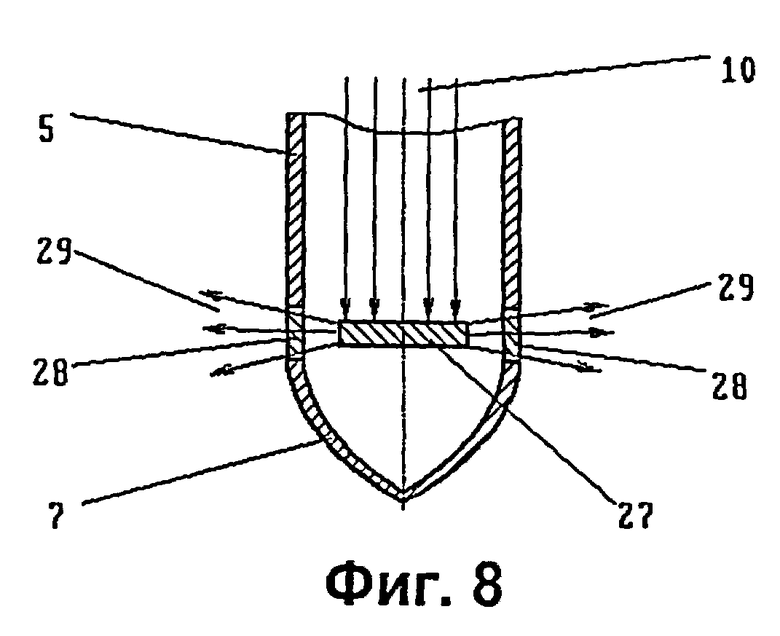
на фиг.8 - дистальный конец зонда с установленной в нем вторичной мишенью, облучаемой квазипараллельным пучком;
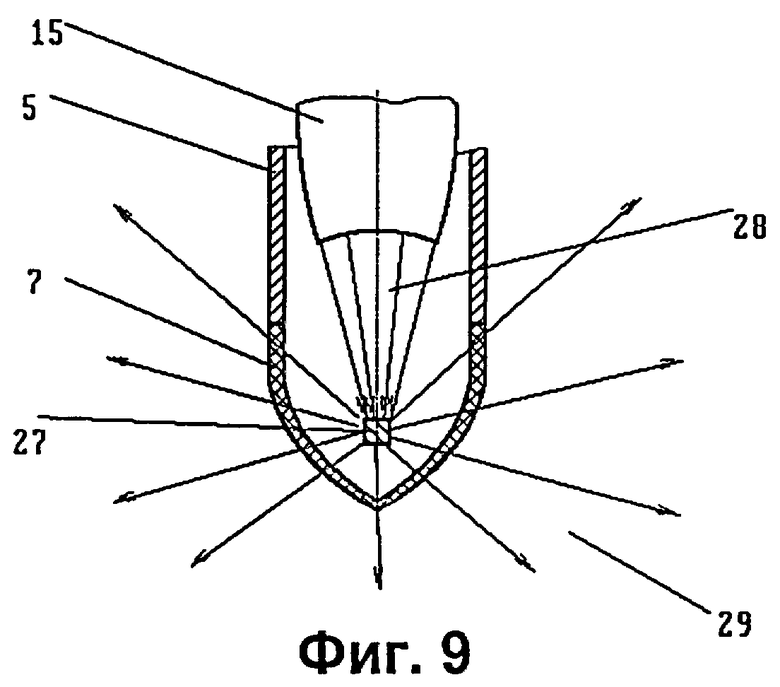
на фиг.9 - дистальный конец зонда с установленной в нем вторичной мишенью, облучаемой сфокусированным пучком;
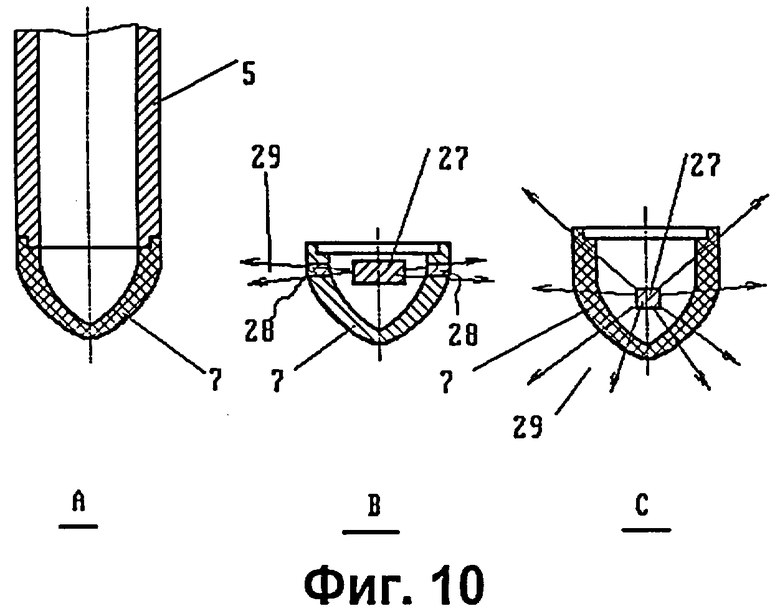
на фиг.10 - зонд с несколькими съемными дистальными концами.
Варианты осуществления изобретения
Предлагаемое устройство содержит (фиг.1, А) источник 1 нейтральных частиц (рентгеновских ли гамма-квантов либо нейтронов), защитный экран 2 с диафрагмой 3, расположенной перед выходной апертурой источника 1, средство 4 для формирования пучка частиц, ориентированного по продольной оси зонда 5. Последний имеет сужающийся дистальный конец 7. Проксимальный конец 6 зонда 5 может быть выполнен таким образом, чтобы обеспечить возможность снятия зонда (например, для стерилизации и замены его другим). В комплект устройства могут входить несколько зондов, например, разной длины (фиг.1, В и С).
Зонд внешне может напоминать и иметь размеры, характерные для пункционной иглы для биопсии.
При использовании устройства зонд вводят, в зависимости от локализации патологического очага, в один из естественных проходов тела больного или осуществляют пунктирование, аналогично тому, как это делается при биопсии.
На фиг.2 показано положение зонда 5 в теле пациента 11. В проксимальный конец 6 зонда поступает квазипараллельный пучок 10 излучения. Этот пучок проходит по внутреннему каналу зонда 5 и выходит через прозрачный для излучения дистальный конец 7. Последний в показанном на фиг.2 случае находится в непосредственной близости от протяженной опухоли 12. Направление введения зонда выбрано так, чтобы выходящее из дистального конца 7 излучение входило в опухоль 12 и распространялось в ней в направлении большего размера. Излучение, проникшее в опухоль, непосредственно воздействует на находящиеся на его пути ткани срединной части опухоли. На ткани опухоли, окружающие срединные, воздействует вторичное излучение, возбужденное в срединных тканях. Поскольку выходящее из дистального конца зонда излучение практически не воздействует на здоровые ткани, интенсивность первичного излучения источника можно выбрать так, чтобы интенсивность вторичного излучения срединных тканей, достигшего периферии опухоли, была на уровне минимально достаточной для поражения периферийных тканей. В этом случае вторичное излучение, выходящее за пределы опухоли, не будет поражать окружающие ее здоровые ткани.
Для воздействия на новообразования малых размеров более целесообразно использовать сфокусированный пучок, выходящий из дистального конца 7 зонда 5. На фиг.3 показан вариант выполнения устройства, в котором расходящееся излучение от рентгеновского источника с малой апертурой 14 фокусируется рентгеновской линзой 15 и передается через зонд 5, введенный в тело больного, в центр 16 опухоли 13. Как и в предыдущем рассмотренном случае, периферийные ткани опухоли 13 облучаются возбужденным вторичным излучением.
При использовании в качестве источника излучения источника нейтронов применение предлагаемого устройства может быть совмещено с методом борозахватной терапии, при котором обеспечивается концентрация бора в опухоли 5 (Advances in Neutron Capture Theraphy. Editors: B. Larsson, J. Crawford, R. Weinrech. Elserier, 1997 [5]).
Современная технология изготовления рентгеновских линз позволяет получать монолитные линзы малых размеров (см., например, M.A. Kumakhov. A history of the X-Ray and neutron capillary optics. Optic of beams, p.p. 3 - 17, Moscow, 1993 [6]), приемлемых для расположения линзы частично или полностью внутри зонда. Соответствующие варианты выполнения устройства показаны на фиг.4 и 5.
На фиг.4 внутри зонда 5 расположена фокусирующая линза 15, на вход которой поступает расходящееся излучение источника с малой апертурой 14. Фокусирование происходит в точке 16, находящейся вне прозрачного для излучения дистального конца 7 зонда 5 на продолжении его продольной оси.
На фиг.5 линза 18 формирует пучок, сфокусированный в точке 16 внутри патологического очага 13, из излучения источника 1, имеющего сравнительно большую выходную апертуру 17. Верхняя часть линзы 18 имеет параллельные каналы и выполняет роль коллиматора. В этой части линзы формируется квазипараллельный поток частиц, распространяющихся по ее каналам. Затем, как в обычной линзе для фокусирования квазипараллельного излучения, он преобразуется в сфокусированный пучок, выходящий из нижнего конца линзы 18. Защитный экран 2 предохраняет пациента 11 от излучения источника 1, распространяющегося мимо линзы 18.
Во всех рассмотренных случаях используемое излучение, несмотря на то, что оно создается источником, находящимся вне тела больного, не воздействует на здоровые ткани, находящиеся на пути к патологическому очагу. Это обеспечивается благодаря тому, что здоровые ткани механически изолированы от трассы пучка излучения стенками зонда, а также благодаря их экранирующему действию. Для этого они выполнены непроницаемыми для используемого излучения. Хотя направляемый в зонд ориентированный поток излучения, если он сформирован достаточно точно, может и не пересекать стенок зонда, такая мера является дополнительной гарантией того, что излучение будет исходить только из предназначенных для этого участков дистального конца зонда.
На фиг.6 показано использование устройства, в котором формирование близкого к параллельному пучка, выходящего из дистального конца 7 зонда 5, осуществляется самим зондом. Он в данном случае выполняет функцию коллиматора, имеющего единственный канал, образованный боковыми стенками зонда 5. При соответствующем выборе длины зонда и расстояния между его проксимальным концом 6 и выходной апертурой 14 источника излучения выходящее из дистального конца 7 излучение 20 имеет малый угол расходимости и близко к параллельному. Такая работа устройства эквивалентна расположению средства формирования квазипараллельного потока частиц внутри зонда.
Для осуществления лучевого воздействия возможно одновременное применение нескольких зондов, вводимых в разные части опухоли.
Во всех случаях использования в качестве источника излучения рентгеновского источника последний может быть выполнен с секционированным анодом для оперативного изменения энергии частиц.
С целью обеспечения по завершении лечебной процедуры коагуляции раневого канала, возникшего при осуществлении пункции с помощью зонда, последний может быть выполнен электропроводящим и имеющим снаружи (см. фиг.7) изоляционное покрытие 23, за исключением наиболее удаленной части 22 дистального конца. В этом случае зонд должен иметь возможность подключения к электрокоагулятору 24. При подаче электрического напряжения от коагулятора между зондом 5 телом пациента 11 в процессе извлечения зонда (стрелка 25 на фиг.7) происходит “заваривание” раневого канала 26. Это предотвращает распространение клеток опухоли 13 за пределы злокачественного очага (в данном случае используется прием, аналогичный описанному в патенте Российской Федерации №2120787 [7]).
В дистальном конце зонда может быть расположена вторичная мишень. В этом случае для лучевого воздействия используется рассеянное вторичной мишенью излучение источника или вторичное излучение мишени.
На фиг.8 показан случай, когда используется возбужденное в веществе вторичной мишени излучение 29, выводимое из дистального конца зонда через прозрачные для такого излучения окна 28. Последние расположены таким образом, чтобы сформировать желаемую диаграмму направленности выходящего излучения. Например, при равномерном расположении окон в узкой полосе по периметру дистального конца 7 излучение будет сконцентрировано в узком шаровом секторе. Изменяя глубину введения зонда в тело пациента (в частности, в опухоль), можно регулировать положение этого сектора и воздействовать на выбранную часть опухоли. При этом может быть реализована та или иная тактика лечения. Например, зонд можно перемещать с переменной скоростью или останавливать его на разное время в разных положениях, регулируя тем самым степень лучевого воздействия на разные части опухоли, в зависимости от ее размеров в направлении, перпендикулярном продольной оси зонда.
На фиг.9 показано использование рассеянного вторичной мишенью 27 излучения. Благодаря изотропному характеру последнего при выполнении дистального конца 7 зонда прозрачным для излучения при расположении мишени ближе к наиболее удаленной части дистального конца можно получить излучение 29, близкое к всенаправленному, распространяющееся, в том числе и частично назад (вверх по фиг.9). Введение дистального конца 7 непосредственно в опухоль обеспечивает облучение большей части тканей опухоли, окружающих этот конец.
При использовании вторичных мишеней в еще большей степени реализуются преимущества предлагаемого устройства, не требующего вакуумирования зонда. Возможна смена не только зонда в целом, но и его дистального конца 7, например, для перехода от используемой вторичной мишени одного типа к мишени другого типа. На фиг.10 показаны выполнение зонда 5 со съемным дистальным концом 7 и варианты выполнения дистального конца с двумя рассмотренными выше типами вторичных мишеней 27 и формированием двух видов диаграмм направленности вторичного излучения 28, 29 (см. соответственно фиг.10, А, В и С).
Для изменения характеристик рассеянного и вторичного излучения дистальный конец зонда может быть выполнен разъемным с возможностью смены установленной в нем мишени. При этом в дистальном конце зонда установлена одна из нескольких входящих в комплект устройства мишеней, например, выполненных из разных металлов.
Зонд 5 может иметь один из нескольких входящих в комплект устройства дистальных концов, выполненных с различными соотношениями прозрачности участков поверхности дистального конца зонда для рассеянного и возбужденного в веществе вторичной мишени излучения.
Промышленная применимость
Предлагаемое устройство может быть реализовано с использованием как типовых выпускаемых в промышленных масштабах источников излучения, таких, как рентгеновские трубки, а также источников нейтронного излучения и радиоизотопов.
Источники информации
1. Аспекты клинической дозиметрии. Под ред. Р.В. Ставицкого. Москва, “МНПИ”, 2000.
2. Лучевая терапия злокачественных опухолей. Руководство для врачей. Под ред. проф. Е.С. Киселевой. Москва, “Медицина”, 1996.
3. М.А. Кумахов. Рентгеновские средства для определения местоположения и лучевой терапии злокачественных новообразований. Международная заявка PCT/RU 00/00273, международная публикация WO 01/29845 А1 от 26.04.2001.
4. Nomikos et al. Miniaturized low power X-ray source. Патент США №5153900, опубл. 06.10.1992.
5. Advances in Neutron Capture Theraphy. Editors: B. Larsson, J. Crawford, R. Weinrech. Elserier, 1997.
6. M.A. Kumakhov. A history of the X-Ray and neutron capillary optics. Optic of beams, p.p.3-17, Moscow, 1993.
7. С.А. Астраханцев и др. Игольное устройство для биопсии и коагуляции. Патент Российской Федерации №2120787, опубл. 27.10.1998.

Изобретение относится к средствам для лучевой терапии злокачественных и незлокачественных новообразований и некоторых других заболеваний. Устройство содержит полый зонд, источник излучения нейтральных частиц рентгеновских или гамма-квантов, либо нейтронов, и средство формирования пучка частиц этого излучения, ориентированного по продольной оси зонда. Средство формирования пучка частиц выполнено в виде коллиматора или линзы, представляющей собой совокупность изогнутых каналов транспортировки излучения с полным внутренним отражением. Указанное средство может быть размещено внутри зонда, выполненного съемным. Использование изобретение позволяет повысить легкость его эксплуатации за счет отказа от вакуумирования зонда и использования в последнем высокого напряжения, легкой трансформируемости путем замены зонда, в частности, для изменения его размеров, изменения энергии и диаграммы направленности излучения, воздействующего на патологический очаг. Выполнение зонда съемным упрощает его стерилизацию. 32 з.п. ф-лы, 10 ил.
| ИСТОЧНИК РЕНТГЕНОВСКОГО ИЗЛУЧЕНИЯ С СФОРМИРОВАННОЙ РАДИАЦИОННОЙ КАРТИНОЙ | 1995 |
|
RU2155413C2 |
| КАМЕРА СГОРАНИЯ КАРБЮРАТОРНОГО ДВИГАТЕЛЯ | 1999 |
|
RU2164301C2 |
| WO 00/5727 Al, 03.02.2000 | |||
| Рентгенотехника | |||
| /Под ред | |||
| В.В.КЛЮЕВА, т.1 | |||
| - M.: Машиностроение, 1980, с.74 и 75. | |||
Авторы
Даты
2004-10-27—Публикация
2001-09-19—Подача