Изобретение относится к новым токсинам из Xenorhabdus nematophilus, Xenorhabdus poinarii и Photorhabdus lumintecens, к нуклеотидным последовательностям, в результате экспрессии которых образуются токсины, и к способам получения и способам применения токсинов и соответствующих нуклеотидных последовательностей для борьбы с насекомыми.
Насекомые-вредители являются основной причиной потерь урожая. Только в США ежегодные потери урожая вследствие поражения различными видами насекомых оцениваются приблизительно в 7,7 миллиардов долларов. Помимо того, что они приводят к потерям урожая полевых культур, насекомые-вредители также осложняют работу овощеводов и плодоводов, производителей декоративных цветов, и они являются источником неприятностей для садоводов и домовладельцев.
В основном с насекомыми-вредителями борются путем интенсивного применения химических инсектицидов, обладающих активностью в отношении ингибирования роста насекомых, предотвращения питания или размножения насекомых, или приводящих к их гибели. Этот метод позволяет эффективно бороться с насекомыми, но такие химические средства борьбы иногда также поражают другие полезные виды насекомых. Другой проблемой, возникающей при широком применении химических пестицидов, является возникновение устойчивых штаммов насекомых. Эта проблема частично решается с помощью различных стратегий управления устойчивостью, однако существует все возрастающая потребность в создании альтернативных агентов для борьбы с вредителями. Также применяли с удовлетворительным результатом биологические агенты борьбы с насекомыми, такие как штаммы Bacillus thuringiensis, экспрессирующие инсектицидные токсины, такие как δ-эндотоксины, и они представляют собой альтернативу и дополнение к химическим инсектицидам. Недавно были выделены гены, кодирующие некоторые из этих δ-эндотоксинов, и было установлено, что их экспрессия в гетерологичных хозяевах представляет собой еще одно средство борьбы с важными с экономической точки зрения насекомыми-вредителями. В частности, экспрессия в трансгенных растениях инсектицидных токсинов, таких как δ-эндотоксины Bacillus thuringiensis, обеспечивает эффективную защиту от определенных насекомых-вредителей, а трансгенные растения, экспрессирующие такие токсины, имеются в продаже, что позволяет фермерам уменьшить количества применяемых химических агентов борьбы с насекомыми. Однако даже в этом случае сохраняется возможность развития устойчивости и может быть ограничена численность только небольшого количества определенных видов насекомых-вредителей. Таким образом, сохраняется давно осознанная, но не удовлетворенная потребность в создании новых и эффективных агентов для борьбы с насекомыми, которые приносили бы фермерам экономическую выгоду и были приемлемыми с точки зрения воздействия на окружающую среду.
Настоящее изобретение направлено на решение давней проблемы создания новых агентов для борьбы с насекомыми. Прежде всего необходимы агенты, которые направлены на борьбу с важными с экономической точки зрения насекомыми-вредителями и которые позволяют эффективно бороться с штаммами насекомых, устойчивыми к существующим агентам для борьбы с насекомыми. Кроме того, предпочтительными являются агенты, применение которых наносит минимальный ущерб окружающей среде.
При поиске новых агентов для борьбы с насекомыми особый интерес представляют определенные классы нематод из родов Heterorhabdus и Steinernema, что обусловлено их инсектицидными свойствами. Они убивают личинки насекомых и их потомство питается в мертвых личинках. В действительности инсектицидная активность обусловлена симбиотическими бактериями, живущими в нематодах. Такими симбиотическими бактериями являются Photorhabdus в случае Heterorhabdus и Xenorhabdus в случае Steinernema. Настоящее изобретение относится к нуклеотидным последовательностям, выделенным из Xenorhabdus nematophilus, к нуклеотидным последовательностям, практически аналогичным им, экспрессия которых приводит к продуцированию инсектицидных токсинов, которые являются высокотоксичными для важных с экономической точки зрения вредителей, прежде всего вредителей растений. Кроме того, изобретение относится к инсектицидному токсину, образующемуся в результате экспрессии нуклеотидной последовательности, и к композициям и препаративным формам, включающим инсектипидный токсин, которые обладают способностью ингибировать (подавлять) выживаемость насекомых-вредителей, их рост или репродуктивную способность, или ограничивать вызываемые насекомыми повреждения или потери урожая культурных растений. Кроме того, изобретение относится к способу получения токсина и к способам применения нуклеотидной последовательности, например, в микроорганизмах, для борьбы с насекомыми или в трансгенных растениях для придания устойчивости к насекомым, а также к способу применения токсина, и композиций и препаративных форм, включающих токсин, например, путем обработки токсином, композицией или препаративной формой зараженных насекомыми площадей, или для профилактической обработки восприимчивых к насекомым площадей или растений, которые являются потенциальными мишенями, с целью обеспечения защиты или создания устойчивости в отношении вредных насекомых.
Новый токсин обладает высокой инсектицидной активностью в отношении Plutella xylostella (моль капустная), важного с экономической точки зрения насекомого-вредителя. Токсин может применяться в многочисленных стратегиях борьбы с насекомыми, приводя к достижению максимальной эффективности в сочетании с минимальным воздействием на окружающую среду.
Одним из объектов настоящего изобретения является выделенная молекула нуклеиновой кислоты, включающая: (а) нуклеотидную последовательность, практически аналогичную нуклеотидной последовательности, выбранной из группы, включающей: нуклеотиды 569-979 SEQ ID NО:1, нуклеотиды 1045-2334 SEQ ID NО:1, SEQ ID NО:4, SEQ ID NО:6, SEQ ID NО:8, SEQ ID NО:10, SEQ ID NО:12 и SEQ ID NО:14; или (б) нуклеотидную последовательность, изокодонной нуклеотидной последовательности, указанной в подпункте (а); причем экспрессия молекулы нуклеиновой кислоты приводит к образованию по крайней мере одного токсина, обладающего активностью в отношении насекомых. В одном из вариантов осуществления изобретения нуклеотидная последовательность является изокодонной нуклеотидной последовательности, практически аналогичной нуклеотидам 569-979 SEQ ID NО:1, нуклеотидам 1045-2334 SEQ ID NО:1, SEQ ID NО:4, SEQ ID NО:6, SEQ ID NО:8, SEQ ID NО:10, SEQ ID NО:12 или SEQ ID NО:14. Предпочтительно нуклеотидная последовательность является практически аналогичной нуклеотидам 569-979 SEQ ID NО:1, нуклеотидам 1045-2334 SEQ ID NО:1, SEQ ID NО:4, SEQ ID NО:6, SEQ ID NО:8, SEQ ID NО:10, SEQ ID NО:12 или SEQ ID NО:14. Более предпочтительно нуклеотидная последовательность кодирует аминокислотную последовательность, выбранную из группы, включающей SEQ ID NО:2, 3, 5, 7, 9, 11, 13 и 15. Наиболее предпочтительно нуклеотидная последовательность включает нуклеотиды 569-979 SEQ ID NО:1, нуклеотиды 1045-2334 SEQ ID NО:1, SEQ ID NО:4, SEQ ID NО:6, SEQ ID NО:8, SEQ ID NО:10, SEQ ID NО:12 или SEQ ID NО:14. В другом варианте осуществления нуклеотидная последовательность включает фрагмент ДНК длиной приблизительно 3,0 т.п.н., содержащийся в pCIB9369 (NRRL В-21883).
Согласно предпочтительному варианту осуществления токсины, образующиеся в результате экспрессии молекул нуклеиновой кислоты по изобретению, обладают активностью в отношении Plutella xylostella.
Другим объектом настоящего изобретения является выделенная молекула нуклеиновой кислоты, включающая состоящую из 20, 25, 30, 35, 40, 45 или 50 (предпочтительно 20) пар оснований часть нуклеотидной последовательности, идентичную соответствующей состоящей из 20, 25, 30, 35, 40, 45 или 50 (предпочтительно 20) последовательных пар оснований части нуклеотидной последовательности, выбранной из группы, включающей: нуклеотиды 569-979 SEQ ID NО:1, нуклеотиды 1045-2334 SEQ ID NО:1, SEQ ID NО:4, SEQ ID NО:6, SEQ ID NО:8, SEQ ID NО:10, SEQ ID NО:12 и SEQ ID NО:14, причем экспрессия молекулы нуклеиновой кислоты приводит к образованию по крайней мере одного токсина, обладающего активностью в отношении насекомых.
Объектом настоящего изобретения также является химерный ген, содержащий гетерологичную промоторную последовательность, функционально связанную с молекулой нуклеиновой кислоты по изобретению. Кроме того, объектом настоящего изобретения является рекомбинантный вектор, содержащий такой химерный ген. Еще одним объектом настоящего изобретения является клетка-хозяин, содержащая такой химерный ген. Клетка-хозяин согласно данному объекту изобретения может представлять собой бактериальную клетку, клетку дрожжей или растительную клетку, предпочтительно растительную клетку. И еще одним объектом настоящего изобретения является растение, содержащее такую растительную клетку. Предпочтительно растение представляет собой кукурузу.
Другим объектом настоящего изобретения являются токсины, образующиеся в результате экспрессии молекул ДНК по настоящему изобретению. Согласно предпочтительному варианту осуществления токсины по настоящему изобретению обладают активностью в отношении Plutella xylostella.
В одном из вариантов осуществления токсины продуцируются штаммом Е.coli, имеющим регистрационный номер NRRL В-21883.
В другом варианте осуществления токсин по изобретению содержит аминокислотную последовательность, выбранную из группы, включающей SEQ ID NО:2, 3, 5, 7, 9, 11, 13 и 15.
Также объектом изобретения является композиция, включающая эффективное в качестве инсектицида количество токсина по изобретению. Другим объектом настоящего изобретения является способ получения токсина, обладающего активностью в отношении насекомых, предусматривающий: (а) получение клетки-хозяина, содержащей химерный ген, который включает гетерологичную промоторную последовательность, функционально связанную с молекулой нуклеиновой кислоты по изобретению; и (б) экспрессию молекулы нуклеиновой кислоты в клетке, что приводит к образованию по крайней мере одного токсина, обладающего активностью в отношении насекомых.
Еще одним объектом настоящего изобретения является способ получения устойчивого к насекомым растения, предусматривающий интродукцию в растение молекулы нуклеиновой кислоты по изобретению, причем молекула нуклеиновой кислоты способна экспрессироваться в растении в количестве, эффективном в отношении борьбы с насекомыми. Согласно предпочтительному варианту осуществления насекомым является Plutella xylostella.
И еще одним объектом настоящего изобретения является способ борьбы с насекомыми, предусматривающий введение насекомому эффективного количества токсина по настоящему изобретению. Согласно предпочтительному варианту осуществления насекомое представляет собой Plutella xylostella. Предпочтительно токсин поступает в организм насекомого оральным путем.
Еще одним объектом настоящего изобретения является способ осуществления мутации молекулы нуклеиновой кислоты по настоящему изобретению, согласно которому молекулу нуклеиновой кислоты расщепляют с получением популяции случайных двухцепочечных фрагментов нужной длины и осуществляют следующие стадии:
а) добавление к полученной популяции случайных двухцепочечных фрагментов одного или нескольких одно- или двухцепочечных олигонуклеотидов, причем каждый из олигонуклеотидов содержит область идентичности и область гетерологичности по отношению к двухцепочечному матричному полинуклеотиду;
б) денатурацию образовавшейся смеси случайных двухцепочечных фрагментов и олигонуклеотидов с получением одноцепочечных фрагментов;
в) инкубацию полученной популяции одноцепочечных фрагментов с полимеразой в условиях, в которых происходит ренатурация указанных одноцепочечных фрагментов в области идентичности с образованием пар ренатурированных фрагментов, причем указанные области идентичности являются достаточными для того, чтобы один член из пары примировал репликацию другого, приводя к образованию двухцепочечного полинуклеотида, содержащего мутацию; и
г) повторение второй и третьей стадий по крайней мере в течение еще двух циклов, причем образовавшаяся смесь на второй стадии дополнительного цикла содержит двухцепочечный полинуклеотид с мутацией, полученный на третьей стадии предыдущего цикла, в результате чего дальнейшие циклы приводят к образованию дополнительного количества двухцепочечного полинуклеотида, содержащего мутацию.
Другие объекты и преимущества настоящего изобретения будут очевидны для специалистов в данной области на основе изучения описания изобретения и примеров, не ограничивающих его объема.
Определения
Понятие "активность" применительно к токсинам по изобретению означает, что действие токсинов как агентов для борьбы с насекомыми, обладающих активностью при оральном введении, приводит к токсическому воздействию, или они обладают способностью прекращать или нарушать питание насекомого, что может вызвать или может не вызвать гибель насекомого. Если токсин по изобретению поступает в организм насекомого, то результатом, как правило, является смерть насекомого, или насекомое перестает питаться от источника, от которого токсин поступает к насекомому.
Понятие "соединенный с/функционально связанный с" относится к двум нуклеотидным последовательностям, которые связаны физически или функционально. Например, промоторная или регуляторная последовательность ДНК "связана с" последовательностью ДНК, кодирующей РНК или протеин, если две последовательности являются функционально связанными или расположены так, что регуляторная последовательность ДНК оказывает воздействие на уровень экспрессии кодирующей или структурной последовательности ДНК.
Понятие "химерный ген" обозначает рекомбинантную нуклеотидную последовательность, в которой промоторная или регуляторная нуклеотидная последовательность функционально связана или соединена с нуклеотидной последовательностью, которая кодирует мРНК или которая экспрессируется в виде протеина, так что регуляторная нуклеотидная последовательность способна регулировать транскрипцию или экспрессию связанной с ней нуклеотидной последовательности. Регуляторная нуклеотидная последовательность химерного гена в норме не является функционально связанной с соединенной с ней нуклеотидной последовательностью, как это происходит в естественных условиях.
Понятие "кодирующая последовательность" обозначает нуклеотидную последовательность, которая транскрибируется с образованием РНК, такой как, например, мРНК, рРНК, тРНК, snPHK (М.я.РНК), смысловая РНК или антисмысловая РНК. Предпочтительно затем РНК транслируется в организме с образованием протеина.
Понятие "бороться" с насекомыми означает ингибировать в результате токсического действия способность насекомых-вредителей выживать, расти, питаться и/или размножаться, или ограничивать связанные с насекомыми повреждения или потери урожая культурных растений. При "борьбе" с насекомыми можно убивать или не убивать насекомых, хотя предпочтительно это понятие означает убивать насекомых.
Понятие "введение (поступление в организм)" токсина означает, что токсин вступает в контакт с насекомым, что приводит к токсическому действию и борьбе с насекомым. Токсин может поступать в организм многими известными путями, например, орально при поедании насекомым, или при контакте с насекомым в результате экспрессии токсина трансгенным растением, с использованием препаративной(ых) формы на основе протеина, композиции (й) для опрыскивания на основе протеина, основы приманки или любых других известных в данной области систем введения токсина.
Понятие "кассета экспрессии" в контексте настоящего описания обозначает нуклеотидную последовательность, способную обеспечивать экспрессию конкретной нуклеотидной последовательности в соответствующей клетке-хозяине, которая включает промотор, функционально связанный с представляющей интерес нуклеотидной последовательностью, которая функционально связана с сигналами терминации. Она в норме также включает последовательности, необходимые для правильной трансляции нуклеотидной последовательности. Кассета экспрессии, содержащая представляющую интерес нуклеотидную последовательность, может быть химерной, это означает, что по крайней мере один ее компонент является гетерологичным по отношению по крайней мере к одному из остальных компонентов. Кассета экспрессии также может представлять собой кассету, которая встречается в естественных условиях, но которая была получена в рекомбинантной форме, пригодной для гетерологичной экспрессии. Однако, как правило, кассета экспрессии является гетерологичной относительно хозяина, т.е. определенная последовательность ДНК кассеты экспрессии не встречается в естественных условиях в клетке-хозяине и должна быть интродуцирована в клетку-хозяина или в предка клетки-хозяина путем трансформации. Экспрессия нуклеотидной последовательности в кассете экспрессии может находиться под контролем конститутивного промотора или индуцибельного промотора, который инициирует транскрипцию только тогда, когда клетку-хозяина обрабатывают определенным внешним стимулом. В случае многоклеточного организма, такого как растение, промотор также может быть специфичным по отношению к определенной ткани или органу или стадии развития.
Понятие "ген" обозначает определенную область внутри генома, которая помимо указанной выше кодирующей последовательности содержит другие, прежде всего регуляторные нуклеотидные последовательности, ответственные за контроль экспрессии, т.е. за транскрипцию и трансляцию кодирующей области. Ген также может включать другие 5’- и 3’-нетранслируемые последовательности и терминирующие последовательности. Другими элементами, которые также могут присутствовать в гене, являются, например, интроны.
Понятие "представляющий интерес ген" обозначает любой ген, который при переносе в растение придает растению требуемые свойства, такие как устойчивость к антибиотикам, устойчивость к вирусам, устойчивость к насекомым, устойчивость к болезням или устойчивость к другим вредителям, устойчивость к гербицидам, улучшенная питательная ценность, улучшенные характеристики с точки зрения промышленной переработки или измененная способность к размножению. "Представляющий интерес ген" может представлять собой ген, который переносят в растения для производства важных с экономической точки зрения ферментов или метаболитов в растении.
"Гетерологичная" нуклеотидная последовательность обозначает нуклеотидную последовательность, которая в естественных условиях не связана с клеткой-хозяином, в которую ее вводят, включая не встречающиеся в естественных условиях множественные копии встречающихся в естественных условиях нуклеотидных последовательностей.
"Гомологичная" нуклеотидная последовательность обозначает нуклеотидную последовательность, которая в естественных условиях связана с клеткой-хозяином, в которую ее вводят.
Понятие "гомологичная рекомбинация" обозначает взаимный обмен фрагментами нуклеиновой кислоты между гомологичными молекулами нуклеиновых кислот.
Понятие "инсектицидный" относится к токсической биологической активности, с помощью которой оказывается возможным бороться с насекомыми, предпочтительно убивать их.
Нуклеотидная последовательность является "изокодонная" нуклеотидной последовательности, с которой производится сравнение, если нуклеотидная последовательность кодирует полипептид, имеющий такую же аминокислотную последовательность, что и полипептид, кодируемый нуклеотидной последовательностью, с которой производится сравнение.
"Выделенная" молекула нуклеиновой кислоты или "выделенный" фермент обозначают молекулу нуклеиновой кислоты или фермент, которые благодаря человеку существуют вне их естественного окружения и, следовательно, не являются природными продуктами. Выделенная молекула нуклеиновой кислоты или фермент могут существовать в очищенной форме или могут существовать в неестественном окружении, таком как, например, рекомбинантная клетка-хозяин.
"Молекула нуклеиновой кислоты" или "нуклеотидная последовательность" обозначает линейный сегмент одно- или двухцепочечной ДНК или РНК, который может быть выделен из любого источника. В контексте настоящего изобретения молекула нуклеиновой кислоты предпочтительно обозначает сегмент ДНК. Понятие "ORF" обозначает открытую рамку считывания.
Понятие "растение" обозначает любое растение на любой стадии развития, в частности семенной материал растения.
Понятие "растительная клетка" обозначает структурную и физиологическую единицу растения, включающую протопласт и клеточную оболочку. Растительная клетка может находиться в форме выделенной отдельной клетки или культивируемой клетки, или представлять собой часть высокоорганизованной единицы, такой как, например, ткань растения, орган растения или целое растение.
Понятие "культура растительных клеток" обозначает культуры структурных или физиологических единиц растения, таких как, например, протопласты, клетки в культуре клеток, клетки в тканях растения, пыльца, пыльцевые трубки, семяпочки, зародышевые мешки, зиготы и зародыши на различных стадиях развития.
Понятие "растительный материал" относится к листьям, стеблям, корням, цветкам или частям цветков, плодам, пыльце, яйцеклеткам, зиготам, семенам, отводкам, культурам клеток или тканей, или любой другой части или продукту растения.
Понятие "орган растения" обозначает отдельную и структурно оформленную дифференцированную часть растения, такую как корень, стебель, лист, листовая почка или зародыш.
Понятие "ткань растения" в контексте настоящего описания обозначает группу растительных клеток, организованных в структурную или функциональную единицу. Подразумевается любая ткань растения in planta или в культуре. Это понятие включает целые растения, органы растений, семена растений, культуру ткани и любые группы растительных клеток, организованные в структурные и/или функциональные единицы, но не ограничено ими. Применение этого понятия в сочетании с конкретным типом растительной ткани, как она определена выше, или по каким-то другим признакам подпадает под это определение, или вне зависимости от типа ткани, не подразумевает, что при этом исключается любой другой тип растительной ткани.
Понятие "промотор" обозначает нетранслируемую последовательность ДНК, расположенную против хода транскрипции кодирующей области, которая содержит сайт связывания РНК-полимеразы II и инициирует транскрипцию ДНК. Промоторная область также может включать другие элементы, которые действуют в качестве регуляторов экспрессии гена.
Понятие "протопласт" обозначает выделенную растительную клетку без клеточной оболочки или только с частью клеточной оболочки.
Понятие "регуляторные элементы" относится к последовательностям, участвующим в контроле экспрессии нуклеотидной последовательности. Регуляторные элементы включают промотор, функционально связанный с представляющей интерес нуклеотидной последовательностью, и сигналы терминации. Они также обычно включают последовательности, необходимые для правильной трансляции нуклеотидной последовательности.
В наиболее широком смысле понятие "практически аналогичная", когда оно используется в настоящем описании применительно к нуклеотидной последовательности, обозначает нуклеотидную последовательность, соответствующую нуклеотидной последовательности, с которой производится сравнение, причем рассматриваемая последовательность кодирует полипептид, имеющий практически такую же структуру и функции, что и полипептид, кодируемый нуклеотидной последовательностью, с которой производится сравнение, например, полипептид, имеющий только такие замены аминокислот, которые не влияют на функцию полипептида. Предпочтительно практически аналогичная нуклеотидная последовательность кодирует полипептид, кодируемый нуклеотидной последовательностью, с которой производится сравнение. Желательно, чтобы процент идентичности практически аналогичной нуклеотидной последовательности и нуклеотидной последовательностью, с которой производится сравнение, составлял по меньшей мере 80%, более желательно по меньшей мере 85%, предпочтительно по меньшей мере 90%, более предпочтительно по меньшей мере 95%, еще более предпочтительно по меньшей мере 99%. Нуклеотидная последовательность, "практически аналогичная" нуклеотидной последовательности, с которой производится сравнение, как правило, гибридизуется с молекулой нуклеиновой кислоты, с которой проводится сравнение, в следующих условиях: 7%-ный додецилсульфат натрия (ДСН), 0,5М NaPО4, 1 мМ ЭДТК при 50°С; отмывка двукратным SSC (2xSSC), 0,1%-ным ДСН при 50°С, более желательно 7%-ный додецилсульфат натрия (ДСН), 0,5М NaPО4, 1 мМ ЭДТК при 50°С; отмывка однократным SSC (1xSSC), 0,1%-ным ДСН при 50°С, еще более желательно 7%-ный додецилсульфат натрия (ДСН), 0,5 М NaPО4, 1 мМ ЭДТК при 50°С; отмывка 0,5xSSC, 0,1%-ным ДСН при 50°С, предпочтительно 7%-ный додецилсульфат натрия (ДСН), 0,5М NaPО4, 1 мМ ЭДТК при 50°С; отмывка 0,1xSSC, 0,1%-ным ДСН при 50°С, более предпочтительно 7%-ный додецилсульфат натрия (ДСН), 0,5 М NaPО4, 1 мМ ЭДТК при 50°С; отмывка 0,1xSSC, 0,1%-ным ДСН при 65°С.
Понятие "синтетическая" относится к нуклеотидной последовательности, включающей структурные особенности, которые не присутствуют во встречающейся в естественных условиях последовательности. Например, синтетической последовательностью называют искусственную последовательность, характеризующуюся наиболее близким содержанием G+C и нормальным распределением кодонов, свойственным генам двудольных и/или однодольных растений.
Понятие "трансформация" обозначает интродукцию гетерологичной нуклеотидной последовательности в клетку-хозяина или в организм. В частности, "трансформация" обозначает стабильную интеграцию молекулы ДНК в геном представляющего интерес организма.
Понятие "трансформированный/трансгенный/рекомбинантный" относится к организму-хозяину, такому как бактерия или растение, в который введена гетерологичная молекула нуклеиновой кислоты. Молекула нуклеиновой кислоты может быть стабильно интегрирована в геном хозяина или молекула нуклеиновой кислоты также может присутствовать в виде внехромосомной молекулы. Такая внехромосомная молекула может обладать способностью к саморепликации. Следует понимать, что понятия трансформированные клетки, ткани или растения включают не только конечный продукт процесса трансформации, но также и его трансгенное потомство. Понятия "нетрансформированный", "нетрансгенный" или "нерекомбинантный" относятся к организму дикого типа, например бактерии или растению, который не содержит гетерологичную молекулу нуклеиновой кислоты.
Нуклеотиды обозначены по их основаниям с помощью следующих стандартных сокращений: аденин (А), цитозин (С), тимин (Т) и гуанин (G). Аналогично этому аминокислоты обозначены следующими стандартными сокращениями: аланин (Аlа; А), аргинин (Arg; R), аспарагин (Asn; N), аспарагиновая кислота (Asp; D), цистеин (Cys; С), глутамин (Gln; Q), глутаминовая кислота (Glu; Е), глицин (Gly; G), гистидин (His; Н), изолейцин (Ilе; I), лейцин (Leu; L), лизин (Lys; К), метионин (Met, М), фенилаланин (Phe, F); пролин (Pro, Р); серин (Ser, S); треонин (Thr, Т); триптофан (Trp; W), тирозин (Тyr; Y) и валин (Val; V). Кроме того, (Хаа; X) обозначает любую аминокислоту.
Краткое описание последовательностей, представленных в перечне последовательностей
SEQ ID NO:1 представляет собой последовательность фрагмента ДНК длиной приблизительно 3,0 т.п.н., содержащуюся в клоне Xenorhabdus nematophilus pCIB9369, которая включает перечисленные ниже ORF в указанных положениях нуклеотидов:

SEQ ID NO:2 представляет собой последовательность протеина с молекулярной массой ~15 кДа, кодируемую orf1 клона pCIB9369.
SEQ ID NO:3 представляет собой последовательность сходного с протеином эстеразы ювенильного гормона с молекулярной массой ~47,7 кДа, кодируемую orf2 клона рСIВ9369.
SEQ ID NO:4 представляет собой последовательность ДНК orf1 клона Xenorhabdus nematophilus pCIB9381.
SEQ ID NO:5 представляет собой последовательность протеина, кодируемого orf1 клона pCIB9381.
SEQ ID NO:6 представляет собой последовательность ДНК orf2 клона Xenorhabdus nematophilus pCIB9381.
SEQ ID NO:7 представляет собой последовательность сходного с протеином эстеразы ювенильного гормона, кодируемую orf2 клона pCIB9381.
SEQ ID NO:8 представляет собой последовательность ДНК orf1 клона Xenorhabdus poinarii pCIB9354.
SEQ ID NO:9 представляет собой последовательность протеина, кодируемого orf1 клона pGIB9354.
SEQ ID NО:10 представляет собой последовательность ДНК orf2 клона Xenorhabdus poinarii pCIB9354.
SEQ ID NO:11 представляет собой последовательность сходного с протеином эстеразы ювенильного гормона, кодируемую orf2 клона pCIB9354.
SEQ ID NО:12 представляет собой последовательность ДНК orf1 клона Photorhabdus luminescens pCIB9383-21.
SEQ ID NО:13 представляет собой последовательность протеина, кодируемого orf1 клона pCIB9383-21.
SEQ ID NО:14 представляет собой последовательность orf2 клона Photorhabdus luminescens pCIB9383-21.
SEQ ID NO:15 представляет собой последовательность сходного с протеином эстеразы ювенильного гормона, кодируемую orf2 клона pCIB9383-21.
Депонирование
Перечисленные ниже продукты были депонированы в Коллекции запатентованных культур службы сельскохозяйственных исследований (Agricultural Research Service, Patent Culture Collection (NRRL), 1815 Northern University Street, Пеория, Иллинойс 61604, США) в соответствии с Будапештским договором о международном признании депонированных микроорганизмов для целей процедуры патентования. Все ограничения по доступности депонированных продуктов должны быть необратимым образом устранены после выдачи патента.

Новые нуклеотидные последовательности, экспрессия которых приводит к образованию инсектицидных токсинов
Настоящее изобретение относится к нуклеотидным последовательностям, экспрессия которых приводит к образованию новых токсинов, и к получению и применению токсинов для борьбы с насекомыми-вредителями. Нуклеотидные последовательности выделяют из Xenorhabdus nematophilus, Xenorhabdus poinarii и Photorhabdus luminescens, являющихся представителями семейства Enterobacteriaceae. Бактерии рода Xenorhabdus представляют собой симбиотические бактерии нематод рода Steinernema. Бактерии рода Photorhabdus представляют собой симбиотические бактерии нематод рода Heterorhabditis. Нематоды колонизируют личинку насекомого, убивают ее и их потомство питается мертвой личинкой. В действительности инсектицидная активность обусловлена симбиотическими бактериями р.р. Xenorhabdus и Photorhabdus. Заявители были первыми, кому удалось выделить нуклеотидные последовательности по настоящему изобретению. Экспрессия нуклеотидных последовательностей по настоящему изобретению приводит к образованию токсинов, которые могут быть использованы для борьбы с чешуекрылыми насекомыми, такими как Plutella xylostella (моль капустная).
Нуклеотидная последовательность по настоящему изобретению, содержащаяся в клоне рСIВ9369, характеризуется наличием фрагмента ДНК длиной приблизительно 3,0 т.п.н., который депонирован согласно Будапештскому договору о депонировании для целей патентования под регистрационным номером NRRL В-21883. Последовательность этого фрагмента ДНК представлена в SEQ ID NО:1. В SEQ ID NО:1 присутствуют две открытые рамки считывания (ORF) (нуклеотиды 569-979 и нуклеотиды 1045-2334 соответственно), кодирующие протеины с предсказанными молекулярными массами 15 кДа и 47,7 кДа (последовательности SEQ ID NО:2 и SEQ ID NО:3 соответственно). Две ORF упорядочены в виде оперон-подобной структуры. Поиск известных последовательностей, обладающих гомологией с каждой отдельной ORF, с помощью программ UWGCG Blast и Gap не выявил последовательности, обладающей какой-либо значительной гомологией с ОRF№1, и выявил лишь 21%-ную идентичность между ОRF№2 и последовательностью протеина cry3А Bacillus thuringiensis, которая в данной области не считается значительной. Gap-анализ протеина, кодируемого ORF№2 рСIВ9369, проведенный с помощью программы Blast, выявил 30,6%-ную идентичность аминокислотной последовательности и 44,1%-ное сходство аминокислотной последовательности с последовательностью протеина, связанного с эстеразой ювенильного гормона (GenBank, регистрационный номер 2921553, Henikoff и др., PNAS USA 89: 10915-10919 (1992)). Нуклеотидную последовательность по настоящему изобретению также сравнивали с известными последовательностями Xenorhabdus nematophilus, кодирующими инсектицидный токсин tox4 (WO 95/00647), однако значительной гомологии обнаружено не было. Фрагмент ДНК длиной 3,0 т.п.н. также сравнивали с нуклеотидной последовательностью, опубликованной в WO 98/08388. С использованием программы UWGCG Gap сравнивали двадцать две последовательности по 60 нуклеотидов каждая (60-меры) из фрагмента ДНК длиной 38,2 т.п.н., описанного в WO 98/08388, с фрагментом ДНК длиной 3,0 т.п.н. по настоящему изобретению. Нуклеотидная последовательность первого 60-мера начинается с основания 1 фрагмента ДНК длиной 38,2 т.п.н., а остальные 60-меры расположены с интервалами приблизительно 2,0 т.п.н. Анализировали каждую из 22 последовательностей, а также комплементарные им последовательности. Наибольший процент идентичности, который был обнаружен между фрагментом ДНК длиной 3,0 т.п.н. по настоящему изобретению и одним из этих 60-меров, был равен 53%, что не считается значительной гомологией. Кроме того, методом Саузерн-блоттинга пять различных фрагментов ДНК последовательности длиной 38,2 т.п.н. тестировали в отношении гибридизации с фрагментом ДНК длиной 3,0 т.п.н. по настоящему изобретению. Ни для одной из них не был выявлен положительный сигнал гибридизации.
В нуклеотидных последовательностях каждого из клонов рСIВ9381, рСIВ9354 и рСIВ9383-21 также были обнаружены две открытые рамки считывания. Нуклеотидные последовательности двух ORF в каждом из рСIВ9381 и рСIВ9383-21 обладали высокой степенью гомологии с последовательностями ORF рСIВ9369. Следовательно, ОRF№2 протеинов рСIВ981 и рСIВ9383-21 обладают практически такой же гомологией с протеином, связанным с эстеразой ювенильного гормона, что и ОRF№2 протеина рСIВ9369. Нуклеотидная последовательность ОRF№1 рСIВ9354 на 77% идентична нуклеотидной последовательности ORF№1 рСIВ9369, нуклеотидная последовательность ОRF№2 рСIВ9354 на 79% идентична нуклеотидной последовательности ОRF№2 pCIB9369. ORF№2 протеина рСIВ9354 также обладает гомологией с протеином, связанным с эстеразой ювенильного гормона (29,2%-ная идентичность аминокислотных последовательностей, 42,2%-ное сходство аминокислотных последовательностей).
В предпочтительном варианте осуществления изобретение включает нуклеотидную последовательность, практически аналогичную нуклеотидам 569-979 SEQ ID NO:1, нуклеотидам 1045-2334 SEQ ID NO:1, SEQ ID NO:4, SEQ ID NO:6, SEQ ID NO:8, SEQ ID NO:10, SEQ ID NO:12 и SEQ ID NO:14, экспрессия которых приводит к образованию инсектицидного токсина. Под объем настоящего изобретения также подпадают рекомбинантные векторы, содержащие нуклеотидные последовательности по настоящему изобретению. В этих векторах нуклеотидные последовательности предпочтительно включены в кассеты экспрессии, содержащие регуляторные элементы, необходимые для экспрессии нуклеотидных последовательностей в клетке-хозяине, способные экспрессировать нуклеотидные последовательности. Такие регуляторные элементы, как правило, включают промотор и сигналы терминации, и они предпочтительно также включают элементы, позволяющие осуществлять эффективную трансляцию полипептидов, кодируемых нуклеотидными последовательностями по настоящему изобретению. Векторы, включающие нуклеотидные последовательности, как правило, обладают способностью реплицироваться в конкретных клетках-хозяевах, предпочтительно в виде внехромосомных молекул, и, следовательно, их можно использовать для амплификации нуклеотидных молекул по настоящему изобретению в клетках-хозяевах. В одном из вариантов осуществления клетки-хозяева для таких векторов представляют собой микроорганизмы, такие как бактерии, прежде всего Е.coli. В другом варианте осуществления клетки-хозяева для таких рекомбинантных векторов представляют собой эндофиты или эпифиты. Предпочтительной клеткой-хозяином для таких векторов является эукариотическая клетка, такая как клетка дрожжей, клетка растения или клетка насекомого. Наиболее предпочтительными клетками-хозяевами являются клетки растения, такие, как клетки кукурузы. В другом предпочтительном варианте осуществления такими векторами являются вирусные векторы и их используют для репликации нуклеотидных последовательностей в конкретных клетках-хозяевах, например, клетках насекомых или клетках растений. Для трансформации клеток-хозяев нуклеотидными последовательностями по настоящему изобретению также применяют рекомбинантные векторы, при этом нуклеотидные последовательности стабильно интегрируют в ДНК таких клеток-хозяев. В одном из вариантов осуществления такими клетками-хозяевами являются прокариотические клетки. В предпочтительном варианте осуществления такие клетки-хозяева представляют собой эукариотические клетки, такие как клетки дрожжей, клетки насекомых или клетки растений. В наиболее предпочтительном варианте осуществления клетки-хозяева представляют собой клетки растения, такие как клетки кукурузы.
Нуклеотидные последовательности по изобретению могут быть выделены с помощью методов, описанных ниже в примерах, или с помощью ПЦР с использованием последовательностей, перечисленных в перечне последовательностей, в качестве основы для конструирования праймеров для ПЦР. Например, олигонуклеотиды, имеющие последовательности, включающие соответственно первые и последние 20-25 последовательных пар нуклеотидов последовательности orf1 SEQ ID NO:1 (например, нуклеотиды 569-588 и 957-976 SEQ ID NO:1) могут быть использованы в качестве праймеров для ПЦР для амплификации кодирующей последовательности orf1 (нуклеотиды 569-976 SEQ ID NO:1) непосредственно из штамма-источника (штамм Xenorhabdus nematophilus ATCC 19061). Аналогичным образом из соответствующих штаммов-источников с помощью ПЦР с использованием концов кодирующих последовательностей, перечисленных в перечне последовательностей, в качестве основы для праймеров для ПЦР могут быть амплифицированы другие последовательности генов по изобретению.
В другом предпочтительном варианте осуществления инсектицидные токсины включают по меньшей мере один полипептид, кодируемый нуклеотидной последовательностью по изобретению. Молекулярная масса инсектицидного токсина по настоящему изобретению по данным экспериментов с фракционированием по размерам составляет более 6000 Да. После обработки протеиназой К в биоанализе на насекомых наблюдается лишь минимальное уменьшение инсектицидной активности, это свидетельствует о том, что инсектицидные токсины практически устойчивы к обработке протеиназой К. Инсектицидные токсины сохраняют свою инсектицидную активность после хранения в течение 2 недель при 22°С или при 4°С. Они также сохраняют свою инсектицидную активность после высушивания замораживанием и хранения в течение 2 недель при 22°С. Инсектицидные токсины также еще обладают активностью после инкубации в течение 5 мин при 60°С, однако они теряют свою инсектицидную активность после инкубации в течение 5 мин при 100°С или при 80°С.
Согласно другим вариантам осуществления нуклеотидные последовательности по настоящему изобретению могут быть модифицированы путем включения неспецифических (случайных) мутаций с помощью метода, известного как рекомбинация in-vitro или перестановка ДНК. Этот метод описан у Stemmer и др., Nature 370: 389-391 (1994) и в патенте США 5605793, которые включены в настоящее описание в виде ссылок. На основе исходной нуклеотидной последовательности, представленной в настоящем описании, и ее вариантов с улучшенными свойствами, такими как повышенная инсектицидная активность, повышенная стабильность или различная специфичность или более широкий спектр насекомых-вредителей, являющихся мишенями, получают миллионы копий нуклеотидных последовательностей с мутациями. Метод предусматривает формирование двухцепочечного полинуклеотида с мутацией на основе матрицы, представляющей собой двухцепочечный полинуклеотид, который включает нуклеотидную последовательность по настоящему изобретению, причем представляющий собой матрицу двухцепочечный полинуклеотид расщеплен на два двухцепочечных случайных фрагмента требуемого размера, и предусматривает стадии добавления к полученной популяции двухцепочечных случайных фрагментов одного или нескольких одно- или двухцепочечных олигонуклеотидов, причем эти олигонуклеотиды включают область идентичности и область гетерологичности относительно представляющего собой матрицу двухцепочечного полинуклеотида; денатурации полученной смеси двухцепочечных случайных фрагментов и олигонуклеотидов с получением одноцепочечных фрагментов; инкубации полученной популяции одноцепочечных фрагментов с полимеразой в условиях, которые приводят к ренатурации этих одноцепочечных фрагментов в указанных областях идентичности с получением пар ренатурированных фрагментов, причем этих областей идентичности достаточно для примирования репликации одного из членов пары другим, что приводит к получению двухцепочечного полинуклеотида с мутацией; и повторения второй и третьей стадий по меньшей мере еще в течение двух циклов, причем полученная на второй стадии дополнительного цикла смесь включает двухцепочечный полинуклеотид с мутацией, полученный на третьей стадии предыдущего цикла, и с помощью дополнительного цикла получают дополнительное количество двухцепочечного полинуклеотида с мутацией. Согласно предпочтительному варианту осуществления концентрация отдельных видов двухцепочечного случайного фрагмента в популяции двухцепочечных случайных фрагментов составляет менее 1% в пересчете на массу общей ДНК. Согласно другому предпочтительному варианту осуществления представляющий собой матрицу двухцепочечный нуклеотид включает по меньшей мере примерно 100 видов полинуклеотидов. Согласно еще одному предпочтительному варианту осуществления размер двухцепочечных случайных фрагментов составляет примерно от 5 пар оснований до 5 т.п.н. И согласно еще одному предпочтительному варианту осуществления четвертая стадия способа включает повторение второй и третьей стадий по меньшей мере в течение 10 циклов.
Экспрессия нуклеотидных последовательностей в гетерологичных микроорганизмах-хозяевах
Инсектицидные токсины, представляющие собой биологические агенты для борьбы с насекомыми, продуцируются при экспрессии нуклеотидных последовательностей в гетерологичных клетках-хозяевах, способных экспрессировать нуклеотидные последовательности. В первом варианте осуществления описаны клетки Xenorhabdus nematophilus, Xenorhabdus poinarii и Photorhabdus luminescens, включающие модификации по меньшей мере одной нуклеотидной последовательности по настоящему изобретению в месте ее расположения в хромосоме. Такие модификации включают мутации или делеции существующих регуляторных элементов, приводящие к изменению экспрессии нуклеотидной последовательности, или включение новых регуляторных элементов, контролирующих экспрессию нуклеотидной последовательности. В другом варианте осуществления в клетки Xenorhabdus nematophilus, Xenorhabdus poinarii и Photorhabdus luminescens вводят дополнительные копии одной или нескольких нуклеотидных последовательностей либо путем встраивания в хромосому, либо путем интродукции реплицирующихся вне хромосомы молекул, которые содержат нуклеотидные последовательности.
Еще в одном варианте осуществления по меньшей мера одну нуклеотидную последовательность по изобретению встраивают в пригодную кассету экспрессии, содержащую промотор и сигналы терминации. Экспрессия нуклеотидной последовательности может быть конститутивной или для инициации трансляции может быть использован индуцибельный промотор, реагирующий на различные типы стимулов. В предпочтительном варианте осуществления клетка, в которой экспрессируется токсин, представляет собой микроорганизм, такой как вирус, бактерия или гриб. В предпочтительном варианте осуществления вирус, такой как бакуловирус, содержит нуклеотидную последовательность по изобретению в своем геноме и экспрессирует большие количества соответствующего инсектицидного токсина после заражения соответствующих эукариотических клеток, пригодных для репликации вируса и экспрессии нуклеотидной последовательности. Продуцируемый таким образом инсектицидный токсин используется в качестве инсектицидного агента. В альтернативном варианте используют бакуловирусы, сконструированные так, чтобы они включали нуклеотидную последовательность, для того, чтобы инфицировать насекомых in vivo и убивать их либо в результате экспрессии инсектицидного токсина, либо с помощью сочетания вирусной инфекции и экспрессии инсектицидного токсина.
Бактериальные клетки также могут служить в качестве хозяев для экспрессии нуклеотидных последовательностей по изобретению. В предпочтительном варианте используют непатогенные симбиотические бактерии, которые способны жить и размножаться в тканях растений, так называемые эндофиты, или непатогенные симбиотические бактерии, которые способны колонизировать филлосферу или ризосферу, так называемые эпифиты. Такие бактерии включают бактерии родов Agrobacterium, Alcaligenes, Azospirillum, Azotobacter, Bacillus, Clavibacter, Enterobacter, Erwinia, Flawobacter, Klebsiella, Pseudomonas, Rhizobium, Serratia, Streptomyces и Xanthomonas. Симбиотические грибы, такие как Trichoderma и Gliocladium, также являются возможными хозяевами для экспрессии нуклеотидных последовательностей по изобретению с указанной целью.
Методы осуществления таких генетических манипуляций известны в данной области, и они являются специфическими в отношении различных пригодных хозяев. Например, для экспрессии гетерологичных генов в Е. coli могут использоваться экспрессионные векторы рКК.223-3 и рКК.223-2, встроенные в виде транскрипционного или трансляционного слияния под контролем промотора tac или trc. Для экспрессии оперонов, кодирующих множественные ORF, наиболее простой метод состоит во встраивании оперона в виде транскрипционного слияния в такой вектор как рКК.223-3, что позволяет использовать родственный сайт связывания рибосомы гетерологичных генов. В данной области также известны методы осуществления сверхэкспрессии в грамположительных видах, таких как Bacillus, и они могут использоваться в контексте настоящего изобретения (Quax и др., Industrial Microorganisms: Basic and Applied Molecular Genetics, Baltz и др. (ред-ры), American Society for Microbiology, Washington (1993)). Альтернативные системы для обеспечения сверхэкспрессии основаны, например, на дрожжевых векторах, и они включают использование Pichia, Saccharomyces и Kluyveromyces (Sreekrishna, Industrial Microorganisms: Basic and Applied Molecular Genetics, Baltz, Hegeman и Skatrud (ред-ры), American Society for Microbiology, Washington (1993)); Deguin и Barre, Biotechnology 12: 173-177 (1994); van den Berg и др., Biotechnology 8: 135-139 (1990)).
В другом предпочтительном варианте осуществления по меньшей мере одну из описанных нуклеотидных последовательностей переносят и экспрессируют в штамме Pseudomonas fluorescens CGA267356 (описанный в опубликованной заявке на патент EU 0472494 и в WO 94/01561), который обладает характеристиками, необходимыми для биологической борьбы. В другом предпочтительном варианте осуществления нуклеотидную последовательность по изобретению переносят в штамм Pseudomonas auerofaciens 30-84, который также обладает характеристиками, необходимыми для биологической борьбы. Экспрессия в гетерологичных штаммах, предназначенных для биологической борьбы, требует отбора векторов, пригодных для репликации в выбранном хозяине, и соответствующего выбора промотора. В данной области хорошо известны методы осуществления экспрессии в грамотрицательных и грамположительных бактериях и грибах.
Экспрессия нуклеотидных последовательностей в тканях растения
В наиболее предпочтительном варианте осуществления по крайней мере один из инсектицидных токсинов по изобретению экспрессируют в высшем организме, например, в растении. В этом случае трансгенные растения, экспрессирующие эффективные количества токсинов, защищают сами себя от насекомых-вредителей. Если насекомое начинает поедать такое трансгенное растение, то оно также поглощает экспрессированные токсины. Это может отпугнуть насекомое от дальнейшего поедания ткани растения или даже может оказать на него отрицательное воздействие или убить насекомое. Нуклеотидную последовательность по настоящему изобретению встраивают в экспрессионную кассету, которую предпочтительно стабильно интегрируют в геном растения. В другом предпочтительно варианте осуществления нуклеотидную последовательность включают в непатогенный саморплицирующийся вирус. Растения, трансформированные согласно настоящему изобретению, могут предоставлять собой однодольные или двудольные растения, такие как кукуруза, пшеница, ячмень, рожь, сладкий картофель, бобы, горох, цикорий, салат, капуста, цветная капуста, брокколи, турнепс, редис, шпинат, спаржа, лук, чеснок, перец, сельдерей, тыква крупноплодная, тыква пепо, конопля, цуккини, яблоня, груша, айва, дыня, слива, вишня, персик, нектарин, абрикос, земляника, виноград, малина, ежевика, ананас, авокадо, папайя, манго, банан, соя, табак, томаты, сорго, сахарный тростник, сахарная свекла, подсолнечник, рапс, клевер, табак, морковь, хлопчатник, люцерна, рис, картофель, баклажан, огурец, Arabidopsis thalaiana и древесные растения, такие как хвойные и лиственные деревья, но не ограничены ими.
После того как требуемой нуклеотидой последовательностью трансформированы определенные виды растений, она может быть размножена в этих видах или перенесена в другие сорта этих же видов, прежде всего в имеющие коммерческое значение сорта, с помощью традиционных методов селекции.
Нуклеотидную последовательность по настоящему изобретению предпочтительно экспрессируют в трансгенных растениях, приводя таким образом к биосинтезу соответствующего токсина в трансгенном растении. Таким путем получают трансгенные растения, обладающие повышенной устойчивостью к насекомым. Для их экспрессии в трансгенных растениях молекулы ДНК могут нуждаться в модификации и оптимизации. Хотя во многих случаях гены микроорганизмов могут экспрессироваться с высоким уровнем в растениях без модификации, низкая экспрессия в трансгенных растениях может быть обусловлена тем, что нуклеотидные последовательности микроорганизмов имеют кодоны, которые не являются предпочтительными для растений. В данной области известно, что все организмы обладают конкретными предпочтениями в отношении наиболее часто встречающегося кодона, и кодоны в нуклеотидной последовательности, которая включает молекулы ДНК по настоящему изобретению, могут быть заменены для того, чтобы соответствовать специфическим предпочтениям растения, с сохранением аминокислотных последовательностей, которые кодируются ими. Кроме того, высокий уровень экспрессии в растениях наиболее легко достигается при использовании кодирующих последовательностей, в которых содержание GC составляет по меньшей мере приблизительно 35%, предпочтительно более чем приблизительно 45%, более предпочтительно более чем приблизительно 50%, и наиболее предпочтительно более чем приблизительно 60%. Нуклеотидные последовательности микроорганизмов, имеющие низкое содержание GC, могут плохо экспрессироваться из-за присутствия мотивов АТТТА, которые могут дестабилизировать транскрипты, и мотивов ААТААА, которые могут вызывать неадекватное полиаденилирование. Хотя предпочтительные последовательности генов могут соответствующим образом экспрессироваться как в однодольных, так и в двудольных видах растений, последовательности могут быть модифицированы для того, чтобы удовлетворять специфическим предпочтениям однодольных или двудольных растений в отношении кодона и в отношении содержания GC, поскольку, как было установлено, эти предпочтения является различными (Murray и др., Nucl. Acid. Res. 17: 477-498 (1989)). Кроме того, нуклеотидные последовательности подвергают скринингу в отношении наличия незаконных сайтов сплайсинга, которые могут приводить к укорачиванию транскриптов. Все необходимые изменения в нуклеотидных последовательностях, такие как описанные выше изменения, осуществляют с помощью хорошо известных методов сайтнаправленного мутагенеза, ПЦР и конструирования синтетических генов с помощью методов, описанных в опубликованных заявках на патент ЕР 0385962 (на имя фирмы Monsanto), EP 0359472 (на имя фирмы Lubrisol) и WO 93/07278 (на имя фирмы Ciba-Geigy).
Для эффективной инициации трансляции может оказаться необходимым модифицировать последовательности, соседние с сайтом инициации метионина. Например, они могут быть модифицированы путем включения последовательностей, для которых известно, что они являются эффективными в растениях. Joshi предложил пригодную для растений консенсусную последовательность (NAR 15: 6643-6653 (1987)), а фирмой Clontech предложен дополнительный консенсусный инициатор трансляции (каталог 1993/1994 г., стр. 210). Эти консенсусные последовательности могут применяться с нуклеотидными последовательностями по данному изобретению. Эти последовательности включают в конструкции, которые содержат нуклеотидную последовательность, до ATG включительно (оставляя при этом вторую аминокислоту немодифицированной) или в альтернативном варианте до следующего за ATG кодона GTC включительно (в этом случае допускается возможность модификации второй аминокислоты трансгена).
В трансгенных растениях экспрессия нуклеотидных последовательностей находится под контролем промотора, для которого установлена способность функционировать в растениях. Выбор промотора может варьироваться в зависимости от временной и пространственной схемы экспрессии, а также в зависимости от целевых видов. Так предпочтительной является экспрессия нуклеотидных последовательностей по настоящему изобретению в листьях, в початках, в соцветиях (например, в колосьях, метелках, стержнях кукурузных початков и т.д.), в корнях и/или в проростках. Однако во многих случаях требуется иметь защиту от более чем одного типа насекомых-вредителей, поэтому желательно, чтобы экспрессия происходила в нескольких видах ткани. Хотя установлено, что многие промоторы из двудольных растений могут функционировать в однодольных и наоборот, в идеальном варианте для экспрессии в двудольных выбирают промоторы двудольных, и для экспрессии в однодольных выбирают промоторы однодольных. Однако не существует ограничений в отношении источника выбранных промоторов; достаточно, чтобы они были функционально активными в отношении контроля экспрессии молекул ДНК в требуемой клетке.
Предпочтительные промоторы, которые экспрессируются конститутивно, включают промоторы из генов, кодирующих актин или убикитин, и промоторы 35S и 19S CaMV. Нуклеотидные последовательности по настоящему изобретению также могут экспрессироваться под контролем химически регулируемых промоторов. Это позволяет синтезировать инсектицидные токсины только тогда, когда культурные растения обрабатывают индуцирующими химическими соединениями. Предпочтительный метод химической индукции экспрессии генов подробно описан в опубликованной заявке ЕР 0332104 (на имя фирмы Ciba-Geigy) и в патенте США 5614395. Предпочтительным химически индуцируемым промотором является промотор PR-1a табака.
Предпочтительной категорией промоторов являются индуцируемые ранением промоторы. Описаны многочисленные промоторы, которые обеспечивают экспрессию в местах ранения, а также в местах заражения патогеном. В идеальном варианте такой промотор должен проявлять активность только локально в месте инфекции, и в этом случае инсектицидные токсины накапливаются только в тех клетках, в которых необходимо синтезировать инсектицидные токсины для того, чтобы убить атакующее насекомое-вредитель. Предпочтительные промоторы этого типа включают промоторы, описанные у Stanford и др., Mol. Gen. Genet. 215: 200-208 (1989), у Xu и др. Plant Molec. Biol. 22: 573-588 (1993), у Logemann и др. Plant Cell 1: 151-161 (1989), у Rohrmeier и Lehle, Plant Molec. Biol. 22: 783-792 (1993), у Firek и др. Plant Molec. Biol. 22: 129-142 (1993) и у Warner и др. Plant J. 3: 191-201 (1993)).
Предпочтительные тканеспецифичные схемы экспрессии включают экспрессию, специфичную для зеленой ткани, специфичную для корня, специфичную для стебля и специфичную для цветка. Промоторы, пригодные для экспрессии в зеленой ткани, включают многие промоторы, которые регулируют экспрессию генов, участвующих в фотосинтезе, и многие из них, происходящие как из однодольных, так и из двудольных растений, были клонированы. Предпочтительным промотором является промотор РЕРС гена фосфоенолкар-боксилазы кукурузы (Hudspeth и Grula, Plant Molec. Biol. 12: 579-589 (1989)). Предпочтительным промотором для специфичной для корня экспрессии является промотор, описанный de Framond (FEBS 290: 103-106 (1991); ЕР 0452269 на имя фирмы Ciba-Geigy). Предпочтительным специфичным для стебля промотором является промотор, описанный в патенте США 5625136 (на имя фирмы Ciba-Geigy), который контролирует экспрессию гена trpA кукурузы.
В предпочтительных вариантах осуществления изобретения трансгенные растения экспрессируют нуклеотидные последовательности по изобретению специфичным для корня образом. В других предпочтительных вариантах осуществления трансгенные растения экспрессируют нуклеотидные последовательности под контролем промотора, индуцируемого ранением или индуцируемого заражением патогеном.
Помимо выбора приемлемого промотора, в конструкциях, предназначенных для экспрессии протеина в растениях, требуется наличие соответствующего терминатора транскрипции, который должен быть присоединен по ходу транскрипции относительно гетерологичной нуклеотидной последовательности. В данной области известны и могут использоваться несколько таких терминаторов (например, tm1 CaMV, E9 rbcS). Согласно настоящему изобретению может применяться любой терминатор, для которого известно, что он функционируют в растениях.
В кассеты экспрессии, представленные в данном описании, могут быть включены многочисленные другие последовательности. Они включают последовательности, для которых установлена способность усиливать экспрессию, такие как интронные последовательности (например, генов Adh1 и bronze1) и вирусные лидерные последовательности (например, вируса табачной мозаики (TMV), вируса хлорозной пятнистости кукурузы (MCMV) и вируса мозаики люцерны (AMV)).
Может оказаться предпочтительным направлять экспрессию молекул ДНК в различные клеточные компартменты растения. В некоторых случаях может требоваться локализация в цитозоле, в то время как в других случаях может быть предпочтительной локализация в какой-либо субклеточной органелле. Субклеточная локализация кодируемого трансгеном фермента может осуществляться с помощью хорошо известных в данной области методов. Как правило, ДНК, кодирующую направляющий пептид из известного генного продукта, осуществляющего направленный перенос в определенную органеллу, обрабатывают и сливают против хода транскрипции относительно нуклеотидной последовательности. Для хлоропласта известен целый ряд таких направляющих перенос последовательностей и установлено, что они функционируют в гетерологичных конструкциях. Экспрессию нуклеотидных последовательностей по настоящему изобретению также направляют в эндоплазматический ретикулум или в вакуоли клеток-хозяев. В данной области хорошо известны методы, позволяющие достичь этого.
Векторы, пригодные для трансформации растений, приведены ниже в настоящем описании. Для опосредованной Adrobacterium трансформации могут применяться бинарные векторы или векторы, несущие по меньшей мере одну пограничную последовательность Т-ДНК, однако для прямого переноса гена пригоден любой вектор и может оказаться предпочтительной линейная ДНК, содержащая только представляющую интерес конструкцию. В случае прямого переноса генов может применяться трансформация отдельными видами ДНК или котрансформация (Schocher и др., Biotechnology 4: 1093-1096 (1986)). Как для прямого переноса генов, так и для опосредованного Adrobacterium переноса обычно (но не обязательно) применяют трансформацию с использованием селектируемого маркера, который может придавать устойчивость к антибиотику (канамицин, гигромицин или метатрексат) или гербициду (баста). Примерами таких маркеров являются неомицинтрансфераза, гигромицинфосфотрансфераза, дигидрофолатредуктаза, фосфинотрицинацетилтрансфераза, дегалогеназа 2,2-дихлорпропионовой кислоты, синтаза ацетооксикислот, 5-енолпирувилшикимат-фосфатсинтаза, галоарилнитрилаза, протопорфириногеноксидаза, ацетил-СоА-карбоксилаза, дигидроптероатсинтаза, хлорамфениколацетилтрансфераза и β-глюкуронидаза. Однако выбор селектируемого маркера не имеет решающего значения для изобретения.
Описанные выше рекомбинантные молекулы ДНК по изобретению могут быть интродуцированы в растительную клетку многочисленными известными в данной области методами. Специалистам в данной области должно быть очевидно, что выбор метода может зависеть от типа растения, предназначенного для трансформации. Пригодные методы трансформации растительных клеток включают микроинъекцию (Crossway и др., BioTechniques 4: 320-334 (1986)), электропорацию (Riggs и др., Proc. Natl. Acad. Sci. USA, 83: 5602-5606 (1986); трансформацию, опосредуемую Agrobacterium (Hinchee и др., Biotechnology 6: 915-921 (1988); (касательно трансформации растений кукурузы см. у Ishida и др., Nature Biotechnology 14: 745-750 (июнь 1996)), непосредственный перенос гена (Paszkowski и др., EMBO J. 3: 2717-2722 (1984)), баллистическое введение частиц с помощью устройств, поставляемых фирмами Agracetus, Inc., Madison, Wisconsin и Dupont, Inc. Wilmington, Delaware (см., например, у Sanford и др., патент США 4945050; и у McCabe и др., Biotechnology 6: 923-926 (1988)). См. также у Weissinger и др., Annual Rev. Genet. 22: 421-477 (1988); Sanford и др., Particulate Science and Technology 5: 27-37 (1987) (лук); Svab и др., Proc. Natl. Acad. Sci. USA 87: 8526-8530 (1990) (хлоропласт табака); Christou и др., Plant Physiol. 87: 671-674 (1988) (соя); McCabе и др., Bio/Technology 6: 923-926 (1988) (соя); McCabe и др., Bio/Technology 6: 923-926 (1988) (соя); Klein и др., Proc. Natl. Acad. Sci. USA, 85: 4305-4309 (1988) (кукуруза); Klein и др., Bio/Technology 6: 559-563 (1988) (кукуруза); Klein и др., Plant Physiol. 91: 440-444 (1988) (кукуруза); Fromm и др., Bio/Technology 8: 833-839 (1990); Gordon-Kamm и др., Plant Cell 2: 603-618 (1990) (кукуруза); Koziel и др., Biotechnology 11: 194-200 (1993) (кукуруза); Shimamoto и др., Nature 338: 274-277 (1989) (рис); Christou и др., Biotechnology 9: 957-962 (рис); Datta и др., Bio/Technology 8: 736-740 (1990) (рис); заявка на европейский патент ЕР 0332581 (ежа сборная и другие виды Pooideae); Vasil и др., Biotechnology 11: 1553-1558 (1993) (пшеница); Weeks и др., Plant Physiol. 102: 1077-1084 (1993) (пшеница); Wan и др.. Plant Physiol. 104; 37-48 (1994) (ячмень); Jahne и др., Theor. Appl. Genet. 89: 525-533 (1994) (ячмень); Umbeck и др., Bio/Technology 5: 263-266 (1987) (хлопчатник); Casas и др., Proc. Natl. Acad. Sci. USA, 90: 11212-11216 (декабрь 1993) (сорго); Somers и др., Bio/Technology 10: 1589-1594 (декабрь 1992) (овес); Torbert и др., Plant Cell Reports 14: 635-640 (1995) (овес); Weeks и др., Plant Physiol. 102: 1077-1084 (1993) (пшеница); Chang и др., WO 94/13822 (пшеница) и Nehra и др., The Plant Journal 5: 285-297 (1994) (пшеница). Наиболее предпочтительный ряд вариантов осуществления интродукции рекомбинантных молекул ДНК в растения кукурузы с помощью бомбардировки микроснарядами можно найти у Koziel и др., Biotechnology 11: 194-200 (1993), у Hill и др., Euphytica 85: 119-123 (1995) и у Koziel и др., Annals of the New York Academy of Sciences 792: 164-171 (1996). Дополнительным предпочтительным вариантом осуществления является метод трансформации протопласта кукурузы, описанный в ЕР 0292435. Трансформация может осуществляться с использованием отдельных видов ДНК или нескольких видов ДНК (т.е. котрансформация), и оба эти метода пригодны для использования с применением последовательности, кодирующей пероксидазу.
Согласно другому предпочтительному варианту осуществления нуклеотидной последовательностью по настоящему изобретению непосредственно трансформируют пластидный геном. Основное преимущество пластидной трансформации заключается в том, что пластиды, как правило, способны экспрессировать бактериальные гены без существенной модификации и в том, что пластиды способны экспрессировать множественные открытые рамки считывания под контролем одного промотора. Метод трансформации пластид описан подробно в патентах US 5451513, 4545817 и 5545818; в международной заявке на патент WO 95/16783; и у McBride и др., Proc. Natl. Acad. Sci. USA 91: 7301-7306 (1994). Основная методика трансформации хлоропласта включает введение в пригодную ткань-мишень участков клонированной пластидной ДНК, фланкирующих селектируемый маркер вместе с представляющим интерес геном, например, с использованием способа биобаллистического переноса или трансформации протопласта (например, трансформации, опосредуемой хлоридом кальция или ПЭГ). Фланкирующие области длиной 1-1,5 т.п.н., называемые последовательностями, обеспечивающими направленный перенос, облегчают гомологичную рекомбинацию с пластидным геномом и, таким образом, позволяют заменять или модифицировать специфические области пластома. Первоначально в качестве селектируемых маркеров для трансформации использовали точковые мутации в хлоропластных генах 16S-pPHK и rps12, которые обусловливают устойчивость к спектиномицину и/или стрептомицину (Svab Z., Hajdukiewicz P. и Maliga P., Proc. Natl. Acad. Sci. USA 87: 8526-8530 (1990); Staub J.M. и Maliga P., Plant Cell 4: 39-45 (1992). Это приводит к получению стабильных гомоплазматических трансформантов с частотой примерно 1 трансформант на 100 бомбардировок листьев-мишеней. Присутствие клонирующих сайтов между этими маркерами позволяет создавать вектор для интродукции чужеродных генов, обеспечивающий направленный перенос в пластиду (Staub J.M. и Maliga P., EMBO J. 12: 601-606 (1993)). Существенное увеличение частоты трансформации получают, замещая гены рецессивной рРНК или р-протеина, обусловливающие устойчивость к антибиотикам, доминантным селектируемым маркером, бактериальным геном aadA, кодирующим спектиномициндетоксицирующий фермент аминогликозид-3’-аденилтрансферазу (Svab Z. и Maliga P. Proc. Natl. Acad. Sci. USA 90: 913-917 (1993)). Ранее этот маркер был успешно использован для происходящей с высокой частотой трансформации пластидного генома зеленой водоросли Chlamydomonas reinhardtii (Goldschmidt-Clermont M., Nucl. Acids Res. 19: 4083-4089 (1991)). В данной области известны другие селектируемые маркеры, пригодные для трансформации пластид, и они подпадают под объем изобретения. Как правило, для достижения гомопластидного состояния после трансформации требуется приблизительно 15-20 циклов деления клетки. Экспрессия в пластидах, в которые гены встроены путем гомологичной рекомбинации во все несколько тысяч копий кольцевого пластидного генома, присутствующего в каждой растительной клетке, имеет преимущество, состоящее в том, что огромное количество копий, превосходящее количество копий, экспрессируемых генами ядерной ДНК, позволяет обеспечить уровни экспрессии, которые легко могут превысит 10% от общего растворимого протеина растения. В предпочтительном варианте осуществления нуклеотидную последовательность по настоящему изобретению встраивают в вектор, обеспечивающий направленный перенос в пластиду, и трансформируют им пластидный геном соответствующего растения-хозяина. Получают растения, гомопластические в отношении пластидных геномов, которые содержат нуклеотидную последовательность по настоящему изобретению и которые предпочтительно способны осуществлять экспрессию нуклеотидной последовательности с высоким уровнем.
Приготовление препаративных форм, содержащих инсектицидные композиции
Под объем изобретения также подпадают композиции, включающие по крайней мере один из инсектицидных токсинов по настоящему изобретению. Для эффективной борьбы с насекомыми-вредителями такие композиции предпочтительно должны содержать достаточное количество токсина. Эти количества варьируются в зависимости от подлежащей защите культуры, от конкретного вредителя-мишени и от условий окружающей среды, таких как влажность, температура или тип почвы. В предпочтительном варианте осуществления композиции, включающие инсектицидные токсины, содержат клетки-хозяева, экспрессирующие токсины, не подвергнутые дополнительной очистке. В другом предпочтительном варианте осуществления клетки, экспрессирующие инсектицидные токсины, подвергают лиофилизации перед их использованием в качестве инсектицидного агента. В другом варианте осуществления создают такие инсектицидные токсины, которые секретируются клетками-хозяевами. В тех случаях, когда желательна очистка токсинов из клеток-хозяев, в которых они экспрессируются, могут быть достигнуты различные степени очистки инсектицидных токсинов.
Под объем настоящего изобретения также подпадает способ приготовления композиций, включающих по крайней мере один инсектицидный токсин по настоящему изобретению, смешанный до однородного состояния с одним или несколькими соединениями или группами соединений, перечисленных в настоящем описании. Настоящее изобретение также относится к способам обработки растений, предусматривающим обработку растений инсектицидными токсинами или композициями, содержащими инсектицидные токсины. Инсектицидные токсины могут быть внесены в виде композиций на возделываемую посевную площадь или на растение, подлежащее обработке, одновременно или последовательно с другими биологически активными соединениями. Эти соединения могут представлять собой как удобрения или доноры микроэлементов, так и другие препараты, оказывающие влияние на рост растения. Они также могут представлять собой обладающие избирательным действием гербициды, инсектициды, фунгициды, бактерициды, нематоциды, моллюскициды или смеси, состоящие из нескольких этих препаратов, при необходимости вместе с другими носителями, поверхностно-активными веществами или способствующими нанесению адъювантами, обычно применяемыми в области изготовления препаративных форм. Пригодные носители и адъюванты могут быть твердыми или жидкими, и они представляют собой вещества, обычно применяемые в области изготовления препаративных форм, т.е. пригодные или регенерированные минеральные вещества, растворители, диспергирующие агенты, смачивающие агенты, прилипатели, связующие вещества или удобретния.
Предпочтительным способом применения инсектицидных токсинов по настоящему изобретению является опрыскивание местообитания насекомого-вредителя, например почвы, водной поверхности или листьев растения. Количество обработок и нормы внесения зависят от типа и интенсивности заражения насекомым-вредителем. Инсектицидные токсины также могут проникать в растение через корни из почвы (системное действие) в результате пропитки места произрастания растения жидкой композицией или в результате внесения в почву соединений в твердой форме, например в гранулированной форме (внесение в почву). Инсектицидные токсины также могут быть нанесены на семенной материал (покрытие) либо путем пропитки семян жидкой композицией, содержащей инсектицидные токсины, либо нанесения на них покрытия из твердой композиции. В отдельных случаях также можно применять другие типы обработки, например выборочную обработку стволов или почек растения. Инсектицидные токсины также могут применяться в виде приманок, помещенных на поверхности почвы или под ее поверхностью.
Инсектицидные токсины применяют в немодифицированной форме или предпочтительно вместе с адъювантами, обычно применяемые в области техники изготовления препаративных форм, и, следовательно, они могут быть приготовлены обычным способом в виде эмульсионных концентратов, покрывающих паст, готовых к употреблению разбрызгиваемых или разбавляемых растворов, разбавленных эмульсий, смачивающихся порошков, растворимых порошков, дустов, гранул, а также в инкапсулированном виде, например, в полимерных веществах. В зависимости от природы композиций в соответствии с поставленными целями и превалирующими обстоятельствами выбирают способы обработки, такие как опрыскивание, мелкокапельное опрыскивание, опыливание, разбрасывание или орошение.
Препаративные формы, композиции или препараты, содержащие инсектицидные токсины и при необходимости твердый или жидкий адъювант, получают известным способом, например, путем гомогенного смешения и/или размалывания действующих веществ с наполнителями, например с растворителями, твердыми носителями и при необходимости с поверхностно-активными веществами (детергентами).
Пригодные растворители включают ароматические углеводороды, предпочтительно фракции, имеющие 8-12 атомов углерода, например, ксилоловые смеси или замещенные нафталины, фталаты, такие как дибутилфталат или диоктилфталат, алифатические углеводороды, такие как циклогексан или парафины, спирты и гликоли и их простые и сложные эфиры, такие как этанол, монометиловый или моноэтиловый эфиры этиленгликоля, кетоны, такие как циклогексанон, высокополярные растворители такие как N-метил-2-пирролидон, диметилсульфоксид или диметилформамид, а также растительные масла или эпоксидированные растительные масла, такие как эпоксидированное кокосовое масло или соевое масло, или воду.
Твердые носители, применяемые, например, для дустов и диспергируемых порошков, обычно представляют собой природные минеральные наполнители, такие как кальцит, тальк, каолин, монтмориллонит или аттапульгит. Для того чтобы улучшить физические свойства, также можно добавлять высокодисперсную кремниевую кислоту или высокодисперсные адсорбирующие полимеры. Пригодными гранулированными адсорбционными носителями являются таковые пористого типа, например пемза, битый кирпич, сепиолит или бентонит; а пригодными несорбирующим носителями являются такие материалы, как кальцит или песок. Кроме того, может применяться большое число предварительно гранулированных материалов неорганического или органического происхождения, например, особенно предпочтительны доломит или растертые в порошок растительные остатки.
Пригодными поверхностно-активными соединениями являются неионогенные, катионогенные и/или анионогенные поверхностно-активные вещества, обладающие хорошими эмульгирующими, диспергирующими и смачивающими свойствами. Под понятие "поверхностно-активные вещества" также подпадают смеси поверхностно-активных веществ. Пригодные анионогенные поверхностно-активные вещества могут представлять собой как водорастворимые мыла, так и водорастворимые синтетические поверхностно-активные вещества.
Пригодными мылами являются соли щелочных металлов, соли щелочноземельных металлов или незамещенные или замещенные соли аммония и высших жирных кислот (имеющие цепи, содержащие 10-22 атомов углерода), например натриевые или калиевые соли олеиновой или стеариновой кислоты, или смесей природных жирных кислот, которые могут быть получены, например, из кокосового или таллового масла. Кроме того, также могут использоваться метилтауриновые соли жирных кислот.
Более часто, однако, применяют так называемые синтетические поверхностно-активные вещества, особенно жирные сульфонаты, жирные сульфаты, сульфированные производные бензимидазола или алкиларилсульфонаты.
Жирные сульфонаты или сульфаты обычно применяют в виде солей щелочных металлов, солей щелочноземельных металлов или незамещенных или замещенных аммонийных солей, и они обычно имеют алкильный радикал, содержащий 8-22 атомов углерода, который также включает алкильный фрагмент ацильных радикалов, например, в виде натриевой или кальциевой соли лигносульфоновой кислоты, додецилсульфата или смеси сульфатов жирных спиртов, полученных из природных жирных кислот. Эти соединения также включают соли эфиров серной кислоты и аддуктов сульфоновых кислот жирного спирта/этиленоксида. Сульфированные производные бензимидазола предпочтительно содержат 2 группы сульфоновой кислоты и один радикал жирной кислоты, содержащий от 8 от 22 атомов углерода. Примерами алкиларилсульфонатов являются натриевые, кальциевые или триэтаноламиновые соли додецилбензолсульфоновой кислоты, дибутилнафталинсульфоновой кислоты или продукта конденсации нафталинсульфоновой кислоты/формальдегида. Также пригодными являются соответствующие фосфаты, например соли эфира фосфорной кислоты и аддукта пара-нонилфенола с 4-14 молями этиленоксида.
Неионогенные поверхностно-активные вещества предпочтительно представляют собой производные полигликолевого эфира и алифатических или циклоалифатических спиртов, или насыщенных или ненасыщенных жирных кислот и алкилфенолов, эти производные содержат 3-30 гликольных эфирных групп и 8-20 атомов углерода в (алифатическом) углеводородном фрагменте и 6-18 атомов углерода в алкильном фрагменте алкилфенолов.
Кроме того, пригодными неионогенными поверхностно-активными веществами являются водорастворимые аддукты полиэтиленоксида и полипропиленгликоля, этилендиаминпропиленгликоля и алкилпропиленгликоля, содержащие 1-10 атомов углерода в алкильной цепи, причем аддукты содержат 20-250 групп этиленгликолевого эфира и 10-100 групп пропиленгликолевого эфира. Эти соединения обычно содержат 1-5 фрагментов этиленгликоля на фрагмент пропиленгликоля.
Характерными примерами неионогенных поверхностно-активных веществ являются нонилфенолполиэтоксиэтанолы, простые эфиры касторового масла и полигликоля, аддукты полипропилена/полиэтиленоксида, трибутилфеноксипо-лиэтоксиэтанол, полиэтиленгликоль и октилфеноксиэтоксиэтанол. Эфиры жирных кислот и полиоксиэтиленсорбитана, такие как триолеат полиоксиэти-ленсорбитана, также являются пригодными неионогенными поверхностно-активными веществами.
Катионогенные поверхностно-активные вещества предпочтительно представляют собой соли четвертичного аммония, которые имеют в качестве N-заместителя по крайней мере один С8-С22алкильный радикал и, кроме того, в качестве дополнительных заместителей незамещенные или галогенированные низшие алкильные, бензильные или гидрокси-(низший) алкильные радикалы. Предпочтительны соли в виде галогенидов, метилсульфатов или этилсульфатов, например хлорид стеарилтриметиламмония или бромид бензилди(2-хлорэтил)этиламмония.
Поверхностно-активные вещества, обычно применяемые в области приготовления препаративных форм, описаны, например, в "McCutcheon's Detergents and Emulsifiers Annual", MC Publishing Corp. Ridgwood, New Jersey, 1979; и у Sisley и Wood, "Encyclopedia of Surface Active Agents", Chemical Publoshing Co., Inc. New York, 1980.
Примеры
Изобретение описано далее со ссылкой на приведенные ниже примеры. Эти примеры приведены только для целей иллюстрации и не направлены на ограничение объема изобретения, если не указано иное. Использованные стандартные методы рекомбинантной ДНК и молекулярного клонирования хорошо известны в данной области и описаны у Ausubel (ред.), Current Protocols in Molecular Biology, John Wiley and Sons, Inc. (1994); у Т.Maniatis, E.F. Fritsch и J.Sambrook, Molecular Cloning: A Laboratory Manual, Cold Spring Laboratory, Cold Spring Harbor, NY (1989); и у T.J.Silhavy, M.L.Berman и L.W.Enquist, Ezperiments with Gene Fusions, Cold Spring Laboratory, Cold Spring Harbor, NY (1984).
А. Выделение нуклеотидных последовательностей, экспрессия которых приводит к образованию токсинов, обладающих активностью в отношении насекомых из отряда чешуекрылых
Пример 1. Выращивание штаммов Xenorhabdus и Photorhabdus
Для анализов биологической активности в отношении насекомых перечисленные ниже штаммы выращивают в питательной среде, рекомендованной АТСС, при 25°С в течение 3 дней. Для выделения ДНК культуры выращивают в тех же условиях в течение 24 ч.
Штамм Xenorhabdus nematophilus ATCC 19061.
Штамм Xenorhabdus nematophilus Pst1, изолят USDA.
Штамм Xenorhabdus poinarii ATCC 49122.
Штамм Photorhabdus luminescens Ps5, изолят USDA.
Пример 2
Анализы биологической активности в отношении Plutella xylostella (Px) проводят путем внесения аликвот по 50 мкл каждой из культур Е. coli на твердую искусственную питательную среду для Р. xylostella (Biever и Boldt, Annals of Entomological Society of America, 1971; Shelton и др., J. Ent. Sci. 26: 17). По 5 только что вылупившихся гусениц Р. xylostella из лабораторной колонии, адаптированной к корму, помещают в каждую чашку, содержащую корм, и затем закрывают белой бумажной крышкой (продукт фирмы Bioserve №9049). Активность для в каждой концентрации анализируют с использованием 10 гусениц. Лотки с чашками помещают в термостат при 72°F на 3 дня со световым циклом свет:темнота 14:10 (в часах). Регистрируют количество живых гусениц в каждой чашке.
Пример 3. Результаты анализа биологической активности
В анализе биологической активности согласно методу, описанному в примере 2, использование бульона, содержащего штамм Xenorhabdus nematophilus ATCC 19061, приводит к 100%-ной смертности Plutella xylostella (Px). Аналогично этому в анализе биологической активности согласно методу, описанному в примере 2, использование каждого из бульонов, содержащего штамм Xenorhabdus nematophilus Pst1, штамм Xenorhabdus poinarii ATCC 49122 и штамм Photorhabdus luminescens Ps5, приводит к 100%-ной смертности Plutella xylostella (Px).
Пример 4. Конструирование космидной библиотеки
Полную ДНК выделяют из штамма Xenorhabdus nematophilus ATCC 19061 путем обработки свежевыращенных клеток, ресуспендированных в 100 мМ Трис, рН 8, 10 мМ ЭДТК, в течение 30 мин при 37°С лизозимом, взятым в концентрации 2 мг/мл. Добавляют протеиназу К в конечной концентрации 100 мкг/мл в 0,5%-ном ДСН и инкубируют при 45°С. Раствор становится прозрачным и очень вязким. Концентрацию ДСН повышают до 1% и добавляют 300 мМ NaCl и равное количество смеси фенол-хлороформ-изоамиловый спирт. Образец осторожно перемешивают в течение 5 мин и центрифугируют при 3К (3 × лизин). Процесс повторяют дважды. Затем водную фазу смешивают с 0,7 объемами изопропанола и центрифугируют. Дебрис ДНК промывают трижды 70%-ным этанолом и осторожно ресуспендируют в 0,5хТЕ (перемешивающий элемент). 6 мкг ДНК обрабатывают 0,3 ед. Sau3А/мкг ДНК при 37°С в течение 3,5 мин в объеме 100 мкл. Затем образец выдерживают в течение 30 мин при 65°С для инактивации фермента, после чего инкубируют в течение 30 мин при 37°С с 2 ед. щелочной фосфатазы из кишки теленка. Образец смешивают с равным объемом смеси фенол-хлороформ-изоамиловый спирт и центрифугируют. Водную фазу удаляют и смешивают с 0,7 объемами изопропанола и центрифугируют. Дебрис ресуспендируют в 0,5хТЕ с концентрацией 100 нг/мл.
Космидный вектор SuperCos (фирма Stratagene, Ла Джолла, штат Калифорния) получают согласно инструкциям поставщика с использованием сайта клонирования BamHI. Полученный вектор SuperCos в концентрации 100 нг/мл лигируют в течение ночи при 6°С в объеме 5 мкл в соотношении 2:1 с ДНК X. nematophilus, предварительно расщепленной с помощью Sau3A. Полученную в результате лигирования смесь упаковывают с помощью набора Gigapack XL III (фирма Stratagene) согласно инструкциям поставщика. Упакованными фагами инфицируют клетки штамма Е.coli XL-1MR (фирма Stratagene) согласно инструкциям поставщика. Космидную библиотеку высевают на L-агар, содержащий 50 мкг/мл канамицина и инкубируют в течение 16 ч при 37°С. 500 колоний помещают в виде бляшек на свежеобработанные L-kan пластины с плотностью 50 колоний/пластину. Клетки промывают L-бульоном и смешивают с 20%-ным глицерином и замораживают при -80°С.
Для генома X. nematophilus размером 4,2 м.п.н. 450 клонов со средним размером 40 т.п.н. соответствуют 4-кратному перекрытию генома. Следовательно, при скрининге 450 клонов имеется 99%-ная вероятность выявления любого гена.
Космидные библиотеки штамма Xenorhabdus nematophilus Pst1, штамма Xenorhabdus poinarii ATCC 49122 и штамма Photorhabdus luminescens Ps5 конструируют аналогичным образом.
Пример 5. Результаты биологического анализа космид и идентификация клонов, обладающих инсектицидной активностью
Для анализа биологической активности в отношении насекомых подвергают скринингу 400 клонов Е.coli из каждой космидной библиотеки с целью выявления клонов, обладающих активностью в отношении Plutella xylostella. Клонированную космиду штамма Xenorhabdus nematophilus ATCC 19061, обладающую инсектицидной активностью, обозначают как рСIВ9362. Обладающую инсектицидной активностью клонированную космиду длиной 42 т.п.н. из штамма Xenorhabdus nematophilus Pst1 обозначают как рСIВ9379. Обладающую инсектицидной активностью клонированную космиду длиной 42 т.п.н. из штамма Xenorhabdus poinarii ATCC 49122 обозначают как рСIВ9354. Обладающую инсектицидной активностью клонированную космиду длиной 7 т.п.н. из штамма Photorhabdus luminescens Ps5 обозначают как рСIВ9383-21.
Пример 6. Выделение субклонов, обладающих инсектицидной активностью Клон рСIВ9362 расщепляют с помощью SacII и выделяют фрагмент ДНК длиной 9 т.п.н. Этот фрагмент встраивают в вектор Bluescript, расщепленный с помощью SacII. Полученной в результате лигирования смесью трансформируют клетки штамма Е.coli DH5α согласно методу, описанному в Molecular Cloning, 2-е издание (Sambrook и др.). Полученную в результате трансформации смесь высевают на L-агар, содержащий 100 мкг/мл ампициллина, и инкубируют в течение ночи при 37°С. Выделенные колонии выращивают в L-бульоне, содержащем 100 мкг/мл ампициллина, и плазмидную ДНК выделяют с помощью щелочных минипрепов согласно методу, описанному в Molecular Cloning, 2-е издание. Выделенный с помощью SacII клон длиной 9 т.п.н. обозначают как рСIВ9362-3, и он обладает инсектицидной активностью, вызывающей 100%-ную смертность Plutella xylostella. Выделяют 3 мкг рСIВ9362-3, расщепляют с помощью 0,3 ед. Sau3A на 1 мкг ДНК в течение 4, 6 и 8 мин при 37°С и выдерживают при 75°С в течение 15 мин. Образцы объединяют в группы и встраивают в плазмиду pUC19, предварительно расщепленную с помощью BamHI, и обрабатывают щелочной фосфатазой кишки теленка. Полученным в результате лигирования продуктом трансформируют клетки штамма E.coli DH5α, высевают на L-агар, содержащий XgaI/Amp, согласно методу, описанному в Molecular Cloning, и выращивают в течение ночи при 37°С. Колонии белого цвета отбирают и выращивают в L-бульоне, содержащем 100 мкг/мл ампициллина, и плазмидную ДНК выделяют согласно описанному выше методу. ДНК расщепляют с помощью EcoRI/HindIII и новые полученные в результате рестрикции фрагменты подвергают секвенированию. Праймеры для секвенирования получают от фирмы Genosys Biotechnologies (Вудленд, штат Техас). Секвенирование осуществляют согласно дидезокси-методу на основе разрыва цепи и осуществляют с использованием автоматического секвенатора ДНК модели 377 фирмы Applied Biosystems Inc. (Форстер сити, штат Калифорния). Последовательности объединяют с использованием программы Sequencher 3.0 фирмы Gene Code Corporation (Анн Арбор, штат Мичиган).
После идентификации сайтов рестрикции и возможных ORF плазмиду рСIВ9362-3 расщепляют с помощью ClaI и фрагмент длиной 3,0 т.п.н. выделяют, клонируют в векторе Bluescript и трансформируют им клетки штамма Е.coli DH5α. Выделенные колонии выращивают согласно описанному выше методу, и плазмидную ДНК выделяют методом щелочного лизиса. Субклон идентифицируют как рСIВ9369 и он вызывает 100%-ную гибель Plutella xylostella в опытах по изучению биологической активности. Штамм рСIВ9369 депонировали в Коллекции культур для целей патентования USDA ARS 12 ноября 1997 г. под регистрационным номером NRRL В-21883.
Фрагмент длиной 20 т.п.н., обозначенный как рСIВ9381, субклонируют из космиды рСIВ9379, используя расщепление с помощью NotI.
Пример 7. Результаты анализа биологической активности
Анализы биологической активности pCIB9369 проводят для различных видов насекомых.
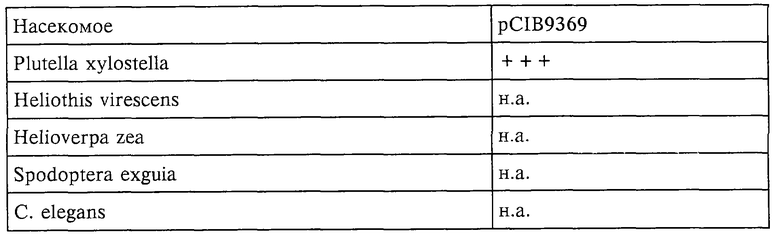
н.а. - не обнаружено активности,
+ - существенное ингибирование роста,
+ + - гибель >40%, но менее 100%,
+ + + - 100%-ная гибель.
Эти результаты свидетельствуют о том, что инсектициный токсин, образующийся в результате экспрессии в pCIB9369 нуклеотидной последовательности длиной 3,0 т.п.н., обладает высокой активностью в отношении Plutella xylostella.
Анализы биологической активности штаммов рСIВ9381, рСIВ9354 и рСIВ9383-21 показывают, что эти штаммы также обладают высокой инсектицидной активностью в отношении Plutella xylostella.
Пример 8. Определение размеров фракции, обусловливающей инсектицидную активность
Космидный клон Xenorhabdus nematophilus pCIB9369 и вектор BlueScript фирмы Stratagene в штамме E.coli DH5α выращивают в среде, состоящей из 50% бульона Terrific и 50% бульона Луриа, дополненной 50 мкг/мл ампициллина. Культуры выращивают во встряхиваемых колбах (300 мл в колбах с перегородками объемом 1000 мл) при 250 об/мин в течение ночи при 37°С. Культуры каждого штамма центрифугируют при 7000 об/мин в центрифуге типа Sorvall GS при 4°С. Пеллетированные клетки ресуспендируют в 30 мл 50 мМ NaCI, 25 мМ Трис-буфера, рН 7,0. Концентрированные клетки разрушали путем облучения ультразвуком с помощью устройства типа Branson Model 450 Sonicator в течение приблизительно восьми 10-секундных циклов с использованием охлаждения на льду в промежутке между циклами. Полученный в результате ультразвукового облучения продукт центрифугируют в центрифуге типа Sorvall SS34 при 6000 об/мин в течение 10 мин при 4°С. Образовавшиеся супернатанты фильтруют через фильтр с размерами пор 0,2 мкм. Дебрисы центрифугированных продуктов, полученных в результате облучения ультразвуком, ресуспендируют в 30 мл 50 мМ NaCl, 25 мМ Трис-буфера, рН 7,0.
Фракции фильтратов объемом по 3 мл вносят в колонки типа Bio-Rad Econo-Pac 10DG, предварительно уравновешенные 10 мл 50 мМ NaCl, 25 мМ Трис-буфера, рН 7,0. Отбрасывают поток, собранный во время загрузки образцов. Образцы фракционируют путем последовательного добавления двух порций по 4 мл каждая уравновешивающего буфера NaCl-Трис. Первые три фракции отбирают для анализа. Первая фракция должна содержать все продукты, имеющие молекулярную массу выше приблизительно 6000 Да. Следующие фракции должны содержать продукты с молекулярной массой меньше, чем 6000 Да.
Образец подвергнутого ультразвуковому облучению фильтрата и ресуспендированный дебрис после ультразвукового облучения тестируют наряду с тремя фракциями, полученными с использованием колонки 10DG, на их активность в отношении свежевылупившихся гусениц Р. xylostella методом контактирования с зараженной поверхностью. Профильтрованный супернатант продукта, полученного в результате облучения, и первая фракция образца 9369, полученная с колонки, оказались высокоэффективными в отношении Р. xylostella. Вторая и третья фракции образца 9369 оказались неактивными. Ни один из образцов, полученных из культуры штамма DH5α в плазмиде BlueScript, не обладал активностью. Эти результаты свидетельствуют о том, что инсектицидная активность, присущая клону X. nematophilus pCIB9369, а также его гомологам рСIВ9381, рСIВ9354 и рСIВ9383-21, обусловлена фрагментом, имеющим молекулярную массу, превышающую 6000 Да.
Пример 9. Стабильность инсектицидной активности
300 мл бульона Луриа, дополненного 100 мкг/мл ампициллина, инокулируют плазмидой pCIB9369 и выращивают в течение ночи при 37°С.
Образцы помещают в стерильные пробирки с завинчивающимися крышками объемом 15 мл и хранят при 22°С и 4°С. Один образец центрифугируют, супернатант удаляют, сушат замораживанием и хранят при 22°С. Эти образцы хранят в указанных условиях в течение 2 недель и затем анализируют их биологическую активность в отношении Р. xylostella. Продукт, получаемый путем сушки замораживанием, ресуспендируют в равном объеме как описано ранее для образца, высушиваемого замораживанием. Все образцы ресуспендируют при встряхивании. Еще один образец выдерживают при 100°С в течение 5 мин.

н.а. – не обнаружено активности
Пример 10. Инактивация инсектицидной активности при нагревании Определяют стабильность токсина при нагревании. Культуры штамма Е. coli рСIВ9369 (штамм-хозяин Е.coli DH5α, несущий фрагмент ДНК Xenorhabdus nematophilus длиной 3,0 т.п.н.) выращивают в смеси (50:50) бульона Луриа и Terrific-бульона. Культуры выращивают при 37°С в пробирках на роторном шейкере. Образцы каждой культуры объемом по 1 мл помещают в пробирку Эппендорфа объемом 1,5 мл и выдерживают при 60°С и 80°С. Через 5 мин образцы удаляют из термостата и дают охладиться до комнатной температуры. Образец наряду с необработанной порцией культуры анализируют в отношении активности к Р. xylostella. 50 мкл образца наносят опрыскиванием на корм, дают высохнуть и на поверхность помещают свежевылупившиеся гусеницы Р. xylostella. Образцы инкубируют в течение 5 дней при комнатной температуре.
Необработанный образец и образец, обработанный нагреванием до 60°С, вызывали 100%-ную гибель. Образец, обработанный нагреванием до 80°С и контрольный образец, представляющий собой только корм, не вызывали заметной гибели.
Пример 11. Влияние протеазной обработки на инсектицидную активность
Космидный клон Xenorhabdus nematophilus pCIB9369 и вектор BlueScript фирмы Stratagene в штамме-хозяине E.coli DH5α выращивают в среде, состоящей из 50% бульона Terrific и 50% бульона Луриа, дополненной 50 мкг/мл ампициллина. Культуры выращивают во встряхиваемых колбах (300 мл в колбах с перегородками объемом 1000 мл) при 250 об/мин в течение ночи при 37°С. Культуры каждого штамма центрифугируют при 7000 об/мин в центрифуге типа Sorvall GS при 4°С. Пеллетированные клетки ресуспендируют в 30 мл 50 мМ NaCl, 25 мМ Трис-буфера, рН 7,0. Концентрированные клетки разрушают путем облучения ультразвуком с помощью устройства типа Branson Model 450 Sonicator в течение приблизительно восьми 10-секундных циклов с использованием охлаждения на льду в промежутке между циклами. Полученный в результате ультразвукового облучения продукт центрифугируют в центрифуге типа Sorvall SS34 при 6000 об/мин в течение 10 мин при 4°С. Образовавшиеся супернатанты фильтруют через фильтр с размерами пор 0,2 мкм. Концентрацию Са++ в образцах супернатанта объемом 1 мл доводят до 5 мМ путем добавления СаСl2. Добавляют протеазу К (фирма Gibco BRL; Гейтерсбург, MD) до концентрации 500 мкг/мл. Образцы инкубируют при 37°С в течение 2 и 24 ч. Приготавливают и инкубируют контрольные образцы, в которые добавляют Са++, но не добавляют протеазу.
Фильтрат, облученный ультразвуком, полученный из образцов, содержащих pCIB9369, и образцы, содержащие pCIB9369, инкубированные в присутствии 5 мМ Ca++, вызывали 100%-ную гибель свежевылупившихся гусениц Plutella xylostella. Образцы, содержащие pCIB9369, инкубированные в присутствии протеазы К (с добавлением Са++) вызывали несколько меньшую гибель гусениц Plutella, составляющую приблизительно 90%).
Пример 12. Сравнительный анализ последовательности и последовательности протеина сry3А и последовательности протеина ювенильного гормона эстеразы
Нуклеотидная последовательность pCIB9369 (SEQ ID NO:1) имеет две открытые рамки считывания (ORF) в положениях нуклеотидов 569-976 и 1045-2334. По результатам поиска с использованием программ UWGCG Blast и Gap ORF №1 не имеет гомологии ни с одной из последовательностей из GenBank. Gap-анализ протеина, кодируемого ORF №2 рСIВ9369, проведенный с помощью программы Blast, выявил незначительную гомологию (21%-ная идентичность) с протеином Bacillus thuringensis сry3А. При этом Gap-анализ протеина, кодируемого ORF №2 рСIВ9369, проведенный с помощью программы Blast, выявил определенную степень гомологии (30,6%-ная идентичность аминокислотных последовательностей и 44,1%-ное сходство аминокислотных последовательностей) с протеином, сходным с эстеразой ювенильного гормона (регистрационный номер GenBank 2921553; Henikoff и др., PNAS USA 89: 10915-10919 (1992).
Нуклеотидные последовательности pCIB9381, pCIB9354 и рСIВ9383-21 также имеют по две открытые рамки считывания каждая. Нуклеотидные последовательности двух ОRF в каждом из pCIB9381 и рСIВ9383-21 более чем на 90% идентичны ORF pCIB9369) Следовательно, ORF №2 протеинов pCIB9381 и рСIВ9383-21 обладает практически такой же гомологией со связанным с эстеразой ювенильного гормона протеином, что и ORF №2 протеина рСIВ9369. Нуклеотидная последовательность ORF №1 протеина pCIB9354 идентична на 77% нуклеотидной последовательности ORF №1 протеина pCIB9369, a нуклеотидная последовательность ORF №2 протеина pCIB9354 идентична на 79% нуклеотидной последовательности ORF №2 протеина pCIB9369. ORF №2 протеина pCIB9354 также обладает гомологией со связанным с эстеразой ювенильного гормона протеином (идентичность аминокислотных последовательностей 29,2%, сходство аминокислотных последовательностей 42,2%).
Пример 13. Сравнение последовательности pCIB9369 с последовательностями, описанными в WO 98/08388
Из фрагмента ДНК длиной 38,2 т.п.н., нуклеотидная последовательность которого описана в WO 98/08388, выделяют двадцать две последовательности по 60 нуклеотидов каждая (60-меры) и их сравнивают с нуклеотидной последовательностью рСIВ9362-3, включающей pCIB9369. Первый 60-мер начинается с основания 1 фрагмента ДНК длиной 38,2 т.п.н., а остальные расположены на фрагменте ДНК с интервалами приблизительно 2 т.п.н. Их положения на фрагменте ДНК длиной 38,2 т.п.н. перечислены ниже:
1-60; 2041-2100; 4021-4080; 6001-6060; 8041-8100; 10021-10080; 12001-12060; 14041-14100; 16021-16080; 18001-18060; 20041-20100; 22021-22080; 24001-24060; 26041-26100; 28021-28080; 30001-30060; 32041-32100; 34021-34080; 36001-36060; 38041-38100; 38161-38220.
Последовательности сравнивали с использованием программы UWGCG Gap и при этом анализировали как каждую из 22 60-мерных последовательностей, так и комплементарные им последовательности. Результаты этого сравнительного анализа свидетельствуют о том, что наибольший процент идентичности составляет 53%, что в данной области не рассматривается как значительная степень гомологии.
Пример 14. Анализ методом Саузерн-блоттинга с использованием зондов, полученных на основе последовательностей из WO 98/08388
Для амплификации фрагментов ДНК из фрагмента ДНК длиной 38,2 т.п.н., описанного в WO 98/08388, конструируют пары олигонуклеотидов. Олигонуклеотиды получают от фирмы Genosys Biotechnologies (The Woodlands, штат Техас) и их положения на фрагменте ДНК длиной 38,2 т.п.н. указаны ниже. Также указаны их размеры и размеры амплифицированных с помощью ПЦР фрагментов:
VK1046: положения 20-40,
VK1047: положения 2078-2100.
Размер фрагмента, амплифицированного с помощью ПЦР с использованием праймеров VK1046 и VK1047: 2080 пар оснований,
VK1048: положения 11221-11241,
VK1049: положения 13360-13380.
Размер фрагмента, амплифицированного с помощью ПЦР с использованием праймеров VK1048 и VK1049: 2120 пар оснований,
VK1050: положения 26581-26601,
VK1051: положения 28537-28560.
Размер фрагмента, амплифицированного с помощью ПЦР с использованием праймеров VK1050 и VK1051: 1979 пар оснований,
VK1052: положения 18901-18921,
VK1053: положения 20321-20340.
Размер фрагмента, амплифицированного с помощью ПЦР с использованием праймеров VK1052 и VK1053: 1439 пар оснований.
VK1054: положения 34261-34281,
VK1055: положения 35320-35340 пар оснований,
Размер фрагмента, амплифицированного с помощью ПЦР с использованием праймеров VK1054 и VK1055: 1079 пар оснований.
ПЦР проводят в термоячейке типа Perkin-Elmer 9600, используя следующие условия: 94°С, 2 мин; затем 30 циклов при 94°С, 30 с; 54°С, 30 с; 72°С, 4 мин. Образцы содержат 800 нг ДНК Xenorhabdus nematophilus, 0,1-0,5 мкМ каждой пары олигонуклеотидов, 250 мкМ дНТФ, 5 ед. полимеразы Taq и однократный (1х) буфер (фирма Perkin-Elmer) в конечном объеме 100 мкл. Полученные реакционные смеси осаждают этанолом, ресуспендируют в ТЕ и вносят в 1%-ный ТВЕ-гель SeaPlaque (фирма FMC, Rocklend, Maine). После электрофореза и окрашивания бромидом этидия фрагменты вырезают из геля и визуализируют в УФ-лучах. Срезы геля расплавляют при 65°С и аликвоты по 10 мкл смешивают с 10 мкл дистиллированной воды, кипятят в течение 5 мин и помещают на лед. Затем смешивают с 15 мкл буфера для мечения методом случайного примирования (фирма GIBCO-BRL, Gaitersburg, MD), 6 мкл смеси дНТФ (не содержащей дЦТФ), 80 мкКи α-дЦТФ32P и 1 мкл полимеразы Кленова. Реакцию введения метки проводят в течение 60 мин при комнатной температуре. Образцы очищают на колонках типа Nick (фирма Pharmacia Biotech) согласно рекомендациям поставщика. Зонды кипятят в течение 5 мин и помещают на лед.
Анализ методом Саузерн-блоттинга проводят путем расщепления общей ДНК Xenorhabdus nematophilus, ДНК, выделенной из космид рСIВ9362 и рСIВ9363 (эти космиды имеют перекрывающий участок длиной 25 т.п.н. и они обе содержат фрагмент ДНК рСIВ9369; рСIВ9362 используют для субклонирования), ДНК, выделенной из субклонов рСIВ9362-3 (SacII-фрагмент длиной 9 т.п.н.) и pCIB9369 (ClaI-фрагмент длиной 2,96 т.п.н.), расщепленных с помощью ClaI, SacII или HindIII. Продукты, полученные в результате расщепления, помещают на 0,75%-ный агарозный ТВЕ-гель и разгоняют в течение ночи. Делают снимки и гель обрабатывают согласно инструкциям фирмы Bio-Rad, касающихся блоттинга с использованием мембраны для гибридизации с Zeta-зондом. После блоттинга мембрану выдерживают при 80°С в течение 30 мин. Затем мембрану помещают в 7%-ный ДСН, содержащий 250 мМ фосфат натрия, рН 7,2, и инкубируют при 67°С в течение 30 мин. Добавляют свежий раствор и после уравновешивания при 67°С добавляют указанные выше радиоактивные зонды, и проводят гибридизацию в течение ночи. Мембрану отмывают 2xSSC, 0,5%-ным ДСН в течение 30 мин при 67°С, а затем 0,5xSSC, 0,5%-ным ДСН в течение 30 мин при 67°С. Мембрану экспонируют на пленку в течение 1 ч и 3 ч. Пленку проявляют, и результаты свидетельствуют о том, что зонды для ПЦР, созданные на основе последовательности, описанной в WO 98/08388, не гибридизуются с ДНК космид или с ДНК субклонов, описанных в настоящей заявке. Однако для ДНК X. nematophilus наблюдается сильный сигнал гибридизации.
Эти результаты подкрепляют результаты сравнительного анализа последовательностей и свидетельствуют о том, что нуклеотидная последовательность клона рСIВ9369 отлична от нуклеотидной последовательности, описанной в WO 98/08388.
Б. Экспрессия нуклеотидных последовательностей по изобретению в гетерологичных микроорганизмах-хозяевах
Микроорганизмами, пригодными для гетерологичной экспрессии нуклеотидных последовательностей по изобретению, могут служить любые микроорганизмы, которые способны колонизировать растения или ризосферу. Для этого они должны быть приведены в контакт с насекомыми-вредителями. Они включают грамотрицательные микроорганизмы, такие как Pseudomonas, Enterobacter и Serratia, грамположительный микроорганизм Bacillus и грибы Trichoderma и Gliocladium, и дрожжи Saccharomyces cerevisiae. Наиболее предпочтительными гетерологичными хозяевами являются Pseudomonas fluorescens, Pseudomonas putida, Pseudomonas cepacia, Pseudomonas aureofaciens, Pseudomonas aurantiaca, Enterobacter cloacae, Serratia marscesens, Bacillus subtilis, Bacillus cereus, Trichoderma viride, Trichoderma harzianum, Gliocladium virens и Saccharomyces cerevisiae.
Пример 15. Экспрессия нуклеотидных последовательностей в Е.coil и других грамотрицательных бактериях
Многие гены экспрессировали в грамотрицательных бактериях гетерологичным образом. Экспрессионный вектор рКК223-3 (каталожный номер фирмы Pharmacia №27-4935-01) позволяет осуществлять экспрессию в Е. coli. Этот вектор имеет сильный промотор tac (Brosius J. и др., Proc. Natl. Acad. Sci. USA 81), регулируемый репрессором lac и индуцируемый IPTG (изопропил-β-D-тиогалактозид). Для применения в Е. coli разработано большое количество других экспрессионных систем. Индуцируемый нагреванием экспрессионный вектор рРL (каталожный номер фирмы Pharmacia №27-4946-01) содержит строго регулируемый промотор бактериофага λ, позволяющий осуществлять экспрессию протеинов с высоким уровнем. Промотор lac представляет собой другой обеспечивающий экспрессию промотор, однако он не позволяет достичь таких высоких уровней экспрессии, как промотор tac. При добавлении в эти экспрессионные векторные системы репликонов с широким спектром хозяев становится возможной экспрессия нуклеотидных последовательностей в близкородственных грамотрицательных бактериях, таких как Pseudomonas, Enterobacter, Serratia и Erwinia. Например, плазмида pLRKD211 (Kaiser и Kroos, Proc. Natl. Acad. Sci. USA 81: 5816-5820 (1984)) содержит репликон ori Т с широким спектром хозяев, позволяющий осуществлять репликацию во многих видах грамотрицательных бактерий.
Для экспрессии в Е.coli под контролем промотора tac (т.е. trp-lac) требуется индукция с помощью IPTG. Если же этот промотор (например, в составе плазмиды с широким спектром хозяев pLRKD211) встраивают в Pseudomonas, то он будет обладать конститутивной активностью, не требующей индукции с помощью IPTG. Этот промотор trp-lac может быть помещен перед любым геном или опероном, представляющим интерес, для экспрессии в Pseudomonas или любой другой близкородственной бактерии с целью осуществления конститутивной экспрессии такого гена. Таким образом, нуклеотидная последовательность, экспрессия которой приводит к образованию инсектицидного токсина, может находиться под контролем сильного конститутивного промотора, и перенесена в бактерию, обладающую способностью колонизировать растение или ризосферу, что превращает этот организм в инсектицидный агент. Другие пригодные промоторы могут быть использованы для осуществления конститутивной экспрессии нуклеотидной последовательности в грамотрицательных бактериях. Они включают, например, промотор регуляторных генов gafA и lemA (WO 94/01561) из Pseudomonas и промотор оперона IAA Pseudomonas savastanoi (Gaffney и др., J. Bacteriol. 172: 5593-5601 (1990)).
Пример 16. Экспрессия нуклеотидных последовательностей в грамположительных бактериях
Гетерологичная экспрессия нуклеотидной последовательности в грамположительных бактериях представляет собой другое средство продуцирования инсектицидных токсинов. Наиболее полно охарактеризованы экспрессионные системы для Bacillus и Streptomyces. Установлено, что промотор гена, обусловливающего устойчивость к эритромицину (ermR) из Streptococcus pneumoniae обладает активностью в грамположительных аэробных и анаэробных микроорганизмах, а также в Е.coli (Trieu-Cuot и др., Nucl. Acids Res. 18: 3660 (1990)). Другой промотор гена, придающего устойчивость к антибиотику тиострептону, использовали в клонирующих векторах Streptomyces (Bibb, Mol. Gen. Genet. 199: 26-36 (1985)). Для экспрессии в Bacillus также пригоден челночный вектор рНТ3101 (Lereclus, FEMS Microbiol. Lett. 60: 211-218 (1989)). Большим преимуществом этого подхода является то, что многие грамположительные бактерии образуют споры, которые могут использоваться в композициях, что позволяет создать инсектицидные агенты, обладающие большим сроком хранения. Виды Bacillus и Streptomyces являются активными колонизаторами почв.
Пример 17. Экспрессия нуклеотидных последовательностей в грибах
Установлено, что Trichoderma harzianum и Gliocladium virens позволяют достичь различных уровней биологического контроля в полевых условиях (US 5165928 и US 4996157, оба патента на имя Корнелльского исследовательского фонда (Cornell Research Foundation)). Нуклеотидная последовательность, экспрессия которой приводит к образованию инсектицидного токсина, также может экспрессироваться в грибах. Это может быть осуществлено различными методами, хорошо известными в данной области. Одним из них является трансформация протопластов гриба, опосредуемая ПЭГ или осуществляемая методом электропорации. Альтернативно этому для трансформации протопластов или других клеток гриба, обладающих способностью развиваться в регенерированные зрелые структуры, может применяться бомбардировка частицами. Вектор pAN7-1, первоначально созданный для трансформации Aspergillus и в настоящее время широко применяемый для трансформации грибов (Curragh и др., Mycol. Res. 97(3): 313-317 (1992); Tooley и др., Curr. Genet. 21: 55-60 (1992); Punt и др., Gene 56: 117-124 (1987)), конструируют так, чтобы он содержал нуклеотидную последовательность. Эта плазмида содержит ген, обусловливающий устойчивость к гигромицину В, из Е.coli, фланкированный промотором gpd и терминатором trpC Aspergillus nidulans (Punt и др., Gene 56: 117-124 (1987)).
В предпочтительном варианте осуществления нуклеотидные последовательности по изобретению экспрессируют в дрожжах Saccharomyces cerevisiae. Например, каждую из двух ORF рСIВ9369, рСIВ9381, рСIВ9354 или рСIВ9383 клонируют в отдельных векторах вместе с индуцибельным промотором GAL1 и терминатором CYC1. Каждый вектор имеет ген, обусловливающий устойчивость к ампициллину и репликон размером 2 мкм. Векторы предпочтительно различаются своими маркерами роста в дрожжах. S. cerevisiae трансформируют конструкциями по отдельности и в сочетании друг с другом. ORF экспрессируются вместе и их тестируют в отношении экспрессии протеина и наличия инсектицидной активности.
В. Препаративные формы, содержащие инсектицидный токсин
Инсектицидные препаративные формы приготавливают с использованием действующих веществ, которые включают либо выделенный токсин, либо в альтернативном варианте суспензии или концентраты клеток, продуцирующих его, и которые описаны выше в примерах. Например, для борьбы с насекомыми-вредителями могут быть использованы клетки Е.coli, экспрессирующие инсектицидный токсин. Ниже описаны Препаративные формы, которые могут быть приготовлены в жидкой или твердой форме.
Пример 18. Жидкие препаративные формы инсектицидных композиций
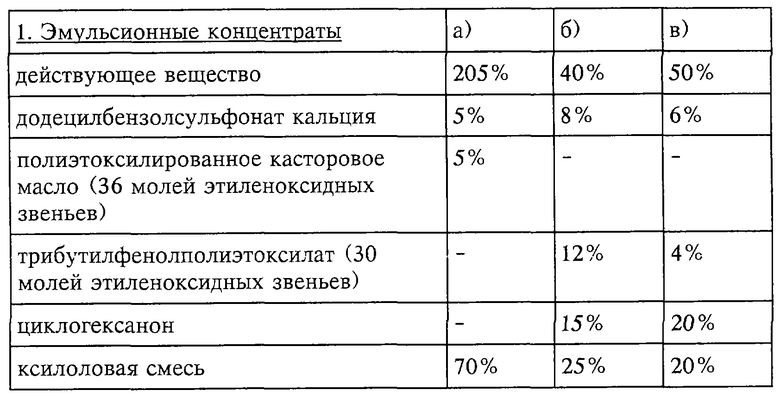


Действующее вещество растворяют в метиленхлориде, раствор распыляют на носитель и затем растворитель выпаривают под вакуумом.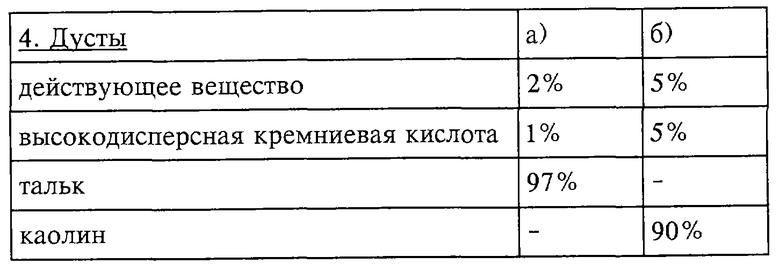
Путем тщательного смешения носителей с действующим веществом получают готовые к применению дусты.
Пример 19. Твердые препаративные формы инсектицидных композиций
В приведенных ниже примерах процентное содержание ингредиентов в композиции дано в мас.%.

Действующее вещество тщательно смешивают с адъювантами и смесь тщательно измельчают в пригодной мельнице, получая смачивающиеся порошки, которые могут быть разбавлены водой до получения суспензий требуемой концентрации.


Эмульсии требуемой концентрации получают из этого концентрата разбавлением водой.
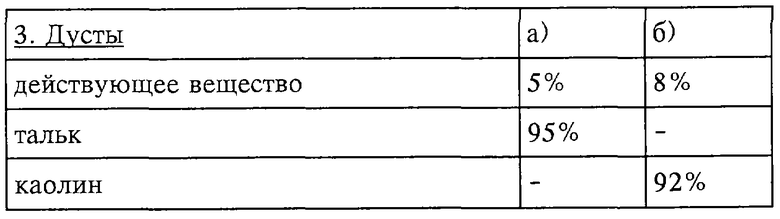
Готовые к применению дусты получают путем смешения действующего вещества с носителями и измельчения смеси в пригодной мельнице.

Действующее вещество смешивают и измельчают с адъювантами и затем смесь увлажняют водой. Смесь экструдируют и затем сушат в потоке воздуха.
Тонкоизмельченное действующее вещество равномерно подают в смеситель к каолину, увлажненному полиэтиленгликолем. Таким способом получают беспылевые гранулы с покрытием.
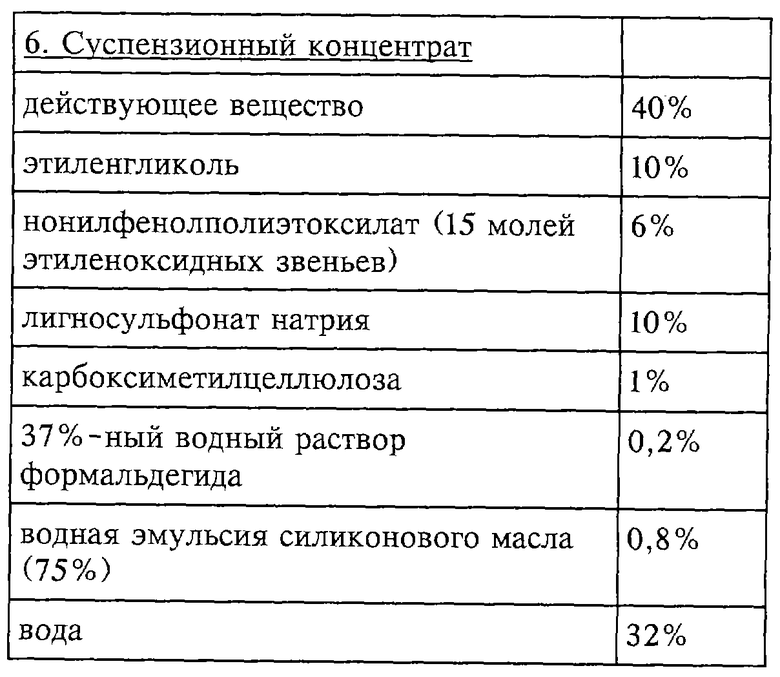
Тонкоизмельченное действующее вещество тщательно смешивают с адъювантами, получая суспензионный концентрат, из которого суспензии требуемой концентрации могут быть получены разбавлением водой.
Описанными выше инсектицидными препаративными формами обрабатывают растения согласно методам, хорошо известным в данной области, в таких количествах, которые достаточны для борьбы с насекомыми-вредителями с помощью инсектицидного токсина.
Г. Экспрессия нуклеотидных последовательностей в трансгенных растениях
Нуклеотидные последовательности, представленные в настоящем описании, могут быть введены в клетки растения с помощью обычных методов рекомбинантной ДНК. Как правило, в них используется встраивание кодирующей последовательности по изобретению в экспрессионную систему, по отношению к которой кодирующая последовательность является гетерологичной (т.е., не присутствует в ней в нормальном состоянии), с помощью стандартных методов клонирования, известных в данной области. Вектор содержит элементы, необходимые для транскрипции и трансляции встроенных кодирующих протеин последовательностей. Могут применяться многочисленные известные в данной области векторные системы, такие как плазмиды, бактериофаги и другие модифицированные вирусы. Пригодные векторы включают вирусные векторы, такие, как системы на основе лямбда-векторов λgtl1, λgt10 и Charon 4; плазмидные векторы, такие как рВl121, pBR322, pACYC177, pACYC184, серии pAR, pKK223-3, pUC8, pUC9, pUC18, pUC19, pLG339, pRK290, pKC37, pKC101, pCDNAII; и другие аналогичные системы, но не ограничены ими. Компоненты экспрессионной системы также могут быть модифицированы для увеличения уровня экспрессии. Например, могут применяться укороченные последовательности, замены нуклеотидов или другие модификации. Приведенные в настоящем описании экспрессионные системы могут использоваться для трансформации практически любой клетки культурного растения в соответствующих условиях. Трансформированные клетки могут быть регенерированы с получением целых растений, при этом нуклеотидная последовательность по изобретению придает трансгенным растениям устойчивость к насекомым.
Пример 22. Модификация кодирующих последовательностей и смежных последовательностей
Молекулы ДНК, представленные в данном описании, могут быть модифицированы для экспрессии в трансгенных растениях-хозяевах. Растение-хозяин, которое экспрессирует нуклеотидные последовательности и которое продуцирует в своих клетках инсектицидные токсины, обладает повышенной устойчивостью к нападению насекомых и, таким образом, лучше способно противостоять потерям урожая, связанным с таким нападением.
Трансгенная экспрессия в растениях генов, происходящих из микроорганизмов, может потребовать модификации этих генов с целью достижения и оптимизации их экспрессии в растениях. В частности, бактериальные ORF, кодирующие различные ферменты, но которые в нативном микроорганизме кодируются одним и тем же транскриптом, экспрессируются в растении лучше в том случае, если они кодируются различными транскриптами. Для достижения этого каждую ORF, происходящую из микроорганизма, выделяют по отдельности и клонируют в кассете, которая имеет промоторную последовательность растения на 5’-конце ORF и терминатор транскрипции растения на 3’-конце ORF. Выделенная последовательность ORF предпочтительно включает инициирующий кодон ATG и терминирующий стоп-кодон, но она может содержать дополнительную последовательность кроме инициирующего кодона ATG и стоп-кодона. Кроме того, ORF может быть укороченной, но еще сохранять требуемую активность; в случае особенно длинных ORF укороченные версии, сохраняющие активность, могут оказаться предпочтительными для экспрессии в трансгенных организмах. Подразумевается, что понятия "промотор растения" и "терминатор транскрипции растения" обозначают промоторы и терминаторы транскрипции, функционирующие в растении. Они также включают промоторы и терминаторы транскрипции, которые могут быть выделены из источников, не представляющих собой растения, таких как вирусы (например, вирус мозаики цветной капусты (CaMV)).
В некоторых случаях модификация кодирующих последовательностей ORF и смежных последовательностей может не требоваться. Достаточно выделить фрагмент, содержащий представляющую интерес ORF, и встроить ее по ходу транскрипции относительно промотора растения. Например, Gaffney и др., (Science 261: 754-756 (1993)) успешно осуществили экспрессию гена nahG Pseudomonas в трансгенных растениях под контролем промотора 35S CaMV и терминатора tml CaMV без модификации кодирующей последовательности, при этом x пар оснований гена Pseudomonas еще оставались присоединенными к ORF nahG против хода транскрипции относительно кодона ATG и у пар оснований еще оставались присоединенными к ней по ходу транскрипции относительно стоп-кодона. Предпочтительно, чтобы небольшие смежные участки последовательности из микроорганизма оставались присоединенными против хода транскрипции относительно кодона ATG и по ходу транскрипции относительно стоп-кодона. На практике возможность создания такой конструкции может зависеть от доступности сайтов рестрикции.
В других случаях при экспрессии генов, выделенных из источников, представляющих собой микроорганизмы, могут возникнуть проблемы. Эти проблемы хорошо известны в данной области и они являются общими для генов, выделенных из определенных источников, таких как Bacillus. Эти проблемы могут возникнуть и для нуклеотидных последовательностей по настоящему изобретению, и для их преодоления могут быть осуществлены модификации этих генов с использованием хорошо известных в данной области методов. Могут встретиться следующие проблемы:
1. Наиболее часто встречающиеся кодоны
В растениях наиболее часто встречающиеся кодоны отличаются от наиболее часто встречающихся кодонов в некоторых видах микроорганизмов. Сравнение наиболее часто встречающихся кодонов в клонированной ORF микроорганизма с наиболее часто встречающимися кодонами генов растений (и прежде всего генов растения-мишени) дает возможность выявить в ORF кодоны, которые предпочтительно следует модифицировать. Как правило, в результате эволюции растений однодольные растения обладают выраженной предпочтительностью в отношении нуклеотидов С и G в третьем положении нуклеотидной последовательности, в то время как у двудольных растений в этом положении наиболее часто встречаются нуклеотиды А или Т. С помощью модификации гена путем включения наиболее часто встречающегося кодона для конкретного трансгенного вида-мишени многие из описанных ниже проблем, касающихся содержания GC/AT и незаконных сайтов сплайсинга могут быть преодолены.
2. Содержание GC/AT
Как правило, растения имеют содержание GC более 35%. Использование последовательностей ORF, имеющих высокое содержание нуклеотидов А и Т, может представлять серьезные проблемы для растений. Во-первых, по-видимому, мотивы АТТТА вызывают дестабилизацию транскриптов, и их обнаруживают на 3’-конце многих короткоживущих мРНК. Во-вторых, наличие сигналов полиаденилирования, таких как ААТААА, в несоответствующих положениях в транскрипте, по-видимому, вызывает преждевременное окончание транскрипции. Кроме того, в однодольных растениях последовательности с высоким содержанием AT могут распознаваться как сайты сплайсинга (см. ниже).
3. Последовательности, смежные с инициирующим метионином
Растения отличаются от микроорганизмов тем, что их транскрипты не имеют определенного сайта связывания рибосомы. По-видимому, рибосомы присоединяются к 5’-концу транскрипта и отыскивают первый доступный кодон ATG, в котором может быть начата трансляция. Тем не менее, имеется предположение о том, что существует предпочтение в отношении определенных нуклеотидов, смежных с кодоном ATG, и что экспрессия молекул ДНК по настоящему изобретению может быть усилена путем включения эукариотического консенсусного инициатора трансляции рядом с ATG. Фирмой Clontech (каталог 1993/1994 г., стр. 210) предложена последовательность в качестве консенсусного инициатора трансляции для экспрессии гена uidA E.coli в растениях. Кроме того, Joshi (NAR 15: 6643-6653 (1987)) провел сравнительный анализ большого количества последовательностей из растений, смежных с кодоном ATG, и предложил другую консенсусную последовательность. В тех ситуациях, когда имеются трудности, связанные с экспрессией молекул ДНК в растениях, включение одной из таких последовательностей рядом с инициирующим кодоном ATG может улучшить трансляцию. В таких случаях последние три нуклеотида консенсусной последовательности могут не подходить для включения в модифицированную последовательность вследствие их модификации второго остатка АА. Предпочтительные последовательности, смежные с инициирующим метионином, могут быть различными у различных видов растений. Анализ последовательностей 14 генов кукурузы, депонированных в базе данных GenBank, дал следующие результаты.
Положение перед инициирующим кодоном ATG в последовательностях 14 генов кукурузы:
Такой анализ может быть проведен для целевых видов растения, в которое встраивают нуклеотидную последовательность, и последовательность, смежная с ATG, может быть модифицирована с целью включения предпочтительных нуклеотидов.
4. Удаление незаконных сайтов сплайсинга
Гены, клонированные из источников, не относящихся к растениям, и не оптимизированные для экспрессии в растениях, также могут содержать мотивы, которые могут распознаваться в растениях как 5’- или 3’-сайты сплайсинга и в них может происходить расщепление, в результате которого образуются укороченные или имеющие делеции транскрипты. Такие сайты могут быть удалены с помощью известных в данной области методов.
Методы модификации кодирующих последовательностей и смежных последовательностей хорошо известны в данной области. В тех случаях, когда исходный уровень экспрессии молекулы ДНК по настоящему изобретению является низким и представляется желательным осуществить описанные выше модификации последовательности, конструирование синтетических генов может быть осуществлено согласно методам, хорошо известным в данной области. Эти методы описаны, например, в опубликованных заявках на патент ЕР 0385962 (на имя фирмы Monsanto), ЕР 0359472 (на имя фирмы Lubrizol) и WO 93/07278 (на имя фирмы Ciba-Geygi), все они включены в настоящее описание в виде ссылки. Во многих случаях предпочтительно анализировать уровень экспрессии генных конструкций с использованием протоколов кратковременных анализов (которые являются хорошо известными в данной области) перед их переносом в трансгенные растения.
Пример 23. Конструирование растительных кассет экспрессии
Кодирующие последовательности, предназначенные для экспрессии в трансгенных растениях, сначала объединяют в кассеты экспрессии за пригодным промотором, обладающим способностью экспрессироваться в растении. Кассеты экспрессии также могут включать любые другие последовательности, необходимые или выбранные для экспрессии трансгена. Такие последовательности включают терминаторы транскрипции, чужеродные последовательности, предназначенные для усиления экспрессии, такие как интроны, витальные последовательности и последовательности, предназначенные для направленного переноса генного продукта в конкретные органеллы и клеточные компартменты, но не ограничены ими. После этого такие кассеты экспрессии легко могут быть перенесены в растительные трансформирующие векторы согласно описанному ниже методу. Ниже приведено описание различных компонентов типичных кассет экспрессии.
1. Промоторы
Выбор промотора, применяемого в кассетах экспрессии, определяет пространственную и временную схему экспрессии трансгена в трансгенном растении. Выбранные промоторы позволяют осуществлять экспрессию трансгенов в определенных типах клеток (таких, как эпидермальные клетки листьев, мезофильные клетки, клетки коры корня) или в определенных тканях или органах (например, в корнях, листьях или цветках), и этот выбор зависит от желаемого места накопления генного продукта. В альтернативном варианте выбранный промотор может управлять экспрессией гена при различных условиях индуцирования. Промоторы могут различаться по своей силе, т.е. способности стимулировать транскрипцию. В зависимости от используемой системы клетки-хозяина может применяться любой из многочисленных пригодных промоторов, включая нативный промотор гена. Ниже приведены примеры промоторов, которые могут использоваться в кассетах экспрессии, не ограничивающие объема изобретения.
а. Конститутивная экспрессия: промотор убикитина
Убикитин представляет собой другой генный продукт, известный способностью накапливаться во многих типах клеток, и его промотор клонировали из нескольких видов для применения в трансгенных растениях (например, в подсолнечнике - Binet и др., Plant Science 79: 87-94 (1991), в кукурузе - Christensen и др., Plant Molec. Biol. 12: 619-632 (1989); и в Arabidopsis - Norris и др., Plant Mol. Biol. 21: 895-906 (1993)). Промотор гена убикитина кукурузы исследовали в трансгенных системах однодольных растений и его последовательность и векторы, сконструированные для трансформации однодольных, описаны в опубликованном патенте ЕР 0342926 (на имя фирмы Lubrizol), включенном в настоящее описание в виде ссылки. Кроме того, у Taylor и др. (Plant Cell Rep. 12: 491-495 (1993) описан вектор (рАНС25), который содержит промотор убикитина кукурузы и первый интрон, и отмечена его высокая активность в клеточных суспензиях многочисленных однодольных растений при введении с помощью бомбардировки микроснарядами. Промотор убикитина Arabidopsis идеален для применения с нуклеотидными последовательностями по настоящему изобретению. Промотор убикитина пригоден для экспрессии гена в трансгенных растениях, как в однодольных, так и в двудольных. Пригодные векторы являются производными вектора рАНС25 или любых трансформирующих векторов, представленных в настоящем описании, модифицированных путем встраивания соответствующего промотора убикитина и/или интронных последовательностей.
б. Конститутивная экспрессия, промотор 35S СаМV
Конструкция плазмиды pCGN1761 описана в опубликованной заявке на патент ЕР 0392225 (пример 23), которая включена в настоящее описание в виде ссылки. Плазмида pCGN1761 содержит "двойной" промотор 35S и терминатор транскрипции tml с уникальным сайтом EcoRI между промотором и терминатором и имеет каркас pUC-типа. Конструируют плазмиду, являющуюся производной pCGN1761, которая несет модифицированный полилинкер, включающий сайты NotI и XhoI в дополнение к существующему сайту EcoRI. Эту производную плазмиду обозначают как pCGN1761ENX. pCGN1761ENX может применяться для клонирования последовательностей кДНК или последовательностей гена (включая последовательности микробных ORF) внутри ее полилинкера с целью их экспрессии в трангенных растениях под контролем промотора 35S. Полная кассета такой конструкции, включающая промотор 35S-кодирующую последовательность-терминатор tml, может быть отщеплена в сайтах HindIII, SphI, SalI и XbaI на 5’-конце промотора и сайтов XbaI, BamHI и BglI на 3’-конце терминатора для переноса в трансформирующие векторы, такие, как описаны выше. Кроме того, фрагмент двойного промотора 35S может быть удален путем 5’-отщепления с помощью HindIII, SphI, SalI, XbaI или PstI, на 3’-конце в любых сайтах рестрикции полилинкера (EcoRI, NotI или XhoI) для замены на другой промотор. При необходимости вокруг клонирующих сайтов могут быть сделаны модификации путем встраивания последовательностей, которые могут усиливать трансляцию. Это особенно предпочтительно в тех случаях, когда требуется сверхэкспрессия. Например, pCGN1761ENX может быть модифицирована путем оптимизации сайта иницииации трансляции согласно методу, описанному в примере 37 патента US 5639949, который включен в настоящее описание в виде ссылки.
в. Конститутивная экспрессия: промотор актина
Известно несколько изоформ актина, экспрессируемых в большинстве типов клеток, и следовательно, промотор актина представляет собой хороший выбор в качестве конститутивного промотора. В частности, был клонирован и охарактеризован промотор гена риса Act1 (McElroy и др., Plant Cell 2: 163-171 (1990)). Установлено, что фрагмент промотора длиной 1,3 т.п.н. содержит все регуляторные элементы, необходимые для экспрессии в протопластах риса. Кроме того, были сконструированы многочисленные векторы экспрессии, включающие промотор Act1, специально для применения в однодольных растениях (McElroy и др., Mol.Gen. Genet. 231: 150-160 (1991)). Они включают интрон 1 Act1, 5’-фланкирующую последовательность Adh1 и интрон 1 Adh1 (из гена алкогольдегидрогеназы кукурузы) и последовательность из промотора 35S CaMV. Проявившие наибольшую экспрессию векторы представляли собой слияния 35S и интрона Act1 или 5’-фланкирующей последовательности Adh1 и интрона Act1. Оптимизация последовательностей, смежных с инициирующим кодоном ATG (репортерный ген GUS) также усиливает экспрессию. Промотор кассет экспрессии, описанный у (McElroy и др., Mol.Gen. Genet. 231: 150-160 (1991)), может быть легко модифицирован для экспрессии гена по настоящему изобретению и он особенно пригоден для использования в однодольных растениях-хозяевах. Например, фрагменты, содержащие промотор, могут быть удалены из конструкций McElroy и применены для замены двойного промотора 35S в pCGN1761ENX, которая после этого становится пригодной для встраивания специфичных последовательностей гена. Слитые гены, сконструированные таким образом, затем могут быть перенесены в соответствующие трансформирующие векторы. В другом научном отчете сообщается, что промотор риса Act1 со своим первым интроном также обусловливает высокий уровень экспрессии в культивируемых клетках ячменя (Chibbar и др., Plant Cell Rep. 12: 506-509 (1993)).
г. Индуцибельная экспрессия, промотор PR-1a
Двойной промотор 35S в pCGN1761ENX может быть заменен любым другим выбранным промотором, который обеспечивает высокий уровень экспрессии. Например, двойной промотор 35S может быть заменен одним из химически регулируемых промоторов, которые описаны в патенте США 5614395. Выбранный промотор предпочтительно отщепляют из его источника с помощью рестриктаз, но в альтернативном варианте он может быть амплифицирован с помощью ПЦР с использованием праймеров, несущих соответствующие терминирующие сайты рестрикции. После ПЦР-амплификации промотор должен быть ресеквенирован с целью проверки ошибок амплификации после клонирования амплифицированного промотора в векторе-мишени. Химически/патогеном регулируемый промотор PR-1a табака, выделяют из плазмиды рСIВ1004 (касательно конструирования см. пример 21 описания патента ЕР 0332104, включенного в настоящее описание в виде ссылки) и переносят в плазмиду pCGN1761ENX (Ukness и др., 1992). Плазмиду рС1В1004 расщепляют с помощью NcoI и полученный в результате 3’-выступающий конец линеаризованного фрагмента "затупляют" путем обработки ДНК-полимеразой фага Т4. Затем фрагмент расщепляют с помощью HindIII и полученный в результате фрагмент, содержащий промотор PR-la, подвергают очистке с помощью геля и клонируют в pCGN1761ENX, из которой удален двойной промотор 35S. Это осуществляют путем расщепления с помощью XhoI и "затупления" конца с помощью полимеразы фага Т4, с последующим расщеплением с помощью HindIII и выделением более крупного фрагмента, содержащего вектор-терминатор, в котором клонируют фрагмент промотора рСIВ1004. Это позволяет получить вектор, являющийся производным pCGN1761ENX, который содержит промотор PR-1a и терминатор tml и встроенный полилинкер с уникальными сайтами EcoRI и NotI. Выбранная кодирующая последовательность может быть встроена в этот вектор, и продукты слияния (т.е. промотор-ген-терминатор) затем могут быть перенесены в любой выбранный трансформирующий вектор, включая векторы, приведенные ниже. Различные химические регуляторы могут применяться для индуцирования экспрессии кодирующей последовательности в растениях, трансформированных согласно настоящему изобретению, в том числе производные бензотиадиазола, изоникотиновой кислоты и салициловой кислоты, описанные в патентах US 5523311 и 5614395.
д. Индуцибельная экспрессия, промотор. индуцируемый этанолом
Для обеспечения индуцибельной экспрессии кодирующей последовательности по настоящему изобретению также может применяться промотор, индуцируемый определенными спиртами или кетонами, например, этанолом. Таким промотором является, например промотор гена alcA Aspergillus nidulans (Caddick и др., Nat. Biotechnol. 16: 177-180 (1998)). В A. nidulans ген alcA кодирует алкогольдегидрогеназу I, экспрессия которой регулируется факторами транскрипции AlcR в присутствии химического индуктора. Для целей настоящего изобретения кодирующие последовательности CAT в плазмиде ра1сА:САТ, включающей последовательность промотора гена аlсА, слитую с минимальным промотором 35S (Caddick и др., Nat. Biotechnol. 16: 177-180 (1998)), заменяют кодирующей последовательностью по настоящему изобретению, получая кассету экспрессии, содержащую кодирующую последовательность, находящуюся под контролем промотора гена alcA. Это может быть осуществлено с помощью хорошо известных в данной области методов.
е. Индуцибельная экспрессия, промотор, индуцируемый глюкокортикоидом
Также может рассматриваться индукция экспрессии нуклеотидной последовательности по настоящему изобретению с использованием систем, основанных на стероидных гормонах. Например, можно использовать систему индукции, опосредуемую глюкокортикоидом (Aoyama и Chua, The Plant Journal, 11: 605-612 (1997)), и индуцировать экспрессию гена обработкой глюкокортикоидом, например, синтетическим глюкокортикоидом, предпочтительно дексаметазоном, предпочтительно в концентрации, находящейся в диапазоне от 0,1 до 1 мМ, более предпочтительно в диапазоне от 10 до 100 мМ. Для целей настоящего изобретения последовательности гена люциферазы заменяют нуклеотидной последовательностью по изобретению, конструируя кассету экспрессии, содержащую нуклеотидную последовательность по изобретению, находящуюся под контролем шести копий GAL4, расположенных против хода транскрипции относительно активирующих последовательностей, слитых с минимальным промотором 35S. Это осуществляют с помощью методов, хорошо известных в данной области. Трансактивирующий фактор включает ДНК-связывающий домен GAL4 (Keegan и др., Science 231: 699-704 (1986)), слитый с трансактивирующим доменом протеина вируса герпеса VP16 (Triezenberg и др., Genes Devel. 2: 718-729 (1988)), слитым с гормонсвязывающим доменом рецептора глюкокортикоида крысы (Picard и др., Cell 54: 1073-1080 (1988)). Экспрессия слитого протеина контролируется любым известным в данной области промотором, пригодным для экспрессии в растениях. Эту кассету экспрессии, содержащую нуклеотидную последовательность по изобретению, слитую с конструкцией 6GАL4/минимальный промотор, встраивают в растение. Таким образом обеспечивают специфичность слитого протеина в отношении ткани или органа, что приводит к индуцибельной экспрессии инсектицидного токсина специфическим в отношении ткани или органа образом.
ж. Специфичная для корня экспрессия
Другой схемой экспрессии гена является экспрессия в корне. Пригодным промотором для экспрессии в корне является промотор, описанный de Framound (FEBS 290: 103-106 (1991), а также в опубликованной заявке на патент ЕР 0452269, которая включена в настоящее описание в виде ссылки. Этот промотор переносят в пригодный вектор, такой, как pCGN1761ENX, для встраивания выбранного гена и последующего переноса полной кассеты промотор-ген-терминатор в представляющий интерес трансформирующий вектор.
з. Промоторы, индуцируемые ранением
Индуцируемые ранением промоторы также могут применяться для экспрессии гена. Описаны многочисленные такие промоторы (см., например, у Хu и др., Plant Molec. Biol. 22: 573-588 (1993), Logemann и др. Plant Cell 1: 151-151 (1989), Rohrmeier Lehle, Plant Molec. Biol. 22: 783-792 (1993), Firek и др. Plant Molec. Biol. 22: 129-142 (1993), Warner и др. Plant J. 3: 191-201 (1993), и они все пригодны для применения в соответствии с настоящим изобретением. Logemann с соавторами описали последовательности, расположенные против хода транскрипции по отношению к 5’-концу гена wun1 двудольного растения - картофеля. Хu с соавторами установили, что индуцируемый ранением промотор из двудольного растения - картофеля (pin2) обладает активностью в однодольном растении - рисе. Кроме того, Rohrmeier и Lehle описали клонирование кДНК Wip1 кукурузы, которая индуцируется ранением и которую можно применять для выделения родственного промотора, используя стандартные методы. Аналогично этому Firek с соавторами и Warmer с соавторами описали индуцируемый ранением ген из однодольного растения Asparagus officinalis, который локально экспрессируется в месте ранения и в местах внедрения патогена. Используя методы клонирования, хорошо известные в данной области, эти промоторы могут быть перенесены в пригодные векторы, слиты с генами и применены для экспрессии этих генов в местах повреждения растения ранением.
и. Предпочтительная для сердцевины экспрессия
В заявке на патент WO 93/07278, включенной в настоящее описание в виде ссылки, описано выделение гена trpA кукурузы, который предпочтителен для экспрессии в клетках сердцевины. Представлены последовательность гена и промотор, расположенные от начала транскрипции до нуклеотида - 1726. С использованием стандартных методов молекулярной биологии этот промотор или его части могут быть перенесены в такой вектор, как pCGN1761, в котором он может заменить промотор 35S и применяться для обеспечения экспрессии чужеродного гена предпочтительным для сердцевины образом. В сущности фрагменты, содержащие предпочтительный для сердцевины промотор или его части, могут быть перенесены в любой вектор и модифицированы для применения в трансгенных растениях.
к. Специфичная для листьев экспрессия
Ген кукурузы, кодирующий фосфоенолкарбоксилазу (РЕРС) описан Hudspeth и Grula (Plant Molec. Biol. 12: 579-589 (1989)). С использованием стандартных методов молекулярной биологии промотор этого гена может быть использован для обеспечения экспрессии любого гена в трансгенных растениях специфическим в отношении листьев образом.
л. Специфичная для пыльцы экспрессия
В заявке на патент WO 93/07278 описано выделение гена кальцийзависимой протеинкиназы (CDPK) кукурузы, который экспрессируется в клетках пыльцы. Последовательность гена и промотора простирается до положения 1400 пар оснований от сайта инициации транскрипции. С использованием стандартных методов молекулярной биологии этот промотор или его части могут быть перенесены в вектор, такой как pCGN1761, где им можно заменить промотор 35S, и он может быть использован для обеспечения экспрессии нуклеотидной последовательности по настоящему изобретению специфическим в отношении пыльцы образом.
2. Терминаторы транскрипции
Для применения в кассетах экспрессии пригодно широкое разнообразие терминаторов транскрипции. Они ответственны за прекращение транскрипции за трансгеном и за его правильное полиаденилирование. Соответствующие терминаторы транскрипции представляют собой терминаторы, для которых известно, что они обладают способность функционировать в растениях, и они включают терминатор 35S CaMV, терминатор tml, терминатор нопалинсинтазы, терминатор Е9 rbcS гороха. Они могут применяться как в однодольных, так и в двудольных растениях. Кроме того, могут применяться нативные терминаторы транскрипции генов.
3. Последовательности для усиления или регуляции экспрессии
Известны многочисленные последовательности, усиливающие экспрессию единицы транскрипции гена, и эти последовательности могут применяться в сочетании с генами по настоящему изобретению для усиления их экспрессии в трансгенных растениях.
Установлено, что различные интронные последовательности усиливают экспрессию, прежде всего в клетках однодольных растений. Например, установлено, что интроны гена Adhl кукурузы при интродукции в клетки кукурузы значительно усиливают экспрессию гена дикого типа под контролем родственного промотора. Установлено, что интрон 1 является особенно эффективным и усиливает экспрессию в гибридных конструкциях при слиянии с геном хлорамфеникол-ацетилтрансферазы (Callis и др., Genes Develop. 1: 1183-1200 (1987)). В этой же экспериментальной системе интрон гена bronzel кукурузы проявляет аналогичное действие по отношению к усилению экспрессии (Callis и др., выше). Последовательности интрона включают обычным способом в растительные трансформирующие векторы, обычно в составе нетранслируемой лидерной последовательности.
Также известно большое количество нетранслируемых лидерных последовательностей, происходящих из вирусов, которые усиливают экспрессию, и которые особенно эффективны в клетках двудольных растений. В частности, установлено, что лидерные последовательности из вируса табачной мозаики (TMV, "Ω-последовательность"), из вируса хлорозной пятнистости кукурузы (MCMV) и из вируса мозаики люцерны (AMV) эффективно усиливают экспрессию (см. например, у Galliе и др. Nucl. Acids Res. 15: 8693-8711 (1987); Skuzeski и др., Plant Molec. Biol. 15: 65-79 (1990)).
4. Направленный перенос генного продукта в клетке
У растений известны различные механизмы направленного переноса генных продуктов, и последовательности, контролирующие функционирование этих механизмов, охарактеризованы весьма подробно. Например, направленный перенос генных продуктов в хлоропласт контролируется сигнальной последовательностью, обнаруженной на N-конце различных протеинов, которая отщепляется во время импорта к хлоропласту, в результате чего получается зрелый протеин (см., например, у Comai и др., J. Biol. Chem. 263: 15104-15109 (1988)). Эти сигнальные последовательности могут быть слиты с гетерологичными генными продуктами для осуществления эффективного импорта гетерологичных продуктов в хлоропласт (van den Broeck и др., Nature 313: 358-363 1985)). ДНК, кодирующая соответствующие сигнальные последовательности, может быть выделена из 5’-конца кДНК, кодирующих протеин RUBISCO, протеин CAB, фермент EPSP-синтазу, протеин GS2 и целый ряд других протеинов, для которых известно, что они локализованы в хлоропласте. См. также раздел, озаглавленный "Экспрессия при направленном переносе в хлоропласт" в примере 37 патента US 5639949).
Другие генные продукты локализованы в других органеллах, таких как митохондрия и пероксисома (см., например, у Unger и др., Plant Molec. Biol. 13: 411-418 (1989)). кДНК, кодирующие эти продукты, также могут быть подвергнуты воздействиям для осуществления направленного переноса гетерологичных генных продуктов в эти органеллы. Примерами таких последовательностей являются кодируемые ядерной ДНК АТФазы и специфичные для митохондрий изоформы аспартат-аминотрансферазы. Направленный перенос в клеточные протеиновые тельца был описан у Rogers и др. (Proc. Natl. Acad Sci. USA 82: 6512-6516 (1985)).
Кроме того, были охарактеризованы последовательности, приводящие к направленному переносу генных продуктов в другие клеточные компартменты. N-концевые последовательности ответственны за направленный перенос в эндоплазматический ретикулум (ЭР), апопласт и за внеклеточную секрецию из алейронных клеток (Koehler и Но, Plant Cell 2: 769-783 (1990)). Кроме того, N-концевые последовательности в сочетании с С-концевыми последовательностями ответственны за направленный перенос генных продуктов в вакуоли (Shinshi и др., Plant Molec. Biol. 14: 357-368 (1990)).
Путем слияния описанных выше соответствующих направляющих последовательностей с представляющими интерес трансгенными последовательностями можно направлять трансгенный продукт в любую органеллу или любой компартмент клетки. Для направленного переноса, например, в хлоропласт сигнальную последовательность хлоропласта гена RUBISCO, гена CAB, гена EPSP-синтазы или гена GS2 сливают в рамке считывания с N-концевым кодоном ATG трансгена. Выбранная сигнальная последовательность должна включать известный сайт расщепления, и при конструировании гибридов следует учитывать любые аминокислоты, расположенные за сайтом расщепления, которые необходимы для расщепления. В некоторых случаях это требование может быть удовлетворено путем добавления небольшого количества аминокислот между сайтом расщепления и ATG трансгена, или в альтернативном варианте путем замещения нескольких аминокислот внутри последовательности трансгена. Гибриды, сконструированные для импорта в хлоропласт, могут быть оценены в отношении эффективности поглощения хлоропластом путем трансляции in vitro транскрибируемых in vitro конструкций с последующим поглощением in vitro хлоропластом с использованием методов, описанных у Bartlett и др. в: Edelmann и др. (ред.) Methods in Chloroplast Molecular Biology, Elsevier. стр. 1081-1091 (1982)); у Wasmann и др. (Mol. Gen. Genet. 205: 446-453 (1986)). Эти методы конструирования хорошо известны в данной области и одинаково пригодны как для митохондрий, так и для пероксисом.
Вышеописанные механизмы направленного переноса в клетке могут быть использованы не только в сочетании с их родственными промоторами, но также и с гетерологичными промоторами для того, чтобы осуществлять специфический целевой направленный перенос при регуляции транскрипции промотором, который имеет схему экспрессии, отличную от схемы экспрессии промотора, от которого исходит сигнал направленного переноса.
Пример 24. Конструирование растительных трансформирующих векторов
Специалистам в данной области известны многочисленные трансформирующие векторы, пригодные для трансформации растений, и гены по настоящему изобретению могут применяться в сочетании с любым из таких векторов. Выбор вектора зависит от предпочтительного метода трансформации и от видов-мишеней, предназначенных для трансформации. Для определенных видов-мишеней предпочтительными могут оказаться различные маркеры для селекции по признаку устойчивости к антибиотику или гербициду. Обычно применяемые для трансформации селектируемые маркеры включают ген nptII, который обусловливает устойчивость к канамицину и родственным антибиотикам (Messing и Vierra, Gene, 19: 259-268 (1982); Bevan и др., Nature 304: 184-187 (1983)), ген bar, обусловливающий устойчивость к гербициду фосфинотрицину (White и др., Nucl. Acids Res. 18: 1062 (1990), Spencer и др., Theor. Appl. Genet. 79: 625-631 (1990)), ген hpH, обусловливающий устойчивость к антибиотику гигромицину (Blochinger и Diggelmann, Mol. Cell Biol, 4: 2929-2931 (1984)) и ген dhfr, который обусловливает устойчивость к метотрексату (Bourouis и др., ЕМВО J., 2: 1099-1104 (1983)) и ген EPSPS, обусловливающий устойчивость к глифосату (патент US 4940935 и 5188642).
1. Конструирование векторов, пригодных для трансформации с помощью Agrobacterium
Для трансформации с использованием Agrobacterium tumefaciens пригодны многочисленные векторы. Они обычно несут по крайней мере одну пограничную последовательность Т-ДНК и включают такие векторы, как pBIN19 (Bevan, Nucl. Acids Res., (1984)) и pXYZ. Ниже описано конструирование двух типичных векторов, пригодных для трансформации с использованием Agrobacterium.
a. pCIB200 и pCIB2001:
Бинарные векторы рСIВ200 и рСIВ2001 применяют для конструирования рекомбинантных векторов, предназначенных для совместного использования с Agrobacterium, и их конструируют следующим образом. Создают pTJS75kan путем расщепления pTJS75 (Schmidhauser и Helinski, J. Bacteriol, 164: 446-455 (1985)) с помощью NarI, что позволяет вырезать ген устойчивости к тетрациклину, с последующим встраиванием фрагмента АсcI из плазмиды pUC4K, несущей NPTII (Messing и Vierra, Gene, 19: 259-268 (1982)); Bevan и др., Nature, 304: 184-187 (1983); McBridge и др., Plant Molecular Biology, 14: 266-276, (1990)). Линкеры XhoI лигируют с EcoRV-фрагментом рС1В7, содержащим левую и правую пограничные последовательности Т-ДНК, селектируемый в растении химерный ген nos/nptII и полилинкер pUC (Rothstein и др., Gene, 53: 153-161 (1987)), и клонируют расщепленный с помощью XhoI фрагмент в плазмиде pTJS75, расщепленной с помощью SalI, создавая рСIВ200 (см. также ЕР 0332104, пример 19 [1338]). Вектор рСIВ200 содержит в полилинкере следующие уникальные сайты, распознаваемые рестриктазами (сайты рестрикции): EcoRI, SstI, KpnI, BglII, XbaI и SalI. Вектор рСIВ2001 является производным рС1В200 и его создают путем инсерции в полилинкер дополнительных сайтов рестрикции. Уникальными сайтами рестрикции в полилинкере вектора рСIВ2001 являются EcoRI, SstI, KpnI, BglII, XbaI, SalI, МluI, BclI, AvrII, ApaI, HpaI и StuI. В дополнение к тому, что рСIВ2001 содержит эти уникальные сайты рестрикции, он также содержит ген для отбора трансформированных канамицином растений и бактерий, левую и правую пограничные последовательности Т-ДНК для опосредуемой Agrobacterium трансформации, функцию trfA, являющуюся производной RK2, для мобилизации между Е.coli и другими хозяевами, и функции OriT и OriV, также являющиеся производными RK2. Полилинкер рСIВ2001 пригоден для клонирования растительных кассет экспрессии, содержащих их собственные регуляторные сигналы.
б. Вектор pCIB10 и его производные, отобранные по признаку устойчивости к гигромицину
Бинарный вектор pCIB10 содержит ген, обусловливающий устойчивость к канамицину в растениях, правую и левую пограничные последовательности Т-ДНК и включает последовательности из плазмиды pRK252 с широким спектром хозяев, что позволяет осуществлять ее репликацию как в Е.coli, так и в Agrobacterium. Его конструкция описана у Rothstein и др., Gene, 53: 153-161, (1987)). У Gritz и др. (Gene, 25: 179-188, (1983)) описаны различные сконструированные производные pCIB10, которые включают ген фосфотрансфе-разы, обусловливающий устойчивость к гигромицину В. Эти производные дают возможность осуществлять селекцию клеток трансгенных растений либо только по признаку устойчивости к гигромицину (рСIВ743), либо по признаку устойчивости к гигромицину и канамицину (рСIВ715, рСIВ717).
2. Векторы, пригодные для трансформации без использования Agrobacterium
Трансформация без использования Agrobacterium tumefaciens дает возможность обойти требование наличия последовательностей Т-ДНК в выбранном трансформирующем векторе и, следовательно, векторы, в которых отсутствуют эти последовательности, могут быть использованы в дополнение к векторам, таким как описанные выше, которые содержат последовательности Т-ДНК. Методы трансформации, которые не основаны на использовании Agrobacterium, включают трансформацию с помощью бомбардировки частицами, поглощение протопластом (например, с помощью ПЭГ и электропорации) и микроинъекцию. Выбор вектора в значительной степени зависит от выбора предпочтительных видов, подлежащих трансформации. Ниже описано конструирование некоторых типичных векторов.
a. рCIB3064:
рСIВ3064 представляет собой вектор, являющийся производным pUC, пригодный для методов прямого переноса гена в сочетании с селекцией в отношении гербицида basta (или фосфинотрицина). Плазмида рСIВ246 включает промотор 35S CaMV, функционально связанный с геном GUS Е.coli, и терминатор транскрипции 35S CaMV, и она описана в опубликованной заявке РСТ WO 93/07278. Промотор 35S этого вектора содержит две ATG последовательности на 5’-конце сайта инициации. Эти сайты подвергают мутации с использованием стандартных методов ПЦР таким образом, чтобы удалить обе ATG и образовать сайты рестрикции SspI и PvuII. Новые сайты рестрикции находятся на расстоянии 96 и 37 пар оснований от уникального сайта Sall и на расстоянии 101 и 42 пар оснований от действительного сайта инициации. Образовавшееся производное плазмиды рСIВ246 обозначили как рСIВ3025. Затем ген GUS вырезают из рСIВ3025 путем расщепления с помощью Sall и SacI, концы затупляют и повторно лигируют, получая плазмиду рСIВ3060. Плазмиду рJIТ82 получают из John Innes Center, Norwich, и вырезают фрагмент SmaI длиной 400 пар оснований, содержащий ген bar из Streptomyces viridochromogenes, и встраивают в сайт HpaI плазмиды рСIВ3060 (Thompson и др., EMBO J., 6: 2519-2523, (1987)). Это позволяет получить плазмиду рСIВ3064, содержащую ген bar, находящийся под контролем промотора 35S CaMV и терминатора для селекции по признаку устойчивости к гербициду, ген обусловливающий устойчивость к ампициллину (для селекции в Е.coli) и полилинкер с уникальными сайтами SphI, PstI, HindIII и BamHI. Этот вектор пригоден для клонирования растительных кассет экспрессии, содержащих их собственные регуляторные сигналы.
б. pSOG19 и pSOG35:
pSOG35 представляет собой трансформирующий вектор, в котором в качестве селектируемого маркера присутствует ген дигидрофолатредуктазы (DHFR) Е. coli, обусловливающий устойчивость к метотрексату. Для амплификации промотора 35S (~800 пар оснований), интрона 6 гена Adh1 кукурузы (~550 пар оснований) и фрагмента длиной 18 пар оснований нетранслированной лидерной последовательности GUS из плазмиды pSOG10 применяют ПЦР. Фрагмент длиной 250 пар оснований, кодирующий ген дигидрофолатредуктазы типа II Е. coli, также амплифицируют с помощью ПЦР и эти два ПЦР-фрагмента объединяют с фрагментом SacI-PstI из рВI221 (фирмы Clontech), который содержит основу вектора pUC19 и терминатор нопалинсинтазы. Сборка этих фрагментов позволяет получить плазмиду pSOG19, содержащую промотор 35S в слиянии с последовательностью интрона 6, лидером GUS, геном DHFR и терминатором нопалинсинтазы. Замена лидера GUS в pSOG19 на лидерную последовательность вируса хлорозной мозаики кукурузы позволяет получить вектор pSOG35. pSOG19 и pSOG35 несут ген pUC, обусловливающий устойчивость к ампициллину, и имеют сайты HindIII, SphI, PstI и EcoRI, пригодные для клонирования чужеродных последовательностей.
3. Вектор, пригодный для трансформации хлоропласта
Для экспрессии нуклеотидной последовательности по настоящему изобретению в пластидах растения используют пластидный трансформирующий вектор рРН143 (WO 97/32011, пример 36). Нуклеотидную последовательность встраивают в рРН143, заменяя ей кодирующую последовательность PROTOX (протопорфириногеноксидаза). Затем этот вектор используют для трансформации пластид и отбора трансформантов по признаку устойчивости к спектиномицину. В альтернативном варианте нуклеотидную последовательность встраивают в рРН143 таким образом, чтобы она заменяла ген aadH. В этом случае трансформанты отбирают по признаку устойчивости к ингибиторам PROTOX.
Пример 25. Трансформация
После того как нуклеотидная последовательность клонирована в экспрессионной системе, ей трансформируют растительную клетку. Методы трансформации и регенерации растений хорошо известны в данной области. Например, для введения чужеродной ДНК, а также для непосредственного поглощения ДНК, введения с помощью липосом, электропорации, микроинъекции и с помощью микроснарядов, используют Ti-плазмиды. Кроме того, для трансформации растительных клеток могут быть использованы бактерии рода Agrobacterium. Ниже описаны репрезентативные методы трансформации как двудольных, так и однодольных растений, а также репрезентативный метод трансформации пластид.
1. Трансформация двудольных растений
Методы трансформации двудольных растений хорошо известны в данной области и включают методы, основанные на применении Agrobacterium, и методы, для которых не требуется использовать Agrobacterium. Методы, для которых не требуются Agrobacterium, включают поглощение экзогенного генетического материала непосредственно протопластами или клетками. Это может быть осуществлено путем поглощения, опосредованного ПЭГ, или электропорацией, введения с помощью бомбардировки частицами, или путем микроинъекции. Примеры этих методов описаны у Paszkowski и др., EMBO J. 3:2717-2722 (1984), Potrykus и др., Mol. Gen. Genet. 199: 169-177 (1985), Reich и др.. Biotechnology 4: 1001-1004 (1986) и у Klein и др.. Nature 327: 70-73 (1987). В каждом случае трансформированные клетки регенерируют до целых растений, используя стандартные методы, известные в данной области.
Трансформация, опосредуемая Agrobacterium, является предпочтительным методом трансформации двудольных вследствие высокой эффективности трансформации при использовании этого метода и его широкой применимости для целого ряда различных видов. Трансформация с помощью Agrobacterium обычно включает перенос бинарного вектора, несущего представляющую интерес чужеродную ДНК (например, рСIВ200 или рСIВ2001), в пригодный штамм Agrobacterium, который может зависеть от комплемента vir-генов штамма Agrobacterium-хозяина, и которые могут располагаться либо на корезидентной Ti-плазмиде, либо на хромосоме (например, штамм CIB542 для рС1В200 и pCIB2001 (Uknes и др. Plant Cell 5: 159-169 (1993)). Перенос рекомбинантного бинарного вектора в Agrobacterium производят путем трехродительского скрещивания с использованием Е. coli, несущей рекомбинантный бинарный вектор, штамма-хелпера Е. coli, несущего плазмиду, такую как pRK2031, и который способен мобилизировать рекомбинантный бинарный вектор к направленному переносу в штамм-мишень Agrobacterium. В альтернативном варианте рекомбинантный бинарный вектор может быть перенесен в Agrobacterium с помощью ДНК-трансформации ( и Willmitzer, Nucl. Acids Res. 16:9877 (1988)).
и Willmitzer, Nucl. Acids Res. 16:9877 (1988)).
Трансформация видов растений-мишеней с помощью рекомбинантной Agrobacterium обычно включает совместное культивирование Agrobacterium с эксплантатами растения и выполняется в соответствии с протоколами, хорошо известными в данной области. Трансформированную ткань регенерируют на селектируемой среде, содержащей маркер для селекции по признаку устойчивости к антибиотику или гербициду, расположенный между пограничными последовательностями Т-ДНК бинарной плазмиды.
Другой метод трансформации клеток растения геном основан на введении инертных или обладающих биологической активностью частиц в ткани или клетки растения. Этот метод описан в патентах США 4945050, 5036006 и 5100792 (все на имя Sanford и др.). Обычно этот метод состоит во введении инертных или обладающих биологической активностью частиц в клетки в условиях, позволяющих им проникнуть через внешнюю оболочку клетки и осуществить встраивание внутрь нее. Если используются инертные частицы, то вектор может быть введен в клетку путем нанесения на частицы вектора, содержащего целевой ген. В альтернативном варианте клетка-мишень может быть окружена вектором таким образом, что этот вектор переносится внутрь клетки следом за частицей. Для введения внутрь ткани клетки растения также могут использоваться биологически активные частицы (например, высушенные клетки дрожжей, высушенные бактерии или бактериофаги, каждая (ый) из которых содержит ДНК, предназначенную для введения).
2. Трансформация однодольных растений
Трансформация большинства однодольных видов растений в настоящее время также стала традиционной. Предпочтительные методы включают прямой перенос генов в протопласты с использованием методов на основе ПЭГ или электропорации и бомбардировки частицами ткани каллюса. Трансформации могут быть осуществлены с одиночными видами ДНК или с множественными видами ДНК (т.е. котрансформация), и оба эти метода пригодны для использования по настоящему изобретению. Преимуществом котрансформации может состоять в том, что она не требует полной векторной конструкции и дает возможность получать трансгенные растения с несцепленными локусами для представляющего интерес гена и селектируемого маркера, что позволяет удалить селектируемый маркер в последующих поколениях, если это представляется необходимым. Однако недостатком применения метода котрансформации является то, что частота, с которой разные виды ДНК интегрируются в геном, составляет менее 100% (Schocher и др. Biotechnology 4: 1093-1096 (1986)).
В заявках на патенты ЕР 0292435, ЕР 0392225 и WO 93/072778 описаны способы получения каллюса и протопластов элитной инбредной линии кукурузы, трансформации протопластов с использованием ПЭГ или электропорации и регенерации растений кукурузы из трансформированных протопластов. Gordon-Kamm и др., в Plant Cell 2: 603-618 (1990) и Fromm и др., в Biotechnology 8: 833-839 (1990)) описали методы трансформации линии кукурузы, полученной из линии А188, с использованием бомбардировки частицами. Методы трансформации элитных инбредных линий кукурузы путем бомбардировки частицами также описаны в WO 93/07278 и у Koziel с соавторами (Biotechnology 11: 194-200 (1993)). Этот метод включает использование незрелых зародышей кукурузы длиной 1,5-2,5 мм, вырезанных из початка кукурузы через 14-15 дней после опыления, и устройства для бомбардировки типа PDS-l000 He Biolistics.
Трансформация риса также может быть осуществлена с использованием методов прямого переноса гена с использованием протопластов или бомбардировки частицами. Опосредуемая протопластом трансформация описана для японских и индийских типов риса (Zhang и др., Plant Cell Rep. 7: 379-384 (1988); Shimamoto и др., Nature 338: 274-277 (1989); Datta и др., Biotechnology 8: 736-740 (1990)). Оба типа риса также трансформируют стандартными методами с использованием бомбардировки частицами (Christou и др., Biotechnology 9: 957-962 (1991)). Кроме того, в WP 93/21335 описаны методы трансформации риса с помощью электропорации.
В заявке на патент ЕР 0332581 описаны методы получения, трансформации и регенерации протопластов растений сем. мятликовых (Pooideae). Эти методы дают возможность трансформировать ежу (Dactylis spp.) и пшеницу. Кроме того, у Vasil с соавторами (Biotechnology 10: 667-674 (1992)) описана трансформация пшеницы с использованием бомбардировки частицами клеток каллюса типа С с продолжительным временем регенерации, и также у Vasil с соавторами (Biotechnology 11: 1553-1558 (1993)) и у Weekes с соавторами (Plant Physiol. 102: 1077-1084 (1993)) описана трансформация с использованием бомбардировки частицами незрелых зародышей и незрелого каллюса эмбрионального происхождения. Однако предпочтительный метод трансформации пшеницы включает трансформацию пшеницы путем бомбардировки частицами незрелых зародышей, и для него требуется наличие либо стадии высокого содержания сахарозы или высокого содержания мальтозы, предшествующей введению гена. До бомбардировки любое количество зародышей (длиной 0,75-1 мм) высевают в MS-среду с добавлением 3% сахарозы (Murashige и Skoog, Physiologia Plantarum 15: 473-497 (1962)) и 3 мг/л 2,4-Д (дихлорфеноксиуксусная кислота) для индукции соматических зародышей, которым дают возможность развиваться в темноте. В назначенный день бомбардировки зародыши удаляют из среды для индукции и помещают в осмотикум (т.е. в среду для индукции с добавлением сахарозы или мальтозы в нужной концентрации, обычно 15%). Зародышам дают возможность пройти плазмолиз в течение 2-3 ч и затем подвергают бомбардировке. В одной чашке-мишени обычно используют по 20 зародышей, хотя это количество не имеет решающего значения. Соответствующую несущую ген плазмиду (такую, как рСIВ3064 или pSG35) осаждают на золотые частицы размером порядка микрона, используя стандартные методы. Каждую чашку с зародышами обстреливают с помощью устройства на основе гелия DuPont Biolistics® при давлении залпа ~1000 фунтов/кв.дюйм и стандартного экрана с размером пор 80 меш. После бомбардировки зародыши помещают обратно в темноту для восстановления в течение приблизительно 24 ч (все еще в осмотикуме). Через 24 ч зародыши удаляют из осмотикума и помещают назад в среду для индукции, где они остаются в течение приблизительно месяца до регенерации. Приблизительно через один месяц эксплантаты зародышей с развивающимся эмбриогенным каллюсом переносят в среду для регенерации (MS + 1 мг/л НИК, 5 мг/л ГК (гибереллиновая кислота)), содержащую, кроме того, соответствующий селектирующий агент (10 мг/л баста в случае рСIВ3064 и 2 мг/л метотрексата в случае pSOG35). Спустя приблизительно один месяц развившиеся ростки переносят в более крупные стерильные контейнеры, известные, как "GA7s", содержащие MS с половинной крепостью, 2%-ную сахарозу и такую же концентрацию селектирующего агента.
Также описана трансформация однодольных растений с использованием Agrobacterium (см. WP 94/00977 и патент США 5591616, которые оба включены в настоящее описание в виде ссылки).
3. Трансформация пластид
Семена Nicotiana tabacum сорта "Xanthi nc" высаживают из расчета 7 штук на чашку по окружности диаметром 1 дюйм на Т-агаровую среду и через 12-14 дней после посева подвергают бомбардировке частицами вольфрама размером 1 мкм (М10, фирма Biorad, Hercules, CA), покрытыми ДНК плазмид рРН143 и рРН145, в основном согласно методу, описанному у Svab Z. и Maliga P., PNAS 90, 913-917 (1993). Подвергнутые бомбардировке проростки инкубируют на Т-среде в течение двух дней, после чего отрезают листья и помещают абаксиальной стороной кверху под яркое освещение (350-500 мкмолей фотонов/м2/с) на пластины со средой RMOP (Svab Z., Hajdukiewicz P, и Maliga Р. PNAS 87, 8526-8530 (1990)), содержащей 500 мкг/мл дигидрохлорида спектиномицина (фирма Sigma, St.Louis, МО). Устойчивые проростки, у которых через 3-8 недель после бомбардировки появляются обесцвеченные снизу листья, субклонируют на этой же селективной среде, позволяют образовать каллюс и вторичные проростки выделяют и субклонируют. Полное разделение копий трансформированного пластидного генома (гомоплазматическое состояние) в независимых субклонах определяют с помощью стандартных методов Саузерн-блоттинга (Sambrook и др., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, Cold Spring Harbor (1989)). Расщепленную с помощью BamHI/EcoRI общую клеточную ДНК (Mettler I.J. Plant Mol. Biol. Reporter 5, 346-349 (1987)) разделяют на 1%-ных трис-боратных (ТВЕ) агарозных гелях, переносят на найлоновые мембраны (фирма Amersham) и зондируют меченными с помощью 32Р примированными случайным образом последовательностями ДНК, соответствующими BamHI/HindIII-фрагменту ДНК длиной 0,7 т.п.н. из рС8, который содержит часть последовательности rps7/12, обеспечивающий направленный перенос в пластиду. Гомоплазматические побеги высаживают в асептических условиях на содержащую спектиномицин среду MS/IBA (McBride К.Е. и др. PNAS 91, 7301-7305 (1994)) и переносят в теплицу.
Д. Селекция и производство семян
Растения, получаемые путем трансформации нуклеотидной последовательностью по настоящему изобретению, могут относиться к любому из широкого разнообразия видов растений, включая однодольные и двудольные растения; однако предпочтительно растения, используемые в способе по изобретению, выбирают из приведенного выше списка важных с сельскохозяйственной точки зрения целевых культур. Способность к экспрессии гена по настоящему изобретению в сочетании с другими характеристиками, важными с точки зрения продуктивности и качества, может быть придана линиям растений с помощью селекции. Принципы и методы селекции являются известными в данной области (см., например, у Welsh J.R., Fundamentals of Plant Genetics and Breeding, John Wiley & Sons, NY (1981); Crop Breeding, Wood D.R. (ред.) American Society of Agronomy, Madison, Wisconsin (1983); Mayo O. The Theory of Plant Breeding, 2-e изд., Clarendon Press, Oxford (1987); Singh D.P., Breeding for Resistance to Diseases and Insect Pests, Springer-Verlag, NY (1986); и у Wricke и Weber, Quantitative Genetics and Selection Plant Breeding, Walter de Gruyter и Со.,, Берлин (1986)).
Генетические признаки, сконструированные в описанных выше трансгенных семенах и растениях, передаются с помощью полового размножения или вегетативного роста и, таким образом, могут сохраняться и передаваться по наследству потомству растений. Обычно указанное сохранение и передачу потомству осуществляют с использованием известных сельскохозяйственных методов, разработанных для конкретных целей, таких как обработка почвы, посев или сбор урожая. Также могут применяться специализированные способы, такие как гидропоника или выращивание в закрытом грунте. Поскольку выращиваемые культурные растения подвержены нападению и повреждениям, которые вызываются насекомыми или инфекциями, а также подвержены конкуренции со стороны сорных растений, для улучшения урожая проводят мероприятия по борьбе с сорняками, болезнями растений, насекомыми, нематодами и другими вредными факторами. Они включают механические способы, такие как обработка почвы или удаление сорняков и зараженных растений, а также применение средств защиты растений, таких, как гербициды, фунгициды, гаметоциды, нематоциды, регуляторы роста, агенты, способствующие созреванию, и инсектициды.
Кроме того, дающие преимущества генетические особенности трансгенных растений и семян по изобретению могут быть использованы при селекции растений с целью выведения растений с улучшенными свойствами, такими как толерантность к вредителям, гербицидам или стрессу, с улучшенной питательной ценностью, повышенной урожайностью или улучшенным строением, способствующим уменьшению потерь от полегания или осыпания. Для различных стадий селекции характерно целенаправленное вмешательство человека, такое как отбор линий, подлежащих скрещиванию, непосредственное опыление родительских линий или отбор соответствующего потомства растений. В зависимости от требуемых свойств выбирают различные способы селекции. Соответствующие методы хорошо известны в данной области и включают гибридизацию, инбридинг, возвратное скрещивание, многолинейное скрещивание, смешивание сортов, межвидовую гибридизацию, методы анэуплодии и т.д., но не ограничены ими. Методы гибридизации также включают стерилизацию растений с целью получения мужских или женских стерильных растений с помощью механических, химических или биохимических способов. Перекрестное опыление мужского стерильного растения пыльцой различных линий гарантирует, что геном мужского стерильного, но фертильного женского растения будет равным образом приобретать свойства обеих родительских линий. Таким образом, трансгенные семена и растения по настоящему изобретению могут применяться для селекции улучшенных линий растений, что, например, позволяет увеличить эффективность обычных методов, таких как обработка гербицидом или пестицидом, или дает возможность обойтись без этих методов благодаря модифицированным генетическим особенностям этих растений. Кроме того, могут быть получены новые культурные растения с улучшенной толерантностью к стрессу благодаря оптимизации генетического "аппарата", что позволяет получить урожай продуктов лучшего качества по сравнению с продуктами, полученными от растений, которые не обладают способностью сопротивляться аналогичным вредным условиям в процессе их развития.
Пример 27. Производство семян
При производстве семян качество прорастания и однородность семян являются важными характеристиками продукта, в то время как качество прорастания и однородность семян, собираемых и продаваемых фермером, не являются важными. Поскольку трудно выращивать культурное растение вне контакта с семенами другого культурного и сорного растения, для борьбы с передающимися с семенами болезнями и для получения семян с хорошим прорастанием производителями, занимающимися выращиванием, кондиционированием и продажей чистых семян, разработаны довольно обширные и целенаправленные способы производства семян. Так, обычно фермер практикует покупку сертифицированного семенного материала, удовлетворяющего определенным стандартам качества, вместо того, чтобы использовать семенной материал, полученный от его собственной культуры. Материал для размножения, который используют в качестве семенного материала, обычно обрабатывают защитным покрытием, включающим гербициды, инсектициды, фунгициды, бактерициды, нематоциды, моллюскициды или их смеси. Обычно применяемые защитные покрытия включают такие соединения как каптан, карбоксин, тирам (TMTD®), металаксил (Apron®) и пиримифосметил (Actelinc®). При необходимости эти соединения изготавливают в виде препаративных форм вместе с дополнительными носителями, поверхностно-активными веществами или способствующими нанесению адъювантами, обычно применяемыми в области препаративных форм, для защиты от повреждения, вызванного бактериями, грибами или насекомыми-вредителями. Защитные покрытия могут быть нанесены путем пропитывания материала для размножения жидкой композицией или путем покрытия объединенной влажной или сухой композицией. Также возможны другие способы нанесения, такие как обработка почек или плодов.
Еще одним предметом изобретения являются новые сельскохозяйственные методы, такие как приведенные выше методы, для которых характерно применение трансгенных растений, трансгенного растительного материала или трансгенных семян по настоящему изобретению.
Семена могут быть помещены в мешок, контейнер или сосуд, сделанные из пригодного упаковочного материала, мешок или контейнер должны иметь возможность закрываться для сохранности семян. Мешок, контейнер или сосуд могут быть предназначены либо для кратковременного, либо продолжительного хранения семян, либо для того и для другого одновременно. Примеры пригодного упаковочного материала включают бумагу, такую как крафт-бумага, жесткий или гибкий пластик или иной полимерный материал, стекло или металл. Предпочтительно, чтобы мешок, контейнер или сосуд состояли из нескольких слоев упаковочных материалов одного и того же типа или различных типов. В одном из вариантов осуществления мешок, контейнер или сосуд изготавливают таким образом, чтобы исключить или ограничить контакт семян с водой или влагой. В одном примере мешок, контейнер или сосуд запечатывают, например, запечатывают с помощью нагрева, для того, чтобы воспрепятствовать проникновению воды или влаги. В другом варианте между слоями упаковочного материала или на них помещают абсорбирующие воду материалы. Еще в одном варианте осуществления мешок, контейнер или сосуд, или упаковочный материал, из которого он состоит, обрабатывают для того, чтобы ограничить, подавить или предупредить заражение болезнью, загрязнение или другие вредные факторы, возникающие при хранении или транспортировке семян.
Примером такой обработки является стерилизация, например, с помощью химических средств или путем облучения. Под объем настоящего изобретения подпадает мешок, предназначенный для коммерческого использования, содержащий семена трансгенного растения, несущие ген по настоящему изобретению, который экспрессируется в трансформированном растении с более высоким уровнем, чем в растении дикого типа, вместе с пригодным носителем и с инструкцией по применению для обеспечения устойчивости растений к широкому спектру болезней.
Описанные выше варианты осуществления приведены с целью иллюстрации. Данное описание изобретения дает возможность специалисту в данной области осуществить многочисленные вариации изобретения. Следует понимать, что все такие очевидные и предсказуемые вариации подпадают под объем прилагаемой формулы изобретения.
















| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ И СПОСОБЫ КОНТРОЛЯ ВРЕДИТЕЛЕЙ РАСТЕНИЙ | 2016 |
|
RU2759224C2 |
| СКОНСТРУИРОВАННЫЕ ПЕСТИЦИДНЫЕ БЕЛКИ И СПОСОБЫ КОНТРОЛЯ ВРЕДИТЕЛЕЙ РАСТЕНИЙ | 2017 |
|
RU2772947C2 |
| НОВЫЕ ПЕСТИЦИДНЫЕ ПРОТЕИНЫ И ШТАММЫ | 1995 |
|
RU2196824C2 |
| ИНСЕКТИЦИДНЫЕ CRY-ТОКСИНЫ DIG-3 | 2010 |
|
RU2590708C2 |
| ТОКСИН AXMI277 ПРОТИВ НЕМАТОД И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2012 |
|
RU2706488C2 |
| КОМПОЗИЦИИ И СПОСОБЫ КОНТРОЛЯ ВРЕДИТЕЛЕЙ РАСТЕНИЙ | 2016 |
|
RU2745306C2 |
| СПОСОБЫ ГЕНЕТИЧЕСКОГО КОНТРОЛЯ ПОРАЖЕНИЯ РАСТЕНИЙ НАСЕКОМЫМИ И ПРИМЕНЯЕМЫЕ ДЛЯ ЭТОГО КОМПОЗИЦИИ | 2006 |
|
RU2478710C2 |
| ВЫДЕЛЕННАЯ ДНК, ПРЕДСТАВЛЯЮЩАЯ СОБОЙ ПРОМОТОР (ВАРИАНТЫ), ВЕКТОР, СОДЕРЖАЩИЙ ЭТУ ДНК, И СПОСОБ ПОЛУЧЕНИЯ ТРАНСГЕННОГО РАСТЕНИЯ С ПОМОЩЬЮ ЭТОЙ ДНК (ВАРИАНТЫ) | 1999 |
|
RU2245921C2 |
| НОВЫЕ ГЕНЫ РАСТЕНИЙ И ИХ ПРИМЕНЕНИЕ | 2000 |
|
RU2241749C2 |
| ГИБРИДНЫЙ ИНСЕКТИЦИДНЫЙ БЕЛОК, МОЛЕКУЛА НУКЛЕИНОВОЙ КИСЛОТЫ, КОДИРУЮЩАЯ ТАКОЙ БЕЛОК, ТРАНСГЕННЫЕ РАСТЕНИЯ И ИХ СЕМЕНА, СОДЕРЖАЩИЕ ТАКОЙ БЕЛОК, СПОСОБ ПОЛУЧЕНИЯ БЕЛКА И ЕГО ПРИМЕНЕНИЕ | 2008 |
|
RU2497830C2 |
Изобретение относится к биотехнологии, в частности к биотехнологии сельскохозяйственных растений. Выделяют нуклеотидные последовательности из Xenorhabdus nematophilus, Xenorhabdus poinarii и Photorhabdus lumintecens, при экспрессии которых образуются новые инсектицидные токсины. Трансформируют клетку-хозяна химерным геном, включающим одну из выделенных нуклеотидных последовательностей. Получают композиции и препаративные формы, содержащие инсектицидные токсины, пригодные для борьбы с насекомыми-вредителями. Изобретение позволяет повысить устойчивость растений к насекомым-вредителям, и тем самым повысить сбор сельскохозяйственной продукции. 8 н. и 15 з.п. ф-лы.
| WO 9500647 A, 05.01.1995.WO 9303154 A, 18.02.1993.WO 9638547 A, 05.12.1996.RU 2107725 C, 27.03.1998. |
Авторы
Даты
2004-11-20—Публикация
1999-04-19—Подача