Данная заявка связана с патентной заявкой США под номером №09/109,235, поданной 30 июня 1989 года и в настоящее время отозванной, и с предварительной заявкой под номером №60/146,432, поданной 29 июля 1999 года.
Эта заявка была сделана при поддержке правительства Соединенных Штатов, согласно контракту предоставленному Министерством Энергетики США. Правительство имеет некоторые права в этом изобретении.
Предпосылки изобретения
Данное изобретение посвящено средствам, предназначенным для нейтрализации химических и биологических веществ или агентов, в частности - компонентов химического и биологического оружия, а также способу получения этих средств. В частности, данное изобретение посвящено средствам, содержащим солюбилизирующие соединения и реагирующие соединения, которые могут поставляться в виде пенообразующих композиций, распыляемых композиций, жидкостей, туманообразующих композиций и аэрозолей для увеличения скорости реакций нейтрализации химических соединений и других добавок. Эти средства предназначены для нейтрализации или уменьшения влияния некоторых биологических составов или отравляющих веществ (ОВ).
Угрозы террористов, потенциально использующих оружие массового поражения, усиливаются как в Соединенных Штатах, так и за границей. Вопросы применения и угрозы применения химических и биологических ОВ как оружия массового поражения имеют первостепенное значение как для национальной обороны в целом, так и для муниципальных властей.
Некоторые активные компоненты химического оружия (ХО), используемые террористами в качестве угрозы, имеют химические характеристики, которые предоставляют возможность для разработки контрмер. Химические вещества зарин, зоман и табун (G-агенты) являются примерами соединений, содержащих фосфор, которые, изменяясь химически, могут потерять свою токсичность. Горчичный газ, являясь примером Н-агентов, и VX, являясь примером V-агентов, также могут изменяться химически и становиться безопасными. Кроме того, некоторые известные активные компоненты биологического оружия (БО), включая ботулинический токсин, бациллы сибирской язвы и другие спорообразующие бактерии, вегетирующие бактерии, включая бактерии чумы и различные вирусы, также могут подвергаться химической дезактивации.
Использование ХО или БО может сопровождаться локальным или широким рассеиванием ОВ, угрожающих населению. Из-за гибкости развертывания веществ ХО и БО (ХБО), атакуемые могут подвергаться их воздействию во всем разнообразии их физических состояний, в большинстве случаев - в виде аэрозолей и паров.
Для восстановления гражданских средств обслуживания в случае внутреннего террористического нападения требуется эффективная, быстрая и безопасная (не токсичная и не коррозийная) технология обеззараживания. В идеальном случае такая технология должна быть использована в различных ситуациях, таких как обеззараживание открытых, полуоткрытых или закрытых объектов, а также чувствительной аппаратуры. Примеры таких объектов, для деактивации которых могут быть использованы обеззараживающие композиции, включают стадион (открытый), подземную станцию метрополитена (полуоткрытый), и крупный аэропорт или административное здание (закрытый).
Обеззараживание химических соединений в первую очередь сосредоточено на боевых химических ОВ, в частности на нервно-паралитических веществах (таких как G-агенты и V-агенты), и веществах кожно-нарывного действия (таких как горчичный газ или просто горчица). Реакции, участвующие в детоксификации химических веществ, можно разделить на реакции замещения и реакции окисления. Обеззараживание биологических ОВ в первую очередь сосредоточено на бактериальных спорах (напр., спорах сибирской язвы), которые, как считается, из всех микроорганизмов наиболее трудно уничтожить.
Реакции замещения
Гидролиз химических веществ можно осуществить водой, гидроксильными ионами или другими нуклеофильными реагентами. Скорость гидролиза горчичного газа и природа образующихся продуктов в первую очередь зависит от растворимости данного агента в воде и от значения рН раствора. При детоксификации горчичного газа, например, молекула вначале образует циклический сульфониевый катион, который взаимодействует с нуклеофильными реагентами (Янг (Yang), 1995). Доминирующим продуктом является тиодигликоль, однако этот продукт может реагировать с ионами сульфония с образованием вторичных промежуточных продуктов.
В щелочных условиях гидролиз зарина (GB) и зомана (GD) происходит быстро и дает соответствующую О-алкил-метилфосфоновую кислоту. В противоположность этому гидролиз VX ионами ОН- - более сложный процесс. Кроме того, для замещения тиоалкильной группы (т.е. разрыва P-S связи), замещается О-этильная группа (т.е. разрыв Р-О связи), образуя токсичный продукт, известный как ЕА-2192 (Янг и др.(Yang et al.), 1997). Нуклеофильные реагенты входят в состав молекулы и отделяют промежуточный продукт из апикального положения. Электроотрицательные группы, такие как RO группы, предпочтительно занимают апикальные положения, а группы, которые являются объемистыми или донорами электронов, такие как RS группы, занимают экваториальные положения. Структура конечного продукта будет зависеть от баланса между апикофильностью и реакционной способностью уходящей группы. В результате, разрыв P-S связи стимулируется разрывом Р-О связи приблизительно в 5 раз. С другой стороны, оказалось, что пероксигидролиз с использованием ионов ООН- в щелочной среде обеспечивает количественный разрыв P-S связи в 30-40 раз быстрее, чем при использовании ионов ОН-. Такая селективность была связана с относительной щелочностью анионного нуклеофильного реагента и уходящих анионов.
Были описаны каталитические реагенты для ускорения реакций замещения. Примером такого реагента является о-йодозобензоат (ИБ). Пример, который иллюстрирует каталитическую реакцию с участием этого соединения, приводят Мосс (Moss) и Жанг (Zhang )(1993). В этом примере ИБ превращается в йодоксизобензоат (ИОБ) путем окисления и дальше в таком виде участвует в реакции с ОВ.
С целью придания активной группе поверхностно-активных свойств в молекулу IBA были введены функциональные группы (Мосс и др.(Moss et al.), 1986). Были также получены комплексы ионов металлов с аминами, обладающие поверхностно-активными свойствами, которые, как было показано, проявляли каталитическую активность в реакциях замещения. Было также показано, что энзимы, такие как ангидролаза органофосфорной кислоты, ускоряют реакции замещения у G- и VX-агентов.
Реакции окисления
Методы окислительного обеззараживания могут успешно применяться для горчичного газа и VX (Yang, 1995). Раньше в качестве окислителя использовали перманганат калия. Недавно была предложена смесь KHSО5, KHSО4 и K2SО4. Было показано, что некоторые перекисные соединения (напр., перборат, надуксусная кислота, м-хлор-пероксибензойная кислота, монопероксифталат магния и перекись бензоила) также окисляют химические вещества. Совсем недавно было показано, что гидропероксикарбонатные анионы, образовавшиеся в результате взаимодействия бикарбонатного иона и перекиси водорода, эффективно окисляют горчичный газ и VX. Полиоксиметаллаты катализируют окисление химических веществ при комнатной температуре, однако, как известно, скорость таких реакций низкая. Некоторые из этих соединений при взаимодействии с химическими ОВ меняют окраску, что указывает на присутствие химического ОВ.
Угроза БО может быть более серьезной, чем угроза ХО. Это частично объясняется высокой токсичностью агентов БО, легкостью их приобретения и производства и сложностью их обнаружения. Существуют сотни боевых биологических средств, которые доступны террористам. Они могут быть сгруппированы по следующим категориям: спорообразующие бактерии (напр., сибирская язва), вегетативные бактерии (напр., чума, холера), вирусы (напр., оспа, желтая лихорадка) и бактериальные токсины (напр., ботулизм, рицин). Считают, что из всех микроорганизмов наиболее трудно уничтожить бактериальные споры.
Бактериальные споры - это исключительно резистентные структуры, которые образуются некоторыми грамположительными бактериями, обычно, в ответ на стрессовые условия окружающей среды. Наиболее важными спорообразующими являются представители родов Bacillus и Clostridium. Споры - значительно более сложные образования, чем растительные клетки. Внешняя поверхность споры состоит из оболочки споры, которая, как правило, представляет собой плотный слой нерастворимых протеинов, обычно содержащих большое число дисульфидных связей. Кора состоит из пептидоглюкана, первичная структура полимера построена из сшитых N-ацетилглюкозамина и N-ацетилмурамовой кислоты. Ядро споры содержит нормальные (вегетативные) клеточные структуры, такие как рибосомы и нуклеоид.
Начиная с их открытия, значительные исследования были проведены для разработки методов уничтожения бактериальных спор. Как правило, споры обладают высокой устойчивостью по отношению ко многим обычным физическим и химическим воздействиям, однако некоторые антибактериальные вещества являются спорицидными. Большинство мощных бактерицидных веществ могут подавлять лишь прорастание и развитие спор, т.е. являются спористатическими, но не спорицидными. Примеры спорицидных реагентов, применяемых в относительно высоких концентрациях, включают глутаральдегид, формальдегид, кислородные кислоты йода и хлора, пероксикислоты и окись этилена. В основном, все эти вещества являются токсичными.
Существуют несколько способов для уничтожения спор. Эти способы могут применяться по отдельности или одновременно. Один из способов предусматривает растворение или химическое разрушение внешней оболочки споры, что позволит окислителю проникнуть внутрь споры. Ряд исследований (Кинг и Гулд (King and Gould), 1969; Гулд и др. (Gould et al.), 1970) показывает, что богатый S-S (дисульфидными) связями протеин оболочки споры образует структуру, которая успешно маскирует участки, способные реагировать с окислителем. Реагенты, разрушающие водородные и S-S связи, увеличивают чувствительность спор к окислителям.
Пептидоглюкан, который менее сшит и электроотрицателен, составляет кору споры. Согласно другому способу, катионное взаимодействие между дезинфицирующим раствором и пептидоглюканом может вызывать коллапс коры и потерю устойчивости.
Пептидоглюкан спорообразующих бактерий содержит тейхоевые кислоты (т.е полимеры глицерина или рибитола, связанные фосфатными группами). По другому механизму, разрушение полимерных тейхоевых кислот может вызвать дефекты в структуре пептидоглюкана и тем самым сделать споры более чувствительными к атаке.
Кроме того, некоторые поверхностно-активные вещества могут увеличить потенциал смачиваемости оболочки споры до такой степени, что в результате увеличится проникновение окислителей внутри споры.
Имеется разнообразие материалов, которые могут использоваться для обеззараживания большего или меньшего числа ОВ химического или биологического оружия. Исторически, обеззараживающие растворы были строго сосредоточены на уничтожение и нейтрализации химических и биологических ОВ. Мало внимания уделялось восстановлению и повторному использованию аппаратуры и оборудования. Считалось, что эти средства невосстановимы и должны быть заменены в случае применения как ХО так и БО. Таким образом большинство обеззараживающих композиций, используемых в настоящее время, являются высокотоксичными и высококоррозийными. Кроме того, большинство используемых обеззараживающих материалов направлено на химические или биологические ОВ, но не на оба, и часто на ОВ подкласса ХО или БО.
Нейтрализация боевых химических ОВ началась с применения хлорной извести для нейтрализации горчичного газа. В дальнейшем была создана композиция, супертропикальная хлорная известь, смесь 93% гипохлорита кальция и 7% гидроокиси натрия, которая более стабильна при длительном хранении, чем хлорная известь и более легко распыляется. Горчичный газ реагирует с хлорной известью, причем сульфид окисляется в сульфоксид и в сульфон, и в результате дегидрохлорирования образуются соединения, такие как О2S(CHCH2)2. В результате гидролиза G-агенты превращаются в соответствующие фосфониевые кислоты, последние образуют гипохлоритный анион, обладающий каталитической активностью. В кислых растворах VX-агенты быстро окисляются хлорной известью у атома серы и растворяются из-за протонизации атома азота. С другой стороны при высоких значениях рН растворимость VX значительно уменьшается и депротонированный азот окисляется, что приводит к поглощению больших количеств хлорной извести, чем стехиометрические количества.
Неводная жидкость, состоящая из 70% диэтилентриамина, 28% монометилового эфира этиленгликоля и 2% гидроокиси натрия, обозначенная как Обеззараживающая Жидкость №2 (DS2), является высокоэффективным обеззараживающим средством для химических ОВ. Монометиловый эфир этиленгликоля вызывал у мышей тетрагонность, поэтому было предложено заменить указанный эфир монометиловым эфиром пропиленгликоля, в результате чего была получена новая композиция, обозначенная как DS2P. Кроме того, DS2 действует на краски, пластмассы и кожаные материалы. Для решения этой проблемы продолжительность контакта с DS2 обычно сокращают до 30 минут и затем объект ополаскивают большим количеством воды. Требуется, чтобы персонал, работающий с DS2, носил респираторы с защитными стеклами для глаз и химические защитные перчатки. Реакции DS2 с горчичным газом сопровождаются элиминацией НСl. Нервно-паралитические вещества реагируют с образованием DS2 диэстеров, которые далее разлагаются с образованием соответствующей фосфоновой кислоты. DS2 не очень сильное вещество для уничтожения спор. В случае Bacillus subtilis только 1-лог убитых (90%) были обнаружены после 1-часовой обработки (Такер (Tucker), 2000).
Было показано, что смесь, состоящая из 76% воды, 15% тетрахлорэтилена, 8% гипохлорита кальция и 1% смеси анионных поверхностно-активных веществ, способствует растворению ОВ, сохраняя при этом токсичность и коррозийную способность (Форд и Ньютон (Ford и Newton), 1989). Кроме того, указанная смесь нестабильна и разделяется.
Имеются разнообразные композиции, которые в настоящее время применяются для обеззараживания персонала в случае атаки ХО. Эти композиции впервые были применены войсками США и, как правило, в гражданском сообществе они не применяются. Одна композиция, М258 - набор для обеззараживания кожи, является имитацией Советского набора, обнаруженного в Египетских танках в  Кипурской войне (Yom Kippur war). Набор состоит из двух пакетов: пакет I содержит полотенце, предварительно смоченное фенолом, этанолом, гидроокисью натрия, аммиаком и водой. Пакет II содержит полотенце, пропитанное хлорамином-В, и запаянную стеклянную ампулу, наполненную раствором хлорида цинка. Ампулу из пакета II разбивают, и полотенце смачивают раствором непосредственно перед использованием. Содержащийся в растворе хлорид цинка поддерживает значение рН водного раствора хлорамина-В в пределах 5-6, которое иначе подскочило бы до 9,5.
Кипурской войне (Yom Kippur war). Набор состоит из двух пакетов: пакет I содержит полотенце, предварительно смоченное фенолом, этанолом, гидроокисью натрия, аммиаком и водой. Пакет II содержит полотенце, пропитанное хлорамином-В, и запаянную стеклянную ампулу, наполненную раствором хлорида цинка. Ампулу из пакета II разбивают, и полотенце смачивают раствором непосредственно перед использованием. Содержащийся в растворе хлорид цинка поддерживает значение рН водного раствора хлорамина-В в пределах 5-6, которое иначе подскочило бы до 9,5.
Другая композиция - М291 - является твердой системой сорбента (Янг (Yang), 1995). Набор используется для удаления массы жидкого вещества с кожи и состоит из нетканых подушек из волокна, заполненных смесью смолы. Смола изготовлена из сорбирующего материала на основе стирола/дивинилбензола, а карбонизированная макросетчатая смола - из стирола/дивинилбензола. Эта смола, обладая большой поверхностью, имеет катионообменные (сульфокислотные группы) участки и анионообменные (группы гидроокиси тетраалкиламмония) участки. Сорбирующая смола может абсорбировать жидкие агенты, а реагирующие смолы предназначены стимулировать реакции гидролиза. Однако, по данным недавнего исследования ядерного магнитного резонанса (ЯМР), ни VX-агент, ни имитатор горчичного газа не подвергались гидролизу на поверхности ХЕ-555 смолы за первые 10 дней (Лесли и дрю (Leslie et al.), 1991). GD-агент подвергался медленному гидролизу, с периодом полупревращения приблизительно 30 часов. В полевых условиях быстрое обеззараживание агента достигается его удалением с кожи именно таким путем. Оказалось, что эта смоляная смесь менее разъедает кожу, чем система М258.
Большинство композиций, используемые для обеззараживания биологических ОВ как военными, так и гражданскими ведомствами, содержат гипохлоритный анион (т.е. хлорную известь или хлорсодержащие растворы). Было показано, что растворы, содержащие хлорную известь в концентрациях 5% и более, убивают споры (Саприпанти и Бонифацио (Sapripanti and Bonifacio), 1996). Для обеззараживания биологических ОВ был предложен ряд гипохлоритных растворов, включая 2-6%-ный водный раствор гипохлорита натрия (хозяйственная хлорная известь), 7%-ная водная суспензия или твердый гипохлорит кальция (НТН), 7-70%-ная водная суспензия гипохлорита кальция и окиси кальция (супертропическая хлорная известь, STB), твердая смесь гипохлорита кальция и окиси магния, 0,5%-ный водный раствор гипохлорита кальция, буферированный дигидрофосфатом натрия и детергентом и 0,5%-ный водный раствор гипохлорита кальция, буферированный натрием. Хотя все эти растворы способны с различной эффективностью уничтожать споры, каждый из них, однако, является высококоррозийным для оборудования и токсичным для персонала.
Композиции, которые были созданы для детоксификации ОВ химического и биологического оружия, использовались различными путями, включая жидкости. пены, туманы и аэрозоли. Стабильные водные пены применяют в различных вариантах, включая тушение огня и борьбу с правонарушениями (такими, как например, тюремный бунт). Однако такие пены получают с использованием анионных поверхностно-активных веществ и анионных или неионогенных полимеров. К сожалению, такие пены не эффективны для химического разложения и нейтрализации большинства ОВ боевых химических и биологических средств. Они не обладают необходимой химической активностью для разложения или изменения ОВ, они не эффективны для уничтожения или нейтрализации бактерий, вирусов и спор, которые в большей или меньшей степени связаны с биологическими ОВ.
Привлекает внимание возможность использования газообразных реагентов в качестве обеззараживающих средств в случае, если такой газ соответствует экологическим требованиям. Преимущество газообразных обеззараживающих веществ заключается в их способности проникать (диффундировать), что делает их необходимым дополнением к другим методам обеззараживания. Озон, двуокись хлора и параформальдегид - все они были исследованы на предмет обеззараживания. Известно, что эти реагенты эффективны против биологических ОВ. Эффективность озона для уничтожения спор точно установлена (Рабер и дрю (Raber et al.), 1998). Хотя озон является перспективным обеззараживающим средством, эксперименты Эджвудского химико-биологического центра (ЭХБС) (Edgewood Chemical Biological Center (ECBC)) показывают, однако, что он неэффективен в случае GD-агентов, а в случае VX-агентов он приводит к образованию токсичных продуктов путем расщепления Р-О связи (Хованик (Hovanic), 1998).
Необходимы дезактиваторы, экологически безопасные для людей и их собственности, которые эффективно обеззараживают боевые химические и биологические ОВ и проявляют свою активность над всеми поверхностями, потенциально опасными в данный момент, а также такие, которые можно включить в состав разнообразных носителей (таких как пены, гели, туманы, аэрозоли), удовлетворяющих разнообразным эксплуатационным целям.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1 показывает часть релевантных заявленному изобретению химических структур некоторых химических ОВ.
Фиг. 2 показывает, как компоненты пены согласно данному изобретению образуют мицеллы.
Фиг. 3 показывает механизм мицеллярного катализа согласно данному изобретению.
Фиг. 4 показывает степень расширения и стабильность пены, образовавшейся без перекиси водорода, согласно примеру осуществления данного изобретения.
Фиг. 5 показывает степень расширения и стабильность пены, образовавшейся в присутствии перекиси водорода.
Фиг. 6 показывает результаты нейтрализации живых организмов на бумажных пробах.
Фиг. 7 показывает результаты проб, проведенных G имитирующим агентом (дифенилхлорфосфатом).
Фиг. 8 показывает результаты для G имитирующего агента на разных поверхностях.
Фиг. 9 показывает результаты применения пены при различных температурах.
Фиг. 10 показывает нейтрализацию В. globigii в жидких пробах.
Фиг. 11 показывает нейтрализацию В. globigii в поверхностных пробах.
Фиг. 12 показывает нейтрализацию Е. herbicola в растительных клетках, в жидких пробах.
Фиг. 13 показывает нейтрализацию бактериофага MS-2 в жидких пробах.
Фиг. 14 показывает нейтрализацию спор В. anthracis в жидких пробах.
Фиг. 15 показывает нейтрализацию спор В. anthracis в поверхностных пробах.
Фиг. 16 показывает нейтрализацию суррогата сибирской язвы, В. globigii.
Фиг. 17 представляет собой график, показывающий результаты нейтрализации, полученные при действии пены по данному изобретению на дифенилхлорфосфат (имитатор химического ОВ).
Фиг. 18 представляет собой график, показывающий результаты нейтрализации, полученные при действии пены по данному изобретению на малатион (имитатор химического ОВ).
Фиг. 19 представляет собой график, показывающий результаты нейтрализации, полученные при действии пены, полученной согласно данному изобретению на полугорчичный газ (имитатор горчичного газа).
Фиг. 20 представляет собой график, показывающий результаты нейтрализации спор В. globigii при помощи пены, полученной согласно данному изобретению.
Фиг. 21 представляет собой график, показывающий результаты воздействия пены, полученной согласно данному изобретению, на Е. herbicola.
ДЕТАЛЬНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Цель данного изобретения - создание единой композиции, которая нейтрализует неблагоприятные эффекты химических и биологических ядов, где ядом является любое химическое или биологическое вещество, компонент, вид или агент, который, оставаясь необработанным, путем химического или биологического воздействия на жизненные процессы может вызвать смерть, временную нетрудоспособность или оказывать постоянное вредное воздействие на людей и животных. Такие яды включают все химические и биологические ОВ, независимо от их происхождения или метода получения и независимо от того, где они произведены, содержатся ли они в боеприпасах или в другом месте. Нейтрализация определяется как миграция, детоксификация, обезвреживание или другие виды разрушения ядов в такой мере, что яды становятся неспособными оказывать острые неблагоприятные влияния на людей и животных.
Сущность настоящего изобретения заключается в том, что композиция для нейтрализации по меньшей мере одного ОВ содержит
по меньшей мере два солюбилизирующих компонента, где один из солюбилизирующих компонентов является катионным поверхностно-активным веществом, указанное катионное поверхностно-активное вещество является четвертичной аммониевой солью;
по меньшей мере, один из солюбилизирующх компонентов является катионным гидротропным веществом; один реагирующий компонент отобран из нуклеофильных и окисляющих соединений, и воду для образования водной композиции;
четвертичная аммониевая соль имеет концентрацию в пределах приблизительно 0,1-10 вес.% от водной композиции;
по меньшей мере два указанных солюбилизирующих компонента и по меньшей мере один реагирующий компонент, при смешивании с водой и нанесении по меньшей мере на одну зараженную ОВ поверхность, нейтрализуют указанное по меньшей мере одно ОВ.
По меньшей мере одно ОВ является биологическим или химическим ОВ. Указанные химические ОВ отобраны из группы: о-алкил-фосфонофторидаты, о-алкил-фосфорамидоцианидаты, о-алкил,s-2-диалкил-аминоэтил-алкилфосфонотиолаты и соответствующие алкилированные и протонизированные соли, 2-хлорэтилхлорметилсульфид, бис(2-хлорэтил)сульфид, бис(2-хлорэтилтио)метан, 1,2-бис(2-хлорэтилтио)этан, 1,3-бис(2-хлорэтилтио)-н-пропан, 1,4-бис(2-хлорэтилтио)-н-бутан, 1,5-бис(2-хлорэтилтио)-н-пентан, бис(2-хлорэтилтиометил)эфир, бис(2-хлорэтилтиоэтил)эфир. Люизиты, сакситоксин, рицин, алкил-фосфонилдифторид, алкил-фосфониты, хлорзарин, хлорзоман, амитон, 1,1,3,3,3-пентафтор-2-(трифторметил)-1 пропен, 3-квинуклидинил-бензалат, метилфосфонил-дихлорид, диметил-метилфосфонат, дигалогениды диалкил-фосфорамидов, диалкил-фосфорамидаты, мышьяка трихлорид, дифенил-гидроксиуксусная кислота, квинуклидинил-3-ол, диалкил-аминоэтил-2-хлориды, диалкил-аминоэтан-2-олы, диалкил-аминоэтан-2-тиолы, тиодигликоли, пинаколиловые спирты, фосген, хлорциан, синильная кислота, хлорпикрин, фосфора оксихлорид, треххлористый фосфор, пятихлористый фосфор, алкилфосфиты, однохлористая сера, двухлористая сера, и тионилхлорид; предпочтительно, где указанные биологические ОВ отобраны из бактериальных спор, вегетирующих бактериальных клеток и вирусов.
Композиция дополнительно содержит растворимый в воде полимер с концентрацией в пределах между 0 и 10% от водной композиции, предпочтительно, что растворимый в воде полимер отобран из поливинилового спирта, гуаровой смолы, катионного хлорида полидиаллил-диметил-аммония, неионогенного хлорида полидиаллил-диметил-аммония и полиакриламида, и предпочтительно далее включает ингибитор коррозии и, более предпочтительно, чтобы ингибитор коррозии был отобран из диметил-этаноламина, триэтаноламина, смесей этаноламинных солей С9, С 10 и С 12 двухосновных кислот, нитрита дициклогексиламина и N,N-дибензиламина.
Композиция дополнительно содержит жирный спирт с 10-16 углеродными атомами в молекуле с концентрацией в пределах между 0 и 1% от водной композиции и предпочтительно, чтобы в композицию дополнительно был включен катализатор, который может быть отобран из йодозобензоата и медно-аминных комплексов.
Реагирующий компонент композиции может быть отобран из перекиси водорода, мочевины-перекиси водорода, гидропероксикарбоната, оксиматов, алкоксидов, арилоксидов, альдегидов, пероксимоносульфата, реактива Фентона, и гипохлорита натрия, и в качестве среды-носителя для указанной композиции включает воду для получения водной композиции, способной нейтрализовать химические и биологические агенты.
Композиция представляет собой комплект компонентов, может являться бинарным комплектом, включающим предварительно перемешанные компоненты, по меньшей мере, два солюбилизирующих вещества, водорастворимый полимер и жирный спирт и компонент, состоящий из реагирующего соединения, которое путем перемешивания с водой можно использовать для нейтрализации, по меньшей мере, одного ОВ и более предпочтительно.
Комплект может является тернарным комплектом, включающим первый предварительно перемешанный компонент, водную смесь четвертичной соли аммония и катионного гидротропного вещества, второй компонент может являться перекисью водорода и третий компонент - солью бикарбоната.
рН композиции находится в пределах между 8 и 11, для использования ее для дезактивации предпочтительно, чтобы рН композиции была равна 9.
Композиции используют в виде пены, тумана, геля, аэрозоля, жидкости в качестве дезинфицирующего средства. Пена имеет степень расширения в пределах между 20 и 125, в которой после обработки композицией больше чем 99,99% спор В. globigii погибают в течение одного часа. Больше чем 99,9999% спор В. globigii погибают в течение приблизительно одного часа после обработки композицией, где катионное гидротропное вещество отобрано из бромида тетрапентиламмония, бромида триацетилметиламмония и бромида тетрабутиламмония, с концентрацией в пределах между 0,1 и 10% от водной композиции.
Композиция, где катионным поверхностно-активным веществом является четвертичная соль аммония, с концентрацией в пределах между 0,1 и 10 вес.% от водной композиции. Четвертичную соль аммония отбирают из бромида цетилтриметиламмония, хлорида бензалкония, хлорида бензетония, хлорида цетилпиридиния, бромида тетрабутиламмония и полимерных четвертичных соединений.
Композиция для нейтрализации химических токсичных веществ включает, по меньшей мере, два солюбилизирующих компонента, где один из солюбилизирующих компонентов является четвертичной солью аммония и один из солюбилизирующх компонентов является катионным гидротропным веществом, и водорастворимый полимер; а один реагирующих компонентов отобран из нуклеофильных и окисляющих соединений и воды в жидкой фазе, где указанные по меньшей мере два солюбилизирующих компонента и один реагирующий компонент при смешивании с указанной водой в жидкой фазе образуют композицию, которая нейтрализует химические токсичные вещества.
Композиция в виде пены для нейтрализации химических токсичных веществ, где катионным поверхностно-активным веществом является четвертичная соль аммония, которая имеет концентрацию между приблизительно 0,1 и приблизительно 10 вес.% от водной композиции. Катионное гидротропное вещество отобрано из бромида тетрапентиламмония, бромида триацетилметиламмония и бромида тетрабутиламмония, с концентрацией в пределах между 0,1 и 10 вес.% от водной композиции, и водорастворимый полимер отобран из поливинилового спирта, гуаровой смолы, катионного хлорида полидиаллилдиметиламмония, неионогенного хлорида полидиаллилдиметил-аммония, и полиакриламида.
Композиция для нейтрализации биологических токсичных агентов включает один солюбилизирующий компонент, отобранный из четвертичной соли аммония, катионного гидротропного вещества или жирного спирта, и один реагирующий компонент. Реагирующий компонент является окислителем, отобранным из перекиси водорода, мочевины - перекиси водорода и гидропероксикарбоната, и предпочтительно спирт, имеющий 2-6 углеродных атомов. После обработки указанной композицией больше чем 99,99% спор В. globigii погибают в течение приблизительно одного часа.
Способ получения водной пенообразующей композиции для нейтрализации, по меньшей мере, одного токсичного агента, включает следующие стадии:- солюбилизацию катионного гидротропного вещества, по меньшей мере, одного спиртового соединения с короткой цепью и водорастворимого полимера в воде; - добавление четвертичной соли аммония; - последующее добавление, по меньшей мере, одного жирного спирта; - добавление реагирующего компонента, указанный реагирующий компонент отобран из перекиси водорода, мочевины - перекиси водорода, гидропероксикарбоната, оксиматов, алкоксидов, арилоксидов, альдегидов, пероксимоносульфата, реактива Фентона, и гипохлорита натрия;
Предпочтительно, чтобы концентрация катионного гидротропного вещества находилась в пределах между 0,1 и 10 вес.%, концентрация четвертичной соли аммония - между 0,1 и 10 вес.%, концентрация одного спиртового соединения с короткой цепью - между 0 и 4 вес.%, концентрация водорастворимого полимера - между 0 и 10 вес.%, концентрация одного жирного спирта - между 0 и 1 вес.% и концентрация реагирующего компонента - между 0,1 и 10 вес.%.
Композиции и описанные варианты данного изобретения могут нейтрализовать инфекцию, однако сами они не вызывают значительного отрицательного воздействия на здоровье людей и животных. Данное изобретение направлено на важное подмножество химических и биологических соединений. которое охватывает боевые химические и биологические средства массовою уничтожения. Однако настоящее изобретение направлено также и на ядовитые вещества, которые потенциально способны оказать вредное влияние на здоровье животных и людей. Такие вредные воздействия включают инфекции, острые и хронические заболевания и фатальные исходы. Кроме того, данное изобретение направлено на удовлетворение в потребности такой композиции, которая сама не является токсичной и коррозийной и которая может быть использована разнообразными средствами и в различных видах.
В основном наиболее опасными химическими и биологическими соединениями, в случае которых будет необходимо применение настоящего изобретения, являются химические и биологические ОВ. Оказалось что композиция, описанная в данном изобретении, успешно нейтрализует или детоксицирует химические и/или биологические ОВ и может быть применена в случае менее опасных химических и биологических ОВ. Некоторые из известных химических ОВ, которые могут быть применены террористами, химически аналогичны в том смысле, что являются соединениями, содержащими фосфор и могут видоизменяться в результате нуклеофильной атаки или окислительного процесса. Эти вещества включают зарин (О-изопропил-метилфосфонофторидат), зоман (О-пинаколил-метилфосфонофторидат), табун (О-этил-N,N-диметилфосфорамидоцианидат) и VX (О-этил-S-2-диизопропиламиноэтил-метилфосфонотиолат). Химические структуры этих соединений показаны на фиг.1. В случае если применяемое химическое ОВ содержит фосфор и химически изменяется в результате гидролиза или окисления, то оно детоксицируется и при этом нейтрализуется как ОВ. Эти нервно-паралитические ОВ мало растворимы в воде.
На фиг.1 показана также химическая структура горчичного газа, (бис(2-хлорэтил)сульфид). Горчичный газ химически значительно отличается от указанных выше других химических ОВ тем, что у него нет группы, содержащей фосфор. Однако он содержит атомы хлора, связанные с углеродными атомами в обеих концах молекулы. Эти связи между атомами углерода и хлора также могут подвергаться гидролизу, а центральный атом серы может окисляться до сульфона и сульфоксида, делая таким образом химическое ОВ нетоксичным. Аналогично нервно-паралитическим ОВ горчичный газ тоже мало растворим в воде.
Механизм, по которому композиция данного изобретения уничтожает или нейтрализует биологические ОВ, окончательно еще не выяснен. В случае вегетативных бактериальных клеток и вирусов механизмом уничтожения, по-видимому, является окислительное влияние окисляющих реагентов, таких как перекись водорода (Рассел (Russell), 1990). Обычно перекись водорода в концентрациях 10-20% используется для уничтожения спор (Russell, 1990). Известно, что низкие концентраций перекиси водорода (4% и ниже), не способны эффективно уничтожать бактериальные споры. Для обеззараживания спорового агента необходимо, чтобы ДНК споры была доступна для окислителя. ДНК споры защищена оболочкой и для эффективного уничтожения спорового агента она должна быть разрушена.
В настоящем изобретении композиция содержит, по меньшей мере, один растворяющий компонент, который делает химические и биологические токсичные вещества, в особенности химические и биологические ОВ, более восприимчивыми к воздействию антидотов, и, по меньшей мере, один реагирующий компонент, который воздействует на токсичные вещества и нейтрализует их. По меньшей мере, один реагирующий компонент может быть окисляющим соединением, нуклеофильным соединением или их смесью; соединение может быть и окисляющим и нуклеофильным. В случае химических ОВ и аналогичных по структуре химических соединений растворяющий компонент служит для растворения малорастворимых химических ОВ и активизации нуклеофильного/окисляющего соединения, находящегося в непосредственной близости к химическому ОВ. Это достигается вследствие того, что нуклеофильные соединения заряжены отрицательно, а растворяющий компонент может быть катионным поверхностно-активным веществом, которое образует положительно заряженные мицеллы, тем самым возбуждая нуклеофильные реагенты, такие как гидроксильные ионы, гидроперекисные ионы, или гидроперкарбонатные ионы. В случае биологических ОВ растворяющий компонент служит для солюбилизации и размягчения внешней оболочки биологического агента, что делает ДНК биологического ОВ более доступным для реагирующего компонента и тем самым стимулирует способность композиции убивать или нейтрализовывать.
Несмотря на то, что композиция, описанная в данном изобретении, имеет определенное сходство с коммерчески доступными детергентами и шампунями, содержащими катионные поверхностно-активные вещества для образования мицеллярных растворов (смотрите, например, Юнейа (Juneja), США патент №4,824,602); эти растворы не содержат реагирующее соединение, которое согласно данному изобретению могло бы нейтрализовать токсичные соединения. Кроме того, композиции, предложенные Юнейа (Juneja), не содержат катионные поверхностно-активные и катионные гидротропные вещества; композиций Юнейа (Juneja) содержат анионные гидротропные вещества.
Фиг.2 показывает пример катионной мицеллы, которая образована при применении композиции данного изобретения. В водной среде 25 гидролизуемое или окисляемое химическое токсичное вещество (например, химическое ОВ) 5, локализован внутри мицеллы 10, содержащей совокупность поверхностно-активных молекул с гидрофобными хвостами 15, которые образуют внутреннее ядро мицеллы, и с гидрофильными головами 20, сконцентрированными на поверхности мицеллы. Как указано выше, эти положительно заряженные головы притягивают нуклеофильные соединения, в результате чего скорость реакции возрастает. Фиг.2 показывает также, что отрицательно заряженные гидроксильные ионы 30 прикреплены к мицелле. Это отличается от ситуации, которая наблюдается в водных композициях, содержащих анионные поверхностно-активные вещества, где мицеллы заряжены отрицательно и отталкивают гидроксильные ионы.
Фиг.3 показывает механизм, катализируемой нуклеофильным агентом типичной реакции, согласующейся с принципами данного изобретения. Эта фигура показывает часть токсичного вещества 35, которая подвергается нуклеофильной атаке. В этом примере, атакуемой ординарной ковалентной связью, является связь 40 между атомами фосфора и фтора. Из-за природы двойной связи между атомами фосфора и кислорода согласно хорошо известного химикам феномена парциальных зарядов показанный на чертеже атом фосфора является носителем положительного парциального заряда и поэтому притягивает нуклеофильные группы, такие как гидроксильная группа. Происходит реакция, где при наличии в качестве нуклеофильного агента гидроксильной группы в молекуле токсичного вещества фтор замещается гидроксильной группой и выделяется фтористоводородная кислота
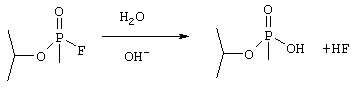
Следует отметить, что этот механизм нуклеофильной атаки обеззараживания таких токсичных веществ как химические ОВ может функционировать в присутствии любого сильного нуклеофильного реагента. Указанные здесь гидроксильные ионы являются примером нуклеофильных групп, которые в данном изобретении способны выполнять эту функцию. Кроме того, этот механизм обеззараживания и нейтрализации может функционировать в основном в случаях, где токсичное вещество является носителем химической группы, содержащей фосфор, и уязвимо при нуклеофильной атаке. Например, аналогичная реакция происходит в примерах, где циановая группа (как в случае табуна) связана с фосфором вместо упомянутого выше фтора. Подобно этому (как и в VX-агентах), вследствие аналогичной нуклеофильной атаки и реакции гидролиза может быть удалена и более большая химическая группа, в результате чего вещество теряет токсичность. В конкретном случае VX-агента гидроксильнный ион не является предпочтительным нуклеофильным агентом, так как он не специфичен при расщеплении P-S связи; он расщепляет также и Р-О связь. Это нежелательно, так как продукт такой реакции тоже обладает высокой токсичностью. Поэтому для детоксификации VX агента лучше использовать другие нуклеофильные реагенты. Примером нуклеофильного реагента, специфически расщепляющего P-S связь, является гидроперекисный анион.
Гидролиз происходит также и в случае горчичного газа, хотя механизм нуклеофильной атаки не совпадает в точности с механизмом, описанным в случае токсичных веществ, содержащих фосфор. Примером реакции, соответствующей этому механизму, является
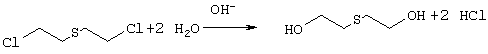
Гидролиз - это только один из механизмов, путем которого такие токсичные вещества, как химические ОВ, могут быть обеззаражены. Как показывает следующий пример, окисление приводит к обеззараживанию химических ОВ и других химических соединений в соответствие с принципами данного изобретения

В одном из способов осуществления композиция данного изобретения нейтрализует токсичные вещества, такие как химические и биологические OВ, и содержит солюбилизирующие соединения, которые включают как катионное поверхностно-активное вещество, так и катионное гидротропное вещество, а также, по меньшей мере, одно реагирующее соединение, где реагирующим соединением может быть или нуклеофильное вещество, или окисляющее вещество (окислитель), или их смесь. Несмотря на то, что применение композиции согласно данному изобретению сосредоточено на химических и биологических OВ, эта композиция может применяться и для обеззараживания других токсичных веществ, как химических, так и биологических, которые могут подвергаться гидролизу или окислению композицией, описанной в данном изобретении. Композиция добавляется к носителю, такому как вода в жидкой фазе, для взаимодействия с гидролизуемыми или окисляемыми токсичными веществами. Для нейтрализации малорастворимого токсичного соединения оно солюбилизируется катионным поверхностно-активным веществом и к нему прибавляется катионное гидротропное вещество - аналог поверхностно-активного ионного материала с короткими углеводородными сегментами с целью увеличения растворимости токсичного вещества в водной среде и соответствующего повышения скорости реакции между реагирующим компонентом и токсичным веществом. В производстве детергентов с целью солюбилизации поверхностно-активных веществ и почвы обычно применяются анионные гидротропные соединения, такие как поверхностно-активные композиций натрий-ксилола; однако в контексте данного изобретения для достижения совместимости с катионными поверхностно-активными веществами используются катионные гидротропные вещества. Чтобы еще повысить растворимость и объемную вязкость, можно по выбору добавить растворимый в воде полимер. Катионный гидротропный реагент значительно повышает скорость гидролиза токсичного вещества. Используемый для нейтрализации биологического OВ солюбилизирующий агент может быть катионным поверхностно-активным веществом, спиртом, таким как спирт жирного ряда, или катионным гидротропным веществом. Известно, что поверхностно-активные вещества денатурируют протеины, такие как биологические токсичные агенты, и действуют как бактерициды и альгициды. В числе таких поверхностно-активных веществ находятся четвертичные аммонийные соединения, такие как хлорид бензалкония, хлорид цетилпиридиния и бромид цетилтриметиламмония. Катионные поверхностно-активные вещества, жирные спирты и катионные гидротропные вещества предназначены для того, чтобы сделать ДНК биологических OВ доступным для реагирующего соединения. Поэтому смесь катионного поверхностно-активного вещества и катионного гидротропного соединения состоит из нужного комплекта солюбилизирующих агентов, которые делают токсичные соединения, особенно химические и биологические OВ, доступными для реагирующего соединения. После того как солюбилизирующее соединение сделает доступным токсичный агент для реагирующего соединения, последнее реагирует с токсичным агентом путем окисления или путем реакции гидролиза, что приводит к нейтрализации токсичного агента. В зависимости от концентраций различных компонентов, которые используются в композиции данного изобретения, приблизительно за час нейтрализуется более чем 99,999%, и часто 99,99999% биологического OВ.
Исходя из цели данного изобретения, катионными поверхностно-активными веществами обычно являются четвертичные аммонийные соли, такие как бромид цетилтриметиламмония, бензалконий и хлорид бензалкония, и полимерные четвертичные соединения. Примеры соответствующих гидротропных компонентов включают бромид тетрапентиламмония, бромид триацетилметиламмония, бромид тетрабутиламмония и др. Примеры соответствующих растворимых в воде полимеров включают поливиниловый спирт, гуаровую смолу, (катионный и неионогенный) хлорид полидиаллилдиметиламмония, полиакриламиды и др.
Жирные спирты могут содержать 10-16 углеродных атомов. (Обычно термин "жирный спирт" подразумевает первичный спирт с прямой цепью, содержащий 8-20 углеродных атомов). Совместная функция полимера и жирного спирта - это повышение объемной и поверхностной вязкости ламелл пены и увеличение стабильности пены относительно дренажа и разрушения пузырьков. Другие вещества, которые могут быть добавлены к композиции, включают спирты с короткой цепью (в концентрации примерно 0-4 вес.%), которые используются с целью солюбилизации, и эфир гликоля, который также используется для солюбилизации жирных спиртов.
Реагирующим компонентом, который следует добавить, может быть окисляющее вещество (окислитель), такой как перекись, например перекись водорода, комплекс мочевины с перекисью водорода и перкарбонаты, которые добавляются с целью нейтрализации химических и биологических ОВ, включая споры и бактерии. Добавление бикарбоната, например бикарбоната калия или бикарбоната натрия, когда окислителем является перекисное соединение, например перекись водорода, приводит к образованию гидроперекиси карбоната, который особенно энергично реагирует с биологическими токсичными агентами и нейтрализует их.
Другие вещества, которые могут быть применены вместо карбонатного соединения, включают борат, молибдат, сульфат и вольфрамат. В одном осуществлении данного изобретения перекись водорода является основным реагирующим реагентом и к композиции добавляется бикарбонатное соединение. Недавние исследования показали, что перекись водорода можно активировать бикарбонатом с образованием гидроперекисных карбонатных групп (НСO
При нейтрализации биологических OВ оказалось, что эффект синергизма между катионными поверхностно-активными веществами и перекисью водорода/бикарбоната (т.е. гидроперекисными карбонатными группами) обуславливает высокую спороуничтожающую активность, которая проявляется при воздействии композиции на споры. Возможный механизм уничтожения спор заключается в том, что катионное поверхностно-активное вещество размягчает и разрушает оболочку споры, образуя в ней бреши, через которые перекись водорода может проникнуть внутрь и воздействовать на споры ДНК. Этот синергистический эффект был подтвержден экспериментальными результатами. Другие окисляющие соединения, которые могут использоваться для нейтрализации спор, включают альдегиды, такие как глутаровый альдегид (в концентрациях 1-4%), пероксимоносульфат (1-4%), реактив Фентона (смесь железа и перекиси), и гипохлорит натрия.
Следующая таблица представляет список компонентов композиции одного способа осуществления данного изобретения. Приведены пределы концентраций, эффективно нейтрализующие химические и биологические OВ, где в качестве носителя использована вода.

Химические OВ, которые должны подвергаться воздействию композиции, описанной в данном изобретении, включают о-алкил-фосфонофторидаты, такие как зарин и зоман, о-алкил-фосфорамидоцианидаты, такие как табун, о-алкил-, S-2-диалкил-аминоэтил-алкилфосфонотиолаты и соответствующие алкилированные или протонизированные соли, такие как VX, соединения типа горчичного газа, в том числе 2-хлорэтилхлорметилсульфид, бис(2-хлорэтил)сульфид, бис(2-хлорэтилтио)метан, 1,2-бис(2-хлорэтилтио)этан, 1,3-бис(2-хлорэтилтио)-н-пропан, 1,4-бис(2-хлорэтилтио)-н-бутан, 1,5-бис(2-хлорэтилтио)-н-пентан, бис(2-хлорэтилтиометил)эфир и бис(2-хлорэтилтиоэтил)эфир. Люизиты, в том числе 2-хлорвинилдихлорарсин, бис-(2-хлорвинил)хлорарсин, трис(2-хлорвинил)арсин, бис(2-хлорэтил)этиламин и бис(2-хлорэтил)метиламин, сакситоксин, рицин, алкил-фосфонилдифторид, алкил-фосфониты, хлорзарин, хлорзоман, амитон, 1,1,3,3,3-пентафтор-2-(трифторметил)-1-пропен, 3-квинуклидинил-бензилат, метилфосфонил-дихлорид, диметил-метилфосфонат, диалкил-фосфорамидовые дигалиды, диалкил-фосфорамидаты, треххлористый мышьяк, дифенилгидроксиуксусная кислота, квинуклидин-3-ол, диалкил-аминоэтил-2-хлориды, диалкил-аминоэтан-2-олы, диалкил-аминоэтан-2-тиолы, тиодигликоли, пинаколиловые спирты, фосген, хлорциан, синильная кислота, хлорпикрин, оксихлорид фосфора, треххлористый фосфор, пятихлористый фосфор, алкилфосфиты, однохлористая сера, двухлористая сера и тионил-хлорид и др. Эти и другие химические соединения могут быть нейтрализованы (напр., детоксицированы) нуклеофильными и окислительными композициями, описанными в данном изобретении.
Кроме того, в состав композиций данного изобретения с целью увеличения скорости реакции были успешно включены катализаторы. Например, были использованы йодозобензоат и медно-аминные комплексы, и оказалось, что они увеличивают скорости реакций. Для стимулирования других реакций (например, окислительных реакций) с OВ в композицию можно вводить и другие вещества. Следует ожидать, что такие добавки позволят специалистам адаптироваться к существующим требованиям без проведения ненужных экспериментов и придерживаясь принципов и цели данной заявки и прилагаемой формулы изобретения.
Одним из преимуществ данного изобретения является то, что реагирующее соединение и носитель (обычно вода) могут храниться отдельно от других компонентов композиции до его применения. Отделение реагирующего соединения от других компонентов композиции необходимо с целью повышения стабильности хранения. Так как обычно вода доступна на местности, требующей дезактивации, то не следует предварительно смешивать с водой другие составляющие компоненты композиции, их лучше транспортировать к указанной местности отдельно, и здесь, на месте, и в нужное время смешивать с водой. Это способствует уменьшению транспортных расходов. Поэтому композицию данного изобретения лучше использовать в виде пакета.
В другом осуществлении предложена композиция, которая главным образом применяется для нейтрализации химических токсичных агентов, таких как химические OВ. Указанная композиция содержит солюбилизирующие вещества, включая как катионные поверхностно-активные, так и катионные гидротропные соединения, и, по меньшей мере, один реагирующий компонент, где реагирующим компонентом может быть нуклеофильное соединение, окисляющее соединение (окислитель) или их смесь. По желанию можно добавить также и водорастворимый полимер. Эта композиция добавляется к такому носителю, как вода в жидкой фазе для нанесения на химическое токсичное соединение. После того, как солюбилизирующее соединение увеличит доступность токсичного агента для реагирующего компонента, последний, в основном мягкий окислитель, например перекисное соединение, реагирует с токсичным агентом путем окисления или путем реакции гидролиза, что приводит к нейтрализации токсичного агента.
В следующем осуществлении предложена композиция, которая главным образом применяется для нейтрализации биологических OВ. Указанная композиция содержит солюбилизирующее вещество, отобранное из катионного поверхностно-активного вещества, катионного гидротропного соединения и жирного спирта и, по меньшей мере, одного реагирующего компонента, где реагирующим компонентом может быть нуклеофильное соединение, окисляющее соединение (окислитель) или их смесь. Эта композиция добавляется к такому носителю как вода в жидкой фазе для обработки пораженного биологическим OВ участка. После того как солюбилизирующее соединение увеличит доступность биологического OВ для реагирующего компонента, последний реагирует с ним путем окисления или путем реакции гидролиза, что приводит к нейтрализации ОВ. В основном в качестве реагирующего компонента выступает гипероксикарбонатное соединение, которое образовано при взаимодействии гидропероксидного соединения с бикарбонатным соединением, например, с бикарбонатом калия или бикарбонатом натрия.
В одном из способов осуществления композиция данного изобретения состоит из следующих компонентов.

Кроме того, по желанию, можно добавить также и растворимый полимер в пределах концентраций 0-10 вес.%. Эта композиция особенно эффективна для нейтрализации биологических токсичных агентов. Композицию можно легко наносить или диспергировать в виде пены.
Обычно катионные поверхностно-активные вещества являются четвертичными солями аммония, такими как цетилметиламмоний-бромид. Жирные спирты могут содержать 10-16 углеродных атомов. Примерами соответствующих гидротропных веществ могут служить тетрафениламмоний-бромид, триацетилметиламмоний-бромид и тетрабутиламмоний-бромид. Комбинация бикарбоната и перекиси водорода образует окислитель (гидропероксикарбонатные группы, обладающие высокой реакционной способностью), который является фактическим уничтожителем спор.
Эта композиция не токсична для людей и животных, в основном не является коррозийной и может быть использована для нейтрализации как химических, так и биологических OВ. Композиция позволяет обеззараживать населенные территории и места с чувствительным оборудованием. Композиция особенно эффективна для нейтрализации биологических OВ, таких как anthrax. При 1-часовой обработке спор Bacillus anthracis (т.е. спор anthrax) раствором нетоксичной и некоррозийной композиции (которая описана ниже), смертность спор составила 7-лог. (99,99999%).
Для достижения нужной степени детоксификации (обеззараживания) композицию, описанную в данном изобретении, можно наносить на зараженные участки различными путями и в разном виде. Эффективной формой для нанесения композиции является пена. В качестве составной части данного изобретения была разработана нетоксичная, некоррозийная водяная пена, обладающая повышенной физической стабильностью для быстрой нейтрализации токсичных агентов, особенно химических и биологических OВ. Пенообразующая композиция основана на поверхностно-активной системе, с гидротропными компонентами для солюбилизации малорастворимых токсичных агентов и для увеличения скорости реакции с нуклеофильными реагентами. Композиция включает также мягкие окисляющие соединения для нейтрализации биологических OВ, а также жирные спирты и водорастворимые полимеры для увеличения физической стабильности пены.
Данная технология нейтрализации по некоторым соображениям привлекательна как для гражданского, так для военного применения, в том числе 1) можно использовать один нейтрализующий раствор как для химических, так и для биологических OВ, 2) композиция наносится быстро, 3) композицию можно использовать в виде порошка, аэрозоля или пара, 4) вред причиненный здоровью и сопутствующие отрицательные факторы минимальны, 5) требует минимального материально-технического обеспечения, 6) потребляет минимальное количество жидкости и не оказывает никакого длительного экологического воздействия и 7) композиция относительно дешевая. Эта пенообразующая композиция данного изобретения может быть нанесена различными методами. Один из эффективных методов основан на аспирации или эффекте Вентури, что устраняет потребность нагнетать дополнительный воздух в закрытое зараженное пространство. Оказалось, что пены, полученные этим методом, имеют максимальную степень расширения приблизительно 60-100:1 и в зависимости от природных условий (температуры, ветра, относительной влажности) стабильны приблизительно в течение 1-4 часов. Пена может быть образована также системами сжатый воздух - пенообразующая композиция, где воздух непосредственно впрыскивают в жидкую пену. Образованная этим методом пена обычно имеет степень расширения приблизительно 20-60:1 и стабильна в течение 1-4 часов.
Пену можно наносить различными приспособлениями в зависимости от ее объема. Для этого успешно используются похожие на огнетушитель ручные аппараты, а также крупномасштабные пенообразующие аппараты. Было показано, что с использованием этих аппаратов можно успешно обеззараживать химические и биологические OВ и их аналоги. При химических OВ испытания на живых существах были проведены с GD-агентом (зоман), VX-агентом, и HD-агентом (горчичный газ). Время полураспада для обеззараживания этих агентов в системе пены составляет 2-20 минут. В случае биологических OВ смертность спор сибирской язвы порядка 7-лог. (99,99999%) была достигнута при 1-часовой экспозиции в пене. В другом исследовании по биологическим OВ была продемонстрирована быстрая смерть в случае имитаторов чумы (вегетативных бактериальных клеток) и вируса оспы.
В композициях данного изобретения использованы принципы катионного мицеллярного катализа и солюбилизирующая способность катионных гидротропных веществ для растворения малорастворимых другим путем токсичных агентов. Композиции, описанные в данном изобретении, могут быть применены в виде пены с помощью известной специалистам пенопроизводящей технологии. Для целей данного изобретения особенно подходит пенообразующий аппарат, в котором использованы принципы Вентури, где через пенообразующее сопло воздух нагнетается предпочтительно из зараженной окружающей среды, а не из другого источника. Этим обуславливается непосредственный контакт между зараженным воздухом и составляющими ингредиентами пены. Таким образом значительно возрастает эффективность нейтрализации OВ.
Используя пенообразующие композиции данного изобретения в комбинации с механическими пенообразующими аппаратами, хорошо известными специалистам, можно добиться желаемого быстрого получения большого количества аэрозоля и пара для нейтрализации боевых OВ. Если применяется пенопроизводящее оборудование, которое использует при нагнетании окружающий зараженный воздух, то содержащиеся в воздухе токсичные вещества физически непосредственно соприкасаются со слоями пены. Таким путем усиливаются нейтрализующие способности композиции, описанной в данном изобретении.
Пена является нейтрализующей композицией, которая может использоваться для двух общих целей: (1) в случае химического или биологического нападения обеспечивать поражаемого способностью к быстрым ответным мерам и готовностью иметь дело с потенциальными последствиями применения OВ; и (2) полностью восстановить оборудование после нападения.
Для поражаемого объекта исключительно важно обеззараживание зданий и оборудования на соответствующем уровне и за очень короткое время таким образом, чтобы причины заражения были локализованы и устранены. В процессе восстановления время имеет меньшее значение, чем сопутствующие разрушения, общественное мнение и последующее восстановление (т.е. полное обеззараживание), которые являются болеее важными. Необходима обычная композиция, эффективная против всех химических и биологических OВ, которая пригодна для применения в случае различных строительных материалов, обычно используемых в гражданских объектах. Композиция должна применяться в больших количествах, оставаясь при этом сравнительно безвредной для людей и их собственности. Кроме того, она должна обезвреживать химические и биологические OВ в разумном отрезке времени, чтобы достичь сравнительно быстрого восстановления объектов.
Композиция данного изобретения соответствует этим целям. Пенообразующая композиция данного изобретения эффективна для нейтрализации химических и биологических OВ. Она экологически безвредна для людей и их собственности, эффективна на поверхностях практически всех материалов и может быть включена в состав разнообразных носителей (пены, геля, тумана, аэрозоля), что в совокупности удовлетворяет широкое разнообразие эксплуатационных целей.
Кроме того, композиции данного изобретения оказались способными нейтрализовать большую часть токсичных веществ в виде аэрозоля и пара и могут применяться в разнообразных вариантах для обеззараживания оборудования, открытых областей, средств обслуживания и зданий. Композиция настоящего исследования может быть применена также при дезинфекции животных и неодушевленных объектов.
Пенообразующая композиция данного изобретения базируется на катионной поверхностно-активной системе с катионными гидротропными веществами для усиления солюбилизации химических агентов и реагирующей способности с нуклеофильными реагентами. К пене добавляется также низкая концентрация мягкого окисляющего агента (перекисное соединение, например перекись водорода). Перекись водорода реагирует с бикарбонатом в пене с образованием гидропероксикарбонатных групп, обладающих высокой реакционной способностью. Кроме указанных ингредиентов композиция также содержит водорастворимый катионный полимер для увеличения объемной вязкости раствора и жирные спирты для увеличения поверхностной вязкости композиции.
Необходимо смешать компоненты пены согласно определенной процедуре, чтобы растворить ключевые ингредиенты, такие как полимер и жирные спирты. Воду и катионный гидротропный компонент смешивают в контейнере. Далее к этой смеси прибавляют спиртовый компонент или смесь спиртовых соединений. Водорастворимый полимер прибавляют медленно, во избежание образования твердых частиц, и растворяют. Полимер не является обязательным компонентом, а добавляется с целью увеличения вязкости смеси и образования более стабильной пены. С целью увеличения растворимости полимера можно регулировать рН. После этого добавляют катионное поверхностно-активное вещество. С целью увеличения поверхностного натяжения и стабильности пены добавляют жирный спирт, например додеканол. В качестве растворителя для жирных спиртов обычно применяют монобутиловый эфир диэтиленгликоля или другой подобный растворитель. Раствор можно хранить для последующего применения. Процесс приготовления композиции для одного способа осуществления описан в примере 3. После этого раствор можно смешать с реагирующим компонентом, таким как перекисное соединение. Обычно для практического использования раствор предварительно смешивают и хранят, а реагирующий компонент добавляют позже. Реагирующий компонент, например перекись водорода, добавляется к композиции непосредственно перед употреблением, так как со временем реакционная способность уменьшается. Следует отметить, что перекись водорода можно прибавить к пене в виде твердого вещества (мочевина - перекись водорода), которое считается безопасным для отгрузки и обработки. Это устраняет потребность в использовании высококонцентрированной жидкой перекиси водорода.
Большинство видов пен можно хранить и использовать в виде концентратов. Имеющиеся в наличии типичные пены для тушения пожара имеют концентрацию 0,1%-6%. Другими словами, в случае 0,1% концентрата, каждые 100 галлонов пены приготовлены из 0,1 галлона раствора концентрата и 99,9 галлонов воды. В случае 6% концентрата каждые 100 галлонов пены приготовлены из 6 галлонов раствора концентрата и 94 галлонов воды. Пенообразующая композиция данного изобретения была приготовлена также и в виде концентрата. Были созданы 14%-25% композиций (т.е. в случае 25% концентрата, каждые 100 галлонов пены приготовлены из 25 галлонов раствора концентрата и 75 галлонов воды). Один из примеров композиции пенообразующего концентрата приведен в примере 4. Пенообразующий концентрат не содержит перекись водорода и бикарбонат. Эти составные компоненты в основном добавляются к пенообразующему раствору перед употреблением пены в целях обеззараживания.
Полезным атрибутом пены, описанной в данном изобретении, является то, что композиция очень устойчива и имеет среднюю или высокую степень расширения. Степень расширения пены определяется отношением между объемом образующейся пены и исходным объемом жидкости. Это свойство является важным, так как более высокая степень расширения позволяет использовать меньше воды в случае обеззараживания. Однако, если степень расширения слишком велика, в формулировке может не оказаться достаточно воды для эффективной дезактивации. Кроме того, при высокой степени расширения (выше 60) трудно получить поток пены, который можно направить в разные направления (т.е. пена просто падает прямо вниз как только выходит из пенообразующего сопла). Однако пена с высокой степенью расширения (приблизительно 80-120) исключительно эффективна для заполнения объемов пространства и для покрытия больших поверхностей. С другой стороны, пена со средней степенью расширения (приблизительно 20-60) очень эффективна для покрытия специальных целей, для покрытия вертикальных поверхностей и нижних сторон горизонтальных поверхностей. Композиция, описанная в данном изобретении, может быть применена для получения пены со средней и высокой степенью расширения в системе производства пены с аспирационным воздухом путем простого выбора соответствующего генерирующего пену сопла и регулирования объемной вязкости композиции. После выхода композиции из пенообразующего сопла объемная вязкость композиции определяет степень ее расширения, что позволяет жидкости направить конус сопла в соответствующее местоположение с целью образования пены. Все пенообразующие сопла предназначены для применения с жидкими композициями, объемная удельная вязкость которых меняется в определенных пределах. Водорастворимый полимер добавлялся в соответствующей концентрации, для достижения желаемой объемной вязкости, соответствующей для используемого пенообразующего сопла. В пенообразующей системе со сжатым воздухом степень расширения регулируется путем изменения объема воздуха, впрыснутого в жидкий поток.
Важным физическим свойством пены является ее стабильность. Стабильность пены измеряется временем ее полудренажа, что определяется как время, требуемое для пены, чтобы терять половину ее жидкого первоначального объема. Например, если 1 л раствора используется для образования пены, то время его полудренажа определяется как время, требуемое чтобы из пены стекло 500 мл раствора. Это свойство весьма важно, так как стабильная пена обусловливает более долгий контакт между композицией и химическим или биологическим OВ. Стабильность пены достигается путем увеличения времени, требуемого для дренажа жидкости от пленки. Путем увеличения поверхностной активности жидкости можно регулировать дренаж жидкости от пленки. Чем выше поверхностная вязкость, тем больше стабильность пены. Жирные спирты увеличивают поверхностную вязкость вследствие их расположения между поверхностными молекулами и увеличением сопротивления. Таким образом, композиция течет в жидкой пленке, образуя при этом более стабильные пузыри. Пенообразующая композиция данного изобретения образует пену со временем полудренажа продолжительностью в несколько часов.
Фиг.4 показывает степень расширения и стабильность пены одного способа осуществления данного изобретения, при котором пена образована без перекиси водорода в случае пены с аспирационным воздухом. У композиции степень расширения 125 и время полудренажа приблизительно 3 часа. На фиг.5 приведены те же данные для полной пенообразующей композиции (т.е. с перекисью водорода). В данном случае степень расширения составляет 87, а время полудренажа 2,25 часа.
Были проведены исследования с применением композиции данного изобретения с целью определения эффективности нейтрализации химических и биологических OВ. Работа с химическими OВ сосредоточилась на двух общих классах OВ - нервно-паралитических OВ и на OВ кожно-нарывного действия. Примеры нервно-паралитических агентов включают зарин (GB), зоман (GD), табун (GA) и VX. Примером OВ кожно-нарывного действия является горчичный газ (HD). Первое исследование было проведено с имитаторами химических OВ. В случае G-агентов в качестве имитатора был использован дифенилхлорфосфат. В случае VX имитатором был малатион (O,S-диэтилфенил-фосфонотиоат). В случае горчичного газа имитаторами были полугорчичный газ (2-хлорэтилсульфид) и полу-2-хлорэтилфенилсульфид.
Испытания на живых организмах были проведены в Иллинойском институте Института Технологичесих исследований (ИлИТИ) (Illinois Institute of Technology Research Institute (I1TRI)) и в Эджвудском химико-биологическом центре (ЭХБЦ) (Edgewood Chemical Biological Center (ECBC)) при Абердинском испытательном центре вооруженных сил США в Мэриленде. (U.S. Army Aberdeen Proving Grounds, MD). Ряд поверхностных испытаний был проведен для определения эффективности пены. Общий протокол по поверхностным испытаниям приведен ниже.
Метод поверхностного испытания
1. Сделайте прививку испытательного купона с известной массой химического OВ или имитатора.
2. Подождите 15 минут.
3. Нанесите пену на испытательный купон.
4. Подождите указанный период времени.
5. Экстрагируйте нереагировавшее OВ (или имитатор) ацетонитрилом.
6. Анализируйте экстракт газовой хроматографией, чтобы определить массу непрореагировавшего OВ.
7. В случае G-агентов и горчичного газа все испытания проводятся при рН 8. В случае VX все испытания проводятся при рН 10,5 (регулируется 3 N NaOH). Такая методика применяется и к OВ и к их имитаторам.
Фиг.6 показывает результаты дезактивации живых организмов на бумажных пробах. Исключительно быстрая дезактивация достигается для зомана и VX. Дезактивация горчичного газа происходила медленнее, но все же весьма эффективно. Исследования 13Р ЯМР VX имитатора, О-этил-S-этил-фенилфосфонотиоата с использованием пены данного изобретения показали эксклюзивное расщепление P-S связи. Следовательно, токсичный продукт, который обычно образуется в результате расщепления Р-O связи в VX, не должен образоваться в результате нейтрализации пены.
Пенообразующая композиция оказалась эффективной для нейтрализации, в данном случае для обеззараживания, поверхностей различных субстратов (таких как дерево, пластмасса, ковровая облицовка, бетон). Результаты испытаний, проведенные с имитатором G-агента (дифенил-хлорфосфата), показаны на фиг.7. Время экспозиции пены составляет 15 минут.
Композиция оказалась эффективной также и против имитаторов веществ-концентраторов. Ниже приведенные результаты для имитатора G-агента на различных поверхностях (фиг.8). Имитатор был сконцентрирован с помощью 5% К 125 полимера (Rohm & Haas, Inc.). R125 является органическим полимером. Полимеры часто добавляются к растворам чистых веществ для стабилизации или защиты вещества (или имитатора) во время его применения, чтобы минимизировать воздействие условий окружающей среды (т.е. солнце, ветер, дождь) и сделать вещество более эффективным.
Аналогичные исследования были проведены с целью выяснения влияния температуры на эффективность нейтрализации пены. Нейтрализация VX имитатора (О,S-диэтилфенил-фосфонотиоата) была оценена при 4 и 23° С (комнатная температура). Результаты, приведенные на фиг.9, показывают, что пена эффективна (хотя и не в такой степени) даже при низких температурах.
Испытания на живых организмах были проведены в ЕСВС. Два типа живых организмов были подвергнуты кинетическим (по скорости реакции) испытаниям и испытаниям на опасность контакта. Были применены следующие методики испытания.
Методика ЕСВС для испытания скорости реакции
1. Все испытания были проведены на веществах CASARM-классификации (Chemical Agent Standard Analytical Reference Material - Стандартный аналитический справочник химических веществ ).
2. К испытуемым растворам для нейтрализации перекись водорода прибавлялась в день испытания.
3. Все испытания проводились в размешиваемом реакционном сосуде, снабженном теплозащитной рубашкой, при 25° С.
4. Нейтрализующий раствор (100 мл) был помещен в реакционный сосуд и перемешан в течение периода, достаточного для достижения равновесия (в случае пены испытание было проведено с пенообразующей жидкостью, а не со вспененным материалом).
5. В случае пены испытания для GD и HD были проведены при рН 8. Испытания для VX были проведены при рН 10,5 (регулировался 3 N NaOH).
6. В начале испытании 2 мл агента были помещены в реакционный сосуд.
7. Через определенные интервалы (10 минут или 1 час) образцы вынимали из реакционного сосуда. К образцам добавляли растворитель и анализировали на газовом хроматографе - масс-спектрометре (GC MS), для определения не вступившего в реакцию агента.
8. Все испытуемые образцы были проанализированы трижды.
Методика ЕСВС для испытания на опасность контакта
1. Все вещества были CASARM-классификации. Все испытания были проведены при комнатной температуре (23° С).
2. Применялись следующие испытательные купоны:
a. Chemical Agent Resistant Coating (CARC) - MIL-C-53039A, Polyurethane Topcoat with Primer MIL-P-53022B epoxy.
b. Navy Non-Skid Paint - MIL-C-24667A.
c. Aircraft (AC) Topcoat MIL - PRF-85285C.
d. Navy Alkyd Paint DOD-E-24634, цвет 26270 (серый туман).
3. На всех испытательных купонах граница была нанесена черным жирным карандашом.
4. Каждый испытательный купон (помещенный горизонтально) был загрязнен каплями 2 μ л VX, TGD (концентратор GD), или HD с плотностью (концентрацией) 1 мг/см2.
5. OВ было накрыто стеклянным колпаком в течение 1 часа для исключения испарения.
6. Свежую нейтрализующую композицию смешивали непосредственно перед употреблением.
7. После этого загрязненные купоны обрабатывались 1 мг нейтрализующего вещества в течение 15 минут (в случае пены - испытание было проведено с пенообразующей жидкостью, а не со вспененным материалом).
8. После 15 минут нейтрализующиее вещество смывали с загрязненных купонов (спереди и сзади) деионизированной/дистиллированной водой (37 мл) с помощью лабораторного насоса. Насос подавал 30 мл/мин.
9. Купоны высушивались на воздухе в течение 2 минут, после чего 20 см2 кусок дентальной подпорки помещали на загрязненный участок. Сверху дентальной подпорки помещли груз весом 1 кг.
10. После контакта продолжительностью 15 минут из дентальной подпорки OВ экстрагировалось 18 мл хлороформа в течение 15 минут.
11. Не вступившиее в реакцию OВ, экстрагированное растворителем, анализировалось на GC (газовом хромотографе).
Результаты испытаний скорости реакции, показывающие весовой процент нейтрализованного химического OВ, приведены ниже. Результаты сравнены с DS2.

Результаты этих испытаний наглядно показывают, что пена, описанная в данном изобретении, весьма эффективна для нейтрализации химических OВ. Ясно также, что DS2 является очень эффективным обеззараживающим раствором, и причинами, побуждающими к поиску его замены, являются высокая токсичность и коррозийность, но не неспособность дезактивировать химические OВ.
Одна из проблем композиции касается возможности использования пены при обработке персонала, вовлеченного в дезактивацию зараженного помещения. При использовании пены для дезактивации помещения примененное химическое или биологическое OВ скорее всего точно известно. В этом случае рН композиции легко можно отрегулировать до величины, оптимальной специально для данного OВ. Это регулирование может быть выполнено с помощью предварительно нормированных пачек, в которые помещено основание (такое как, например, NaOH) вместе с твердой перекисью водорода, и которые будут добавлены к жидкой пенообразующей композиции непосредственно перед употреблением. Композиция будет функционировать при значениях рН приблизительно 5-12. При нейтрализации различных химических и биологических OВ с помощью композиции данного изобретения оптимальное значение рН нейтрализации в основном лежит в пределах 8-11. Однако для первых поражаемых конкренто примененное OВ будет в основном неизвестно. Поэтому следует выбрать такое промежуточное значение рН, при котором композиция будет эффективно реагировать со всеми OВ. Такое промежуточное значение рН, обусловленное необходимостью, будет компромиссом. Пригодным для первого пораженного значением рН был является приблизительно 9. Нейтрализующая эффективность пены относительно химических и биологических OВ и их имитаторов приведена в таблице ниже, где показан процент OВ или имитатора, нейтрализованного в течение различного времени экспозиции. (В итоге, нейтрализацию испытанных химических и биологических OВ можно выполнить за период приблизительно 2-60 минут, в зависимости от типа OВ).

Работа с биологическими ОВ была сосредоточена на наиболее трудных для уничтожения веществах - бактериальных спорах (напр., Bacillus anthracis или сибирской язвы). Многочисленные испытания были проведены со спорообразующими бактериями Bacillus globigii (общепризнанный имитатор сибирской язвы) с целью определения эффективности пенообразующей композиции данного изобретения при уничтожении этих микроорганизмов. Испытания были проведены также с целью определения эффективности пены при уничтожении имитатора чумы (Erwinia herbicola - вегетативной бактериальной клетки) и имитатора вируса оспы (бактериофаг MS-2). Кроме того, испытания с живыми агентами были проведены с Bacillus anthracis ANR-1, в Иллинойском институте Института Технологических исследований в Чикаго (Illinois Institute of Technology Research Institute in Chicago, I1). Пена оказалась эффективным уничтожителем для всех этих организмов.
Были проведены два основных типа испытаний, чтобы проверить эффективность пены при уничтожении биологических OВ и их имитаторов. В первом типе испытания - испытания в растворе - микроорганизмы были распределены непосредственно в жидкий раствор, из которого получали пену. После определенного периода времени микроорганизмы отделяли от раствора путем центрифугирования, промывали и высеивали на чашки с соответствующей биологической средой, чтобы определить были ли они убиты. Общий испытательный протокол для испытаний в растворе с использованием спор и вегетативных клеток приведен ниже. В испытаниях были использованы микроорганизмы Bacillus globigii (ATCC 9372) и Bacillus anthracis ANR-1. В испытаниях на вегетативные клетки был использован микроорганизм (ATCC 39368). Бактериофаг MS-2 (ATCC 15597В) с бактериальным хозяином Escherichia coli (ATCC 15597) использовались для испытаний по инактивации вирусов.
Протокол для испытания растворов:
1. Приготовьте суспензию промытых микроорганизмов в стерильной деионизированной воде. Популяция должна быть приблизительно 5× 107 микроорг./мл.
2. Поместите по 5 мл суспензии микроорганизмов в каждой из 12 пробирок центрифуги. Центрифугируйте пробирки в течение 15 минут для осаждения микробов. Отбросьте надосадочную жидкость.
3. Добавьте по 5 мл испытуемого раствора в каждую пробирку.
4. Ресуспендируйте микроорганизмы в испытательные растворы.
5. После контакта в течение указанного времени (15 минут, 30 минут, или 1 час) разбавьте испытуемые растворы десятикратно стерильной деионизированной водой и центрифугируйте в течение 30 минут для осаждения микроорганизмов.
6. Отбросьте надосадочную жидкость и ресуспендируйте микроорганизмы в 15 мл стерильной деионизированной воды.
7. Повторите процесс промывания два раза. После конечного промывания ресуспендируйте микроорганизмы в 5 мл свежего стерильного питательного бульона.
8. Высейте на чашки каждый испытуемый раствор и исходную суспензию микробов в Brain Heart Infusion Agar (для Bacillus globigii и Bacillus anthracis) или в Nutrient Agar (для Erwinia herbicola) в последовательных разбавлениях 100-10-7, и инкубируйте при 37° С в течение 48 часов.
9. Сосчитайте чашки, чтобы определить убивающую эффективность для каждого испытуемого раствора.
Протокол для испытания растворов вирусов
1. Вырастите 18-часовую культуру Е. coli в трипсиновый бульон сои, при 37° С.
2. Делайте прививку свежего трипсинового бульона сои культурой Е. coli. Инкубируйте этот прививочный материал в течение 3-6 часов, при 37° С, при непрерывном встряхивании.
3. Добавьте исходный MS-2 к следующим растворам:
а. к стерильной деионизированной воде;
b. к пенообразующей композиции.
4. Спустя час разбавьте испытуемые растворы десятикратно стерильной деионизированной водой. Центрифугируйте и удалите надосадочную жидкость. Ресуспендируйте осадок в 5 мл стерильного буфера Tris при рН 7,3.
5. Последовательно растворите суспензию фага по сериям разбавления 100-10-7.
6. В пробирках со слоем плавленого агара (трипсиновый бульон сои с 1% агаром), добавьте 0,1 мл суспензии фага и 1 мл культуры Е. coli. Смешайте и лейте на пластины с трипсиновым соевым агаром.
7. После 18-24-часовой инкубации при 37° С считайте единицы бактерий чумы на пластинах с трипсиновым соевым агаром.
Поверхностные испытания были проведены только на уничтожение спор (для Bacillus globigii и Bacillus anthracis). Этот протокол также приведен ниже.
Протокол для поверхностных испытаний
1. Приготовьте суспензию отмытых спор в стерильной деионизированной воде, концентрации приблизительно 5× 108 спор/мл.
2. Равномерно распределите 0,2 мл суспензии спор на девяти матовых стеклянных слайдах (22 × 30 мм) и сушите на воздухе в стерильных условиях в течение 24 часов.
3. Разместите шесть из стеклянных слайдов в отдельные стерильные стеклянные мензурки на 400 мл.
4. Разместите по 100 мл следующих испытуемых растворов в отдельные стерильные стеклянные мензурки на 250 мл:
а. пена (без перекиси водорода);
b. пена + 4% перекись водорода.
5. Для образования пены пропустите через испытуемый раствор воздух сверхвысокой чистоты в виде пузырьков. Дайте пене стечь в мензурку, в которой помещен стеклянный слайд, пока пена не достигнет приблизительно 1/2 дюйма от края мензурки. Закройте мензурку стерильной крышкой и ждите один час. Повторите этот шаг, пока 3 стеклянных слайда не помещены в Испытуемый Раствор "а", и три помещены в Испытуемый Раствор "b"
6. После 1-часовой экспозиции стерильно удалите стеклянный слайд из мензурки на 400 мл и поместите его в мензурку на 250 мл, которая содержит 50 мл стерильной деионизированной воды (т.е. в раствор для полоскания) и снабжена мешалкой. Помешивайте в течение двух часов со средней скоростью. Повторите этот шаг для всех слайдов, которые были помещены в испытуемый раствор (т.е. для всех шести слайдов).
7. Поместите три необработанных стеклянных слайда (контроль) в мензурку на 250 мл, содержащую 50 мл стерильной деионизированной воды и помешивайте в течение двух часов.
8. Немедленно соберите раствор разрушенной пены из каждой 400 мл испытательной мензурки при помощи стерильной пипетки на 10 мл. Делайте запись объема собранного раствора пены. Поместите собранный раствор пены в пробирку центрифуги и разбавьте десятикратно стерильной деионизированной водой. Центрифугируйте в течение 30 минут.
9. Тщательно слейте жидкость и ресуспендируйте споры в 15 мл стерильной деионизированной воды. Повторите промывание еще два раза. После конечного промывания ресуспендируйте споры в 5 мл свежего, стерильного, питательного бульона.
10. Высейте на чашки, на Brain Heart Infusion Agar (или на соответствующей среде в случае сибирской язвы) споры, полученные из раствора пены (после шага промывания), по сериям разбавления 100-10-7 и инкубируйте при 37° С в течение 48 часов.
11. Высейте на чашки, на Brain Heart Infusion Agar (или на соответствующей среде, в случае сибирской язвы) споры, находящиеся в отмывающей жидкости, по сериям разбавления 100-10-7 и инкубируйте при 37° С в течение 48 часов.
12. Сосчитайте чашки и вычислите общее количество полученных спор.
13. Высейте на чашки, на Brain Heart Infusion Agar (или на соответствующей среде в случае сибирской язвы) первоначальный суспензионный раствор спор по сериям разбавления 100-10-7 и инкубируйте при 37° С в течение 48 часов.
14. Сосчитайте чашки и вычислите общее количество спор, первоначально помещенных в стеклянные чашки.
Все испытания были проведены в асептических условиях для уменьшения возможности загрязнения аборигенными микроорганизмами. Ставились контрольные опыты, чтобы удостовериться, что условия экспериментов были стерильными. К раствору пены перекись водорода добавлялась непосредственно перед началом испытаний. рН окончательной композиции (пена + 4% перекись водорода) был 8,0. Все испытания повторялись три раза. Результаты этих испытаний были следующие:
- полная смертность (определенная, как 7 лог смертности или смертность 99,99999% первоначально существующих биологических компонентов) спор В. globigii и В. anthracis была достигнута при 1-часовой экспозиции в пене при в испытаниях как в растворе, так и на поверхности.
- полная смертность (7 лог) клеток Е. herbicola была достигнута через 15 минут при испытаниях в растворе.
- полная дезактивация (4 лог) бактериофага MS-2 была достигнута после 60-минутной экспозиции в растворе пены (примечание: единственный испытанный период времени был 60 минут).
Результаты всех этих испытаний показаны на фиг.10-15.
Кроме описанных выше испытаний, различные компоненты пены были индивидуально испытаны на их спороубивающую эффективность. В испытаниях растворов споры Bacillus globigii были исследованы относительно следующих компонентов пенообразующей композиции.
Деионизированная вода (контроль).
Раствор катионного поверхностно-активного вещества в деионизированной воде, 3%.
Раствор катионного гидротропного вещества в деионизированной воде, 3,8%.
Спиртовая смесь 2% (изобутанол 36,4%, монобутиловый эфир диэтиленгликоля 56,4% и 1-додеканол 7,3%) в деионизированной воде.
Перекись водорода 4% и бикарбонат натрия 4% в деионизированной воде.
Спиртовая смесь 2%, перекись водорода 4%, и бикарбонат натрия 4% в деионизированной воде.
Катионное поверхностно-активное вещество 3% и перекись водорода 4% в деионизированной воде.
Катионное гидротропное вещество 3,8%, перекись водорода 4% и бикарбонат натрия 4% в деионизированной воде.
Катионное поверхностно-активное вещество 3%, перекись водорода 4% и бикарбонат натрия 4% в деионизированной воде.
Результаты этих испытаний показаны на фиг.16. Результаты ясно показывают синергизм между катионным поверхностно-активным веществом, перекисью водорода и бикарбонатом натрия, чем объясняется сильный спороубивающий эффект пенообразующей композиции данного изобретения.
К пенообразующей композиции данного изобретения можно добавить дополнительный компонент, чтобы ингибировать коррозию металла, который подвергается воздействию пены. В одном способе осуществления данного изобретения диметил-этаноламин добавлялся для предотвращения коррозии субстрата из стали, не приуменьшая при этом детоксификацию имитаторов химических и биологических ОВ. Фактически это вещество возможно усилило химическую дезактивацию, так как известно, что этаноламин катализирует реакцию гидролиза некоторых химических OВ, таких как G-агенты. Пределы для добавления диметил-этаноламина - от 0,1 до 10%. Другие потенциальные ингибиторы коррозии включают триэтаноламин, смеси солей этаноламина с С9, С10 и С12 двухосновными кислотами, нитрит дициклогексил-амина, и N,N-дибензиламин.
Пенообразующая композиция данного изобретения была успешно применена маленькими устройствами типа огнетушителя, снабженными патронами со сжатым СО2, переносными устройствами, в которых давление возникает при их присоединений к пожарному насосу и большими насосам военного типа. Каждое такое пенообразующее устройство использует пенообразующее сопло, через которое согласно эффекту Вентури в пену нагнетается воздух. Здесь не требуется снабжать воздухом пенообразующее сопло - пена образуется путем использования воздуха из помещения. Это важно, так как пенообразующий генератор с подачей воздуха добавит воздух в помещении, где образуется пена, выталкивая существующий воздух из помещения, что вызовет перемещение химических и биологических OВ.
Пена также успешно образуется пенообразующими системами со сжатым воздухом. В эти системы воздух нагнетается непосредственно в жидкий поток до того, как жидкость оставит пенообразующее сопло.
Другая важная проблема, касающаяся применения пены, - это ее уборка после того, как проведено обеззараживание химических и биологических OВ. Хотя пена очень стабильна, она может легко разрушаться при использовании коммерчески доступных пеногасителей. Спустя определенное время, достаточное для обеззараживания OВ, пену, после применения, можно удалить водяной струей, содержащей низкие концентрации (1-2%) пеногасителя. В результате этого процесса пена возвращается в жидкое состояние.
Композицию, описанную в данном изобретении, можно применять и другими способами. Пена является не более чем жидким раствором с газовой фазой (в данном случае воздухом). Для деструкции/нейтрализации химических и биологических OВ эффективна именно композиция, а не сама пена (другими словами, химические и биологические OВ обеззараживаются жидкой композицией, а не воздухом). Поэтому для той же основной композиции можно использовать и альтернативные методы применения, например брызги, дым и туман. Цель этих альтернативных методов - уменьшить количество воды, которая требуется для дезактивации пораженных объектов (типа оборудования, находящегося в помещении), и облегчить доступ композиции к объектам, пораженным химическим и биологическим оружием.
Эти альтернативные методы применения могут иметь ряд преимуществ перед применением пены. Например, туман можно использовать для эффективного обеззараживания тех районов, обеззараживание которых пеной затруднено или невозможно. В качестве примера приведем интерьер трубочек для кондиционирования воздуха. Туман можно производить в заслонках и других отверстиях в трубочке; при этом он будет перемещаться на существенное расстояние внутри трубочки и дезактивировать труднодостижимые места. Дополнительным преимуществом тумана является то, что на месте потенциального применения OВ может быть установлена относительно автоматизированная система дезактивации. Чтобы полностью дезактивировать здание, дистанционно управляемые аэрозольные генераторы тумана могут быть помещены внутри здания и периодически включаться через определенные интервалы времени. Этот метод значительно уменьшил бы вероятность того, что занятый дезактивацией персонал будет подвержен воздействию химического и/или биологического оружия.
В одном из методов осуществления изобретения основой для композиции является вода и данная композиция способна к развертыванию в виде тумана (т.е. в виде аэрозоля, с размерами частиц в пределах 1-30 микрон), для быстрой нейтрализации боевых химических и биологических OВ. Композиция характеризуется низкой коррозийной активностью и слабыми токсичными свойствами и может быть развернута доступными коммерческими аэрозольными генераторами. Композиция содержит катионные поверхностно-активные вещества и катионные гидротропные вещества в комбинации с низкими концентрациями перекиси водорода и бикарбонатной соли (например, бикарбонат натрия, калия или аммония). Находящиеся в обращении обеззараживающие композиции для деструкции химических и биологических ОВ используют токсичные и/или коррозийные химические соединения, которые потенциально могут повредить чувствительную аппаратуру, вступая с ней в контакт. Кроме того, большинство находящихся в обращении композиций требует для обеззараживания большое количество воды.
Композиция содержит аналогичные компоненты, что и водная пенообразующая композиция. Однако из пенообразующей композиции удалены различные составные компоненты, которые необходимы для образования пены. Состав туманообразующей композиции на основе воды, следующий

Обычно, катионные поверхностно-активные вещества являются четвертичными аммонийными солями, такими как цетилтриметил-аммоний бромид. Другие примеры катионных поверхностно-активных веществ включают полимерные четвертичные соединения. Примеры подходящих гидротропных веществ включают тетрафенил-аммоний бромид, триацетил-метил-аммоний бромид и тетрабутил-аммоний бромид. Комбинация бикарбоната и перекиси водорода образует окислитель (гидропероксикарбонатные группы, обладающие высокой реакционной способностью), который вносит существенный вклад в нейтрализацию химических и биологических OВ.
В одном испытании для демонстрации нейтрализации химического OВ 25 микролитров (-20 мг) имитатора химического OВ (дифенилхлор-фосфат) были помещены на испытательный купон (защитный слой, металл, дерево, и т.д.). Купон был помещен внутрь испытательной камеры, которая после этого была заполнена композицией тумана, произведенного коммерческим аэрозольным генератором (размеры капельки в пределах между 1-20 микронами). Тот же самый имитатор был помещен на идентичные испытательные купоны, которые служили контрольными экземплярами. Спустя час контрольные и опытные испытательные купоны были помещены в раствор ацетонитрила на один час с целью экстракции не вступившего в реакцию имитатора. Затем раствор ацетонитрила был проанализирован газовой хроматографией с целью определения массы вступившего в реакцию имитатора. В результате 1-часовой экспозиции в испытательной камере с туманом была достигнута более чем 99% нейтрализация имитатора G-агента (дифенилхлор-фосфат) на всех испытанных поверхностях и полная нейтрализация для всех поверхностей после четырех последующих обработок туманом (с 1-часовым интервалом между каждой обработкой). После четырех последовательных обработок туманом была достигнута нейтрализация имитатора VX (О-этил-S-этил-фенил-фосфонотиоата) в пределах 70-99% и нейтрализация имитатора горчичного газа (хлорэтил-этилсульфида) в пределах 30-85%. После четырех последовательных обработок туманом была достигнута 7 лог смертность имитатора сибирской язвы (споры В. globigii).
Одно из различий между этой композицией и существующими туманообразующими растворами для обеззараживания химических и биологических OВ заключается в том, что основу настоящей композиции составляет вода. Существующие же туманообразующие растворы для обеззараживания химических и биологических OВ являются органическими жидкостями. Данная композиция характеризуется малой токсичностью и низкими коррозийными свойствами. Это позволяет применять ее в условиях, где контакт с людьми, животными или оборудованием может быть необходим или целесообразен.
Два следующих примера описывают, как приготовить две пенообразующие композиции согласно данному изобретению. После этого представлены результаты испытаний, полученные с использованием пены, приготовленной согласно данному изобретению. Хотя последовательность шагов, указанных в примерах 1 и 2, представляет предпочтительные способы реализации изобретения, описанные здесь последовательности необязательны для реализации целей настоящего изобретения.
Пример 1. Смешайте следующее в 100 мл воды:
WITKO ADOGEN 477™ (50%) - Катионное гидротропное вещество, 3,84 вес.%.
Спиртовую смесь 2,0 вес.% (изобутанол 36,4 вес.%, монобутиловый эфир диэтиленгликоля 56,4 вес.%, додеканол /тетрадеканол, С12-14 7,3 вес.%) - жирный спирт с длинной цепью. JAGUAR 8000ТМ полимер - водорастворимый полимер 0,2 вес.%. Соляная кислота (для регулирования рН приблизительно в пределах 6,5, для повышения растворимости полимера).
Пример 2.Смешайте следующее в 100 мл воды в указанном порядке:
WITKO ADOGEN 477™ (50%) - Катионное гидротропное вещество, 3,84 вес.%.
Спиртовую смесь 2,0 вес.% (изобутанол 36,4 вес.%, монобутиловый эфир диэтиленгликоля 56,4 вес.%, додеканол 7,3 вес.%) - жирный спирт с длинной цепью.
JAGUAR 8000TМ полимер - водорастворимый полимер 0,2 вес.%. Соляную кислоту (для регулирования рН приблизительно в пределах 6,5) - для активации полимера и достижения в смеси желаемой вязкости.
Катионное поверхностно-активное вещество WITCO VARIQUAT ТМ 80 МС 3 вес.%, для солюбилизации (растворения) химических агентов. Смесь додеканола и монобутилового эфира диэтиленгликоля 1:1, 1,5 вес.%, для стабилизации пены. Перекись водорода 2,0 вес.%.
Бикарбонат натрия (NaHCO3) 2,0 вес.%. Перекись водорода и бикарбонат натрия вместе играют роль сильного нуклеофильного агента.
Приведенное ниже обобщение результатов и данных основано на проведенных испытаниях с использованием стандартных имитаторов химических и биологических ОВ. Из-за высокой токсичности натуральных ОВ подобраны такие имитаторы, которые подражают их химическим и физическим свойствам. Так, например, дифенил-хлорфосфат - это жидкое малорастворимое в воде соединение, которое химически похоже на G-агенты. Малатион - другой имитатор, которым часто замещают VX-агенты в лабораторных испытаниях.
Имитаторы химических OВ
1. Протокол испытания:
25 мг имитатора было распределено на поверхности 25 см2 на 25 см2, т.е. 10 г/м2 (использовались поверхности обычной бумаги для печати и натриево-кальциево-силикатного стекла), на образец наносили пену (высота пены была 12 см). Через некоторое время образец был удален. Образец экстрагировали ацетонитрилом или четыреххлористым углеродом. В случае применения ацетонитрила можно проследить образование полярных продуктов методом газовой хроматографии (GC) или методом газовой хроматографии / масс-спектрометрии (GC/MS), что невозможно сделать при применении четыреххлористого углерода. После разрушения пены и образования жидкого остатка, 15 мл, последний анализировали методами GC и GC/MS. Анализ проводили на приборе Хьюлетт Пакард (Hewlett Packard TM) HP-6890 GC, с детектором Флейм Фотометрик (Flame PhotometricTM) (6% CNPRPH силоксан), проба для инъекции 1 микролитр, щель 1:100, температура инъекции 250° С, температура детектора 250° С, температура колонки (термостата) возрастала от 100 до 250° С за 9,5 минут, скорость потока гелия 2 мл/мин. Для определения каталитического эффекта на пену были проведены контрольные опыты с использованием системы вода + добавки.
2. Результаты:
Дифенил-хлорфосфат. Фиг.17 показывает сравнение эффектов обеззараживания, полученных с использованием пены, описанной в данном изобретенияи с результатами, полученными в системе пена плюс перекись/бикарбонат (добавка), и системой вода плюс та же самая добавка. Результаты, показанные на фиг.17, получены в случае обеззараживания 25 мг дифенил-хлорфосфата на 25 см2 обыкновенной бумаге для печати (время полураспада приблизительно 2 минуты). Результаты показывают, что его добавка в воду неэффективна, однако в пене с добавкой наблюдается усиление эффекта в результате синергизма. Такие же результаты были получены и в случае поверхностей из натриево-кальциево-силикатного стекла.
Малатион. Фиг.18 показывает сравнение результатов обеззараживания малатиона на бумаге, с использованием пены данного изобретения и с использованием воды. На стекле (матовые слайды микроскопа, 1× 3 дюйма) мы наблюдали, что некоторое количество малатиона физически смывается со стекла в жидкость пены. Аналогичные наблюдения были сделаны также и в контрольных опытах, но только с водой. Для этого в случае малатиона мы анализировали как поверхность, так и остаточную жидкость, и складывали, чтобы определить общее количество не вступившего в реакцию малатиона. Оказалось, что результаты на стекле были сопоставимыми с результатами на бумаге.
Результаты ядерного магнитного резонанса (ЯМР) показали, что скорее происходит P-S расщепление, чем Р-O расщепление, что более желательно.
2-Хлорэтил-этилсульфид (полугорчичный газ). В случае полугорчичного газа невозможно провести надежное испытание поверхности, так как он быстро испаряется (улетучивается) с поверхности. По этой причине были проведены модифицированные эксперименты в закрытом контейнере с использованием 500 мг полугорчичного газа и 100 мл пены. Результаты этого испытания приведены на фигуре 19.
В отличие от 2-хлорэтил-этилсульфида, 2-хлорэтил-фенилсульфид испаряется медленно и его можно использовать для поверхностных испытаний. Однако было отмечено, что его реакционная способность намного ниже, чем горчичного газа. Результаты ЯМР анализа показывают, что пена реагирует с этим довольно инертным материалом.
Имитаторы биологических OВ.
1. Поверхностные испытания со спорами Bacillus globigii:
Bacillus globigii (ATCC 9372 были использованы в качестве суррогата Bacillus anthracis во всех испытаниях. Бактерии культивировали на среде скошенного агара Tryptic Soy Agar slants в течение трех дней. Бактерии в асептических условиях переносили на скошенный агар, Endospore agar (Nutrient Agar, обогащенный 0,002% МnСl2 ·4Н20), и инкубировали при 37° С 17-20 дней. За процессом споруляции (формирования спор) наблюдали с использованием метода окрашивания по Schaeffer-Fulton (с малахитовым зеленым).
Испытания на уничтожение спор проводили как в растворе пены (в пробирках), так и во вспененной пене с глутаровым альдегидом (3%) в качестве добавки (поверхностные испытания).
Процедура поверхностного испытания:
Споры В. globigii суспендировали в стерильной деионизированной воде. После этого определенный объем суспензии спор наносили на пластинки из матового стекла, высушивали на воздухе в стерильных условиях и обрабатывали вспененной пеной с добавкой в течение 0,5 часа при 25° С. После этого стеклянные поверхности вынимали из пены и промывали стерильным раствором соли, помешивая их в течение 2 часов. Раствор пены, отмывающий раствор и исходная суспензия спор были испытаны на споры В. globigii путем высевания спор на чашки, на Brain Heart Infusion Agar, no сериям разбавления 100-10-7, и подсчета после 48 часов.
Результаты.
Фиг.20 показывает результаты, полученные согласно вышеизложенной процедуре. Эксперименты были начаты с 107 спор и оставшиеся в живых споры наблюдались после 30-минутного контакта с пеной. Были также проведены эксперименты с раствором, которые подтвердили эффективность пены.
2. Испытания раствора с Erwina herbicola
Мы показали также полное уничтожение (7-лог смертность) Erwina herbicola (ATCC 39368) в растворе пены за 15 минут. Экспериментальный метод для уничтожения спор, по которому был проведен этот опыт, описан выше с тем различием, что вместо Brain Heart Infusion Agar бактерии были культивированы на трипсиновом агаре сои. Фиг.21 показывает, что согласно полученным данным обработка пеной, описанной в данном изобретении, вызывает гибель всех бактерий.
Пример 3. Процедура приготовления пены
В следующих примерах Variquat BOMC является смесью хлоридов бензил-(С12-С16)-алкилдиметаммония; Adogen 477 - это дихлорид пентаметил-жирный алкил-триметилендиаммония; и Jaguar 8000 - это 2-гидроксипропиловый эфир гуаровой смолы.
1. Налейте 18 литров деионизированной воды в большую оплетенную бутыль, снабженную, по возможности, большой мешалкой.
2. Добавьте 691,2 г Adogen 477 (Witco) [гидротропное соединение]. Ополосните используемую мензурку, чтобы из оплетенной бутыли отмерить 477 w / Н2О, и слейте раствор, использованный для полоскания, обратно в оплетенную бутыль.
3. Добавьте 360 г Спиртовой смеси 1 (изобутанол 36,4%; DEGMBE 56,4%; додеканол 7,3%). Отметьте рН и продолжайте измерять рН во время всей процедуры.
4. Добавьте 36 г Jaguar 8000 [водорастворимый полимер]. Добавте Jaguar 8000 медленно, чтобы избежать образования твердых частиц; слегка обстучите сосуд шпателем. После окончания добавления Jaguar 8000 размешивайте в течение 15 минут. По мере растворения Jaguar 8000 рН должен повыситься. Примечание: Этот полимер слегка увеличивает вязкость воды, образуя более устойчивую пену.
5. Осторожно регулируйте рН раствора, добавляя по каплям 10% НС1. Доведите рН до 6,5; это требует добавления всего нескольких миллилитров. Перемешивайте в течение 1 часа. Снизите рН, чтобы растворить полимер, % НСl: 53,5 мл НСl (37,4%)+146,5мл dH2O.
6. Осторожно добавьте 540 г Variquat 80 МС [Поверхностно-активное вещество]. Контролируйте рН (не должен подниматься). Ополосните мензурку, которая использовалась, чтобы из оплетенной бутыли отмерить w / раствор Variquat, и слейте раствор, использованный для полоскания, обратно в оплетенную бутыль. Отберите пробы для определения рН и закройте бутыль. Перемешивайте в течение 2 часов.
7. Добавьте 270 г додеканола и DEGMBE 1:1 (вес.%), монобутиловый эфир диэтиленгликоля. Добавляйте по каплям в течение 1 часа. Перемешивайте еще в течение 1 часа. Отметьте конечное значение рН пены. DEGMBE применяется в качестве растворителя для додеканола. Додеканол применяется для повышения поверхностного натяжения системы - w / двухслойная ламинарная стена пены. Повышенное поверхностное натяжение обеспечивает более высокую стабильность пены, так как жидкий слой между ламинарными стенами не будет так быстро иссушаться.
8. Налейте раствор в бутыль для хранения.
Пример 4. Приготовление 25% концентрата пены
1. Добавьте полимер Jaguar 8000 (2,6 г) к деионизированной воде (280 г). Полимер должен добавляться осторожно, приблизительно в течение 5-10 минут так, чтобы не образовались твердые частицы. Однако, если полимер добавляется слишком медленно, то при данном соотношении полимера и воды может образоваться гель. Помешивайте раствор в течение 2 часов.
2. Смешайте Adogen (76,8 г) и Спиртовую смесь 1 (40,0 г); добавьте ее к раствору полимера. Доведите рН до 6,5 при помощи 10% НСl. Накройте и перемешивайте в течение более 1 часа. Примечание: Спиртовая смесь 1 состоит из изобутанола 36,4%, монобутилового эфира диэтиленгликоля (DEGMBE) 56,4% и додеканола 7,3%.
3. Добавьте Variquat 80 МС (60,0 г) и перемешивайте в течение более 1/2 часа.
4. Добавьте Смесь жирных спиртов (93,4 г). Накройте и перемешивайте в течение более 1 часа. Примечание: Смесь жирных спиртов содержит DEGMBE 69%, додеканола 15%. 1-тридеканола 6% и 1-тетрадеканола 10%.
Пример 5. Полевая демонстрация (показ) пенообразующей композиции
Для определения эффективности уничтожения пенообразующей композицией бактериальных спор в служебных помещениях был проведен эксперимент на полигоне армии США Дагвей Прувинг Граундс в штате Юта (U.S. Army Dugway Proving Grounds, UT). Были установлены и проверены шесть испытательных панелей (16"× 16"). Испытательные панели состояли из потолочной плиты, окрашенного обшивочного листа, ковра, окрашенного металла, офисных разделителей и бетона. Панели (за исключением бетона) были установлены вертикально. Панели были обрызганы суспензией спор Bacillus globigii и оставлены на ночь для высыхания. Затем были отобраны пробы для определения исходной концентрации спор. Концентрация композиции, которой обрабатывали панель, была приблизительно 100 мл на квадратный метр поверхности. Пенообразующую композицию (при рН 8,0) распылили на поверхности испытуемых панелей и оставили на ночь. Приблизительно через 20 часов с испытуемых панелей были отобраны пробы для определения оставшихся в живых спор. Испытания повторялись каждый день в течение последующих четырех дней.
Результаты ежедневных испытаний исходных (т.е. загрязненных) и конечных (т.е. обеззараженных) проб показывают, что во всех случаях наблюдаются хорошие данные по уничтожению спор (между минимумом 4 лог и максимумом 7 лог смертности).
Пример 6. Детоксификация спор
Следующий материал описывает эксперимент по уничтожению спор. 1 мл испытуемого раствора помещают в стерильную пробирку и добавляют к нему 0,1 мл суспензии спор В. globigii. Через час раствор разбавляют десятикратно стерильной деионизированной водой и центрифугируют в течение 30 минут. Супернатант (жидкость) отделяют в стерильных условиях, а на дне пробирки остаются споры в виде осадка. Споры ресуспендируют в 5 мл стерильной деионизированной воды и снова центрифугируют в течение 30 минут. Супернатант снова отделяют, а споры ресуспендируют в 5 мл стерильной деионизированной воды. Раствор снова центрифугируют и Супернатант снова отделяют. Споры ресуспендируют в 5 мл стерильной DI воды и этот раствор высевают на среде Brain Heart Infusion Agar, с использованием серий последовательных разбавлений 10ЕО-10Е-7 на стерильные чашки Петри. Чашки Петри инкубируют при 37° С в течение 48 часов, после чего считают и регистрируют образующие колонию единицы. Фиг.16 показывает уничтожение суррогата сибирской язвы, В. globigii, через час после экспозиции в растворе 1) одной деионизированной воды (контроль), 2) одного катионного поверхностно-активного вещества (без перекиси водорода и бикарбоната), 3) одного жирного спирта (без перекиси водорода и бикарбоната), 4) одного катионного гидротропного вещества (без перекиси водорода и бикарбоната), 5) перекиси водорода и бикарбоната в деионизированной воде (без катионного поверхностно-активного вещества или жирного спирта или катионного гидротропного вещества, 6) катионного поверхностно-активного вещества с перекисью водорода и бикарбонатом, 7) жирного спирта с перекисью водорода и бикарбонатом и 8) катионного гидротропного вещества с перекисью водорода и бикарбонатом. Все эксперименты были проведены при рН 8,0.
Из предшествующего описания квалифицированный специалист может легко установить существенные характеристики изобретения, определенного в этом описании и прилагаемой формуле, и, придерживаясь принципов данного изобретения, может предложить различные изменения и модификации изобретения, чтобы приспособить его к различным способам реализации и условиям. Такие изменения и модификации, очевидные для квалифицированного специалиста, должны быть включены в диапазоны пунктов прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭМУЛЬСИОННАЯ РЕЦЕПТУРА ДЛЯ ОБЕЗЗАРАЖИВАНИЯ ПОВЕРХНОСТЕЙ | 2015 |
|
RU2599004C1 |
| ДЕКОНТАМИНИРУЮЩИЙ И ПЕНООБРАЗУЮЩИЙ ВОДНЫЙ РАСТВОР | 2009 |
|
RU2484869C2 |
| ПОЛИФУНКЦИОНАЛЬНАЯ ПЕННАЯ КОМПОЗИЦИЯ ДЛЯ КОМПЛЕКСНОЙ СПЕЦИАЛЬНОЙ ОБРАБОТКИ ПОВЕРХНОСТЕЙ, ОБЪЕМОВ И ОБЪЕКТОВ ОТ ОПАСНЫХ АГЕНТОВ И ВЕЩЕСТВ | 2004 |
|
RU2290208C2 |
| ГЕЛЕОБРАЗУЮЩАЯ РЕЦЕПТУРА ОКИСЛИТЕЛЬНОГО И НУКЛЕОФИЛЬНОГО ДЕЙСТВИЯ ДЛЯ ОБЕЗВРЕЖИВАНИЯ ПОВЕРХНОСТЕЙ | 2007 |
|
RU2351380C1 |
| СПОСОБ ОБРАБОТКИ ПЕРЕКИСНЫХ РАСТВОРОВ | 2011 |
|
RU2565435C2 |
| КОМПОЗИЦИЯ ДЛЯ ДЕЗИНФЕКЦИИ И ДЕКОНТАМИНАЦИИ ПРЕДМЕТОВ, ЗАРАЖЕННЫХ ПРИОНАМИ, А ТАКЖЕ ОБЫЧНЫМИ ИНФЕКЦИОННЫМИ АГЕНТАМИ | 2009 |
|
RU2494762C2 |
| СПОСОБ ОБЕЗЗАРАЖИВАНИЯ ВНУТРЕННЕЙ ПОВЕРХНОСТИ ХИМИЧЕСКИХ БОЕПРИПАСОВ ОТ ОСТАТКОВ ФОСФОРОРГАНИЧЕСКИХ ОВ ТИПА "ЗАРИН" И "ЗОМАН" | 2001 |
|
RU2200045C1 |
| КОМПОЗИЦИЯ ДЛЯ ОБРАБОТКИ ВОЛОС | 2001 |
|
RU2269336C2 |
| КОМПОЗИЦИЯ ДЛЯ ДЕГАЗАЦИИ ОТРАВЛЯЮЩИХ ВЕЩЕСТВ И ДЕЗИНФЕКЦИИ ОБЪЕКТОВ САНИТАРНОГО НАДЗОРА | 2006 |
|
RU2322265C1 |
| СПОСОБ ДЕЗИНФИЦИРОВАНИЯ ПОВЕРХНОСТЕЙ, КОНТАКТИРУЮЩИХ С ПИЩЕВЫМИ ПРОДУКТАМИ, В МАШИНЕ ДЛЯ УПАКОВКИ ПИЩЕВЫХ ПРОДУКТОВ | 1995 |
|
RU2149024C1 |

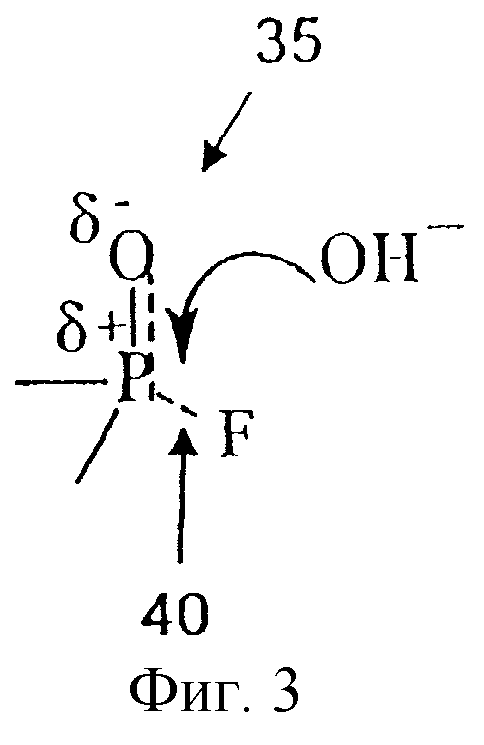
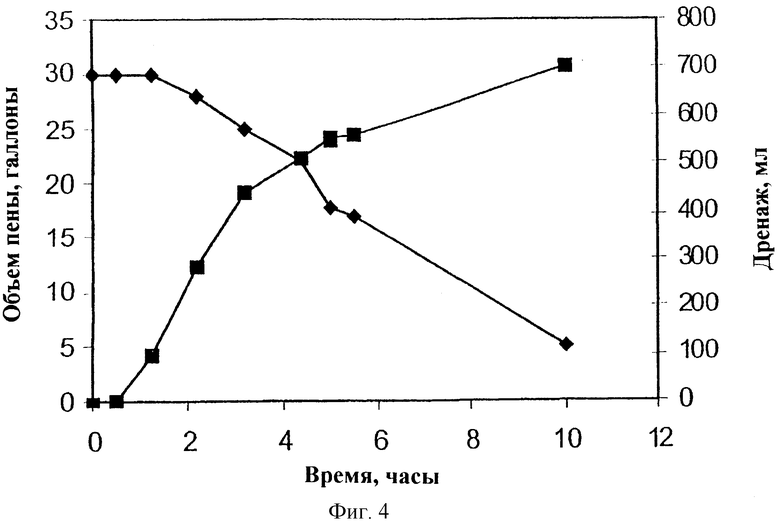









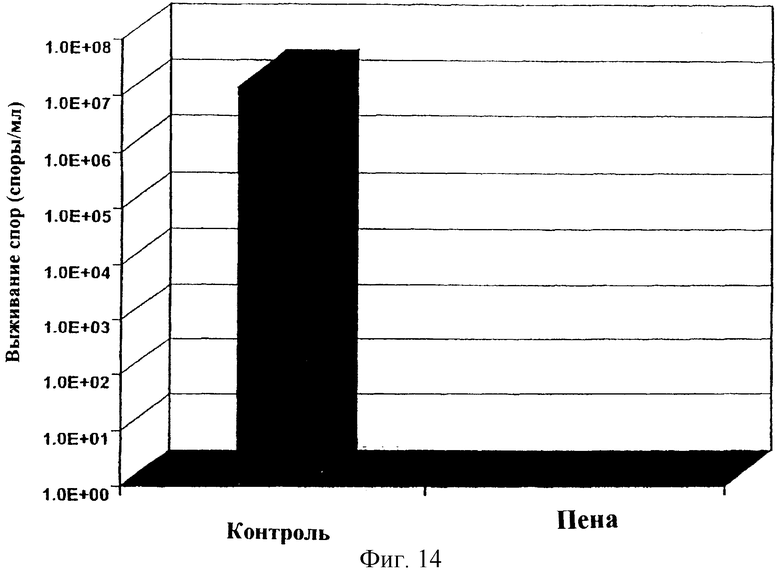







Композиция предназначена для нейтрализации химических и биологических агентов, особенно агентов боевых химических и биологических средств, оказывающие неблагоприятное влияние на здоровье. Сущность изобретения: композиция содержит, по меньшей мере, два солюбилизирующих компонента, один из которых является катионным поверхностно-активным веществом, например, четвертичной солью аммония, концентрацией в пределах приблизительно 0,1-10 вес.%, а другой - катионным гидротропным веществом, по меньшей мере, один реагирующий компонент, который может быть окисляющим или нуклеофильным соединением или их смесью, и воду для образования водной композиции. Композиция не токсична и некорродирующая и может быть нанесена различными способами и в виде различных фаз. Композиция способна уничтожать до 99,99999% бактериальных спор в пределах одного часа обработки. 4 н. и 6 з.п. ф-лы, 21 ил.

| Саморазгружающаяся железнодорожная платформа | 1921 |
|
SU366A1 |
| Изделие для проведения эстетического массажа лица, шеи, декольте и волосистой части головы | 2021 |
|
RU2766724C1 |
| US 5859064 А, 12.01.1999 | |||
| US 5760089 А, 02.06.1998. | |||
Авторы
Даты
2004-12-10—Публикация
2000-12-08—Подача