Изобретение относится к ультразвуковой медицинской диагностике и может быть использовано в акушерстве и гинекологии, маммографии, онкологии, педиатрии и других медицинских областях, где применяются ультразвуковые исследования.
Известен способ обработки и отображения эхо-сигналов, позволяющий осуществлять дифференциацию (различение) биологических тканей по акустическому изображению, получаемому в ультразвуковых диагностических сканерах, для чего эхо-сигналы, принимаемые сканером, подвергают обработке с целью отображения их на дисплее, на котором в результате строится двумерное серо-шкальное изображение, в котором яркость отдельных элементов пропорциональна амплитуде отображаемых эхо-сигналов. Режим получения такого изображения получил название В-режим, а само изображение получило название В-эхограммы (Осипов Л.В. “Ультразвуковые диагностические приборы: Практическое руководство для пользователей”, М., "Видар", 1999 г., стр. 33-35; см. приложение).
Получение В-эхограмм широко используется при ультразвуковых исследованиях (УЗИ) в медицине для оценки состояния биологических структур и органов человека, а также для выявления патологий.
Недостатком способа, использующего для диагностики формирование и отображение В-эхограммы, является то, что получаемое при этом акустическое изображение дает информацию только о положении по глубине и уровне эхо-сигналов от акустических неоднородностей исследуемых биологических тканей. В то же время большой диагностический интерес представляют такие физические характеристики, как частотно-зависимый характер затухания ультразвуковых сигналов в биологических тканей и частотно-зависимый характер обратного рассеяния (отражения) ультразвуковых сигналов на акустических неоднородностях.
Известен способ оценки частотно-зависимого затухания (ослабления) ультразвуковых сигналов, который предлагают применять для дифференциации биологических тканей в целях диагностики и выявления патологий (R. Kuc. Bounds of estimating the acoustic attenuation of small tissue regions from reflected ultrasound. TIEEE, v.73, N 7, July, 1985, pp.1159-1168). В соответствии с этим способом вычисляют наклон по частоте удельного коэффициента ослабления акустических волн в биологических тканях, для чего определяют сдвиг спектра ультразвуковых сигналов, отраженных от рядом расположенных областей тканей. Полученное численное значение наклона коэффициента ослабления предлагают использовать для диагностики. Недостатками данного способа являются отсутствие возможности оценивать указанный параметр одновременно в различных участках исследуемой области, трудность визуализации результатов на двухмерной картине в удобном для исследователя виде, а также невозможность учесть влияние на результат оценки частотно-зависимого характера обратного рассеяния и спекл-шума, являющегося следствием когерентности эхо-сигналов, используемых при обработке. По этим причинам указанный способ не нашел широкого практического применения.
Известен способ цветового картирования движения биологических структур, прежде всего кровотока, при котором в ультразвуковых сканерах, получающих и отображающих В-эхограмму в выделенной для анализа области, строят цветовое изображение движущихся структур, для чего фильтруют и оценивают среднее значение доплеровского спектра эхо-сигналов, полученных на различных участках исследуемой области, в результате чего отображают на цветовом дисплее двумерную картину распределения оценок средних скоростей кровотока в выделенной области (Осипов Л.В. “Ультразвуковые диагностические приборы: Практическое руководство для пользователей”; М.; “Видар”, 1999. стр. 164-166). Данный способ позволяет получать информацию о движении не только кровотока, но и тканей, но не дает возможности оценить характеристики затухания и обратного рассеяния в тканях для диагностики их состояния.
Настоящее изобретение решает задачу цветовой дифференциации биологических тканей пациента и повышение уровня и качества диагностических ультразвуковых исследований.
Решение поставленной задачи достигается следующим образом.
В способе обработки и отображения эхо-сигналов для дифференциации биологических тканей в ультразвуковых диагностических сканерах, включающем оценку спектра эхо-сигналов и цветовое картирование сигналов на цветном дисплее, согласно настоящему изобретению, оценивают амплитудный спектр принятых в процессе сканирования реализации эхо-сигналов для каждого положения луча на отдельных интервалах глубин в выделенной области, при этом разделяют эхо-сигналы на низкочастотную, среднечастотную и высокочастотную составляющие в трех каналах фильтрации, после чего строят двумерное акустическое изображение биологических тканей, в элементах которого отображают результаты оценки спектра с использованием различных оттенков цветовой палитры.
Согласно изобретению, для каждого канала фильтрации устанавливают ширину полосы частот, меньшую максимальной ширины спектра эхо-сигналов, а суммарную полосу частот трех каналов фильтрации устанавливают не меньшей, чем максимальная ширина спектра эхо-сигналов. После чего три составляющие детектируют и используют для формирования цветового изображения в качестве основных цветов: низкочастотную - для красного (R), среднечастотную - для зеленого (G), высокочастотную - для синего (В). Далее цветовое изображение отображают на цветном дисплее.
Изобретение предусматривает, что одновременно с разделением реализации эхо-сигналов на три составляющие вводят сдвиги по центральной частоте и изменяют ширину полосы частот в каждом канале фильтрации в соответствии с ожидаемым смещением спектра эхо-сигналов с увеличением глубины в сторону нижних частот вследствие частотно-зависимого затухания.
Согласно настоящему изобретению, для снижения влияния спекл-шума полосу частот каждого из каналов фильтрации делят на более узкополосные подканалы, осуществляют фильтрацию реализации эхо-сигналов в каждом узкополосном подканале, затем результаты фильтрации в узкополосных подканалах детектируют и суммируют отдельно в каждом из трех каналов фильтрации, после чего три составляющие используют для формирования цветовых изображений и отображение на цветном дисплее.
Технический результат настоящего изобретения заключается в том, что после обработки реализации эхо-сигналов и оценки их спектра на различных интервалах по глубине в каждом из лучей, устанавливаемых в процессе сканирования, достигается возможность реализации акустического изображения биологических тканей пациента, на котором с помощью различных оттенков цветовой палитры отображается в двумерном сечении биологических тканей пространственное изменение спектра эхо-сигналов, несущее информацию о частотно-зависимом характере затухания и частотно-зависимом обратном рассеянии. Это позволяет:
- существенно повысить эффективность и качество диагностических исследований, осуществляемых с помощью ультразвуковых сканеров;
- повысить вероятность выявления патологий и определять их местоположение и границы;
- значительно повысить информативность и объективность визуальной диагностической информации о состоянии пациента;
- ускорить процедуру обследования пациента.
Сущность настоящего изобретения поясняется примером реализации патентуемого способа обработки и отображения эхо-сигналов для дифференциации биологических тканей и чертежами, на которых представлены:
Фиг.1 - блок-схема варианта устройства, реализующего данный способ;
Фиг.2 - вид спектра эхо-сигналов на входе устройства обработки и после преобразования в процессе обработки;
Фиг.3 - вид обычного черно-белого ультразвукового изображения печени и молочной железы и вид цветового изображения этих органов, полученного в результате реализации данного способа.
Патентуемый способ обработки и отображения эхо-сигналов для дифференциации биологических тканей осуществляют с помощью устройства обработки (фиг.1), которое содержит три канала фильтрации, соответствующие каналам цветности цветового дисплея:
R, G и В.
На каждый из каналов фильтрации поступает реализация эхо-сигнала с выхода приемного тракта ультразвукового сканера. В качестве ультразвукового сканера может быть использован любой серийно выпускаемый прибор с цветным дисплеем, например, "Эхоскан-10", который производится фирмой “ИзоМед” (г.Москва).
Каждый канал фильтрации включает в себя однотипные элементы. На входе канала фильтрации имеется перестраиваемый фильтр 1, на первый вход которого поступает реализация эхо-сигнала, выход перестраиваемого фильтра 1 соединен с входом детектора 2 и с первыми входами узкополосных фильтров 8/1, 8/2, количество которых в данном примере принято равным двум, но может быть увеличено до трех или более. Выходы узкополосных фильтров 8/1 и 8/2 соединены с входами детекторов 9/1 и 9/2 соответственно, выходы указанных детекторов соединены с входами сумматора 10.
Выход сумматора 10 соединен с вторым входом коммутатора 3. Первый вход коммутатора 3 соединен с выходом детектора 2.
Элементы каждого канала фильтрации: фильтры, детекторы, коммутатор и сумматор могут быть выполнены в аналоговом виде, однако в современных ультразвуковых сканерах предпочтительной является реализация их в цифровом виде с использованием известных методов (см. Гольденберг Л.М. и др. “Цифровая обработка сигналов”; Справочник; М.; Радио и связь, 1985 г.)
В этом случае с выхода приемного тракта на входы каналов фильтрации реализация эхо-сигналов поступает в цифровом виде, что соответствует цифровому построению приемного тракта, принятому в настоящее время в большинстве современных полностью цифровых ультразвуковых сканеров.
Выходы коммутаторов 3 каждого из каналов фильтрации R, G и В соединены с соответствующими входами цифрового блока обработки, преобразования и запоминания сигналов 4. Выходы R, G и В цифрового блока обработки, преобразования и запоминания сигналов 4 соединены с соответствующими входами R, G и В цветного дисплея 5.
Каналы фильтрации R, G и В, состоящие из однотипных элементов, отличаются между собой тем, что в каждом из перестраиваемых фильтров 1 устанавливают отличающиеся друг от друга центральные частоты: в фильтре 1 канала фильтрации R устанавливают частоту ниже, чем в фильтре 1 канала фильтрации G, а в последнем устанавливают частоту ниже, чем в фильтре 1 канала фильтрации В. У всех трех перестраиваемых фильтров 1 выбирают ширину полосы частот пропускания, меньшую ширины спектра эхо-сигналов, а суммарную полосу перестраиваемых фильтров 1 в трех каналах фильтрации устанавливают не меньшей, чем ширина спектра эхо-сигналов. Ширину спектра эхо-сигналов принимают равной ширине полосы частот приемного тракта ультразвукового сканера.
На второй вход каждого из перестраиваемых фильтров 1 подают сигналы управления с выхода блока управления 6. По этим сигналам управления осуществляют одновременную перестройку центральных частот всех трех фильтров 1 каналов фильтрации.
Ширину полосы частот и центральные частоты узкополосных фильтров 8/1 и 8/2 в каждом из каналов фильтрации выбирают таким образом, чтобы их суммарная ширина полосы частот была близка ширине полосы частот соответствующего перестраиваемого фильтра 1. На второй вход каждого узкополосного фильтра 8/1 и 8/2 в каждом из каналов фильтрации также подают сигнал управления от блока управления 6. По этим сигналам управления осуществляют одновременную перестройку центральных частот всех узкополосных фильтров 8 таким образом, чтобы суммарная полоса частот узкополосных фильтров в каждом канале фильтрации совпадала с полосой частот перестраиваемого фильтра 1.
Блок управления 6 является цифровым устройством, которое вырабатывает сигналы управления сдвигом частот в фильтрах 1 и 8 в каждом из каналов фильтрации на основе известных усредненных данных о смещении спектра частот сигналов в низкочастотную область с увеличением глубины.
Цифровой блок обработки, преобразования и запоминания сигналов 4 предназначен для обработки сигналов, поступающих из каналов фильтрации с целью вычисления глубины акустических неоднородностей по результатам измерения времени задержки эхо-сигналов, оценки уровня амплитуд эхо-сигналов на всех глубинах при каждом положении сканирующего луча ультразвукового сканера, преобразования координат и амплитуд принятых эхо-сигналов и, наконец, для запоминания цветных кадров изображения с целью обеспечить их считывание с темпом, соответствующим частоте кадров цветного дисплея 5.
В качестве блока управления 6 и цифрового блока обработки, преобразования и запоминания сигналов 4 могут быть использованы аналогичные блоки, входящие в состав серийно выпускаемых ультразвуковых сканеров (например, фирм “Алока”, “Филипс” или российской фирмы “ИзоМед”).
Цветной дисплей 5 осуществляет визуализацию акустических кадров, сформированных блоком обработки, преобразование и запоминание сигналов 4. Применим любой стандартный телевизионный или компьютерный дисплей на электронно-лучевой трубке или жидкокристаллических индикаторах.
Для управления и синхронизации работы блоков и элементов устройства используют контроллер 7, который соединен первым многоканальным выходом с многоканальным входом цифрового блока обработки, преобразования и запоминания сигналов 4.
Второй многоканальный выход контроллера 7 соединен с многоканальным входом блока управления 6, а третий выход - с третьими входами коммутаторов 3 в каналах фильтрации. В качестве контроллера 7 может быть применен аналогичный блок на базе процессоров и программ серийно выпускаемых ультразвуковых сканеров упомянутых выше фирм. Полная документация в части программного обеспечения работы контроллера 7 и устройства в целом содержится в технической документации фирмы “ИзоМед”, на которой работает заявитель (АСПИ 469.158.004).
Предлагаемый способ обработки и отображения эхо-сигналов для дифференциации биологических тканей в ультразвуковых диагностических сканерах реализуют следующим образом.
В процессе обследования пациента ультразвуковым сканером находят путем перемещения датчика прибора требуемый ракурс наблюдения, в котором полученное В-изображение позволяет наблюдать интересующую исследователя область, где необходимо осуществить дифференциацию биологических тканей, например, область молочной железы, область печени, почки и т.д.
Далее оценивают спектр принятых реализации эхо-сигналов на отдельных интервалах глубин для каждого положения луча при сканировании выделенной области, после чего формируют двумерное изображение биологических тканей, которое подобно В-изображению, но отличается от него тем, что каждый элемент изображения окрашивается с помощью цветовой палитры в зависимости от результатов оценки спектра. Различия в спектре сигналов, отображаемые в виде меняющихся цветовых оттенков, используют для дифференциации биологических тканей.
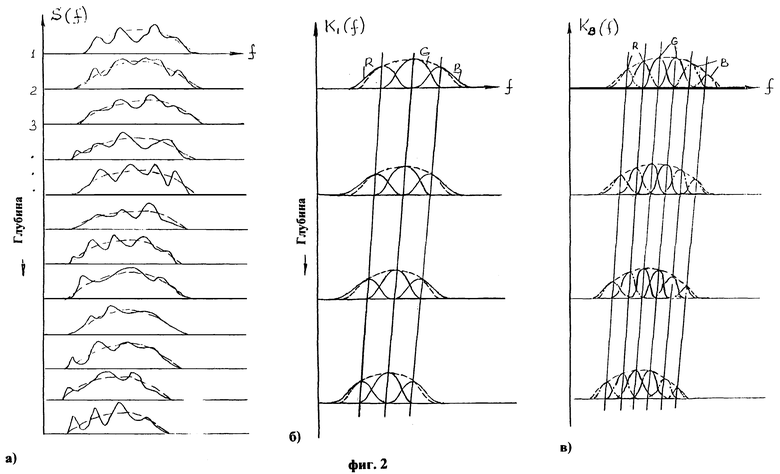
На фиг.2-а показан пример, иллюстрирующий возможные изменения спектра сигнала S (f) (сплошные линии) на различных участках глубины по мере ее увеличения (номера 1, 2 и т.д. графиков спектра соответствуют увеличивающейся глубине). Сглаженный спектр (пунктирные линии) смещается с глубиной в сторону нижних частот, что объясняется частотно-зависимым характером затухания ультразвуковых сигналов в биологических тканях. Неравномерности спектра относительно сглаженного значения обусловлены частотно-зависимым обратным рассеянием и, в существенно большей мере, спекл-шумом.
Для оценки спектра сигналов с целью отображения этого спектра на цветном дисплее используют три канала фильтрации, каждый из которых соответствует одному из основных каналов цветности дисплея 5: канал фильтрации R, канал фильтрации G и канал фильтрации В. На вход каналов фильтрации подают реализацию эхо-сигналов, которая расфильтровывается на три составляющие - низкочастотную (R), среднечастотную (G) и высокочастотную (В).
Разделение реализации эхо-сигналов на три составляющие (R, G и В) осуществляют с помощью перестраиваемых фильтров 1 в каждом канале фильтрации. Вид частотных характеристик K1 (f) перестраиваемых фильтров 1 для каналов фильтрации R, G и В показан на фиг.2-б (сплошные кривые). Ширину полосы для каждого перестраиваемого фильтра 1 выбирают одинаковой и меньшей, чем ширина полосы частот приемного тракта и, следовательно, ширина спектра реализации эхо-сигналов на входе (штриховой кривой на фиг.2-а показана ширина полосы частот приемного тракта). Расстановку центральных частот и ширину полосы частот перестраиваемых фильтров 1 выбирают такими, чтобы их суммарная ширина полосы была не меньше, чем ширина спектра эхо-сигналов на входе.
Пропущенные через три перестраиваемых фильтра 1 реализации эхо-сигналов подают на детекторы 2 и далее на коммутаторы 3.
От контроллера 7 на третьи (управляющие) входы коммутаторов 3 подают сигналы управления, которые обеспечивают прохождение сигналов с выходов детекторов 2 на входы R, G и В цифрового блока обработки, преобразования и запоминания сигналов 4. В этом блоке осуществляют обработку R, G и В составляющих сигналов, аналогичную той, которая реализуется в ультразвуковых сканерах с цветовым картированием кровотока, т.е. вычисляют время прихода и, следовательно, глубину для каждого эхо-сигнала, уровень его амплитуды, и преобразуют координаты и амплитуды принятых сигналов из системы координат, соответствующей способу сканирования, в систему координат, в которой строится изображение на цветном дисплее 5. В цифровом блоке 4 формируют кадры изображения и запоминают их на определенное время, а далее по сигналам, поступающим с первого выхода контроллера 7, обеспечивают их считывание и поступление в цветной дисплей 5 с темпом, соответствующим частоте кадров дисплея.
Отображаемое на дисплее цветное изображение содержит информацию об изменении спектра эхо-сигналов на отдельных интервалах глубины в виде изменяющихся цветовых оттенков изображения и может быть использовано для выявления различий, т.е. дифференциации биологических тканей по цветовым оттенкам. Получаемое цветовое изображение имеет ту же самую поперечную разрешающую способность, что и В-изображение, т.к. она зависит только от ширины луча. Продольная разрешающая способность (или разрешающая способность по глубине) может снижаться в результате обработки, что обусловлено несколько меньшей шириной спектра сигналов в каждом из каналов R, G и В по сравнению со спектром реализации на входе.
В описанной процедуре цветовое изображение несет в себе суммарную информацию о частотно-зависимом характере затухания и о частотно-зависимом обратном рассеянии.
Изобретение предусматривает, что для повышения информативной процедуры следует исключить влияние медленно меняющейся с глубиной составляющей частотно-зависимого затухания, для чего вводят сдвиги по центральной частоте и изменяют ширину полосы в трех перестраиваемых фильтрах 1, отслеживая медленное смещение спектра эхо-сигналов в сторону низких частот, увеличивающееся с глубиной. Сдвиги по частоте и изменение полосы в перестраиваемых фильтрах 1 осуществляют путем подачи на второй вход фильтров 1 сигналов управления от блока управления 6. Закономерность изменения параметров перестраиваемых фильтров известна, т.к. во всех современных ультразвуковых сканерах реализуют изменение полосы приема в соответствии с усредненными по различным типам тканей результатам измерения зависимости затухания от частоты ультразвука на различных глубинах. Характер изменения полосы фильтров 1 с глубиной показан на фиг.2-б: прямые сплошные линии показывают, как изменяют с глубиной центральные частоты каждого из фильтров 1 в каналах R, G и В. После устранения влияния медленного изменения смещения спектра с глубиной можно более четко наблюдать на цветной картине изменения спектра, отличные от усредненной закономерности и обусловленные различием затухания в тканях, а также частотно-зависимым обратным рассеянием, различающимся в разных биологических тканях.
С целью лучшего отображения изменения частотно-зависимого затухания и частотно-зависимого обратного рассеяния следует снизить влияние спекл-шума, которое приводит к неравномерности спектра в пределах полосы частот каждого из фильтров (см. вид спектров на фиг.2-а). С этой целью полосу частот каждого из фильтров 1 в каналах фильтрации R, G и В делят на более узкие интервалы частот с помощью узкополосных фильтров 8/1, 8/2 (и, может быть, большего количества узкополосных фильтров). На фиг.2-в показан вид частотных характеристик K8 (f) узкополосных фильтров 8/1 и 8/2 в каналах фильтрации R, G и В. Частотные характеристики узкополосных фильтров 8/1 и 8/2 смещают с глубиной так же, как и частотные характеристики перестраиваемых фильтров 1 по сигналам управления от блока управления 6. На фиг.2-в прямыми линиями обозначено смещение с глубиной центральных частот узкополосных фильтров с глубиной, отслеживающее медленное изменение спектра эхо-сигналов вследствие частотно-зависимого затухания.
Реализацию эхо-сигналов после фильтрации в узкополосных фильтрах 8/1 и 8/2 детектируют в детекторах 9/1 и 9/2 и суммируют в сумматоре 10 в каждом из каналов фильтрации.
По сигналу управления от контроллера 7 коммутатор 3 подключает (вместо выходов детекторов 2) выходы сумматоров 10 соответственно на входы R, G и В блока 4, где формируется цветовое изображение и далее отображается на цветном дисплее 5.
Обработка с использованием узкополосной фильтрации в фильтрах 8 уменьшает влияние спекл-шума в тем большей степени, чем большее число узкополосных фильтров используется в каждом канале фильтрации. Однако при этом в той же мере ухудшается разрешающая способность по глубине. По этой причине количество узкополосных фильтров 8 в каждом канале фильтрации ограничивают числом 2 или 3. Если важно иметь по возможности высокую разрешающую способность по глубине, то используют обработку с использованием фильтров 1 в каждом канале фильтрации.
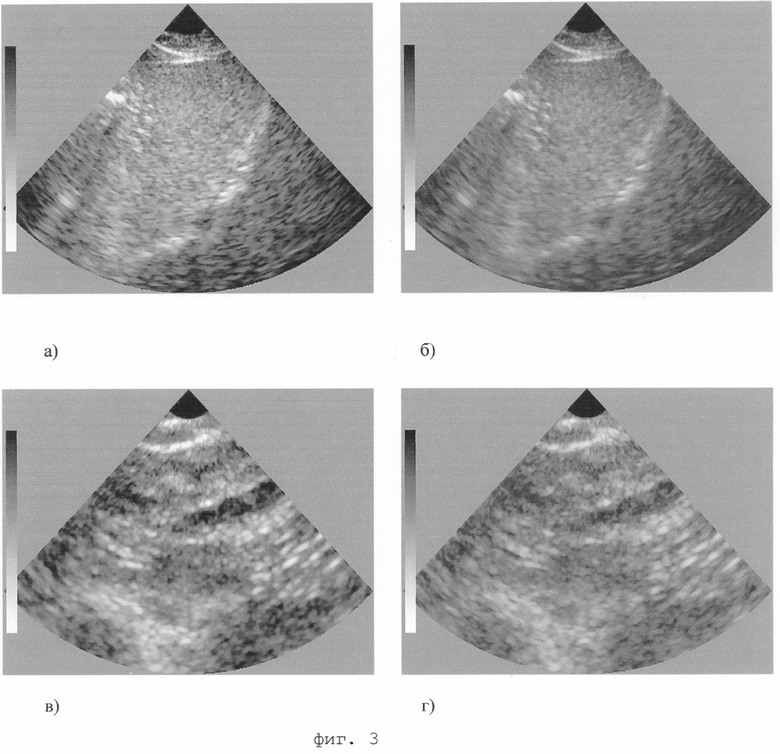
Заявителем было проведено моделирование предлагаемого способа и разработана цифровая установка, реализующая предлагаемое изобретение. На фиг.3 показаны результаты экспериментальных исследований на указанной установке. Обрабатывались реализации эхо-сигналов, получаемые в процессе сканирования печени и молочной железы.
На фиг.3-а показано обычное ультразвуковое изображение печени, а на фиг.3-б цветовое изображение той же печени, полученное в результате обработки по предлагаемому способу. На фиг.3-в дано обычное ультразвуковое изображение молочной железы, а на фиг.3-г - цветовое изображение молочной железы, полученное в результате обработки по предлагаемому способу. На цветовых изображениях можно видеть цветовые различия, позволяющие дифференцировать биологические ткани с различными свойствами. В частности, на фиг.3-б по цвету четко дифференцируется область печени (голубой оттенок). На фиг.3-г можно выделить на общем синеватом фоне области более синего и зеленоватого оттенков, которые свидетельствуют об изменении тканей, что требует дополнительных специальных исследований характера изменений тканей. Дополнительные исследования с помощью биопсийной пробы позволят определить злокачественные это изменения или нет. Таким образом, патентуемый способ обработки и отображения эхо-сигналов обеспечивает эффективное решение задачи цветовой дифференциации биологических тканей и позволяет врачу получить дополнительную диагностическую визуальную информацию о состоянии тканей пациента.
Изобретение относится к медицинской технике и может быть использовано в акушерстве и гинекологии, маммографии, онкологии, педиатрии и других медицинских областях, где применяются ультразвуковые исследования. Способ обработки и отображения эхо-сигналов для дифференциации биологических тканей в ультразвуковых диагностических сканерах включает оценку спектра эхо-сигналов и цветовое картирование сигналов на цветовом дисплее, при этом оценивают амплитудный спектр эхо-сигналов на отдельных интервалах глубин для каждого положения луча в процессе сканирования в выделенной области биологических тканей, разделяют эхо-сигналы на низкочастотную, среднечастотную и высокочастотную составляющие в трех каналах фильтрации, после чего формируют цветное двумерное изображение биологических тканей, в элементах которого отображают результаты оценки амплитудного спектра эхо-сигналов с использованием различных оттенков цветовой палитры. Использование изобретения позволяет повысить эффективность диагностических исследований за счет повышения информативности и объективности визуальной диагностики при обработке реализации эхо-сигналов и оценке их спектра на различных интервалах по глубине в каждом из лучей 3 з.п. ф-лы, 3 ил.

| ОСИПОВ Л.В | |||
| Ультразвуковые диагностические приборы | |||
| М.: ВИДАР, 1999, с.164-166 | |||
| Устройство для воспроизведения изображений в условных цветах | 1983 |
|
SU1141590A1 |
| RU 2172617 С2, 27.08.2001 | |||
| US 5226420 A, 13.07.1993 | |||
| US 5494037 A, 27.02.1996 | |||
| US 6176830 A, 23.01.2001 | |||
| US 6238342 A, 29.05.2001. | |||
Авторы
Даты
2005-06-10—Публикация
2004-04-19—Подача