Настоящая заявка притязает на приоритет по предварительной патентной заявке США № 61/426,669, поданной 23 декабря 2010 г.
Настоящее изобретение относится к системам медицинской ультразвуковой диагностики и, в частности к применению систем диагностических систем ультразвукового формирования изображений для анализа регургитационного потока митрального клапана.
Регургитационный поток является тяжелым медицинским состоянием, которое требует анализа и соответствующего лечения. Непосредственно перед сокращением левого желудочка для накачивания крови в тело митральный клапан должен полностью закрыться, чтобы сокращение вытолкнуло всю кровь в аорту. Если клапан закрывается не полностью, то некоторое количество крови, находящейся в левом желудочке, будет выталкиваться обратно в левое предсердие через отверстие в не полностью закрытом клапане. Данный обратный ток крови, представляющий собой обычно небольшую, кратковременную струю кровотока через не полностью закрытые створки клапана, уменьшает отток крови от сердца и, следовательно, снижает эффективность каждого сердечного сокращения. В таком случае, сердцу приходится быстрее качать кровь, чтобы подавать кровь для необходимого снабжения питающим кровотоком. Сердце переутомляется вследствие его неэффективности, что приводит к сердечной недостаточности.
Врачи уже много лет применяли ультразвуковое формирование изображений для обнаружения регургитационного кровотока. Ультразвуковое обнаружение клапанной регургитации сначала осуществляли путем поиска вышеупомянутой струи крови в ультразвуковом изображении левой стороны сердца. За последние двадцать лет наблюдение струи удалось облегчить благодаря двумерному (2-мерному) цветовому доплеровскому формированию изображений потока, в процессе которого высокую скорость и турбулентность небольшой струи крови обнаруживают посредством внимательного поиска упомянутых аномальных локальных скоростей крови вблизи подтекающего сердечного клапана. Однако сбор данных плоскости изображения, в которой струя является наиболее мощной, в сочетании с движением сердца и клапана и турбулентностью кровотока около митрального клапана, а также кратковременным появлением струи, осложняет упомянутый субъективный подход. В последние годы, в случаях, когда местонахождение струи можно наблюдать ультразвуковым способом, врачи применяли метод, называемый PISA, сокращение от площади проксимальной изоскоростной поверхности, для количественного определения регургитационного кровотока. При данном способе, подозрительный клапан и область внутри сердечной камеры левого желудочка (LV) и проксимальную относительно клапана формируют изображения методом цветового доплеровского картирования потока. Во время появления струи область конвергенции потока (FCR) формируется в проксимальной области, когда скорости кровотока в области мгновенно ускоряются к регургитационному отверстию. Данная схема потока приводит к искажениям дискретизации на цветовой карте потока, когда скорости потока на мгновение превышают диапазон скоростей, используемый для цветовой карты потока. В данный момент цветовая карта потока вводится и фиксируется на экране дисплея. Затем выполняется измерение скорости v на первой линии с искажениями дискретизации в области конвергенции потока (FCR), и выполняется измерение расстояния r от линии с искажениями дискретизации до предполагаемого центра отверстия клапана. Затем два данных измерения используют для вычисления объемной скорости кровотока через отверстие с использованием выражения Qt=2πr2v.
При проведении вышеописанной процедуры возникает ряд затруднений. Одно затруднение заключается в том, что максимальную точность получают, когда струю на цветовой карте потока записывают в момент ее пика. Продолжительность струи во время сердечного цикла может составлять только 300-450 миллисекунд, однако, тогда как типичная частота кадров цветовой карты потока может быть в диапазоне 10-20 кадров в секунду. Таким образом, вероятно, что время сбора данных одного из кадров цветовой карты потока не будет в точности совпадать с моментом, когда струя проходит свой пик. Врач может повторять последовательность сбора данных цветовой карты потока в течение дополнительных сердечных циклов или может вводить поправку на причины неточности при выполнении измерений не точно в момент пика струи.
Другая проблема заключается в том, что на цветовой карте потока не просто определить центр отверстия клапана. Ткань клапана создает сильные отражения ультразвука и быстро двигается, когда выполняют сканирование, и может представляться в виде большой, размытой или нечеткой массы в изображении. Таким образом, возможно, точность измерения r будет снижена из-за невозможности оценки точного местонахождения отверстия.
Третья проблема заключается в том, что базовый метод PISA включает в себя только одно одномерное измерение. Выполняют только одно измерение скорости, и в вычислении используют только один радиус r для отверстия. Способ предполагает, что остальной кровоток в области FCR имеет такие же характеристики, как при единственном измерении. Очевидно, любая неточность при выполнении единственного измерения приведет к неточному результату.
Расширение базового метода PISA, которое имеет целью устранение упомянутых неточностей, предполагает выполнение нескольких измерений скорости по дуге, определяющей внешнюю границу области FCR в двумерном изображении. От каждой точки измерения скорости измеряют расстояние r до отверстия, и несколько измерений используют для вычисления объемной скорости потока Qt. Хотя несколько измерений могут исключить зависимость от единственного неточного измерения, возникает другая проблема. Метод (1-мерный) с единственным измерением обычно исполняют путем направления центрального пучка ультразвукового датчика через верхушку сердца и непосредственно через предполагаемое регургитационное отверстие и путем выполнения измерений скорости v и расстояния r вдоль данной линии пучка. С использованием линии пучка, выставленной вышеописанным образом по упомянутому вектору регургитационного потока, измеренная скорость будет точной и не зависящей от ненулевого доплеровского угла. Как известно, ультразвуковые доплеровские измерения скорости зависят от угла между направлением потока и направлением ультразвукового пучка. Поток, который точно совпадает с направлением пучка, будет измерен точно, а поток, который направлен под ненулевым углом к направлению пучка, будет приведенным из-за умножения на косинус угла. Поток, который направлен ортогонально (90°) к направлению пучка, не создаст доплеровского отклика. Следовательно, доплеровскую скорость, измеренную ультразвуковым способом, следует корректировать в зависимости от угла между вектором потока и направлением пучка, чтобы получить более точное измерение скорости. В случае 2-мерного метода PISA, дополнительное измерения скорости по дуге области FCR будут неточными из-за изменения углов между векторами потока и направлением пучка в каждой точке, в которой выполняют измерение скорости. Таким образом, несмотря на то что несколько измерений могут компенсировать погрешность, получаемую при однократном измерении скорости, совокупность измерений даст заниженную объемную скорость потока вследствие изменения доплеровских углов в каждой точке измерения.
Еще одной проблемой, характерной для метода PISA, является недостоверность знания точного местонахождения регургитационного отверстия клапана. Как упоминалось выше, искажения дискретизации на цветовой карте потока преобладают вблизи места утечки через клапан вследствие резкого ускорения кровотока к отверстию и через него. Тем самым цветовое изображение потока забивается вспышкой паразитных цветов в доплеровском изображении вблизи отверстия.
Кроме того, плоскость митрального клапана находится в движении во время сокращения сердца. Так как точность метода PISA зависит от знания местонахождения отверстия для измерения расстояния r, то упомянутые помехи точному знанию местонахождения отверстия могут привести к неточному измерению r и, следовательно, неточному вычислению объемной скорости потока. Эксперименты показали, что погрешность всего в один миллиметр в определении местонахождения отверстия может привести к значительной погрешности при вычислении объемной скорости потока через место утечки. Кроме того, известно, что многие клапаны с регургитацией характеризуются местом утечки не в форме единственного небольшого отверстия, а местом утечки в форме щели при неточном закрытии клапана. Следовательно, предположение, что место утечки является единственным небольшим сквозным отверстием в клапане, может быть необоснованным.
В соответствии с вышеизложенным, существует необходимость в создании способа и устройства для количественного определения объемной скорости потока и объемного потока регургитации митрального клапана, которые лишены вышеописанных ограничений метода PISA. Целью настоящего изобретения является достоверная идентификация точного местонахождения регургитационного отверстия клапана. Дополнительной целью настоящего изобретения является создание комплекса измерений, которые не зависят от доплеровского угла в каждом месте измерения. Дополнительной целью настоящего изобретения является создание возможности идентификации и количественного определения регургитации митрального клапана, обусловленной наличием места утечки не в виде единственного небольшого отверстия, но также обусловленной щелью вдоль линии закрытия клапана.
В соответствии с принципами настоящего изобретения предлагаются диагностическая система ультразвукового формирования изображений и способ для количественного определения регургитационного кровотока. Определяют контуры аркообразной (двумерной) или полусферической (трехмерной) области кровотока, близкой к предполагаемому месту утечки митрального клапана на ультразвуковом изображении клапана с регургитацией. Внутренняя граница области находится непосредственно на границе или немного за границей области с искажениями дискретизации, прилегающей к отверстию утечки, и внешняя граница области находится снаружи внутренней границы и концентрично ей. Делают исходные предположения относительно регургитационного потока, в том числе относительно местонахождения регургитационного отверстия. Упомянутые предположения используют для вычисления модели поля скоростей регургитационного потока. Параметры модели корректируют в соответствии с физическими параметрами ультразвукового излучения и/или настройками ультразвуковой системы, чтобы определить ожидаемые вектора скорости, которые должны наблюдаться ультразвуковой системой VOBS в оконтуренной области. В оконтуренной области выполняют измерения скорости ультразвуковой системой, и измеренные скорости сравнивают с ожидаемыми скоростями. Вычисляют разности между измеренными и ожидаемыми значениями и, посредством подбора нелинейной аппроксимирующей кривой, вносят поправки в, по меньшей мере, одно значение модели. Процедуру итерационно повторяют вплоть до допустимого схождения ожидаемых и измеренных значений. Параметры итерационно скорректированной модели можно использовать для получения количественного измерения объемной скорости потока или местонахождения подтекающего отверстия в клапане.
В соответствии с дополнительным аспектом настоящего изобретения, исходно принятое местонахождение регургитационного отверстия на ультразвуковом изображении автоматически корректируется посредством выполнения вышеописанной процедуры, для указания фактического местонахождения отверстия на изображении. Таким образом, врачу представляется точное местонахождение регургитационного отверстия, независимо от присутствия искажений в изображении вблизи митрального клапана.
В соответствии с еще одним аспектом настоящего изобретения, вышеописанный метод повторяют в нескольких пространственных положениях вдоль митрального клапана. Совокупный регургитационный поток, измеренный в пространственных положениях, обеспечивает количественный показатель регургитационного потока, обусловленного утечкой регургитации, местом которой является щель по линии закрытия митрального клапана, а не одно подтекающее небольшое отверстие.
В соответствии с дополнительным аспектом настоящего изобретения предлагается описание характеристик нескольких фильтров выделения стенок, которые являются предпочтительными для осуществления измерения регургитационного потока в соответствии с настоящим изобретением, в том числе фильтра выделения стенок с характеристикой, которая имеет пик при промежуточных скоростях потока, которые часто обнаруживаются в области потока вблизи регургитационного отверстия.
На чертежах:
Фиг.1 - блок-схема диагностической системы ультразвукового формирования изображений, выполненной в соответствии с принципами настоящего изобретения.
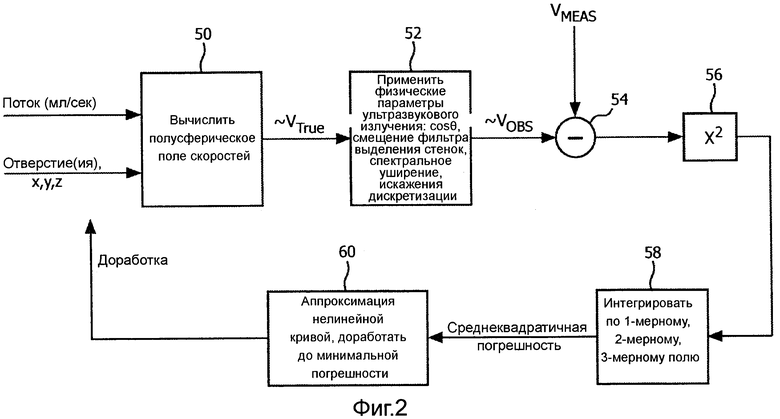
Фиг.2 - блок-схема, поясняющая функционирование процессора для вычисления потоков, показанного на фиг.1.
Фиг.3 - ультразвуковое доплеровское изображение регургитационной струи.
Фиг.4 - ультразвуковое изображение с исходно принятым местонахождением отверстия и автоматически указанным местонахождением отверстия в соответствии с настоящим изобретением.
Фиг.5 - иллюстрирует метод количественного определения регургитационного потока через щель в клапане, в соответствии с настоящим изобретением.
Фиг.6 - иллюстрирует амплитудно-частотную характеристику фильтра выделения стенок, пригодного для использования в ультразвуковой системе в соответствии с настоящим изобретением.
На фиг.1 представлена блок-схема диагностической системы ультразвукового формирования изображений, выполненной в соответствии с принципами настоящего изобретения. Как показано на фиг.1, в ультразвуковом датчике 10 обеспечена матрица 10' преобразователей для излучения ультразвуковых волн и приема эхосигнальной информации. В предпочтительном варианте, матрица 10' преобразователей является двумерной матрицей преобразовательных элементов, способных сканировать в трех измерениях, например, как по углу места, так и по азимуту около местонахождения митрального клапана, для 3-мерного формирования изображений. Матрица преобразователей соединена с формирователем 12 тонко-сфокусированных пучков в датчике, который управляет излучением и приемом сигналов элементами матрицы. Формирователи тонко-сфокусированных пучков способны, по меньшей мере, частично формировать пучок из сигналов, принятых группой или «участками» преобразовательных элементов, как подробно поясняется в патентах США 5,997,479 (Savord et al.), 6,013,032 (Savord) и 6,623,432 (Powers et al.). Формирователь тонко-сфокусированных пучков соединен кабелем датчика с переключателем 16 излучения/приема (T/R), который переключается между излучением и приемом и защищает основной формирователь 20 пучка от высокоэнергетических излучаемых сигналов. Излучение ультразвуковых пучков матрицей 10 преобразователей под управлением формирователя 12 тонко-сфокусированных пучков направляется контроллером 18 излучения, соединенным с переключателем T/R 16 и формирователем 20 пучка, который принимает данные ввода от пользователя, работающего на пользовательском интерфейсе или панели 38 управления. Одной из функций, управляемых контроллером излучения, является направление, в котором направляют пучки. Пучки могут быть направлены прямо вперед (ортогонально) от матрицы преобразователей или под разными углами для расширения поля обзора.
Сигналы, полученные методом формирования частичных пучков в формирователе 12 тонко-сфокусированных пучков, подаются в основной формирователь 20 пучка, в котором сигналы, обработанные методом формирования частичных пучков, из отдельных участков элементов объединяются в сигнал, обработанный методом формирования полного пучка. Например, основной формирователь 20 пучка может содержать 128 каналов, каждый из которых получает сигнал, обработанный методом формирования частичных пучков, от участка из 12 преобразовательных элементов. При этом сигналы, полученные более чем 1500 преобразовательными элементами двумерной матрицы, могут обеспечивать эффективный вклад в один сигнал, обработанный методом формирования пучка.
Сигналы, обработанные методом формирования пучка, подаются в сигнальный процессор 22. Сигнальный процессор 22 может обрабатывать полученные эхо-сигналы различным образом, например, полосовой фильтрацией, прореживанием, разделением на I и Q составляющие, а также выделением гармонических сигналов, которое выполняет функцию разделения линейных и нелинейных сигналов, чтобы допускать идентификацию нелинейных эхо-сигналов, отраженных от ткани и микропузырьков. Сигнальный процессор может также выполнять дополнительное повышение отношение сигнала к шуму, например, удаление спеклов, смешение сигналов и подавление шумов.
Обработанные сигналы подаются в процессор 26 B-режима и доплеровский процессор 28. Процессор 26 B-режима использует амплитудное детектирование для формирования изображений таких структур в теле, как ткань сердечной стенки, митральный клапан и клетки крови. Изображения структуры тела в B-режиме могут быть сформированы либо в режиме гармоники, либо в основном режиме, либо в режиме, сочетающем оба упомянутых режима, как поясняется в патенте США 6,283,919 (Roundhill et al.) и патенте США 6,458,083 (Jago et al.). Доплеровский процессор 28 обрабатывает различные по времени сигналы от ткани и кровотока для обнаружения движения веществ, например, потока клеток крови в поле изображения. Доплеровский процессор обычно содержит фильтр выделения стенок с параметрами, которые могут быть установлены для пропускания и/или подавления эхо-сигналов, отраженных от материалов выбранных типов в теле. Например, фильтр выделения стенок может быть настроен на такую характеристику полосы пропускания данного фильтра, чтобы пропускать сигнал с относительно низкой амплитудой от материалов с более высокой скоростью, при подавлении относительно сильных сигналов от материала с меньшей или нулевой скоростью. Данная характеристика полосы пропускания будет пропускать сигналы от протекающей крови, при подавлении сигналов от соседних неподвижных или медленно двигающихся объектов, например, стенки сердца. Обратная характеристика будет пропускать сигналы от движущейся ткани сердца, при подавлении сигналов кровотока, что применяется для так называемого доплеровского формирования изображений тканей, обнаружения и описания движения ткани. Доплеровский процессор принимает и обрабатывает последовательность различные по времени эхо-сигналы из разных точек в поле изображения, при этом последовательность эхо-сигналов от конкретной точки называется набором. Набор эхо-сигналов, принятых в быстрой последовательности в течение относительно короткого интервала, можно использовать для оценки частоты доплеровского сдвига протекающей крови, при соответствии доплеровской частоты скорости, указывающей скорость кровотока. Набор эхо-сигналов, принятых в течение более длительного периода времени, используют для оценки скорости медленнее протекающей крови или медленно движущейся ткани. Для оценки митральной регургитации быстро протекающей струи, обычно используют короткие длины наборов (меньшее число отсчетов), чтобы можно было реализовать высокую частоту кадров сбора данных. Доплеровский сдвиг Δf можно вычислить из уравнения 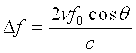
Сигналы структур и движения, формируемые процессором B-режима и доплеровским процессором, подаются в сканирующий преобразователь 32 и устройство 44 мультипланарного переформатирования. Сканирующий преобразователь упорядочивает эхо-сигналы в пространственном соотношении из того, в котором они были приняты, в требуемом формате изображения. Например, сканирующий преобразователь может упорядочивать эхо-сигнал в двумерный (2-мерный) секторный формат или пирамидальное трехмерное (3-мерное) изображение. Сканирующий преобразователь может покрывать изображение структур в B-режиме цветами, соответствующими движению в точках в поле изображения, соответствующему их скоростям, рассчитанным доплеровским методом, для получения цветовой доплеровской карты потока, которое описывает движение ткани и кровоток в поле изображения. Устройство мультипланарного переформатирования будет преобразовывать эхо-сигналы, которые приняты из точек в общей плоскости в объемной области тела, в ультразвуковое изображение данной плоскости, как поясняется в патенте США 6,443,896 (Detmer). Блок 42 объемного рендеринга преобразует эхо-сигналы набора 3-мерных данных в проектируемое 3-мерное изображение, наблюдаемое из данной начальной точки, как поясняется в патенте США № 6,530,885 (Entrekin et al.). 2-мерные или 3-мерные изображения выводятся из сканирующего преобразователя 32, устройства 44 мультипланарного переформатирования и блока 42 объемного рендеринга в процессор 30 изображений для дальнейшего улучшения, буферизации и временного хранения для отображения на дисплее 40 изображений.
В соответствии с принципами настоящего изобретения, значения скорости кровотока, полученные доплеровским процессором 28, подаются в процессор 34 для вычисления потоков. Процессор для вычисления потоков работает, как поясняется ниже, для получения количественного показателя объемной скорости потока через регургитационное отверстие, объемного потока через отверстие и пространственного местонахождения отверстия. Процессор для вычисления потоков может принимать данные ввода с панели 38 пользовательского управления, например, исходную оценку местонахождения отверстия, как поясняется ниже. Выходные данные из процессора для вычисления потоков подаются в графический процессор 36 для воспроизведения выходных данных из процессора вместе с изображением на дисплее 40. Графический процессор 36 может также формировать графические оверлеи для отображения с ультразвуковыми изображениями. Упомянутые графические оверлеи могут содержать стандартную идентификационную информацию, например имя пациента, дату и время изображения, параметры формирования изображений и т.п. С данной целью, графический процессор принимает данные ввода из пользовательского интерфейса 38, например введенное на клавиатуре имя пациента. Пользовательский интерфейс соединен также с контроллером 18 излучения для управления генерацией ультразвуковых сигналов из матрицы 10' преобразователей и, следовательно, формированием изображения, получаемого матрицей преобразователей и ультразвуковой системой. Пользовательский интерфейс соединен также с устройством 44 мультипланарного переформатирования для выбора и управления отображением нескольких мультипланарно переформатированных (MPR) изображений, которые можно использовать для количественного определения регургитационного потока в MPR изображениях, в соответствии с настоящим изобретением, как поясняется ниже.
На фиг.2 поясняется работа процессора для вычисления потоков, показанного на фиг.1. В основу процессора положена математическая модель поля скоростей потока в точках дискретизации внутри зоны включения, как поясняется ниже. В варианте осуществления с 2-мерным изображением, зона включения является, предпочтительно, изогнутой полосой, оконтуренной двумя дугами с центрами на местонахождении регургитационного отверстия, {x0, y0, z0}. В варианте осуществления с 3-мерным изображением, изогнутая полоса имеет форму полусферического слоя, как поясняется ниже в связи с фигурой 3. В предпочтительном варианте осуществления, является векторной моделью скоростей поля скоростей потока вида

или
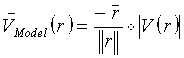
где 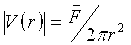
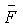
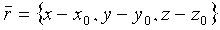
В ходе операции 50 на фиг.2 описанным образом моделируется скорость потока в каждой точке в зоне включения. Первоначально модель может начинаться с предположения или оценки значений неизвестных параметров, например потока 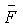
Модель поля скоростей потока аппроксимирует векторы скоростей, которые были бы точными, если бы были известны истинные вектора физиологической скорости. Вектора скоростей, аппроксимированные моделью, указаны как ~VTRUE на выходе операции 50. Затем операция 52 вводит некоторые ограничения и поправки для ~VTRUE, обусловленные такими практическими факторами, как физические свойства ультразвука и рабочие параметры используемой ультразвуковой системы. Затем модель поля скоростей потока корректируется или изменяется в масштабе для учета упомянутых практических факторов при рассмотрении фактических значений скорости, которые будут наблюдаться ультразвуковой системой. Одним из практических факторов, с учетом которого может выполняться коррекция, является доплеровский угол. Как упоминалось выше, доплеровские измерения, выполненные ультразвуковой системой, являются высокоточными только в том случае, когда направление потока совпадает с направлением ультразвукового пучка, т.е. доплеровский угол равен нулю. Для всех других углов между направлением пучка и направлением потока скорость занижается. В вышеприведенном уравнении доплеровского сдвига доплеровский угол умножается на весовой коэффициент в результате члена cosθ, где θ является доплеровским углом. Другим практическим фактором ультразвуковой системы является смещение фильтра выделения стенок. Доплеровский фильтр выделения стенок будет иметь, обычно, нелинейную характеристику, которая, для обнаружения кровотока, будет иметь нулевой отклик при постоянном сигнале (в отсутствие движения) и повышаться для максимального отклика на выбранной высокой частоте ±f. В альтернативном варианте, фильтр выделения стенок может иметь максимальный отклик на частоте, которая ниже частоты, определяемой пределом Найквиста частоты дискретизации по набору, как поясняется ниже. Отсчетный объем в теле, в котором измеряется доплеровский сдвиг, будет не одной точкой в теле, а будет иметь конечные размеры, что будет приводить к отраженным доплеровским сигналам, характеризующим диапазон скоростей. Неравномерный отклик фильтра выделения стенок может вызывать широкий разброс скоростей с получением более высокого усиления в разных местах амплитудно-частотной характеристики, например более высокие скорости выделяются сильнее, чем меньшие скорости. Данный неравномерный отклик может создать сдвиг воспринимаемого центра разброса скоростей, называемый смещением фильтра выделения стенок. Эффект смещения фильтра выделения стенок также можно учесть коррекцией модели. Другим связанным фактором, который можно учитывать, является спектральный разброс, эффект доплеровского спектрального уширения, обусловленный разными траекториями и углами из отсчетного объема к каждому приемному элементу активной апертуры матричного преобразователя. Смотри патент США 5,606,972 (Routh). Еще одним фактором, который можно учитывать, является эффект искажений дискретизации, сообщение неверных доплеровских частот и скоростей, когда движение кровотока происходит со скоростью, превышающей скорость, которую можно однозначно обнаружить по пределу Найквиста для частоты дискретизации набора эхо-сигналов. В процессе операции 52 такие факторы, как, например, вышеописанные факторы, учитываются коррекцией скалярным произведением модели поля скоростей потока, что, для вышеописанных моделей, может иметь вид

где 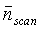
Компаратор 54 сравнивает ожидаемые значения скоростей из модели поля скоростей потока, V0BS, с фактическими измерениями скоростей в точках (отсчетных объемах) поля, VMEAS, полученными доплеровским процессором 28. В ходе операции 56, разности между ожидаемыми и принятыми значениями возводятся в квадрат для получения члена погрешности для каждой точки. Члены погрешности интегрируются по всей зоне включения, которая может быть одномерной (например, 1-мерной линией), двумерной (например, 2-мерной аркообразной зоной) или трехмерной (например, 3-мерным полусферическим слоем) зоной включения, чтобы получить член среднеквадратической погрешности для всей зоны. Затем член погрешности служит для коррекции таких параметров модели поля, как r и объемная скорость потока, чтобы обеспечить уменьшение измеряемого впоследствии члена погрешности. Предпочтительный метод коррекции заключается в использовании аппроксимации нелинейной кривой для доработки модели в сторону уменьшения погрешности. Один подобный метод аппроксимации нелинейной кривой, которым можно воспользоваться, представлен алгоритмом Левенберга-Марквардта, который уточняет координаты местонахождения регургитационного отверстия и поток 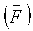
Цикл на фиг.2 итерационно повторяется для уменьшения члена погрешности. С каждым проходом цикла более точно доработанная модель корректируется и сравнивается с измерениями скорости ультразвука из зоны приема, и член погрешности итерационно уменьшается. Когда член погрешности уменьшен до допустимого низкого значения, модель представляет собой требуемые фактические измерения местонахождения отверстия и кровотока через отверстие. Упомянутые члены и, по желанию, другие формируются как выходные данные процессором 34 для вычисления потоков и представляются на дисплее для пользователя.
На фиг.3 представлено схематичное 2-мерное ультразвуковое изображение, поясняющее практическое применение настоящего изобретения для измерения регургитации митрального клапана. Линия 100 представляет плоскость митрального клапана, на которой существует место утечки регургитации в виде отверстия O. Когда левый желудочек сокращается, струя крови 102 истекает обратно в правое предсердие. По способу PISA, данную струю зондировали бы доплеровским пучком 110, продолжающимся через отверстие O. В патенте США 6,719,697 (Li) предложено усовершенствование метода PISA, в соответствии с которым формируется цветное отображение M-режима в течение сердечного цикла из местоположения доплеровского пучка 110. Дисплейный процессор для цветового доплеровского картирования настроен на пределы отображения, указанные контрольной цветной полосой 120 с правой стороны изображения, продолжающейся из центральной начальной точки нулевой скорости (BK=черный) к +V и -V максимальным скоростям в противоположных направлениях. Диапазон цветов (Y=желтый; DR-темно-красный и т.п.) отображается в соответствии с данным диапазоном скоростей. Искажения дискретизации возникают, когда измеряемая скорость превышает пределы Найквиста +V и -V. Непосредственно вблизи отверстия находится область 104 конвергенции потока (FCR). За пределами области конвергенции потока находится зона 112 приема (S), используемая в варианте осуществления настоящего изобретения.
В основу как метода PISA, так и настоящего изобретения положено предположение, что регургитационный поток в левом желудочке вблизи отверстия сходится и протекает к местонахождению O отверстия. Упомянутое схождение показано векторами 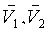
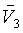
Цветовое доплеровское изображение области FCR 104 будет хаотичной и непостоянной. Данный эффект объясняется тем, что пространственная ориентация клеток крови и скорости кровотока изменяются в данной области очень быстро по мере того, как кровоток изменяет направление и немедленно ускоряется к отверстию O во время систолического сокращения. Отсчеты набора, полученные во время данного интервала, часто не коррелируются между собой, что нарушает корреляцию внутри набора, которая положена в основу обычных процессоров, выполняющих доплеровские расчеты. В результате, даже если поток в области FCR может быть, в основном, ламинарным, цветовое отображение потока может быть таким, как для сильно турбулентного потока с искажениями дискретизации. Внутреннюю границу 108 зоны S приема устанавливают, предпочтительно, за пределами области 104 конвергенции потока, чтобы исключить использование непостоянных оценок скорости из области FCR. Один подход к установке границы 108 заключается в установке границы на или за пределами границы сдвига скорости. Такой подход можно реализовать визуально по отображению цветовой карты потоков или автоматически, по отношению к порогу сдвига скорости.
Внешнюю границу 106 зоны приема можно установить в зависимости от измеримых скоростей. Хотя скорости регургитационного потока вблизи отверстия являются относительно высокими, упомянутые скорости постепенно уменьшаются с увеличением расстояний от отверстия. Внешнюю границу 106 можно установить на таком расстоянии от отверстия O, на котором все еще можно надежно измерять небольшие доплеровские скорости. В данном случае, решение можно принимать в зависимости от процента от предела Найквиста или в зависимости от низкой скорости потока, например, 5 мм/сек. Тем самым внешнюю границу 106 можно установить на расстоянии, на котором доплеровским процессором еще можно обеспечить приемлемую чувствительность к низкоскоростным потокам.
Зона 112 приема в примере, представленном на фиг.3, изображена в виде двумерной дугообразной зоны S с центром поворота на отверстии O. Настоящее изобретение можно использовать в одном, двух или трех измерениях. Одномерные вариант осуществления и модель могут рассматривать только сегмент линии 110 пучка, который находится, например, между дугами 108 и 106. Двумерный вариант осуществления будет вариантом, в котором дискретизируется зона приема, которая является плоской, например, зона 112 приема, показанная на фиг.3. Трехмерный вариант осуществления будет рассматривать дугообразную зону приема, например 112, но в полной полусфере с центром на отверстии. Предполагается, что с использованием двух- и трехмерных вариантов осуществления будет обеспечиваться более высокая точность. Предпочтительный вариант осуществления будет использовать датчик для 3-мерной визуализации с двумерным матричным преобразователем, показанным на фиг.1, со сбором данных и моделированием, выполняемыми в полусферическом или четвертьсферическом объемном слое вокруг отверстия. При двумерной визуализации можно реализовать более высокие частоты кадров, и, в данном случае, кадр MPR изображения через отверстие и струю можно выбирать из объема, сканированного датчиком для 3-мерной визуализации, с использованием устройства 44 мультипланарного переформатирования. Искомую плоскость можно многократно сканировать с высокой частотой кадров сбора данных, и измерения скоростей и вычисления потоков можно выполнять с двумерной зоной приема, показанной на 2-мерном MPR изображении.
Несмотря на то что, как показано на фиг.3, могут существовать зоны приема, из которых поток сходится к отверстию по круговой схеме, в некоторых случаях, как выяснилось, схемы должны быть другими, некруговыми. Иначе говоря, вектора потока, направленные к отверстию, могут располагаться по схеме, отличающейся от дуги точной окружности. Вместо круговой формы, показанной на фиг.3, зона приема может иметь параболическую или уплощенную круговую форму. В трехмерных вариантах осуществления, зона приема может быть параболоидным или сплющенным сфероидным слоем. Форма зоны приема, то есть зона или объем, в которой(ом) скорости измеряют и сравнивают с моделью, может динамически изменяться во время итерационных проходов по циклу обработки информации, показанному на фиг.2, так что процедура будет адаптироваться и сходиться к зоне приема с формой, измененной в сравнении с формой, использованной в исходной модели.
Как упоминалось выше, врачу часто трудно точно определить местонахождение очень маленького регургитационного отверстия на ультразвуковом изображении. Когда сердце не сокращается, отверстие отсутствует, и когда отверстие присутствует, его местонахождение искажено артефактами формирования изображений, обусловленными образующейся, в результате, турбулентностью, например, артефактами вблизи области конвергенции потока. В соответствии с дополнительным аспектом настоящего изобретения, в одном варианте осуществления настоящего изобретения возможно автоматическое указание местонахождения подтекающего отверстия на ультразвуковом изображении. На фиг.4 показано ультразвуковое изображение, на котором элементам, ранее описанным в связи с фиг.3, присвоены те же самые числовые позиции. Данное изображение содержит также небольшую рамку 130, которая наложена на изображение врачом в начале диагностики, чтобы указать предполагаемое местонахождение регургитационного отверстия. Врач манипулирует элементом управления на панели 38 управления, например трекболом, чтобы поместить пиктограмму 130 в местонахождении на изображении, где, как полагает врач, находится отверстие. Координаты указанной пиктограммы 130 отверстия используют для начала обработки в процессоре для вычисления потоков, показанном на фиг.2, а именно координаты используются как исходные координаты отверстия в математической модели на операции 50. Процессор 34 итерационно уточняет смоделированные значения векторов скоростей потока, направленные к местонахождению отверстия, в ответ на прием измеренных значений VMEAS скоростей. Как оказалось, вертикальное размещение местонахождения отверстия оказывает сильнейшее влияния на схождение смоделированных векторов скоростей с измеренными значениями скоростей. Хотя сердце сокращается во время систолы, перемещение сокращения вызывает вертикальное перемещение митрального клапана на изображении к центру левого желудочка. Таким образом, естественное сократительное перемещение сердца может быть источником максимальной ошибки при оценке регургитационного потока. Процессор 34 итерационно уточняет местонахождение отверстия, чтобы уменьшить погрешность различия между измеренными и оценочными значениями скоростей в поле скоростей потока (зоне S приема) между границами 106 и 108. Когда процессор для вычисления потоков выполняет итерации для приближения к истинным координатам отверстия, окончательно вычисленные координаты используются процессором 34 для вычисления потоков и графическим процессором 36 для автоматического перемещения пиктограммы 130 отверстия к вычисленным координатам в изображении. В альтернативном варианте, графический процессор будет помещать другую (вычисленную) пиктограмму 132 отверстия на дисплее в местонахождении с истинными координатами, вычисленном посредством итерационной коррекции модели. Как упоминалось выше, всего 1-мм неточность размещения отверстие может значительно повлиять на вычисления объемной скорости потока через отверстие и объемного потока, при этом объемный поток является интегралом объемной скорости потока по времени, в течение которого сокращается сердце (приблизительно, 1/3 от сердечного цикла). Объемный поток будет достигать пика, приблизительно, в середине периода систолы. На фиг.4 показано, что система поместила вычисленную пиктограмму 132 отверстия в его истинном местонахождении в поле изображения, которое отличается от исходной оценки врачом местонахождения отверстия. Когда ультразвуковое исследование выполняют с 2-мерным формированием изображений, координаты отверстия будут находиться в прямоугольной системе координат (x, y, z). Когда применяют 3-мерное формирование изображений, то, обычно, будут использовать сферическую (r, θ, φ) систему координат. Кроме того, как видно из ультразвукового изображения на фиг.4, на отображаемом ультразвуковом изображении графически оконтурена зона S приема, и любая вышеописанная модификация формы зоны приема включается в отображаемую форму и графическое оконтуривание зоны приема на дисплее.
Как упоминалось выше, регургитационные отверстия не всегда существуют как места утечек в форме единственного небольшого отверстия в закрытом клапане. Места утечек могут создаваться щелевыми отверстиями или несколькими местами небольших утечек. На фиг.5 поясняется вариант осуществления настоящего изобретения для оценки объемной скорости потока и объемного потока через щели и несколько мест утечки по линии закрытия клапана. Как показано на фиг.5, процедура в соответствии с настоящим изобретением выполняется для группы местонахождений отверстий, упорядоченных вдоль подтекающего митрального клапана 100'. Упомянутые отдельные местонахождения небольших отверстий можно использовать для моделирования комплексных щелевидных отверстий или нескольких отверстий в закрытом клапане. На фиг.5 показан пример трех подобных определений, каждое с собственной зоной приема, обозначенной внешней границей 106, 106' и 106" зоны, и своими векторами потока (указанными небольшими стрелками), направленными для схождения к разным местонахождениям отверстий вдоль клапана 100'. Векторное поле скоростей, соответствующее каждому небольшому отверстию, векторно суммируется с полями других отверстий таким образом, что устанавливаются границы одной комбинированной зоны приема, вместе с одним комбинированным векторным полем скоростей. Для нескольких отверстий, теперь комбинированное векторное поле скоростей аппроксимирует истинные физиологические вектора скоростей (~Vtrue, данные на выходе операции 50, показанные на фиг.2). Обработка комбинированного векторного поля скоростей определяет объемную скорость потока или объемный поток всех небольших отверстий, соответствующих всей щели вдоль линии закрытия митрального клапана. Хотя на фиг.5 приведен пример векторного поля скоростей, созданного тремя небольшими отверстиями, для соответствующего моделирования щели можно применить любое число отверстий. Зоны приема, используемые для каждого измерения можно объединять, как показано на фиг.5, так как поток, который определяют для суммируемых отверстий, является векторным потоком, направленным к однозначно определяемому отверстию или положению вдоль щели. В трехмерном варианте осуществления, линия измерений не ограничена прямой линией в плане, но может проходить по нелинейной траектории закрытия створок митрального клапана.
На фиг.6 показаны амплитудно-частотные характеристики двух доплеровских фильтров выделения стенок, которые можно использовать в варианте осуществления настоящего изобретения. Координаты по оси абсцисс графика на фиг.6 представлены в единицах пределов Найквиста фильтра выделения стенок из дискретизированных данных, где пределы +1 и -1 являются нормированными пределами Найквиста фильтра, соответствующего скоростям кровотока. Нулевое состояние (постоянного сигнала или в отсутствие потока) находится в центре. Координаты по оси ординат указывают относительную амплитудную характеристику характеристики фильтра. Характеристическая кривая 140 является типичной характеристической кривой фильтра выделения стенок для измерения кровотока и может быть использована в варианте осуществления настоящего изобретения. Приведенная характеристика имеет нулевой отклик в центре, что имеет следствием отсутствие отклика на неподвижные объекты, например, неподвижные стенки сосудов. Как показано, отклик монотонно возрастает по мере того, как кривая продолжается от нуля, с максимальным откликом на пределах Найквиста для потоков с максимальной скоростью, обнаруживаемых без искажений дискретизации при выбранном интервале дискретизации. В результате, приведенная амплитудно-частотная характеристика наиболее чувствительна к потоку с максимальными скоростями потока.
Характеристическая кривая 150 является кривой, которую часто предпочитают для фильтра выделения стенок в соответствии с вариантом осуществления настоящего изобретения. Как можно видеть, отклик данной кривой 150 имеет пик при относительно высокой, но промежуточной частоте дискретизации немного выше ±0,5 частоты Найквиста, предпочтительно, в диапазоне от 1/2 до 2/3 частоты Найквиста, и снижается до нулевого отклика на пределах Найквиста. Приведенная характеристика фильтра предназначена для повышения чувствительности к меньшим скоростям потока, которые можно ожидать около внешней границы 106 зоны S приема. Приведенная характеристика полезна для смещения низкой чувствительности к низкоскоростному потоку, который получается из коротких наборов, обычно используемых для цветового картирования потока регургитационного потока. Данный подход можно наблюдать как более высокий отклик кривой 150 при меньших скоростях ближе к центру графика. Хотя видно, что кривая 150 снижается до нуля на пределах Найквиста, данная потеря чувствительности к высоким скоростям, в общем, допускается в обмен на повышение чувствительности к низкоскоростным потокам.




Изобретение относится к медицинской технике, а именно к средствам для оценки регургитационного потока. Система содержит ультразвуковой датчик, содержащий матрицу преобразователей, процессор изображений, доплеровский процессор, процессор для вычисления потоков, выполненный с возможностью создания модели поля скоростей потока около местонахождения регургитационного потока и устройство отображения. Способ содержит этапы, на которых формируют изображения местонахождения регургитационного потока, создают модель поля скоростей потока, получают доплеровские ультразвуковые измерения скорости кровотока, сравнивают аппроксимированные значения скоростей потока, полученные из модели, корректируют параметр модели и отображают местонахождение регургитационного потока. Изобретение позволяет улучшить точность местонахождения регургитационного отверстия клапана. 2 н. и 15 з.п. ф-лы, 6 ил. 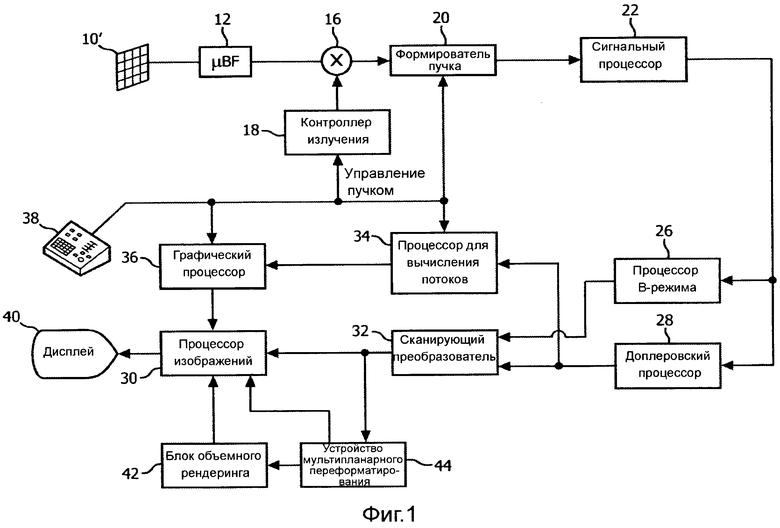
1. Диагностическая ультразвуковая система для измерения регургитационного потока, содержащая:
ультразвуковой датчик, содержащий матрицу преобразователей для излучения ультразвуковой энергии по направлению к местонахождению регургитационного потока в теле и приема ультразвуковых эхо-сигналов из упомянутого места;
процессор изображений, чувствительный к принятым эхо-сигналам, для формирования ультразвукового изображения местонахождения регургитационного потока;
доплеровский процессор, чувствительный к принятым эхо-сигналам, для формирования доплеровских ультразвуковых измерений скорости кровотока около местонахождения регургитационного потока;
процессор для вычисления потоков, выполненный с возможностью создания модели поля скоростей потока около местонахождения регургитационного потока, сравнения аппроксимированных значений скоростей потока, полученных из модели, с измерениями скорости, сформированными доплеровским процессором, и коррекции модели по результату сравнения; и
устройство отображения, соединенное с процессором изображений и процессором для вычисления потоков, для отображения ультразвукового изображения местонахождения регургитационного потока и измерения потока, полученного из скорректированной модели поля скоростей потока.
2. Диагностическая ультразвуковая система по п. 1, в которой процессор для вычисления потоков дополнительно выполнен с возможностью коррекции аппроксимированных значений скоростей потока с учетом факторов, встречающихся при использовании ультразвуковой системы для измерения скорости.
3. Диагностическая ультразвуковая система по п. 2, в которой факторы содержат, по меньшей мере, один из эффектов, обусловленных физическими параметрами ультразвукового излучения и рабочими параметрами ультразвуковой системы, используемой для измерения скорости.
4. Диагностическая ультразвуковая система по п. 3, в которой один из факторов содержит доплеровский угол.
5. Диагностическая ультразвуковая система по п. 3, в которой один из факторов содержит смещение фильтра выделения стенок.
6. Диагностическая ультразвуковая система по п. 3, в которой один из факторов содержит доплеровское спектральное уширение.
7. Диагностическая ультразвуковая система по п. 3, в которой один из факторов содержит эффекты искажений дискретизации.
8. Диагностическая ультразвуковая система по п. 1, в которой поле скоростей потока содержит зону приема около отверстия, при этом зона приема характеризуется двумерной дугообразной формой.
9. Диагностическая ультразвуковая система по п. 1, в которой поле скоростей потока содержит зону приема около отверстия, при этом зона приема характеризуется трехмерной полусферической формой.
10. Диагностическая ультразвуковая система по п. 1, в которой коррекция модели по результату сравнения содержит коррекцию аппроксимированных значений скоростей потока, полученных из модели.
11. Диагностическая ультразвуковая система по п. 1, в которой коррекция модели по результату сравнения содержит коррекцию формы поля скоростей потока.
12. Диагностическая ультразвуковая система по п. 11, в которой скорректированная форма поля скоростей потока содержит одну из параболической формы, уплощенной круглой формы, параболоида или сплющенного сфероида.
13. Диагностическая ультразвуковая система по п. 1, в которой коррекция модели по результату сравнения содержит коррекцию местонахождения или расстояния до регургитационного отверстия.
14. Способ оценки регургитационного потока ультразвуковой системой, при этом способ содержит следующие этапы:
формируют изображения, ультразвуковым датчиком и процессором изображений, местонахождение регургитационного потока в теле;
создают модель поля скоростей потока около местонахождения регургитационного потока;
создают доплеровские ультразвуковые измерения скорости кровотока около местонахождения регургитационного потока;
сравнивают аппроксимированные значения скоростей потока, полученные из модели, с доплеровскими ультразвуковыми измерениями скорости кровотока;
корректируют, по меньшей мере, параметр модели по результату сравнения; и
отображают ультразвуковое изображение местонахождения регургитационного потока и измерения потока, полученного из параметра скорректированной модели.
15. Способ по п. 14, дополнительно содержащий этап коррекции модели поля скоростей потока с учетом влияния, по меньшей мере, одного из физических параметров ультразвукового излучения или рабочего параметра ультразвуковой системы перед этапом сравнения.
16. Способ по п. 14, в котором этап создания дополнительно содержит создание модели дугообразного поля скоростей потока, находящегося около регургитационного отверстия.
17. Способ по п. 14, в котором этап создания дополнительно содержит создание модели полусферического поля скоростей потока, находящегося около регургитационного отверстия.
| US 6719697 B2, 13.04.2004 | |||
| US 4913159 A, 03.04.1990 | |||
| US 6620103 B1, 16.09.2003 | |||
| Ультразвуковой импульсно-допплеровский измеритель скорости кровотока | 1984 |
|
SU1178411A1 |
Авторы
Даты
2015-11-27—Публикация
2011-12-16—Подача