Область техники
Настоящее изобретение относится к бензопирановым производным, обладающим пролонгированным действием в рефрактерный период, которые могут использоваться для лечения аритмии у млекопитающих, включая человека.
Предпосылки изобретения
В качестве бензопирановых производных были известны 4-ациламинобензопирановые производные, описанные Cromakalim (японская выложенная заявка No. Sho 58-67683). Известно, что эти 4-ациламинобензопирановые производные, описанные Cromakalim, открывают ATP чувствительный K+ канал и являются эффективными для лечения гипертонии и астмы, но не было никаких упроминаний о возможности лечения аритмии на основе пролонгированного действия в рефрактерный период.
В настоящее время известно, что обычные антиаримические средства, обладающие в качестве основной функции пролонгированным действием в рефрактерный период (такие как I класс лекарственных средств по классификации антиаримических средств согласно Vaughan Williams, или d-солатол (d-sotalol), относящийся к III классу) обладают сильными вызывающими опасную аритмию воздействиями, что может приводить к внезапной смерти, такими как трепетание-мерцание желудочков на основе возможности продолжительного воздействия на мышцы желудочка в процессе, относящемся к пролонгированному действию в рефрактерный период, что стало терапевтической проблемой. Таким образом, желательными являются средства, обладающие меньшими побочными эффектами.
Описание изобретения
Авторы настоящего изобретения провели интенсивный поиск и исследование соединений, обладающих пролонгированным действием в рефрактерный период, более избирательным по отношению к мышце предсердия, чем к мышце желудочка, и обнаружили, что соединение формулы (1) обладает пролонгированным действием, избирательным по отношению к мышце предсердия без какого-либо влияния на рефрактерный период и сильного действия на мышцу желудочка.
Авторы настоящего изобретения активно исследовали бензопирановые производные, и неожиданно обнаружили, что соединение формулы (1) обладает сильным пролонгированным действием в рефрактерный период и что они могут использоваться в качестве антиаритмического средства. Настоящее изобретение было разработано на основании этого открытия.
Настоящее изобретение относится к бензопирановому производному формулы (1)
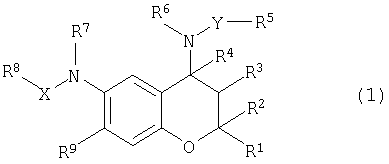
где R1 и R2 представляют собой, каждый, независимо, атом водорода или C1-6алкильную группу, в которой указанная алкильная группа может быть необязательно замещена атомом галогена, гидроксильной группой или C1-6алкоксильной группой, и где указанная алкоксильная группа может быть необязательно замещена атомом фтора,
R3 представляет собой гидроксильную группу или C1-6алкилкарбонилоксигруппу,
R4 представляет собой атом водорода или R3 и R4 вместе образуют связь,
R6 представляет собой атом водорода,
R7 представляет собой атом водорода или C1-6алкильную группу,
X отсутствует или представляет собой C=O или SO2,
R8 представляет собой атом водорода или C1-6алкильную группу, в которой указанная алкильная группа может быть необязательно замещена гидроксильной группой или C1-6алкоксильной группой,
R9 представляет собой атом водорода или нитрогруппу,
когда R9 представляет собой атом водорода,
Y представляет собой C3-8алкиленовую группу или группу -(CH2)m-CR11R12-(CH2)n-, в которой m и n равны, каждый, независимо, 0, 1, 2, 3 или 4, и m+n равно или больше 2; когда m равно 0, R11 и R12 представляют собой, каждый, независимо, C1-6алкильную группу, и когда m иной, чем 0, R11 и R12 представляют собой, каждый, независимо, C1-6алкильную группу или гидроксильную группу, или R11 и R12 вместе образуют атом кислорода,
R5 представляет собой атом фтора, трифторметильную группу, аминогруппу, C1-6алкилтиогруппу, C1-6алкиламиногруппу, ди-C1-6алкиламиногруппу, C1-6алкилкарбониламиногруппу, C1-6алкилсульфониламиногруппу, аминокарбонильную группу, C1-6алкиламинокарбонильную группу, ди-C1-6алкиламинокарбонильную группу, C1-6алкилкарбонильную группу, C1-6алкоксикарбонильную группу, C1-6алкоксикарбониламиногруппу, аминосульфонильную группу, C1-6алкилсульфонильную группу, карбоксильную группу или бензоильную группу, в которой указанная бензоильная группа может быть необязательно замещена C1-6алкильной группой, C1-6алкоксильной группой, атомом галогена, нитрогруппой или цианогруппой, и
когда R9 представляет собой нитрогруппу,
Y представляет собой C4-8алкиленовую группу, группу -(CH2)m-CR11R12-(CH2)n- в которой m, n, R11 и R12 такие, как указано выше, или группу -(CH2)0-O-(CH2)P-, в которой о и p равны, каждый, независимо, 2, 3 или 4,
R5 представляет собой атом водорода, атом фтора, трифторметил группу, гидроксильную группу, формамидную группу, аминогруппу, C1-6алкоксильную группу, C3-8циклоалкильную группу, C1-6алкилтиогруппу, C1-6алкиламиногруппу, ди-C1-6алкиламиногруппу, C1-6алкилкарбониламиногруппу, C1-6алкилсульфониламиногруппу,аминокарбонильную группу, C1-6алкиламинокарбонильную группу, ди-C1-6алкиламинокарбонильную группу, C1-6алкилкарбонильную группу, C1-6алкоксикарбонильную группу, C1-6 алкоксикарбониламиногруппу, аминосульфонильную группу, C1-6алкилсульфонильную группу, карбоксильную группу или бензоильную группу, в которой указанная бензоильная группа может быть необязательно замещена C1-6алкильной группой, C1-6алкоксильной группой, атомом галогена, нитро группой или циано группой; или его фармацевтически приемлемая соль.
Соединение по настоящему изобретению обладает сильным пролонгированным действием в рефрактерный период и может быть использовано в качестве лекарственного средства для лечения аритмии.
Соответствующие заместители для соединения (1) по настоящему изобретению конкретно проиллюстрированы следующим образом.
Здесь, "н" означает нормальный, "изо" означает изо, "сек" означает вторичный, "трет" означает третичный, "цикло" означает цикло, и "п" означает пара.
В качестве C1-6алкильных групп могут быть указаны метил, этил, н-пропил, изо-пропил и циклопропил, и так далее.
В качестве C1-6алкильных групп могут быть указаны метил, этил, н-пропил, изо-пропил, циклопропил, н-бутил, изо-бутил, втор-бутил, трет-бутил, циклобутил, 1-пентил, 2-пентил, 3-пентил, изо-пентил, неопентил, 2,2-диметилпропил, циклопентил, 1-гексил, 2-гексил, 3-гексил, 1-метил-н-пентил, 1,1,2-триметил-н-пропил, 1,2,2-триметил-н-пропил, 3,3-диметил-н-бутил и циклогексил, и так далее. Предпочтительно, могут быть указаны метил, этил, н-пропил, изо-пропил и н-бутил.
В качестве атомов галогенов могут быть указаны атом фтора, атом хлора, атом брома и атом иода. Предпочтительно, могут быть указаны атом фтора, атом хлора и атом брома.
В качестве C1-6алкоксильных групп могут быть указаны метокси, этокси, н-пропокси, изо-пропокси, н-бутокси, изо-бутокси, втор-бутокси, трет-бутокси, 1-пентилокси, 2-пентилокси, 3-пентилокси, изопентилокси, неопентилокси, 2,2-диметилпропокси, 1-гексилокси, 2-гексилокси, 3-гексилокси, 1-метил-н-пентилокси, 1,1,2-триметил-н-пропокси, 1,2,2-триметил-н-пропокси и 3,3-диметил-н-бутокси, и так далее. Предпочтительно, могут быть указаны метокси, этокси, н-пропокси и изопропокси.
В качестве C4-8алкиленовых групп могут быть указаны бутилен, пентилен, гексилен, гептилен и октилен, и так далее. Предпочтительно может быть указан пентилен.
В качестве C3-8алкиленовых групп может быть указан пропилен, в добавление к вышеуказанным C4-8алкиленовым группам. Предпочтительно, может быть указан пентилен.
В качестве C1-6алкилкарбонилоксигрупп могут быть указаны метилкарбонилокси, этилкарбонилокси, н-пропилкарбонилокси, изопропилкарбонилокси, н-бутилкарбонилокси, изобутилкарбонилокси, втор-бутилкарбонилокси, трет-бутилкарбонилокси, 1-пентилкарбонилокси, 2-пентилкарбонилокси, 3-пентилкарбонилокси, изопентилкарбонилокси, неопентилкарбонилокси, трет-пентилкарбонилокси, 1-гексилкарбонилокси, 2-гексилкарбонилокси, 3-гексилкарбонилокси, 1-метил-н-пентилкарбонилокси, 1,1,2-триметил-н-пропилкарбонилокси, 1,2,2-триметил-н-пропилкарбонилокси и 3,3-диметил-н-бутилкарбонилокси, и так далее. Предпочтительно, могут быть указаны метилкарбонилокси, этилкарбонилокси, н-пропилкарбонилокси, изопропилкарбонилокси, н-бутилкарбонилокси и трет-бутилкарбонилокси.
В качестве C3-8циклоалкильных групп могут быть указаны циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил, и так далее. Предпочтительно, могут быть указаны циклопропил, циклобутил и циклогексил.
В качестве C1-6алкилтиогрупп могут быть указаны метилтио, этилтио, н-пропилтио, изопропилтио, циклопропилтио, н-бутилтио, изобутилтио, втор-бутилтио, трет-бутилтио, циклобутилтио, 1-пентилтио, 2-пентилтио, 3-пентилтио, изопентилтио, неопентилтио, трет-пентилтио, циклопентилтио, 1-гексилтио, 2-гексилтио, 3-гексилтио, циклогексилтио, 1-метил-н-пентилтио, 1,1,2-триметил-н-пропилтио, 1,2,2-триметил-н-пропилтио и 3,3-диметил-н-бутилтио, и так далее. Предпочтительно, могут быть указаны метилтио, этилтио, н-пропилтио, изопропилтио и н-бутилтио.
В качестве C1-6алкиламиногрупп могут быть указаны метиламино, этиламино, н-пропиламино, изопропиламино, циклопропиламино, н-бутиламино, изобутиламино, втор-бутиламино, трет-бутиламино, циклобутиламино, 1-пентиламино, 2-пентиламино, 3-пентиламино, изопентиламино, неопентиламино, трет-пентиламино, циклопентиламино, 1-гексиламино, 2-гексиламино, 3-гексиламино, циклогексиламино, 1-метил-н-пентиламино, 1,1,2-триметил-н-пропиламино, 1,2,2-триметил-н-пропиламино и 3,3-диметил-н-бутиламино, и так далее. Предпочтительно, могут быть указаны метиламино, этиламино, н-пропиламино, изопропиламино и н-бутиламино.
В качестве ди-C1-6алкиламиногрупп могут быть указаны диметиламино, диэтиламино, ди-н-пропиламино, диизопропиламино, дициклопропиламино, ди-н-бутиламино, диизобутиламино, ди-втор-бутиламино, ди-трет-бутиламино, дициклобутиламино, ди-1-пентиламино, ди-2-пентиламино, ди-3-пентиламино, диизопентиламино, ди-неопентиламино, ди-трет-пентиламино, дициклопентиламино, ди-1-гексиламино, ди-2-гексиламино, ди-3-гексиламино, дициклогексиламино, ди-(1-метил-н-пентил)амино, ди-(1,1,2-триметил-н-пропил)амино, ди-(1,2,2-триметил-н-пропил)амино, ди-(3,3-диметил-н-бутил)амино, метил-(этил)амино, метил(н-пропил)амино, метил(изопропил)амино, метил(циклопропил)амино, метил(н-бутил)амино, метил(изобутил)амино, метил(втор-бутил)амино, метил(трет-бутил)амино, метил(циклобутил)амино, этил(н-пропил)амино, этил(изопропил)амино, этил(циклопропил)амино, этил(н-бутил)амино, этил(изобутил)амино, этил(втор-бутил)амино, этил(трет-бутил)амино, этил(циклобутил)амино, н-пропил(изопропил)амино, н-пропил(циклопропил)амино, н-пропил(н-бутил)амино, н-пропил(изобутил)амино, н-пропил(втор-бутил)амино, н-пропил(трет-бутил)амино, н-пропил(циклобутил)амино, изопропил(циклопропил)амино, изопропил(н-бутил)амино, изопропил(изо-бутил)амино, изопропил(втор-бутил)амино, изопропил(трет-бутил)амино, изопропил(циклобутил)амино, циклопропил(н-бутил)амино, циклопропил(изо-бутил)амино, циклопропил(втор-бутил)амино, циклопропил(трет-бутил)амино, циклопропил(циклобутил)амино, н-бутил(изобутил)амино, н-бутил(втор-бутил)амино, н-бутил(трет-бутил)амино, н-бутил(циклобутил)амино, изобутил(втор-бутил)амино, изобутил(трет-бутил)амино, изобутил(циклобутил)амино, втор-бутил(трет-бутил)амино, втор-бутил(циклобутил)амино и трет-бутил(циклобутил)амино, и так далее. Предпочтительно, могут быть указаны диметиламино, диэтиламино, ди-н-пропиламино, диизопропиламино и ди-н-бутиламино.
В качестве C1-6алкилкарбониламиногрупп могут быть указаны метилкарбониламино, этилкарбониламино, н-пропилкарбониламино, изопропилкарбониламино, н-бутилкарбониламино, изобутилкарбониламино, втор-бутилкарбониламино, трет-бутилкарбониламино, 1-пентилкарбониламино, 2-пентилкарбониламино, 3-фенилкарбониламино, изопентилкарбониламино, неопентилкарбониламино, трет-пентилкарбониламино, 1-гексилкарбониламино, 2-гексилкарбониламино и 3-гексилкарбониламино, и так далее. Предпочтительно, могут быть указаны метилкарбониламино, этилкарбониламино, н-пропилкарбониламино, изопропилкарбониламино и н-бутилкарбониламино.
В качестве C1-6алкилсульфониламино групп могут быть указаны метилсульфониламино, этилсульфониламино, н-пропилсульфониламино, изопропилсульфониламино, н-бутилсульфониламино, изобутилсульфониламино, втор-бутилсульфониламино, трет-бутилсульфониламино, 1-пентилсульфониламино, 2-пентилсульфониламино, 3-пентилсульфониламино, изопентилсульфониламино, неопентилсульфониламино, трет-пентилсульфониламино, 1-гексилсульфониламино, 2-гексилсульфониламино и 3-гексилсульфониламино, и так далее. Предпочтительно, могут быть указаны метилсульфониламино, этилсульфониламино, н-пропилсульфониламино, изопропилсульфониламино и н-бутилсульфониламино.
В качестве C1-6алкиламинокарбонильных групп могут быть указаны метиламинокарбонил, этиламинокарбонил, н-пропиламинокарбонил, изопропиламинокарбонил, н-бутиламинокарбонил, изобутиламинокарбонил, втор-бутиламинокарбонил, трет-бутиламинокарбонил, 1-пентиламинокарбонил, 2-пентиламинокарбонил, 3-пентиламинокарбонил, изопентиламинокарбонил, неопентиламинокарбонил, трет-пентиламинокарбонил, 1-гексиламинокарбонил, 2-гексиламинокарбонил и 3-гексиламинокарбонил, и так далее. Предпочтительно, могут быть указаны метиламинокарбонил, этиламинокарбонил, н-пропиламинокарбонил, изопропиламинокарбонил и н-бутиламинокарбонил.
В качестве ди-C1-6алкиламинокарбонильных групп могут быть указаны диметиламинокарбонил, диэтиламинокарбонил, ди-н-пропиламинокарбонил, диизопропиламинокарбонил, дициклопропиламинокарбонил, ди-н-бутиламинокарбонил, диизобутиламинокарбонил, ди-втор-бутиламинокарбонил, ди-трет-бутиламинокарбонил, дициклобутиламинокарбонил, ди-1-пентиламинокарбонил, ди-2-пентиламинокарбонил, ди-3-пентиламинокарбонил, диизопентиламинокарбонил, ди-неопентиламинокарбонил, ди-трет-пентиламинокарбонил, дициклопентиламинокарбонил, ди-1-гексиламинокарбонил, ди-2-гексиламинокарбонил и ди-3-гексиламинокарбонил, и так далее. Предпочтительно, могут быть указаны диметиламинокарбонил, диэтиламинокарбонил, ди-н-пропиламинокарбонил, диизопропиламинокарбонил, дициклопропиламинокарбонил и ди-н-бутиламинокарбонил.
В качестве C1-6алкилкарбонильных групп могут быть указаны метилкарбонил, этилкарбонил, н-пропилкарбонил, изопропилкарбонил, н-бутилкарбонил, изобутилкарбонил, втор-бутилкарбонил, трет-бутилкарбонил, 1-пентилкарбонил, 2-пентилкарбонил, 3-пентилкарбонил, изопентилкарбонил, неопентилкарбонил, трет-пентилкарбонил, 1-гексилкарбонил, 2-гексилкарбонил и 3-гексилкарбонил. Предпочтительно, могут быть указаны метилкарбонил, этилкарбонил, н-пропилкарбонил, изопропилкарбонил и н-бутилкарбонил.
В качестве C1-6алкоксикарбонильных групп могут быть указаны метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, н-бутоксикарбонил, изобутоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, 1-пентилоксикарбонил, 2-пентилоксикарбонил, 3-пентилоксикарбонил, изопентилоксикарбонил, неопентилоксикарбонил, трет-пентилоксикарбонил, 1-гексилоксикарбонил, 2-гексилоксикарбонил и 3-гексилоксикарбонил, и так далее. Предпочтительно, могут быть указаны метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, н-бутоксикарбонил, изобутоксикарбонил, втор-бутоксикарбонил и трет-бутоксикарбонил.
В качестве C1-6алкоксикарбониламиногрупп могут быть указаны метоксикарбониламино, этоксикарбониламино, н-пропоксикарбониламино, изопропоксикарбониламино, н-бутоксикарбониламино, изобутоксикарбониламино, втор-бутоксикарбониламино, трет-бутоксикарбониламино, 1-пентилоксикарбониламино, 2-пентилоксикарбониламино, 3-пентилоксикарбониламино, изопентилоксикарбониламино, неопентилоксикарбониламино, трет-пентилоксикарбониламино, 1-гексилоксикарбониламино, 2-гексилоксикарбониламино и 3-гексилоксикарбониламино, и так далее. Предпочтительно, могут быть указаны метоксикарбониламино, этоксикарбониламино, н-пропоксикарбониламино, изопропоксикарбониламино, н-бутоксикарбониламино, изобутоксикарбониламино, втор-бутоксикарбониламино и трет-бутоксикарбониламино.
В качестве C1-6алкилсульфонильных групп могут быть указаны метансульфонил и этансульфонил.
В качестве предпочтительного соединения, используемого в настоящем изобретение, могут быть указаны следующие соединения.
(1) Бензопирановое производное формулы (I) или его фармацевтически приемлемая соль, где R1 и R2 представляют собой метильную группу, R3 представляет собой гидроксильную группу и R4 представляет собой атом водорода.
(2) Бензопирановое производное или его фармацевтически приемлемая соль в соответствии с вышеуказанным (1), где X представляет собой C=O, R7 представляет собой атом водорода, R8 представляет собой метильную группу.
(3) Бензопирановое производное или его фармацевтически приемлемая соль в соответствии с вышеуказанным (1), где X отсутствует, R7 и R8 представляют собой атом водорода.
(4) Бензопирановое производное или его фармацевтически приемлемая соль в соответствии с вышеуказанным (2), где R9 представляет собой атом водорода.
(5) Бензопирановое производное или его фармацевтически приемлемая соль в соответствии с вышеуказанным (2), где R9 представляет собой нитрогруппу.
(6) Бензопирановое производное или его фармацевтически приемлемая соль в соответствии с вышеуказанным (3), где R9 представляет собой атом водорода.
(7) Бензопирановое производное или его фармацевтически приемлемая соль в соответствии с вышеуказанным (3), где R9 представляет собой нитрогруппу.
Конкретные примеры соединений, которые могут использоваться по настоящему изобертению, показаны далее, но настоящее изобретение ими не ограничивается. Здесь "Me" означает метильную группу, "Et" означает этильную группу, "Pr" означает пропильную группу, "Bu" означает бутильную группу, "Pen" означает пентильную группу, "Hex" означает гексильную группу, "Ac" означает ацетильную группу (COCH3), "Ph" означает фенильную группу, "n" означает нормальный, "i" означает изо, "t" означает третичный и "c" означает цикло соответственно.

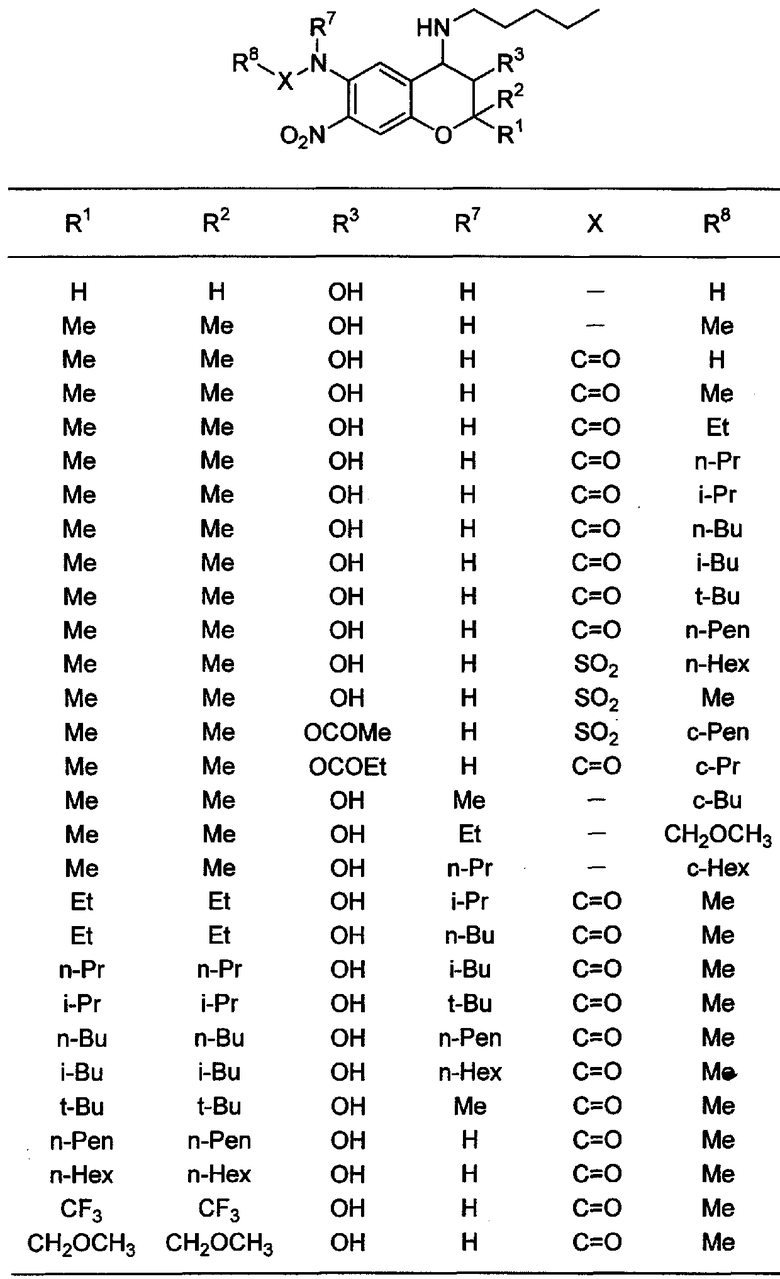
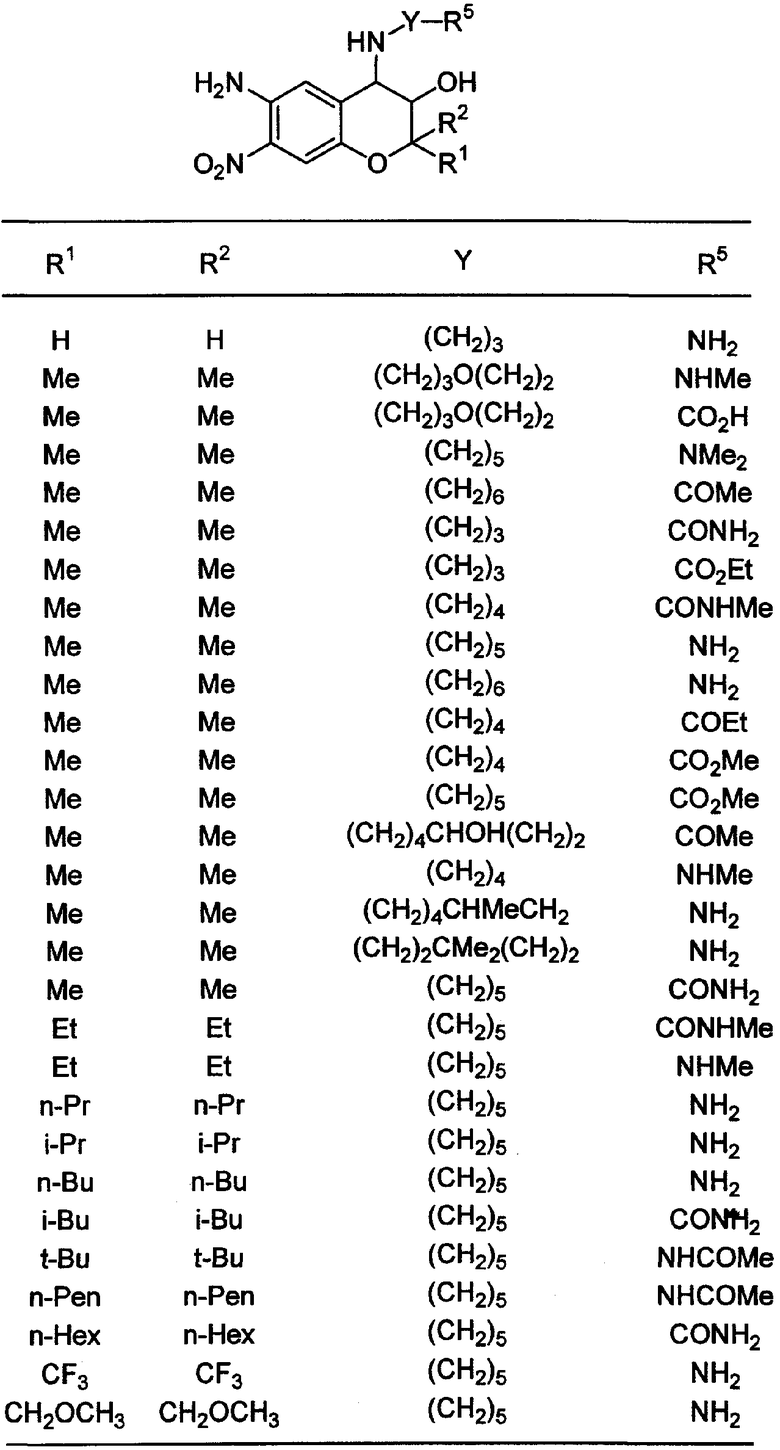


Соединение по настоящему изобретению содержит асимметрические атомы углерода, поэтому существуют оптические изомеры на основе асимметрических атомов углерода, которые могут использоваться в заявке настоящего изобретения подобно рацематам. Кроме того, могут быть включеы цис- и трансизомеры на основе конфигурации в 3-положении и в 4-положении, но трансизомер является предпочтительным.
Далее, когда соединения могут образовывать соли, в качестве активных компонентов могут также использоваться их фармацевтически приемлемые соли.
В качестве фармацевтически приемлемых солей могут быть указаны гидрохлориды, гидробромиды, сульфаты, метансульфонаты, ацетаты, бензоаты, тартраты, фосфаты, лактаты, малеаты, фумараты, малаты, глюконаты и салицилаты и так далее. Предпочтительно, могут быть указаны гидрохлориды, метансульфонаты и малеаты.
Затем проиллюстрирован способ получения соединения по настоящему изобретению.
Такие соединения общей формулы (1), где R4 представляет собой атом водорода и R3 представляет собой гидроксильную группу, которые представляют собой соединения формулы (1-a), могут быть получены путем взаимодействия соединения общей формулы (2) с соединением (3) в инертном растворителе, как показано на следующей реакционной схеме.
Соединение общей формулы (2) может быть синтезировано извествнми способами (способы, описанные J. M. Evans et al., J. Med. Chem. 1984, 27, 1127; J. Med. Chem. 1986, 29, 2194; J. T. North et al., J. Org. Chem. 1995, 60, 3397; а также в японской выложенной заявке на патент No. Sho 56-57785, японской выложенной заявке на патент No. Sho 56-57786, японской выложенной заявке на патент No. Sho 58-188880, японской выложенной заявке на патент No. Hei 2-141, японской выложенной заявке на патент No. Hei 10-87650 и японской выложенной заявке на патент No. Hei 11-209366, и так далее).
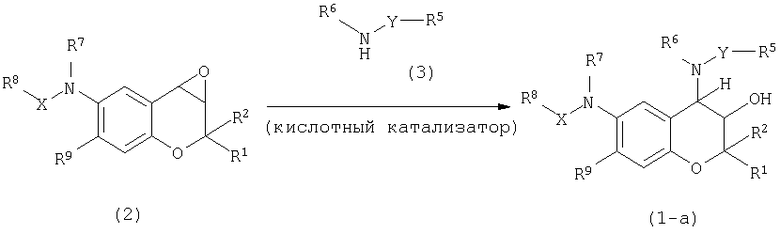
В качестве растворителей, используемых при взаимодействии соединения общей формулы (2) с соединением (3), могут быть указаны следующие.
Могут быть указаны растворители сульфоксидного типа, например диметилсульфоксид; растворители амидного типа, например диметилформамид и диметилацетамид; растворители эфирного типа, например диэтиловый эфир, диметоксиэтан и тетрагидрофуран; растворители галогенового типа, например дихлорметан, хлороформ и дихлорэтан; растворители нитрильного типа, например ацетонитрил и пропионитрил; растворители типа ароматических углеводородов, например бензол и толуол; растворители углеводородного типа, например гексан и гептан; и растворители сложноэифрного типа, например этилацетат. Кроме того, взаимодействие можно проводить и в отсутствие растворителя. Предпочтительно, могут быть указаны растворители эфирного типа и растворители нитрильного типа.
Температура реакции обычно составляет от -80°C до температуры кипения реакционного растворителя, предпочтительно от -10 до 100°C.
Мольное соотношение реакционных продуктов находится в интервале 0,5-20,0, предпочтительно 1,0-10,0, для отношения соединение (3)/соединение (2).
В реакции могут быть использованы кислотные катализаторы.
В качестве используемых кислотных катализаторов могут быть указаны неорганические кислоты, например хлористоводородная кислота и серная кислота, и кислоты Льюиса, например хлорид алюминия, тетрахлорид титана, комплекс трифторид бора с диэтиловым эфиром, перхлорная кислота, перхлорат лития, бромид лития и трифторметансульфонат иттербия, и так далее. Предпочтительно, могут быть указаны бромид лития, перхлорная кислота и перхлорат лития.
Такие соединения общей формулы (1), которые отличаются от соединения формулы (1-a) (соединения, где R3 и R4 вместе образуют связь, и соединения, где R4 представляет собой атом водорода и R3 представляет собой C1-6 алкилкарбонилоксигруппу) могут быть получены способами, подобными описанным в японской выложенной заявке на патент No. Sho 52-91866 и японской выложенной заявке на патент No. Hei 10-87650, и так далее.
Синтез оптически активных соединений общей формулы (I) может быть достигнут с помощью методов оптического разделения (японская выложенная заявка на патент No. Hei 3-141286, патент США No. 5097037 и европейский патент No. 409165). Кроме того, синтез оптически активных соединений общей формулы (2) может быть достигнут с помощью методов ассиметрического синтеза (японская национальная публикация No. Hei 5-507645, японская выложенная заявка на патент No. Hei 5-301878, японская выложенная заявка на патент No. Hei 7-285983, европейская выложенная заявка на патент No. 535377 и патент США No. 5420314).
Как описано выше, авторы настоящего изобретения обнаружили, что соединение формулы (1) обладает сильным пролонгированным действием в рефрактерный период. Пролонгированное действие в рефрактерный период представляет собой одну из функций антиаритмического действия иявляется важнымпоказателем возможности экстраполирования на эффективность при клинической аритмии. Обычные антиаритмические средства, обладающие в качестве главной функции сильным пролонгированным действием в рефрактерный период (такие как d-солатол, относящийся III классу по классификации антиаритмических средств по Vaughan Williams), обладают сильными, вызывающими опасную аритмию воздействиями, что может приводить к внезапной смерти, такими как трепетание-мерцание желудочков на основе возможности продолжительного воздействия на мышцы желудочка в процессе, относящемся к пролонгированному действию в рефрактерный период, что является терапевтическими проблемами в случае аритмии, связанной с предсердием (такой как суправентрикулярная тахикардия, трепетание предсердий и мерцательная артмия). Для решения этих проблем авторы настоящего изобретения провели поиски соединений, обладающих пролонгированным действием в рефрактерный период, более избирательным по отношению к мышце предсердия, чем к мышце желудочка, и обнаружили, что соединение формулы (1) обладает пролонгированным действием в рефрактерный период, избирательным по отношению к мышце предсердия без какого-либо влияния на рефрактерный период и сильного воздействия на мышцу желудочка. Отличие полученных авторами настоящего изобретения данных и известных методов состоит в проявлении указанными соединениями пролонгированного действия в рефрактерный период, избирательном по отношению к мышце предсердия, что продемонстрировано следующими фактами: нет влияния на действующий возможный поддерживающий период удаленной желудочковой мышцы, и нет влияния на QT электрокардиограммы анестезированного животного. Согласно вышесказанному соединения по настоящему изобретению не обладают индуцирующим аритмию действием на мышцу желудочка, поэтому они могут обеспечить большую по сравнению с известными методами безопасность при использовании в случае аритмии связанной с мышцей предсердия. Эти методы могут использоваться в терапевтических или профилактических целях в качестве средств против мерцательной артмии, средств против трепетания предсердия и средств против тахикардии предсердия, связанных с пароксизмальной, хронической, предоперационной, операционной или постоперационной аритмией предсердия, для профилактики развития эмбола, основанного на аритмии, профилактики развития желудочковой аримии или тахикардии, вызванной аритмией или тахикардией предсердия, и профилактики прогнозируемого ухудшения уровня жизни, основанной на предупреждающем воздействии на аритмию или тахикардию предсердия, которые могут развиваться при желудочковой аритмии или тахикардии.
Настоящее изобретение относится к фармацевтической композиции или к ветеринарной фармацевтической композиции, содержащей соединение общей формулы (I) в эффективном для лечения количестве.
В качестве путей введения соединения по настоящему изобретению могут быть указаны парентеральное введение посредством инъекций (подкожные, внутривенные, внутримышечные и внутрибрюшинные инъекции), мазей, суппозиториев и аэрозоля, и пероральное введение посредством таблеток, капсул, гранул, пилюль, сиропов, растворов, эмульсий и суспензий, и так далее.
Вышеуказанные фармацевтическая композиция или ветеринарная фармацевтическая композиция содержат соединение по настоящему изобретению в количестве около 0,01-99,5%, предпочтительно около 0,1-30% от всей массы композиции. Помимо соединения по настоящему изобретению или композиции содержащей соединение, в состав могут входить другие фармацевтические или ветеринарные фармацевтические активные соединения. Кроме того, эти композиции могут содержать несколько соединений по настоящему изобретению.
Клинически вводимое количество соединения по настоящему изобретению изменяется в зависимости от возраста, веса и восприимчивости пациента, продолжительности состояния и так далее, и эффективным вводимым количеством является обычно около 0,003-1,5 г, предпочтительно 0,01-0,6 г в день для взрослого. Если необходимо, однако, может быть использовано количесто, выходящее за рамки вышеуказанного.
Препараты для введения, содержащие соединение по настоящему изобретению, получают обычными фармацевтическими способами.
То есть, таблетки, капсулы, гранулы и пилюли для перорального введения получают, используя эксципиенты, такие как сахароза, лактоза, глюкоза, крахмал и маннит; связующие, такие как гидроксипропилцеллюлоза, сироп, гуммиарабик, желатин, сорбит, трагакант, метилцеллюлоза и поливинилпирролидон; разрыхлители, такие как крахмал, карбоксиметил целлюлоза или ее кальциевая соль, микрокристаллическая целлюлоза и полиэтиленгликоль; лабриканты, такие как тальк, стеарат магния или кальция и диоксид кремния; смазывающие агенты, такие как лаурат натрия и глицерин, и так далее.
Инъекции, растворы, эмульсии, суспензии, сиропы и аэрозоли готовят с использованием растворителей для активных соединений, таких как вода, этиловый спирт, изопропиловый спирт, пропиленгликоль, 1,3-бутиленгликоль и полиэтиленгликоль; поверхностно-активные вещества, такие как сорбитановый эфир жирной кислоты, полиоксиэтиленсорбитановый эфир жирной кислоты, полиоксиэтиленовый эфир жирной кислоты, полиоксиэтиленовый эфир гидрированного касторового масла и лецитин; суспендирующие агенты, такие карбоксиметил натриевая соль, производные целлюлозы, такие как метилцеллюлоза, трагакант, и природные каучуки, такие как гуммиарабик; и консерванты, такие как эфиры п-гидроксибензойной кислоты, хлорид бензалкония и соли сорбиновой кислоты, и так далее.
Для мазей, которые являются адсорбируемыми чрезкожно лекарственными препаратами, используют, например, белый вазелин, жидкий парафин, высшие спирты, мази Macrogol, гидрофильные мази и основы типа водных гелей, и так далее.
Суппозитории получают, используя, например, масло какао, полиэтиленгликоль, ланолин, триглицерид жирной кислоты, кокосовое масло и полисорбат и так далее.
Наилучший способ практического воплощения изобретения
Настоящее изобретение проиллюстрировано подробно следующими примерами, но этими примерами настоящее изобретение не ограничивается.
Здесь, в следующих формулах, "Boc" означает трет-бутоксикарбонильную группу.
[Примеры получения]
Пример получения 1
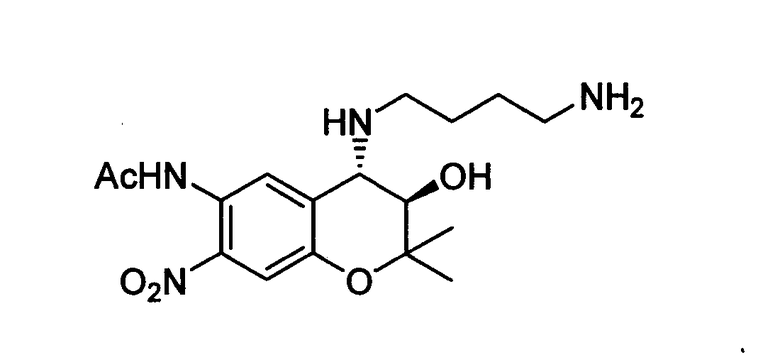
(3R*,4S*)-6-ацетиламино-3,4-дигидро-2,2-диметил-7-нитро-4-н-пентиламино-2H-1-бензопиран-3-ол
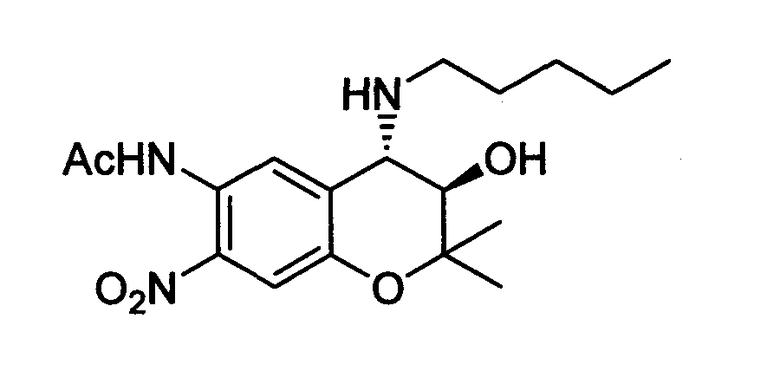
К раствору 1,0 г (3,59 ммоль) (+)-(3R*,4R*)-6-ацетамид-3,4-эпокси-3,4-дигидро-2,2-диметил-7-нитро-2H-1-бензопирана (приблизительно 99% эи) и перхлората лития (1,53 г, 14,36 ммоль) в ацетонитриле (10 мл), при комнатной температуре добавляют н-пентиламин (0,942 мл, 7,18 ммоль) и перемешивают при 65°C в течение 3 часов. После добавления насыщенного водного раствора бикарбоната натрия и экстракции этилацетатом, нагревают с насыщенным водным раствором хлорида натрия и сушат над безводным сульфатом магния. Очищают хроматографией на колонке с силикагелем (Hex/AcOEt = 1/2) и получают желаемое вещество с 60%-ным выходом. Желтое аморфное вещество.
1H-ЯМР (CDCl3)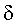 : 0,89 (т, J = 7,0 Гц, 3H), 1,22 (с, 3Н), 1,30-1,36 (м, 4Н), 1,52 (с, 3Н), 1,48-1,56 (м, 2H), 2,55-2,71 (м, 2H), 3,57 (д, J = 10,1 Гц, 1H), 3,70 (д, J = 10,1 Гц, 1H), 7,62 (с, 1H), 8,68 (с, 1H), 10,02 (с, 1H).
: 0,89 (т, J = 7,0 Гц, 3H), 1,22 (с, 3Н), 1,30-1,36 (м, 4Н), 1,52 (с, 3Н), 1,48-1,56 (м, 2H), 2,55-2,71 (м, 2H), 3,57 (д, J = 10,1 Гц, 1H), 3,70 (д, J = 10,1 Гц, 1H), 7,62 (с, 1H), 8,68 (с, 1H), 10,02 (с, 1H).
МС (ЭИ) m/z; 365 [M]+, 308, 293 (bp).
Следующие соединения были получены подобным же образом (примеры получения 2-7).
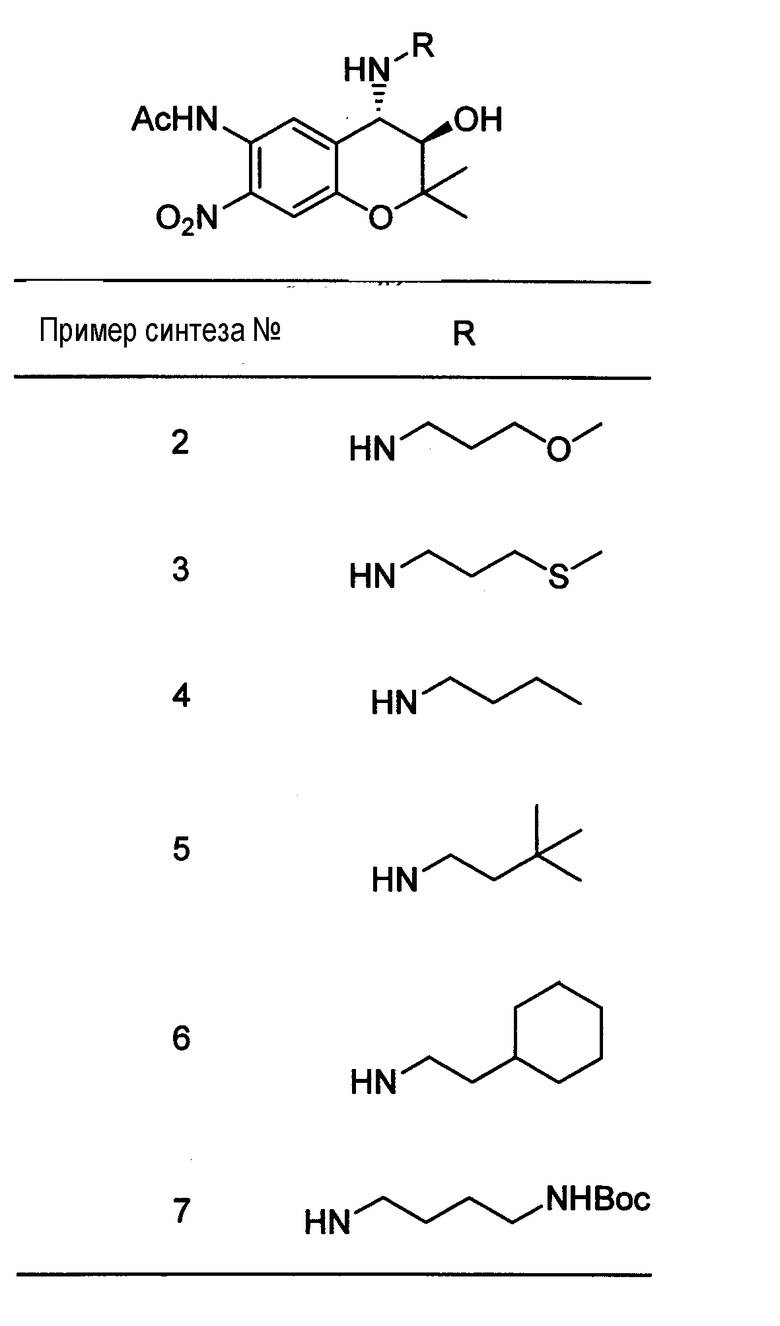
Пример получения 2
56 %-ный выход.
Желтое аморфное вещество.
1Н-ЯМР (CDCl3)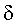 : 1,21 (с, 3Н), 1,52 (с, 3Н), 1,70 (с, 2Н), 1,79 (квинт, J= 6,1 Гц, 2Н), 2,26 (с, 3Н), 2,70-2,85 (м, 2Н), 3,36 (с, 3Н), 3,54 (т, J= 5,8 Гц, 2H), 3,58 (д, J = 10,3 Гц, 1Н), 3,71 (д, J= 10,3 Гц, 1H), 7,62 (с, 1H), 8,68 (с, 1Н), 10,00 (с, 1H). МС (ЭИ) m/z; 367 [M]+, 297 (bp).
: 1,21 (с, 3Н), 1,52 (с, 3Н), 1,70 (с, 2Н), 1,79 (квинт, J= 6,1 Гц, 2Н), 2,26 (с, 3Н), 2,70-2,85 (м, 2Н), 3,36 (с, 3Н), 3,54 (т, J= 5,8 Гц, 2H), 3,58 (д, J = 10,3 Гц, 1Н), 3,71 (д, J= 10,3 Гц, 1H), 7,62 (с, 1H), 8,68 (с, 1Н), 10,00 (с, 1H). МС (ЭИ) m/z; 367 [M]+, 297 (bp).
Пример получения 3
23 %-ный выход.
Желтое маслянистое вещество.
1Н-ЯМР (CDCl3)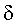 : 1,22 (с, 3Н), 1,53 (с, 3Н), 1,62 (с, 2Н), 1,83 (квинт, J = 6,8 Гц, 2Н), 2,10 (с, 3H), 2,26 (с, 3H), 2,63 (т, J = 7,0 Гц, 2Н), 2,68-2,86 (м, 2H), 3,60 (д, J = 10,2 Гц, 1H), 3,72 (д, J= 10,2 Гц, 1H), 7,63 (с, 1H), 8,70 (с, 1H), 10,01 (с, 1H).
: 1,22 (с, 3Н), 1,53 (с, 3Н), 1,62 (с, 2Н), 1,83 (квинт, J = 6,8 Гц, 2Н), 2,10 (с, 3H), 2,26 (с, 3H), 2,63 (т, J = 7,0 Гц, 2Н), 2,68-2,86 (м, 2H), 3,60 (д, J = 10,2 Гц, 1H), 3,72 (д, J= 10,2 Гц, 1H), 7,63 (с, 1H), 8,70 (с, 1H), 10,01 (с, 1H).
МС (ЭИ) m/z; 383 [M]+, 220 (bp).
Пример получения 4
93 %-ный выход.
Красное маслянистое вещество.
1Н-ЯМР (CDCl3)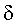 : 0,92 (т, J= 7,2 Гц, 3Н), 1,21 (с, 3Н), 1,33-1,60 (м, 4H), 1,52 (с, 3H), 2,27 (с, 3H), 2,56-2,72 (м, 2H), 3,56 (д, J = 10,2 Гц, 1H), 3,71 (д, J= 10,2 Гц, 1H), 7,63 (с, 1H), 8,68 (с, 1H), 10,03 (с, 1H).
: 0,92 (т, J= 7,2 Гц, 3Н), 1,21 (с, 3Н), 1,33-1,60 (м, 4H), 1,52 (с, 3H), 2,27 (с, 3H), 2,56-2,72 (м, 2H), 3,56 (д, J = 10,2 Гц, 1H), 3,71 (д, J= 10,2 Гц, 1H), 7,63 (с, 1H), 8,68 (с, 1H), 10,03 (с, 1H).
МС (ЭИ) m/z; 353 [M]+, 263,222 (bp).
Пример получения 5
96 %-ный выход.
Красное аморфное вещество.
1Н-ЯМР (CDCl3)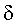 : 0,89 (с, 9H), 1,21 (с, 3H), 1,46 (т, J= 8,1 Гц, 2Н), 1,53 (с, 3H), 2,27 (с, 3H), 2,53-2,72 (м, 2H), 3,69 (д, J= 10,2 Гц, 1H), 3,71 (д, J= 10,2 Гц, 1H), 7,63 (с, 1H), 8,68 (с, 1H), 10,02 (с, 1H).
: 0,89 (с, 9H), 1,21 (с, 3H), 1,46 (т, J= 8,1 Гц, 2Н), 1,53 (с, 3H), 2,27 (с, 3H), 2,53-2,72 (м, 2H), 3,69 (д, J= 10,2 Гц, 1H), 3,71 (д, J= 10,2 Гц, 1H), 7,63 (с, 1H), 8,68 (с, 1H), 10,02 (с, 1H).
МС (ЭИ) m/z; 379 [M]+, 260, 146 (bp).
Пример получения 6
89 %-ный выход.
Желтые кристаллы.
т.пл. 210,0-212,0°С
1Н-ЯМР (CDCl3)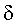 : 0,85-1,90 (м, 13Н), 1,18 (с, 3Н), 1,54 (с, 3Н), 2,25 (с, 3Н), 2,76-2,85 (м, 1H), 3,08-3,18 (м, 1H), 4,05 (д, J = 8,8 Гц, 1H), 4,59 (д, J = 8,8 Гц, 1H), 7,68 (с, 1H), 8,78 (с, 1H), 9,77 (с, 1H).
: 0,85-1,90 (м, 13Н), 1,18 (с, 3Н), 1,54 (с, 3Н), 2,25 (с, 3Н), 2,76-2,85 (м, 1H), 3,08-3,18 (м, 1H), 4,05 (д, J = 8,8 Гц, 1H), 4,59 (д, J = 8,8 Гц, 1H), 7,68 (с, 1H), 8,78 (с, 1H), 9,77 (с, 1H).
МС (ЭИ) m/z; 405 [M]+, 335, 292 (bp).
Пример получения 7
98 %-ный выход.
Красное маслянистое вещество.
1Н-ЯМР (CDCl3)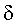 : 1,21 (с, 3H), 1,44 (с, 9H), 1,52 (с, 3H), 1,52-1,61 (м, 2H), 1,63-1,74 (м, 2H), 2,27 (с, 3H), 2,58-2,71 (м, 2H), 3,07-3,16 (м, 2H), 3,60 (д, J = 10,1 Гц, 1H), 3,73 (д, J= 10,1 Гц, 1H), 7,63 (с, 1H), 8,68 (с, 1H), 10,00 (с, 1H).
: 1,21 (с, 3H), 1,44 (с, 9H), 1,52 (с, 3H), 1,52-1,61 (м, 2H), 1,63-1,74 (м, 2H), 2,27 (с, 3H), 2,58-2,71 (м, 2H), 3,07-3,16 (м, 2H), 3,60 (д, J = 10,1 Гц, 1H), 3,73 (д, J= 10,1 Гц, 1H), 7,63 (с, 1H), 8,68 (с, 1H), 10,00 (с, 1H).
МС (ЭИ) m/z; 466 [M]+, 394, 277, 70 (bp).
Пример получения 8
К соединению по примеру получения 7 (500 мг, 1,18 ммоль) при охлаждении льдом добавляют раствор хлористый водород - диоксан (4 моль/л) (1,18 мл, 4,72 ммоль), перемешивают в течение 30 минут, затем нагревают до комнатной температуры и перемешивают еще 30 минут, добавляют водный раствор гидроксида натрия (1 моль/л), экстрагируютхлороформом, органическую фазу промывают один раз насыщенным водным рвствором хлорида натрия и сушат над безводным сульфатом магния. Растворитель отгоняют и получают желаемое вещество со 100%-ным выходом.
Желтый твердый продукт.
1Н-ЯМР (CDCL3) : 1,19 (с, 3H), 1,50 (с, 3H), 1,55-1,67 (м, 4H), 2,26 (с, 3H), 2,58-2,70 (м, 2H), 3,14 (ушир.с, 4H), 3,64 (д, J= 10,2 Гц, 1H), 3,75 (д, J= 10,2 Гц, 1H), 7,61 (с, 1H), 8,65 (с, 1H), 10,02 (с, 1H).
: 1,19 (с, 3H), 1,50 (с, 3H), 1,55-1,67 (м, 4H), 2,26 (с, 3H), 2,58-2,70 (м, 2H), 3,14 (ушир.с, 4H), 3,64 (д, J= 10,2 Гц, 1H), 3,75 (д, J= 10,2 Гц, 1H), 7,61 (с, 1H), 8,65 (с, 1H), 10,02 (с, 1H).
МС (ЭИ) m/z; 394 [M]+, 350 (bp).
Пример получения 9
Транс-6-амино-3,4-дигидро-2,2-диметил-7-нитро-4-н-пентиламино-2H-1-бензопиран-3-ол
К этанольному раствору (11 мл) соединения по примеру получения 1 (550 мг, 1,51 ммоль), при комнатной температуре добавляют 35%-ную соляную кислоту (1,1 мл) и кипятят в течение 12 часов. Добавляют насыщенный водный раствор бикарбоната натрия, экстрагируют этилацетатом, органическую фазу промывают один раз насыщенным водным раствором хлорида натрия и сушат над безводным сульфатом магния. После отгонки растворителя остаток очищают хроматографией на колонке с силикагелем (Hex/AcOEt = 1/1) и получают желаемое вещество с 75%-ным выходом
Красное аморфное вещество.
1Н-ЯМР (CDCl3) : 0,91 (т, J= 8,1 Гц, 3H), 1,19 (с, 3H), 1,25-1,35 (м, 4H), 1,34 (с, 3H), 1,50-1,80 (м, 4H), 2,48-2,75 (м, 2H), 3,58-3,65 (м, 2H), 5,70 (с, 2H), 6,81 (с, 1H), 7,59(с, 1H).
: 0,91 (т, J= 8,1 Гц, 3H), 1,19 (с, 3H), 1,25-1,35 (м, 4H), 1,34 (с, 3H), 1,50-1,80 (м, 4H), 2,48-2,75 (м, 2H), 3,58-3,65 (м, 2H), 5,70 (с, 2H), 6,81 (с, 1H), 7,59(с, 1H).
MC (ЭИ) m/z; 323 [M]+, 252 (bp).
[Примеры препаратов]
Пример препарата 1
Таблетка:
Вышеуказанные компоненты смешивают обычным способом и затем готовят 10000 покрытых сахаром таблеток, содержащих в каждой 1 мг активного компонента на таблетку.
Пример препарата 2
Капсула:
Вышеуказанные компоненты смешивают обычным способом и затем помещают в желатиновые капсулы и готовят 10000 капсул, содержащих в каждой 1 мг активного компонента на капсулу.
Пример препарата 3
Мягкая капсула:
Вышеуказанные компоненты смешивают обычным способом и затем помещают в мягкие желатиновые капсулы No.3 и готовят 10000 мягких капсул, содержащих в каждой 1 мг активного компонента на капсулу.
Пример препарата 4
Мазь:
Вышеуказанные компоненты смешивают обычным способом и получают 1 % -ную мазь.
Пример препарата 5
Суппозиторий:
(* торговое название соединений триглицеридного типа)
Вышеуказанные компоненты смешивают обычным способом, выливают в контейнеры для суппозиториев и охлаждают до отверждения, таким образом получают 1000 суппозиториев (1 г), содержащих в каждом 1 мг активного компонента на суппозиторий.
Пример препарата 6
Инъекционный раствор:
Используют путем растворения при применении.
[Пример фармакологического исследования]
Действие в эффективный рефрактерный период
Метод
Гончих собак анестезируют с помощью пентобарбитала натрия в условиях искусственной вентиляции проводят торактомию вдоль срединного сосуда и надрезают околосердечную сумку для открытия сердца. Показания ЭКГ фиксируют, используя биполярные электроды, присоединенные к поверхности свободной правой стенки предсердия, правому ушку предсердия и свободной правой стенки желудочка. Блуждающие нервы стимулировали с помощью устройства для электрической стимуляции посредством нихромовых проводков, помещенных в билатеральные блуждающие нервы шеи. Условия для электрической стимуляции блуждающих нервов были установлены такими, что интервал КК на ЭКГ продлялся до 1000 мсек по сравнению с тем, который был до начала стимуляции.
Для электрической стимуляции сердца был использован электрический ток в два раза сильнее, чем пороговый, и предварительная стимуляция S2 была использована после дачи 10 серий S1 стимуляций по основному циклу стимуляций. Для определения эффективного рефрактерного периода интервал S1-S2 был уменьшен до 2 мсек, и эффективный рефрактерный период был определен как точка, в которой потерян ответ на предварительную стимуляцию S2.
Для оценки эффективности лекарственного средства, перед введением лекарственного средства определялись эффективные периоды рефрактерности желудочка и предсердия, затем каждое соединение вводили внутривенно в дозе 0,3 мг/кг и через 5 минут после введения определяли эффективные периоды рефрактерности желудочка и предсердия.
Полученные данные представлены в виде времени пролонгации в эффективные периоды рефрактерности желудочка и предсердия, то есть [эффективный период рефрактерности после введения] - [эффективный период рефрактерности перед введением] (мсек).
Выводы
Соединения по настоящему изобретению демонстрируют пролонгированное действие в эффективный рефрактерный период, избирательное по отношению к предсердию.
Полезность изобретения
Соединения по настоящему изобретению обладают пролонгированным действием в эффективный рефрактерный период, избирательным по отношению к предсердию, поэтому могут быть использованы в качестве средств против мерцательной аритмии и средств против суправентрикулярной аритмии, и могут использоваться в виде лекарственных соединений. Кроме того, поскольку соединения по настоящему изобретению обладают наибольшим влиянием на желудочек, они могут вносить свой вклад в безопасность при лечении вышеуказанных состояний аритмии.
| название | год | авторы | номер документа |
|---|---|---|---|
| БЕНЗОПИРАНОВОЕ СОЕДИНЕНИЕ | 2005 |
|
RU2366658C2 |
| БЕНЗОПИРАНОВОЕ ПРОИЗВОДНОЕ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ЕГО ОСНОВЕ | 2000 |
|
RU2234502C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ БЕНЗОПИРАНА ПРОТИВ АРИТМИИ | 2002 |
|
RU2291867C2 |
| ТРИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ БЕНЗОПИРАНА В КАЧЕСТВЕ ПРОТИВОАРИТМИЧЕСКИХ АГЕНТОВ | 2005 |
|
RU2380370C2 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ НЕВРОПАТИИ | 2003 |
|
RU2337682C2 |
| ЦИКЛИЧЕСКОЕ УГЛЕВОДОРОДНОЕ СОЕДИНЕНИЕ | 2015 |
|
RU2676328C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2017 |
|
RU2748693C2 |
| НОВОЕ ПРОИЗВОДНОЕ ГИДРОКСАМОВОЙ КИСЛОТЫ | 2011 |
|
RU2575129C2 |
| МОНОЦИКЛИЧЕСКОЕ ПИРИДИНОВОЕ ПРОИЗВОДНОЕ | 2014 |
|
RU2645352C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2018 |
|
RU2773441C2 |
Данное изобретение относится к новым бензопирановым производным формулы (I)
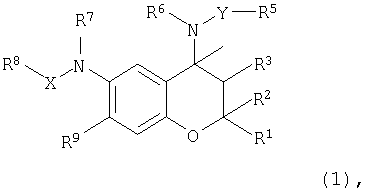
где R1 и R2 представляют собой, каждый, независимо, C1-6алкильную группу, R3 представляет собой гидроксильную группу, R4 представляет собой атом водорода, R6 представляет собой атом водорода, R7 представляет собой атом водорода, Х отсутствует или представляет собой С=O, R8 представляет собой атом водорода или C1-6алкильную группу, R9 представляет собой нитрогруппу, Y представляет собой С3-8алкиленовую группу, группу -(CH2)m-CR11R12-(CH2)n-, в которой m и n равны, каждый, независимо, 0, 1, 2, 3 или 4, и m+n равно или более чем 2; когда m равно 0, R11 и R12 представляют собой, каждый, независимо, C1-6алкильную группу, и когда m иной, чем 0, R11 и R12 представляют собой, каждый, независимо, C1-6алкильную группу или гидроксильную группу, или Y представляет собой группу -(СН2)0-O-(СН2)р-, в которой о и р равны, каждый, независимо, 2, 3 или 4, R5 представляет собой атомом водорода, аминогруппу, C1-6алкоксигруппу, С3-6циклоалкильную группу, С1-6алкилтиогруппу, C1-6алкиламиногруппу, ди-С1-6алкиламиногруппу, C1-6алкоксикарбониламиногруппу, или к их фармацевтически приемлемым солям, а также к антиаритмическому средству. 2 н. и 5 з.п. ф-лы, 1 табл.
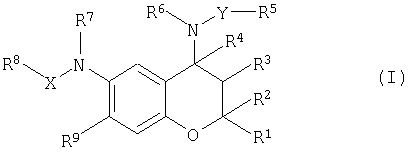
где R1 и R2 представляют собой каждый С1-6алкильную группу;
R3 представляет собой гидроксильную группу;
R4 представляет собой атом водорода;
R6 представляет собой атом водорода;
R7 представляет собой атом водорода;
X отсутствует или представляет собой С=O;
R8 представляет собой атом водорода или C1-6алкильную группу;
R9 представляет собой нитрогруппу;
Y представляет собой С3-8алкиленовую группу или группу -(СН2)m-CR11R12-(СН2)n-, в которой m и n равны каждый независимо 0, 1, 2, 3 или 4, и m+n равно или более 2; когда m равно 0, R11 и R12 представляют собой каждый независимо C1-6алкильную группу, и когда m иной, чем 0, R11 и R12 представляют собой каждый независимо С1-6алкильную группу или гидроксильную группу, или Y представляет собой группу -(СН2)0-O-(СН2)p-, в которой о и р равны каждый независимо 2, 3 или 4,
R5 представляет собой атомом водорода, аминогруппу, С1-6алкоксигруппу, С3-8циклоалкильную группу, С1-6алкилтиогруппу, C1-6алкиламиногруппу, ди-С1-6алкиламиногруппу, С1-6алкоксикарбониламиногруппу,
или его фармацевтически приемлемая соль.
| WO 9113865 А, 19.09.1991 | |||
| WO 9804542 A, 05.02.1998 | |||
| БЕНЗОПИРАНЫ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 1994 |
|
RU2122000C1 |
| RU 2059635 C1, 10.05.1996. | |||
Авторы
Даты
2006-11-27—Публикация
2002-02-14—Подача